Prof Dr Cihat AFAK Eczaclk Fakltesi Farmastik Kimya





























![Adi ışık [ ] = / l. c Polarizör Polarize ışık [ ] = Adi ışık [ ] = / l. c Polarizör Polarize ışık [ ] =](https://slidetodoc.com/presentation_image_h/acdfe1eb1eeb0eb552b39cd827c4502e/image-81.jpg)










![Okunuşları - Spiro öneki - [Küçük halkadaki köşe sayısı, - Büyük halkadaki köşe sayısı] Okunuşları - Spiro öneki - [Küçük halkadaki köşe sayısı, - Büyük halkadaki köşe sayısı]](https://slidetodoc.com/presentation_image_h/acdfe1eb1eeb0eb552b39cd827c4502e/image-100.jpg)











- Slides: 159

Prof. Dr. Cihat ŞAFAK Eczacılık Fakültesi Farmasötik Kimya ABD

csafak@hacettepe. edu. tr http//yunus. hacettepe. edu. tr/ csaf ak

Organik Kimya Amonyum siyanat Üre

10 g maddenin yakılması sonucu 14. 64 CO 2, 6 g su meydana gelsin. 44 g CO 2’de 12 g karbon varsa 14. 64 CO 2 de X: ? --------------------X= 4 g Karbon 4/10 x 100 = % 40 C içerir. 18 g H 2 O’da 2 g hidrojen varsa 6 g H 2 O’da X: ? ---------------------X= 0. 66 g Hidrojen 0. 66/10 x 100 = % 6. 6 H içerir.

Ampirik formül C: % 40. 9, H: % 4. 58 , O: % 54. 51 bulunsun. - Her yüzde değeri, kendine karşı gelen elementin atom ağırlığına bölünür. 40. 91/12= 3. 14 4. 58/1= 4. 58 54. 51/16= 3. 14 -Çıkan değerler en küçük değere bölünür. 3. 14/3. 14= 1, 4. 58/3. 14= 1. 3 3. 14/3. 14=1 - Bu değerlerin hepsini tam sayı yapacak şekilde en küçük sayı saptanır. 1. 3= 3, 1. 3. 3=3. 9 (4) 1. 3= 3 C 3 H 4 O 3 ampirik formülü elde edilir.

• - Eğer bileşiğin molekül ağırlığı 176 olarak verilmişse (C 3 H 4 O 3)n= 176 (12 x 3 + 1 x 4 + 16 x 3)n=176 n = 2 olarak bulunur. (C 3 H 4 O 3)2 = C 6 H 8 O 6 • Dolayısıyla ampirik formül C 6 H 8 O 6 olarak bulunur.

ATOMİK YAPI d p s p+n e Ana yörünge Alt yörünge elektron sayısı K s 2 L s+3 p 8 M s+3 p+5 d 18 N s+3 p+5 d+7 f 32


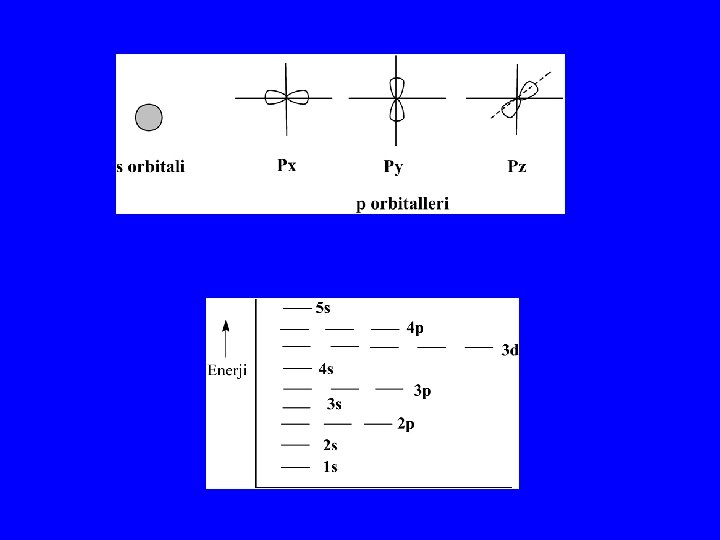
Pauli eksklüsyon prensibi Bir orbitalde ancak iki elektron bulunabilir ve bunların spinleri zıttır. Bunlara eşleşmiş elektronlar adı verilir.

Aufbau kuralı Elektronlar artan enerji düzeyine göre orbitallere yerleşirler.

Hund kuralı Eşit enerji düzeyli orbitallerden (dejenere) herbiri bir elektron almadan ikinci elektronu alamazlar.

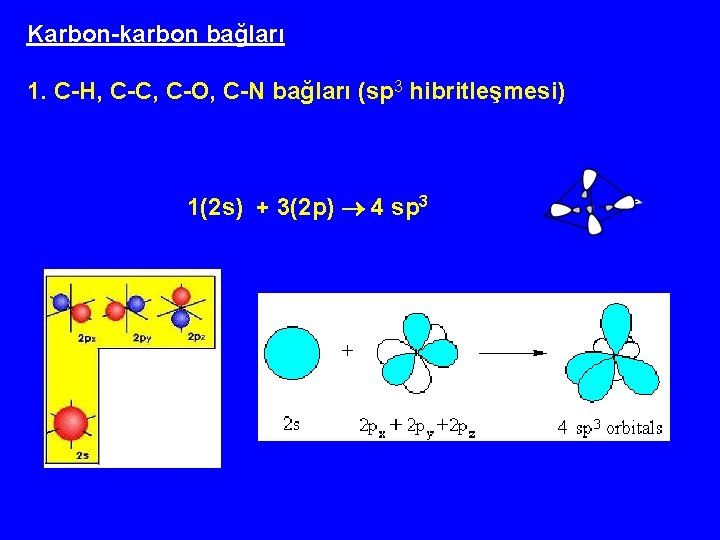
Karbon-karbon bağları 1. C-H, C-C, C-O, C-N bağları (sp 3 hibritleşmesi) 1(2 s) + 3(2 p) 4 sp 3

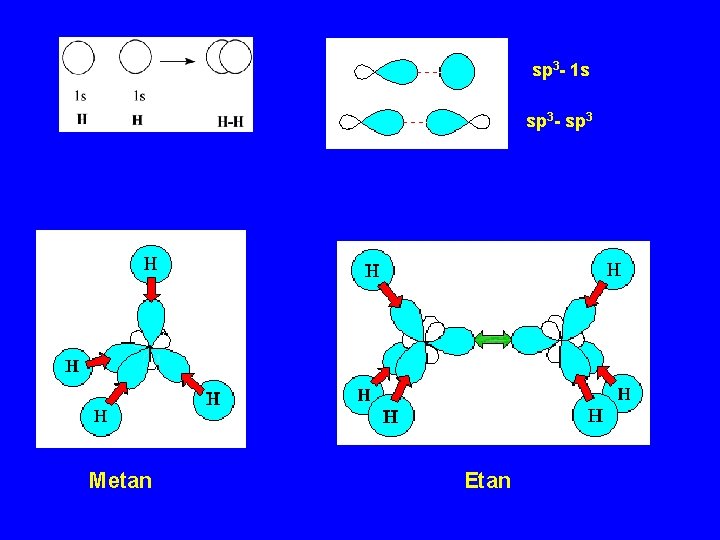
sp 3 - 1 s sp 3 - sp 3 Metan Etan

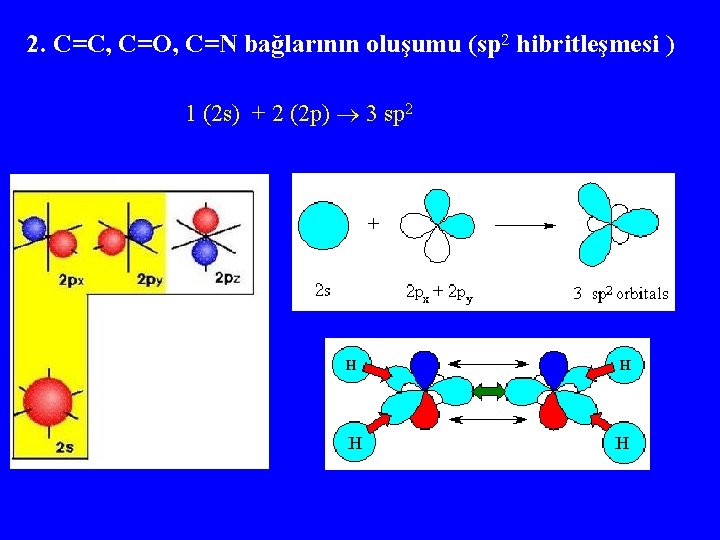
2. C=C, C=O, C=N bağlarının oluşumu (sp 2 hibritleşmesi ) 1 (2 s) + 2 (2 p) 3 sp 2

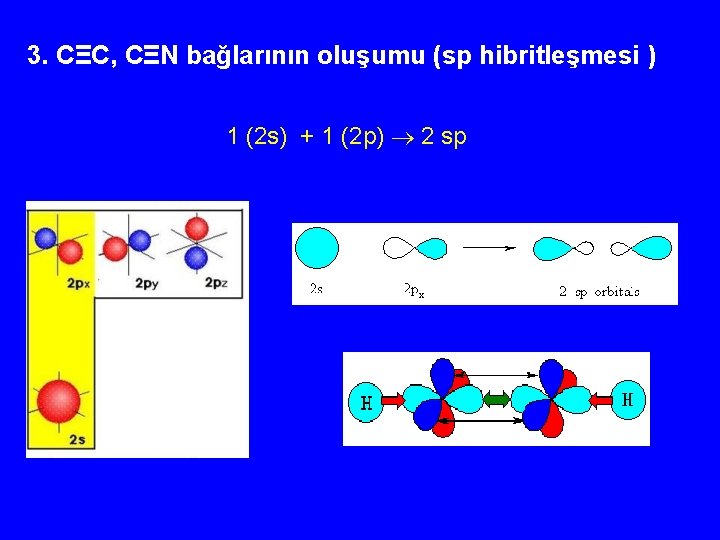
3. CΞC, CΞN bağlarının oluşumu (sp hibritleşmesi ) 1 (2 s) + 1 (2 p) 2 sp

sp hibritleşmesine diğer örnekler

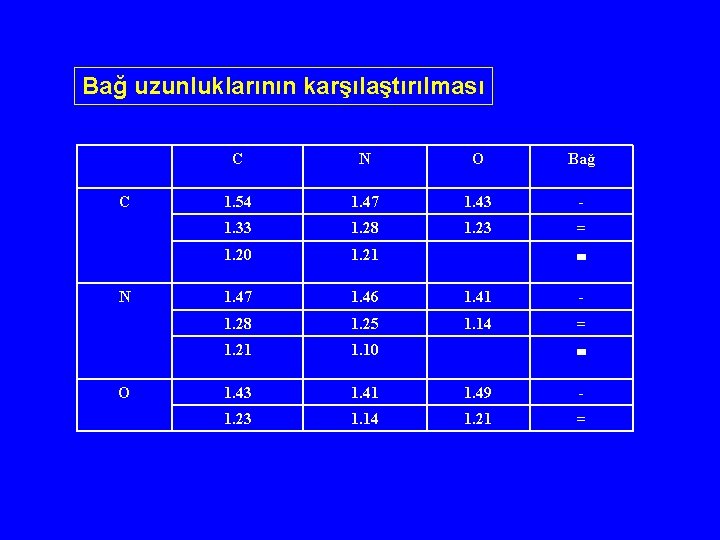
Bağ uzunluklarının karşılaştırılması C N O Bağ 1. 54 1. 47 1. 43 - 1. 33 1. 28 1. 23 = 1. 20 1. 21 1. 47 1. 46 1. 41 - 1. 28 1. 25 1. 14 = 1. 21 1. 10 1. 43 1. 41 1. 49 - 1. 23 1. 14 1. 21 =

Azot atomu (7 elektron) 1 s 2 2 p 3 (1 s 2 2 px 1 2 py 1 2 pz 1) Oksijen atomu (8 elektron) 1 s 2 2 p 4 (1 s 2 2 px 2 2 py 1 2 pz 1)



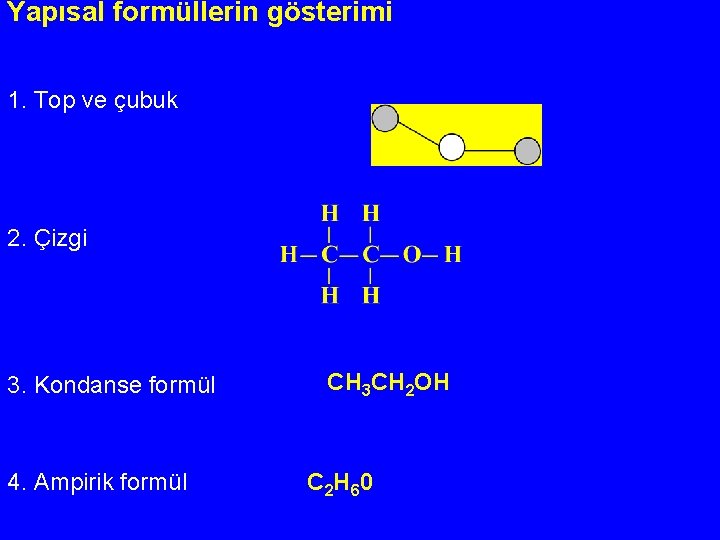
Yapısal formüllerin gösterimi 1. Top ve çubuk 2. Çizgi 3. Kondanse formül 4. Ampirik formül CH 3 CH 2 OH C 2 H 60

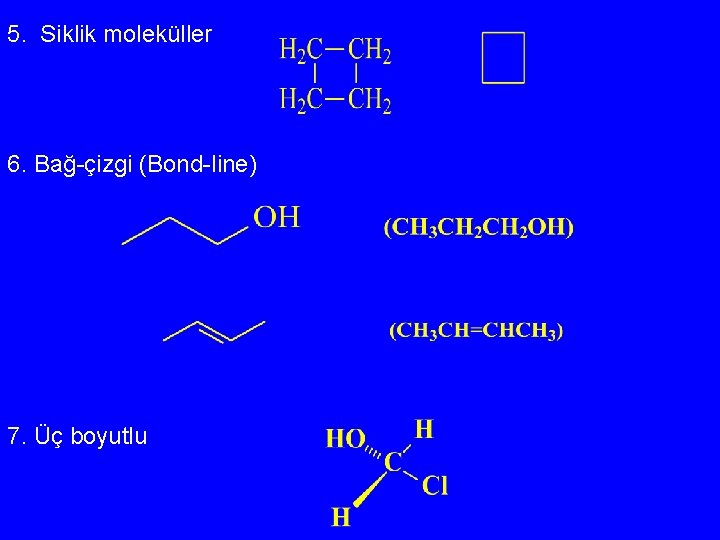
5. Siklik moleküller 6. Bağ-çizgi (Bond-line) 7. Üç boyutlu

KİMYASAL REAKSİYON Substrat + Reaktif -----> Ürün Reaksiyon kordinatları Enerji Aktivasyon enerjisi A Aktivasyon enerjisi B t EKZOTERMİK REAKSİYON t ENDOTERMİK REAKSİYON

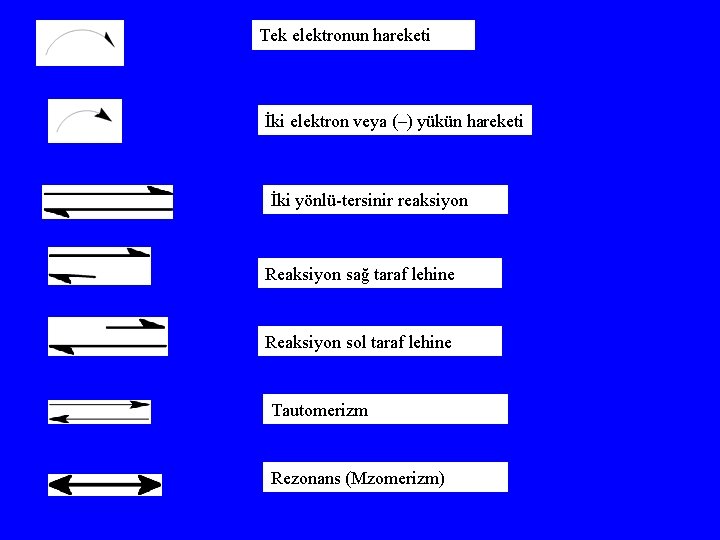
Tek elektronun hareketi İki elektron veya (–) yükün hareketi İki yönlü-tersinir reaksiyon Reaksiyon sağ taraf lehine Reaksiyon sol taraf lehine Tautomerizm Rezonans (Mzomerizm)

Reaksiyonlarda oluşan ara yapılar 1. A-B A. + B. Radikal 2. A-B A+ + BA- karbanyon (nükleofil) B+ karbokatyon (elektrofil)

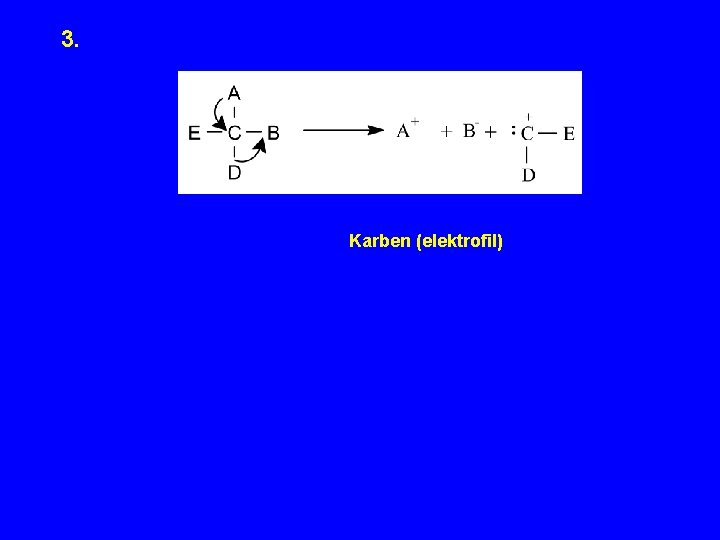
3. Karben (elektrofil)

Reaktifler a. Nükleofil NH 3, RNH 2, R 2 NH, R 3 N, NH 2 -, OH-, ROH, RSR, RSH, SH-, CN-, X-, karbanyon, Li. Al. H 4 (H- verir), R-Mg. X (R- verir), R-Li, RCOOH, R-C C-

Elektrofil Karbakatyon, karben, H+, CO 2, SO 3, Br 2 (önce Br+ verir ), Al. Cl 3, Fe. Cl 3, HNO 3 (NO 2+), HNO 2 (NO+)

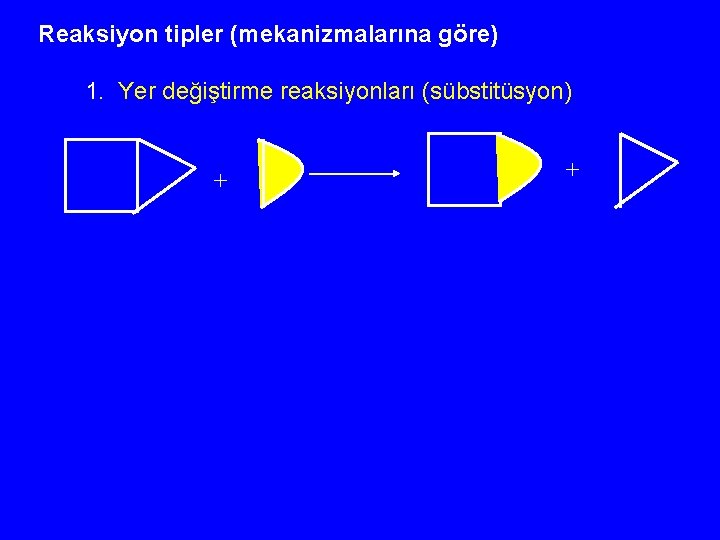
Reaksiyon tipler (mekanizmalarına göre) 1. Yer değiştirme reaksiyonları (sübstitüsyon) + +

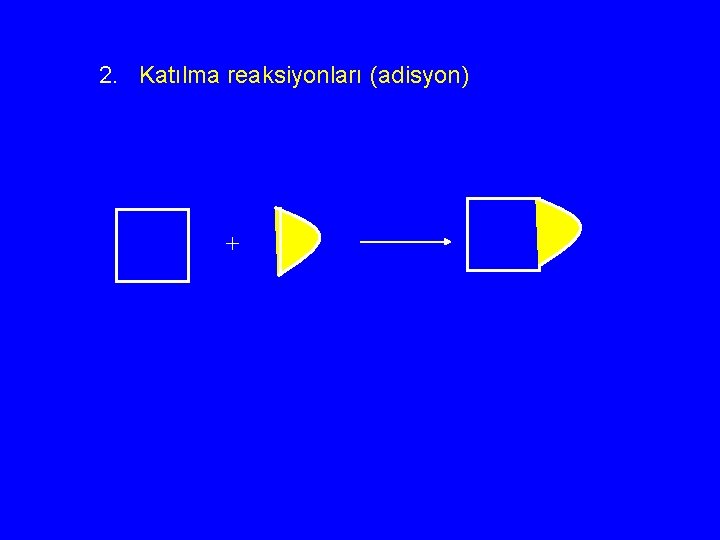
2. Katılma reaksiyonları (adisyon) +

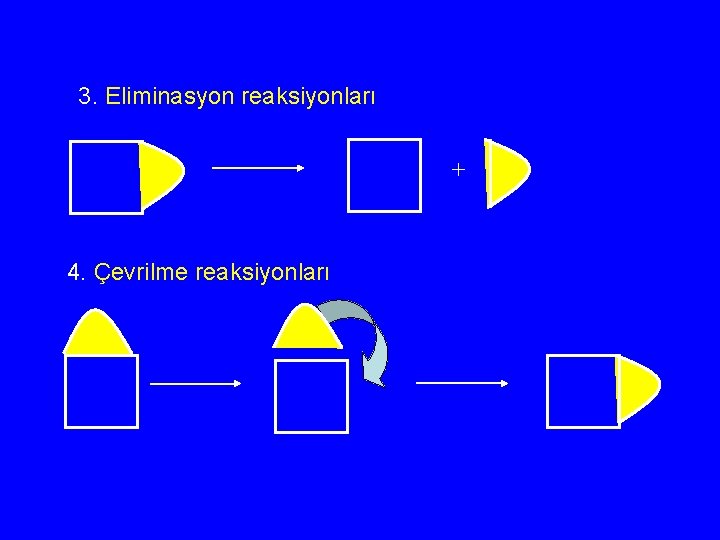
3. Eliminasyon reaksiyonları + 4. Çevrilme reaksiyonları

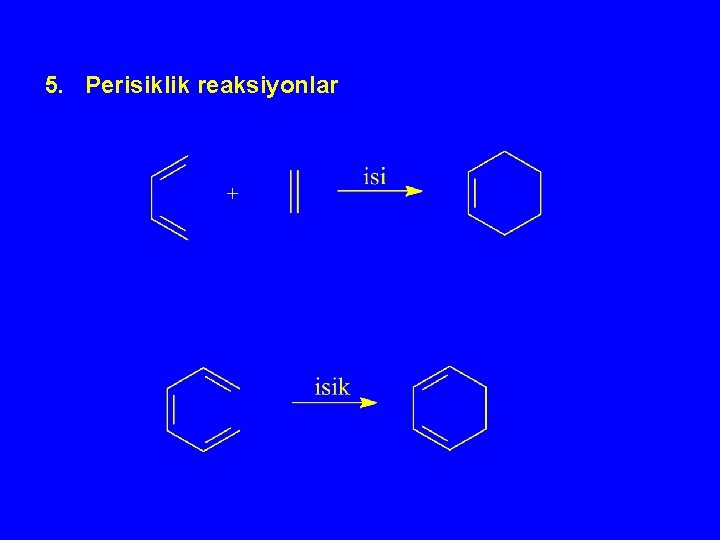
5. Perisiklik reaksiyonlar

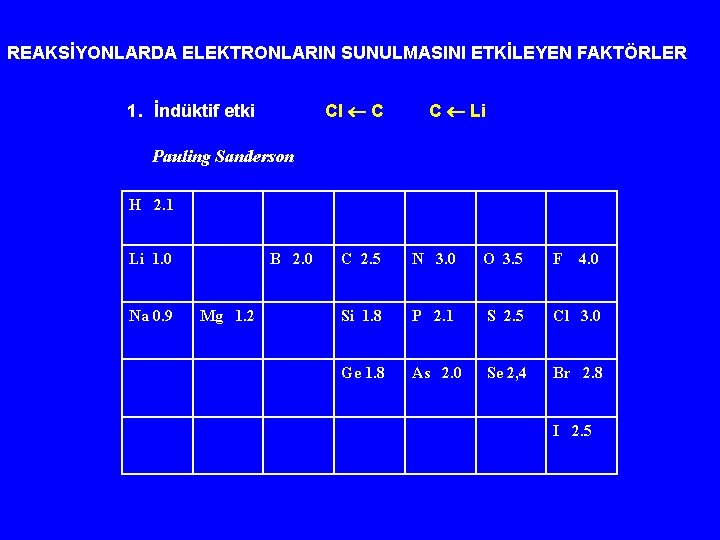
REAKSİYONLARDA ELEKTRONLARIN SUNULMASINI ETKİLEYEN FAKTÖRLER Cl C 1. İndüktif etki C Li Pauling Sanderson H 2. 1 Li 1. 0 Na 0. 9 B 2. 0 Mg 1. 2 C 2. 5 N 3. 0 O 3. 5 F 4. 0 Si 1. 8 P 2. 1 S 2. 5 Cl 3. 0 Ge 1. 8 As 2. 0 Se 2, 4 Br 2. 8 I 2. 5

+I : (İndüktif yolla elektron salan gruplar) COO-, CR 3, CHR 2, CH 3, D - I : (İndüktif yolla elektron çeken gruplar) NR 3+, SR 2+, NH 3+, NO 2, SO 2 R, CN, SO 2, Ar, COOH, F, Cl, Br, I, OR, COR, SH, SR, OH, C CR, Ar, CH=CR 2 azalan kuvvette

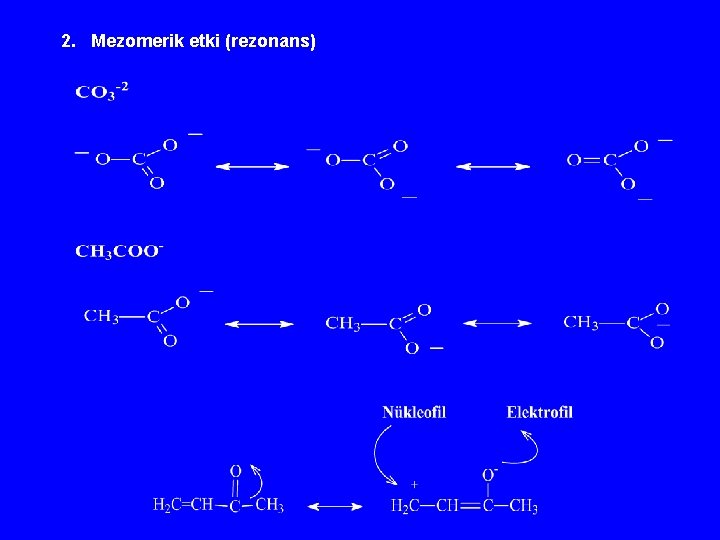
2. Mezomerik etki (rezonans)

(+M) : (Mezomerik yolla elektron salan gruplar) O-, S-, NR 2, NHR, NH 2, NHCOR, OH, OCOR, SH, Br, I, Cl, F, R, Ar (-M): (Mezomerik yolla elektron çeken gruplar) NO 2, CN, COOH, COOR, CONH 2, CONHR, CONR 2, CHO, COR, SO 2 OR azalan kuvvette

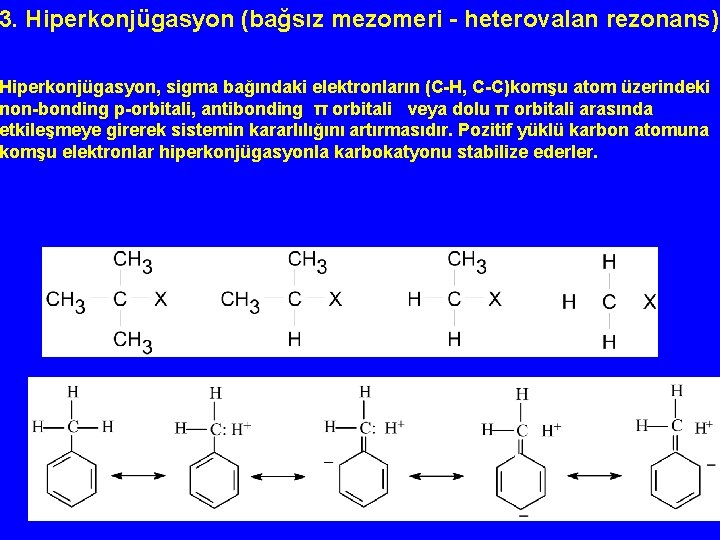
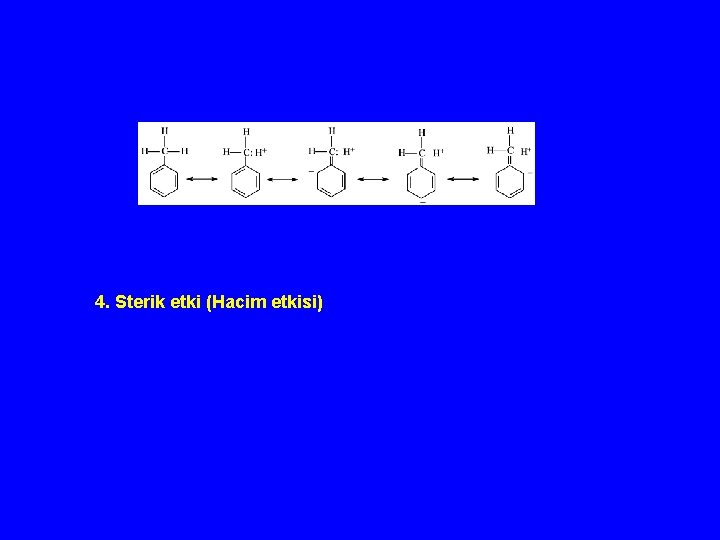
3. Hiperkonjügasyon (bağsız mezomeri - heterovalan rezonans) Hiperkonjügasyon, sigma bağındaki elektronların (C-H, C-C)komşu atom üzerindeki non-bonding p-orbitali, antibonding π orbitali veya dolu π orbitali arasında etkileşmeye girerek sistemin kararlılığını artırmasıdır. Pozitif yüklü karbon atomuna komşu elektronlar hiperkonjügasyonla karbokatyonu stabilize ederler.

Hiperkonjügasyon - Bu tür sistemlerde sigma bağlarını kısalmasına yol açar. 1, 3 -butadienin C- bağları 1. 54 A olması beklenirken 1. 46 A dır. Bağ çifte bağ uzunluğuna ve karakterine yaklaşmıştır. . - Karbokatyonların stabilitesi (CH 3)3 C+ > (CH 3)2 CH+ > (CH 3)CH 2+ > CH 3+ şeklindedir. Katyona komşu C-C sigma bağları dönebilmekte bu yapının daha fazla kararlı olmasına neden olmaktadır. Ne kadar fazla komşu C-H sigma bağı varsa daha büyük hiperkonjügasyon stabilizasyonu olur.

4. Sterik etki (Hacim etkisi)

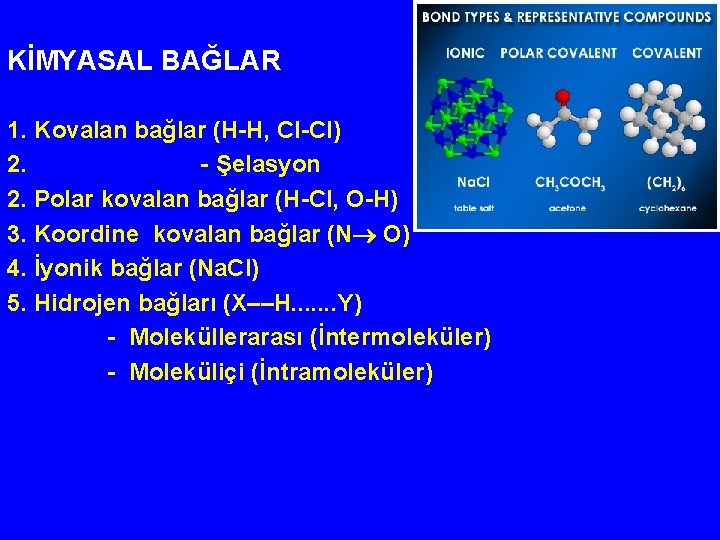
KİMYASAL BAĞLAR 1. Kovalan bağlar (H-H, Cl-Cl) 2. - Şelasyon 2. Polar kovalan bağlar (H-Cl, O-H) 3. Koordine kovalan bağlar (N O) 4. İyonik bağlar (Na. Cl) 5. Hidrojen bağları (X––H. . . . Y) - Moleküllerarası (İntermoleküler) - Moleküliçi (İntramoleküler)

Bağ Tipi İyonik bağ Kovalan bağ Kuvvetlendirilmiş iyonik bağ Hidrojen bağı İyon-dipol bağı Dipol-dipol bağı Yük transfer etkileşmeleri Hidrofobik etkileşmeler Van der Waals etkileşmeleri Etkileşme enerjisi (kcal/mol) 40 -110 10 1 -7 1 -7 1 0. 5 -1

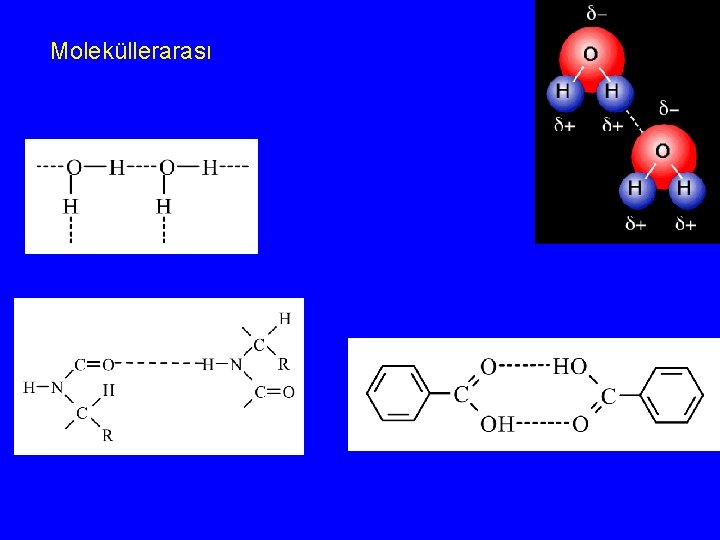
Moleküllerarası

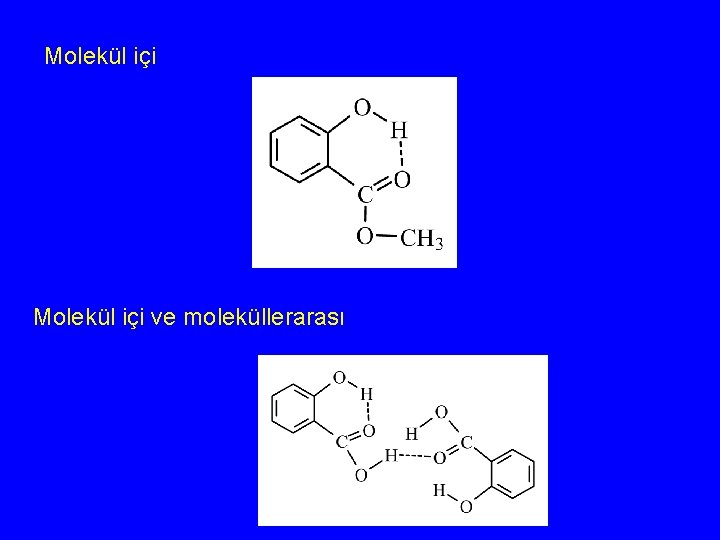
Molekül içi ve moleküllerarası

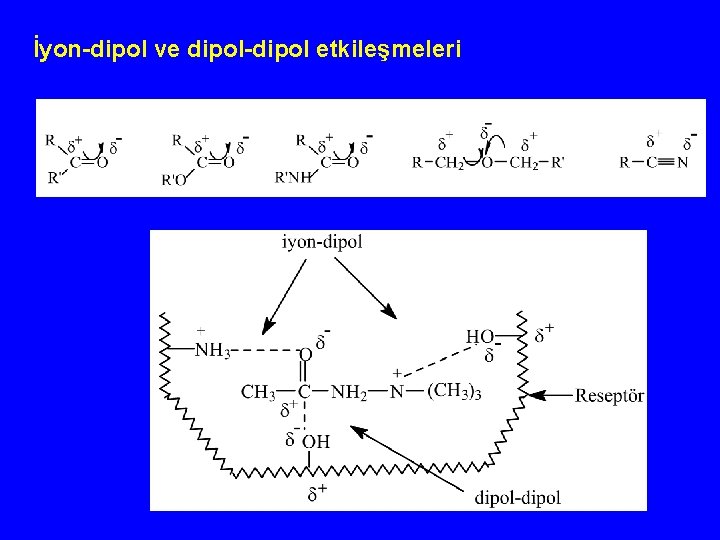
İyon-dipol ve dipol-dipol etkileşmeleri

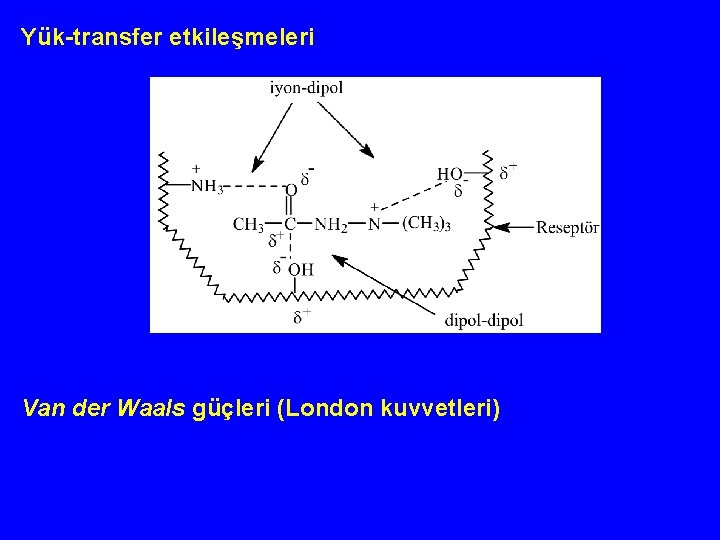
Yük-transfer etkileşmeleri Van der Waals güçleri (London kuvvetleri)

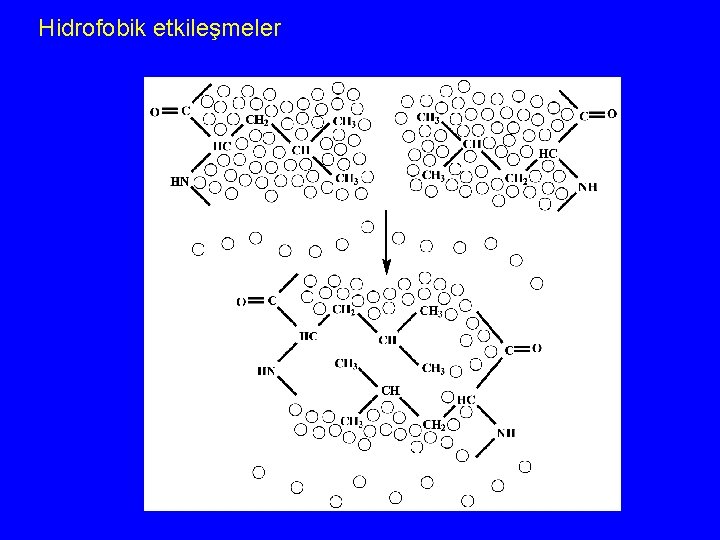
Hidrofobik etkileşmeler

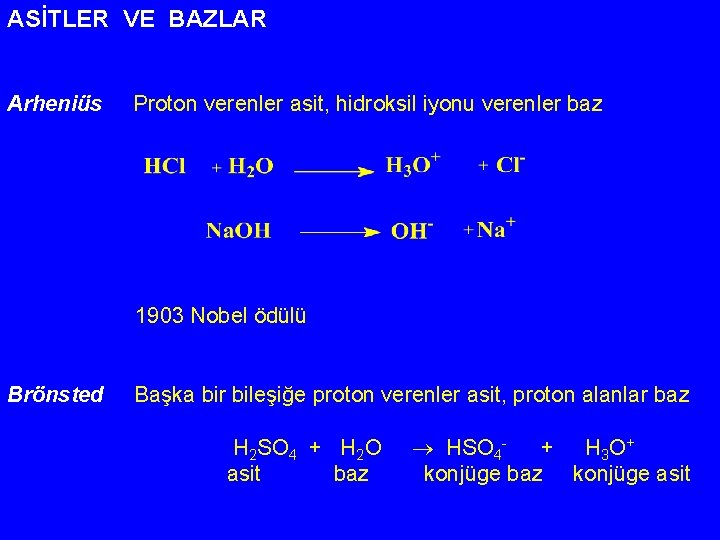
ASİTLER VE BAZLAR Arheniüs Proton verenler asit, hidroksil iyonu verenler baz 1903 Nobel ödülü Brönsted Başka bir bileşiğe proton verenler asit, proton alanlar baz H 2 SO 4 + H 2 O asit baz HSO 4+ H 3 O + konjüge baz konjüge asit

Lewis (1923) Asitler, serbest elektron çiftleriyle bağlanabilen nötr veya iyonik bileşikler, bazlar ise oktet boşluğu olan veya nötr moleküllerle veya katyonlarla bağlanan maddelerdir. H-A + H-O-H H 3 O+ + A A- H 3 O+ Ka = --------- H-A - log ka = Pka

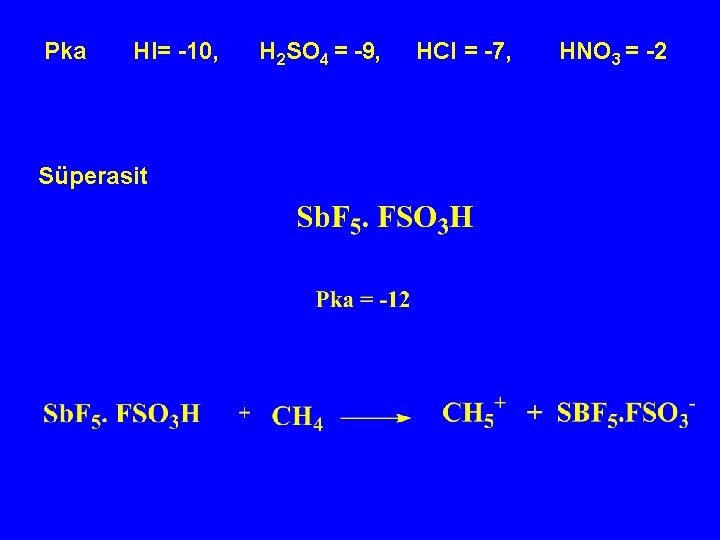
Pka HI= -10, Süperasit H 2 SO 4 = -9, HCl = -7, HNO 3 = -2

Asit yağmuru Su p. H = 7 Karbon dioksit emisyonu olması halinde; p. H=5. 6 civarında (yağmur suyu) Kükürtlü ve azotlu gazların emisyonu halinde sülfürik ve nitrik asit oluşur. Havanın p. H’sı çok düşük değerlere düşer.

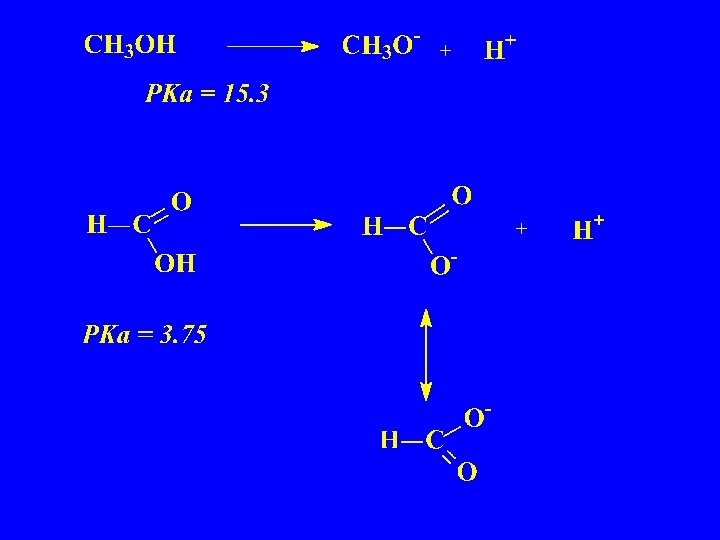
Asitlik ve yapı Bir maddenin asitliği; 1. Kolay proton sunabilmesine (H-X) Hidrojenin bağlandığı atomun elektronegatifliği H-X bağının sağlamlığı 2. Oluşan anyonun stabilize olmasına 3. Çözücüye bağlıdır Bağ ne kadar kuvvetli ise asit o kadar zayıftır Pka H-F 3. 2 H-Cl -7 H-Br -8 H-I -9


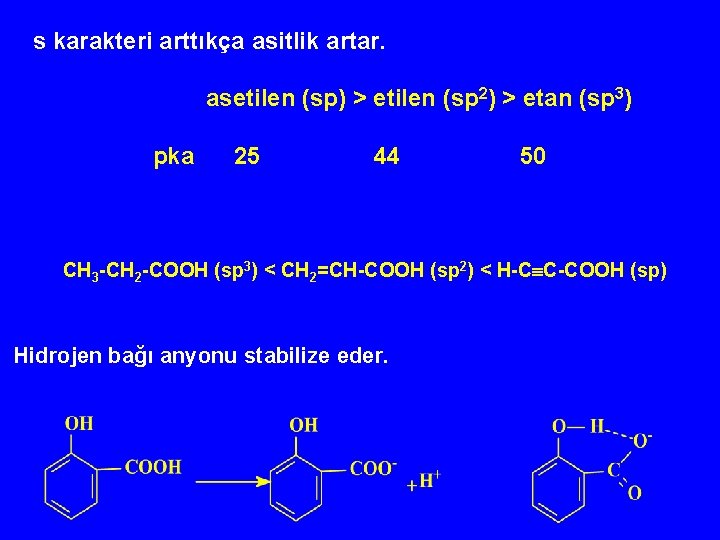
s karakteri arttıkça asitlik artar. asetilen (sp) > etilen (sp 2) > etan (sp 3) pka 25 44 50 CH 3 -CH 2 -COOH (sp 3) < CH 2=CH-COOH (sp 2) < H-C C-COOH (sp) Hidrojen bağı anyonu stabilize eder.

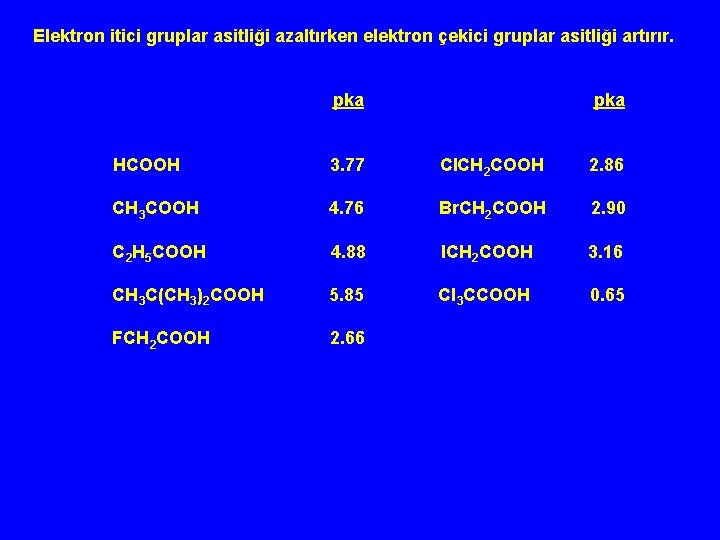
Elektron itici gruplar asitliği azaltırken elektron çekici gruplar asitliği artırır. pka HCOOH 3. 77 Cl. CH 2 COOH 2. 86 CH 3 COOH 4. 76 Br. CH 2 COOH 2. 90 C 2 H 5 COOH 4. 88 ICH 2 COOH 3. 16 CH 3 C(CH 3)2 COOH 5. 85 Cl 3 CCOOH 0. 65 FCH 2 COOH 2. 66

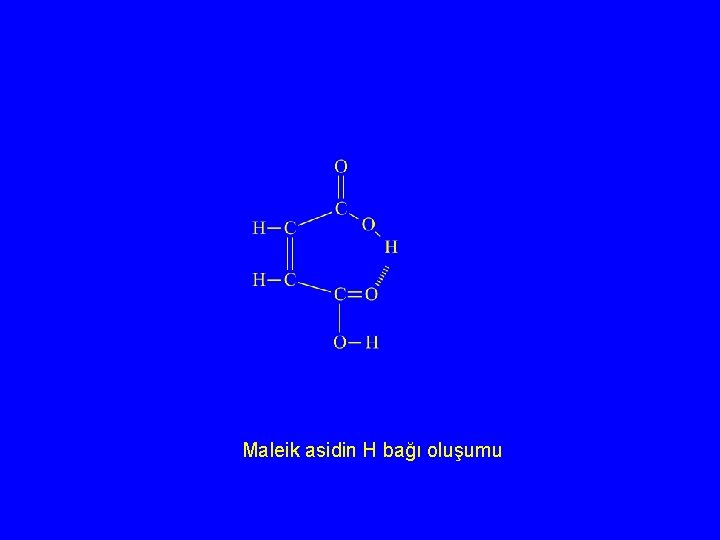
POLİKARBOKSİLLİ ASİTLER Dikarboksilli asitler Fumarik asit Pka 1 Pka 2 3. 02 4. 33 Maleik asit 1. 92 6. 23

Maleik asidin H bağı oluşumu

BAZLAR - log kb = P kb NH 3 Pkb 4. 75 (CH 3)2 NH (CH 3)3 N CH 3 NH 2 3. 22 4. 20 3. 36

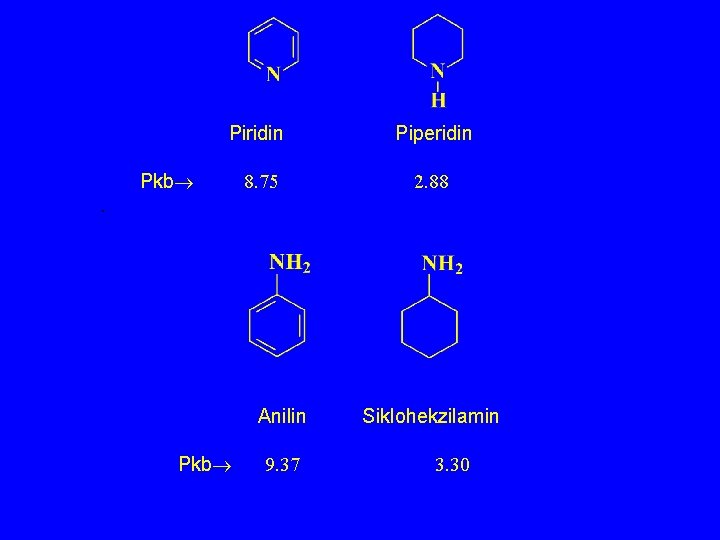
Piridin Piperidin 8. 75 2. 88 Pkb . Anilin Pkb 9. 37 Siklohekzilamin 3. 30

Soğan niye göz yaşartır

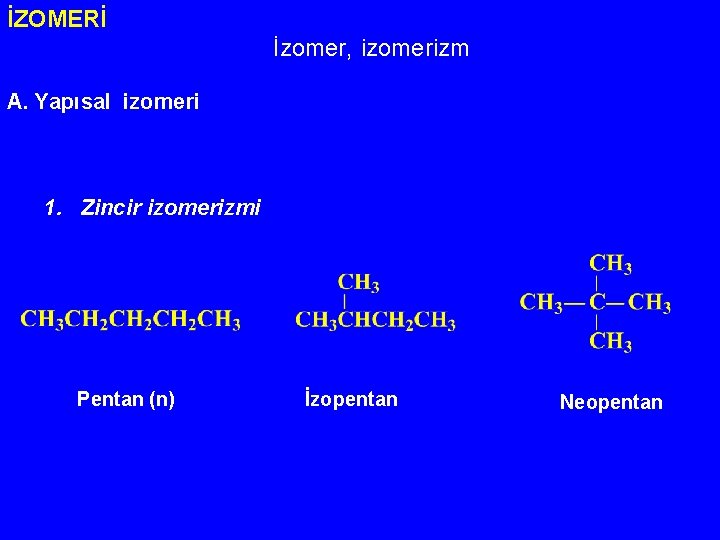
İZOMERİ İzomer, izomerizm A. Yapısal izomeri 1. Zincir izomerizmi Pentan (n) İzopentan Neopentan

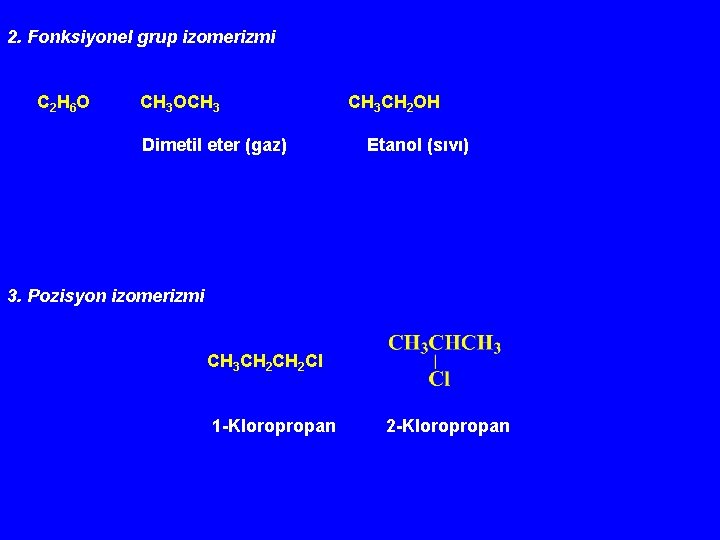
2. Fonksiyonel grup izomerizmi C 2 H 6 O CH 3 OCH 3 Dimetil eter (gaz) CH 3 CH 2 OH Etanol (sıvı) 3. Pozisyon izomerizmi CH 3 CH 2 Cl 1 -Kloropropan 2 -Kloropropan

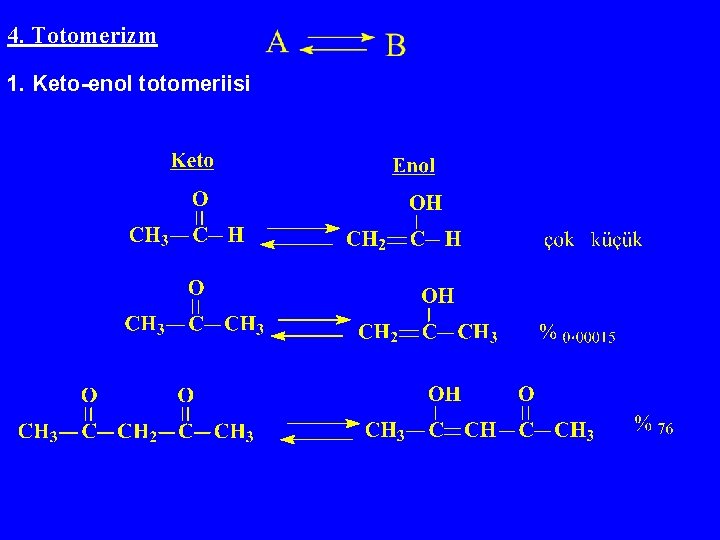
4. Totomerizm 1. Keto-enol totomeriisi

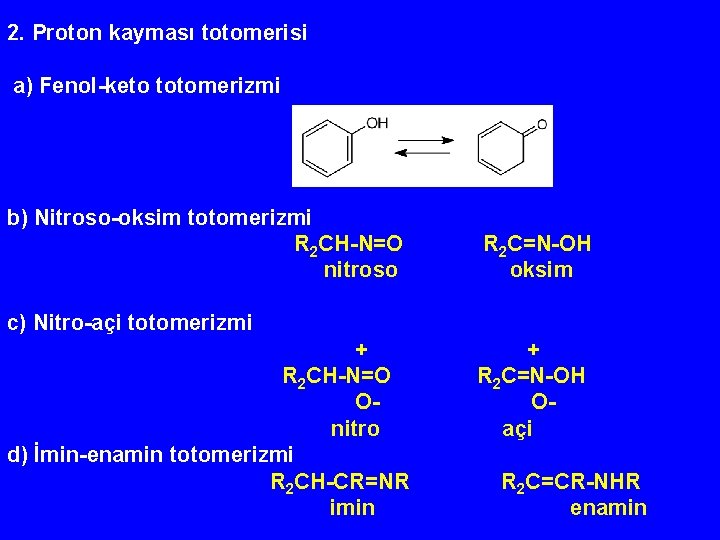
2. Proton kayması totomerisi a) Fenol-keto totomerizmi b) Nitroso-oksim totomerizmi R 2 CH-N=O nitroso R 2 C=N-OH oksim c) Nitro-açi totomerizmi + R 2 CH-N=O Onitro d) İmin-enamin totomerizmi R 2 CH-CR=NR imin + R 2 C=N-OH Oaçi R 2 C=CR-NHR enamin

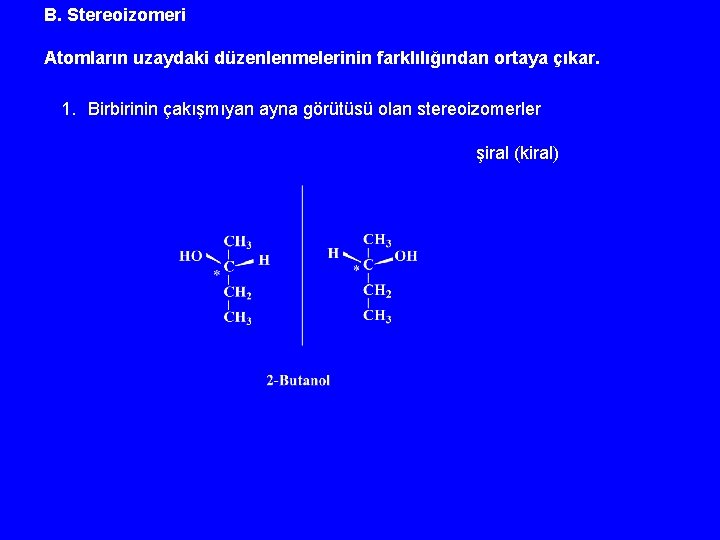
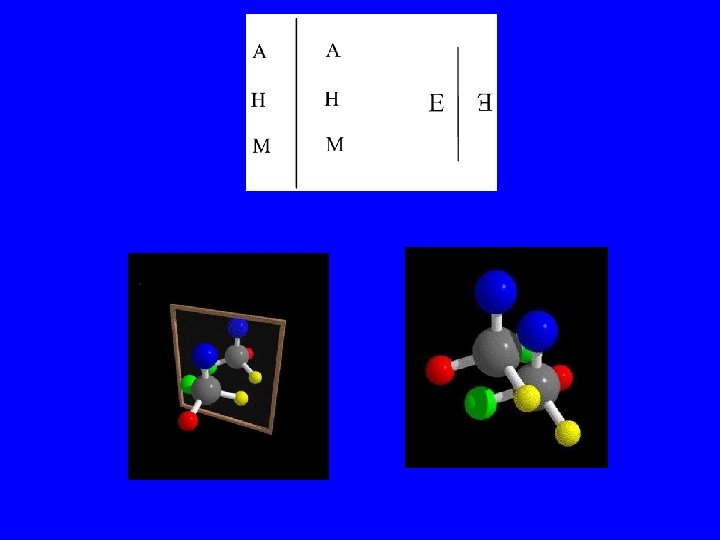
B. Stereoizomeri Atomların uzaydaki düzenlenmelerinin farklılığından ortaya çıkar. 1. Birbirinin çakışmıyan ayna görütüsü olan stereoizomerler şiral (kiral)

2. Diasteromerler Birbirinin ayna görütüsü olmayan stereoizomerler

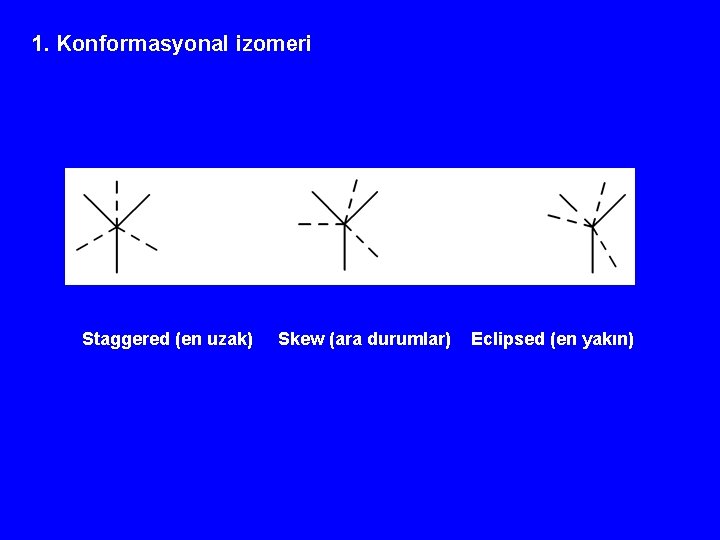
1. Konformasyonal izomeri Staggered (en uzak) Skew (ara durumlar) Eclipsed (en yakın)


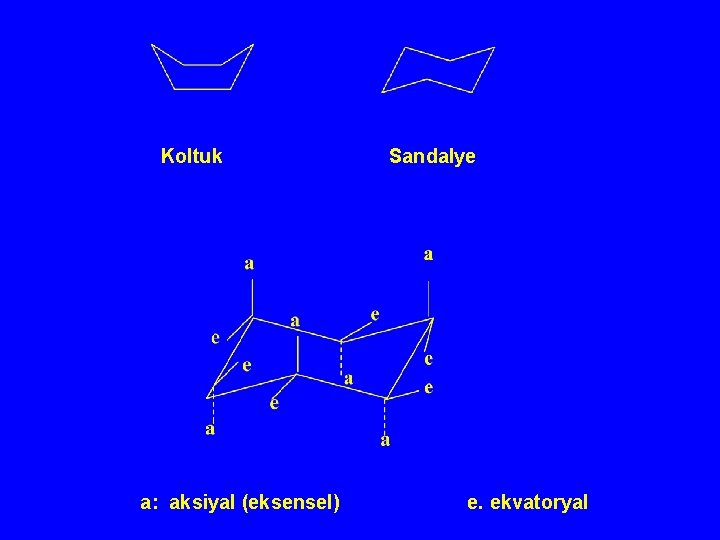
Koltuk a: aksiyal (eksensel) Sandalye e. ekvatoryal

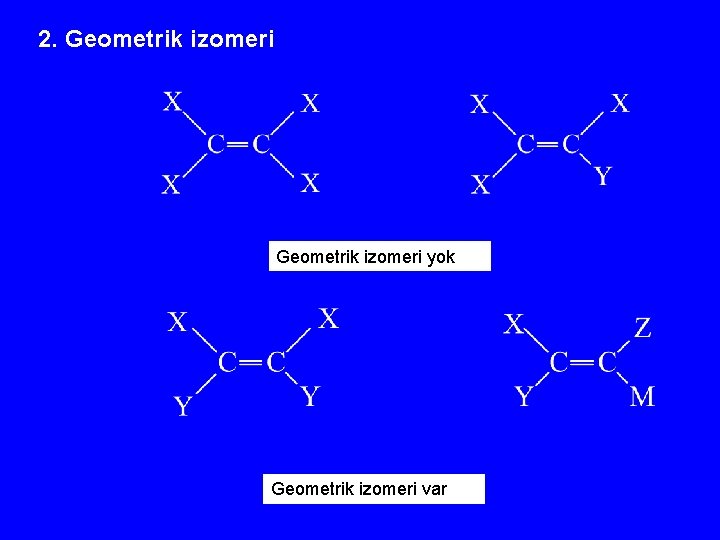
2. Geometrik izomeri yok Geometrik izomeri var

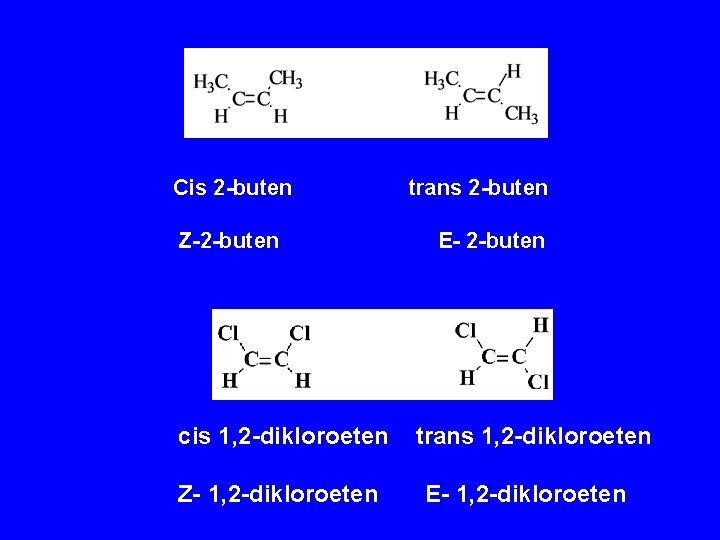
Cis 2 -buten Z-2 -buten cis 1, 2 -dikloroeten Z- 1, 2 -dikloroeten trans 2 -buten E- 2 -buten trans 1, 2 -dikloroeten E- 1, 2 -dikloroeten

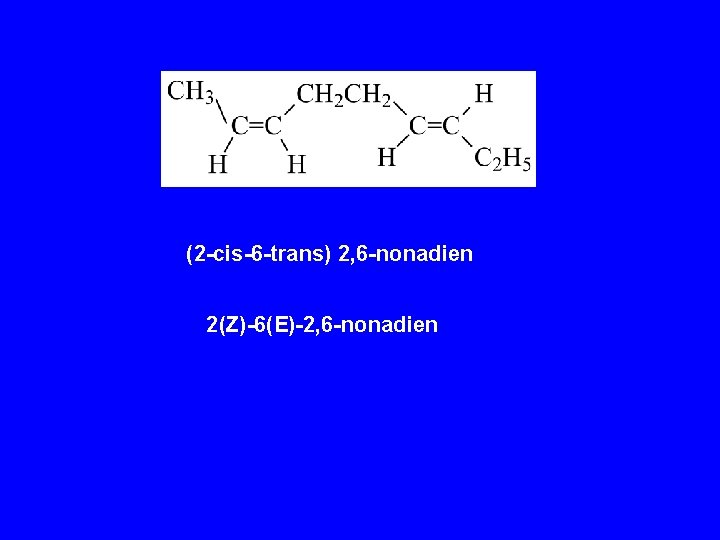
(2 -cis-6 -trans) 2, 6 -nonadien 2(Z)-6(E)-2, 6 -nonadien

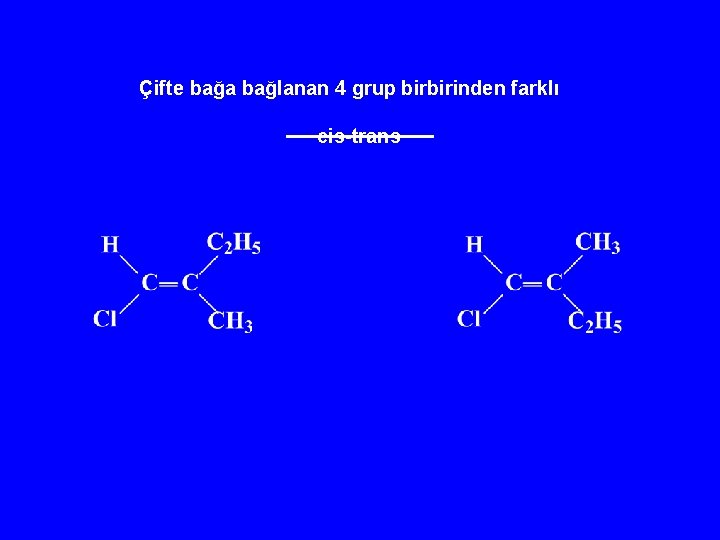
Çifte bağa bağlanan 4 grup birbirinden farklı cis-trans

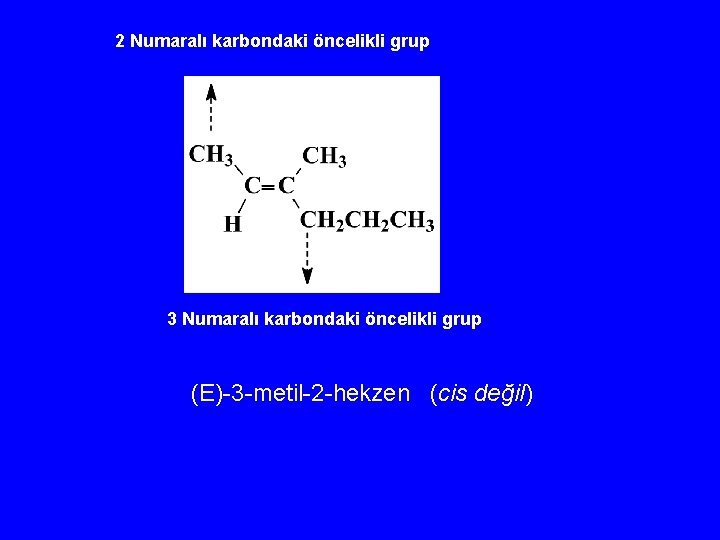
2 Numaralı karbondaki öncelikli grup 3 Numaralı karbondaki öncelikli grup (E)-3 -metil-2 -hekzen (cis değil)

2 Numaralı karbondaki öncelikli grup 3 Numaralı karbondaki öncelikli grup (Z)-3 -metil-2 -hekzen

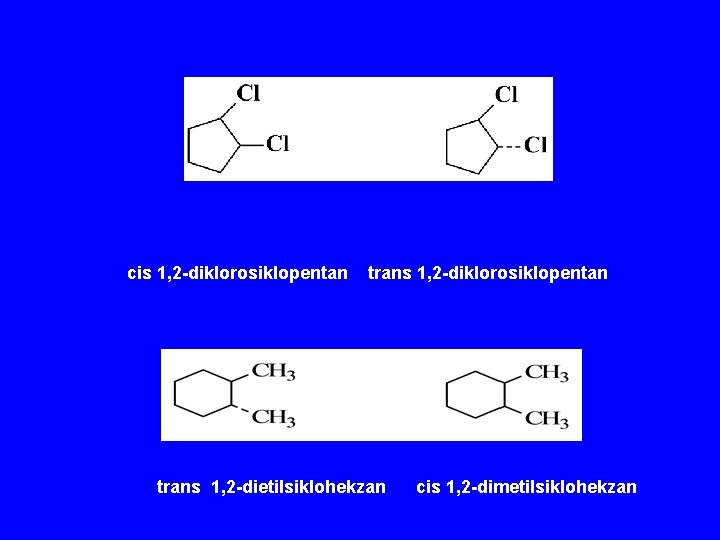
cis 1, 2 -diklorosiklopentan trans 1, 2 -dietilsiklohekzan cis 1, 2 -dimetilsiklohekzan

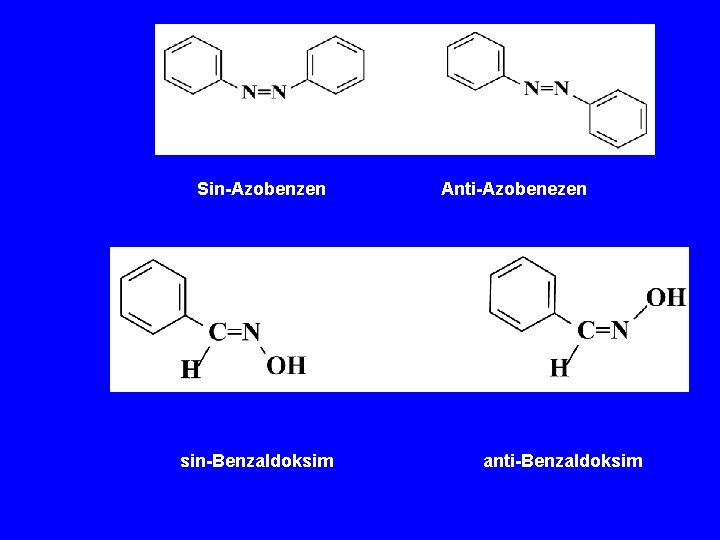
Sin-Azobenzen sin-Benzaldoksim Anti-Azobenezen anti-Benzaldoksim

C. OPTİK İZOMERİ


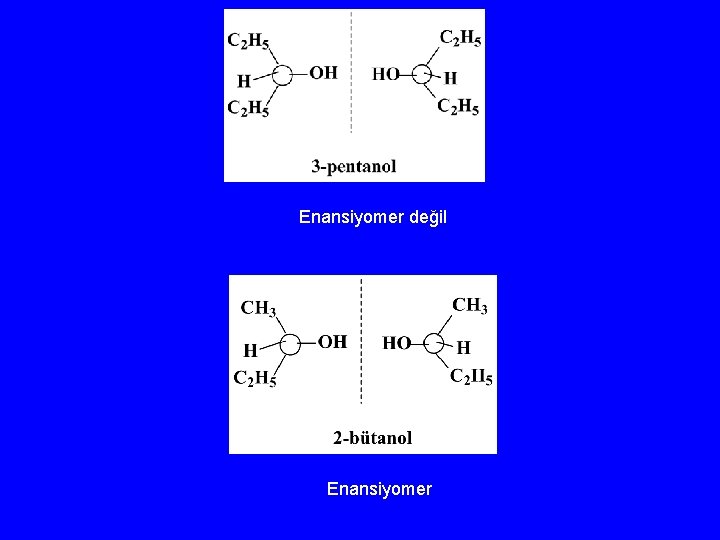
Enansiyomer değil Enansiyomer

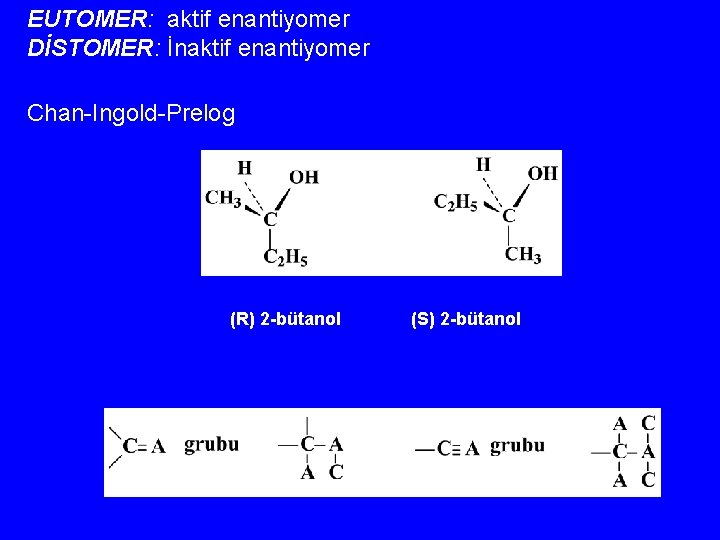
EUTOMER: aktif enantiyomer DİSTOMER: İnaktif enantiyomer Chan-Ingold-Prelog (R) 2 -bütanol (S) 2 -bütanol
![Adi ışık l c Polarizör Polarize ışık Adi ışık [ ] = / l. c Polarizör Polarize ışık [ ] =](https://slidetodoc.com/presentation_image_h/acdfe1eb1eeb0eb552b39cd827c4502e/image-81.jpg)
Adi ışık [ ] = / l. c Polarizör Polarize ışık [ ] = / l. d


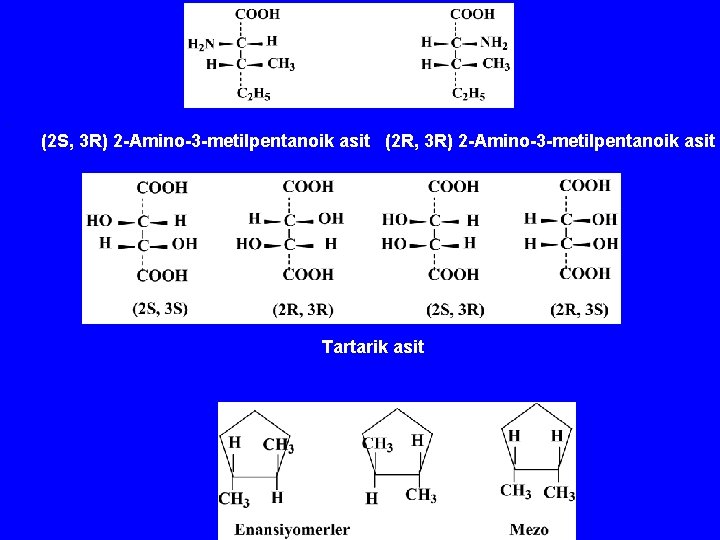
. (2 S, 3 R) 2 -Amino-3 -metilpentanoik asit (2 R, 3 R) 2 -Amino-3 -metilpentanoik asit Tartarik asit

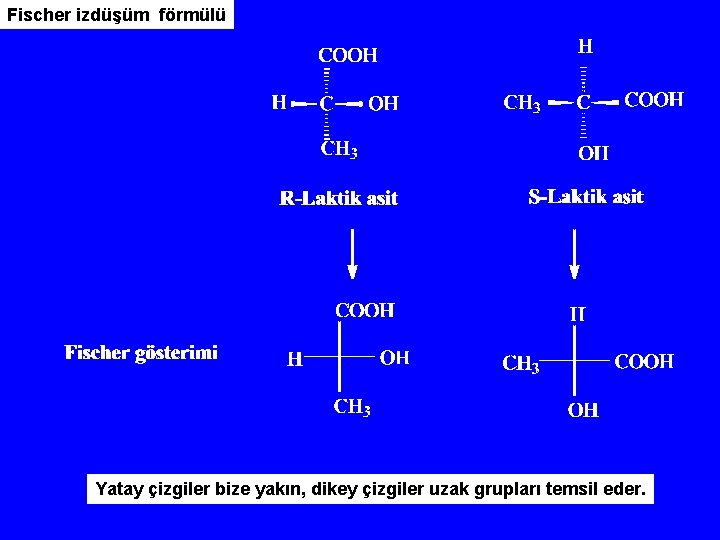
Fischer izdüşüm förmülü Yatay çizgiler bize yakın, dikey çizgiler uzak grupları temsil eder.

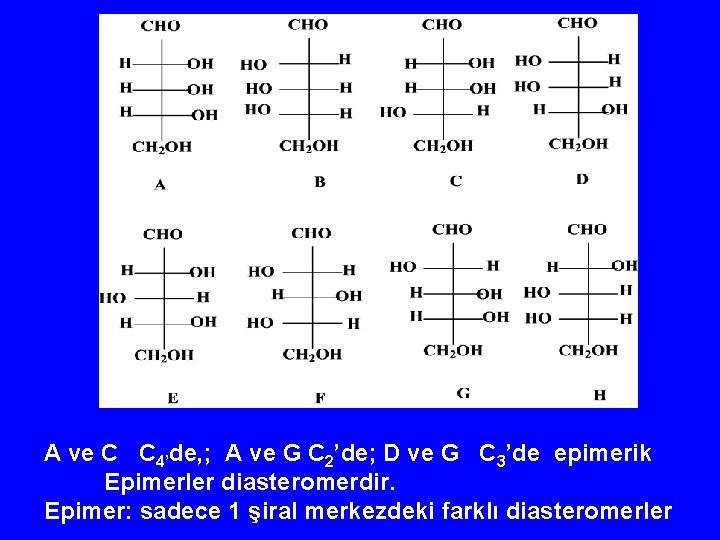
A ve C C 4’de, ; A ve G C 2’de; D ve G C 3’de epimerik Epimerler diasteromerdir. Epimer: sadece 1 şiral merkezdeki farklı diasteromerler

HİDROKARBONLAR ALKANLAR (Cn. H 2 n+2) ≤ 20 C-C 4 Doğal gaz, tüpgaz 20 -60 C 5 -C 6 Petrol eteri, çözücüler 60 -100 C 6 -C 7 Ligroin 40 -200 C 5 -C 10 Benzin 175 -325 C 12 -C 18 Jet yakıtı 250 -400 ≥ C 12 Gazyağı, mazot Uçucu olmayan sıvılar ≥ C 20 Yağ, gres, asfalt, katran

1 2 3 4 CH 4 C 2 H 6 C 3 H 8 C 4 H 10 Metan Etan Propan Bütan Gaz Gaz 6 7 8 9 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 Hegzan Heptan Oktan Nonan 5 C 5 H 12 Pentan Sıvı 10 C 10 H 22 Dekan Sıvı Sıvı

Alkanların isimlendirilmesi 1. Alkanlardan bir hidrojen çıkarılarak oluşturulan yapılara alkil grupları denir ve türedikleri alkana göre adlandırılır. Cn. H 2 n+1 genel formülüne sahiptirler Metan Etan Propan Bütan CH 4 C 2 H 6 C 3 H 8 C 4 H 10 Metil Etil Propil Butil CH 3 C 2 H 5 C 3 H 7 C 4 H 9 Hegzan Heptan Oktan Nonan C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 Hegzil Heptil Oktil Nonil Pentan C 5 H 12 Pentil C 5 H 11 Dekan C 10 H 22 Dekil C 6 H 13 C 7 H 15 C 8 H 17 C 9 H 19 C 10 H 21

2. En uzun zincir belirlenir. Diğer gruplar bağlanma yerinin numarası verilerek bir sübstitüent olarak belirtilir. Sübstitüentlerin bağlanma noktalarının küçük numara alması tercih edilir.

3. Bir zincir üzerinde birden fazla sübstitüent olduğunda - Bu sübstitüentler aynı ise önlerine di, tri, tetra gibi önekler getirilir.

- Aynı karbonda iki sübstitüent varsa o karbonun numarası iki kez kullanılır.

- Sübstitüentler farklı ise alfabetik öncelik veya küçükten büyüğe bir sıra izlenir.

4. Eşit uzunlukta iki zincir olması halinde, üzerinde daha çok sübstitüent bulunan zincir temel zincir olarak alınır.

5. Dallanma ana zincirin her iki ucundan eşit mesafede başlıyorsa numaralar toplamı az olan okunuş seçilir.

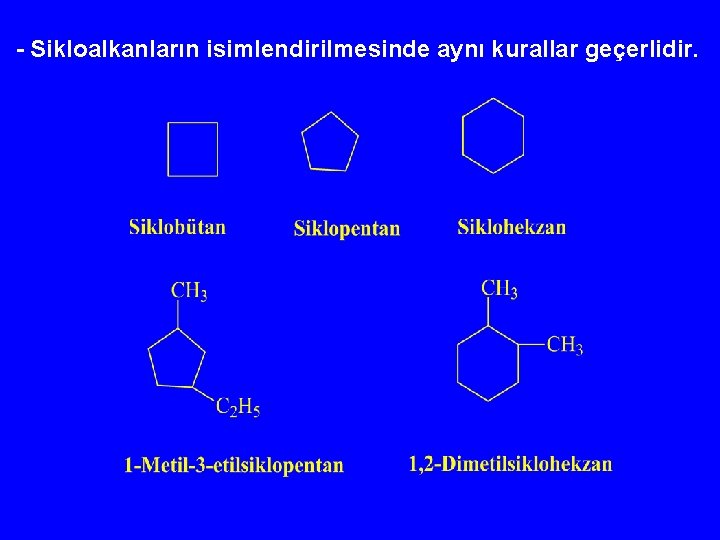
- Sikloalkanların isimlendirilmesinde aynı kurallar geçerlidir.

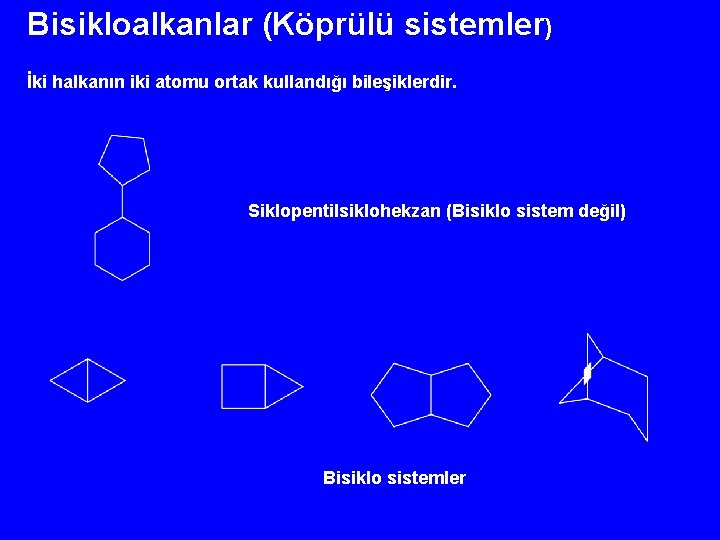
Bisikloalkanlar (Köprülü sistemler) İki halkanın iki atomu ortak kullandığı bileşiklerdir. Siklopentilsiklohekzan (Bisiklo sistem değil) Bisiklo sistemler

* : Köprübaşı atomları

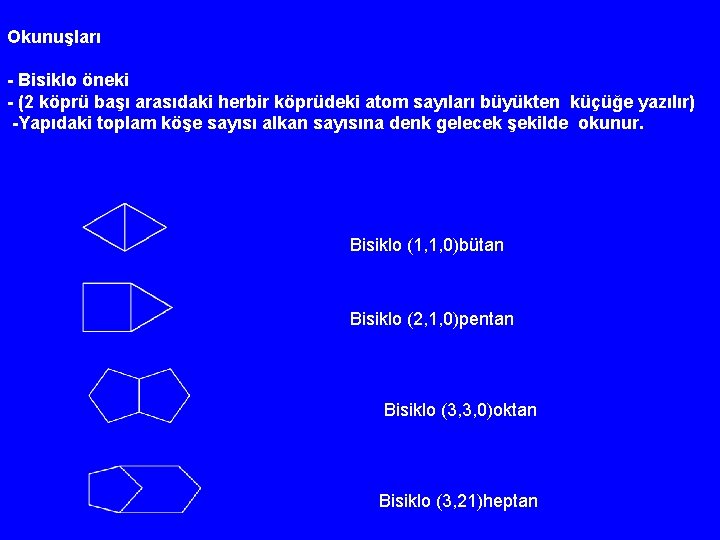
Okunuşları - Bisiklo öneki - (2 köprü başı arasıdaki herbir köprüdeki atom sayıları büyükten küçüğe yazılır) -Yapıdaki toplam köşe sayısı alkan sayısına denk gelecek şekilde okunur. Bisiklo (1, 1, 0)bütan Bisiklo (2, 1, 0)pentan Bisiklo (3, 3, 0)oktan Bisiklo (3, 21)heptan

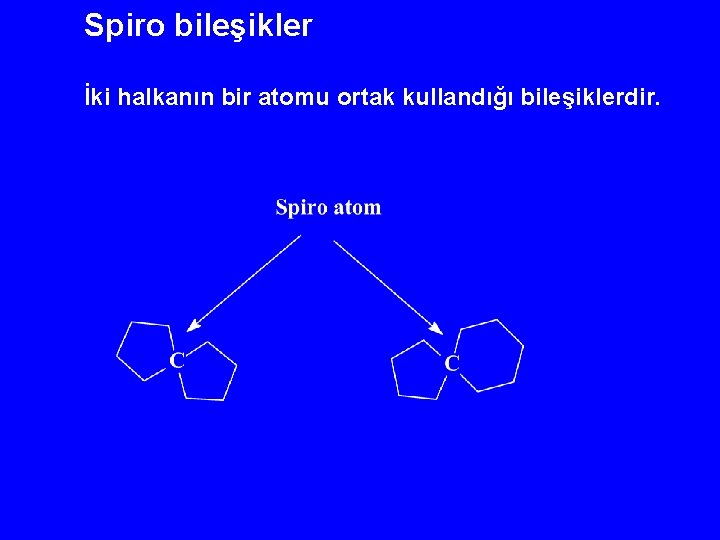
Spiro bileşikler İki halkanın bir atomu ortak kullandığı bileşiklerdir.
![Okunuşları Spiro öneki Küçük halkadaki köşe sayısı Büyük halkadaki köşe sayısı Okunuşları - Spiro öneki - [Küçük halkadaki köşe sayısı, - Büyük halkadaki köşe sayısı]](https://slidetodoc.com/presentation_image_h/acdfe1eb1eeb0eb552b39cd827c4502e/image-100.jpg)
Okunuşları - Spiro öneki - [Küçük halkadaki köşe sayısı, - Büyük halkadaki köşe sayısı] - Yapıdaki toplam köşe sayısı alkan sayısına denk gelecek şekilde okunur. Spiro [4, 4]nonan Spiro [dekan]

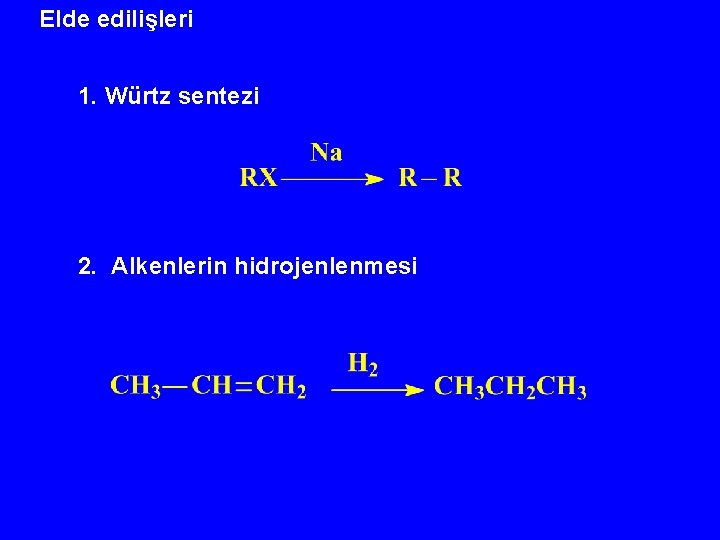
Elde edilişleri 1. Würtz sentezi 2. Alkenlerin hidrojenlenmesi

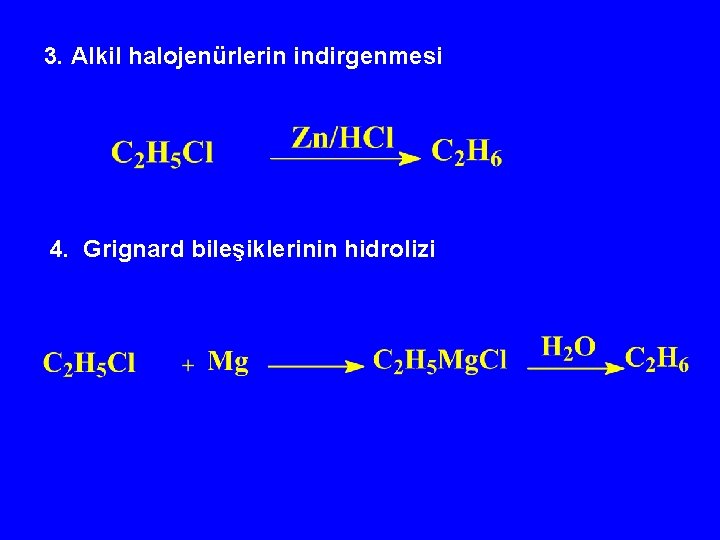
3. Alkil halojenürlerin indirgenmesi 4. Grignard bileşiklerinin hidrolizi

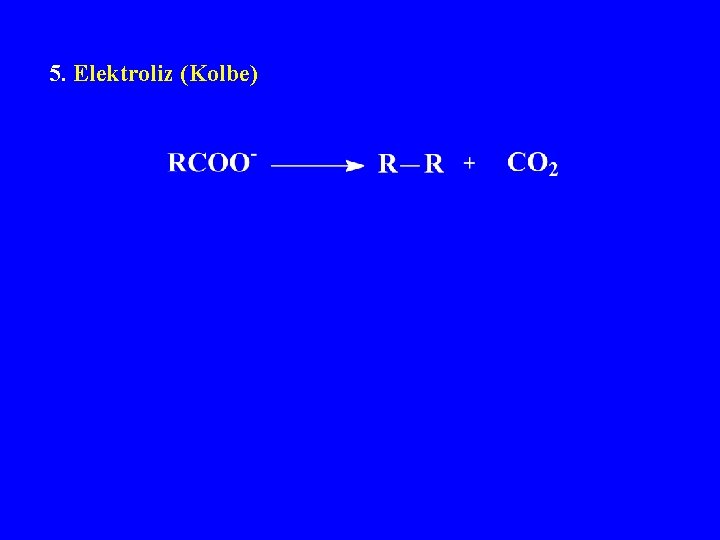
5. Elektroliz (Kolbe)

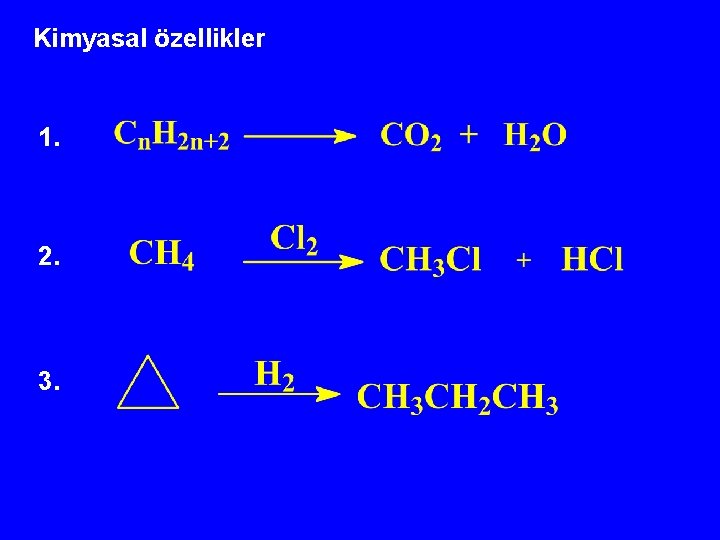
Kimyasal özellikler 1. 2. 3.

ALKENLER (OLEFİNLER) (Cn. H 2 n) İsimlendirilmeleri 1. İkili bağı içeren en uzun zincir seçilir, alkan ismi önüne an eki yerine en eki konur.

2. Numaralandırmaya ikili bağ en küçük numarayı alacak şekilde başlanır.

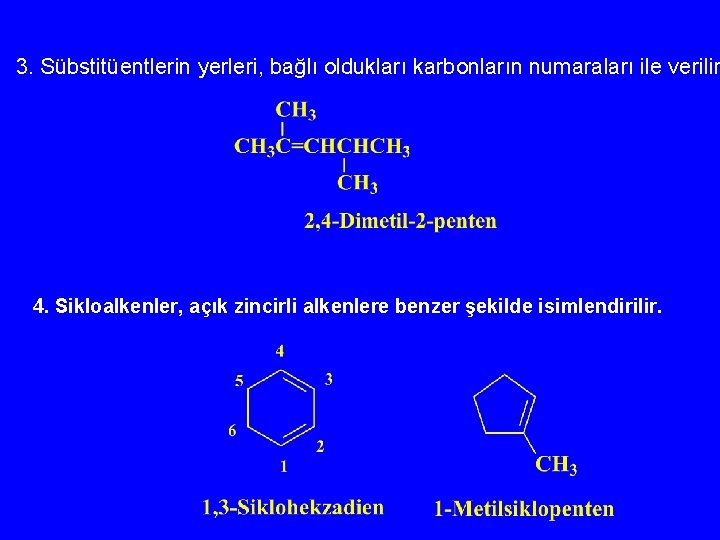
3. Sübstitüentlerin yerleri, bağlı oldukları karbonların numaraları ile verilir 4. Sikloalkenler, açık zincirli alkenlere benzer şekilde isimlendirilir.

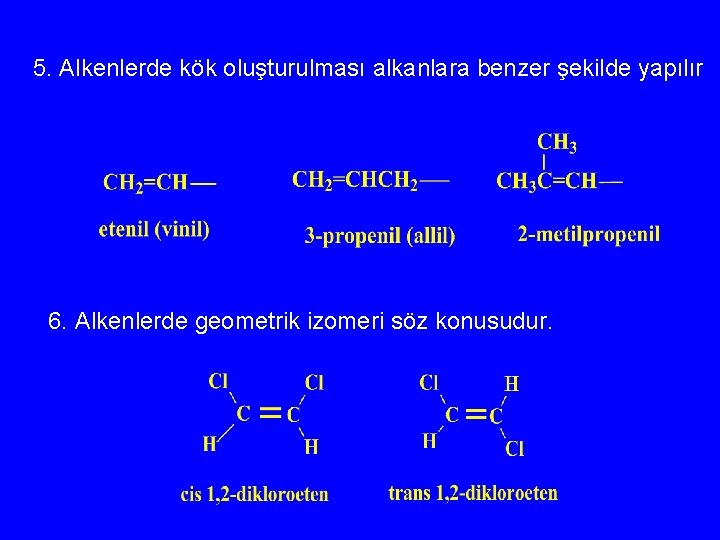
5. Alkenlerde kök oluşturulması alkanlara benzer şekilde yapılır 6. Alkenlerde geometrik izomeri söz konusudur.

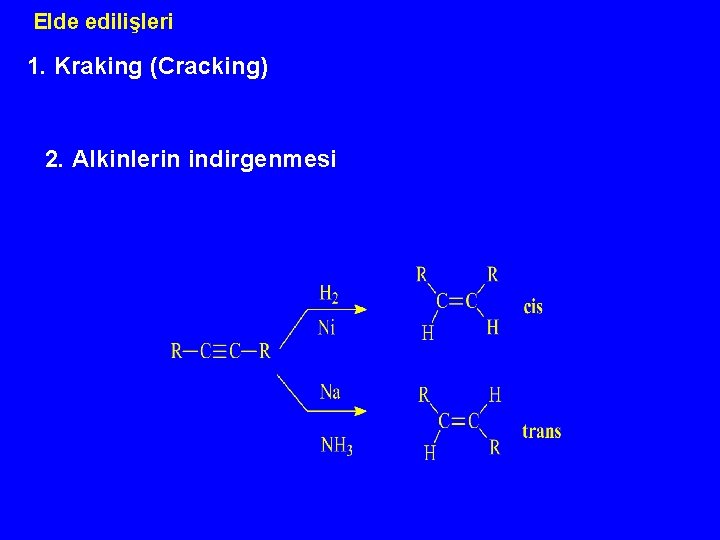
Elde edilişleri 1. Kraking (Cracking) 2. Alkinlerin indirgenmesi

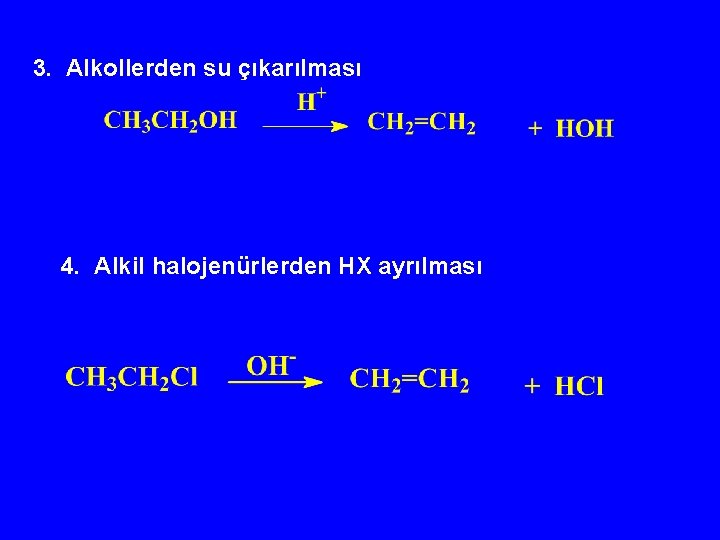
3. Alkollerden su çıkarılması 4. Alkil halojenürlerden HX ayrılması

5. Komşu dihalojenürlerin dehalojenasyonu

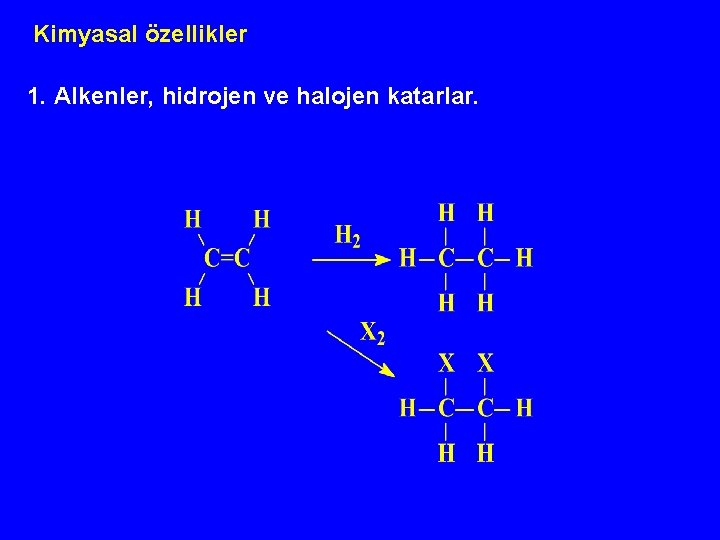
Kimyasal özellikler 1. Alkenler, hidrojen ve halojen katarlar.

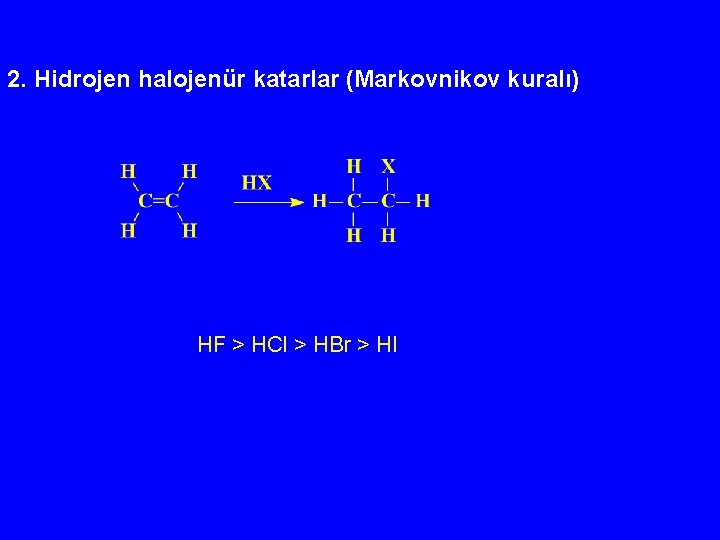
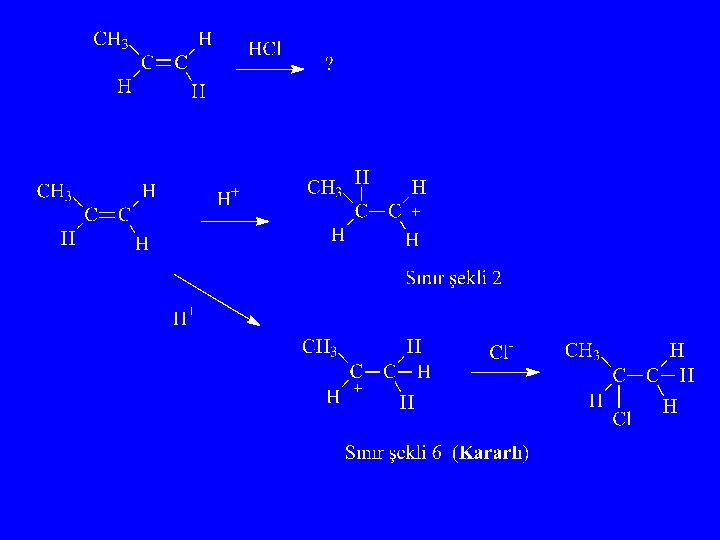
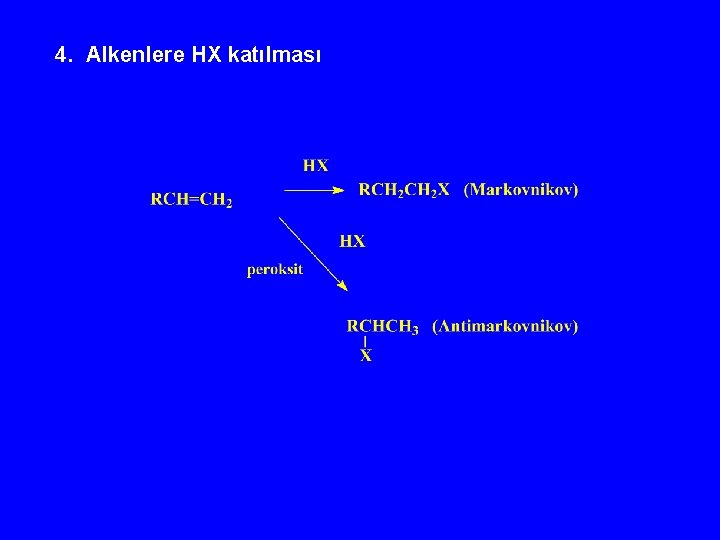
2. Hidrojen halojenür katarlar (Markovnikov kuralı) HF > HCl > HBr > HI


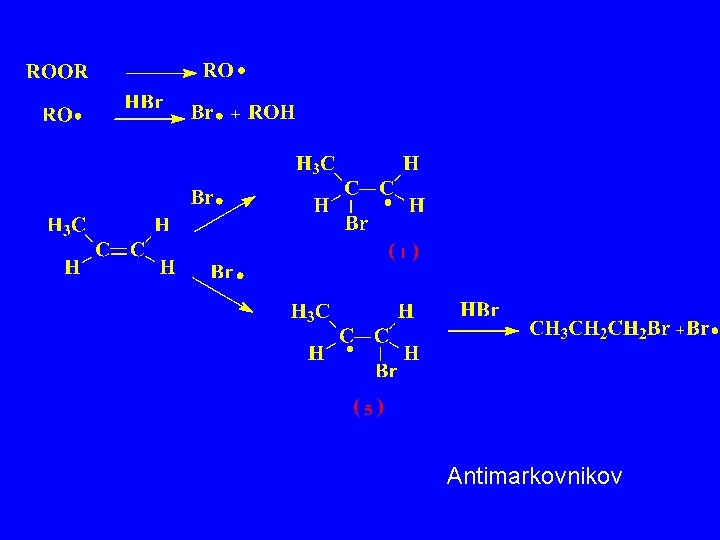
Antimarkovnikov

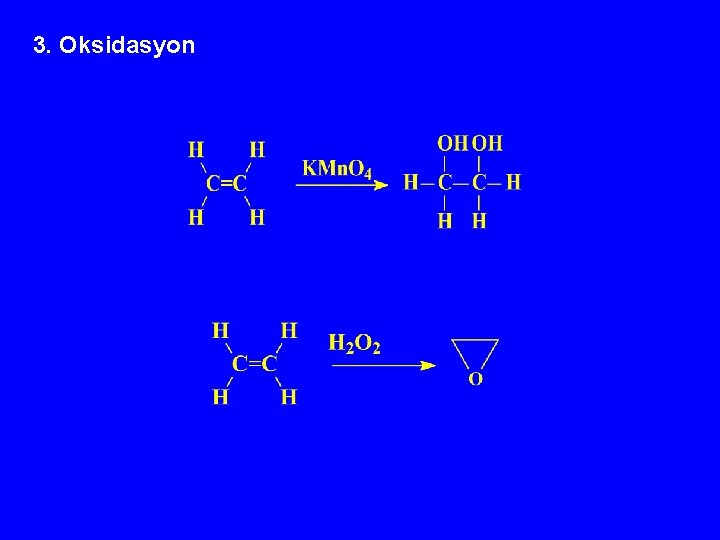
3. Oksidasyon

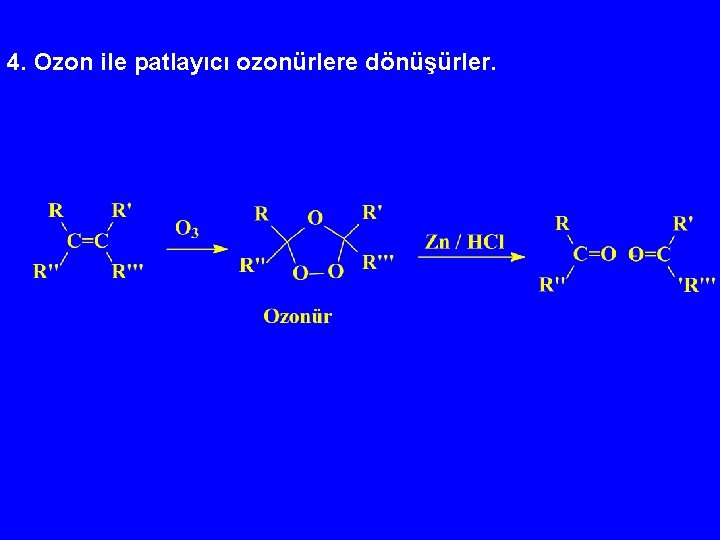
4. Ozon ile patlayıcı ozonürlere dönüşürler.

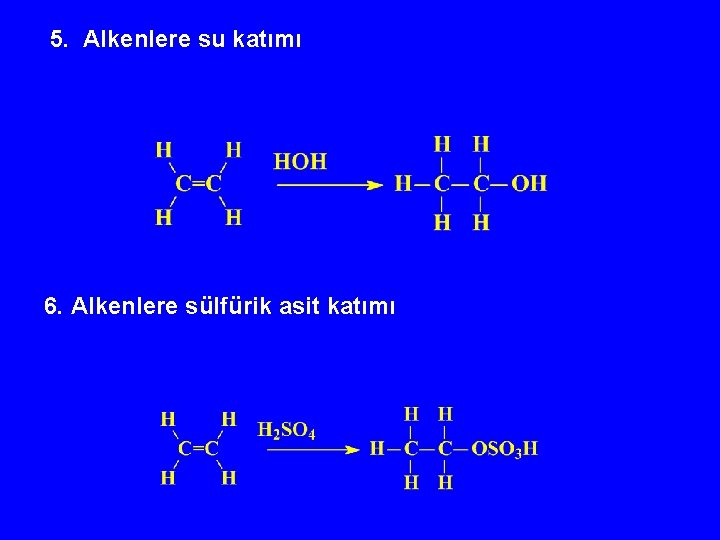
5. Alkenlere su katımı 6. Alkenlere sülfürik asit katımı

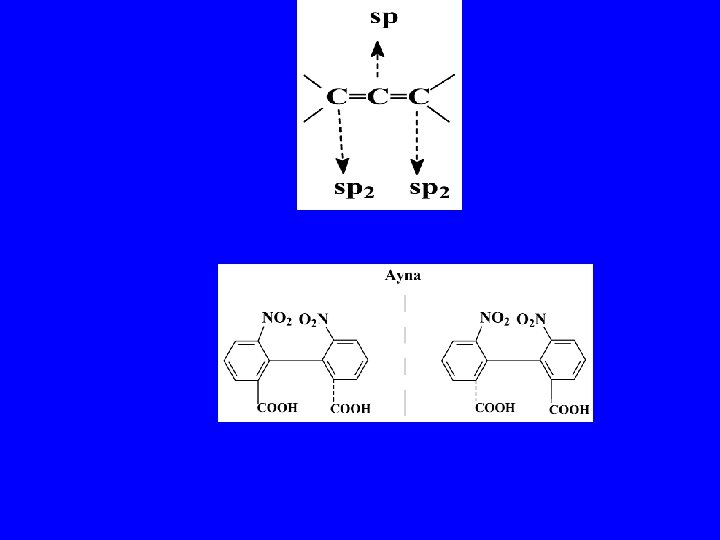
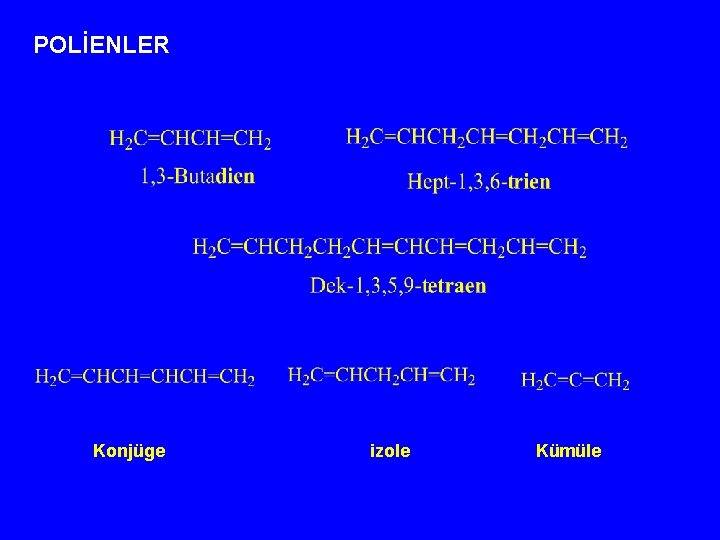
POLİENLER Konjüge izole Kümüle

ALKİNLER (ASETİLENİK BİLEŞİKLER) (C 2 H 2 n-2) İsimlendirilmeleri Karbon sayısına karşı gelen alkan isminin sonuna in eki getirilir. Diğer hususlar, alkan ve alkenlerde olduğu gibidir.

Yapıda hem ikili hem de üçlü bağ olması durumunda, numaralandırmada ikili bağ öncelik alır.

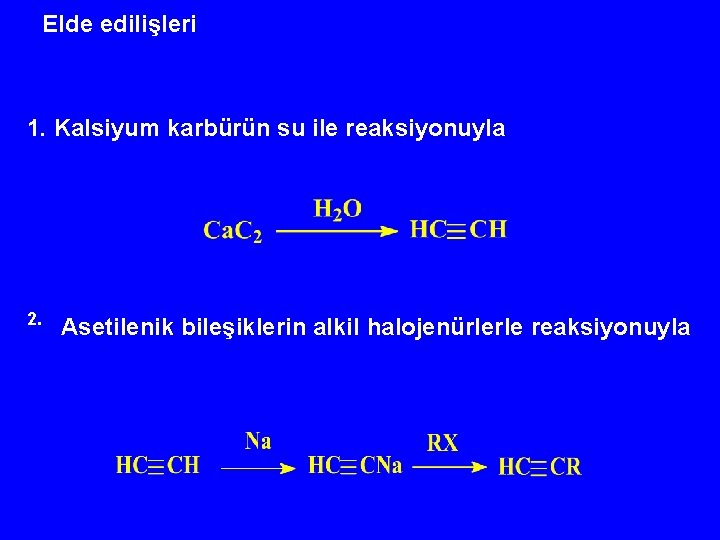
Elde edilişleri 1. Kalsiyum karbürün su ile reaksiyonuyla 2. Asetilenik bileşiklerin alkil halojenürlerle reaksiyonuyla

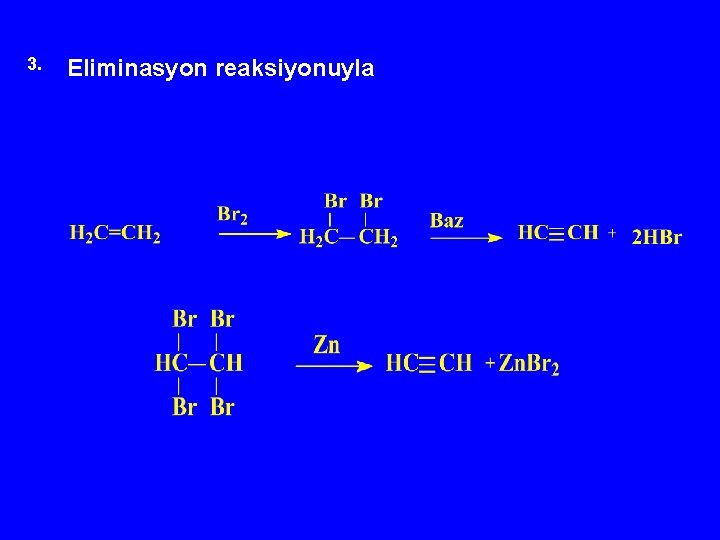
3. Eliminasyon reaksiyonuyla

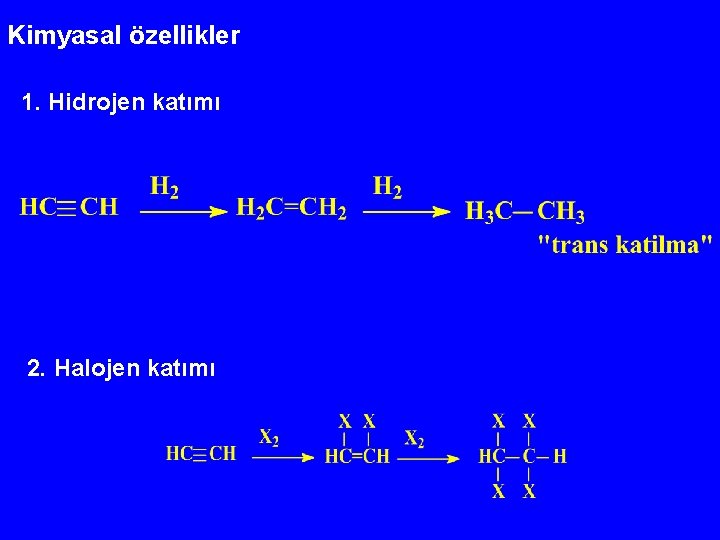
Kimyasal özellikler 1. Hidrojen katımı 2. Halojen katımı

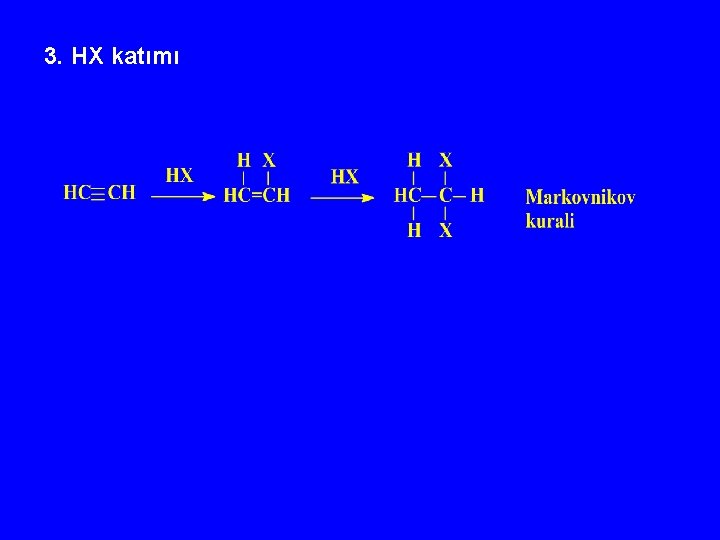
3. HX katımı

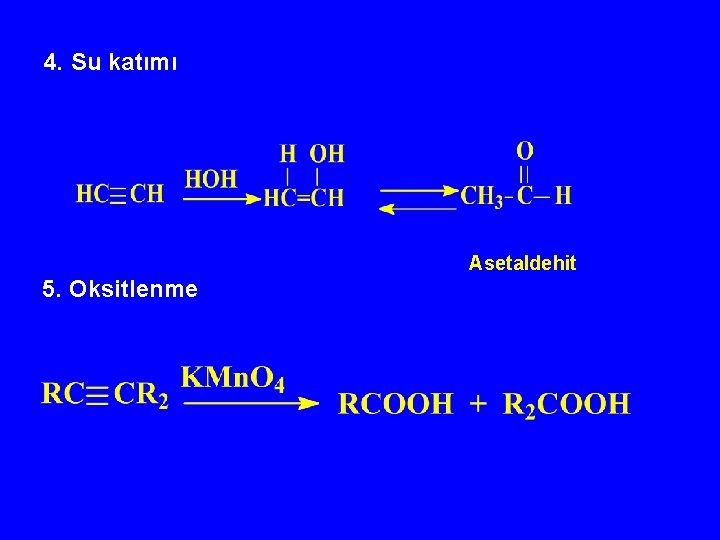
4. Su katımı Asetaldehit 5. Oksitlenme

ALKİL HALOJENÜRLER (R-X) C-X Ao Ej (kcal/mol) C-F C-Cl C-Br 1. 41 1. 76 1. 91 135 103 87. 5 C-I 2. 1 71. 5 İsimlendirilmeleri Yapıdaki alkil grubunun önüne halojenür adı eklenir. CH 3 F Metil fluorür C 2 H 5 Cl C 3 H 7 Br C 5 H 11 I Etil klorür Propil bromür Pentil iyodür

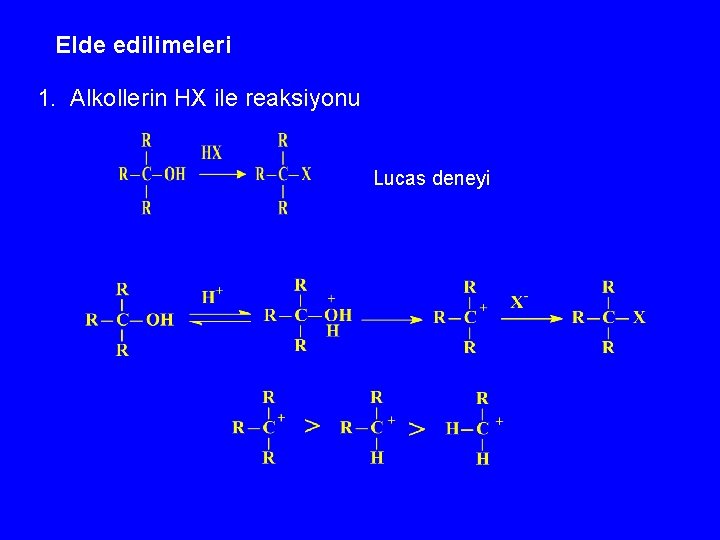
Elde edilimeleri 1. Alkollerin HX ile reaksiyonu Lucas deneyi

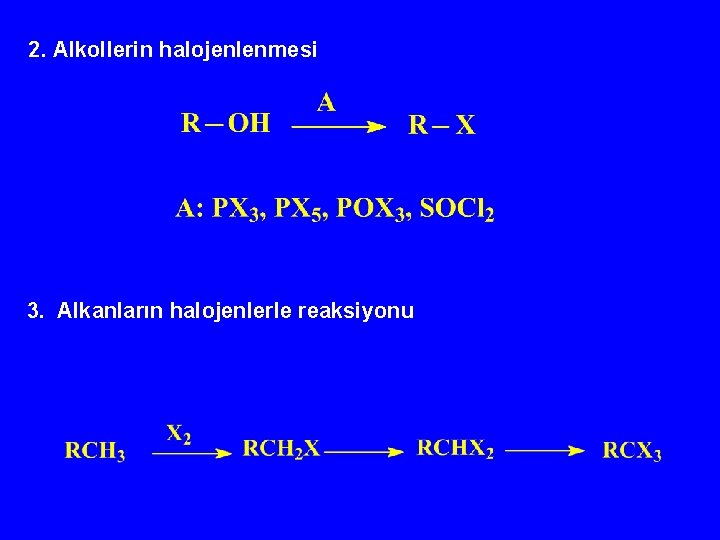
2. Alkollerin halojenlenmesi 3. Alkanların halojenlerle reaksiyonu

4. Alkenlere HX katılması

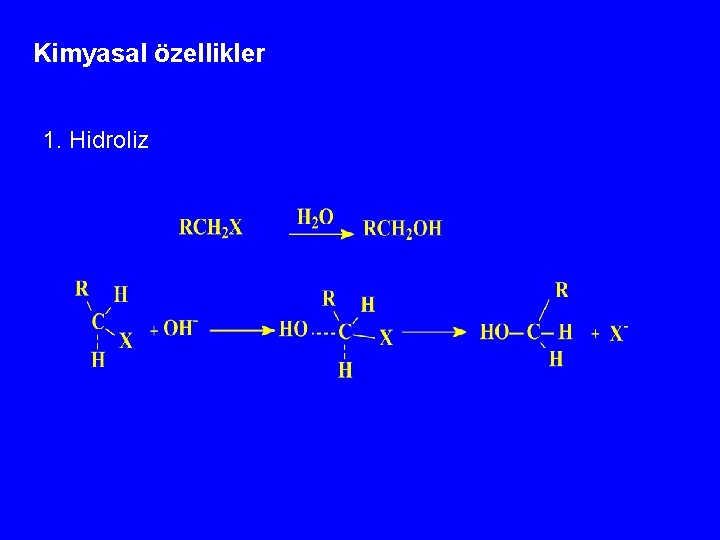
Kimyasal özellikler 1. Hidroliz

2. Grignard bileşikleri

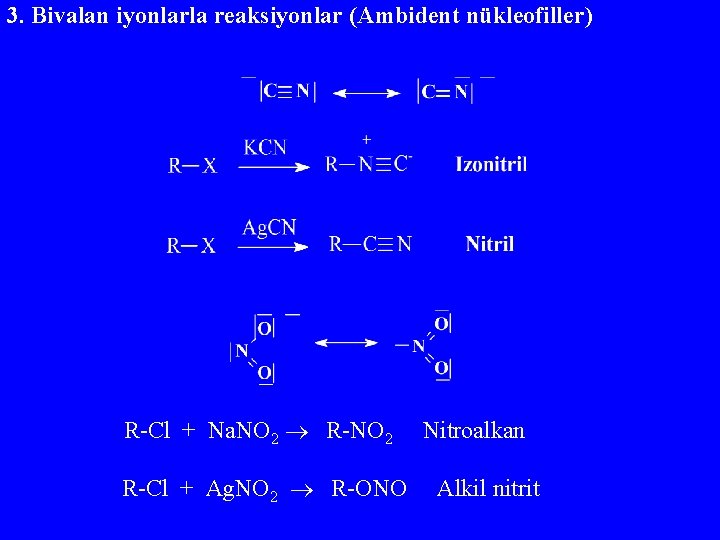
3. Bivalan iyonlarla reaksiyonlar (Ambident nükleofiller) R-Cl + Na. NO 2 R-NO 2 R-Cl + Ag. NO 2 R-ONO Nitroalkan Alkil nitrit

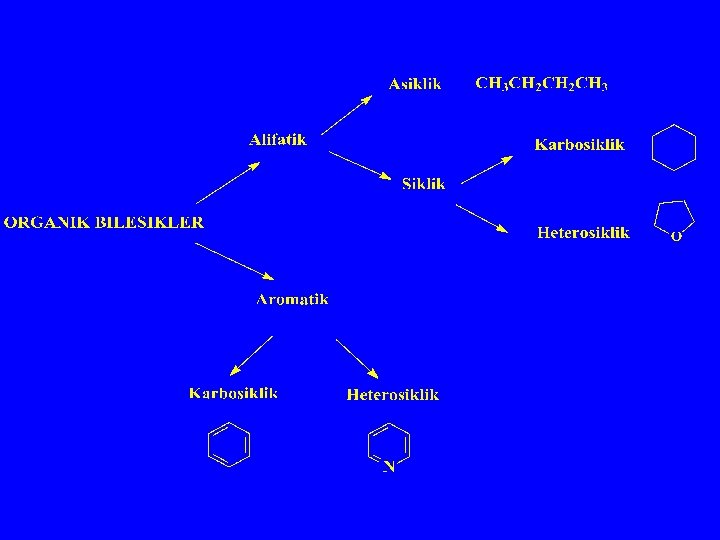
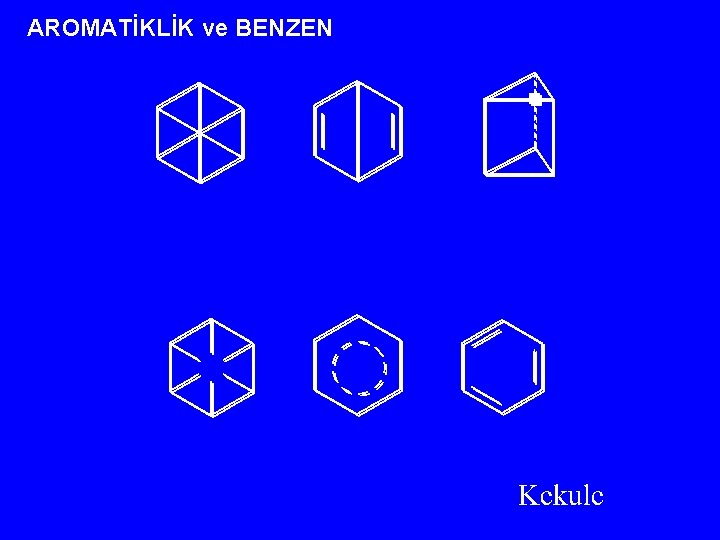
AROMATİKLİK ve BENZEN

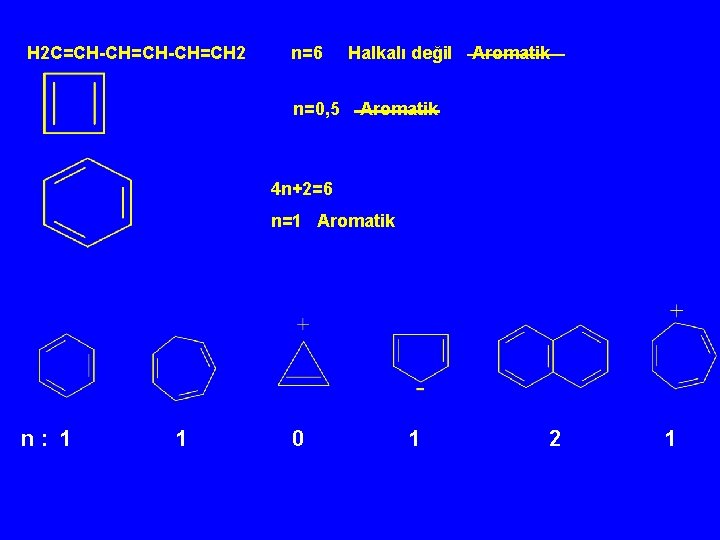
Aromatikliğin temel koşulları: - Halkalı bir yapı - Düzlemsellik - Molekülde konjüge durumda çifte bağlar veya yüklerin bulunuşu - Yapıdaki elektron sayısının n tam sayı olacak şekilde 4 n+2 ‘ye eşit olması (Hückel kuralı). elektron sayısını hesaplamada moleküldeki (+) yükler 0, (-) yükler 2 olarak değerlendirilmelidir.

H 2 C=CH-CH=CH 2 n=6 n=0, 5 Halkalı değil Aromatik 4 n+2=6 n=1 Aromatik n: 1 1 0 1 2 1


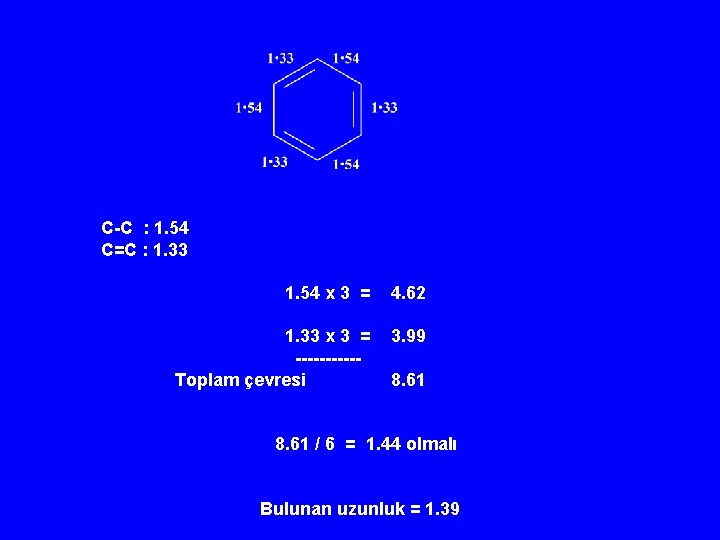
C-C : 1. 54 C=C : 1. 33 1. 54 x 3 = 4. 62 1. 33 x 3 = -----Toplam çevresi 3. 99 8. 61 / 6 = 1. 44 olmalı Bulunan uzunluk = 1. 39

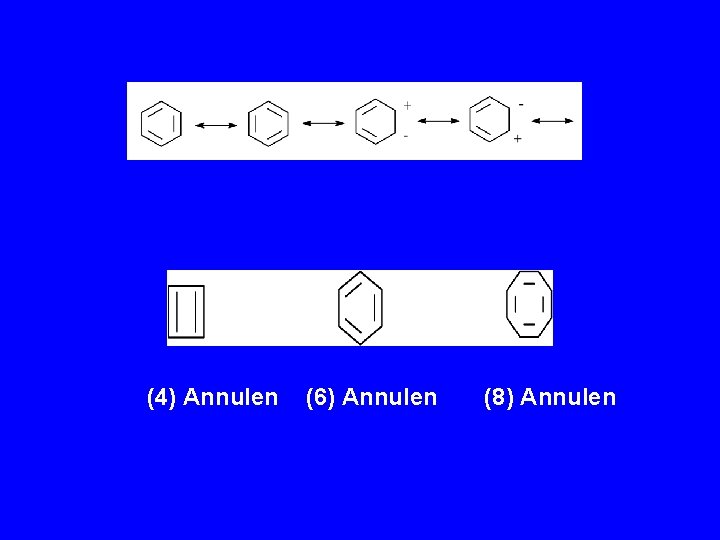
(4) Annulen (6) Annulen (8) Annulen

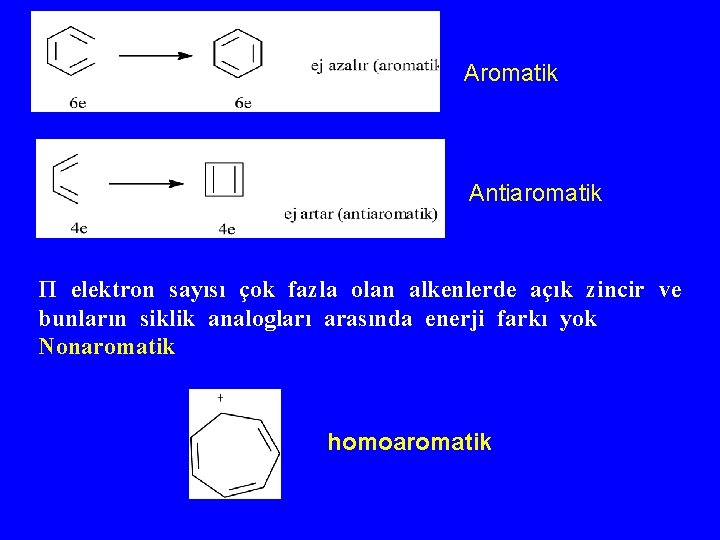
Aromatik Antiaromatik Π elektron sayısı çok fazla olan alkenlerde açık zincir ve bunların siklik analogları arasında enerji farkı yok Nonaromatik homoaromatik

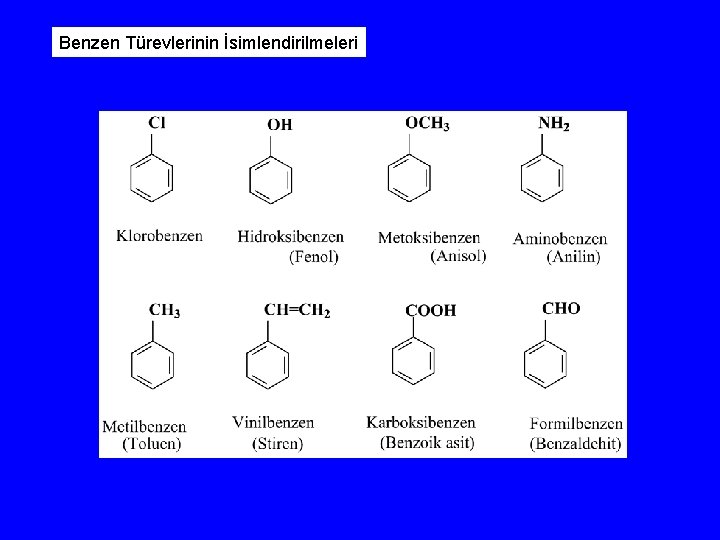
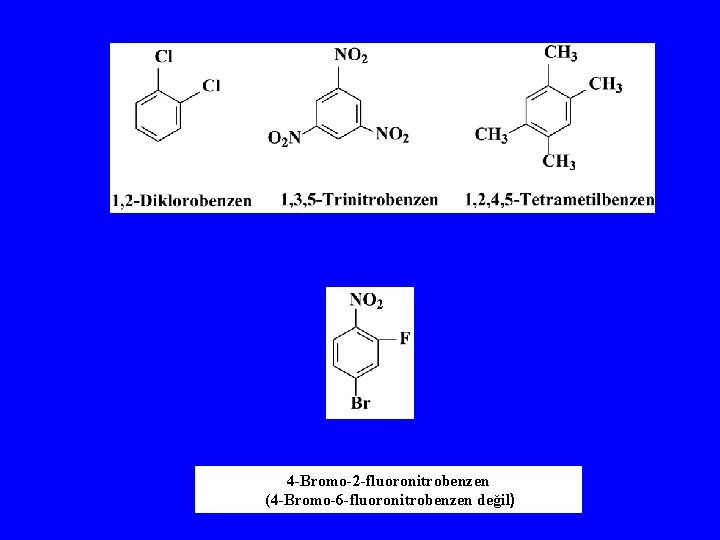
Benzen Türevlerinin İsimlendirilmeleri

4 -Bromo-2 -fluoronitrobenzen (4 -Bromo-6 -fluoronitrobenzen değil)

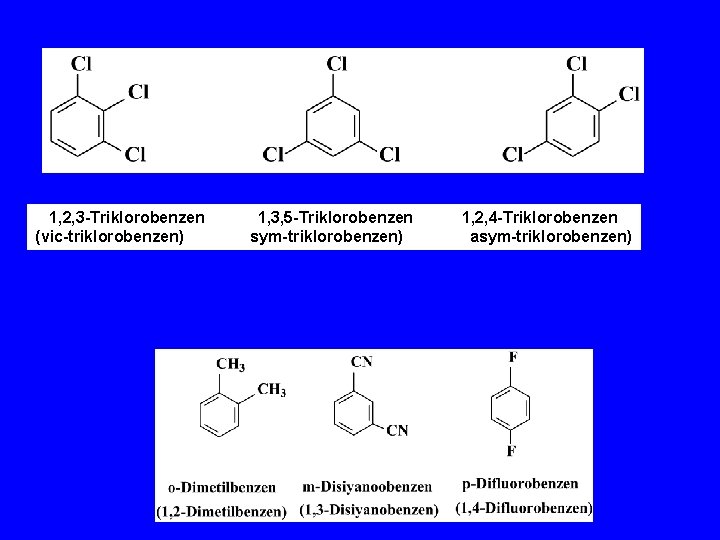
1, 2, 3 -Triklorobenzen (vic-triklorobenzen) 1, 3, 5 -Triklorobenzen sym-triklorobenzen) 1, 2, 4 -Triklorobenzen asym-triklorobenzen)

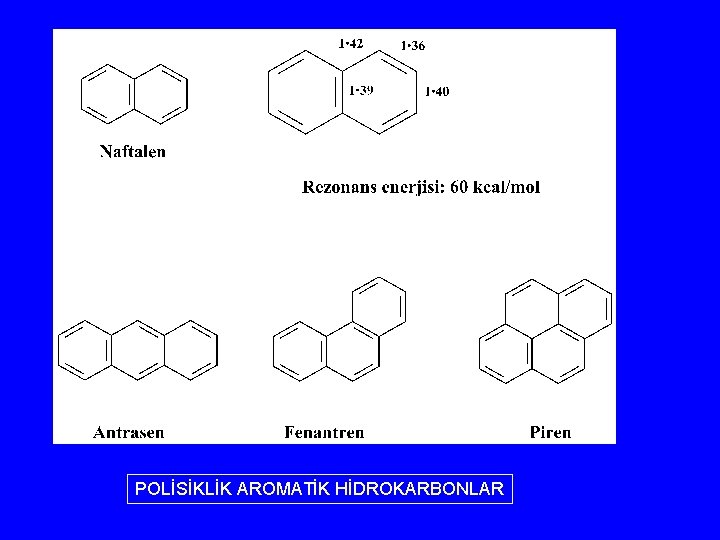
POLİSİKLİK AROMATİK HİDROKARBONLAR

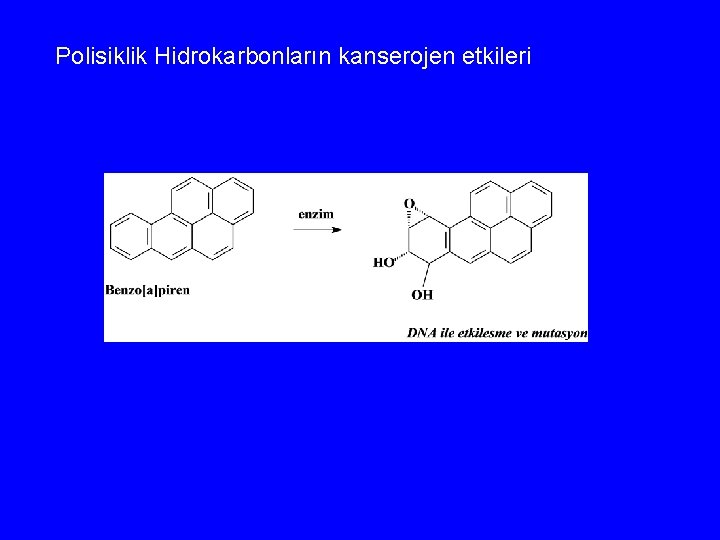
Polisiklik Hidrokarbonların kanserojen etkileri

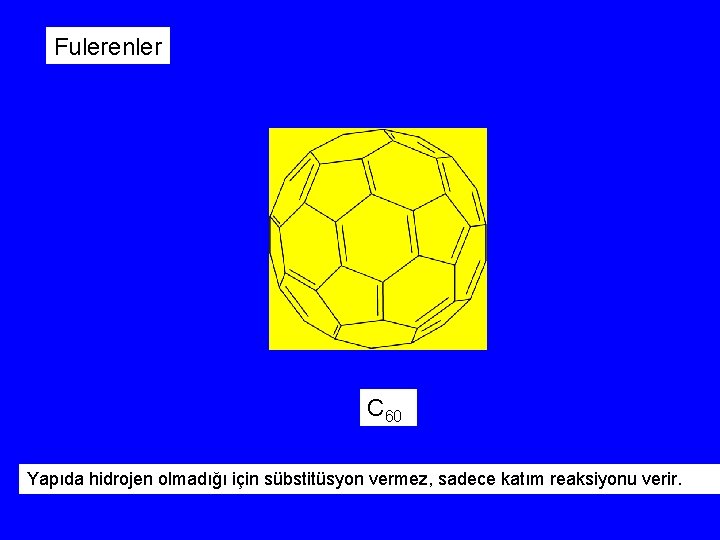
Fulerenler C 60 Yapıda hidrojen olmadığı için sübstitüsyon vermez, sadece katım reaksiyonu verir.

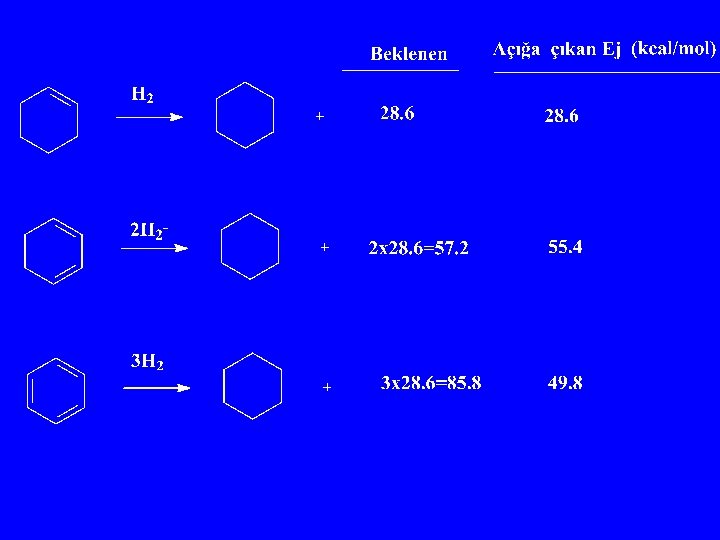
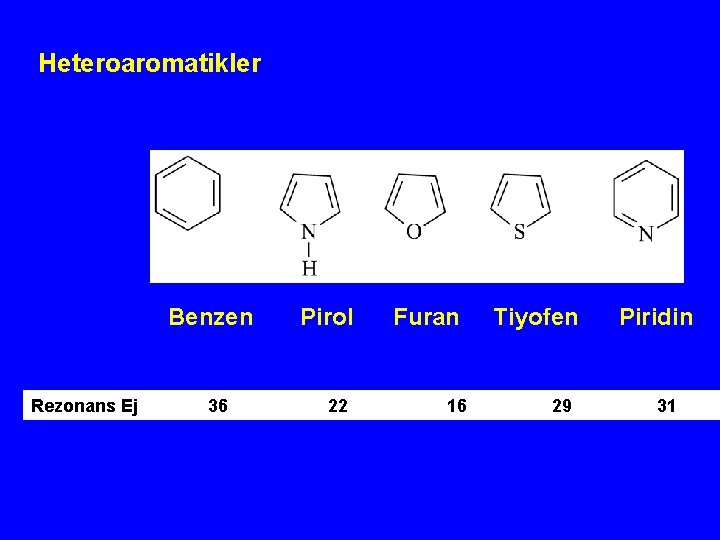
Heteroaromatikler Benzen Rezonans Ej 36 Pirol 22 Furan 16 Tiyofen 29 Piridin 31

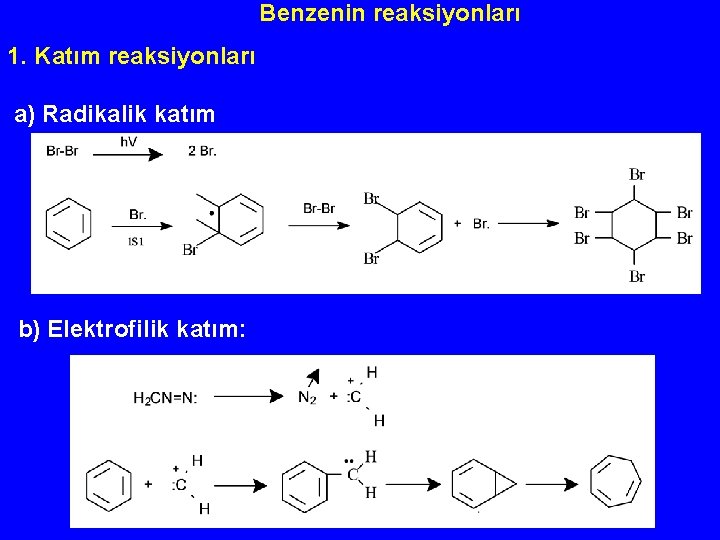
Benzenin reaksiyonları 1. Katım reaksiyonları a) Radikalik katım b) Elektrofilik katım:

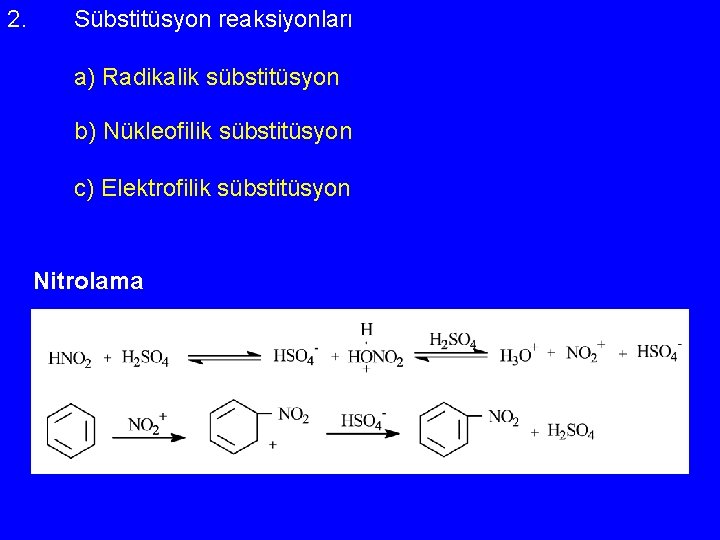
2. Sübstitüsyon reaksiyonları a) Radikalik sübstitüsyon b) Nükleofilik sübstitüsyon c) Elektrofilik sübstitüsyon Nitrolama

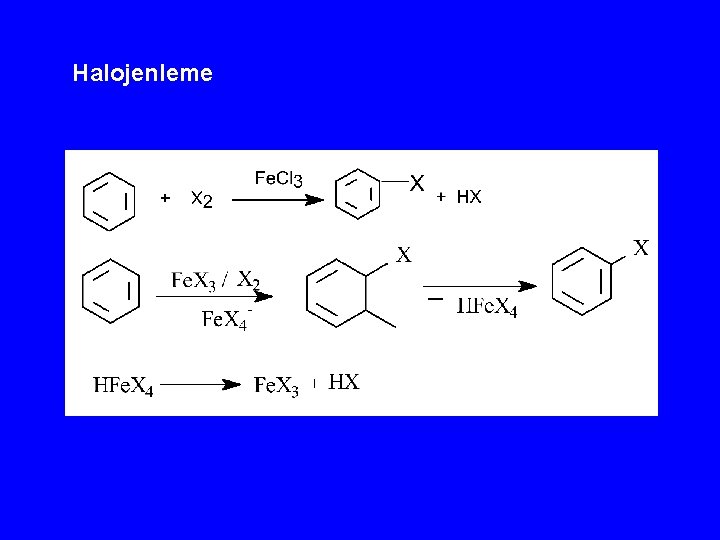
Halojenleme

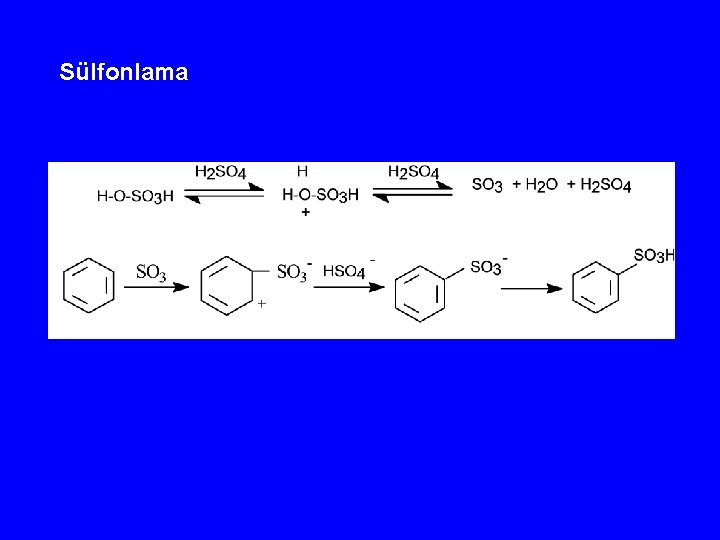
Sülfonlama

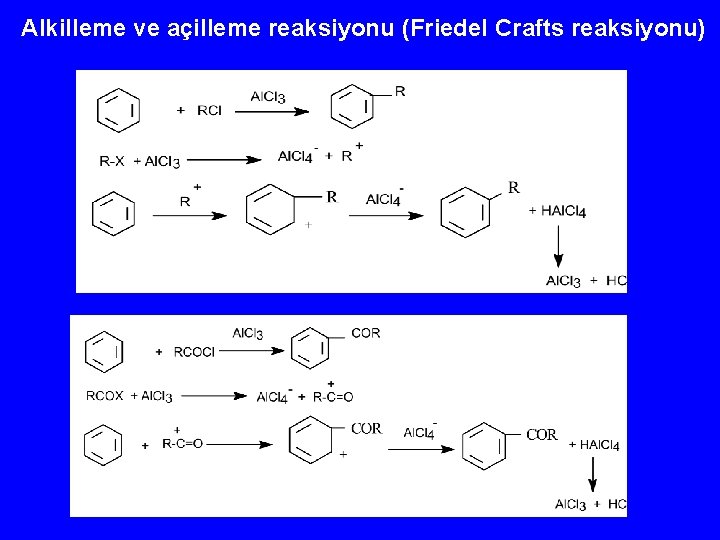
Alkilleme ve açilleme reaksiyonu (Friedel Crafts reaksiyonu)

Monosübstitüe benzen halkasına ikinci sübstitüentin girişi Meta yöneltici gruplar: +NR 3 < CCl 3 < NO 2 < CN < SO 3 H < CHO < COOH Orto-para yöneltici gruplar: OCOR, NHCOR, OH, NH 2, NR 2

X, Y’den daha elektronegatifse o-p yöneltici Y, X’den daha elektronegatifse m yöneltici

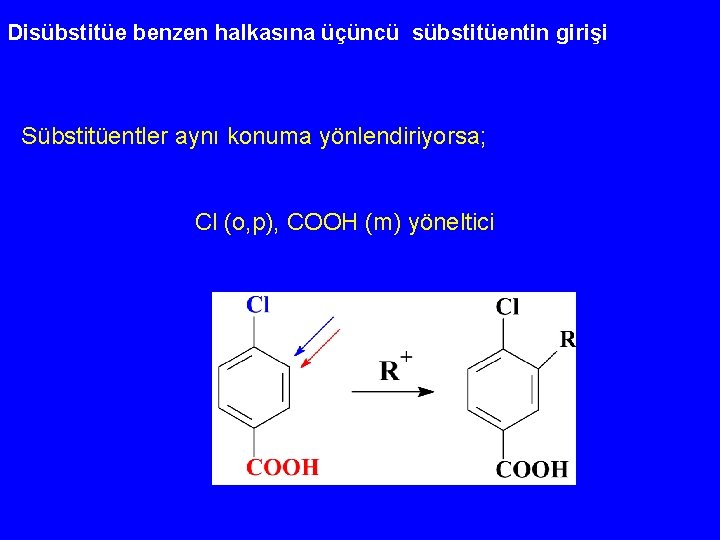
Disübstitüe benzen halkasına üçüncü sübstitüentin girişi Sübstitüentler aynı konuma yönlendiriyorsa; Cl (o, p), COOH (m) yöneltici

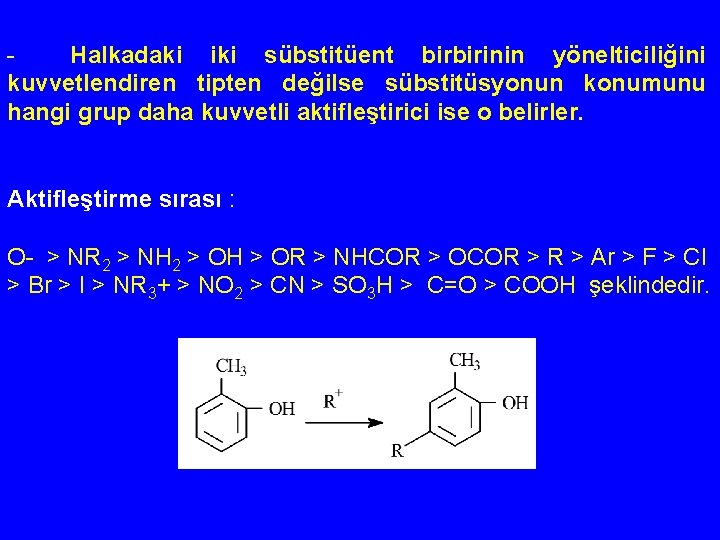
Halkadaki iki sübstitüent birbirinin yönelticiliğini kuvvetlendiren tipten değilse sübstitüsyonun konumunu hangi grup daha kuvvetli aktifleştirici ise o belirler. Aktifleştirme sırası : O- > NR 2 > NH 2 > OH > OR > NHCOR > OCOR > Ar > F > Cl > Br > I > NR 3+ > NO 2 > CN > SO 3 H > C=O > COOH şeklindedir.

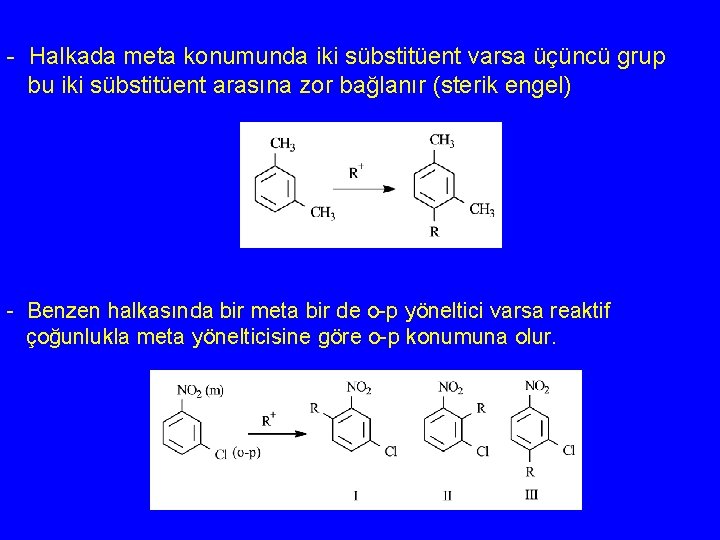
- Halkada meta konumunda iki sübstitüent varsa üçüncü grup bu iki sübstitüent arasına zor bağlanır (sterik engel) - Benzen halkasında bir meta bir de o-p yöneltici varsa reaktif çoğunlukla meta yönelticisine göre o-p konumuna olur.

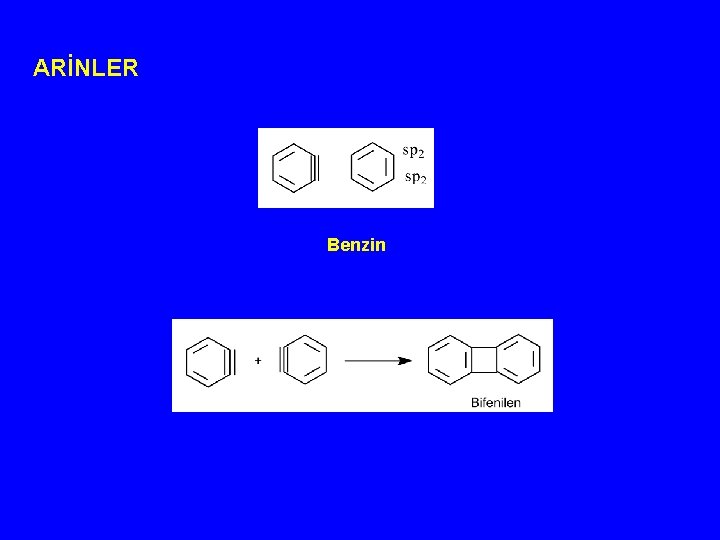
ARİNLER Benzin
