Blm 4 Kimyasal Reaksiyonlar Genel Kimya lkeler ve

Bölüm 4: Kimyasal Reaksiyonlar Genel Kimya İlkeler ve Modern Uygulamalar Petrucci • Harwood • Herring 1

Konular 2 4 -1 Kimyasal Reaksiyonlar ve Kimyasal Denklemler 4 -2 Kimyasal Denklemler ve Stokiyometri 4 -3 Sınırlayıcı Bileşenin Belirlenmesi 4 -4 Çözeltilerdeki Kimyasal Reaksiyonlar 4 -5 Reaksiyon Stokiyometrisinde diğer konular

Kimyasal Reaksiyonlar (Tepkimeler) ve Kimyasal Denklemler Bir kimyasal tepkimede tepkenlerin ürünlere dönüşümü esnasında: q Renk değişimi q Çökelek oluşumu q Gaz çıkışı q Isı salınması yada soğurulması Gibi kimyasal değişimlerin gözlenmesine ihtiyaç vardır. 3

Kimyasal Denklemler Bir veya daha fazla maddenin bir veya daha fazla yeni maddeye dönüştürüldüğü bir işlem kimyasal bir reaksiyondur (tepkime). Kimyasal bir denklem, kimyasal bir reaksiyon sırasında ne olacağını göstermek için semboller kullanır: tepkenler ürünler H 2 ve O 2 tepkimeyle H 2 O oluşturmasını 3 şekille gösterilir. 2 Hidrojen atomu + 1 Oksijen atomu 2 H 2 4 + O 2 1 su molekülü 2 H 2 O

Denkleme Maddelerin Durumunu Eklemek Ek bilgi sağlamak için, tepkenlerin ve ürünlerin fiziksel durumları, sırasıyla sulu çözelti, gaz, katı ve sıvı olmak üzere aq, g, k ve s harfleri kullanılarak gösterilebilir. 2 Mg(k) + O 2(g) 2 Mg. O(k) 2 CO(g) + O 2(g) Na. Cl(k) Ca. H 2(k) + 2 H 2 O(s) 5 2 CO 2(g) H 2 O Na. Cl(aq) Ca(OH)2(aq) + 2 H 2(g)

Kimyasal Tepkimeler Azot monoksit + Oksijen → Azot dioksit Basamak 1: Kimyasal semboller kullanılarak tepkimenin yazılması. Basamak 2: Kimyasal denklemin denkleştirilmesi. 2 NO (g) + 1 O 2 (g) → 2 NO 2 (g) 6

Kimyasal Denklemler Nasıl Okunur? 2 Mg + O 2 2 Mg. O 2 Mg atomu + 1 O 2 atomu 2 Mg. O formül birimi verir veya 2 mol Mg + 1 mol O 2 = 2 mol Mg. O veya 48. 6 gram Mg + 32. 0 gram O 2 = 80. 6 gram Mg. O Yanlış 2 gram Mg + 1 mol O 2 tepkimede 2 g Mg. O verir 7

Denklem Denkleştirmeler 1. Sol tarafta tepkenler için doğru formülleri ve denklemin sağ tarafında ürünler için doğru formülleri yazın. Etan, karbondioksit ve su oluşturmak için oksijenle reaksiyona girer. C 2 H 6 + O 2 CO 2 + H 2 O 2. Her bir elementin atom sayısını denklemin her iki tarafında aynı yapmak için formüllerin (katsayılar) önündeki sayıları değiştirin. Alt indisleri değiştirmeyin. Doğru: 2 C 2 H 6 8 Yanlış: C 4 H 12
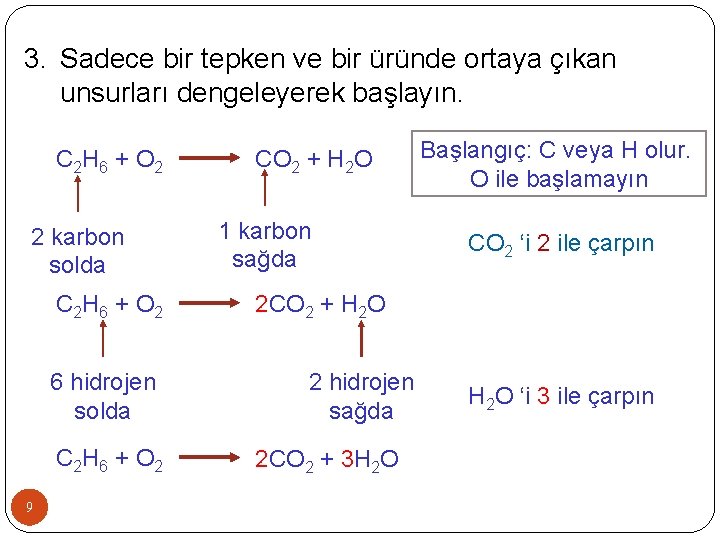
3. Sadece bir tepken ve bir üründe ortaya çıkan unsurları dengeleyerek başlayın. C 2 H 6 + O 2 2 karbon solda C 2 H 6 + O 2 6 hidrojen solda C 2 H 6 + O 2 9 CO 2 + H 2 O 1 karbon sağda Başlangıç: C veya H olur. O ile başlamayın CO 2 ‘i 2 ile çarpın 2 CO 2 + H 2 O 2 hidrojen sağda 2 CO 2 + 3 H 2 O ‘i 3 ile çarpın

4. İki veya daha fazla tepken veya üründe ortaya çıkan elementleri dengeleyin. C 2 H 6 + O 2 2 Oksijen solda 10 2 CO 2 + 3 H 2 O Çarp: O 2 ile 7 2 4 Oksijen + 3 Oksijen = 7 Oksijen sağda (3 x 1) (2 x 2) C 2 H 6 + 7 O 2 2 2 CO 2 + 3 H 2 O 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O Kesiri kaldır; İki tarafıda 2 ile çarpın

5. Denklemin her iki tarafında aynı sayıda atom türünün bulunduğundan emin olun. 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O 4 C (2 x 2) 4 C 12 H (2 x 6) 12 H (6 x 2) 14 O (7 x 2) 14 O (4 x 2 + 6) Sağlaması: Tepkenler 4 C 12 H 14 O 11 Ürünler 4 C 12 H 14 O

Denklem Denkleştirmeler Asla denklem dışı formüller veya atomlar ilave edilmemelidir. NO + O 2 → NO 2 + O Denklemi denkleştirmek için formüller değiştirilmemelidir. NO + O 2 → NO 3 Denkleştirilmiş eşitlikte, her iki taraftaki atom sayıları birbirine eşittir. 12

Denklem Denkleştirmeler q Denlemin her iki tarafında birer bileşikte aynı element mevcutsa önce onu denkleştirin. q Serbest elementleri en son denkleştirin. q Değişmeden kalan çoklu atom gruplarını değiştirmeden denkleştirin. q Katsayılar tam sayı ya da kesirli sayılarla denkleştirilebilir, kesirli sayılardan kurtarabilmek için belirli bir çarpan kullanılabilir. 13

Örnek Trietilenglikol Bir eşitliğin yazılıp denkleştirilmesi; karbon-hidrojenoksijen içeren bir bileşiğin yanması. Sıvı trietilenglikol, C 6 H 14 O 4, vinil ve poliüretan plastikleri için çözücü olarak kullanılır. Bu bileşiğin tam yanmasına ait denklemi yazıp denkleştiriniz. 14
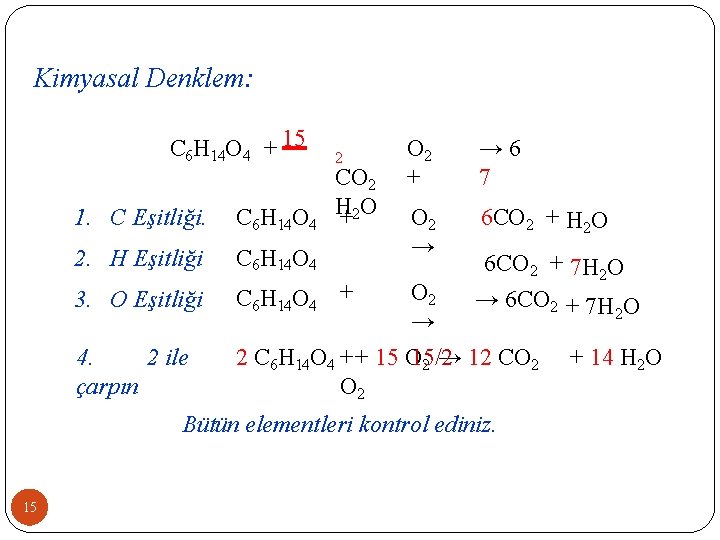
Kimyasal Denklem: C 6 H 14 O 4 + 15 2 CO 2 H +2 O 1. C Eşitliği. C 6 H 14 O 4 2. H Eşitliği C 6 H 14 O 4 3. O Eşitliği C 6 H 14 O 4 + 4. 2 ile çarpın O 2 + → 6 7 O 2 → 6 CO 2 + H 2 O 6 CO 2 + 7 H 2 O → 6 CO 2 + 7 H O O 2 → 2 C 6 H 14 O 4 + + 15 O 15/2 2 → 12 CO 2 Bütün elementleri kontrol ediniz. 15 2 + 14 H 2 O

Alıştırma sorusu: Gece boyunca, karbondioksit (CO 2) bitkilerin yapraklarında glikoz (C 6 H 12 O 6) ve oksijen gazı (O 2) oluşturmak için suyla reaksiyona girer. Üretilen glikoz, bitkiler için enerji kaynağı olarak kullanılır. Bu reaksiyon için dengeli bir denklem yazın. Cvp: 6 CO 2 (g) + 6 H 2 O (s) � C 6 H 12 O 6 (k) + 6 O 2 (g) 16
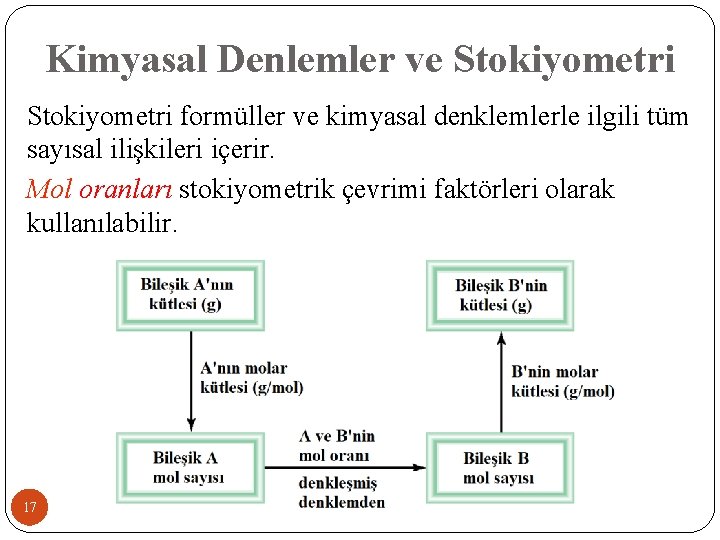
Kimyasal Denlemler ve Stokiyometri formüller ve kimyasal denklemlerle ilgili tüm sayısal ilişkileri içerir. Mol oranları stokiyometrik çevrimi faktörleri olarak kullanılabilir. 17

Tepken ve ürünlerin mol sayıları arasındaki ilişki. 2, 72 mol H 2 nin fazla miktardaki O 2 ile yakılması sonucunda kaç mol H 2 O oluşur? Kimyasal Denklemi yazın Denklemi denkleştirin: 2 H 2 + O 2 → 2 H 2 O Denklemdeki mole oranlarını veya sitokiyometrik faktörü kullanın: n. H 2 O = 2, 72 mol H 2 × 2 mol H 2 O = 2, 72 mol H 2 O 2 mol H 2 18

Sitokiyometrik hesaplamalarda hacim, yoğunluk ve yüzde bileşim gibi ilave dönüşüm faktörlerinin kullanılması. Uçak yapımında kullanılan bir alaşım kütlece 93, 7% Al ve 6, 3% Cu içeriyor. Bu alaşımın yoğunluğu 2, 85 g/cm 3 tür. 0, 691 cm 3 alaşım parçası aşırı miktarda HCl (aq) ile tepkimeye giriyor: Eğer Cu’nun tepkimeye girmediği aluminyumun tamamının HCl ile tepkimeye girdiği varsayılırsa elde edilen H 2(g)’nin kütlesini hesaplayınız. 19
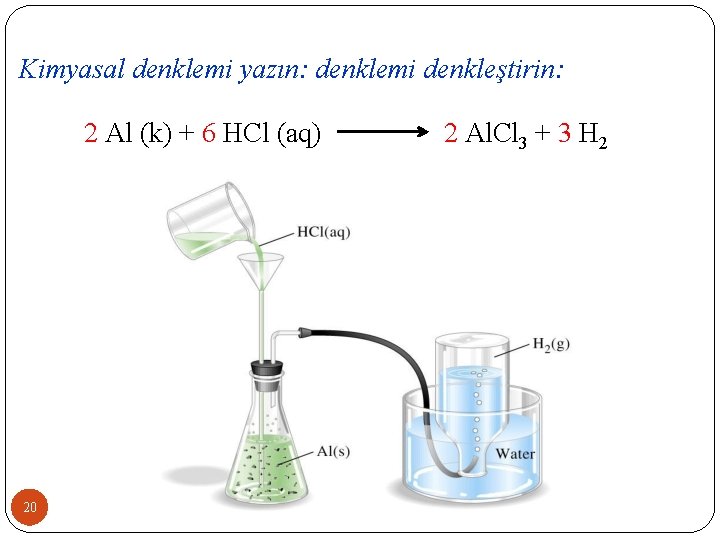
Kimyasal denklemi yazın: denklemi denkleştirin: 2 Al (k) + 6 HCl (aq) 20 2 Al. Cl 3 + 3 H 2

2 Al + 6 HCl → 2 Al. Cl 3 + 3 H 2 Yöntem: cm 3 alloy → g Al → mole Al → mol H 2 → g H 2 5 tane çevrim faktörüne ihtiyaç var! Denklemi yazın ve hesaplayın m. H 2 3 = 0, 691 cm 93, 7 g Al × 2, 85 g alaşım × 3 1 cm alaşım 100 g alaşım 1 mol Al × 3 mol H 2 × 2, 016 g H 2 26, 98 g Al 2 mol Al 1 mol H 2 21 = 0, 207 g H 2

Alıştırma sorusu: Yediğimiz yiyecekler vücudumuzda büyüme ve işlev için enerji sağlamak amacıyla bozulur veya parçalanır. Bu çok karmaşık işlem için genel bir genel denklem, glikozun (C 6 H 12 O 6) karbon dioksit (CO 2) ve suya (H 2 O) parçalanmasını gösterir: Belirli bir süre boyunca bir kişi tarafından 856 g C 6 H 12 O 6 tüketilirse, üretilen CO 2 kütlesi nedir? Cvp: 1, 25 x 103 g CO 2 22

Alıştırma sorusu 2: Tüm alkali metaller su ile reaksiyona girerek hidrojen gazı ve karşılık gelen alkali metal hidroksit üretir. Tipik bir reaksiyon, lityum ve su arasındadır: 9, 89 g H 2 üretmek için kaç gram Li gerekir? Cvp: 68, 1 g Li 23

Alıştırma sorusu 3: Bir otomobilin katalitik konvertörü, egzoz gazındaki toksik gazları daha az toksik gazlara dönüştürür. Bu toksik gazlar genellikle motorlarda petrolün tamamlanmamış yanma ürünleridir. Karbon monoksit bu çok zehirli gazlardan biridir. Karbon monoksit (CO), kimyasal reaksiyona göre bir katalitik konvertörde daha az toksik maddeye sahip olan karbondioksite (CO 2) dönüştürülür: CO (g) + ½ O 2 (g) �CO 2 (g) 100. 0 g karbon monoksitten kaç gram karbondioksit üretilir? (MCO 2 = 44, 01 g/mol, MCO = 28, 01 g/mol) Cvp: 157, 14 g 24

Alıştırma sorusu 4: Diğer bir zehirli egzoz gazı NO 3'tır. Katalitik bir konvertörde, NO 3 reaksiyonla azot (N 2) ve oksijene (O 2) dönüştürülür: 2 NO 3 (g) � 3 O 2 (g) + N 2 (g) 125, 0 g O 2 üretmek için kaç gram NO 3 gerekir? (MNO 3 = 62, 0 g/mol, MO 2 = 32, 0 g/mol) 25 Cvp: 161. 4 g

Sınırlayıcı Bileşenin Belirlenmesi Sınırlayıcı Bileşen: Reaksiyonda ilk olarak kullanılan tepken. Tepkime sırasında tamamen tükenen bileşik. Oluşan ürünlerin miktarlarını belirler. Oluşan en fazla ürün miktarı, bu tepkenin ne kadarının tepkimeye girdiğine bağlıdır. Kimyasal bir reaksiyonda yeterince tepken bulunmadığında, bu tepken tüketilecek ve reaksiyon duracaktır. Maksimum verimin elde edilmesini sağlamak için büyük miktarda başka bir tepken kullanılır verilir (aşırı derecede). Aşırı tepkenler: Sınırlayıcı tepkenin miktarı ile tepkimeye girmek için gerekenden daha büyük miktarlarda bulunan 26 tepkenler.
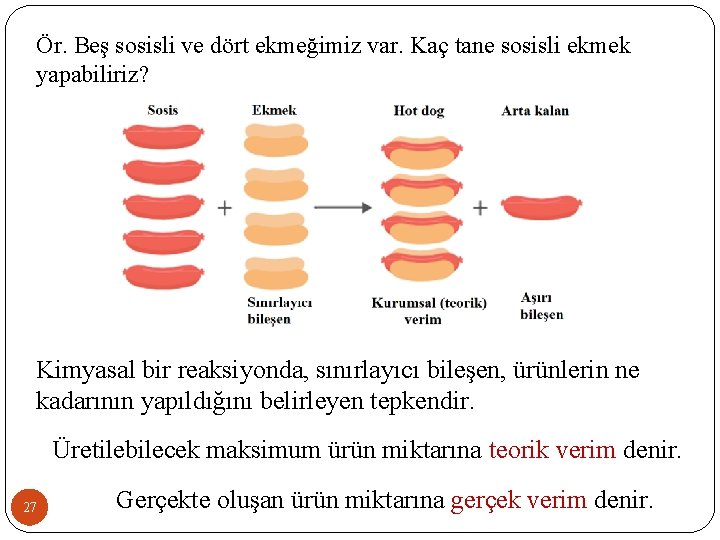
Ör. Beş sosisli ve dört ekmeğimiz var. Kaç tane sosisli ekmek yapabiliriz? Kimyasal bir reaksiyonda, sınırlayıcı bileşen, ürünlerin ne kadarının yapıldığını belirleyen tepkendir. Üretilebilecek maksimum ürün miktarına teorik verim denir. 27 Gerçekte oluşan ürün miktarına gerçek verim denir.

% Verim = Gerçek verim Kurumsal (Teorik) Verim x 100% Teorik verime ulaşan tepken sınırlayıcı bileşendir. Önceki örnekte, Sınırlayıcı Bileşen: Ekmek – 4 tane Daha küçük miktar sınırlayıcı bileşendir. Aşırı Bileşen: Sosis – 5 tane Teorik verim: 4 sosisli ekmek Deney sonucu elde edilen veri – Gerçek verim: 3 sosisli ekmek % Verim = 28 3 x 100% = 75% 4

Sınırlayıcı Bileşen Problemleri a. A+ b. B+ c. C d. D+ e. E+ f F 1. Problemin Sınılayıcı Bileşen problemi olduğunun anlaşılması- 2. 3. 4. 5. 29 problemde birden fazla tepken için kütle, molarite, hacim vb. olarak madde miktarının verilmesi durumu. Her tepkenin mol miktarlarını hesaplayın! Elde edilen mol miktarlarını eşitlikteki katsayılara bölün (a, b, c vs. )! Hangi tepken için elde edilen sayı daha küçükse o tepken sınırlayıcı bileşiktir! Sınırlayıcı bileşiğin mol miktarını kullanarak ürünlerin ve fazla miktardaki diğer tepkenlerin mol miktarlarını hesaplayın. Bu mol miktarlarından istenilen birimlere (kütle, hacim, mol, atom sayısı vs. ) ulaşın.

Örnek: Roketçiliğin ilk zamanlarında yakıt olarak iki sıvı madde olan hidrazin (N 2 H 4) ve diazot tetroksit (N 2 O 4) den oluşan bir karışım kullanılmaktaydı. Bu maddeler birbiriyle temas ettiğinde yanarak azot gazı ve su buharı oluştururlar. Tam olarak 1, 00 x 102 g N 2 H 4 ve 2, 00 x 102 g N 2 O 4 karıştırıldığında kaç gram azot gazı açığa çıkar? Strateji: İki tepken bileşiğin de miktarları verildiğinden sınırlayıcı bileşiğin bulunmasını gerektiren bir problem ile karşıyayız. 30

1. Her bir tepkenin mol miktarlarını hesaplayın. mol kütlesi N 2 H 4 = ( 2 x 14, 01 + 4 x 1, 008 ) = 32, 05 g/mol kütlesi H 2 O 4 = ( 2 x 14, 01 + 4 x 16, 00 ) = 92, 02 g/mol 2. Eşitliği yazıp denkleştirdikten sonra elde edilen bu mol miktarlarını eşitlikteki katsayılara bölün ve sınırlayıcı bileşeği bulun. 2 N 2 H 4 (k) + N 2 O 4 (k) (hidrazin) (diazot tetroksit) 1, 00 x 102 g Mol # N 2 H 4 = 32, 05 g/mol Mol# N 2 O 4 = 31 3 N 2 (g) + 4 H 2 O (g) + Energy = 3, 12 mol N 2 H 4 2, 00 x 102 g 92, 02 g/mol = 2, 17 mol N 2 O 4

Katsayılarla bölün: 3, 12 mol / 2 = 1, 56 mol N 2 H 4 Sınırlayıcı! 2, 17 mol / 1 = 2, 17 mol N 2 O 4 3. Sınırlayıcı bileşiğin mol sayısı ve kimyasal eşitlikteki oranları kullanarak azotun mol sayısını ve bundan da kütlesini hesaplayın. 3 mol N 2 Oluşan Azot = 3, 12 mol N 2 H 4 x = 4, 68 mol N 2 2 mol N 2 H 4 Azotun Kütlesi = 4, 68 mol N 2 x 28, 02 g N 2 / mol = 131 g N 2 32

Başka bir yöntemde ürünün mol sayısını hesaplamaktır. 2. Eşitliği yazıp denkleştirdikten sonra elde edilen bu mol miktarlarınldan kimyasal eşitlikteki oranları kullanarak ürünün mol sayısını bulun ve sınırlayıcı bileşeği bulun. 3 mol N 2 3, 12 mol N 2 H 4 x = 4, 68 mol N 2 2 mol N 2 H 4 Sınırlayıcı: N 2 H 4 3 mol N 2 2, 17 mol N 2 O 4 x = 6, 51 mol N 2 O 4 3. Sınırlayıcı bileşiğin mol sayısından da kütlesini hesaplayın. Azotun Kütlesi = 4, 68 mol N 2 x 28, 02 g N 2 / mol = 131 g N 2 33
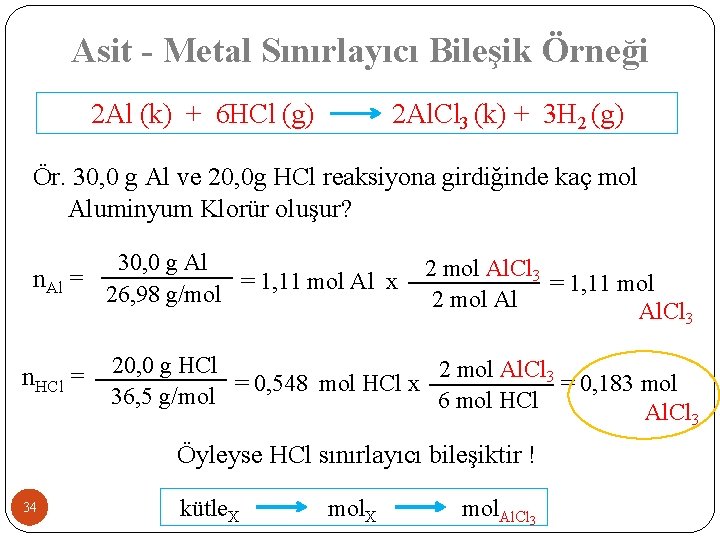
Asit - Metal Sınırlayıcı Bileşik Örneği 2 Al (k) + 6 HCl (g) 2 Al. Cl 3 (k) + 3 H 2 (g) Ör. 30, 0 g Al ve 20, 0 g HCl reaksiyona girdiğinde kaç mol Aluminyum Klorür oluşur? 30, 0 g Al n. Al = = 1, 11 mol Al x 26, 98 g/mol n. HCl = 2 mol Al. Cl 3 = 1, 11 mol 2 mol Al Al. Cl 3 20, 0 g HCl 2 mol Al. Cl 3 = 0, 548 mol HCl x = 0, 183 mol 36, 5 g/mol 6 mol HCl Al. Cl 3 Öyleyse HCl sınırlayıcı bileşiktir ! 34 kütle. X mol. Al. Cl 3
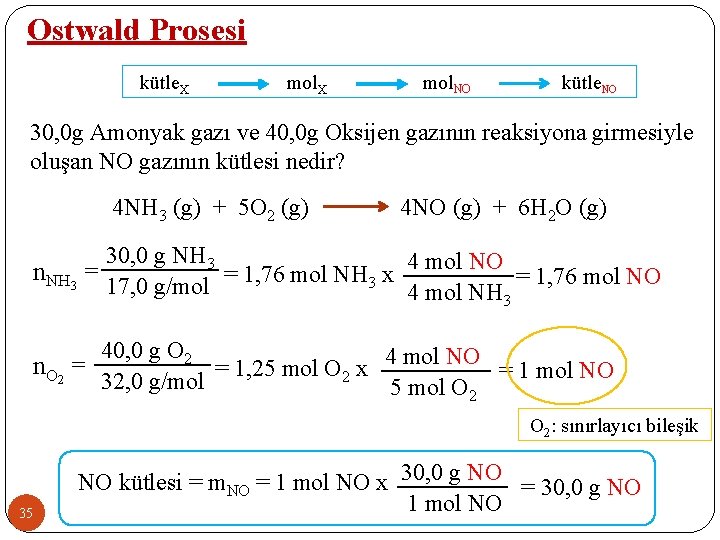
Ostwald Prosesi kütle. X mol. NO kütle. NO 30, 0 g Amonyak gazı ve 40, 0 g Oksijen gazının reaksiyona girmesiyle oluşan NO gazının kütlesi nedir? 4 NH 3 (g) + 5 O 2 (g) 4 NO (g) + 6 H 2 O (g) 30, 0 g NH 3 4 mol NO n. NH 3 = = 1, 76 mol NH 3 x = 1, 76 mol NO 17, 0 g/mol 4 mol NH 3 40, 0 g O 2 4 mol NO n. O 2 = = 1, 25 mol O 2 x = 1 mol NO 32, 0 g/mol 5 mol O 2: sınırlayıcı bileşik 35 NO kütlesi = m. NO = 1 mol NO x 30, 0 g NO = 30, 0 g NO 1 mol NO

% Verim / Sınırlayıcı Bileşen Problemi Haber Prosesi denilen bir proses kullanılarak azot ve hidrojen gazlarından amonyak elde edilir. 85, 90 g azot ile 21, 66 g Hidrojen tepkimeye girdiğinde 98, 67 g amonyak oluşuyorsa tepkimenin % verimi nedir? N 2 (g) + 3 H 2 (g) 2 NH 3 (g) Strateji: Her iki tepkenin de miktarları verildiğinden bu bir sınırlayıcı Bileşik problemidir. 36 Önce sınırlayıcı bileşik bulunduktan sonra kuramsal (teorik) verim ve daha sonra da % verim hesaplanır.

N 2 (g) + 3 H 2 (g) 1. Azot ve Hidrojenin mol miktarları: n. N 2 2 NH 3 (g) 2. Ürün mol sayısı: 85, 90 g N 2 2 mol NH 3 = = 3, 066 mol N 2 x = 6, 132 mol NH 3 28, 02 g/mol N 2 1 mol N 2: sınırlayıcı bileşik 2 mol NH 3 21, 66 g H 2 = 7, 16 mol NH 3 n. H 2 = = 10, 74 mol H 2 x 3 mol H 2 2, 016 g/mol H 2 3. Kurumsal Verim sınırlayıcı bileşik (N 2) üzerinden hesaplanır: m. NH 3 = 6, 132 mol NH 3 x 37 17, 03 g NH 3 = 104, 43 g NH 3 1 mol NH 3 Kurumsal Verim

Kurumsal Verim 104, 427 g NH 3 4. % Verim gerçek ve teorik verim kullanılarak hesaplanır: % Verim = Gerçek verim Kurumsal (Teorik) Verim x 100% Soruda: Hidrojen tepkimeye girdiğinde 98, 67 g amonyak oluşuyorsa tepkimenin % verimi nedir? Gerçek Verim 98, 67 g NH 3 % Verim = 104, 427 g NH 3 38 x 100% = 94, 49 %

Alıştırma sorusu 5: Bisfenol-A, aşağıdaki reaksiyon kullanılarak toluen (C 6 H 6 O) ve asetondan (C 3 H 6 O) sentezlenir. 2 C 6 H 6 O + C 3 H 6 O �C 15 H 16 O 2 + H 2 O Eğer 6, 6 mol tolüen, 4, 0 mol aseton ile karıştırılırsa, a) Sınırlayıcı bileşen nedir? b) Aşırı bileşen nedir? c) Kurumsal (teorik) verim gram cinsinden nedir? (Bisfenol-A için) d) Eğer gerçek verim 643, 7 g bisfenol-A ise, % verim kaçtır? e) Ne kadar miktarda aşırı bileşen reaksiyonda kullanılmamıştır? (MC 6 H 6 O = 94, 1 g/mol, MC 3 H 6 O = 58, 1 g/mol, MC 15 H 16 O 2 = 228, 3 g/mol) Cvp: a) Toluene, b) Acetone, c) 753, 4 g, d)85, 4%, e) 90. 4 g 39

Alıştırma sorusu 6: Titanyum, roketlerde, uçaklarda, jet motorlarında ve bisiklet çerçevelerinde kullanılan güçlü, hafif, korozyona dayanıklı bir metaldir. 950 o. C - 1150 o. C arasında titanyum (IV) klorürün erimiş magnezyum ile tepkimesiyle hazırlanır: Belirli bir endüstriyel işlemde, 3, 54 x 107 g Ti. Cl 4, 1, 13 x 107 g Mg ile reaksiyona sokulur. a) Ti'nin teorik verimini gram cinsinden hesaplayın. b) 7, 91 x 106 g Ti gerçekten elde edilirse, yüzde verimi hesaplayın. Cvp: a) 8, 95 x 10 6 g Ti, b) 88, 4 % 40

Çözeltide Kimyasal Tepkimeler Çözelti içinde tepkenlerin karıştırılarak atomlar, iyonlar ve moleküller arasında tepkime için gerekli yakın temas sağlanır. Çözücü: Çoğunlukla sulu çözeltiler kullanılır; (aq) ile gösterilirler. Çözeltide fazla miktarda bulunan maddeler. Çözünen: Çözücüde çözünen maddeye denir. Çözeltide az miktarda bulunan maddeler. Çözünen + 41 Çözelti = Illustration: http: //mccallscience. pbworks. com Çözücü
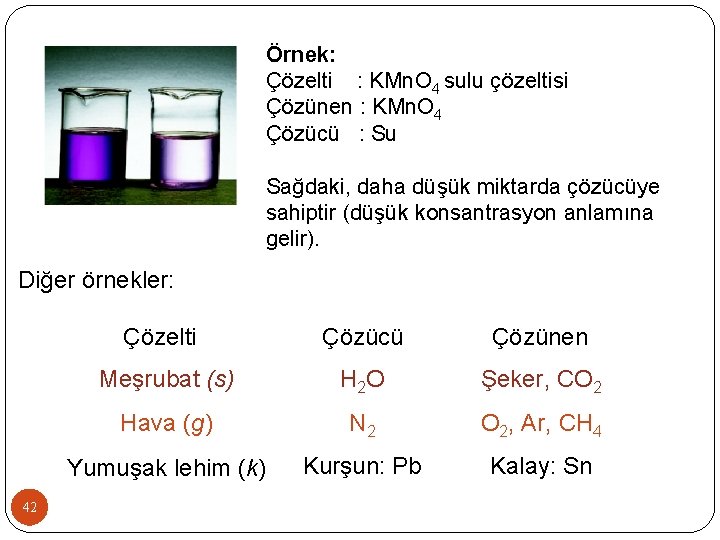
Örnek: Çözelti : KMn. O 4 sulu çözeltisi Çözünen : KMn. O 4 Çözücü : Su Sağdaki, daha düşük miktarda çözücüye sahiptir (düşük konsantrasyon anlamına gelir). Diğer örnekler: 42 Çözelti Çözücü Çözünen Meşrubat (s) H 2 O Şeker, CO 2 Hava (g) N 2 O 2, Ar, CH 4 Yumuşak lehim (k) Kurşun: Pb Kalay: Sn

Çözelti Stokiyometrisi Bir çözeltinin konsantrasyonu (derişimi), belirli bir miktarda çözücü veya çözeltide mevcut çözünen miktarıdır. - Molarite (Molar derişim): sulu çözeltiler için en yaygın kullanılan konsantrasyon birimi Molarite (M) = Çözünen maddenin mol sayısı Çözeltinin Toplam hacmi (L) n = V (L) 43

M sembolü “molar” olarak okunur. (Ör: 0, 24 M = 0, 24 molar) n M= V (L) Ör. 0, 24 M HCl : 0, 24 mol HCl 1 L suda çözülmüştür. Veya: 0, 12 mol HCl, 0, 5 L çözeltide bulunur. Ör. ; Eğer 0, 444 mol CO(NH 2)2 üre sulu çözeltinin 1000 m. L’sinde çözünmüşse, çözeltinin molarite olarak derişimi; curea = 0, 444 mol üre 1, 000 L 44 = 0, 444 M CO(NH 2)2
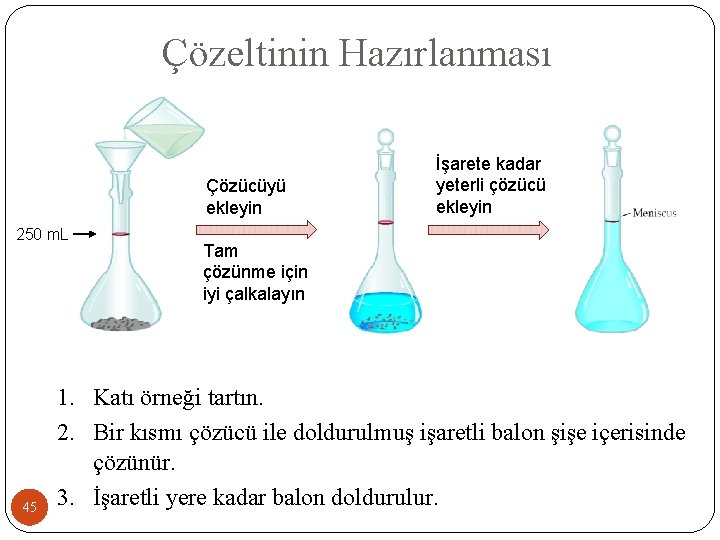
Çözeltinin Hazırlanması Çözücüyü ekleyin 250 m. L 45 İşarete kadar yeterli çözücü ekleyin Tam çözünme için iyi çalkalayın 1. Katı örneği tartın. 2. Bir kısmı çözücü ile doldurulmuş işaretli balon şişe içerisinde çözünür. 3. İşaretli yere kadar balon doldurulur.
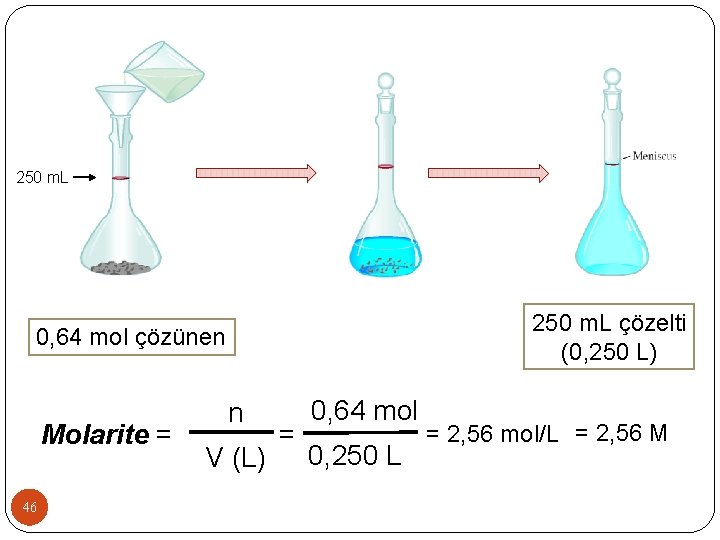
250 m. L çözelti (0, 250 L) 0, 64 mol çözünen Molarite = 46 n V (L) = 0, 64 mol 0, 250 L = 2, 56 mol/L = 2, 56 M

Örnek : Bilinen molarite deki çözeltide çözünenin kütlesinin hesaplanması. 0, 2500 L (250 m. L), 0, 250 M K 2 Cr. O 4 çözeltisi hazırlamak için kaç gram K 2 Cr. O 4 gereklidir. Plan stratejisi 1: Hacim → mol → kütle İki tane çevirme faktörüne ihtiyaç var! Denklemi yazıp hessaplayın: m. K 2 Cr. O 4 = 0, 2500 L × 0, 250 mol × 194, 02 g = 12, 1 g 1, 00 L 47 1, 00 mol

Alıştırma sorusu: 50, 0 m. L 0, 00793 M espresso kahve içindeki kafein miktarı (miligram cinsinden) nedir? (Kafein (C 8 H 10 N 4 O 2), Molar kütle: 194, 2 g/mol) İpucu: M = n / V yani n (mol) = M x V Cvp: 77 mg 48

Alıştırma sorusu: 0, 315 M Na. OH çözeltisi 6, 22 g Na. OH içerirse bu çözeltinin hacmi nedir (mililitre olarak)? Cvp: 494 m. L 49
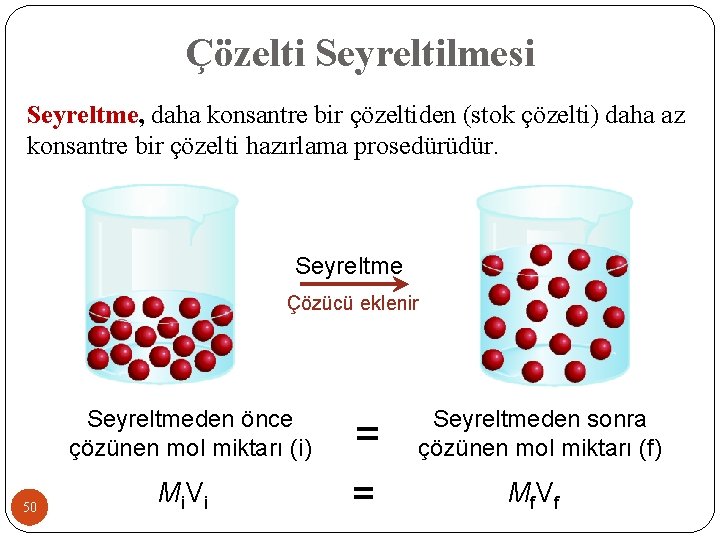
Çözelti Seyreltilmesi Seyreltme, daha konsantre bir çözeltiden (stok çözelti) daha az konsantre bir çözelti hazırlama prosedürüdür. Seyreltme Çözücü eklenir Seyreltmeden önce çözünen mol miktarı (i) 50 Mi V i = Seyreltmeden sonra çözünen mol miktarı (f) = Mf V f
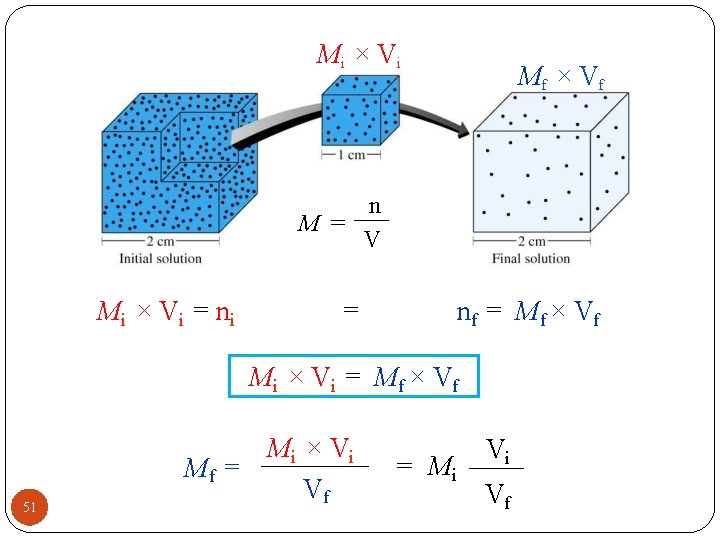
Mi × V i Mf × V f n M = V Mi × Vi = nf = Mf × Vf Mi × V i = Mf × V f Mf = 51 Mi × V i Vf = Mi Vi Vf

Örnek: Seyreltme yaparak çözelti hazırlanması 8, 61 M'lik bir H 2 SO 4 stok çözeltisi ile başlayarak 5, 00 x 102 m. L 1, 75 M H 2 SO 4 çözeltisinin nasıl hazırlanacağını açıklayın. Çözüm: Verilerimizi tablolayarak hesaplamaya hazırlanıyoruz: Formülden: 52 Mi = 8. 61 M Mf = 1. 75 M Vi = ? Vf = 5. 00 × 102 m. L Mi × V i = Mf × V f

Örnek: Analitik kimyanın bir deneyinde 0, 0100 M K 2 Cr. O 4 çözeltisi gereklidir. 0, 250 L of 0, 0100 M’lık K 2 Cr. O 4 çözeltisini hazırlamak için 0, 250 M K 2 Cr. O 4 çözeltisinden ne kadar kullanmak gerekir? Çözüm 1: Formülden Mi × V i = Mf × V f Vi = Vf Mf Mi = 0, 250 L x 0, 0100 M 0, 250 M = 0, 0100 L Çözüm 2: Hacim mol hacim 1, 000 L = 0, 0100 L 0, 0100 mol × VK 2 Cr. O 4 = 0, 2500 L × 0, 250 mol 1, 00 L 53

Alıştırma sorusu: 5, 07 M stok çözeltisi ile başlayarak 2, 00 x 102 m. L 0, 866 M KOH çözeltisini nasıl hazırlarsınız? Cevap: İstenen konsantrasyonu elde etmek için balon şişede 2, 00 x 102 m. L'lik bir son hacim verecek şekilde yeterli su ile 5, 07 M KOH çözeltisinin 34, 2 m. L'sini seyreltin. 54
- Slides: 54