Kimyasal Hesaplamalar l Kimyasal hesaplamalar Miktarl gei problemleri

Kimyasal Hesaplamalar l Kimyasal hesaplamalar; Miktarlı geçiş problemleri, l Artan madde problemleri, l Karışım problemleri, l Basit ve molekül formülü bulma problemleri, l Verim problemleri şeklinde gruplandırılabilir. l 1

Miktarlı geçiş problemleri, l Tepkime denkleminden yararlanılarak miktarı belli olan bir maddeden, tepkimede miktarı belli olmayan diğer maddelere geçiş yapılan problemlerdir. l Verilmemişse ÖNCE denklem yazılır denkleştirilir. l Denklem verilmişse önce denkliğine bakılır sonra tepkime mol sayısı, tanecik sayısı, kütle ya da hacim türünden yorumlanır. 2
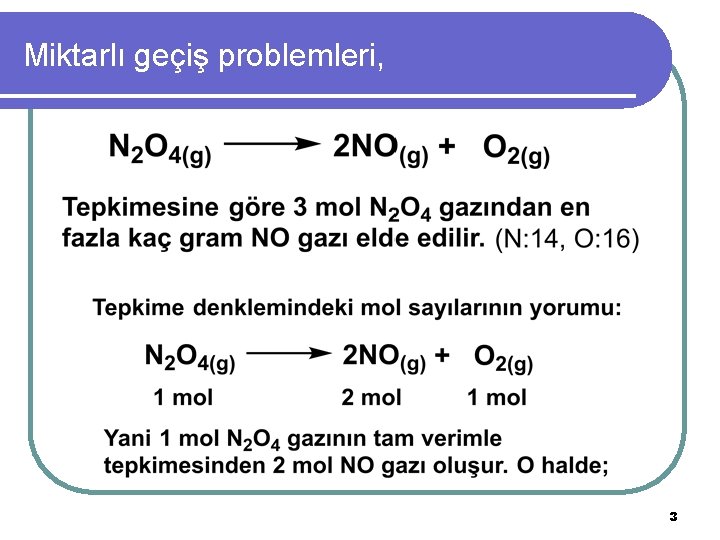
Miktarlı geçiş problemleri, 3

Miktarlı geçiş problemleri, 4

Artan madde problemleri, l Bazı tepkimelerde girenlerin miktarları rastgele alındığında, tepkimeye girenlerden biri tamamen tükenirken diğerleri tamamen tükenmez ya da bir kısmı artar. l Kimyasal tepkimelerde tamamen tükenen reaktife sınırlayıcı reaktif denir. l Sınırlayıcı reaktif oluşan ürünün miktarını belirler. 5

Artan madde problemleri, l N 2 ve O 3 gazlarının tepkimeleri sonucunda sadece N 2 O oluşmaktadır. 0, 9’ar mol alınan N 2 ve O 3 gazları tepkimeye giriyor. Buna göre; l a) Hangi madde tamamen tükenir? l b) Kaç mol N 2 O oluşur? l c) Hangi maddeden kaç mol artar? l 6

Artan madde problemleri, l Artan madde problemlerinde tepkime denklemleri, maddelerin başlangıç, değişim ve son durumdaki miktarları türünden incelenir. 7

Karışım problemleri, l l l Bu sorular iki şekildedir. İlk tipte bazı maddeler tepkime verirken diğerleri vermez. Bu tip sorularda tepkime denklemi yazılarak tepkimeye giren maddenin miktarı bulunur. İkincide karışımdaki bütün maddeler tepkimeye girer. Bu durumda denklemler her madde için ayrı yazılır. 8

Karışım problemleri, l Cu ve Al’den oluşan bir alaşımın 100 gramı yeterince HCl ile tepkimeye sokulduğunda NŞA’ da 67, 2 L H 2 gazı oluşuyor. (Al: 27, Cu: 64) l Buna göre karışımdaki Cu kütlesi kaçtır? 9
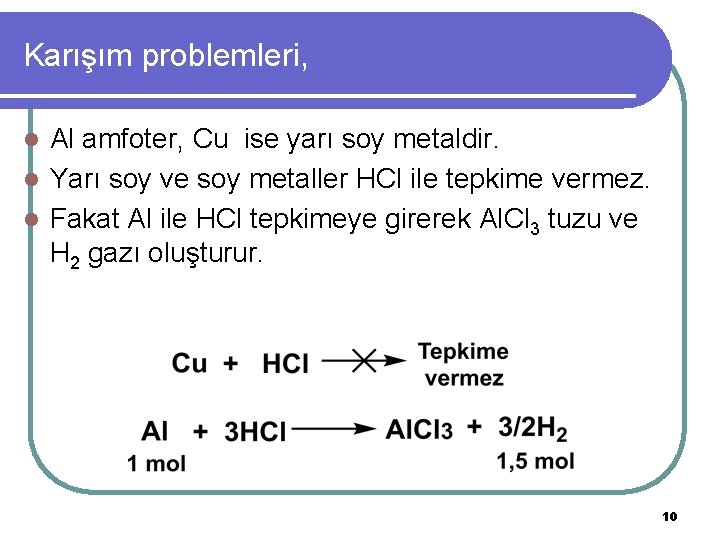
Karışım problemleri, Al amfoter, Cu ise yarı soy metaldir. l Yarı soy ve soy metaller HCl ile tepkime vermez. l Fakat Al ile HCl tepkimeye girerek Al. Cl 3 tuzu ve H 2 gazı oluşturur. l 10

Karışım problemleri, 11

Basit ve molekül formülü bulma problemleri, l Verilen bilgilerden yararlanarak bileşiğin basit ve molekül formüllerinin bulunduğu problemlerdir. l C ve H’den oluşan bir bileşikte kütlece %80 C bulunmaktadır. l Bu bileşiğin basit formülü nedir? (C: 12, H: 1) 12

Basit ve molekül formülü bulma problemleri, 13

Verim problemleri, l Bir tepkimede, tepkimeye giren maddelerden en az biri bitmişse tepkime %100 verimle gerçekleşmiştir. l Fakat bazı tepkimeler maksimum miktarda ürün oluşturamaz. l Örneğin yarısı oluşursa tepkime %50 verimle oluşmuştur. l Ya da tepkimeye girebilecek maddelerin %50’si tepkimeye girmiştir şeklinde yorumlanabilir. 14

Verim problemleri, l KCl. O 3’ün ısıtılarak parçalanmasından O 2 gazı elde edilir. 1, 6 mol KCl. O 3’ün ısıtılarak parçalanmasından 19, 2 gram O 2 elde edilmektedir. (O: 16) l Buna göre tepkime verimi % kaçtır? 15

Verim problemleri, 16

Kimyasal Hesaplamalar l Soru: CO(g) + 2 H 2(g) CH 3 OH(s) tepkime denklemine göre; 320 gram metanol (CH 3 OH) üretmek için kaç gram H 2(g) gereklidir (C: 12, H: 1, O: 16 g/mol). 17
- Slides: 17