IFI por Cndida en pacientes crticos INDICE Epidemiologia



















































































- Slides: 125

IFI por Cándida en pacientes críticos

INDICE • Epidemiologia • Distribución especies: • Candida Albicans vs no Albicans • Datos unidad • Estudio CANDIPOP • Factores de riesgo • Colonización • Diagnostico • Tratamiento

La Infección Fúngica Invasora (IFI) es un problema creciente a nivel mundial en los hospitales en general y en las Unidades de Cuidados Intensivos (UCI) en particular 1. La incidencia de IFI en pacientes críticos ha ido aumentando en las últimas décadas. En EE. UU. la Sépsis relacionada con infección fúngica creció un 207% entre 1979 y 20008 Candida es sin duda, el principal hongo causante de IFI en pacientes críticos, -tanto neutropénicos como no neutropénicos - representando más del 85% del total 1. En el estudio francés Amar. Cand 3 realizado en 101 UCI (44 médicoquirúrgicas, 28 médicas y 29 quirúrgicas), se analizó información de 271 pacientes evaluables con candidiasis invasora: el 39, 5% tenían candidemia aislada, el 28, 4% candidiasis invasora con candidemia y el 32, 1% tenían candidiasis invasora, sin candidemia documentada. La mortalidad al alta fue de 52, 0% y en la UCI de 45, 9%.

Entre un tercio y la mitad de los casos hospitalarios de candidemia, se localizan en la UCI y este porcentaje ha crecido en los últimos años. La frecuencia de candidemia en la UCI es 7 -10 veces superior a la de otros Servicios Hospitalarios, Médicos o Quirúrgicos. Estudio EPIC II llevado a cabo 1265 UCIs de 76 países: 51% pacientes tenían un proceso infeccioso. Candida 3 germen responsable (17%) tras St. Aureus (20, 5%) y Ps. Aerouginosa (19, 9%) Tasa de mortalidad cruda Pacientes neutropénicos: 40 -78% No neutropénicos: 20 -40% Candidemia se asocia a un 14, 5% de incremento de mortalidad en adultos

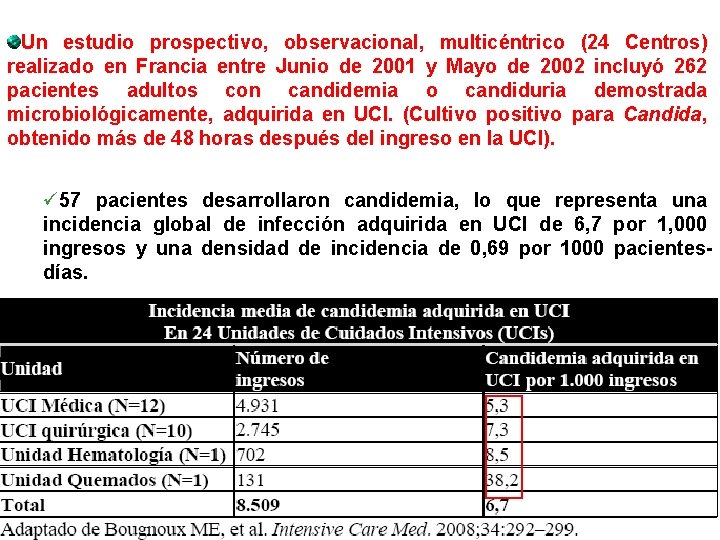
Un estudio prospectivo, observacional, multicéntrico (24 Centros) realizado en Francia entre Junio de 2001 y Mayo de 2002 incluyó 262 pacientes adultos con candidemia o candiduria demostrada microbiológicamente, adquirida en UCI. (Cultivo positivo para Candida, obtenido más de 48 horas después del ingreso en la UCI). ü 57 pacientes desarrollaron candidemia, lo que representa una incidencia global de infección adquirida en UCI de 6, 7 por 1, 000 ingresos y una densidad de incidencia de 0, 69 por 1000 pacientesdías.

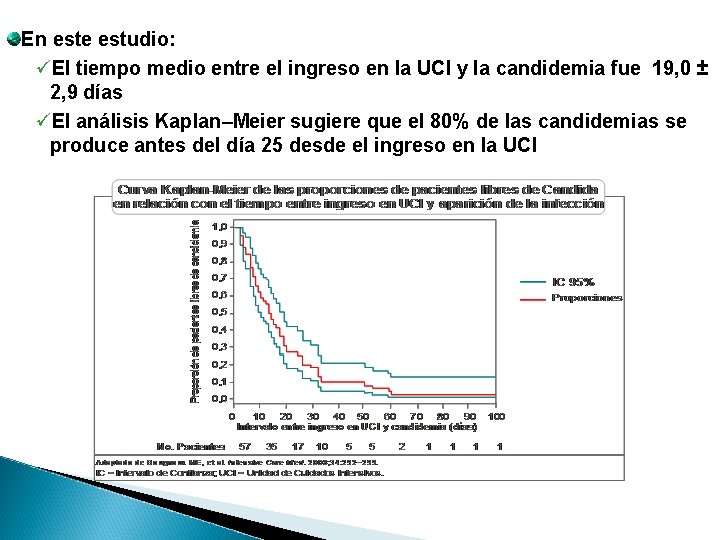
En este estudio: üEl tiempo medio entre el ingreso en la UCI y la candidemia fue 19, 0 ± 2, 9 días üEl análisis Kaplan–Meier sugiere que el 80% de las candidemias se produce antes del día 25 desde el ingreso en la UCI

Resultados del Proyecto EPCAN: Estudio prospectivo, de cohortes, observacional y multicéntrico, realizado por el Grupo de Estudio de Enfermedades Infecciosas de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias. Objetivos. Determinar. (a) la incidencia de infección y/o colonización fúngica en pacientes no neutropénicos de UCI y (b) identificar los factores epidemiológicos y clínicos que favorecen la infección por las diferentes especies de Candida. Conclusiones: üMás de la mitad de los pacientes ingresados en UCI más de 7 días presentaron colonización fúngica, aunque menos del 6% desarrollaron infección fúngica invasora. üLos factores de riesgo independientes asociados con candidiasis invasora fueron: ü sepsis ü colonización multifocal, ü cirugía ü nutrición parenteral total. üLa mortalidad entre los pacientes con infección fúngica fue significativamente superior a la de los pacientes con colonización por Candida, o los no colonizados y no infectados.

IFI por Cándida. Distribución por Especies. Cándida albicans vs. Cándida no-albicans

• 17 especies Candida • 90% casos candidiasis invasiva producidas por 5 especies: • C. Albicans • C. Glabrata • C. Tropicalis • C. Parapsilosis • C. Kruseii C. Albicans C. no Albicans C. Glabrata (alta tasa R Fluconazol) C. Tropicalis C. Parapsilosis C. Kruseii (R Fluconazol)

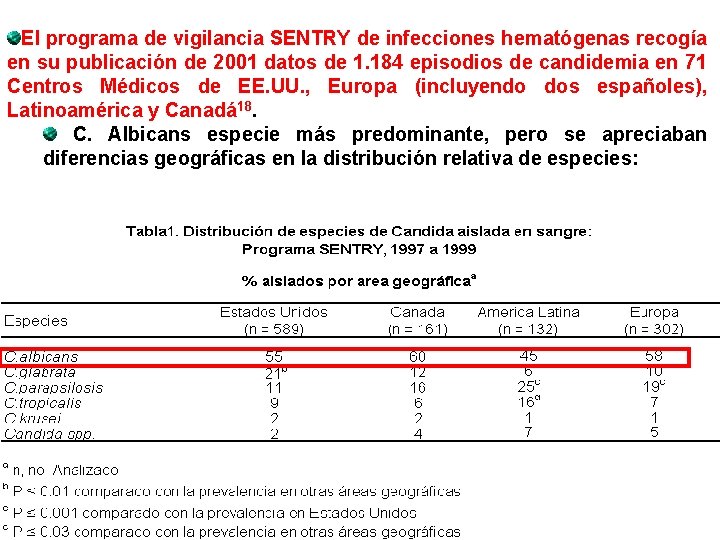
El programa de vigilancia SENTRY de infecciones hematógenas recogía en su publicación de 2001 datos de 1. 184 episodios de candidemia en 71 Centros Médicos de EE. UU. , Europa (incluyendo dos españoles), Latinoamérica y Canadá 18. C. Albicans especie más predominante, pero se apreciaban diferencias geográficas en la distribución relativa de especies:

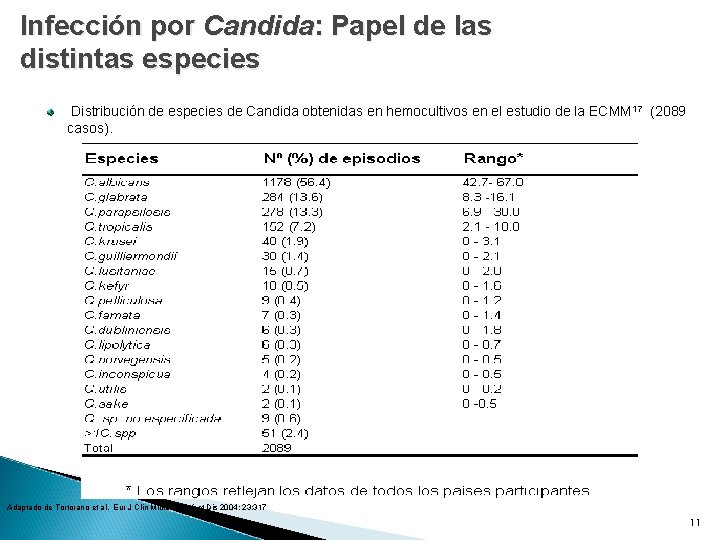
Infección por Candida: Papel de las distintas especies Distribución de especies de Candida obtenidas en hemocultivos en el estudio de la ECMM 17 (2089 casos). Adaptado de Tortorano et al. Eur J Clin Microbiol Infect Dis 2004; 23: 317 11

Con el tiempo, se vienen observando cambios paulatinos en las Especies de Candida productoras de infección; especies no-albicans (C. parapsilosis, C. glabrata, C. tropicalis y C. krusei) están adquiriendo cada vez más protagonismo, en términos relativos 3, 4, 6, 7, 11, 14, 15 sobrepasando incluso en EE. UU. en frecuencia a C. albicans, de forma muy clara en algunos estudios como el de Hajjeh 19.

El amplio empleo de fluconazol parece ser el principal factor asociado a la selección de especies intrínsecamente resistentes, o menos sensibles a fluconazol, como C. glabrata, C. krusei o C. tropicalis 7, 11, 26, 27. En el Hospital San Martino de Génova, la incidencia de infecciones causadas por la mayor parte de las especies de Candida no-albicans cambiaron durante el periodo del estudio. Estos cambios coincidieron con un incremento de cuatro veces del uso de fluconazol” 27

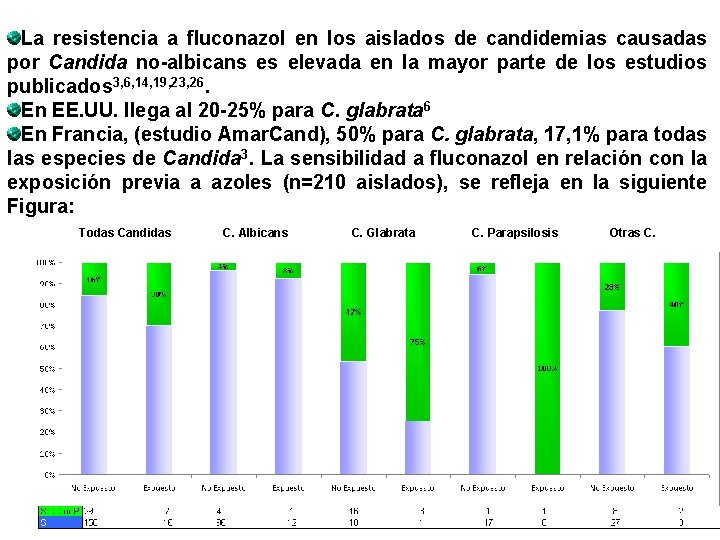
La resistencia a fluconazol en los aislados de candidemias causadas por Candida no-albicans es elevada en la mayor parte de los estudios publicados 3, 6, 14, 19, 23, 26. En EE. UU. llega al 20 -25% para C. glabrata 6 En Francia, (estudio Amar. Cand), 50% para C. glabrata, 17, 1% para todas las especies de Candida 3. La sensibilidad a fluconazol en relación con la exposición previa a azoles (n=210 aislados), se refleja en la siguiente Figura: Todas Candidas C. Albicans C. Glabrata C. Parapsilosis Otras C.

Population-Based Prospective Surveillance No C. C. on Candidemia in Spain (CANDIPOP study): Country Year isolate C. albicans Other glabrata krusei parapsilosis tropicalis s Australia 2001 -2004 1095 47. 3 15. 4 4. 3 19. 9 5. 1 5. 9 209 51. 1 21. 5 4. 7 6. 2 5. 7 10. 5 Barcelona-Bilbao-Madrid-Sevilla-Valencia (29 hospitales) 1999 -2004 Canada A prospective multicenter populationbased surveillance program on Candida BSI was implemented in 29 hospitals from 5 areas in Spain (population 7, 026, 030) from May 2010 to April 2011 Denmark 2004 -2008 1089 59. 8 20. 5 4. 1 4. 0 4. 6 7. 1 Finland 1995 -1999 479 70. 0 9. 0 8. 0 5. 0 3. 0 5. 0 Germany 2004 -2005 561 58. 4 18. 7 1. 6 9. 3 6. 3 5. 7 Iceland 1980 -1999 177 64. 4 12. 4 0. 56 9. 6 5. 6 4. 0 1994 298 53. 6 6. 5 0. 7 11. 9 10. 9 15. 9 Italy 2000 -2003 94 40. 0 12. 8 3. 2 22. 3 16. 0 5. 3 Japan 2001 -2002 535 40. 7 17. 9 2. 4 23. 0 11. 6 4. 3 Mexico 2004 -2007 398 31. 9 8 2. 7 37. 9 14. 8 4. 6 Norway 1991 -2003 1393 69. 8 13. 2 1. 6 5. 8 6. 7 3. 1 Scotland 2005 -2006 300 52. 0 22. 7 1. 0 11. 7 6. 0 8. 0 Spain 2002 -2003 345 51. 0 8. 0 4. 0 23. 0 10. 0 3. 0 Sweden 1998 -1999 191 67. 0 15. 7 1. 0 7. 3 2. 1 4. 1 USA 1998 -2000 1143 45. 0 24. 0 2. 0 13. 0 12. 0 2. 1 Israel

CANDIPOP, preliminary results • 752 cases in 729 patients with yeast BSI were detected. 14 cases had two different species of yeasts, resulting in 766 isolates • Annual incidences were: • 10. 7 h/100, 000 population (Barcelona study 2002, 4. 2/10, 000, geo differences) • 0. 78/1, 000 admissions • 1. 2/10, 000 patient-days

CANDIPOP, preliminary results • 58. 8% cases were men with median age of 63 y (range 0 -103 y), with 13. 3% less than 1 y old • Inpatients comprised 89% of the cases (39. 7% intensive care unit, 31. 8% medical wards, 24% surgical wards and 4. 3% others) • Underlying conditions were: 37. 9% malignancies, 5. 9% transplant recipients, 5. 5% neutropenic and 2. 2% HIV infection • 51. 3% patients underwent surgery 3 months prior to candidemia, and 24. 2% had received previous antifungal drugs. 76. 3% cases had central venous catheter (CVC) (56. 9% for parenteral nutrition) • Candidemia was primary in 60% cases and secondary in 40% (31. 3% catheter-related, 4. 5% urologic source, 3. 9% abdominal origin, and 0. 3% others).

CANDIPOP, preliminary results • Mortality: 37. 7% • Catheter removal in first 48 h: protective • C. krusei and signs of severity: associated to mortality

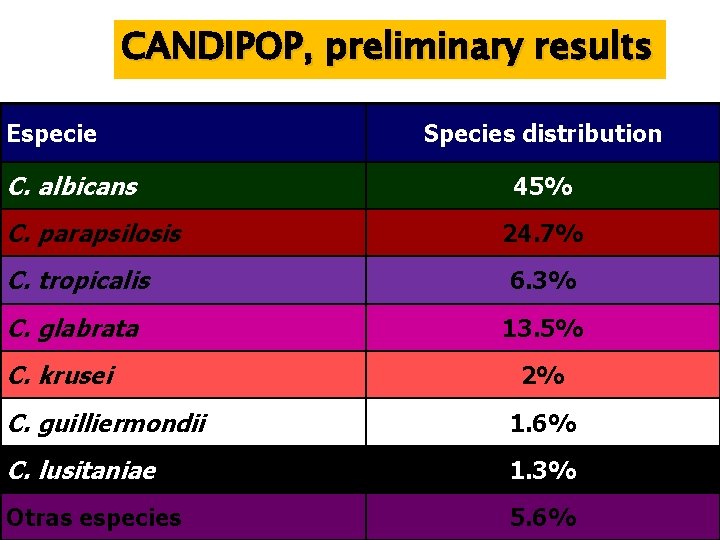
CANDIPOP, preliminary results Especie C. albicans C. parapsilosis Species distribution 45% 24. 7% C. tropicalis 6. 3% C. glabrata 13. 5% C. krusei 2% C. guilliermondii 1. 6% C. lusitaniae 1. 3% Otras especies 5. 6%

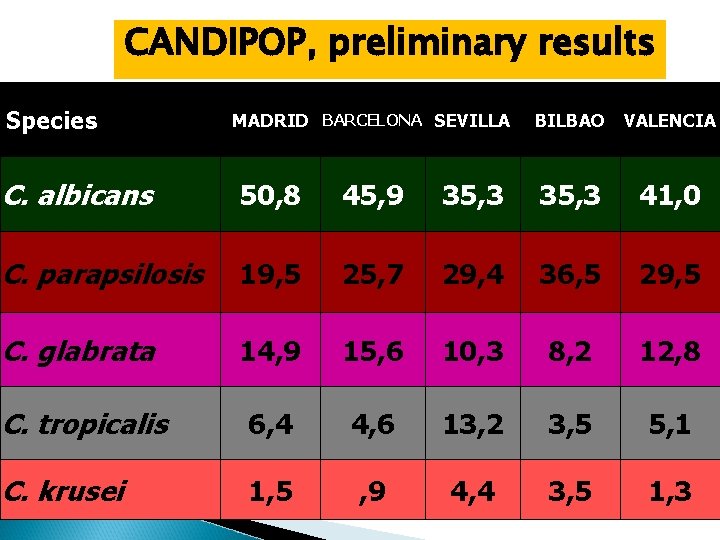
CANDIPOP, preliminary results Species MADRID BARCELONA SEVILLA BILBAO VALENCIA C. albicans 50, 8 45, 9 35, 3 41, 0 C. parapsilosis 19, 5 25, 7 29, 4 36, 5 29, 5 C. glabrata 14, 9 15, 6 10, 3 8, 2 12, 8 C. tropicalis 6, 4 4, 6 13, 2 3, 5 5, 1 C. krusei 1, 5 , 9 4, 4 3, 5 1, 3

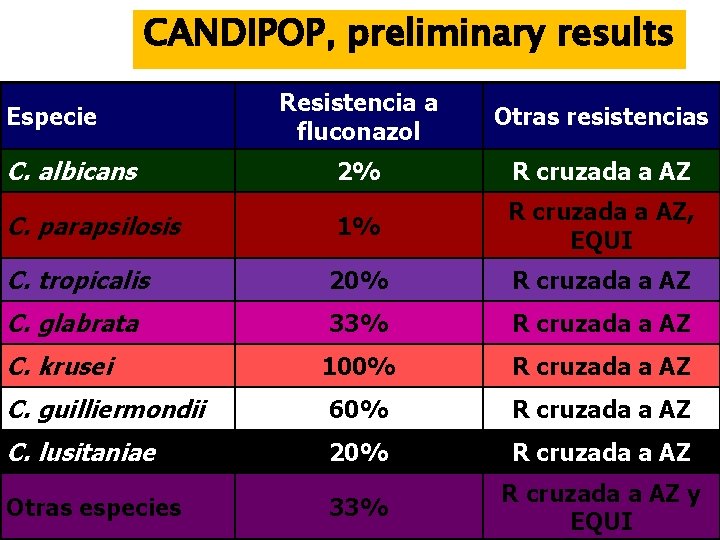
CANDIPOP, preliminary results Resistencia a fluconazol Otras resistencias C. albicans 2% R cruzada a AZ C. parapsilosis 1% R cruzada a AZ, EQUI C. tropicalis 20% R cruzada a AZ C. glabrata 33% R cruzada a AZ 100% R cruzada a AZ C. guilliermondii 60% R cruzada a AZ C. lusitaniae 20% R cruzada a AZ 33% R cruzada a AZ y EQUI Especie C. krusei Otras especies

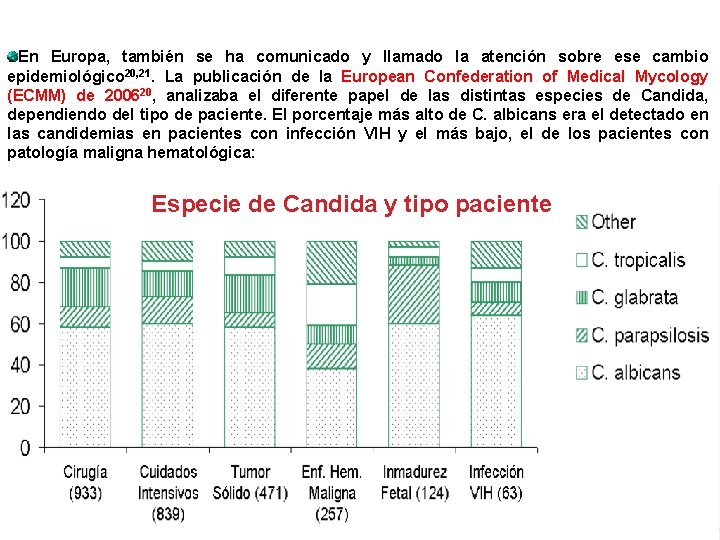
En Europa, también se ha comunicado y llamado la atención sobre ese cambio epidemiológico 20, 21. La publicación de la European Confederation of Medical Mycology (ECMM) de 200620, analizaba el diferente papel de las distintas especies de Candida, dependiendo del tipo de paciente. El porcentaje más alto de C. albicans era el detectado en las candidemias en pacientes con infección VIH y el más bajo, el de los pacientes con patología maligna hematológica: Especie de Candida y tipo paciente

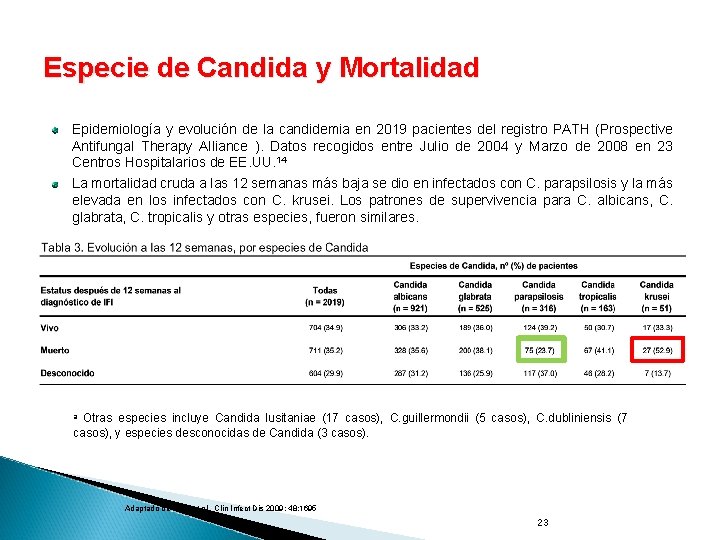
Especie de Candida y Mortalidad Epidemiología y evolución de la candidemia en 2019 pacientes del registro PATH (Prospective Antifungal Therapy Alliance ). Datos recogidos entre Julio de 2004 y Marzo de 2008 en 23 Centros Hospitalarios de EE. UU. 14 La mortalidad cruda a las 12 semanas más baja se dio en infectados con C. parapsilosis y la más elevada en los infectados con C. krusei. Los patrones de supervivencia para C. albicans, C. glabrata, C. tropicalis y otras especies, fueron similares. Otras especies incluye Candida lusitaniae (17 casos), C. guillermondii (5 casos), C. dubliniensis (7 casos), y especies desconocidas de Candida (3 casos). a Adaptado de Horn et al. Clin Infect Dis 2009; 48: 1695 23

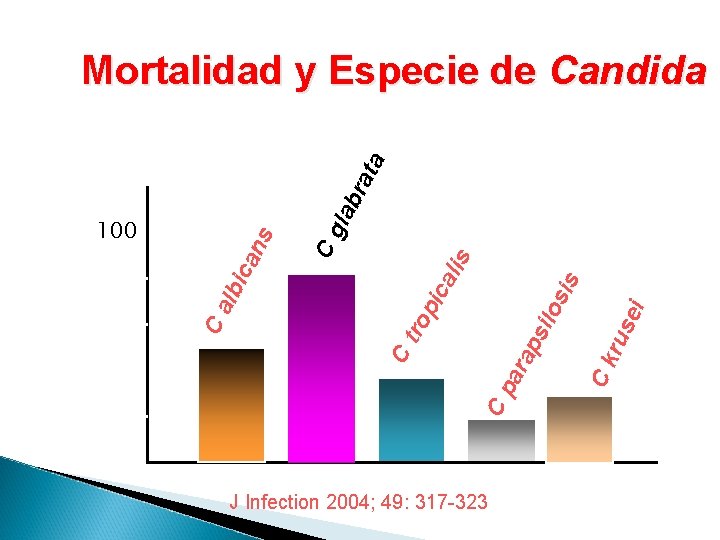
20 J Infection 2004; 49: 317 -323 ei rus ara 0 Ck ps tro ilo s pic is ali s Cg ca ns Cp 40 C 60 lbi 80 Ca 100 lab rat a Mortalidad y Especie de Candida

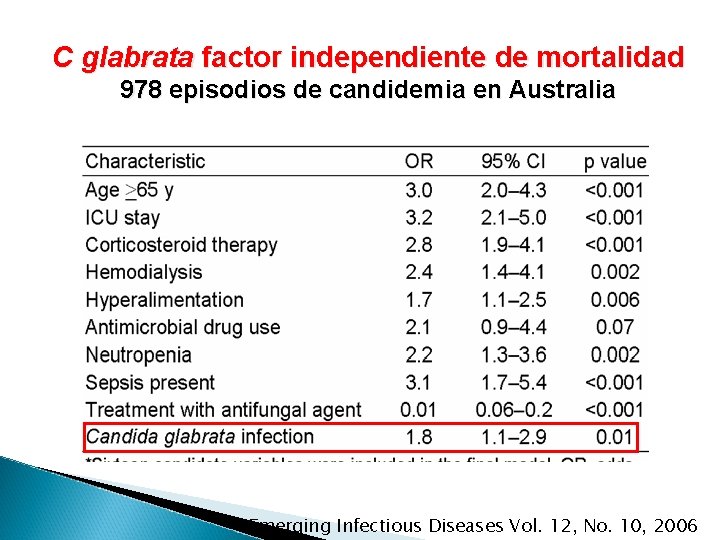
C glabrata factor independiente de mortalidad 978 episodios de candidemia en Australia Emerging Infectious Diseases Vol. 12, No. 10, 2006

ESPECIE CANDIDA Y MORTALIDAD Alta Mortalidad C. Glabrata C. Krusei C. Tropicalis Baja Mortalidad C. Parapsilopsis

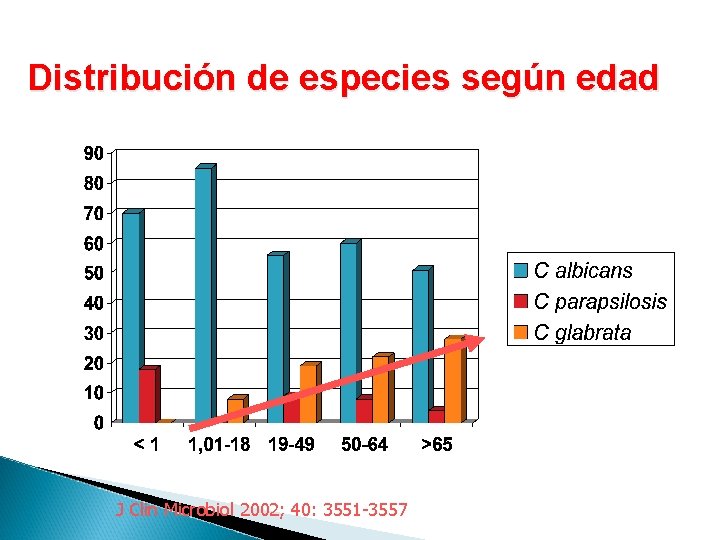
Distribución de especies según edad J Clin Microbiol 2002; 40: 3551 -3557

INFECCION NOSOCOMIAL POR CANDIDAD UCI POLIVALENTE CHUA REVISION 2005 -2012

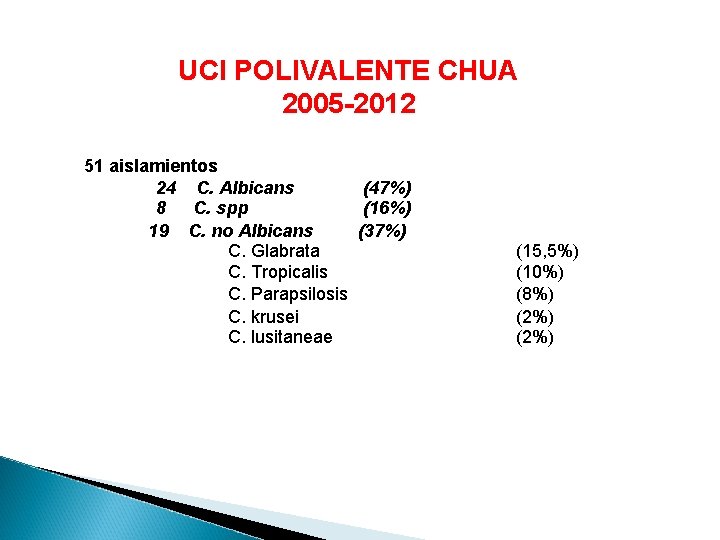
UCI POLIVALENTE CHUA 2005 -2012 51 aislamientos 24 C. Albicans (47%) 8 C. spp (16%) 19 C. no Albicans (37%) C. Glabrata C. Tropicalis C. Parapsilosis C. krusei C. lusitaneae (15, 5%) (10%) (8%) (2%)

INFECCION CANDIDA ASOCIADA USO DISPOSITIVO 46 Infección Urinaria Asociada a Sondaje Vesical (90%) C. Albicans (50%) 4 Candidemia por CVC (8%) C. Parapsilosis (50%) 1 Neumonía Asociada a Ventilación Mecánica (2%) C. spp (2%)

IFI por Candida. Factores de Riesgo 31

Factores de riesgo de IFI por Candida en UCI-Reanimación El conocimiento de los factores y variables que aumentan el riesgo de candidemia es clave para orientar el diagnóstico precoz y el tratamiento adecuado. Los factores de riesgo de IFI en pacientes críticos pueden ser tanto del huésped (paciente), como de las intervenciones médicas a que es sometido. En los últimos años, estos factores de riesgo se han estudiado en multitud de análisis tanto prospectivos como retrospectivos, en todo el mundo. 32

Factores de riesgo de IFI por Candida en UCI-Reanimación Factores de riesgo de candidiasis invasora, según Smith JA y Kauffman CA Factores del huésped ü ü ü Extremos de edad Neutropenia Fallo renal Puntuación más elevada en el score APACHE II Trauma/quemaduras Perforación intestinal Intervenciones médicas ü ü ü ü ü Quimioterapia Diálisis Catéteres venosos centrales Uso de antibiótico. (El riesgo aumenta con cada antibiótico adicional) Nutrición parenteral Cirugía previa. (Especialmente, abdominal) Estancia en UCI > 7 días Sondas nasogástricas Supresión ácida gástrica Colonización por Candida 33 1:

Factores de riesgo de IFI por Candida en UCI-Reanimación Factores de riesgo que predisponen a los pacientes de UCI a infección invasora por Candida, según Glöckner y Karthaus 25. Tabla 1. Factores de riesgo descritos que predisponen a los pacientes de UCI a las infecciones invasivas por Candida Factores del huésped Factores Yatrógenos Neutropenia (especialmente >10 días) Tratamiento inmunosupresor (corticoides) Colonización por Candida (ej. Índice de colonización >0. 5) Terapia con antibióticos de amplio espectro, Nutrición parenteral total Pancreatitis necrosante Perforación gastrointestinal Catéter venoso central Insuficiencia renal aguda Ventilación mecánica Sepsis bacteriana Cirugía Mayor (ej : resección tumor abdominal) Enfermedad hematológica maligna Dehiscencia de anastomosis gastrointestinal Índice APACHE II alto Quimioterapia antineoplásica Diabetes mellitus Hemodiálisis Mayor edad Adaptado de Glöckner et al. Mycoses 2011; 54: 420 -433. . 34

Factores de riesgo de IFI por Candida en UCI-Reanimación Resultados del Proyecto EPCAN 9: Estudio prospectivo, de cohortes, observacional y multicéntrico, realizado por el Grupo de Estudio de Enfermedades Infecciosas de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias. olonización en fúngica infección y/o incidencia de Objetivos: Determinar la (a) pacientes no neutropénicos de UCI (b) identificar los factores epidemiológicos y clínicos que favorecen la infección por las diferentes especies de Candida. Adaptado de León et al. Eur J Clin Microbiol Infect Dis 2009; 28: 233 35

Colonización: presencia de una o mas cepas de Candida spp. en una o mas muestras no estériles: Exudados heridas o mucosas, orina, heces, aspirado traqueal o drenajes abdominales • Colonización multifocal: aislamiento de levaduras en mas de una muestra no estéril • Colonización persistente: identificación de la misma especie de Candida spp. en el mismo foco en dos o mas aislamientos consecutivos. Conlleva mayor riesgo infección fúngica. Muestras significativas: son aquellas muestras en que la identificación del hongo permite asegurar el diagnostico de infección: • Sangre • Líquidos estériles: LCR, pleural, peritoneal, pericardico, artucular • Endoftalmitis: diagnostico endoftalmitis realizado por especialista en un paciente con factores de riesgo y clínica es diagnostico de candidiasis invasiva Las muestras significativas se deben de obtener por un procedimiento estéril o intervención quirúrgica y además existir la sospecha clínica o radiológica de infección

Colonización La colonización multifocal por Candida spp es un factor de riesgo independiente de candidiasis invasiva El 50 -70% de los pacientes críticos se colonizan por Candida spp No obstante, sólo el 5 -20% de ellos desarrollan candidiasis invasiva La mayoría de pacientes tienen aislamientos multifocales que preceden a la infección invasiva Se ha demostrado que la colonización por Candida spp genotípicamente idéntica precede a la candidiasis invasiva

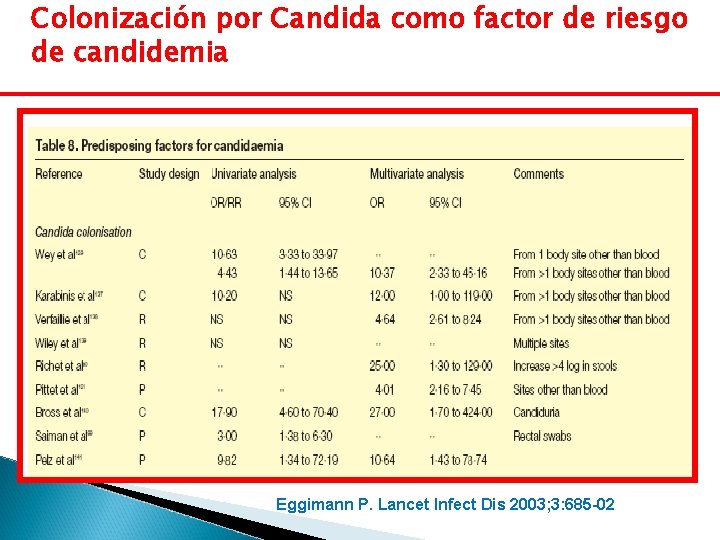
Colonización por Candida como factor de riesgo de candidemia Eggimann P. Lancet Infect Dis 2003; 3: 685 -02

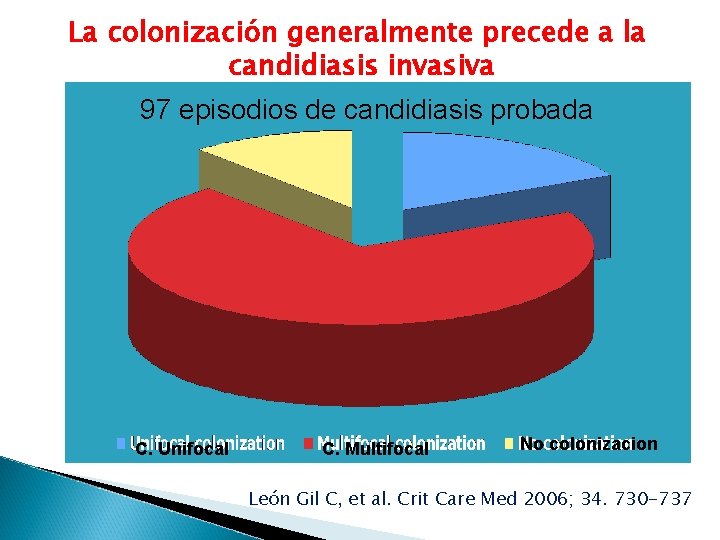
La colonización generalmente precede a la candidiasis invasiva 97 episodios de candidiasis probada C. Unifocal C. Multifocal No colonizacion León Gil C, et al. Crit Care Med 2006; 34. 730 -737

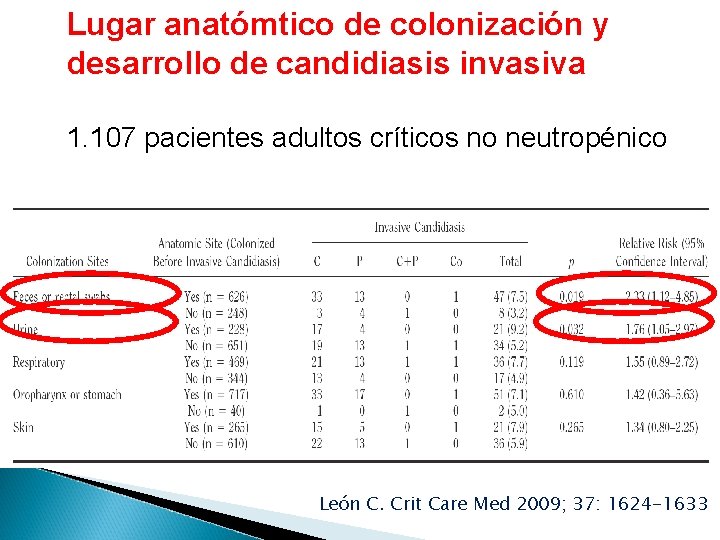
Lugar anatómtico de colonización y desarrollo de candidiasis invasiva 1. 107 pacientes adultos críticos no neutropénico León C. Crit Care Med 2009; 37: 1624 -1633

Lugar anatómico de colonización por Candida spp y riesgo de candidiasis invasiva 182 pacientes críticos quirúrgicos 2851 cultivos de vigilancia tomados de 5 diferentes lugares anatómicos (orina, orofarínge, aspirado traqueal y gástrico y recto u ostomía) Diferencias estadísticamete significativas en: No desarrolló candidiasis invasiva ningún paciente con cultivo negativo en recto/ostomia o los pacientes con cultivos negativos de muestra respiratoria y orina. ◦ Orina: (13. 2% vs 2. 8%, p = 0. 02), ◦ Muestra respiratoria (8. 0% vs 1. 2%, p = 0. 04) ◦ Ostomía/ recto (8. 4% vs 0%, p = 0. 01) Magill S. Diagn Microbiol Infect Dis. 2006; 55: 293 -301.

Factores de Riesgo para especie de Candida potencialmente R a azoles Diseño de casos y controles ◦ 60 episodios de candidemia por C glabrata (56) y C krusei (4). ◦ 68 episodios de candidemia por C albicans. ◦ 128 pacientes sin candidemia (grupo control) El tratamiento previo vancomicina o piperacilina-tazobactam se mostró como un factor de riesgo independiente para aislamiento de Candida potencialmente R a fluconazol. Antimicron Agent Chemother 2005; 49: 4455 -4560

Utilidad cultivos de vigilancia Determinan colonización del paciente Alta valor predictivo negativo de candidiasis invasiva Ayudan a tomar decisiones: ◦ Paciente con colonización múltiple + signos de infección + factores de riesgo ◦ Especie de Cándida implicada en CI

Colonización Cándida • Paciente ingresados UCI mas de 5 -7 días es fundamental conocer el grado de colonización por Cándida. • Focos a vigilar • Respiratorio • Urinario • Recto/Ostomia • Drenajes abdominales • Estomago • Piel • Orofaringe • Tomar muestras la primera semana de ingreso y luego semanalmente

“Foro de debate en Enfermedad Fúngica Invasiva (EFI): Focus en pacientes críticos y postquirúrgicos 2011” Aislamiento de Candida spp. en una muestra de drenaje abdominal. ¿Qué hacer?

COLONIZACION NO TRATAMIENTO INFECCION TRATAMIENTO • Aislamiento de cándida en liquido peritoneal se asocia a un peor pronostico • Peritonitis nosocomiales enfermos críticos

Peritonitis por Candida spp Aislamiento de Candida spp. en una muestra peritoneal obtenida, por medio de laparotomía o punción percutánea en pacientes con clínica asociada y factores de riesgo como perforación de víscera abdominal, dehiscencia de una sutura intestinal con peritonitis, pancreatitis aguda grave o existencia de un catéter para diálisis peritoneal El aislamiento de Candida spp en drenajes abdominales no es equivalente a la peritonitis por Candida spp

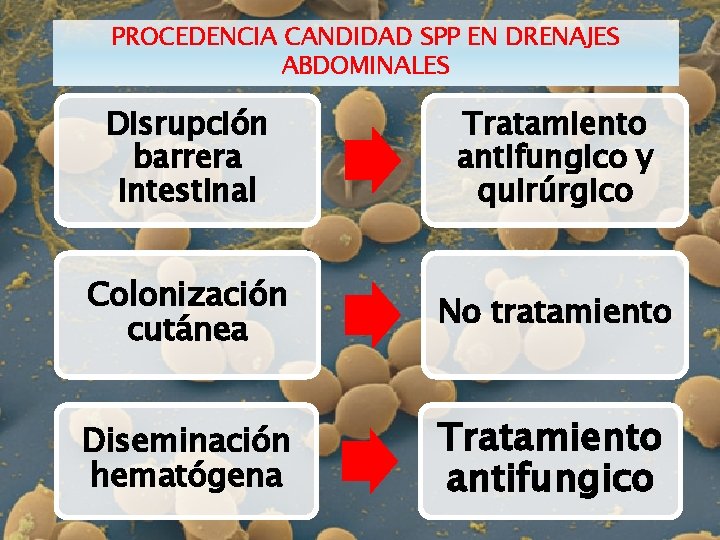
PROCEDENCIA CANDIDAD SPP EN DRENAJES ABDOMINALES Disrupción barrera intestinal Tratamiento antifungico y quirúrgico Colonización cutánea No tratamiento Diseminación hematógena Tratamiento antifungico

PACIENTES RIESGO PERITONITIS CANDIDIASICA • Características clínicas pacientes: Shock cirugía Perforación TGI superior ATB 48 horas previas Sexo femenino APACHE II>17 Fracaso respiratorio Perforación TGI superior Peritonitis nosocomiales • Realizar exploraciones radiológicas y/o quirúrgicas necesarias para buscar dehiscencia de sutura, necrosis intestinal, necrosis pancreática infectada etc. • Valorar respuesta inflamatoria del paciente. • Valorar los factores de riesgo del paciente de desarrollar infección candidiásica. • Valorar si hay colonización candidiásica multifocal. El aislamiento del drenaje se contabilizara como un foco mas. • Valoración Cándida Score. • Microbiología: cultivo y métodos no basados en cultivos.

Revision of guidelines for the treatment of fungal infections in critically ill patients

Pre-emptive Therapy: Candida sp. isolated from respiratory secretions 20% población se aísla Cándida spp en secreciones bronquiales 50% si están en tratamiento antibiótico Popula- Intention Intervention So R Any antifungal D Cure Qo. E Reference IIu Meersseman Int Care Med 2009 Comment • No data from ICU populations • Case series with haematological malignancy Aislamiento Candida spp en secreciones respiratorias debe considerarse una colonización. Aun así es un marcador de gravedad que se asocia a un aumento de la estancia hospitalaria y aumento de mortalidad

Crit Care Med 2006; 34: 857 -863



Seta caña tropicalis

DIAGNOSTICO

IFI por Cándida: Diagnóstico El diagnóstico de la infección por Cándida es complicado por diversas razones como: Variabilidad e inespecificidad de manifestaciones clínicas: ü Uno de cada cinco pacientes puede no tener fiebre. ü En algunas series, sólo la mitad de los pacientes presentan leucocitosis. ü La candidemia puede presentarse como una sepsis fulminante, indistinguible de una bacteriemia. ü Candidemia no neutropenicos menor elevación PCT que en caso bacteriemia ü La candidiasis invasora puede causar abscesos en muchos órganos, sin hemocultivos positivos. ü Cuando aparecen lesiones cutáneas, lo hacen repentinamente y bajo diversas formas. ü Puede presentarse endoftalmitis en forma de corio-retinitis, con o sin extensión al vítreo. (La afectación del vítreo es menos frecuente en la actualidad que hace algunas décadas). Dificultad de diferenciación entre infección y colonización.

Candidiasis Invasiva: Diagnóstico ü ¿Existe alguna estrategia o herramienta diagnóstica simple y sensible? NO ü¿Cuál es la prueba más convincente? Cultivo de Sangre o sitios estériles POSITIVO üDiagnostico certeza candidiasis invasiva no candidémica casi imposible ü¿ Cuál es el hallazgo más común? Paciente con Factores de Riesgo y Cultivos + en sitios NO estériles

DIAGNOSTICO 1. 2. 3. 4. 5. Identificar pacientes con factores de riesgo Uso de Scores Valorar respuesta inflamatoria sistémica Biomarcadores: Procalcitonina Cultivos de muestras clínicas 6. 7. Hemocultivos Cultivos muestras clínicas Cultivos muestras vigilancia epidemiológica colonización Determinaciones serológicas Fondo Ojo: endoftalmitis diagnosticada especialista en paciente con FR y clínica sugestivas Candidiasis invasiva

TESTS DIAGNÓSTICOS ia c en cu Histología fre Especificidad de pr Hemocultivos + ón Proteína C reactiva (CRP), procalcitonina (PCT), ci ta en es Candida en lugares no estériles 1 -3 -ß-D-glucano

DIAGNOSTICO CONVENCIONAL El diagnostico microbiológico convencional IFI se basa en el aislamiento e identificación de los hongos responsables. • Recogida y transporte de muestras • Examen microscópico • Hemocultivos • Cultivos • Identificación hongos

RECOGIDA Y TRANSPORTE MUESTRAS üTomadas en condiciones asepsia antes inicio tratamiento antifúngico üMuestras zonas activas de infección üVolumen suficiente. Mayor cantidad posible üEvitar empleo isópos. Preferible aspiración con jeringa o toma biopsias ü Transporte laboratorio rápido < 2 horas. Si no posible conservar 4ºC üBiopsias: evitar desecación añadiendo pequeña cantidad solución salina estéril. üEvitar transporte condiciones de anaerobiosis üIndicar laboratorio necesidad de buscar crecimiento levaduras

EXAMEN MICROSCOPICO üRealizar siempre un examen microbiológico y microscópico üExamen microscópico: baja sensibilidad. Negativo no excluye infección üEspecialmente indicado pacientes tratamiento antifúngico: puede haber microorganismos no viables üBasado empleo de colorantes que se unen pared fúngica üTinción Gram üTinción blanco de calcofluor üTinción tinta china üLevaduras fácilmente observables. Hongos filamentosos se tiñen con mas dificultad

HEMOCULTIVOS üMejor técnica diagnostico fungemías. Técnica referencia üEscasa sensibilidad global: 50% üVolumen de sangre no inferior 10 ml ni superior 30 ml (20 ml). Tres extracciones por episodios séptico (3 aerobios-3 anaerobios) üSembrar 20 ml sangre: incrementos índice de recuperación de levaduras del 30% de utilizar 20 ml a utilizar 10 ml üIncubar al menos durante 7 días üNo detecta precozmente infección: infección avanzada + periodo incubación

CULTIVO üHongos no son exigentes üPosibilidad crecimiento muchos medios de cultivo üPractica diaria: medios de cultivos selectivos derivados del agar glucosado de Sabouraud suplementados con antibióticos üCrecimiento lento: deben incubarse mínimo de 4 -6 semanas. Si sospecha histoplasmosis incubación 12 semanas. üNo desechar ningún cultivo sin completar periodo de incubación üSi sospecha micosis sistémica con evidencia invasión órganos profundos, realizar biopsia tejido afecto. Estudio microbiológico e histológico

IDENTIFICACION üDeben de identificarse la especie de todas las cepas clínicas causantes de infección. No informe Cándida spp. üIdentificación criterios morfológicos y bioquímicos üSolicitar antifungiograma üSegún importancia muestras: sangre, LCR üSi fracaso terapéutico üTratamiento o profilaxis previa con azoles üCándida no álbicans

TECNICAS ALTERNATIVAS CULTIVO üIncidencia aumento üAlta morbimortalidad üDiagnostico clínico difícil üHemocultivos: baja sensibilidad. No detección precoz üBasadas en la detección de Ag o Ac o componentes fúngicos estructurales. 1. Manano-anti-manano 2. 1 -3 –B-D-glucano 3. Ac antimicelio 4. PCR tiempo real

MANANO-ANTIMANANO üAg pared hongo-Ac frente a este antígeno üRealización conjunta. Escaso rendimiento por separado üAc: Alta prevalencia pacientes colonizados. Respuesta reducida inmunodeprimídos. üAg: rápida eliminación de la circulación determinaciones seriadas (2 a la semana) üSe adelanta aparición manifestaciones clínicas (6 días) üÚtiles pacientes neutropénicos üExcluir CI por alto valor predictivo negativo (95%) üAlta especificidad baja sensibilidad No útil PCNN üSEIMC: B-II

1 -3 -B-D-Glucano üBG componente abundante plantas y pared celular hongos: cándida y aspergillus üNo se encuentra en mamíferos, mayoría de bacterias o virus üEs un marcador panfúngico: completarse identificando el hongo causante üSe libera durante la infección üInterpretación resultados personal con experiencia. Laboratorios de referencia üCriterio microbiológico de infección probable üSe positiviza 10 días antes manifestaciones clínicas

1 -3 -B-D-Glucano üSuele detectarse antes cultivos o radiología üDos determinaciones semanales durante periodo mayor riesgo IFI üFalsos positivos: üHemodiálisis membrana celulosa üAlbumina üContacto con gasas üTto con Igs üATB: Augmentine, Piper/tazo üFalsos negativos. üSueros hiperpigmentados: bilirrubina, TG üTto empírico o profilaxis antifúngica üPacientes neutropénicos üSEIMC: A-I

1 -3 -B-D-Glucano üPuntos de corte diferentes 4 laboratorios comercializan üCut-off 60 pg/ml S: 70% E: 87% VPP: 84% VPN: 75% üCut-off 80 pg/ml S: 65% E: 92% VPP: 89% VPN: 73% üEstudio 57 pacientes críticos quirúrgicos üCut-off 80 pg/ml ü 25% falsos positivos üS: 87% E: 73% üPositivización 4 -8 días antes hemocultivos üSEIMC: A-I

AC anti-micelio üDetecta Ac contra Ag expresados en la fase micelar üSensibilidad: 85% Especificidad: 95% con títulos Ac > 1: 160. VPP: 96% üAdemás diagnostico, permite seguimiento evolutivo üLos pacientes que responden presenta títulos decrecientes que llegan a desaparecer üEstudio multicéntrico, prospectivo críticos: tasa positividad mayor de la esperada. Descenso significativo de la mortalidad en pacientes con títulos crecientes tratados con antifúngicos SEIMC: B-II

PCR tiempo real üDetección ADN Cándida en sangre üNo estandarizado fracción de sangre (sangre completa, suero o plasma) mas adecuada üAlto coste y escasa experiencia üComplementaria cultivo de sangre. üÚtil casos hemocultivos escasa rentabilidad: pacientes en tratamiento antifungico o candidiasis hepatoesplenica üPermite llegar diagnostico CI en unas 6 horas üS: 91% E: 100% üEnfermos críticos sospecha CI la sensibilidad superó 70%. Solo 37% hemocultivos positivos SEIMC: B-II

What are the best tests for diagnosing candidaemia? Specimen Test Serum Considerations Mannan and Anti- • Combined detection Mannan Other antibodies (such as Serion ELISA classic) • Limited data for candidemia Remarks/Recommendations RECOMMENDED Serial determinations may be necessary. High NPV No recommendation • Not specific for Candida ß-D-Glucan Septifast In house PCR RECOMMENDED (for Fungitell) No recommendation for other tests. Serial determinations are recommended (twice a week). High NPV. Not validated in children • Limited data for candidemia • No third party validation data available No recommendation

DIAGNOSTICO 1. 2. 3. 4. 5. Valorar respuesta inflamatoria sistémica Biomarcadores: Procalcitonina Identificar pacientes con factores de riesgo Uso de Scores Cultivos de muestras clínicas 6. 7. Hemocultivos Cultivos muestras clínicas Cultivos muestras vigilancia epidemiológica colonización Determinaciones serológicas Fondo Ojo: endoftalmitis diagnosticada especialista en paciente con FR y clínica sugestivas Candidiasis invasiva

Sepsis grave o Shock séptico Paciente Factores de Riesgo Tratamiento ATB amplio espectro Colonizado Hemocultivos negativos

SCORES


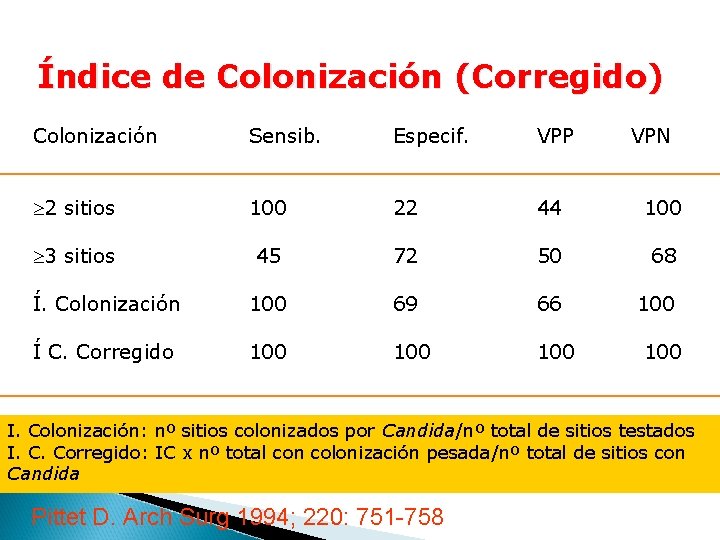
Índice de Colonización (Corregido) Colonización Sensib. Especif. VPP VPN ³ 2 sitios 100 22 44 100 ³ 3 sitios 45 72 50 68 Í. Colonización 100 69 66 100 Í C. Corregido 100 100 I. Colonización: nº sitios colonizados por Candida/nº total de sitios testados I. C. Corregido: IC x nº total con colonización pesada/nº total de sitios con Candida Pittet D. Arch Surg 1994; 220: 751 -758

Factores de riesgo de IFI por Candida en UCI-Reanimación. Candida score 31 Objetivo del estudio: obtener una puntuación (score) para decidir el tratamiento antifúngico temprano cuando se sospecha infección por Candida en pacientes críticos, no neutropénicos. Diseño: análisis de los datos recogidos en la base de datos del proyecto EPCAN: estudio prospectivo, de cohortes, observacional, multicéntrico, de vigilancia de infección y colonización fúngica en pacientes de Unidades de Cuidados Intensivos (UCI). Centros y pacientes: setenta y tres UCIs médico-qirúrgicas de setenta hospitales docentes españoles. En total, 1699 pacientes de > 18 años ingresados al menos 7 días, entre mayo de 1998 y enero de 1999. Intervenciones: cultivos semanales de vigilancia de muestras urinarias, traqueales y gástricas. Los pacientes se clasificaron como no colonizadosno infectados (n = 719); colonización uni/multifocal por Candida (n = 833); infección por Candida demostrada (n = 97). 80

Factores de riesgo de IFI por Candida en UCI-Reanimación. Candida score 31 Al comparar los pacientes infectados con los colonizados por Candida, se encontraron diferencias estadísticamente significativas sólo para algunas variables, con las que se elabora el Candida score: Los pacientes con un Candida score >2, 5 tienen una probabilidad de tener una infección demostrada 7, 75 veces superior a la de los pacientes con Candida score < 2, 5 Adaptado de León et al. Crit Care Med 2006; 34: 730 81

Validación de Candida Score 1107 pacientes incluidos 215 no colonizados/infectados 831 colonizados 58 con infección por Candida spp

Factores de riesgo de IFI por Candida en UCI-Reanimación. Candida score Objetivo del estudio: evaluar la utilidad del “Candida score” (CS) para discriminar entre colonización por especies de Candida y candidiasis invasora, en pacientes críticos no neutropénicos. Diseño: estudio prospectivo, de cohorte, observacional. Centros y pacientes: treinta y seis unidades de cuidados intensivos médico-quirúrgicas de España, Argentina y Francia. Total de 1107 pacientes adultos, ingresados al menos una semana, entre abril de 2006 y junio de 2007. Adaptado de León et al. Crit Care Med 2009; 37: 1624 83

Factores de riesgo de IFI por Candida en UCI-Reanimación. Candida score Tasas de candidiasis invasora en relación con Candida score: En esta cohorte de pacientes no neutropénicos, colonizados por especies de Candida y con estancia mínima de 7 días en UCI … se evidencia la relevancia clínica de CS<3 vs. >3, para discriminar entre colonización e infección. Los hallazgos apoyan el interés de probar la utilización del CS para guiar el eventual comienzo de tratamiento empírico con antifúngicos. Adaptado de León et al. Crit Care Med 2009; 37: 1624 84

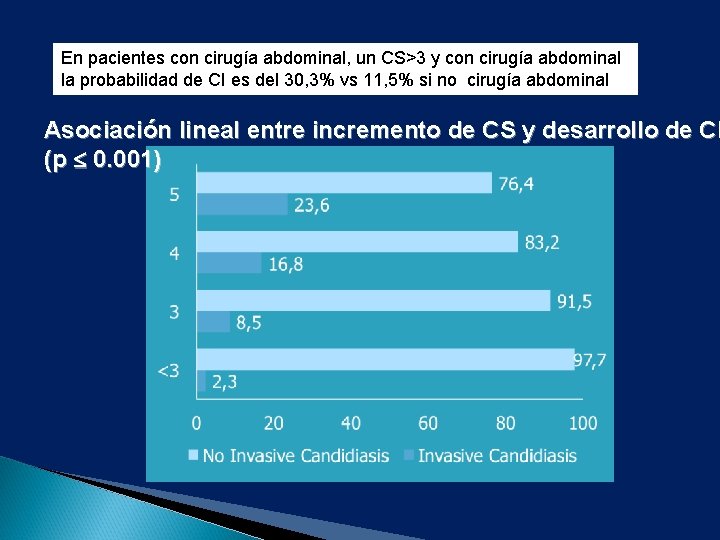
En pacientes con cirugía abdominal, un CS>3 y con cirugía abdominal la probabilidad de CI es del 30, 3% vs 11, 5% si no cirugía abdominal Asociación lineal entre incremento de CS y desarrollo de CI (p 0. 001)

Factores de riesgo de IFI por Candida en UCI-Reanimación. Regla de predicción de Ostrosky-Zeichner et Al. Objetivo del estudio: Desarrollar una regla clínicamente relevante de predicción precoz de candidiasis invasora (CI) utilizando combinaciones de factores de riesgo conocidos, además de la colonización. La regla podría utilizarse en ensayos clínicos que investiguen profilaxis, terapia anticipada o tratamiento empírico. Material y método: Revisión retrospectiva de historias clínicas de pacientes de > 19 años de edad, ingresados por más de 4 días en 12 UCI Médicas y/o Quirúrgicas de EE. UU. y Brasil, entre 2000 y 2002. Se recogió información de presencia/ausencia de factores de riesgo “clásicos” de candidemia desde 7 días antes hasta 3 días después del ingreso en la UCI. Con esta información se construyó y validó la regla de predicción. Resultados: Se diagnosticaron 88 casos de CI (84 casos demostrados y 4 probables) entre el día 4 de hospitalización en UCI y el día 7 después del alta de la UCI. (Tasa: 3, 0%). 86

Factores de riesgo de IFI por Candida en UCI-Reanimación. Regla de predicción de Ostrosky-Zeichner et Al. 35 Tras una validación retrospectiva de variaciones/mejoras de la regla original, la regla queda finalmente así: ü Pacientes con estancia mínima en UCI de 4 días + ü Ventilación mecánica al menos 48 h. + ü Tratamiento con antibacteriano días 1 -3 de estancia en UCI. + ü Catéter venoso central días 1 -3 de estancia en UCI. + ü Al menos uno de los siguientes factores de riesgo: ü Cirugía mayor en los 7 días previos a ingreso en UCI. ü Corticoides u otros inmunosupresores en los 7 días previos a ingreso en UCI. ü Pancreatitis en los 7 días previos a ingreso en UCI. ü Nutrición parenteral días 1 -3 de estancia en UCI. 87

Factores de riesgo de IFI por Candida en UCI-Reanimación. Regla de predicción de Ostrosky-Zeichner et Al. Característica de la regla predictiva: Esta regla se ha creado para ser utilizada en Investigación Clínica. Adaptado de Ostrosky-Zeichner et al. Mycoses 2011; 54: 46. . 88

Nebraska Medical Center Rule NMC Rule: (1. 537 x BSAbx¤) + (0. 873 x CVC¤) + (0. 922 x TPN¤) + (0. 402 x esteroidesΩ) + (0. 879 x cirugía abdominal) + (0. 039 x -Media de duración de estancia antes de ingreso en UCI) ¤Días 1 to 3 en UCI. ΩDías -7 to 3 en UCI Crit Care. 2011; 15(4): R 198.


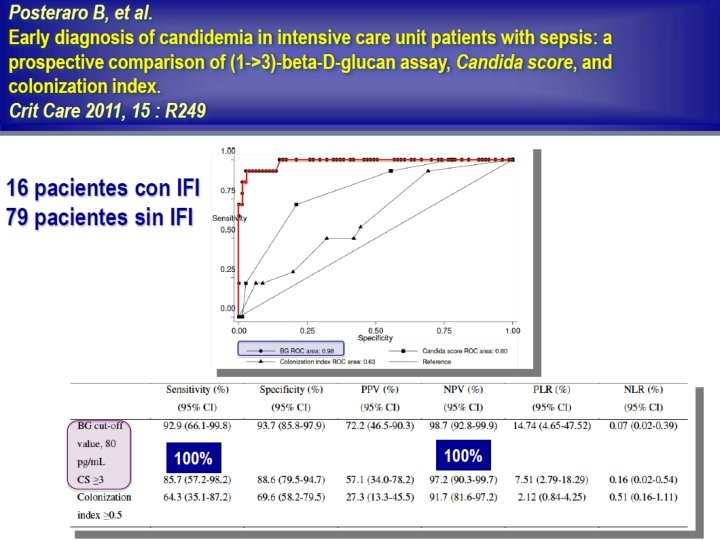
(1– 3)-Beta-D-glucan, Candida Score e Índice de Colonización en pacientes críticos 97 pacientes de UCI. Estancia > 5 días 16 IFI; 14 candidiasis invasiva ◦ 13 BG positivo, 10 con CS >3 y 7 con IC>0. 5.



TRATAMIENTO

DEFINICIONES Profilaxis: administración de tratamiento para prevenir el desarrollo de la enfermedad Tratamiento Anticipado: tratamiento antifúngico precoz mediante uso de marcadores clínicos, radiológicos o de laboratorio en un paciente con factores de riesgo antes de que aparezcan signos y síntomas de infección Tratamiento antifúngico precoz administrado a pacientes colonizados por cándida y con factores de riesgo sin clínica de infección Tratamiento empírico: tratamiento antifúngico administrado a pacientes con factores de riesgo y con clínica de infección

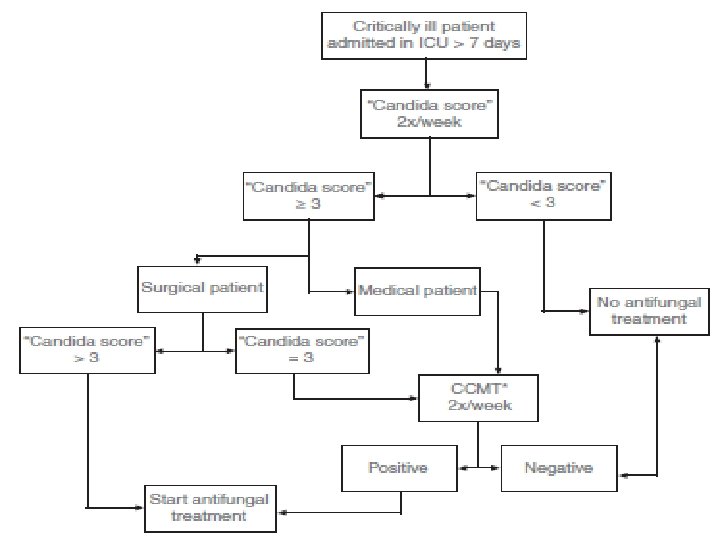
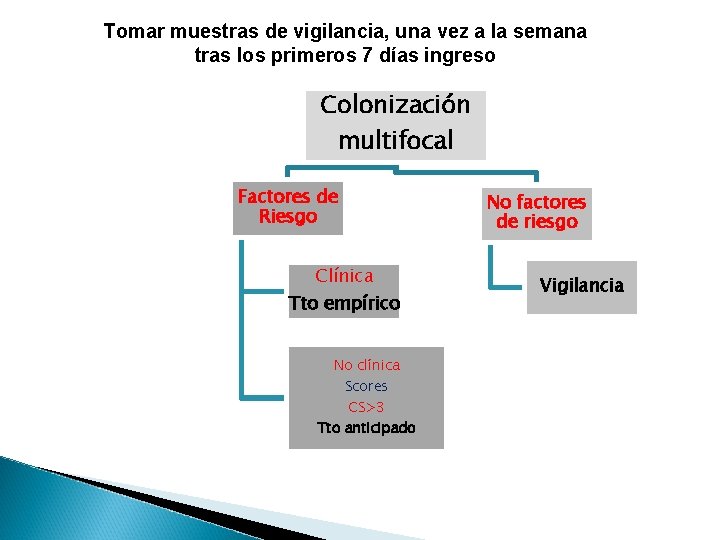
Tomar muestras de vigilancia, una vez a la semana tras los primeros 7 días ingreso Colonización multifocal Factores de Riesgo Clínica Tto empírico No clínica Scores CS>3 Tto anticipado No factores de riesgo Vigilancia

Importancia del diagnóstico y tratamiento precoces de la IFI en pacientes críticos Objetivos del estudio: 1. Identificar la prevalencia del retraso en el tratamiento antifúngico empírico de pacientes con candidemia hasta conocer los resultados de los hemocultivos. 2. Determinar si ese retraso influye en la evolución clínica de los pacientes. Material y métodos: estudio retrospectivo de cohorte, realizado en un hospital universitario de 1200 camas, de EE. UU. Se analizó la mortalidad hospitalaria, pero también otros datos de evolución. Candidatos a participar en el estudio, eran todos los pacientes hospitalizados, con un hemocultivo positivo para Candida (n = 157). 97

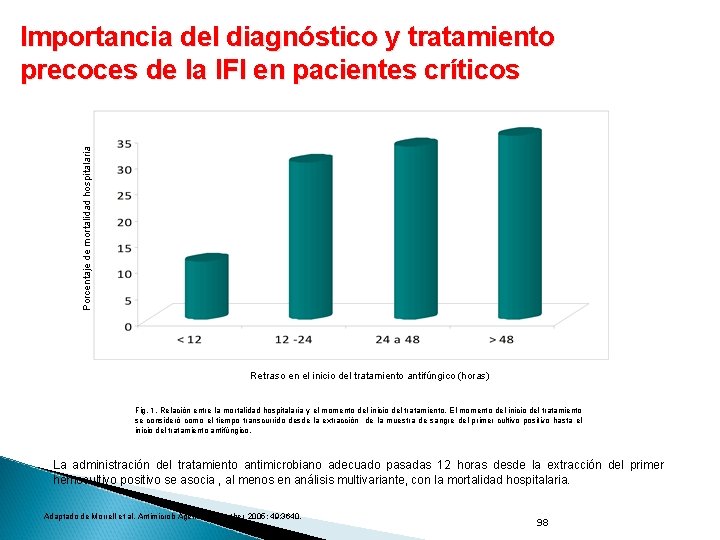
Porcentaje de mortalidad hospitalaria Importancia del diagnóstico y tratamiento precoces de la IFI en pacientes críticos Retraso en el inicio del tratamiento antifúngico (horas) Fig. 1. Relación entre la mortalidad hospitalaria y el momento del inicio del tratamiento. El momento del inicio del tratamiento se consideró como el tiempo transcurrido desde la extracción de la muestra de sangre del primer cultivo positivo hasta el inicio del tratamiento antifúngico. La administración del tratamiento antimicrobiano adecuado pasadas 12 horas desde la extracción del primer hemocultivo positivo se asocia , al menos en análisis multivariante, con la mortalidad hospitalaria. Adaptado de Morrell et al. Antimicrob Agents Chemother 2005; 49: 3640. 98

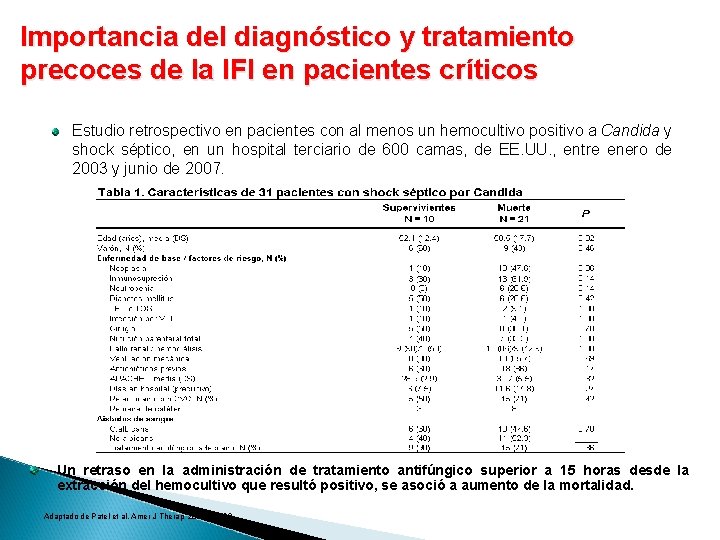
Importancia del diagnóstico y tratamiento precoces de la IFI en pacientes críticos Estudio retrospectivo en pacientes con al menos un hemocultivo positivo a Candida y shock séptico, en un hospital terciario de 600 camas, de EE. UU. , entre enero de 2003 y junio de 2007. Un retraso en la administración de tratamiento antifúngico superior a 15 horas desde la extracción del hemocultivo que resultó positivo, se asoció a aumento de la mortalidad. Adaptado de Patel et al. Amer J Therap 2009; 16: 508.

Importancia del diagnóstico y tratamiento precoces de la IFI en pacientes críticos Objetivos del estudio: 1. Medir en pacientes oncológicos el tiempo transcurrido desde la recogida del hemocultivo (positivo) hasta el inicio de la terapia antifúngica. El tiempo se dividió en tres periodos: ü “Incubación”: desde la toma de la muestra hasta la positivización del cultivo. ü “Notificación”: desde la positivización del cultivo, hasta la notificación al médico a cargo del paciente. ü “Iniciación de tratamiento antifúngico”: desde la notificación, hasta el inicio del tratamiento antifúngico. 2. Ver si existe asociación entre la duración de alguno(s) de estos periodos y la mortalidad. 100

Importancia del diagnóstico y tratamiento precoces de la IFI en pacientes críticos Resultados: ü La mediana total del tiempo fue 43, 2 h. (39, 0 -49, 0 h. IC 95%): Ø Periodo de Incubación: 32, 1 h. (27, 9 -34, 8 h. I. C. 95%). Ø Periodo de Notificación: 0, 3 h. (0, 27 -0, 41 h. I. C. 95%). Ø Periodo de Iniciación de Tratamiento Antifúngico: 7, 5 h. (4, 2 -9, 8 h. I. C. 95%). ü El periodo de incubación fue el único cuya duración se asoció como factor de riesgo independiente, a la mortalidad. La mortalidad hospitalaria aumenta 1, 025 veces por cada hora adicional de periodo de incubación. Adaptado de Taur et al. Antimicrob Agents Chemother 2010; 54: 184. 101

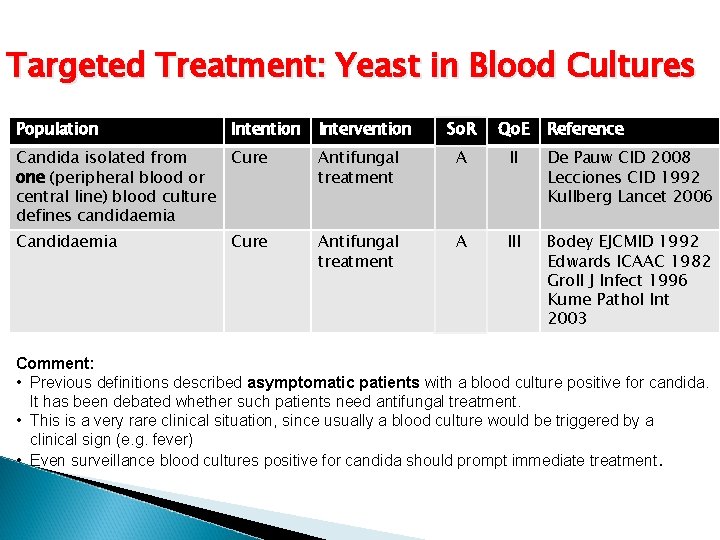
Targeted Treatment: Yeast in Blood Cultures Population Intention Intervention So. R Qo. E Reference Candida isolated from Cure one (peripheral blood or central line) blood culture defines candidaemia Antifungal treatment A II De Pauw CID 2008 Lecciones CID 1992 Kullberg Lancet 2006 Candidaemia Antifungal treatment A III Bodey EJCMID 1992 Edwards ICAAC 1982 Groll J Infect 1996 Kume Pathol Int 2003 Cure Comment: • Previous definitions described asymptomatic patients with a blood culture positive for candida. It has been debated whether such patients need antifungal treatment. • This is a very rare clinical situation, since usually a blood culture would be triggered by a clinical sign (e. g. fever) • Even surveillance blood cultures positive for candida should prompt immediate treatment.

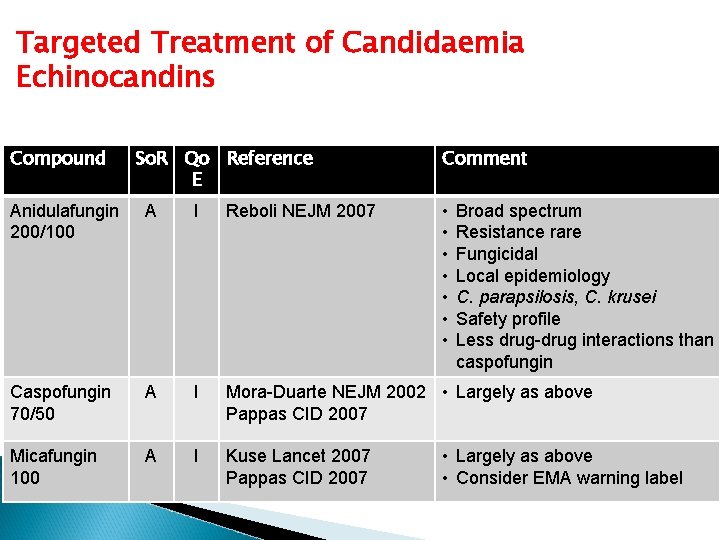
Targeted Treatment of Candidaemia Echinocandins Compound So. R Qo Reference E Comment • • Anidulafungin 200/100 A I Reboli NEJM 2007 Broad spectrum Resistance rare Fungicidal Local epidemiology C. parapsilosis, C. krusei Safety profile Less drug-drug interactions than caspofungin Caspofungin 70/50 A I Mora-Duarte NEJM 2002 • Largely as above Pappas CID 2007 Micafungin 100 A I Kuse Lancet 2007 Pappas CID 2007 • Largely as above • Consider EMA warning label

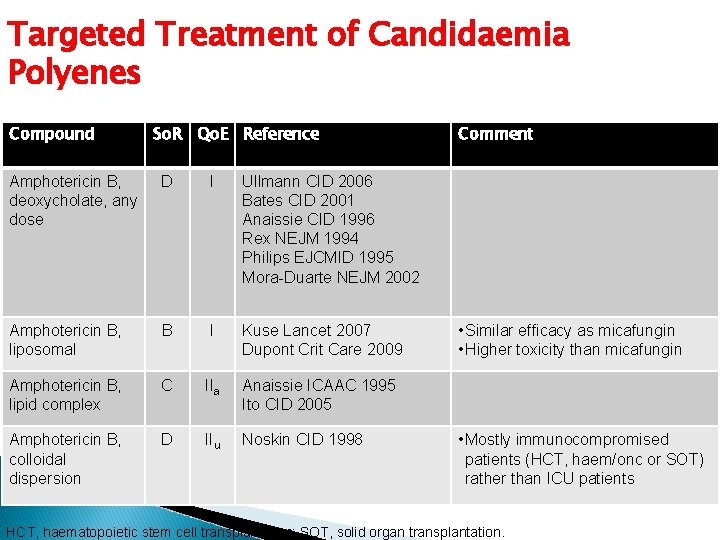
Targeted Treatment of Candidaemia Polyenes Compound So. R Qo. E Reference Amphotericin B, deoxycholate, any dose D I Ullmann CID 2006 Bates CID 2001 Anaissie CID 1996 Rex NEJM 1994 Philips EJCMID 1995 Mora-Duarte NEJM 2002 Amphotericin B, liposomal B I Kuse Lancet 2007 Dupont Crit Care 2009 Amphotericin B, lipid complex C IIa Anaissie ICAAC 1995 Ito CID 2005 Amphotericin B, colloidal dispersion D IIu Noskin CID 1998 Comment • Similar efficacy as micafungin • Higher toxicity than micafungin • Mostly immunocompromised patients (HCT, haem/onc or SOT) rather than ICU patients HCT, haematopoietic stem cell transplantation; SOT, solid organ transplantation.

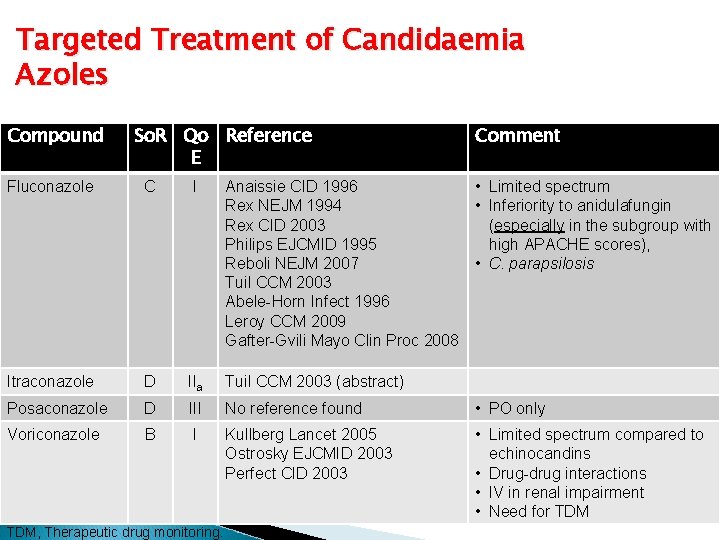
Targeted Treatment of Candidaemia Azoles Compound So. R Qo Reference E Comment Anaissie CID 1996 • Limited spectrum Rex NEJM 1994 • Inferiority to anidulafungin Rex CID 2003 (especially in the subgroup with Philips EJCMID 1995 high APACHE scores), Reboli NEJM 2007 • C. parapsilosis Tuil CCM 2003 Abele-Horn Infect 1996 Leroy CCM 2009 Gafter-Gvili Mayo Clin Proc 2008 Fluconazole C I Itraconazole D IIa Tuil CCM 2003 (abstract) Posaconazole D III No reference found • PO only Voriconazole B I Kullberg Lancet 2005 Ostrosky EJCMID 2003 Perfect CID 2003 • Limited spectrum compared to echinocandins • Drug-drug interactions • IV in renal impairment • Need for TDM, Therapeutic drug monitoring.

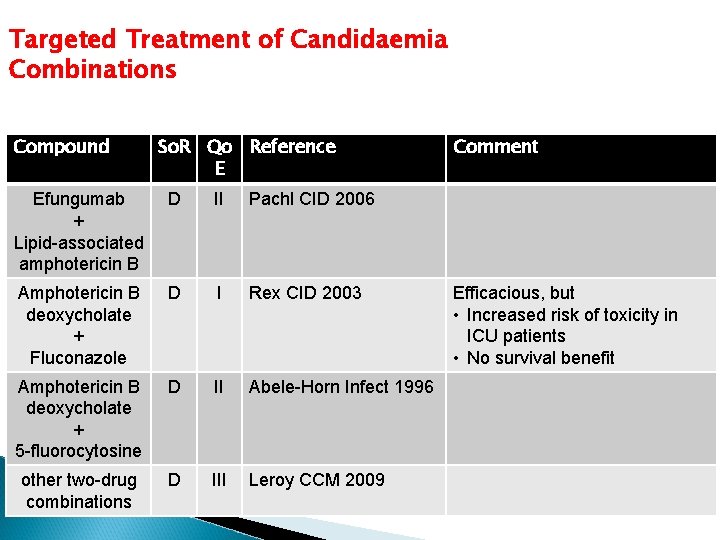
Targeted Treatment of Candidaemia Combinations Compound So. R Qo Reference E Efungumab + Lipid-associated amphotericin B D II Pachl CID 2006 Amphotericin B deoxycholate + Fluconazole D I Rex CID 2003 Amphotericin B deoxycholate + 5 -fluorocytosine D II Abele-Horn Infect 1996 other two-drug combinations D III Leroy CCM 2009 Comment Efficacious, but • Increased risk of toxicity in ICU patients • No survival benefit

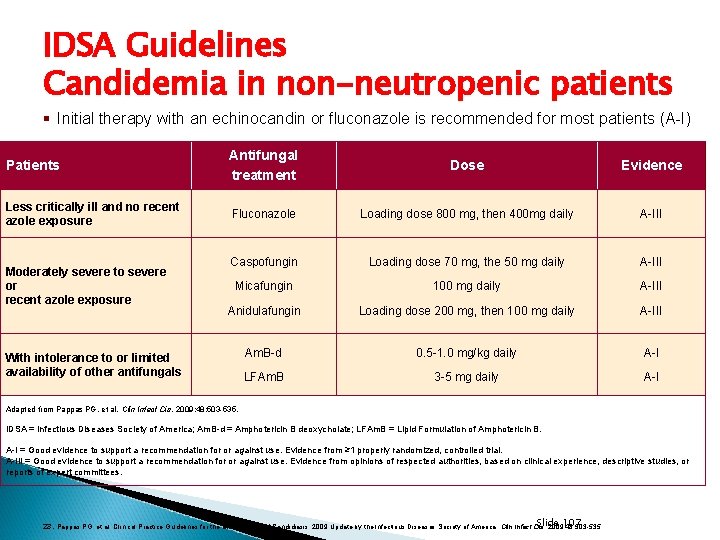
IDSA Guidelines Candidemia in non-neutropenic patients § Initial therapy with an echinocandin or fluconazole is recommended for most patients (A-I) Patients Antifungal treatment Dose Evidence Less critically ill and no recent azole exposure Fluconazole Loading dose 800 mg, then 400 mg daily A-III Caspofungin Loading dose 70 mg, the 50 mg daily A-III Micafungin 100 mg daily A-III Anidulafungin Loading dose 200 mg, then 100 mg daily A-III Am. B-d 0. 5 -1. 0 mg/kg daily A-I LFAm. B 3 -5 mg daily A-I Moderately severe to severe or recent azole exposure With intolerance to or limited availability of other antifungals Adapted from Pappas PG, et al. Clin Infect Dis. 2009; 48: 503 -535. IDSA = Infectious Diseases Society of America; Am. B-d = Amphotericin B deoxycholate; LFAm. B = Lipid Formulation of Amphotericin B. A-I = Good evidence to support a recommendation for or against use. Evidence from ≥ 1 properly randomized, controlled trial. A-III = Good evidence to support a recommendation for or against use. Evidence from opinions of respected authorities, based on clinical experience, descriptive studies, or reports of expert committees. Slide 107 23. Pappas PG, et al. Clinical Practice Guidelines for the Management of Candidiasis: 2009 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2009; 48: 503 -535.

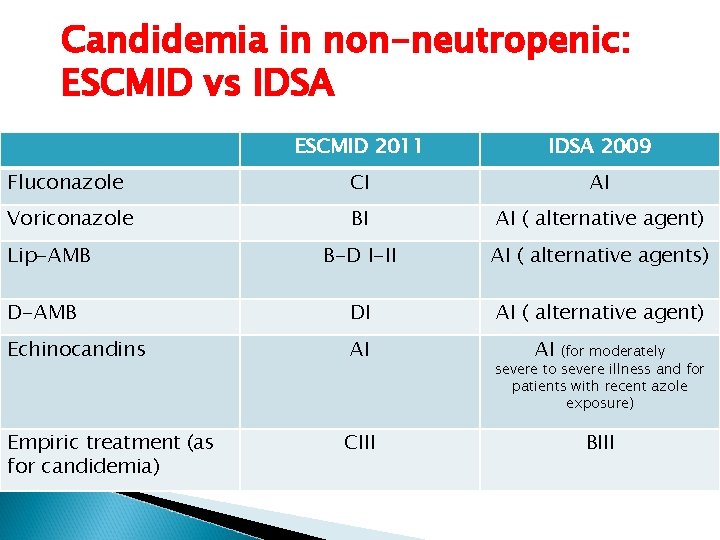
Candidemia in non-neutropenic: ESCMID vs IDSA ESCMID 2011 IDSA 2009 Fluconazole CI AI Voriconazole BI AI ( alternative agent) B-D I-II AI ( alternative agents) D-AMB DI AI ( alternative agent) Echinocandins AI (for moderately severe to severe illness and for patients with recent azole exposure) Empiric treatment (as for candidemia) CIII BIII Lip-AMB AI



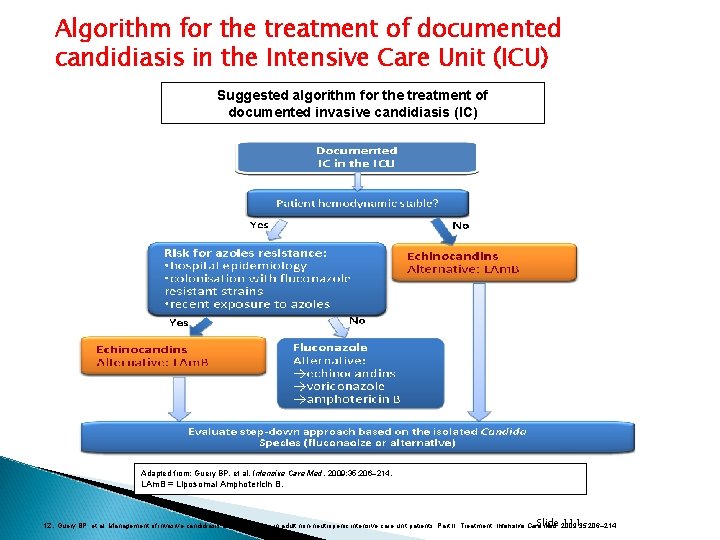
Algorithm for the treatment of documented candidiasis in the Intensive Care Unit (ICU) Suggested algorithm for the treatment of documented invasive candidiasis (IC) Adapted from: Guery BP, et al. Intensive Care Med. 2009; 35: 206– 214. LAm. B = Liposomal Amphotericin B. Slide 111 12. Guery BP, et al. Management of invasive candidiasis and candidemia in adult non-neutropenic intensive care unit patients: Part II. Treatment. Intensive Care Med. 2009; 35: 206– 214.

Treatment of candida in non-neutropenic patients (ESCMID guidelines 2011) Strongly recommended: recommended echinocandin (AI) Blood culture positive for yeast or empiric therapy (CIII) Start antifungal therapy (AII) Not recommeded (D): Conventional Amphotericin B Itraconazole Posaconazole Combination Moderately recommended: L-AMB or voriconazole (BI) Marginally recommended: fluconazole or ABLC (CI) Cornely OA et al. 21 st ECCMID, Milano 20011 http: //www. escmid. org/escmid_library/online_lecture_library/eccmid/21 st_eccmid 27 th_icc_2011_milan/educational_workshops_2011 /

TRATAMIENTO CANDIDEMIA Tratamiento i. v. para todos los pacientes críticos con candidemia Tratamiento precoz Candidemia factor de riesgo para recibir tratamiento empírico inadecuado en pacientes críticos con sepsis Practica diaria tratamiento antifungico se retrasa hasta la confirmación de la candidemia Elevada mortalidad

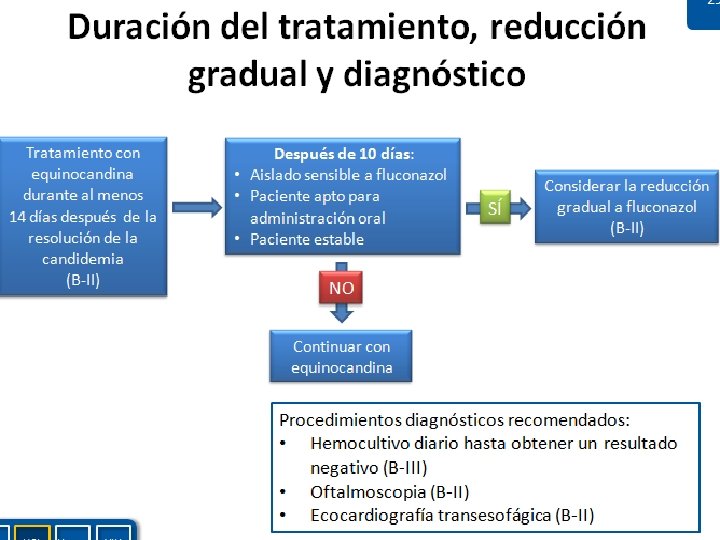
TRATAMIENTO CANDIDEMIA Retirada catéteres Realizar Ecocardiografía y fondo ojo Tratamiento durante 14 días tras el ultimo hemocultivo positivo (cultivo diario)



Candida spp. en punta de catéter sin candidemia Estudio retrospectivo 58 p con asilamiento Candida spp punta catéter (91% UCI). 20 tratamiento antifungico No diferencias mortalidad Analisis multivariante no beneficio tratamiento Estudio retrospectivo 11% pacientes cultivo positivo punta cateter desarrollaron candidemia /CI con aumento mortalidad No evidencia recomendar tratamiento antifungico si no hay candidemia. Valorar scores y/o técnicas alternativas cultivo

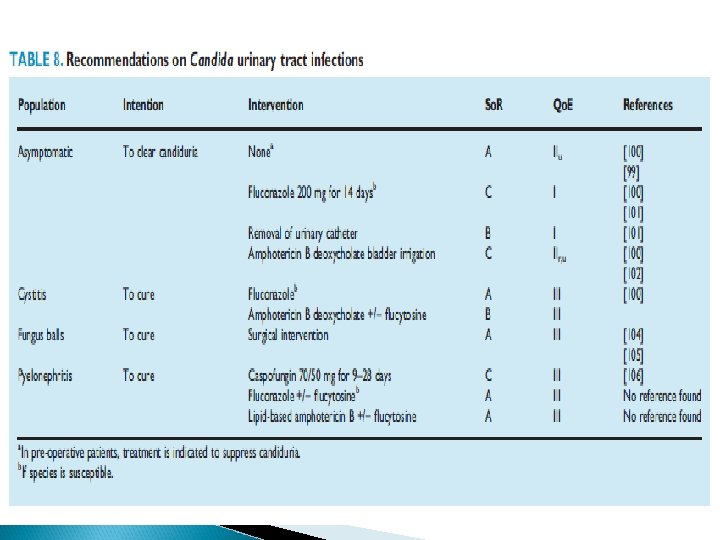
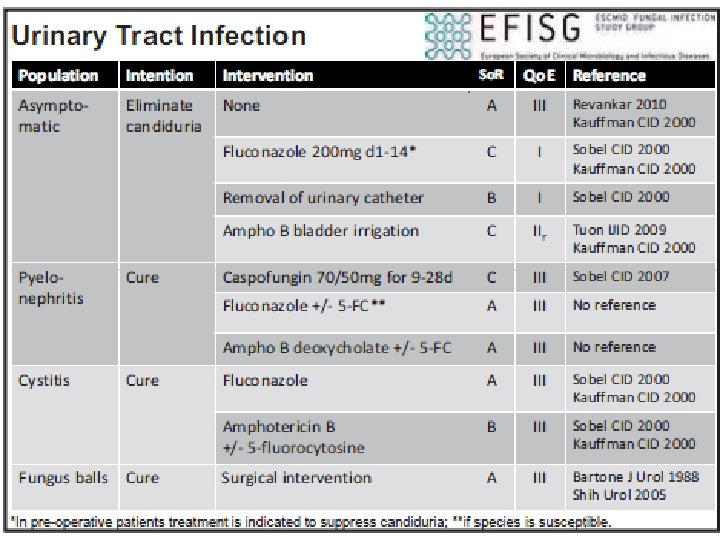
Aislamiento de Candida spp. en orina Candiduria 25% pacientes críticos con estancia > 7 días. Aumento mortalidad 8% candidurias desarrollan candidemia por la misma especie Mayoría pacientes asilamiento cándida orina colonización Retirada sonda vesical logra erradicación candiduria 40% casos Fluconazol altas concentraciones orina. Anfotericina B liposomoal y equinocandinas bajas concentraciones

Aislamiento de Candida spp. en orina Recuento ufc/ml. <103 no infección 103 -104 repetir cultivo 105 infección Candiduria sintomática tratamiento Candiduria asintomática No tratamiento Alto riesgo CI tratamiento Manipulación u obstrucción tratamiento Retirada sonda vesical

Aislamiento de Candida spp. en orina Ø No Ø C. irrigaciones vesicales Albicans Fluconazol Ø C Glabrata Fluconazol dosis altas Ø C. kruseii Anfotericina B. Caspofungina





LO QUE NO MATA ENGORDA