CASO CLNICO Escola Superior de Cincias da Sade














![ETIOLOGIA n n Outras proteínas: transcrição (TAT [p 14]), expressão do RNAm viral (VER ETIOLOGIA n n Outras proteínas: transcrição (TAT [p 14]), expressão do RNAm viral (VER](https://slidetodoc.com/presentation_image_h2/84ed16c335521a8453165d6480933034/image-17.jpg)










































































- Slides: 110

CASO CLÍNICO Escola Superior de Ciências da Saúde – ESCS Pediatria – Internato – HRAS Brasília, 27 de outubro de 2006. Aluna: Gisela de Lima Gomes de Menezes Docente: Elisa de Carvalho www. paulomargotto. com. br

ANAMNESE (03/10/06) Ø Ø Identificação: JVLG, sexo masculino, 6 meses e 22 dias, nascido em 11/03/06, natural de Brasília (DF), residente em Candangolândia(DF). Informante e responsável: Mãe Queixa Principal: Dor de ouvido, febre e perda de peso há 15 dias.

H. D. A: Mãe da criança refere ser portadora do vírus HIV, sendo que a doença foi constatada durante a gestação da criança (no último trimestre). Refere ter feito uso de terapia anti-retroviral somente no final da gestação e no período intra-parto (fez uso de AZT). Refere que, desde que nasceu, a criança realiza acompanhamento no Hospital Dia, sendo confirmada infecção pelo vírus HIV aos dois meses de idade (sic). Refere que a criança evoluiu bem até os 4 meses de vida, quando passou a apresentar otites de repetição, levando a mãe a procurar regularmente acompanhamento médico em função dos quadros, mas não seguia plenamente os tratamentos recomendados.

H. D. A: Refere que, há 15 dias, a criança iniciou quadro de febre não aferida, perda de peso (não sabe quantificar a perda, mas refere frouxidão das roupas), além de saída de secreção amarelada pelos dois ouvidos. Procurou atendimento local, sendo orientado uso de amoxicilina durante 10 dias (mãe cumpriu o tratamento). Há 01 dia a criança apresentou piora do quadro, com surgimento de dispnéia e fraqueza. Procurou auxílio no atendimento ambulatorial do Hospital Dia, sendo então diagnosticada otite supurada bilateral, sendo a criança encaminhada para internação na HRAS.

- - Antecedentes pessoais fisiológicos: Mãe G 2 CI PI A 0. Parto cesáreo, a termo (sic). Nega complicações durante a gestação. Peso: 2920 g PC: 36 cm Est: 49 cm Relatou ter feito pré-natal, mas não dispunha do cartão no momento. APGAR: 8(1º) – 10(2º) Desenvolvimento Psicomotor Normal Nega aleitamento materno. Refere alimentar a criança com NAN I, sopinhas e sucos. Calendário vacinal em dia.

Anamnese - - - Antecedentes pessoais patológicos: Doenças prévias: Nega doenças comuns da infância. Refere IVAS de repetição desde os 4 meses. Refere que esta é a primeira internação. Nega: alergias, hemotransfusões, traumas, cirurgias. Refere que fez uso de AZT xarope somente e estava em uso de Bactrim profilático.

Hábitos de vida e condições sócioeconômicas: - Casa de alvenaria, 4 cômodos, 3 pessoas, esgoto, água encanada. Nega animais. - Antecedentes Familiares: - Mãe, 26 anos, HIV positiva - Nega consangüinidade - Irmão: 9 anos – saudável - Doenças na família: nega

Exame Físico: - REG, hipocorado (+/4+), hidratado, anictérico, acianótico, taquidispnéico, pouco ativo; cooperativo - FC: 128 bpm FR: 47 irpm - ACV: RCR, 2 T , BNF e sem sopros; - AR: Presença de tiragem intercostal discreta; MVF+, presença de crepitações discretas principalmente hemitórax direito; - AB: plano, normotenso, indolor, s/VMG, RHA+; - EXT: Bem perfundidas (<1”) e s/ edemas; - Sist. Nervoso: Pupilas fotorreagentes, nuca livre, ausência de sinais meníngeos. Peso: 7560 g (P 25)

EXAMES LABORATORIAIS (04/10/06): Hemograma: n Hb: 7, 9 g/dl n HT: 25, 0% n HM: 3500000 n Plaq: 283000 n Leucócitos: 14700 SEG: 63% - BAST: 02% - LINF: 30% - MONO: 04% EOS: 01% - BAS: 0 VHS: 65 mm – PCR: 1, 38 mg/dl – LDH: 1495 U/L

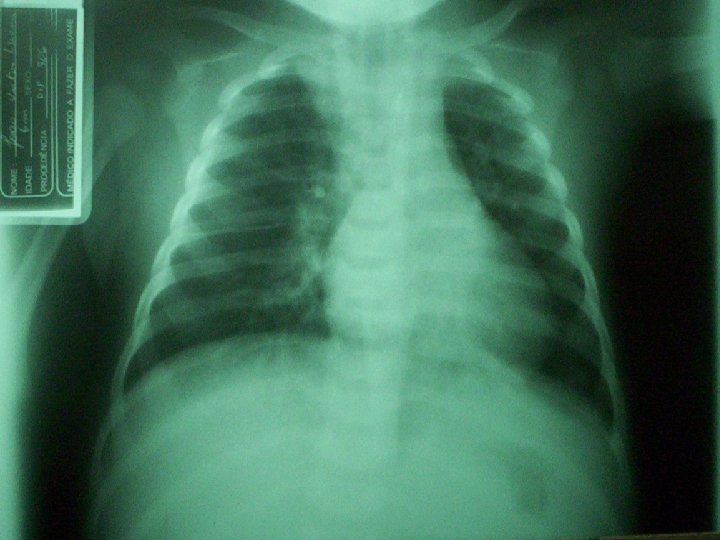
EXAMES LABORATORIAIS (04/10/06): n n n n Uréia: 14 mg% Creatinina: 0, 3 mg% BT: 0, 4 mg% BD: 0, 2 mg% BI: 0, 2 mg% TGO: 42 U/L TGP: 19 U/L Na: 130 m. Eq/L – K: 4, 2 m. Eq/L – Cl: 100 m. Eq/L RX de tórax (05/10/06): Infiltrado em todo o HTD, mais acentuado na base e em LSE e perihilar esquerdo. Seios costofrênicos livres. Coração anatômico. HD: Pneumonia

n n Informações obtidas oralmente do prontuário do Hospital Dia: Carga viral aos 2 meses: >500. 000 cópias CD 4: 1869 CD 8: 2563



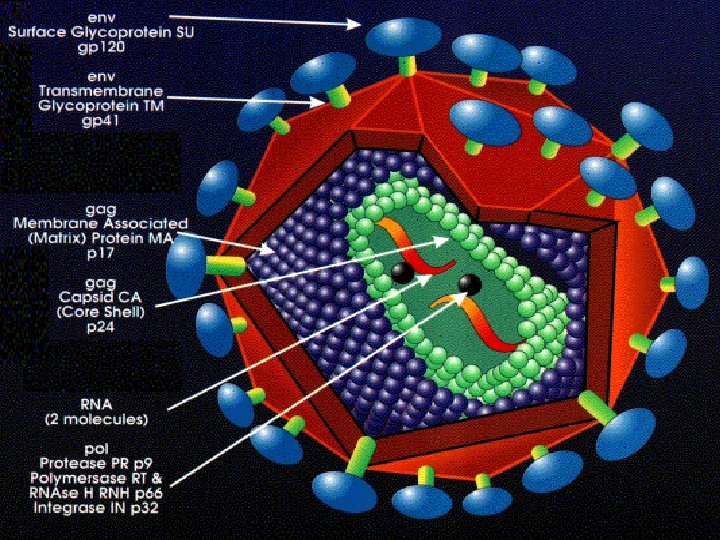
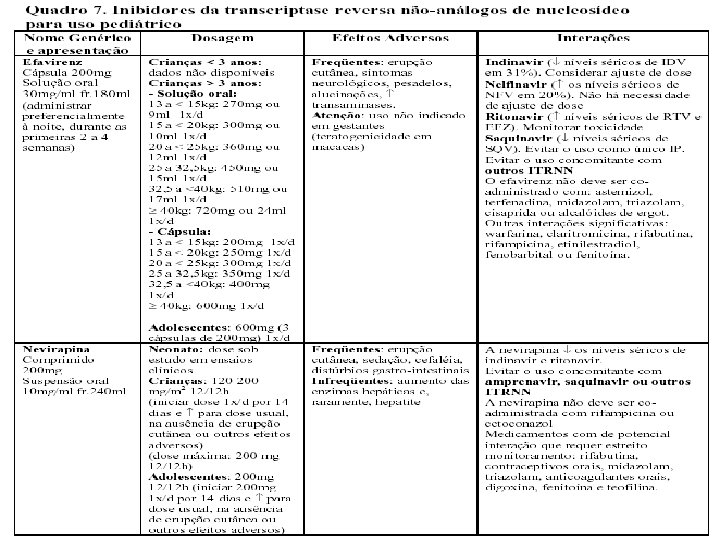
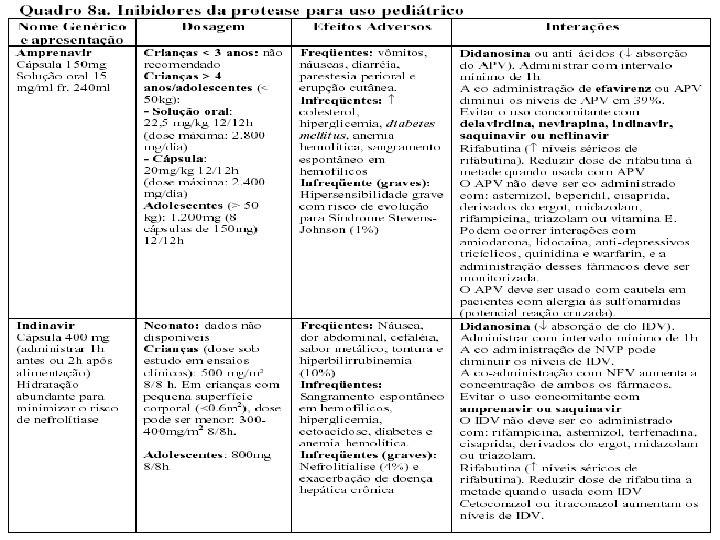
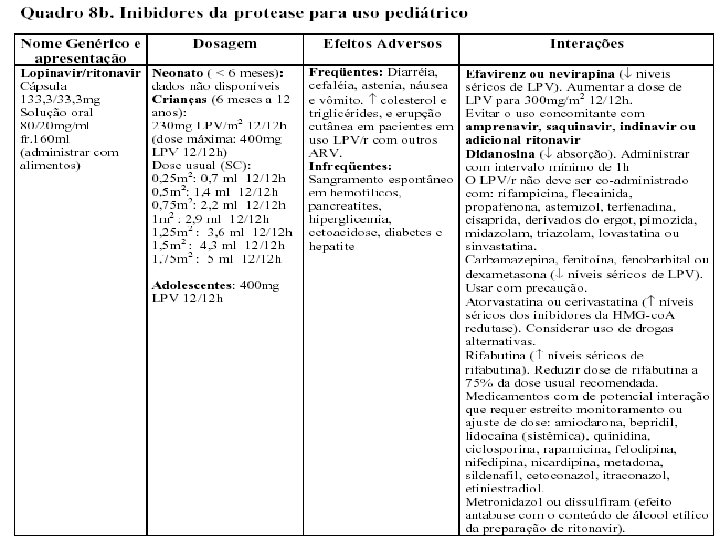
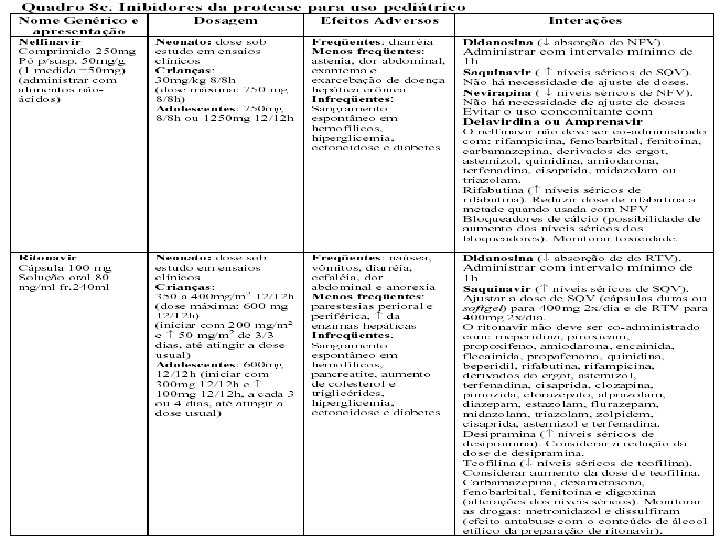
ETIOLOGIA n n n O HIV 1 E 2 são membros da família Retroviridae e pertencem ao gênero Lentivirus, que abrangem os vírus citopáticos. Genoma com RNA de filamento único e e tamanho de 9, 8 kb, com regiões idênticas nas duas extremidades do genoma. O restante do genoma inclui três regiões codificadoras principais:


ETIOLOGIA n n n Região GAG: codifica proteínas do cerne viral – p 24, p 17, p 9, p 6 (derivadas do p 55) Região POL: codifica as enzimas virais transcriptase reversa (p 51), protease (p 10) e integrase (p 32) Região ENV: codifica as proteínas do invólucro viral gp 120 e gp 41 (derivadas da gp 160)
![ETIOLOGIA n n Outras proteínas transcrição TAT p 14 expressão do RNAm viral VER ETIOLOGIA n n Outras proteínas: transcrição (TAT [p 14]), expressão do RNAm viral (VER](https://slidetodoc.com/presentation_image_h2/84ed16c335521a8453165d6480933034/image-17.jpg)
ETIOLOGIA n n Outras proteínas: transcrição (TAT [p 14]), expressão do RNAm viral (VER [p 19]), infecciosidade viral aumentada (NEF [p 27]), liberação viral (VPR [p 15]) e síntese de DNA proviral (NIF [p 23]). A gp 120 é uma molécula complexa que inclui uma alça V 3 altamente variável e sua heterogeneidade é razão das dificuldades para a criação de uma vacina anti-HIV eficaz.

ETIOLOGIA n A gp 120 também possui sítio de ligação para a molécula de CD 4+, que é encontrado principalmente nos linfócitos T auxiliares. Existem também receptores secundários, como o CXCR-4 (co-receptor para fixação do HIV aos linfócitos, o CCR 5, receptor das B-quimiocinas, que facilita a entrada do HIV nos macrófagos, bem como outros co-receptores.

ETIOLOGIA n n Mecanismo menos comum de fixação do HIV: uso de anticorpos não-neutralizantes – a parte Fab (dos anticorpos) liga-se ao vírus e a parte Fc liga-se a células que expressam este mesmo receptor (macrófagos, fibroblastos), facilitando a entrada do vírus na células. Há envolvimento de fatores do complemento como um mecanismo de fixação do HIV às células.

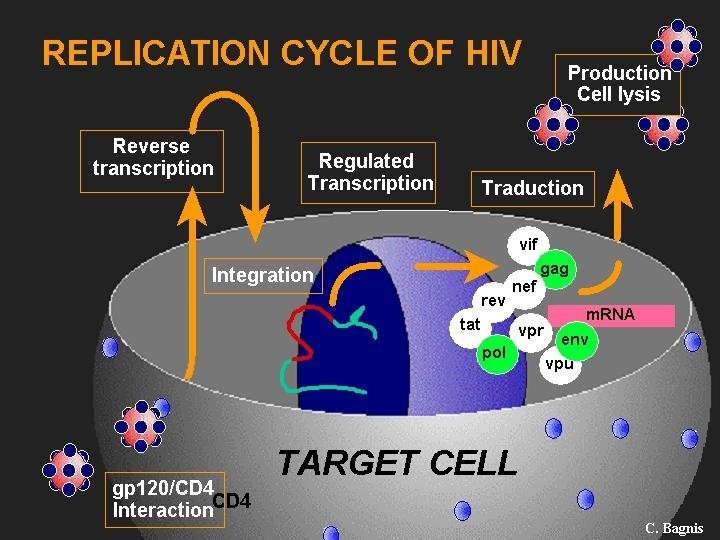
ETIOLOGIA n n 1º Etapa: Fixação Viral à célula. 2º Etapa: Alterações na conformação da gp 120 e da molécula CD 4. 3º Etapa: gp 41 interage com o receptor de fusão na superfície celular, provocando a fusão viral com a membrana celular. 4º Etapa: Entrada do RNA viral no citoplasma celular.

ETIOLOGIA n n 5º Etapa: Transcrição do RNA pela transcriptase reversa (DNA polimerase dependente de RNA) em DNA viral. 6º Etapa: Transporte do DNA do vírus para o núcleo da célula e integração ao DNA da célula = PROVÍRUS

LINHA DE MONTAGEM n De acordo com a expressão dos genes reguladores virais (TAT, ENV, NEF, entre outros), o DNA proviral codifica produção de RNA viral , que leva a produção das “proteínas de montagem”.


Montagem do Vírus n n Ocorre transcrição e tradução do HIV, com clivagem de proteínas para produção de proteases específicas, dentre elas a protease específica do Vírus (p 10). O genoma do RNA é incorporado ao capsídeo viral recém-formado e. Quando o vírus está formado, ele brota da membrana celular e é liberado.

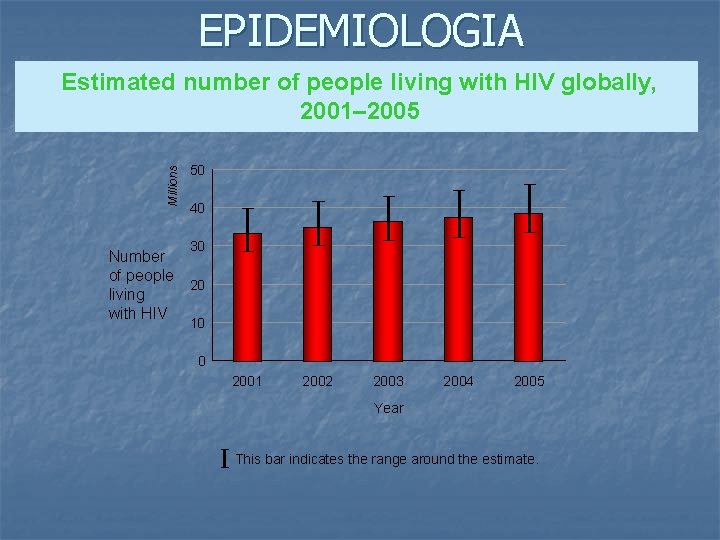
EPIDEMIOLOGIA Millions Estimated number of people living with HIV globally, 2001– 2005 50 40 30 Number of people 20 living with HIV 10 0 2001 2002 2003 2004 2005 Year This bar indicates the range around the estimate.

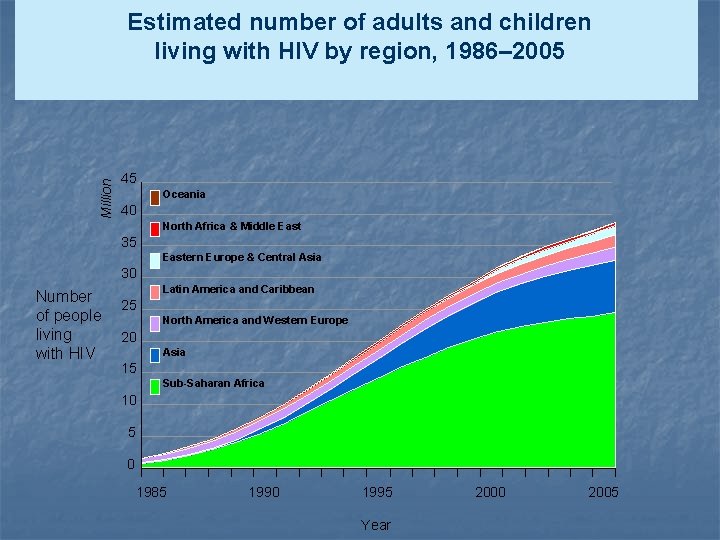
Million Estimated number of adults and children living with HIV by region, 1986– 2005 45 Oceania 40 North Africa & Middle East 35 Eastern Europe & Central Asia 30 Number of people living with HIV Latin America and Caribbean 25 North America and Western Europe 20 Asia 15 Sub-Saharan Africa 10 5 0 1985 1990 1995 Year 2000 2005

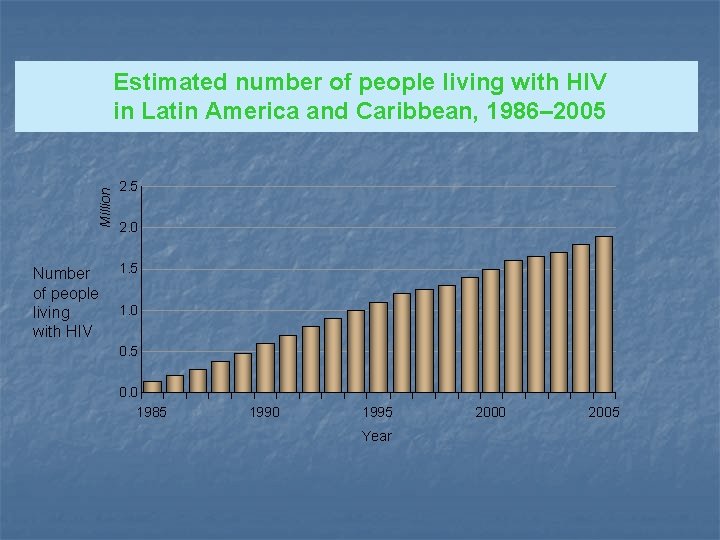
Million Estimated number of people living with HIV in Latin America and Caribbean, 1986– 2005 Number of people living with HIV 2. 5 2. 0 1. 5 1. 0 0. 5 0. 0 1985 1990 1995 Year 2000 2005

TRANSMISSÃO n n n Contato sexual, exposição parenteral a fluidos contaminados, transmissão vertical da mãe para a criança (intra-uterina, intraparto, aleitamento). Existem cerca de 8000 menores de 14 anos portadores de HIV no Brasil. Na população pediátrica, a transmissão vertical responde por praticamente todos os casos. A maioria dos estudos europeus e norte-americanos mostra que, em mulheres não tratadas, a taxa de transmissão varia entre 12 e 30%. O uso de drogas anti-retrovirais reduz esta taxa para 8% em média.

TRANSMISSÃO n n n Transmissão intra-uterina desde o primeiro trimestre – estudos em placentas: 10 semanas Maioria dos casos: aquisição intraparto (secreções cervicovaginais e sangue). Fatores de risco: Parto Prematuro (<34 sem), baixo peso ao nascer, baixa contagem materna de CD 4+, uso de drogas intravenosas na gestação e rotura de membranas (>4 horas).

TRANSMISSÃO n n n Parto cesáreo eletivo + terapia com Zidovudina: ↓ da transmissão vertical em 87% ↑ do risco de transmissão na amamentação: 14 a 30% Transfusões de sangue ou hemoderivados 3 a 6% dos casos pediátricos (diminuição após a triagem).

PATOGENIA n n Ligação às células que expressam CD 4+ (linfócitos T auxiliares, monócitos-macrófagos, micróglia, astrócitos, oligodendróglia, tecido placentário) → células CD 4+ migram para linfonodos e proliferam → Vírions e imunocomplexos migram através dos linfonodos e são aprisionados na rede folicular de células dentríticas → facilita a apresentação de antígenos → Ativação das células CD 4+ com favorecimento da replicação viral Linfadenopatia generalizada (Síndrome Retroviral Aguda – Mononucleose Like) → resposta imune e humoral em 2 a 4 meses

PATOGENIA n n Células T Supressoras CD 8 contêm a infecção. Linfócitos T citolíticos HIV específicos desenvolvem-se contra proteínas virais (ENV, POL, GAG, TAT. . . ). Liberação de fator solúvel que suprime a replicação viral. Anticorpos neutralizantes.

PATOGENIA n n n Processo de Turnover com perda de mais de 1 bilhão de células CD 4 por dia Progressão da doença: ruptura da rede de células dendríticas foliculares → perda da capacidade de aprisionar o HIV → liberação de vírus na circulação → alta viremia Propagação sistêmica no feto é mais rápida pelo imaturo sistema imune → grave comprometimento da imunidade

PATOGENIA n n Presença viral precoce sugere infecção in utero, com aumento rápido da carga viral nos primeiros 2 a 3 meses, chegando a 750000 cópias/ml (paciente com 500000 cópias/ml). Infecção in utero: menor sobrevida Cuidado com a “linfocitose relativa”: mascara a depleção de CD 4+ Hipergamaglobulinemia (>1750 g/L) → desregulação das células T na síntese de anticorpos pelas células B → não serve para nada

MANIFESTAÇÕES CLÍNICAS n Criança x Adultos e Adolescentes Diarréia e Infecção Respiratória x Infecções Oportunistas

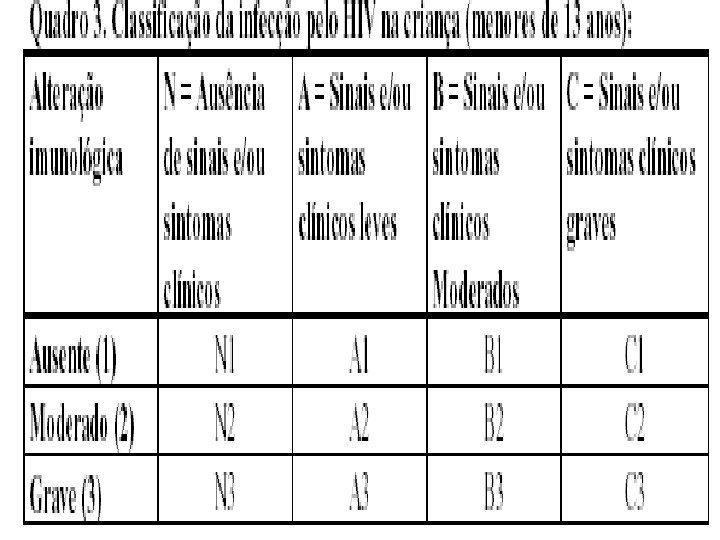
Classificação Pediátrica do HIV n n N: Ausência de Sinais ou sintomas clínicos A: dois sintomas leves (hepatoesplenomegalia, linfadenopatia, paroditite, dermatite, sinusite, otite média) B: sintomas moderados (candidíase, persistente, diarréia recorrente/crônica, febre persistente, varicela grave, acometimento renal ou cardíaco, estomatite, esofagite C: sintomas graves (2 infecções bacterianas graves no espaço de 2 anos, candidíase esofágica ou do trato respiratório, infecções SNC e fúngicas graves, pneumocistose, MAC

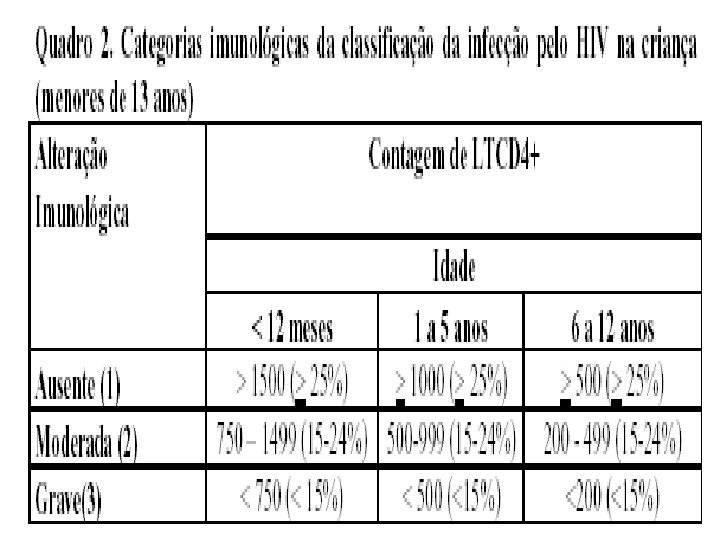
Classificação Pediátrica do HIV Classificação Imune: Contagem CD 4

MANIFESTAÇÕES CLÍNICAS n n A história natural da infecção pelo HIV em crianças tem espectro amplo, com pacientes variando de progressores rápidos a nãoprogressores. Cerca de 10 a 15% evoluem com imunodepressão precoce e deterioração clínica nos primeiros dois anos de vida (progressão rápida). A maior parte, 50% a 70%, apresenta padrão de evolução intermediário, em que predominam sinais e sintomas leves nos primeiros 5 anos de vida. Um terceiro grupo, cerca 10 a 15%, tem progressão lenta e livre de manifestações da doença até 8 anos de idade.

MANIFESTAÇÕES CLÍNICAS n n INFECÇÕES BACTERIANAS Microorganismos encapsulados (Streptococcus pneumoniae e Salmonela spp). Outros patógenos: Staphylococcus, Enterococcus, Pseudomonas aeruginosa, Haemophylus influenzae, outros G+ e GResultam principalmente da perturbação da imunidade humoral Mais comuns: bacteremia, sepse e PNM

MANIFESTAÇÕES CLÍNICAS n n n INFECÇÕES POR MICOBACTÉRIAS ATÍPICAS Mycobacterium avium (MAC) – rara em crianças com terapia anti-retroviral eficaz. Febre, mal-estar, perda ponderal, sudorese noturna, diarréia, dor abdominal. Diagnóstico: Isolamento do MAC no sangue, medula ou tecidos TTO: Macrolídeos + etambutol + rifabutina, cipro ou amicacina

MANIFESTAÇÕES CLÍNICAS n n INFECÇÕES FÚNGICAS Candidíase oral é a mais comum. TTO: Nos casos menos graves, utiliza-se nistatina, clotrimazol, anfotericina oral (suspensão) e fluconazol nos casos mais graves. São MUITO RARAS em pacientes pediátricos: histoplasmose, coccidioidomicose ou criptococose (ocorrem mais em áreas endêmicas).

MANIFESTAÇÕES CLÍNICAS n n OUTRAS PARASITOSES A criptosporidiose, microsporidiose e raramente a isosporíase ou giardíase são infecções oportunistas que causam morbidade significativa em pacientes infectados pelo HIV, levando frequentemente a desnutrição e diarréia crônica.

MANIFESTAÇÕES CLÍNICAS n n INFECÇÕES VIRAIS Herpesvírus → gengivo - estomatite recorrente, complicações pela disseminação local (cutânea) e à distância. Varicela Zoster → complicada com resistência ao aciclovir, exigindo uso de foscarnet. Herpes Zoster → muito debilitantes também com risco de resistência ao aciclovir.

MANIFESTAÇÕES CLÍNICAS n n n Citomegalovírus → retinite, pneumonite, esofagite, gastrite com obstrução pilórica, hepatite, colite, encefalite (tto com ganciclovir e foscanet). Sarampo → pode ocorrer a despeito da imunização e cursar com sintomas atípicos, sem o exantema típico, disseminando-se para pulmão e cérebro com altíssima taxa de mortalidade. Vírus Sincicial Respiratório e Adenovírus

MANIFESTAÇÕES CLÍNICAS n n n SISTEMA NERVOSO CENTRAL Envolvimento do SNC entre 40 -90% com idade média de 19 meses. Encefalopatia progressiva, perda dos marcos de desenvolvimento, deterioração cognitiva, comprometimento do crescimento cerebral (microcefalia adquirida) e disfunção motora simétrica, apatia intensa, espasticidade, hiperreflexia, alteração da marcha, perda da linguagem e habilidades motoras orais refinadas e grosseiras.

MANIFESTAÇÕES CLÍNICAS n n Linfoma do SNC: achados motores focais, cefaléia, convulsões e alterações do estado mental. Toxoplasmose é RARÍSSIMA em lactentes pequenos.

MANIFESTAÇÕES CLÍNICAS n n INFECÇÕES DO TRATO RESPIRATÓRIO SUPERIOR Otites, sinusites, faringites de repetição não são muito comuns, embora alguns patógenos como a P. aeruginosa, leveduras e anaeróbios possam estar presentes e levar a sinusites invasiva e mastoidite.

MANIFESTAÇÕES CLÍNICAS n n SISTEMA CARDIOVASCULAR A incidência das manifestações cardíacas ainda não foi devidamente avaliada, mas cerca de 20% das crianças infectadas pelo HIV têm algum grau de envolvimento cardíaco → Anormalidades hemodinâmicas, arritmias, disfunção ventricular esquerda, insuficiência cardíaca congestiva esquerda e taquicardia sinusal

MANIFESTAÇÕES CLÍNICAS n n TRATOS GASTRINTESTINAL E HEPATOBILIAR As manifestações orais da doença incluem candidíase eritematosa e pseudomembranosa, doença periodontal, das glândulas salivares, leucoplaquia pilosa oral e ulcerações.

MANIFESTAÇÕES CLÍNICAS n n O envolvimento do trato gastrintestinal inferior é comumente causado por bactérias (Salmonella, Campylobacter, MAC), protozoários (Crytosporidium, Isospora, microsporídeos e Giardia), vírus (CMV, herpes simples, rotavírus) e fungos (Candida). Diarréia, dor abdominal, disfagia, atraso do crescimento, mal-absorção, perda ponderal.

MANIFESTAÇÕES CLÍNICAS n n Inflamação Hepática Crônica, evidenciada por níveis séricos flutuantes de transaminases hepáticas com ou sem colestase é relativamente comum, muitas vezes sem um agente etiológico identificado. A pancreatite, com elevação das enzimas pancreáticas pode cursar sem dor abdominal ou outros sintomas típicos pode sobrevir de infecções por MAC, CMV ou pela própria terapia anti - retroviral.

MANIFESTAÇÕES CLÍNICAS n n n DOENÇA RENAL É incomum , mas está relacionada a lesão direta do HIV, além de hiperviscosidade (secundária a hiperglobulinemia) sanguínea, imunocomplexos e drogas nefrotóxicas. Glomeruloesclerose focal (IR), hiperplasia mesangial, glomerulonefrite necrosante segmentar e doença por lesão mínima.

MANIFESTAÇÕES CLÍNICAS n n MANIFESTAÇÕES CUT NEAS Dermatite seborréica ou eczema intenso e refratário ao tratamento, além de episódios recorrentes de molusco contagioso, herpes simples, herpes zoster, verrugas anogenitais, infecções por Candida.

MANIFESTAÇÕES CLÍNICAS n n DOENÇA HEMATOLÓGICA Anemia em 20 -70% das crianças infectadas (parvovírus B 19, fenômeno auto-imune, nutrição deficiente, aplasia eritróide, síndrome hemofagocitária, efeito colateral de medicações. Leucopenia em 1/3 dos infectados, bem como neutropenia (anticorpos antineutrófilos, além de drogas usadas na profilaxia). Trombocitopenia em 10 -20% (imunocomplexos circulantes ou anticorpos antiplaquetários), toxicidade medicamentosa ou idiopática.

MANIFESTAÇÕES CLÍNICAS n n n Cistos tímicos multiloculares no mediastino anterior sem sintomas clínicos, muitas vezes com involução espontânea. C NCER Em contraste com adultos contaminados, as doenças malignas foram infreqüentes em crianças. Os mais comuns são aqueles relacionados ao Epstein-Barr(linfomas e leiomiossarcomas). Sarcoma de Kaposi (pouquíssimos registros).

MANIFESTAÇÕES CLÍNICAS n n Pneumonia por Pneumocystis carinii Aspectos FUNDAMENTAIS: O pico de incidência ocorre entre crianças HIV positivas com menos que 1 ano de vida, principalmente entre os 3 e 6 meses, independente da dosagem de CD 4

MANIFESTAÇÕES CLÍNICAS n n Início Agudo de febre, taquipnéia, dispnéia, hipoxemia progressiva, que pode ocorrer antes dos sintomas. HIPOXEMIA: É comum a ocorrência de hipoxemia sem retenção de CO 2 em pneumonias intersticiais (pneumocistose é a mais provável causa, neste caso).

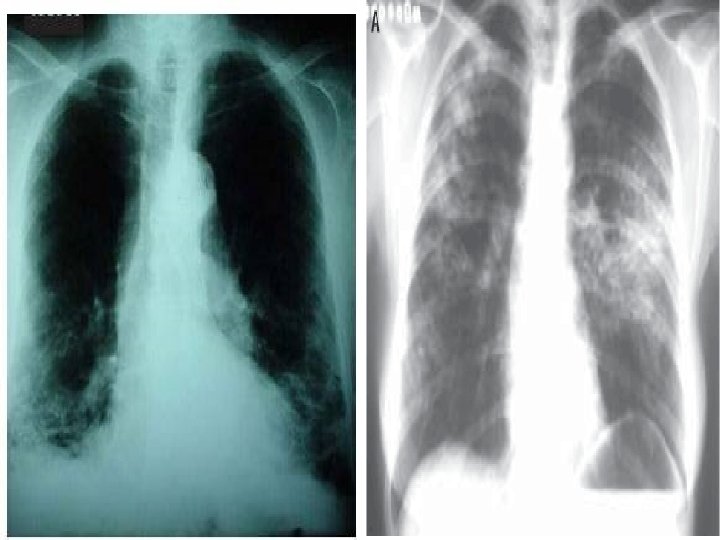
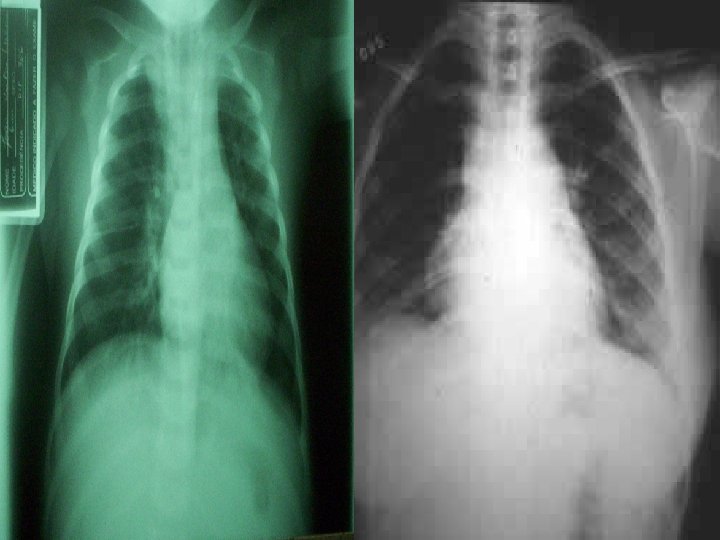
MANIFESTAÇÕES CLÍNICAS n n Achados da radiografia: infiltrados intersticiais ou doença alveolar difusa que progride rapidamente. Às vezes surgem lesões nodulares, infiltrados raiados ou lobares, derrames pleurais. Diagnóstico: Demonstração do P. carinii por coloração apropriada com prata de lavado broncoalveolar; raramente a biópsia é necessária.




MANIFESTAÇÕES CLÍNICAS n n O tratamento de primeira linha é trimetopim (TMP)/sulfametoxazol (SMZ) intravenosos (1520 mg/kg/24 h de TMP e 75 -100 mg/kg/24 h de SMZ dividido 6/6 h), com metilprednisolona adjuvante intravenosa (2 mg/kg/24 h divido a cada 6 ou 12 h por 5 -7 dias). Após melhora clínica, permanecer com TMP/SMZ por 21 dias via oral

MANIFESTAÇÕES CLÍNICAS n n n Associar Prednisona 1 -2 mg/kg/dia, VO 2 x/dia, por 5 dias, depois dar a metade da dose por mais 5 dias, ou Hidrocortisona 5 -10 mg/kg/dia, IV, 6/6 h, por 510 dias ou equivalente. Tratamentos alternativos: Dapsona, 1 mg/kg/dia, VO, 1 x/dia + Trimetoprim, 20 mg/kg/dia VO 4 x/dia por 21 dias Pentamidina, 4 mg/kg/dia, IV, 1 x/dia, por 21 dias. IMPORTANTÍSSIMO: BACTRIN + AZT SÃO MIELOTÓXICOS!!!!

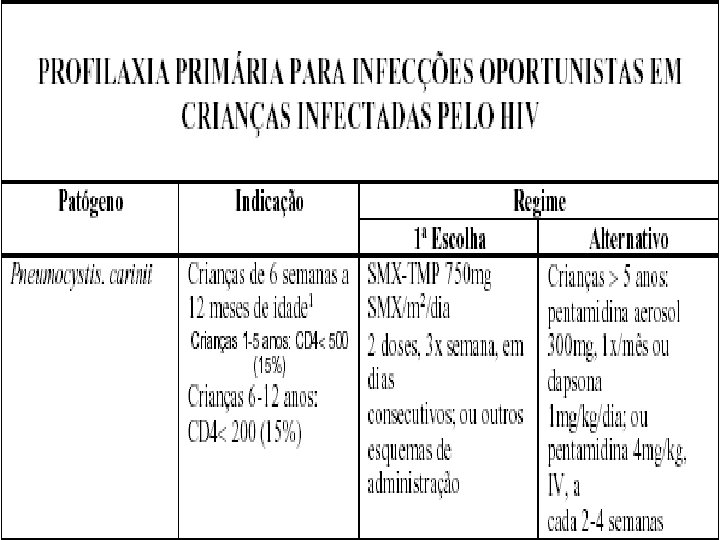
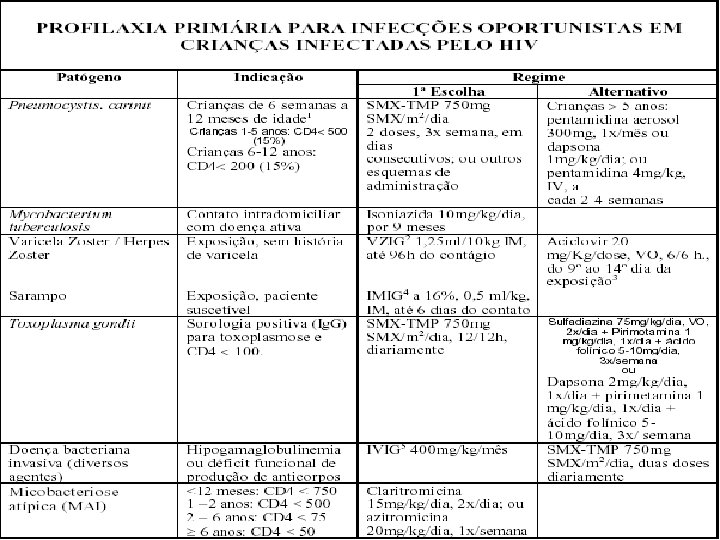
Profilaxia primária contra pneumonia por P. carinii n n Em crianças menores de 12 meses, os níveis de células T-CD 4+ não são marcadores do risco de pneumocistose. Todas as crianças expostas, a partir de 6 semanas de idade, devem receber profilaxia com Sulfametoxazol+Trimetoprim (SMX-TMP) até completar um ano (exceto se a infecção pelo HIV puder ser afastada).


MANIFESTAÇÕES CLÍNICAS n n PNEUMONIA VIRAL Vírus Sincicial respiratório (RSV), parainfluenza e adenovírus Manifestações: Rinite e tosse, febre em temperaturas mais baixas que nas PNM bacterianas, taquipnéia com tiragem e batimento de asas do nariz, cianose e fadiga respiratória. Ausculta: Estertores e sibilos difusos, indistinguível da doença por micoplasma.

MANIFESTAÇÕES CLÍNICAS n n n Diagnóstico: RX de tórax com infiltrados difusos, hiperinsuflação. Contagem de leucócitos normal ou levemente elevada (<20000), com linfócitos predominantes. Reagentes de fase aguda normais ou levemente aumentados. Diagnóstico definitivo: Isolamento do vírus em amostra do trato respiratório e sorologias.

MANIFESTAÇÕES CLÍNICAS n n Tratamento: medidas de apoio, amantadina oral (rimantadina) e rivabirina em aerosol PNEUMONIA BACTERIANA: Streptococcus pneumoniae ainda é a causa mais comum. Lactentes: Obstrução nasal, irritabilidade, anorexia, febre, dispnéia intensa, gemência, taquidispnéia, taquicardia, tiragem e batimento de asas do nariz.

MANIFESTAÇÕES CLÍNICAS n n Ausculta: murmúrio vesicular brônquico e estertores. Crianças e Adolescentes: Infecção respiratória alta leve e breve seguida por calafrios e febre alta, tosse, ansiedade, tiragem, batimento de asas do nariz, murmúrio vesicular brônquico e estertores, macicez em caso de derrame.

MANIFESTAÇÕES CLÍNICAS n n n Contagem de leucócitos elevada, com predomínio de polimorfonucleares. Gasometrias arteriais mostram hipoxemia, sem hipercapnia. Achados Radiográficos: consolidações, infiltrado e derrame em alguns casos. Tratamento: Penicilina G, se S. pneumoniae resistente, cefalosporinas de terceira geração. Caso haja resistência com estes últimas, vancomicina (CULTURA)

MANIFESTAÇÕES CLÍNICAS n n n PNEUMONIA ESTREPCOCÓCICA DO GRUPO A Resultam em faringite, traqueíte, bronquite, ou pneumonia intersticial. Necrose da mucosa traqueobrônquica com formação de úlceras anfractuosas e grandes quantidades de exsudato, edema e hemorragia localizada. Pode envolver linfáticos e o DERRAME é muito comum, volumoso, seroso e sangüinolento e purulento.

MANIFESTAÇÕES CLÍNICAS n n n Manifestações e laboratório similares ao das outras PNM bacterianas. RX: grandes derrames pleurais e pneumatoceles. Elevação da ASLO. Swab de orofaringe, secreções nasofaríngeas ou escarro. Tratamento: Penicilina G

MANIFESTAÇÕES CLÍNICAS n n PNEUMONIA ESTAFILOCÓCICA Causam broncopneumonia confluente, muitas vezes unilateral, ou mais proeminente em um dos lados (RX compatível). Numerosos abcessos, podendo ocorrer piopneumotórax.

MANIFESTAÇÕES CLÍNICAS n n n ATENÇÃO: história de furunculose, internação recente, abcesso do seio materno. Diagnóstico diferencial: cultura por aspiração traqueal ou punção pleural. Tratamento: Penicilina semi-sintética resistente à penicilase.

MANIFESTAÇÕES CLÍNICAS n n n PNEUMONIA POR HAEMOPHILUS INFLUENZAE Vacina Início insidioso e longa evolução. Tosse sem expectoração, tiragem e batimento de asas do nariz, febre, taquipnéia e macicez localizada à percussão, estertores e sopro tubário. RX – líquido pleural

MANIFESTAÇÕES CLÍNICAS n n Diagnóstico: Isolamento do microorganismo no sangue, líquido pleural ou aspirado pulmonar. Leucocitose moderada. Tratamento: medidas de suporte, ceftriaxona ou cefotaxima (RN).

MANIFESTAÇÕES CLÍNICAS n n n MYCOPLASMA PNEUMONIAE Início gradual de cafaléia, mal-estar, febre, rinorréia, dor de garganta, rouquidão, tosse; progressão da doença para dispnéia, febre e tosse intensificadas; não há uma maneira rápida de diagnosticar a doença. Estertores crepitantes; radiografias revelando achados inespecíficos, infiltrado unilaterais e centralmente densos, lobos inferiores.

MANIFESTAÇÕES CLÍNICAS n n Atenção quando a tosse for um achado proeminente! Contagens diferenciais de leucócitos são normais, VHS elevada. Cultura (pelo menos 1 semana). Título sérico de crioemaglutininas de 1: 64 ou maior, ou anticorpos Ig. M anti-M. pneumoniae sustentam o diagnóstico; não há teste diagnóstico rápido. Tratamento: eritromicina, claritromicina, azitromicina e tetraciclinas.

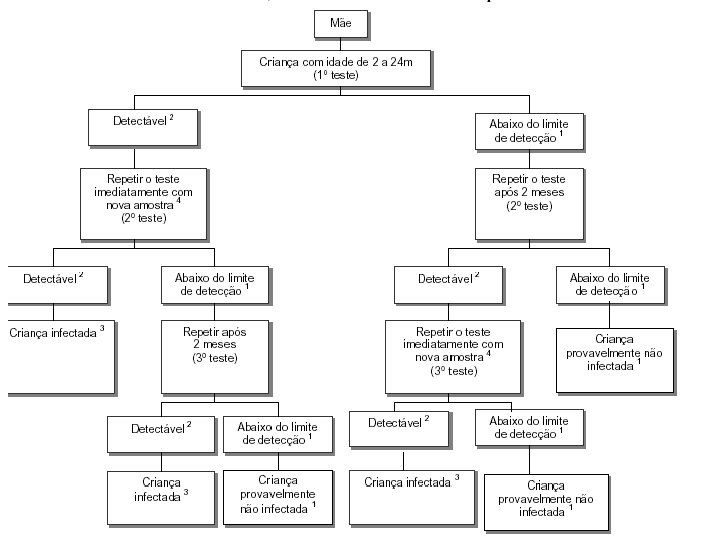
CONSENSO SOBRE TERAPIA ANTIRETROVIRAL PARA CRIANÇAS INFECTADAS PELO HIV n n n Considera-se infectada a criança que apresentar resultado positivo em duas amostras testadas pelos seguintes métodos: Cultivo de vírus Quantificação de RNA viral plasmático Detecção do DNA pró-viral ou Antigenemia p 24 após dissociação ácida de imunocomplexos. Esses testes deverão ser realizados após duas semanas de vida. A antigenemia p 24 com acidificação somente poderá ser utilizada como critério de diagnóstico quando associada a um dos demais métodos citados.


DIAGNÓSTICO n n Em crianças com idade ≥ 18 meses, o diagnóstico será confirmado por meio de 2 testes sorológicos de triagem com princípios metodológicos e/ou antígenos diferentes e um teste confirmatório positivo. Além disso, o fluxograma do Ministério da Saúde deverá ser seguido.

Criança provavelmente não infectada Duas amostras negativas, por meio dos seguintes métodos: n Cultivo do vírus e detecção de RNA OU DNA viral, entre 1 e 6 meses, sendo uma delas após o 4º mês de vida. n Idade ≥ 18 meses → uma amostra negativa em testes de detecção para anticorpos anti-HIV, utilizando fluxograma do Ministério da Saúde. n Observação: Os critérios aplicam-se às crianças que NÃO ESTEJAM E NÃO TENHAM SIDO amamentadas pela mãe HIV-positiva.

DIAGNÓSTICO n n n Manter o acompanhamento clínico nas crianças consideradas como provavelmente não infectadas e fazer sorologia anti-HIV entre 18 e 24 meses de idade. Caso a criança tenha sido amamentada, o algoritmo deve ser iniciado 2 meses após a suspensão do aleitamento materno Valores até 10. 000 cópias/ml sugerem resultados falso-positivos e devem ser cuidadosamente analisados dentro do contexto clínico (nova avaliação em um intervalo de 4 semanas).

MANUSEIO DE CRIANÇAS NASCIDAS DE MÃES SOROPOSITIVAS PARA O HIV n n Cuidados com o Recém-nascido Devido à possibilidade de ocorrência de anemia no recém-nascido em uso de AZT, recomenda-se a realização de hemograma completo da criança no início do tratamento e após 6 e 12 semanas; A criança deve ter alta da maternidade com consulta agendada em serviço especializado para seguimento de crianças expostas ao HIV; Em virtude da contra-indicação do aleitamento materno, a fórmula láctea (leite artificial) deverá ser fornecida de forma contínua, no mínimo por 12 meses.

MANUSEIO DE CRIANÇAS NASCIDAS DE MÃES SOROPOSITIVAS PARA O HIV n n O acompanhamento dessas crianças deve ser mensal ou bimensal nos primeiros 6 meses e trimestral a partir do 2º semestre de vida. A avaliação sistemática de seu crescimento e desenvolvimento é extremamente importante visto que as crianças infectadas podem, já nos primeiros meses de vida, apresentar dificuldade de ganho de peso.

Avaliação Clínico-Laboratorial de Possíveis Co-Infecções n n Recém-nascidos de mulheres infectadas pelo HIV devem receber AZT (zidovudina) solução oral, mesmo que suas mães não tenham recebido anti-retrovirais durante a gestação e/ou parto. Quimioprofilaxia imediatamente após o nascimento (nas duas primeiras horas de vida) ou nas primeiras oito horas de vida Durante as seis primeiras semanas de vida (42 dias), administrar zidovudina solução oral. Não existe estudo que comprove benefício do início da quimioprofilaxia após 48 horas do nascimento (fica a critério do médico).

Vacinação de Crianças Nascidas de Mães Soropositivas para o HIV n n Recomenda-se que, durante o seu acompanhamento, as crianças recebam todas as vacinas do calendário oficial. O tempo para a definição do diagnóstico da infecção é longo → não se justifica a postergação do início da vacinação das crianças assintomáticas e expostas ao HIV (risco de deixá-las sem proteção). Crianças pequenas, menores de 1 ano de idade com diagnóstico definitivo → modificações São crianças filhas de mãe e/ou pai infectados pelo HIV, são oriundas de ambientes de risco aumentado para infecções.

Classificação da Infecção pelo HIV n A classificação da infecção pelo HIV baseia -se em parâmetros clínicos e imunológicos, respectivamente, propostos pelo Centers for Disease Control and Prevention (CDC), n em 1994, conforme os quadros abaixo. Fundamental para nortear o tratamento



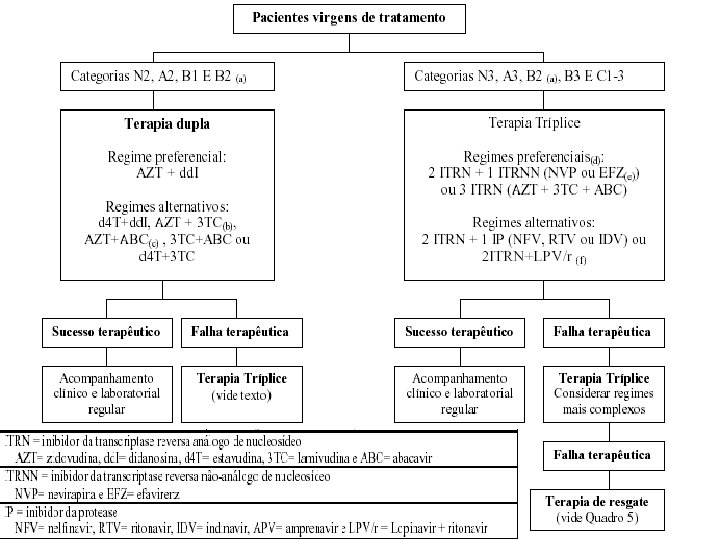
Quando Iniciar o Tratamento Anti-retroviral n n n Nas categorias N 1 e A 1, a recomendação é de acompanhamento clínico e laboratorial regulares, sem tratamento. Nas categorias N 2 e B 1, o tratamento e a introdução da terapia dependerão da evolução clínica e laboratorial (acompanhamento clínicolaboratorial em intervalos inferiores a 3 meses). Nas demais categorias, está indicado o início imediato da terapia.


Conceito de Sucesso Terapêutico n n Redução da carga viral superior a 1 log após 4 a 6 meses de tratamento, a elevação de 5 pontos percentuais na contagem de CD 4 para os pacientes na categoria imunológica 3 e a manutenção ou elevação em qualquer nível para os de categoria 1 ou 2. Retomada do crescimento pôndero-estatural, do desenvolvimento neuropsicomotor e o controle das complicações clínicas da infecção.

Mudança na Terapia Antiretroviral n n A mudança está indicada nas situações de intolerância (cuidado com efeitos colaterias leves), toxicidade e falha terapêutica. Falha Terapêutica (relacionada freqüentemente à dificuldade de adesão).

Falha Terapêutica n n Critérios clínicos (deterioração neurológica; falha no crescimento e/ou desenvolvimento; mudança de categoria clínica). Critérios imunológicos (mudança de categoria imunológica; criança na categoria imunológica 3 (CD 4 < 15%), decréscimo persistente igual ou maior que 5%; redução de >20% na contagem absoluta ou percentual de células. T-CD 4+, em pelo menos duas determinações seriadas).

Falha Terapêutica n n n Critérios virológicos alterações maiores de 5 vezes (0, 7 log) em crianças menores de 2 anos, e de pelo menos 3 vezes (0, 5 log) nas maiores de 2 anos de idade. a) crianças em uso de 2 ITRN + 1 IP, 2 ITRN + 1 ITRNN ou 3 ITRN: redução < 1, 0 log; b) crianças em uso de 2 ITRN: redução < 0, 7 log em relação ao nível inicial; c) aumento persistente da carga viral depois do início do tratamento: > 0, 7 log em crianças < 2 anos, e > 0, 5 log em crianças ≥ 2 anos.

Falha Terapêutica n n Após o início da terapia anti-retroviral, ocorre controle da replicação viral e elevação de linfócitos T CD 4+. Durante esse período infecções oportunistas latentes e sem expressão clínica, por causa da falta de reconhecimento do sistema imunológico, podem se tornar aparentes. Este quadro faz parte do processo de reconstituição imunológica imediata, de duração em média de 4 a 12 semanas e não deve ser considerado como falha terapêutica ou resistência viral.

Falha Terapêutica n n n Toxicidade Em casos de toxicidade ou intolerância, trocar a droga ou, se possível, reduzir a dose temporariamente, dentro da margem de eficácia terapêutica. No caso de falha terapêutica: Em esquema duplo: passar para esquema triplo, trocando pelo menos um ITRN. Em esquema triplo: trocar pelo menos duas drogas, sendo uma de cada classe. Em todas as mudanças de esquema terapêutico, levar em consideração a resistência cruzada.

Falha Terapêutica n n n n Associações Não Aceitáveis AZT + d 4 T 1 ITRN + IP em dupla terapia 1 ITRN + ITRNN em terapia dupla 1 ITRNN + IP em terapia dupla 3 ou mais ITRN, exceto AZT+3 TC+ABC 2 ou mais ITRNN 5 ou mais ARV








Intervenção Terapêutica Anti-Retroviral Precoce em Menores de 12 Meses n n n A indicação do início da terapia nessa população deve seguir os mesmos critérios para outras faixas etárias. Vantagens: O controle precoce da replicação viral em crianças. Preservar a função imune. Diminuir a disseminação viral e resultar em melhor curso clínico. Desvantagens: Efeitos adversos dos medicamentos. Dificuldades na adesão, emergência de resistência, comprometimento da qualidade de vida. Redução de opções de medicamentos para tratamentos subseqüentes.

Intervenção Terapêutica Anti-Retroviral Precoce em Menores de 12 Meses n n Adolescentes Infectados pelo HIV Curso clínico semelhante ao do adulto. A prescrição de medicação anti-retroviral deve ser baseada no estadiamento da puberdade de Tanner e não na idade cronológica. O adolescente nas fases inicias da puberdade (Tanner I e II) deve ser tratado segundo as recomendações pediátricas, enquanto aquele em fase adiantada (Tanner V) deve seguir as recomendações estabelecidas para os adultos

Consultem: n n AIDS PERINATAL Autor(es): Olga Messias Alves de Oliveira, Paulo R. Margotto

Obrigada!