CASO CLNICO HEPATITE MEDICAMENTOSA Escola Superior de Cincias






































- Slides: 47

CASO CLÍNICO HEPATITE MEDICAMENTOSA Escola Superior de Ciências da Saúde - ESCS Hospital Regional da Asa Sul/SES/DF Apresentação: Alessandra Gelande de Souza e José Noleto Sales Neto Coordenação: Dra. Luciana Sugai Brasília, 08 de Agosto de 2012. www. paulomargotto. com. br

Identificação: JLPS, 2 anos e 6 meses, 13 kg natural e residente de Ceilândia. Informante: Mãe (Boa Informante). Queixa Principal: “Olhos amarelos há 10 dias”.

Mãe refere que criança apresentou conjuntivas amarelo-esverdeadas há 10 dias, foi até a farmácia e medicaram-na com remédio parasitose intestinal (oxiúrius) sem melhora do quadro. Paciente evoluiu com piora do quadro ictérico, acolia fecal, colúria e diarréia pastosa sem muco e sangue. Nega náuseas e vômitos. Mãe foi até HRC onde foram realizados exames de urina e de sangue e dado alta no dia seguinte com orientações. Mãe nega febre durante toda história clínica, refere que criança sempre manteve bom estado geral. Como criança não apresentou melhora, persistindo com icterícia, mãe deu entrada nesse serviço ontem à noite.

Pré-Natal: Mãe refere ter realizado oito consultas de pré-natal. Nega intercorrências no período gestacional. Possui calendário vacinal completo. Parto: Nasceu de parto normal a termo (38 semanas), chorou ao nascer, peso ao nascer: 2970 g, cartão da criança não preenchido. Permaneceu internada 4 dias devido a icterícia neonatal, sem necessidade de fototerapia (sic). Aleitamento Materno exclusivo até 07 meses de vida. Nega internações anteriores, nega transfusões. TS materno: O+ TSRN: A+. Nega uso de dipirona, só faz uso de paracetamol. Não fazia seguimento ambulatorial, uma vez que não tinha pediatra nas proximidades de sua residência.

Mãe, 24, saudável /Pai, 29 anos, saudável. Mora em casa de alvenaria, 6 cômodos, saneamento básico completo, com 03 moradores (Pai, mãe e filha); Nega tabagismo e etilismo; Nega presença de animais domésticos na residência.

Ectoscopia: Paciente BEG, chorosa, hidratada, normocorada, ativa, ictérica 3+/4+, acianótica, afebril ao toque, eupneica, pouco colaborativa, orientada. AR: Murmúrio vesicular fisiológico presente em todas áreas pulmonares em ambos hemitóraces, sem presença de ruídos adventícios. ACV: BNF, 2 T, FC: 101 bpm, sem sopros. Abdome: Fígado palpável a 3 cm do rebordo costal D. Baço não palpável, sem outras visceromegalias. RHA presentes. Indolor à palpação abdominal. Genitália externa : sem sinais flogísticos, secreções ou lesões. Não foram visualizados parasitas em região anal. Extremidades: bem perfundidas, sem edemas, TEC <2 segundos. Neuro: ativa/reativa, sem sinais de irritação meníngea. Orofaringe: sem placas, petéquias, hiperemia ou sinais de sangramento.

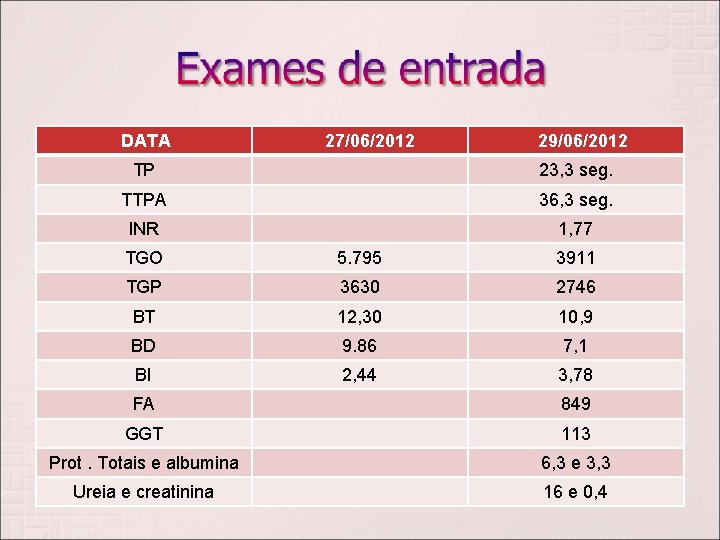
DATA 27/06/2012 29/06/2012 TP 23, 3 seg. TTPA 36, 3 seg. INR 1, 77 TGO 5. 795 3911 TGP 3630 2746 BT 12, 30 10, 9 BD 9. 86 7, 1 BI 2, 44 3, 78 FA 849 GGT 113 Prot. Totais e albumina 6, 3 e 3, 3 Ureia e creatinina 16 e 0, 4

Antígeno Austrália (HBSAG): negativo. Hepatite “B” (Anti HBS): 22, 1 mil/m. L. Hepatite “B” Antígeno “E” (HBe. Ag)/ Anti HBC Ig. G: Negativo. Anticorpos Anti HBE: Negativo. Hepatite “A” (anticorpos anti-HAV Ig. G): Negativo. Ig. M : Negativo. Hepatite “C” (anticorpos anti-HCV): Negativo.

Evolução Avaliação Vespertina (30/06): Evoluiu com melhora discreta da coloração da pele, da urina e fezes. Permanece afebril, sem náuseas, vômitos e dor abdominal. Aceitação parcial da dieta. Devido alteração no TAP e INR foi solicitado regulação para UTI com hipótese de insuficiência hepática. Transferida para UTIPED às 23: 40 h. Solicitadas novas sorologias para Hepatites virais. Iniciado vitamina K. Evolução UTIPED (01/07): Paciente segue clínica e hemodinamicamente estável, afebril, orientada, ictérica +++/4+, acianótica. Refere 01 episódio de vômito pós alimentar em pequena quantidade. Discutida com gastroenterologista que orientou uso de lactulose e ceftriaxona. Regulada USG abdominal.

Evolução UTIPED (02/07): Segue clínica e hemodinamicamente estável, ainda com fezes amolecidas 4 x/dia, discreta acolia e colúria. Sem sangramento, aceitando bem a dieta. Discutido a retirada do antibiótico e lactulose, porém não foi retirado. Encaminhada para UDIP. Admissão UDIP à tarde (02/07): Paciente segue com melhora dos sintomas, ictérica 2+/4+, refere melhora do aspecto das fezes e urina, nega náuseas e vômitos e dor abdominal. Aceitando bem a dieta. Na revisão de sistemas feita na admissão da UDIP a mãe: Refere mialgia em membros superiores três dias antes do inicio do quadro de icterícia; Refere apenas um episódio de vômito no dia anterior ao surgimento da icterícia, conteúdo de cor clara; Refere uso de analgésico há três dias antes do aparecimento da icterícia devido ao quadro de mialgia.

Evolução DIP(03/07): Paciente segue com melhora dos sintomas, mãe refere fezes e urina de aspecto próximo ao habitual. Nega febre, dor abdominal, náuseas e vômitos, alteração do nível de consciência e sangramentos. Suspenso ATB e lactulose após discussão com staff do setor. Realizado USG abdominal com laudo: Aspecto normal. Evolução UDIP (04/07): Alta hospitalar com retorno ambulatorial após resultado de sorologias (Colhidas dia 03/07).

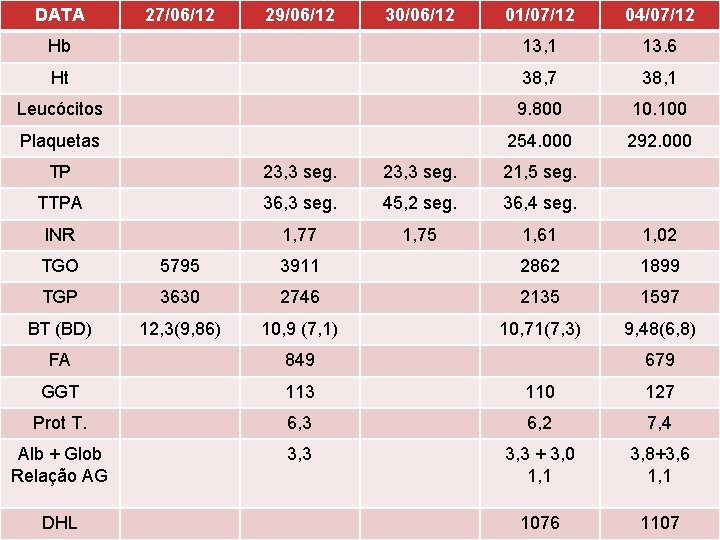
DATA 27/06/12 29/06/12 30/06/12 01/07/12 04/07/12 Hb 13, 1 13. 6 Ht 38, 7 38, 1 Leucócitos 9. 800 10. 100 Plaquetas 254. 000 292. 000 TP 23, 3 seg. 21, 5 seg. TTPA 36, 3 seg. 45, 2 seg. 36, 4 seg. INR 1, 77 1, 75 1, 61 1, 02 TGO 5795 3911 2862 1899 TGP 3630 2746 2135 1597 BT (BD) 12, 3(9, 86) 10, 9 (7, 1) 10, 71(7, 3) 9, 48(6, 8) FA 849 GGT 113 110 127 Prot T. 6, 3 6, 2 7, 4 Alb + Glob Relação AG 3, 3 + 3, 0 1, 1 3, 8+3, 6 1, 1 1076 1107 DHL 679

Antígeno Austrália (HBSAG): negativo. Hepatite “B” – Antígeno “E” (HBe. Ag)/ Anti HBC Ig. G: Não reagente. Anticorpos Anti HBE: Negativo. Hepatite “A” (anticorpos anti-HAV Ig. G): Negativo. Ig. M : Não reagente. Hepatite “C” (anticorpos anti-HCV): Não reagente.

Qual é o diagnóstico?


Lesão hepática causada por inalação, ingestão ou administração parenteral de agentes farmacológicos ou químicos. Toxic hepatitis: literature review, 2005.

OMS : Três milhões de casos notificados desde 1968. Nos EUA mais de 50% dos casos de falência aguda do fígado estão relacionas a drogas. No banco de transplante de órgãos nos EUA: 15% transplantados foram relacionados a drogas. Brasil: Relatos de casos e de casuísticas. Questionário realizado em 2010 em cinco centros de transplantes do país: Total de 1. 622 transplantes, 84 (5%) foram por hepatite fulminante e destes 25 (30%) foram por etiologia por drogas. 2010. Reunião com expertos em hepatologia da SBH, São Paulo,

RUCAM (Roussel Assessment Method): Uclaf Causality Acometimento biológico: ALT abaixo de 6 x o valor normal (VN) ou Fosfatase Alcalina (FA) abaixo de 1, 7 x o VN na ausência de sintomas. Padrão colestático: razão ALT e FA abaixo de 2. Padrão hepatocelular: razão ALT e FA superior a 5. Padrão misto: Razão ALT e FA entre 2 e 5.

Reações hepáticas adversas Importância: Suspensão do desenvolvimento de novas moléculas pela indústria farmacêutica. Não aprovação de novas drogas por parte das agências regulatórias. Retirada da droga no mercado ou de restrição do seu uso.

Idosos; Crianças: idiossincrática é rara. Mulheres; Álcool; Doença hepática prévia; Insuficiência renal; Obesidade; Exposições anteriores a outros fármacos; Infecção HIV/AIDS.

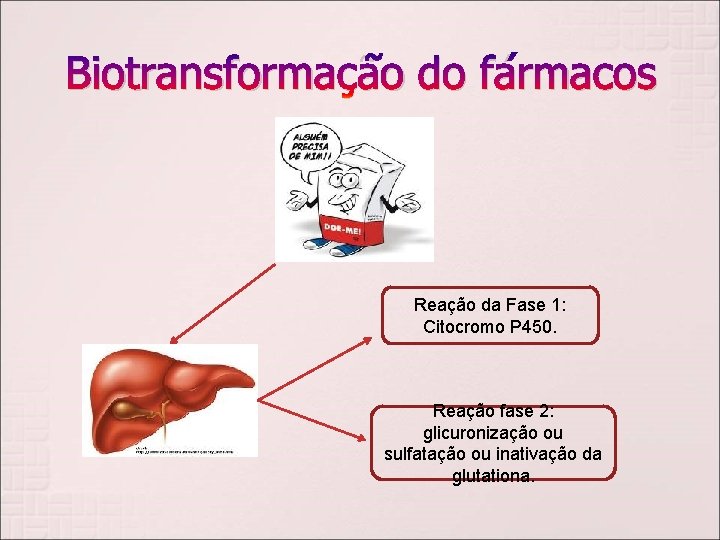
Biotransformação do fármacos Reação da Fase 1: Citocromo P 450. Reação fase 2: glicuronização ou sulfatação ou inativação da glutationa.

Hepatite medicamentosa: Lesão direta ou reação idiossincrática?

Depende : Período latência: Exposição ao agente agressor; Dose. Curto (horas). Pode não ser evidente até o aparecimento da icterícia.

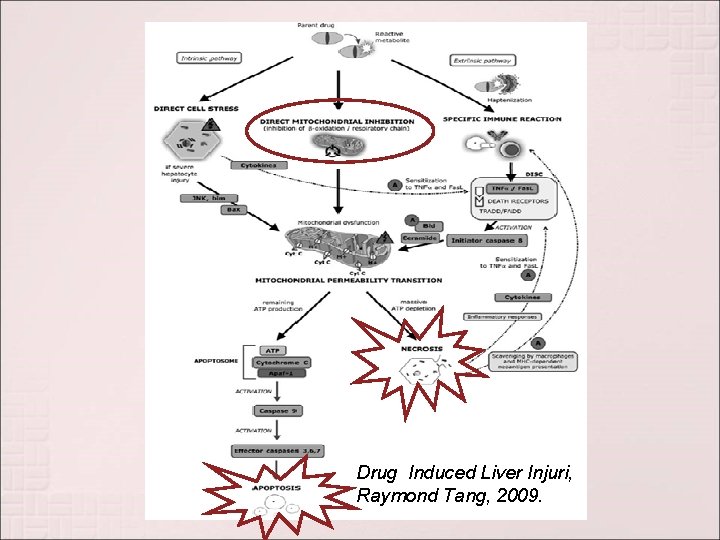
Há três etapas: I: Fadiga celular, com sofrimento da mitocôndria e reações imunológicas específicas. II: Aparece o MPT (Mitochondrial Permeability Transition). III: Apoptose/necrose a depender do acúmulo de radicais livres no hepatócito.

Drug Induced Liver Injuri, Raymond Tang, 2009.

Ocorrência de hepatite é rara e imprevisível. A resposta não é depende da dose. A lesão hepática pode ocorre em qualquer momento, durante ou logo após o fármaco. Elevações ligeiras, transitórias e não progressivas das aminotransferases. Hipersensibilidade ocorre em 25% dos casos.

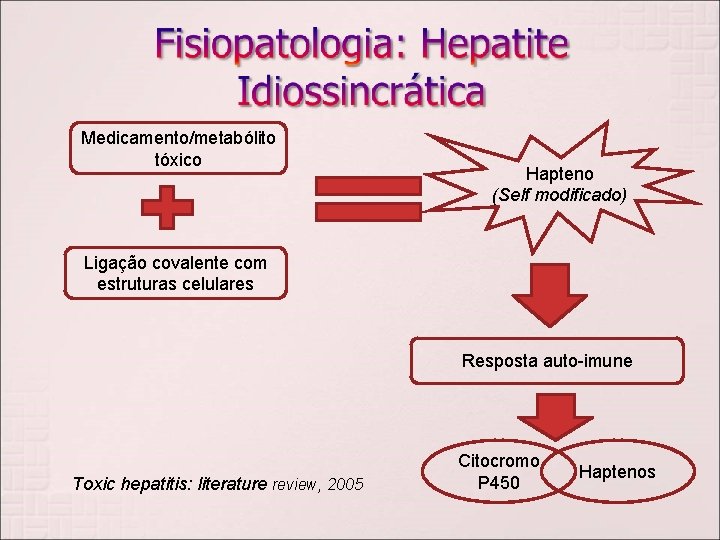
Medicamento/metabólito tóxico Hapteno (Self modificado) Ligação covalente com estruturas celulares Resposta auto-imune Toxic hepatitis: literature review, 2005 Citocromo P 450 Haptenos

Qual foi a droga

De acordo com a OMS, as principais drogas imputadas com lesão hepática sintomática são: Paracetamol 17% Antirretrovirais 17% Anticonvulsivantes 10% Quimioterápicos 12% Antibióticos 9% Agentes anestésicos 5% Tuberculostáticos 3% Diclofenaco 3% Reunião com expertos em hepatologia da SBH, São Paulo, 2010.


Metabólito ativo da fenacetina (efeito analgésico) e inibidor fraco da COX 1 e 2. Analgésico/antipirético. Ausência de atividades anti-inflamatórias. Indicação: dor leve a moderada. Administração: via oral. Dosagem: 10 -15 mg/Kg de 4/4 ou 6/6 horas. Absorção dependente do esvaziamento gástrico. Concentrações sanguíneas máximas: 30 -60 min. Meia- vida: 2 a 3 h. 2008. Katzung, Farmacologia básica e clínica, 10ºed,

Hepatotoxicidade: Dose-dependente. Overdose: >10 g em adultos e até 150 mg/kg em crianças. Os níveis sanguíneos de acetominofeno se correlacionam com a gravidade da lesão hepática. Reunião com expertos em hepatologia da SBH, São Paulo, 2010.

Idade: crianças menores de 5 anos são menos susceptíveis que adultos. Genética: polimorfismos de isoenzimas. Álcool. Jejum prolongado. Tabagismo. Hepatopatias. Reunião com expertos em hepatologia da SBH, São Paulo, 2010.

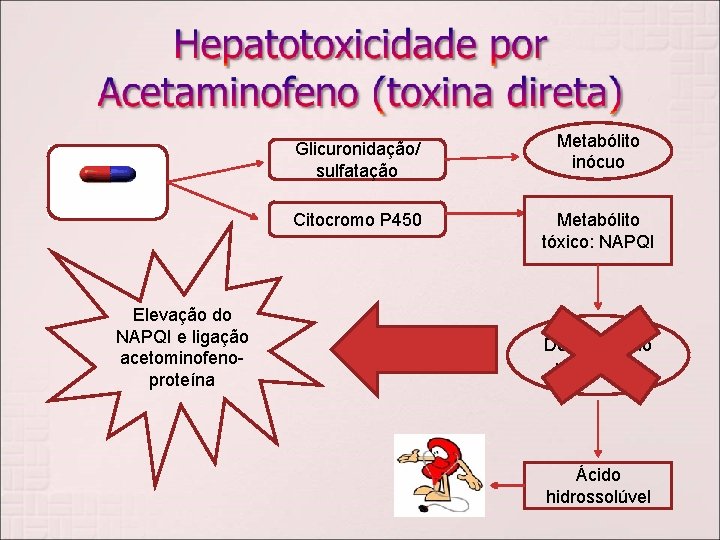
Elevação do NAPQI e ligação acetominofenoproteína Glicuronidação/ sulfatação Metabólito inócuo Citocromo P 450 Metabólito tóxico: NAPQI Destoxificado : glutationa Ácido hidrossolúvel

Apresenta períodos bem definidos após a ingestão do acetominofeno, podendo chegar a um quadro, resolutivo. Intoxicaciones medicamentosas (II). Analgésicos y anticonvulsivantes, vol 26, Suplemento 1, 2003.

Em geral, o paciente é assintomático, mas pode apresentar náuseas, vômitos, dor abdominal, mal-estar, palidez e sudorese. A concentração de aminotransferases (TGO é a mais sensível ) mantêm-se normal. TGO eleva-se em 8 -12 h em caso de overdose. Apenas parte dos pacientes passam para o próximo período. O restante progride bem, sem desenvolver toxicidade hepática.

Sintomatologia leve e similar a do primeiro período. Início de dor em hipocôndrio direito. Características: aumento da TGO, alcançando seu nível máximo em 3 -4 dias, podendo acompanhar-se de sintomatologia similar a da hepatite infecciosa. Outras alterações: bilirrubina, alargamento do TAP/INR.

Período de máxima expressão de hepatotoxicidade. QC: Varia desde pouco sintomático até encefalopatia, coma e / ou distúrbios da coagulação. A TGO-TGP sobem para níveis máximos. Insuficiência hepática: hipoglicemia, INR alterado, bilirrubina e acidose metabólica.

Insuficiência hepática aguda, que não termina em óbito, evolui com regeneração do tecido hepático.

Agudo: Lavado gástrico, administração de carvão vegetal ativado ou de colestiramina em até 30 min após a ingestão do acetominofeno. Primeira escolha: N-acetilcisteína. Outros compostos sulfidrila: cisteamina e cisteína.

N - Acetilcisteína Limita o risco de lesão hepática. Ação: proporciona um reservatório do grupo sufidrila que se unem aos metabólitos tóxicos/ estimulação da síntese de glutationa hepática. Iniciar: até 8 h após a ingestão da droga. Eficaz até 24 -36 h após uma overdose.

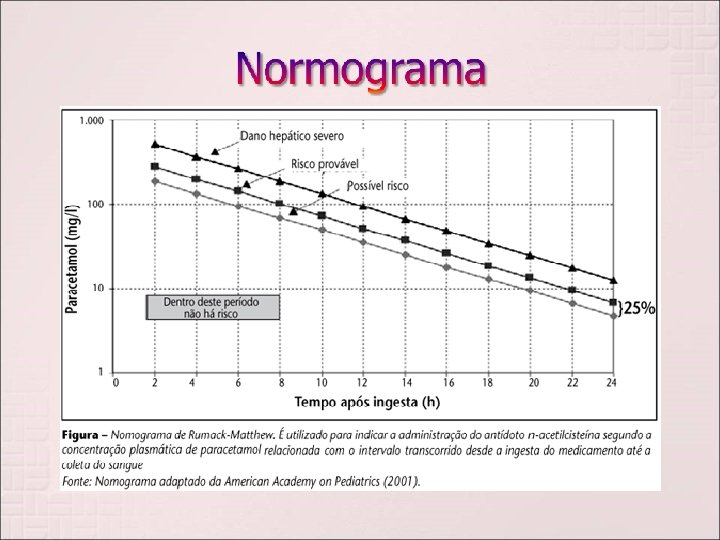
N - Acetilcisteína Avaliação do risco : Normograma de Rumack. Matthew. Risco provável: níveis plasmáticos > 200µg/ml 4 h após a ingestão e 25µg/ml 16 h após a ingestão da droga. Dose: 140 mg/kg em solução a 5% VO (única) seguida por 70 mg/kg VO a cada 4 h por 3 dias. Ou EV 150 mg/kg em 15 minutos e a seguir 300 mg/kg em infusão contínua durante 24 h. Pronto – Socorro, diagnóstico e tratamento em emergências, Herlon Saraiva, SP, 2ºed, 2008.


Indicação: sinais de insuficiência hepática, mesmo com a terapia de N-acetilcisteína. Níveis crescentes de lactato no sangue arterial.

Bibliografia 1 - MUNNÉ P. M; BAÑUELOS J. J. S; IZURA J. J. Intoxicaciones medicamentosas (II). Analgésicos y anticonvulsivantes. ANALES Sis San Navarra 2003; 26 (Supl. 1): 65 -97. 2 - PARANÁ, Raimundo; WASKMAN, J. C. Reunião com Expertos em Hepatotoxicidade da Sociedade Brasileira de Hepatologia. Revista GED Volume 30 - Suplemento nº 01 - Jan/Mar, 2011 p. 1014. 3 - MATOS, Luis Costa; MARTINS, Borges. Hepatite Toxica: Revisão de Literatura. Revista da sociedade portuguesa de medicina interna Vol. 12, nº 4, out/dez 2005. 4 - MEHTA, Nilesh ; MICHAEL, Pinsky. Drug-Induced Hepatotoxicity. Publicado em 26 de abril, 2010. Artigo disponível em: http: //emedicine. medscape. com/article/169814 -overview> Acessado em 01/07/2012. 5 - TANG, Raymond. UC San Diego School of Medicine. Artigo disponível em <http: //gastro. ucsd. edu/fellowship/documents/Drug. Induced. Liver. Injur y. pdf> acessado dia 01/07/2012.

Bibliografia 6 - LEBENSZTEJN , D. M. L. Drug-related hepatotoxicity in children. Revista Experimental & Clinical Hepatology 2009; 5(2): p. 32 -34. 7 - OLIVEIRA, Anabela; RODRIGUES, Sandra. Hepatite aguda medicamentosa tratada com corticosteroides. Revista da sociedade portuguesa de medicina interna Vol. 12, nº 1, Jan/Mar 2005. 8 - SEBBEN, Viviane C; LUGOCH, Rosemeri W. Validação de metodologia analítica e estudo de estabilidade para quantificação sérica de paracetamol. Jornal Brasileiro de Patologia Medica Lab. , v. 46 , n. 2, p. 143 -148, abril 2010. 9 -Saraiva, H. Martins et al. Pronto – Socorro, Diagnóstico e Tratamento em Emergências, 2ºed, SP, 2008. 10 -Emergências em pediatria, protocolos da santa casa, Peixoto F. La Torre et al. , 1ºed, SP, 2011. 11 -Katzung, Bertram G. Farmacologia básica e clínica, 10º ed, SP; Páginas 45— 56 e 531— 532; 2008.

Obrigado!