Cromosomopatie Vincenzo Nigro Laboratorio di genetica Dipartimento di

Cromosomopatie Vincenzo Nigro Laboratorio di genetica - Dipartimento di Patologia Generale, Seconda Università degli Studi di Napoli Telethon Institute of Genetics and Medicine, Napoli

Consulenza genetica La consulenza genetica è comunicazione informata ed appropriata Per essere informata deve partire dall’individuazione di un difetto genetico in un paziente e dal calcolo del rischio per gli altri componenti della famiglia Per poter essere appropriata deve saper stabilire un rapporto di fiducia e di confidenza senza essere direttiva, cioè non deve indirizzare la famiglia verso un unico obiettivo, ma lasciare libertà di valutazione e di scelta La consulenza genetica può riguardare: 1. la diagnosi di una malattia genetica clinicamente manifesta 2. il rischio riproduttivo di una coppia in epoca preconcezionale 3. la diagnosi prenatale 4. la predizione di una malattia genetica futura 5. la suscettibilità genetica

Consulenza genetica distinguiamo due grandi categorie di patologie genetiche: 1) monoalleliche, dovute alla mutazione di una sola copia del DNA 2) bialleliche, dovute a mutazioni di entrambe le copie del DNA 1. patologie a penetranza completa (in genere disordini mendeliani) 2. a penetranza incompleta, o addirittura “circoscritta”. La consulenza genetica cerca di stabilire quali membri della famiglia sono interessati ed eventualmente quali possono essere portatori, e quindi calcolare la probabilità di ogni altra persona nella famiglia (anche non ancora nata) di essere un portatore o di ereditare la malattia

rischio riproduttivo generale per una coppia per cui l’anamnesi personale e familiare abbiano escluso un incremento del rischio rispetto alla popolazione è • 3 -5% in caso di difetti congeniti rilevabili alla nascita (anomalie cromosomiche 0. 65%) • 8 -10% rilevabili entro i 10 anni di età
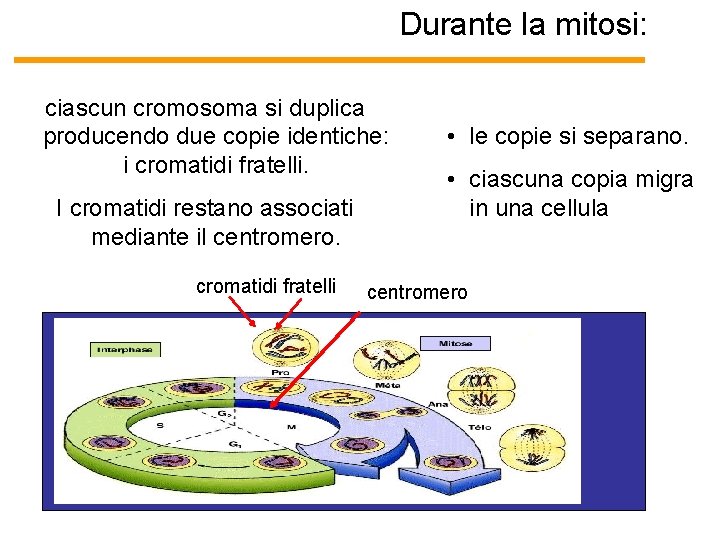
Durante la mitosi: ciascun cromosoma si duplica producendo due copie identiche: i cromatidi fratelli. I cromatidi restano associati mediante il centromero. cromatidi fratelli • le copie si separano. • ciascuna copia migra in una cellula centromero
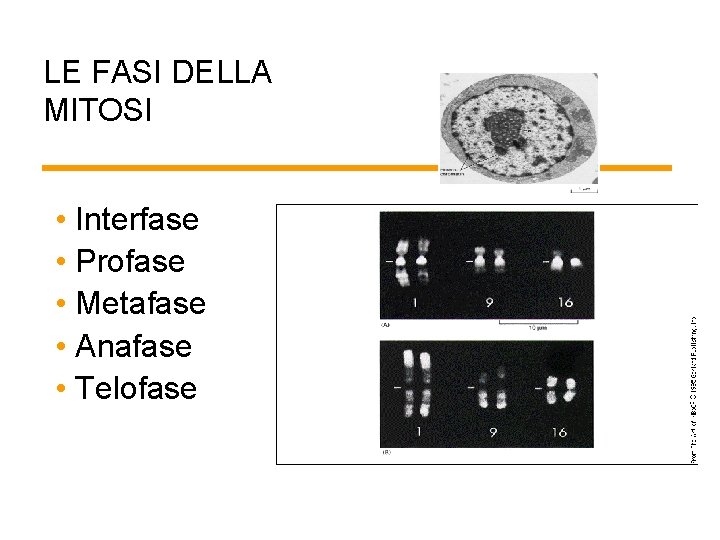
LE FASI DELLA MITOSI • Interfase • Profase • Metafase • Anafase • Telofase

meiosi • La meiosi è il processo che porta alla formazione dei gameti • I gameti sono cellule aploidi: hanno la metà dei cromosomi delle cellule diploidi • 23 è il numero di cromosomi dei gameti • 46 è il numero di cromosomi di ogni altra cellula umana • La meiosi consiste in due divisioni cellulari meiosi I (riduzionale) e meiosi II (equazionale) che producono quattro cellule aploidi

meiosi Meiosi I Replicazione del DNA 46 cromosomi 92 Cromatidi / 92 ds. DNA Divisione riduzionale separazione delle coppie di cromosomi 23 cromosomi 46 cromatidi / 46 ds. DNA Meiosi II Separazione dei cromatidi 23 cromosomi 23 cromatidi / 23 ds. DNA

Meiosi I 46 cromosomi 92 Cromatidi / 92 ds. DNA 1. 2. 3. 4. Profase I: ciascun cromosoma si duplica e le due parti restano strettamente associate. Questi sono chiamati cromatidi fratelli. Il crossing -over avviene in questa fase Metafase I: I cromosomi omologhi si allineano al piano equatoriale Anafase I: Le coppie omologhe si separano e i cromatidi fratelli restano uniti Telofase I: le due cellule figlie contengono solo un cromosoma di ciascuna coppia

meiosi I, profase I • Leptotene – i cromosomi si rendono visibili • Zygotene – le coppie di cromosomi omologhi formano le tetradi • Pachitene – crossing over • Diplotene – i cromosomi iniziano a separarsi ma sono tenuti insieme dai chiasmi • Diacinesi – ulteriore accorciamento dei cromosomi omologhi

Meiosi II 23 cromosomi 23 cromatidi / 23 ds. DNA 1. Profase II: il DNA delle due cellule figlie non si replica. 2. Metafase II: i cromosomi si allineano al piano equatoriale 3. Anafase II: I centromeri si dividono e i cromatidi fratelli migrano separatamente a ciascun polo 4. Telofase II: la seconda divisione cellulare è completa. Quattro cellule figlie aploidi (23) sono ottenute
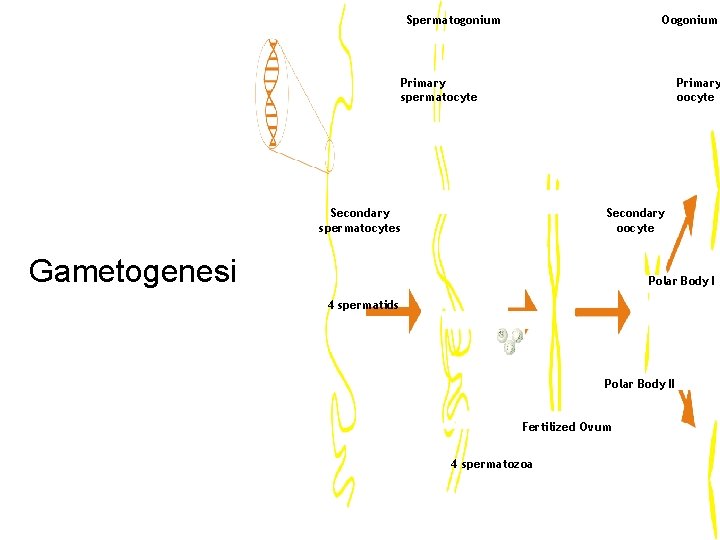
Spermatogonium Oogonium Primary spermatocyte Primary oocyte Secondary spermatocytes Secondary oocyte Gametogenesi Polar Body I 4 spermatids Polar Body II Fertilized Ovum 4 spermatozoa
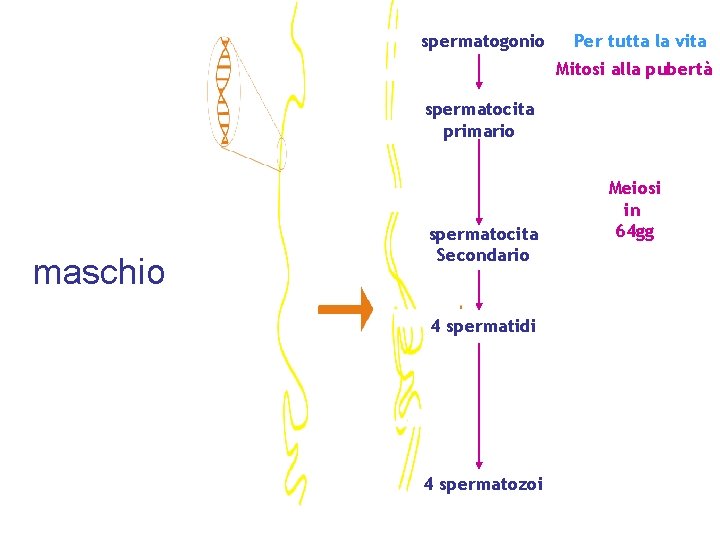
Oogonium spermatogonio Per tutta la vita Mitosi alla pubertà Primary oocyte spermatocita primario maschio spermatocita Secondario Meiosi in Secondary oocyte 64 gg Polar Body I 4 spermatidi Polar Body II Fertilized Ovum 4 spermatozoi
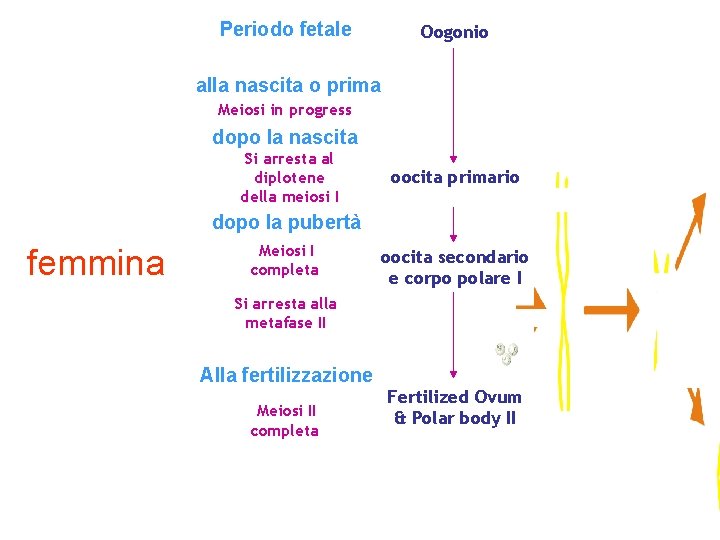
Periodo fetale Oogonio Mitosis alla nascita o prima Meiosi in progress dopo la nascita Si arresta al diplotene della meiosi I oocita primario dopo la pubertà femmina Meiosi I completa oocita secondario e corpo polare I Si arresta alla metafase II Alla fertilizzazione Meiosi II completa Fertilized Ovum & Polar body II

Cromosomi (corpi colorati) • durante il ciclo cellulare i cromosomi replicano e si formano due cromatidi fratelli tenuti insieme dal centromero • braccio corto = p (petit) • braccio lungo = q (lettera successiva)

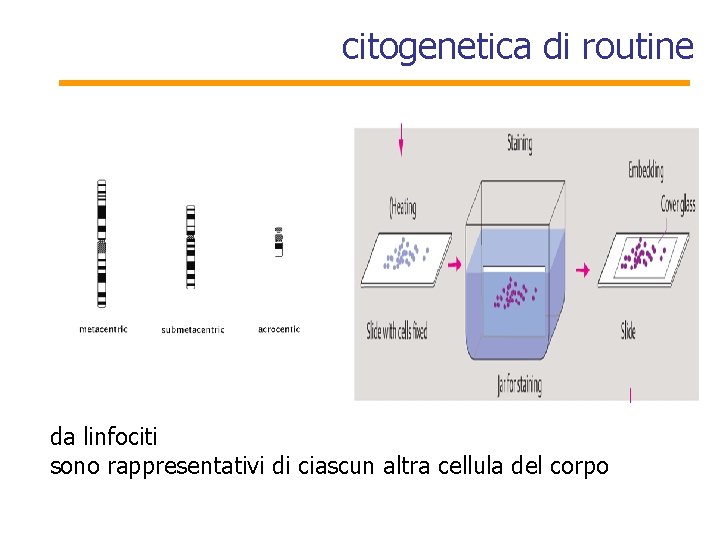
citogenetica di routine da linfociti sono rappresentativi di ciascun altra cellula del corpo
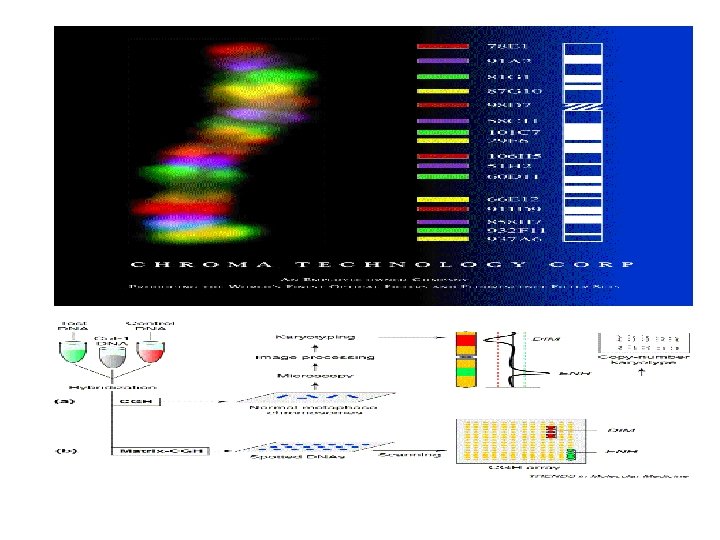

citogenetica prenatale • da amniociti • da villi coriali • dovrebbero essere rappresentativi delle cellule del feto • difficili da ottenere


Cromatina (DNA+proteine) • Eucromatina - meno condensata contiene il DNA codificante • Eterocromatina - più condensata non contiene DNA codificante, ma solo DNA non codificante • Telomeri - cappucci all’estremità dei cromosomi che comprendono ripetizioni multiple della sequenza TTAGGG • Centromeri - regioni specializzate di DNA che forniscono il sito di ancoraggio del fuso mitotico

Eucromatina ed eterocromatina
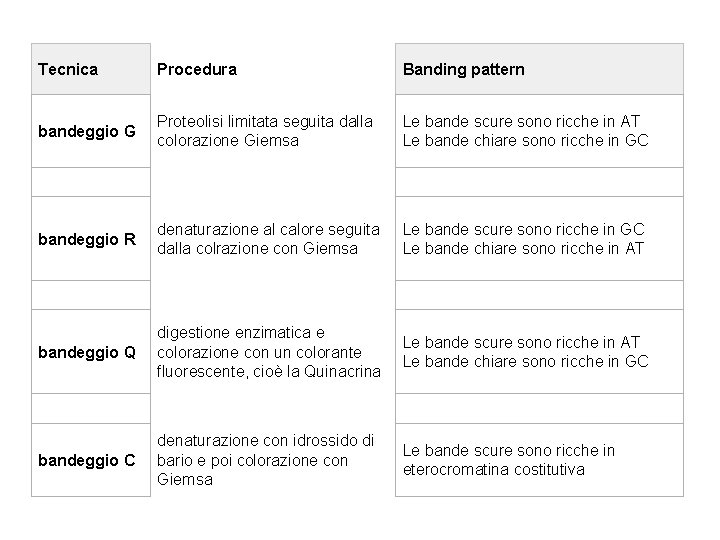
Tecnica Procedura Banding pattern bandeggio G Proteolisi limitata seguita dalla colorazione Giemsa Le bande scure sono ricche in AT Le bande chiare sono ricche in GC bandeggio R denaturazione al calore seguita dalla colrazione con Giemsa Le bande scure sono ricche in GC Le bande chiare sono ricche in AT bandeggio Q digestione enzimatica e colorazione con un colorante fluorescente, cioè la Quinacrina Le bande scure sono ricche in AT Le bande chiare sono ricche in GC bandeggio C denaturazione con idrossido di bario e poi colorazione con Giemsa Le bande scure sono ricche in eterocromatina costitutiva
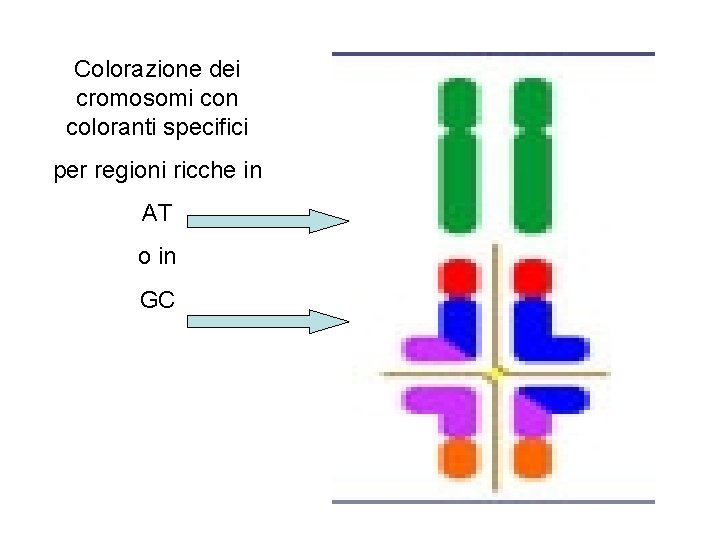
Colorazione dei cromosomi con coloranti specifici per regioni ricche in AT o in GC


• metacentrici, se il centromero è centrale 1, 2, 3, 16, 17, 18, 19 • submetacentrici, se il centromero non è centrale e non è vicino ad un’estremità 4, 5, 6, 7, 8, 9, 10, 11, 12, 20, X, Y • acrocentrici, se il centromero è vicino ad un’estremità 13, 14, 15, 21, 22

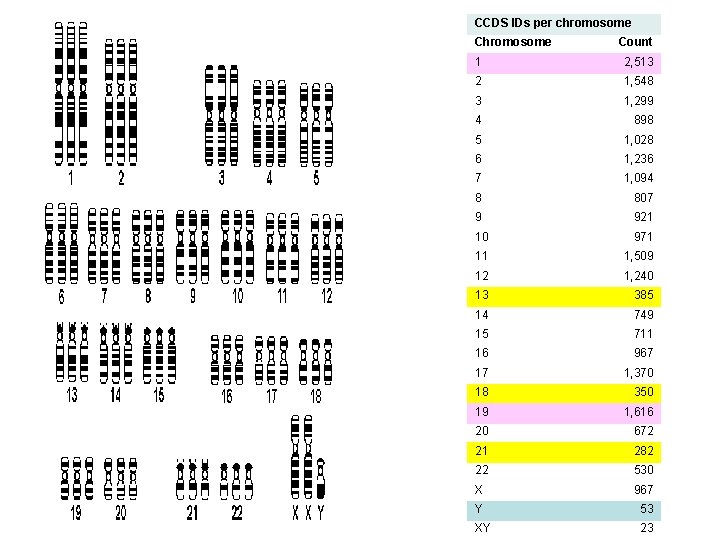
CCDS IDs per chromosome Count 1 2, 513 2 1, 548 3 1, 299 4 898 5 1, 028 6 1, 236 7 1, 094 8 807 9 921 10 971 11 1, 509 12 1, 240 13 385 14 749 15 711 16 967 17 1, 370 18 350 19 1, 616 20 672 21 282 22 530 X 967 Y 53 XY 23
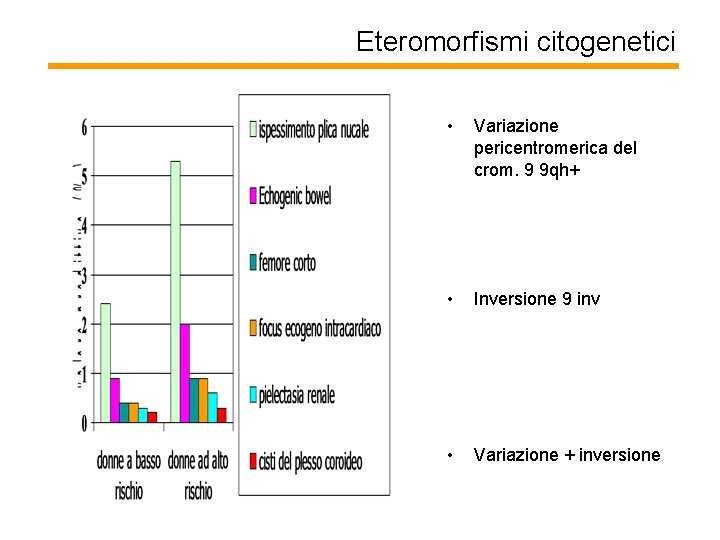
Eteromorfismi citogenetici • Variazione pericentromerica del crom. 9 9 qh+ • Inversione 9 inv • Variazione + inversione

Ereditarietà della variazione pericentromerica del cromosoma 1

Le alterazioni cromosomiche sono più frequenti al crescere dell’età materna, mentre le mutazioni puntiformi sono legate al numero di divisioni cellulari che avvengono circa ogni 15 gg nella linea germinale maschile

tritest interpretazione dei risultati anomalia fetale NTD =difetti del tubo neurale* AFP Beta h. CG Alfa-feto proteina Normale Trisomia 21 Trisomia 18 * NTD: anencefalia, spina bifida and encefalocele u. E estriolo non coniugato Normale
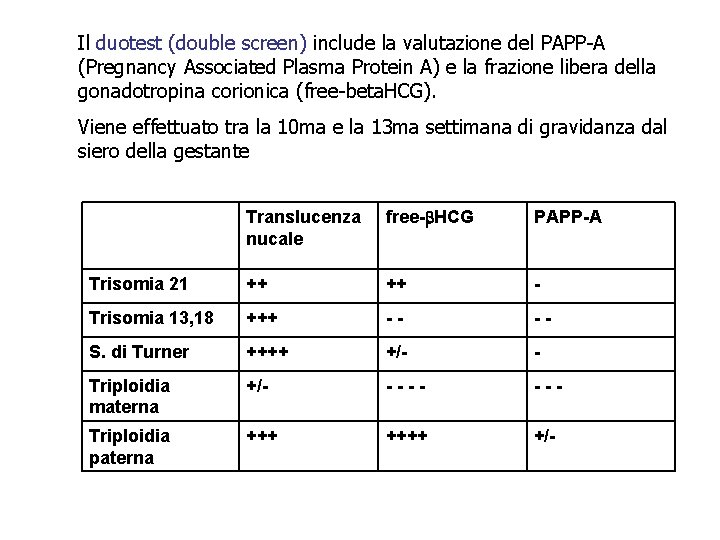
Il duotest (double screen) include la valutazione del PAPP-A (Pregnancy Associated Plasma Protein A) e la frazione libera della gonadotropina corionica (free-beta. HCG). Viene effettuato tra la 10 ma e la 13 ma settimana di gravidanza dal siero della gestante Translucenza nucale free-b. HCG PAPP-A Trisomia 21 ++ ++ - Trisomia 13, 18 +++ -- -- S. di Turner ++++ +/- - Triploidia materna +/- --- Triploidia paterna ++++ +/-

Patologia fetale NTD - AFP solo Trisomia 21 - Tritest Trisomia 18 - Tritest Sensibilità 75 -80% spina bifida 95% anencefalia 70% Down sindrome 80% sindrome di Edward
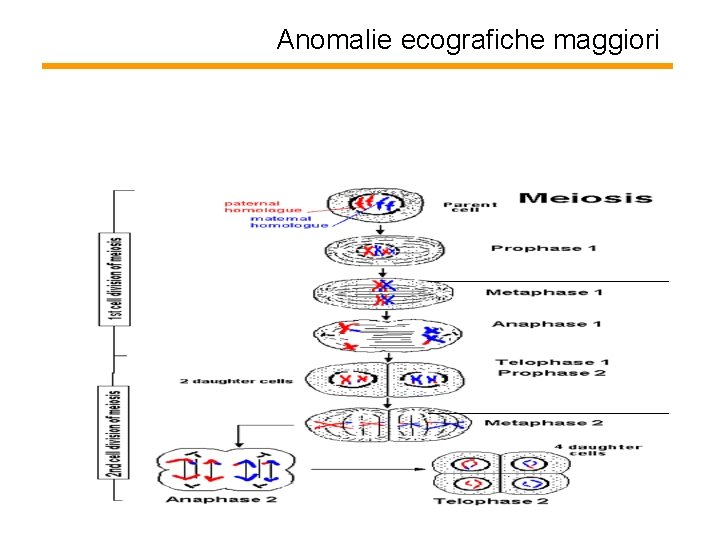
Anomalie ecografiche maggiori
ecografia • “segni minori”

Frequenza di anomalie cromosomiche negli aborti spontanei (39. 8%-40. 9%) • • • trisomie autosomiche 49 -52% Turner (45, X) 15 -19% triploidia (69) 15 -16% tetraploidia (92) 5 -6% altre anomalie 6 -14%
trisomia 21 Down Il 70% delle gravidanze non giunge a termine

1 1 2 2 1 1 2 2 Meiosis 1 error Meiosis 1 1 1 2 + 2 1 Meiosis 2 1 1 SEA 3069 or 1 2 2 1 1 2 1 2 Meiosis 2 error Meiosis 2 1 1 + 2 1 Meiosis 1 or 3 other combinations 1 1 + 1 2 Meiosis 2 1 or other combinations Mitotic error 2 1 1 2 2

origine dell’extra cromosoma 21 MM 2 19. 8% MM 1 68% PM 1 2. 6% PM 2 4. 1% MIT 5. 5% Data from the Antonarakis and Hassold laboratories sea 3109
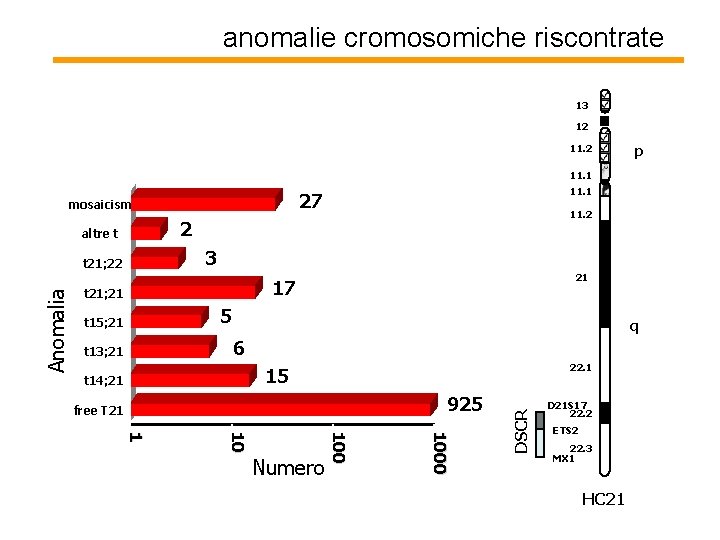
anomalie cromosomiche riscontrate 13 12 11. 2 p 11. 1 mosaicism 11. 2 2 altre t 3 t 21; 22 21 17 t 21; 21 5 t 15; 21 q 6 t 13; 21 22. 1 15 t 14; 21 925 free T 21 1000 10 1 Numero DSCR Anomalia 11. 1 27 D 21 S 17 22. 2 ETS 2 22. 3 MX 1 HC 21
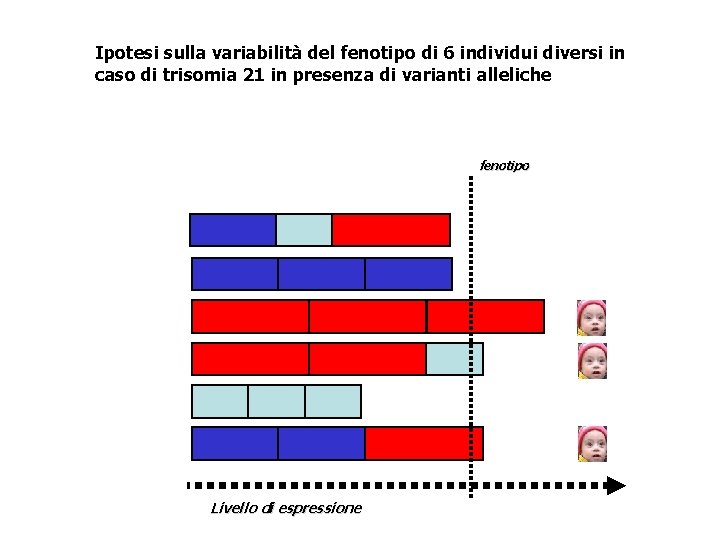
Ipotesi sulla variabilità del fenotipo di 6 individui diversi in caso di trisomia 21 in presenza di varianti alleliche fenotipo Livello di espressione
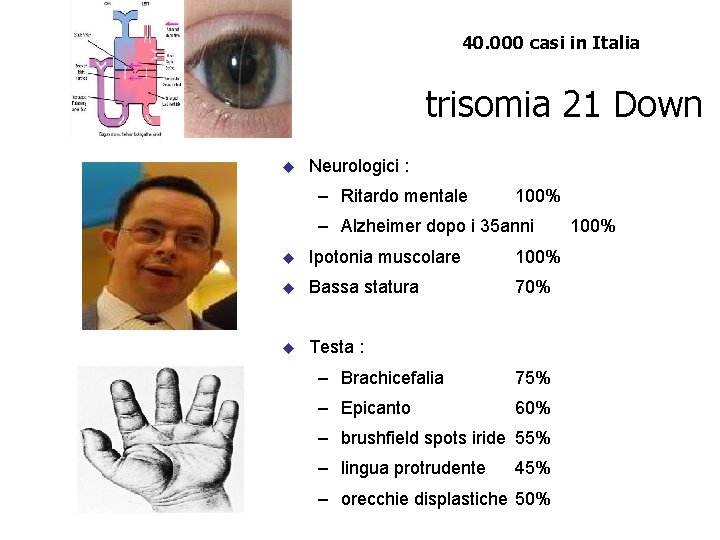
40. 000 casi in Italia trisomia 21 Down u Neurologici : – Ritardo mentale 100% – Alzheimer dopo i 35 anni u Ipotonia muscolare 100% u Bassa statura 70% u Testa : – Brachicefalia 75% – Epicanto 60% – brushfield spots iride 55% – lingua protrudente 45% – orecchie displastiche 50% 100%
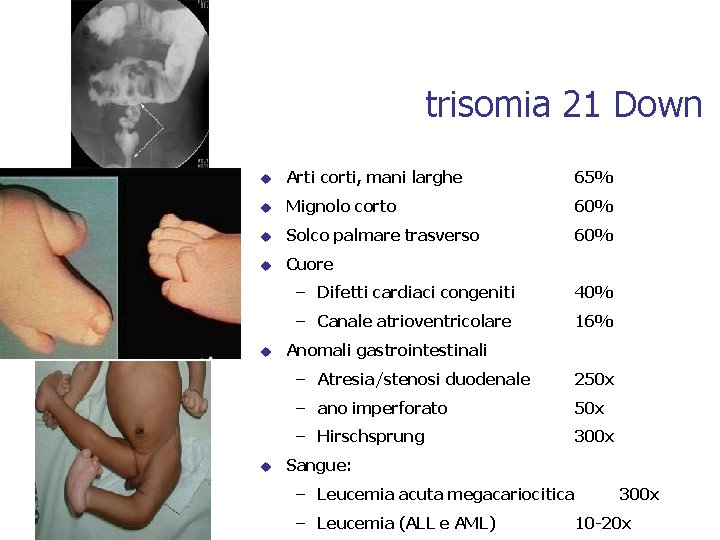
trisomia 21 Down u Arti corti, mani larghe 65% u Mignolo corto 60% u Solco palmare trasverso 60% u Cuore u u – Difetti cardiaci congeniti 40% – Canale atrioventricolare 16% Anomali gastrointestinali – Atresia/stenosi duodenale 250 x – ano imperforato 50 x – Hirschsprung 300 x Sangue: – Leucemia acuta megacariocitica – Leucemia (ALL e AML) 300 x 10 -20 x
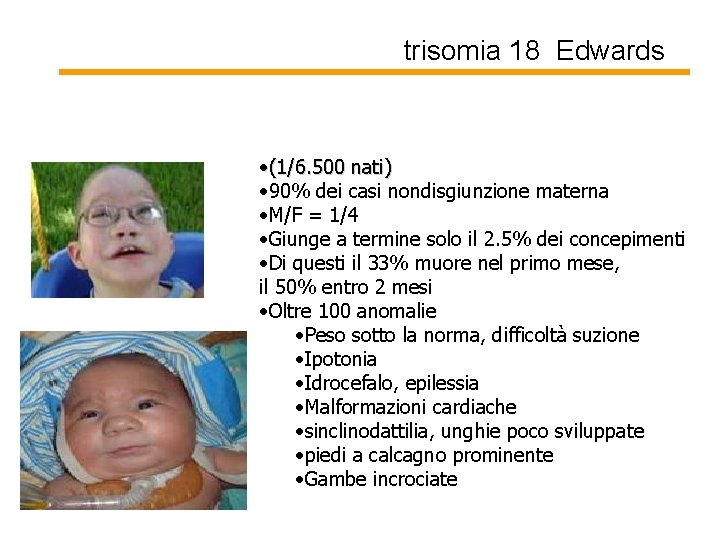
trisomia 18 Edwards • (1/6. 500 nati) • 90% dei casi nondisgiunzione materna • M/F = 1/4 • Giunge a termine solo il 2. 5% dei concepimenti • Di questi il 33% muore nel primo mese, il 50% entro 2 mesi • Oltre 100 anomalie • Peso sotto la norma, difficoltà suzione • Ipotonia • Idrocefalo, epilessia • Malformazioni cardiache • sinclinodattilia, unghie poco sviluppate • piedi a calcagno prominente • Gambe incrociate
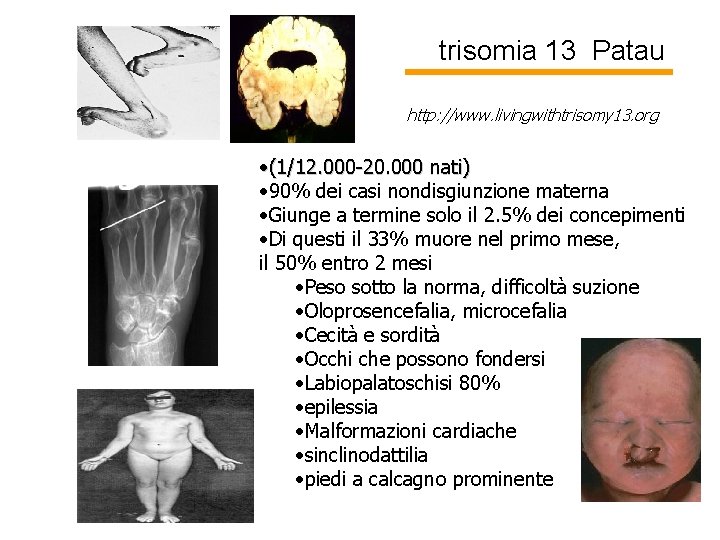
trisomia 13 Patau http: //www. livingwithtrisomy 13. org • (1/12. 000 -20. 000 nati) • 90% dei casi nondisgiunzione materna • Giunge a termine solo il 2. 5% dei concepimenti • Di questi il 33% muore nel primo mese, il 50% entro 2 mesi • Peso sotto la norma, difficoltà suzione • Oloprosencefalia, microcefalia • Cecità e sordità • Occhi che possono fondersi • Labiopalatoschisi 80% • epilessia • Malformazioni cardiache • sinclinodattilia • piedi a calcagno prominente

XX o XY • Il sesso maschile è determinato dalla presenza del cromosoma Y • Si sono evoluti meccanismi per compensare la differenza di dosaggio genico del cromosoma X, presente in 2 copie nelle femmine e in 1 copia nei maschi

2 cromosomi X nelle donne, 1 solo negli uomini? 1. 2. il cromosoma X raddoppia l’espressione di tutti i geni contenuti, cioè si produce 2 volte più RNA nelle femmine uno dei due cromosomi X è inattivato casualmente in ciascuna cellula allo stadio di blastocisti
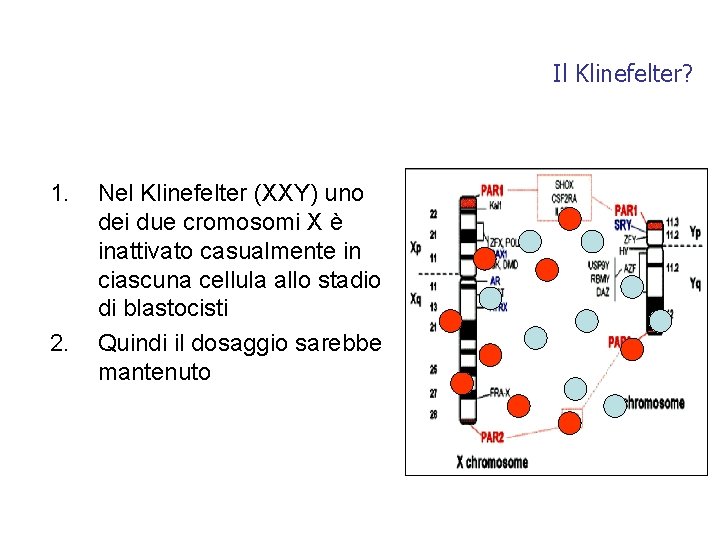
Il Klinefelter? 1. 2. Nel Klinefelter (XXY) uno dei due cromosomi X è inattivato casualmente in ciascuna cellula allo stadio di blastocisti Quindi il dosaggio sarebbe mantenuto

Sindrome di Klinefelter (47, XXY) 1: 900 -1: 600 maschi • Il 50% delle gravidanze giunge a termine • Fenotipo maschile • Caratteristiche principali: • Statura alta – Ipogonadismo, bassi livelli di testosterone, mancata produzione di spermatozoi (azoospermia) e quindi sterilità – Ginecomastia – Sia l’intelligenza sia l’attesa di vita sono quasi normali

Altre forme citogenetiche • Ma ci sono anche Klinefeler 48, XXYY and 48, XXXY in 1 caso su 17, 000 e 1 su 50, 000 mnati maschi • 49, XXXXY in 1 caso su 85, 000 -100, 000 • Ci sono maschi 46, XX in cui avviene una traslocazione di parte di cromosoma Y sul cromosoma X che include la sex determining region (SRY) • mosaici
Le regioni PAR presenti sui cromosomi sessuali contengono geni che non sono inattivati, perché il doppio dosaggio è assicurato comunque PAR 1 ha 24 geni, PAR 2 ha solo 4 geni

Il gene SHOX Short stature HOmeobo. X-containing • Mutazioni o delezioni del gene SHOX nella regione PAR 1 causa ritardo di crescita e bassa statura. • La bassa statura di donne con sindrome di Turner Syndrome (X 0) è il risultato di una sola copia di SHOX (ma anche il quarto metacarpo corto) • La maggiore statura nel Klinefelter (XXY) e nella tripla X (XXX) potrebbe essere il risultato di 3 copie di SHOX
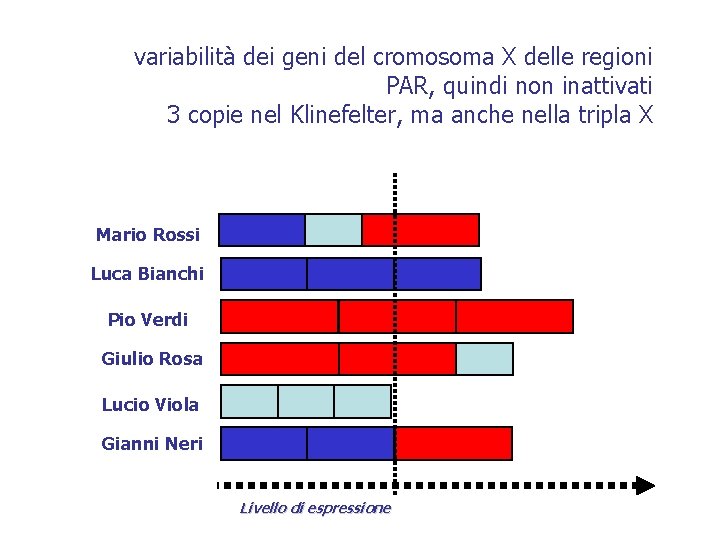
variabilità dei geni del cromosoma X delle regioni PAR, quindi non inattivati 3 copie nel Klinefelter, ma anche nella tripla X Mario Rossi Luca Bianchi Pio Verdi Giulio Rosa Lucio Viola Gianni Neri Livello di espressione

A complicare le cose… • circa il 15 % dei geni umani presenti sull’X sfugge all’inattivazione, mentre nel topo questa è un’evenienza rara (solo 6 geni in tutto) • alcuni sono espressi al 50 -100% altri al 10% • questo fenomeno è quindi incompleto e le donne hanno una elevata eterogeneità nell’espressione di geni dell’X
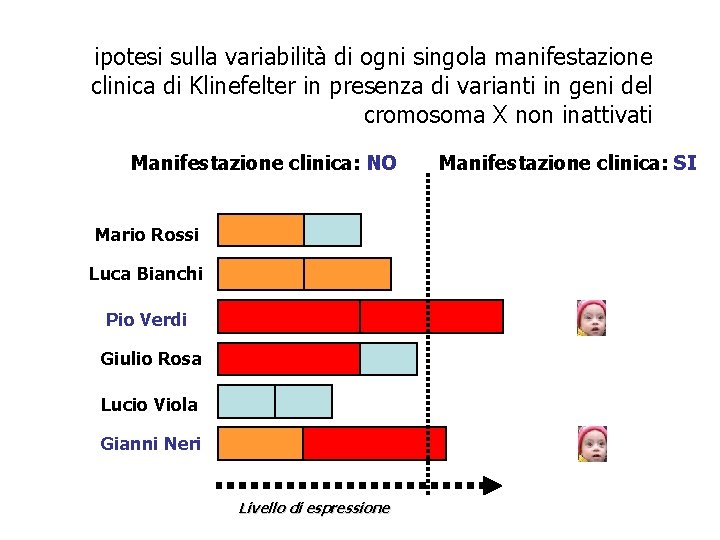
ipotesi sulla variabilità di ogni singola manifestazione clinica di Klinefelter in presenza di varianti in geni del cromosoma X non inattivati Manifestazione clinica: NO Mario Rossi Luca Bianchi Pio Verdi Giulio Rosa Lucio Viola Gianni Neri Livello di espressione Manifestazione clinica: SI

Quanti Klinefelter? • Prevalenza di XXYs è cresciuta da 1. 09 a 1. 72 per 1000 maschi nati (P=0. 023) • Questo incremento non è dovuto all’aumento dell’età materna • Sono nati 290. 330 maschi in Italia e 31. 573 maschi in Campania nel 2007 • max 300 -500 nuovi Klinefelter ogni anno in Italia (32 -52 in Campania) • XXY è la sola trisomia nota in cui circa il 50% dei casi è causato da una non disgiunzione alla prima divisione meiotica paterna

Trisomia X (47, XXX) 1: 1. 200 • Il 70% delle gravidanze giunge a termine • Errore nella disgiunzione materna e correla con l’età materna • Caratteristiche principali: – Statura alta – Fertilità normale, irregolarità ciclo – Sia l’intelligenza sia l’attesa di vita sono normali

Maschio (47, XYY) 1: 1. 000 maschi • Fenotipo maschile • Caratteristiche principali: – Statura alta – Fertilità normale – Non vi è correlazione con l’età paterna – Sia l’intelligenza sia l’attesa di vita sono perfettamente normali

Monosomia X (45, X 0) Turner Prende il nome dall’endocrinologo Henry Turner che la descrisse nel 1938 La sindrome di Turner (TS) definisce un complesso fenotipo umano femminile, dovuto a completa o parziale assenza del secondo cromosoma sessuale Dipende da un errore nella spermatogenesi nell’ 80% dei casi e non correla con l’età dei genitori Un precedente figlio con TS non aumenta il rischio riproduttivo previsto per una coppia di pari età

Monosomia X (45, X 0) Turner È l’unica monosomia compatibile con la vita, ma il 98% di tutti i feti monosomici TS va incontro ad aborto spontaneo L’incidenza negli aborti è circa il 7 -10%, mentre alla nascita è 1/2500 femmine. Non è chiaro perché il cariotipo 45, X 0 sia letale in utero ed invece compatibile con la sopravvivenza postnatale La vera monosomia del cromosoma X è responsabile del 45% dei casi TS; gli altri hanno mosaicismo (45, X 0/46, XX) e/o un anormale cromosoma X o Y Un basso livello di mosaicismo somatico Turner, inferiore al 2%, è di normale riscontro nella popolazione

Monosomia X (45, X 0) Turner “la menopausa precede il menarca” Le ovaie sono allungate e formate da tessuto stromale privo di follicoli: gli oociti sono spesso andati in apoptosi prima dei 2 anni di vita L’insufficienza ovarica prepuberale porta ad amenorrea primaria, sterilità e carenza di estrogeni In meno del 10% dei casi, la pubertà può verificarsi e sono possibili gravidanze con un aumentato rischio di perdita fetale Anche in rapporto all’eterogeneità del genotipo, il fenotipo si manifesta in modo molto variabile
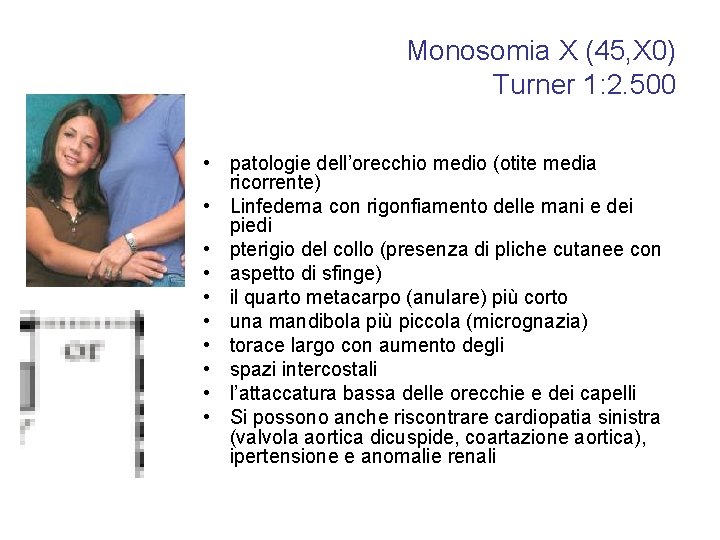
Monosomia X (45, X 0) Turner 1: 2. 500 • patologie dell’orecchio medio (otite media ricorrente) • Linfedema con rigonfiamento delle mani e dei piedi • pterigio del collo (presenza di pliche cutanee con • aspetto di sfinge) • il quarto metacarpo (anulare) più corto • una mandibola più piccola (micrognazia) • torace largo con aumento degli • spazi intercostali • l’attaccatura bassa delle orecchie e dei capelli • Si possono anche riscontrare cardiopatia sinistra (valvola aortica dicuspide, coartazione aortica), ipertensione e anomalie renali

feto con anomalia cromosomica (mosaicismo) • • trisomie a mosaico 8, 9, 13, 18, 21 crescita in coltura di cellule materne mosaicismo vero (livello III) pseudomosaicismo (livelli II e I)
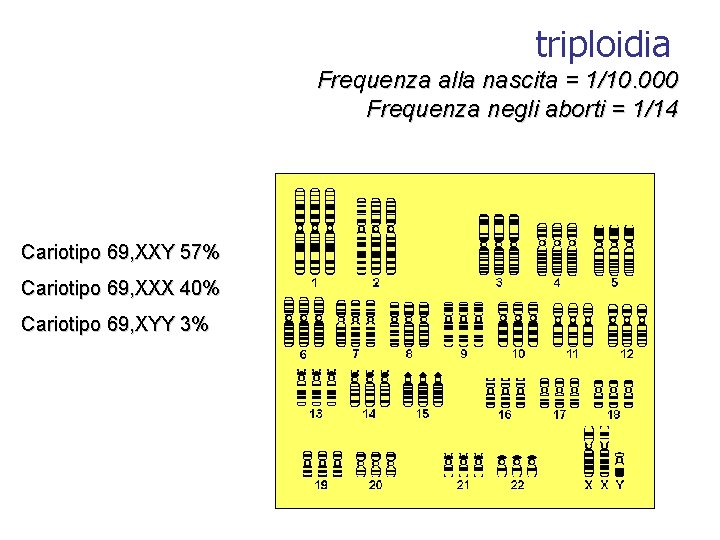
triploidia Frequenza alla nascita = 1/10. 000 Frequenza negli aborti = 1/14 Cariotipo 69, XXY 57% Cariotipo 69, XXX 40% Cariotipo 69, XYY 3%
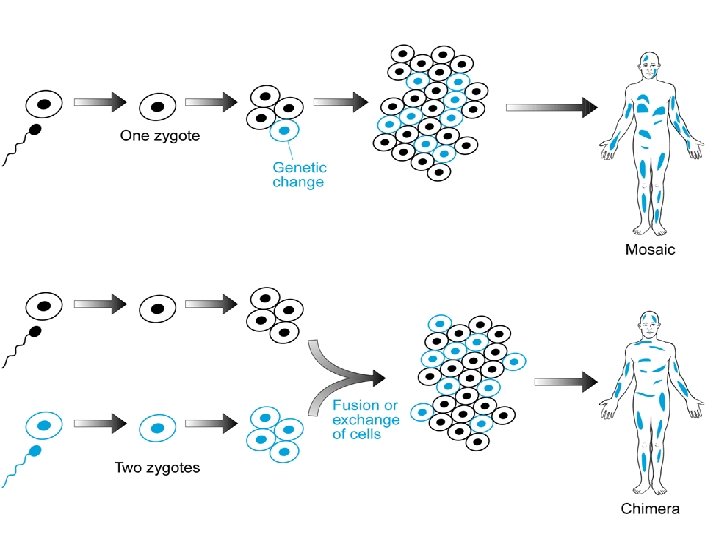

Tipo I, corredo sovrannumerario paterno Feto microcefalico o normale Placenta ingrossata Tipo II, corredo sovrannumerario materno Ritardo di crescita Feto con macrocefalia relativa Placenta poco sviluppata Nati vivi Basso peso Asimmetria cranio-facciale e difetti di ossificazione del cranio Microftalmia, ipertelorismo, micrognazia Sindattilia cutanea, piedi torti Anomalie genitali, ipoplasia delle surrenali Cardiopatie

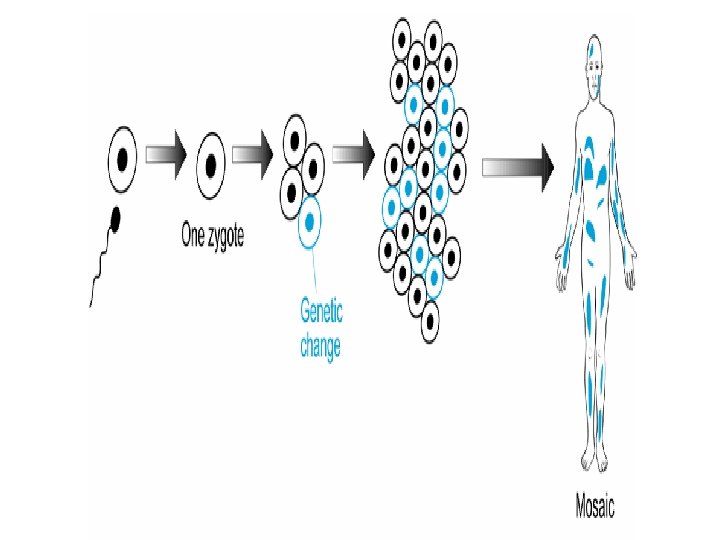
Mosaicismo, quando il cambiamento avviene dopo che si è formato lo zigote 47, XXY/46, XY

Un precedente figlio con anomalie cromosomiche Aumenta il rischio in caso di: • tutte le trisomie non mosaico • riarrangiamenti strutturali • marker cromosomi

Un precedente figlio con anomalie cromosomiche NON aumenta il rischio in caso di: • 47, XYY • triploidia, tetraploidia • sindrome di Turner

Valutazione del rischio riproduttivo nel periodo preconcezionale momento ottimale (ma oltre la metà delle gestazioni insorge inaspettatamente) raccolta dei dati (visita, abitudini, terapie, accertamenti lab) • SCOPO: identificazione dei portatori sani di malattie genetiche – portatori che hanno un rischio riproduttivo a prescindere dal partner – portatori in cui il rischio si manifesta solo nel caso di unione con un partner portatore
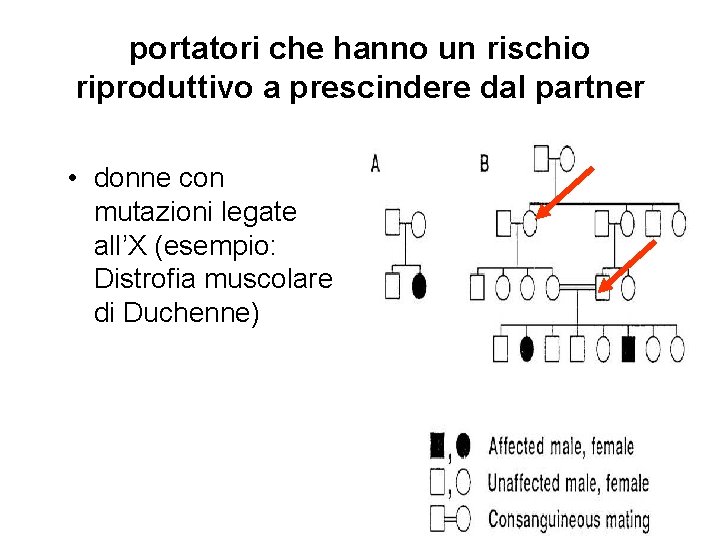
portatori che hanno un rischio riproduttivo a prescindere dal partner • donne con mutazioni legate all’X (esempio: Distrofia muscolare di Duchenne)
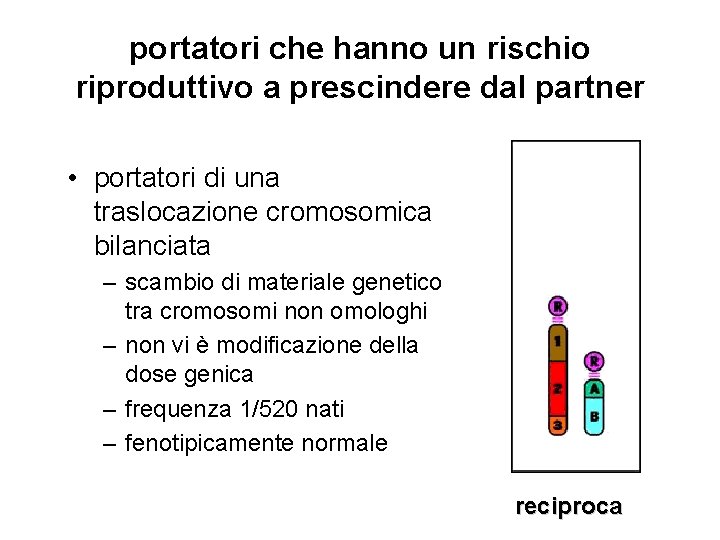
portatori che hanno un rischio riproduttivo a prescindere dal partner • portatori di una traslocazione cromosomica bilanciata – scambio di materiale genetico tra cromosomi non omologhi – non vi è modificazione della dose genica – frequenza 1/520 nati – fenotipicamente normale reciproca

coppia con familiarità per anomalie cromosomiche è indicazione all’esecuzione di un cariotipo fetale e l’estensione dell’indagine ai parenti • traslocazioni X-autosoma – maschi sterili, femmine inattivano la X normale • traslocazioni robertsoniane – non 21 60% cariotipo bilanciato – 21 15% rischio di Down, se è eterozigote la madre 1% se è eterozigote il padre • inversioni – pericentriche varianti dell’ 1, 9, 16 e Y, in altri casi il rischio è 5 -10% – paracentriche, rischi inferiore allo 0. 5%
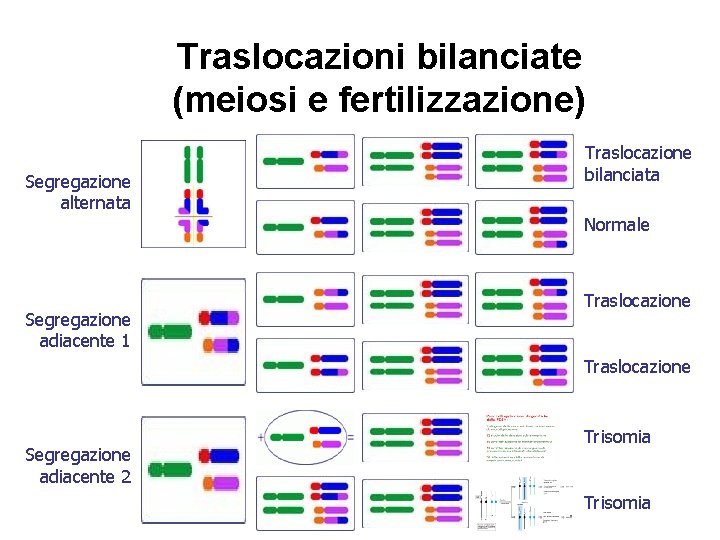
Traslocazioni bilanciate (meiosi e fertilizzazione) Segregazione alternata Traslocazione bilanciata Normale Segregazione adiacente 1 Traslocazione Segregazione adiacente 2 Trisomia

influenze sugli effetti della traslocazione • Cromosomi coinvolti e lunghezza del tratto traslocato (perché vi è una forte selezione pre e postzigotica): maggiori sono le dimensioni cromosomiche minore è la possibilità di una gravidanza a termine • Sesso del genitore donna>uomo (gli spermatozoi hanno il 7. 5% di difetti contro l’ 1% degli oociti, ma sono selezionati) • Il rischio aumenta se il difetto è stato accertato a partire da un figlio precedente con cariotipo sbilanciato

rischio alla nascita di figli con cariotipo sbilanciato • Se non vi sono stati casi in famiglia e la madre è eterozigote per una traslocazione reciproca il rischio è il 7% • Se non vi sono stati casi in famiglia e il padre è eterozigote per una traslocazione reciproca il rischio è il 3% • Se vi sono stati casi di traslocazioni sbilanciate in famiglia e la madre è eterozigote il rischio è il 14% • Se vi sono stati casi di traslocazioni sbilanciate in famiglia e il padre è eterozigote il rischio è l’ 8%

donna eterozigote per una traslocazione bilanciata X-autosoma


Traslocazioni Robertsoniana reciproca

Rischio alla nascita di figli con cariotipo sbilanciato da genitori con traslocazione robertsoniana • • t(13; 14) M=F 1% t(14; 21) F 15% M 2% t(21; 22) F 10% M 5% t(21; 21) M=F 100%

portatori che hanno un rischio riproduttivo a prescindere dal partner • mutazioni dominanti ad esordio tardivo (corea di Huntington, atassie spinocerebellari) • mutazioni dominanti a penetranza incompleta
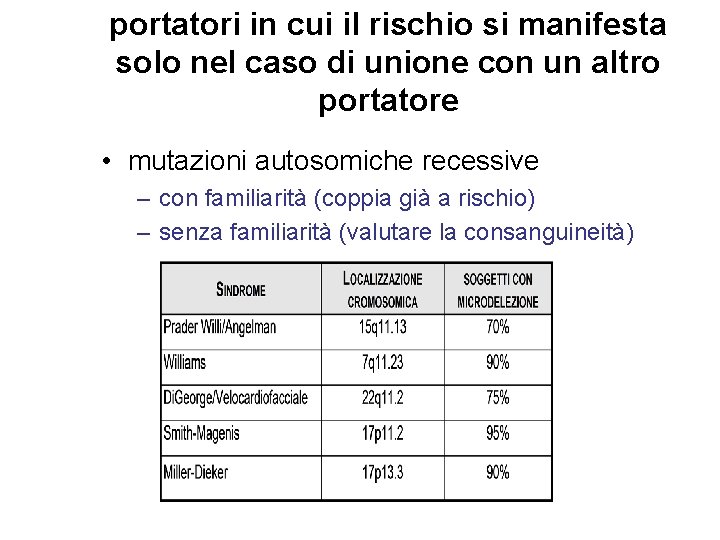
portatori in cui il rischio si manifesta solo nel caso di unione con un altro portatore • mutazioni autosomiche recessive – con familiarità (coppia già a rischio) – senza familiarità (valutare la consanguineità)

ogni individuo è portatore sano di almeno 8 malattie genetiche recessive, di cui 3 letali • • fratelli, genitori-figli fratellastri, zii-nipoti cugini diretti (0. 5%) secondi cugini • • 1/4 omozigosi 1/8 omozigosi 1/16 omozigosi 1/64 omozigosi i difetti congeniti hanno un rischio empirico raddoppiato in caso di cugini primi non è utile l’esame cromosomico
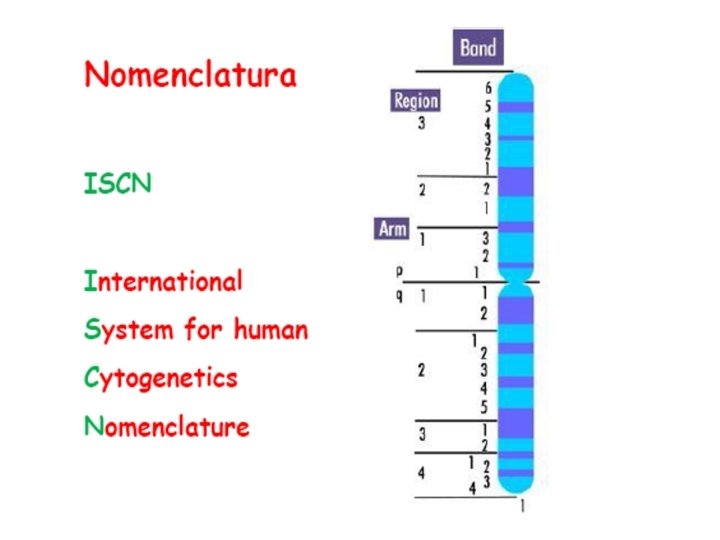

feto con anomalia cromosomica (mosaicismo) • • trisomie a mosaico 8, 9, 13, 18, 21 crescita in coltura di cellule materne mosaicismo vero (livello III) pseudomosaicismo (livelli II e I)

Whitehead Institute, Center for Genome Research, Cambridge, MA


• La grandezza totale del genoma umano aploide è di 3. 070. 000 basi di cui 2. 843. 000 sono di eucromatina
UCSC Genome Browser Screenshot from University of California at Santa Cruz http: //genome. ucsc. edu

disordine genomico submicroscopico Il disordine genomico submicroscopico è una patologia causata da • acquisizione • perdita • alterazione di uno o più geni contigui le cui variazioni di dosaggio possono produrre effetti fenotipici La base molecolare è rappresentata da riarrangiamenti genomici, quali duplicazioni, delezioni, inversioni, senza grosse alterazioni del cariotipo (<5 Mb)
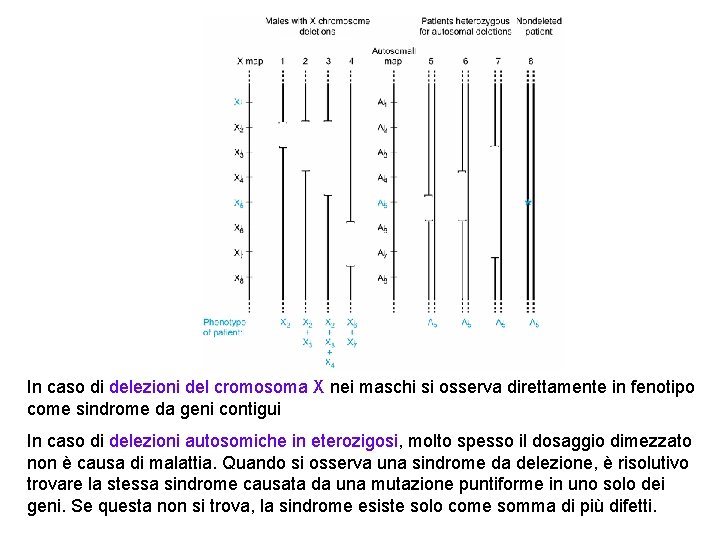
In caso di delezioni del cromosoma X nei maschi si osserva direttamente in fenotipo come sindrome da geni contigui In caso di delezioni autosomiche in eterozigosi, molto spesso il dosaggio dimezzato non è causa di malattia. Quando si osserva una sindrome da delezione, è risolutivo trovare la stessa sindrome causata da una mutazione puntiforme in uno solo dei geni. Se questa non si trova, la sindrome esiste solo come somma di più difetti.

ACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTC CGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGC GACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTA GCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCG CACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCT CTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACCGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGAT ATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGAACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGC TCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGC GCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGG CTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCG ATATAGCTCGCGACACAGA TATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCAC ACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATAT ATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGA GACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACA CCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATA TAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGT AGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGA CGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAG CGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGAC GTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAG ACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCC CTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCG CTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGATAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCT AGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCT AGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTC GCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACC GCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACC GCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTC GAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGA AACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCTCCCTGA AACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGAC ACACACAGATATTATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAG ACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATA GCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACA CGTGCTAGCTCCTCTCGAGACGTTATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTA GCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGAC ACACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCG AGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGC ACACCGCTCGAGATAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCT CGATATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGC TCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCT GAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACAC GTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTC ACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACAC AGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCT CTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGA

ACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTC CGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGC GACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTA GCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCG CACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCT CTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACCGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGAT ATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGAACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGC TCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGC GCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGG CTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCG ATATAGCTCGCGACACAGA TATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCAC ACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATAT ATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGA GACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACA CCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATA TAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGT AGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGA CGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAG CGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACTATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACCGAGACGTAGGGCTCTCGATATA GCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGC TAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCG ACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAG CTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCT AGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACA GCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACA GCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGAC GTAGGGCTCTCGATATAGCTCGCGACA CACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTC CTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACA GATATATAGCGGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGATAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCT CCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGCT CCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGA CCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCT CGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCT CGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTC CGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCT CGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATA TATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAG ATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACAC CGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACAC AGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATAT AGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTTATAGCTCGCGACACAGATATATAGCGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTG AAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGACGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTGACACGTGCTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGACACAGATATATAGCGCTCCCTGAAACAGCTCCGACACAGCTCGCACACCGCTCGAGACCTTAGCTCCTCTCGAGACGTAGGGCTCTCGATATAGCTCGCGA Copy Number Variation 10% of the human genome could vary in copy number 1 2
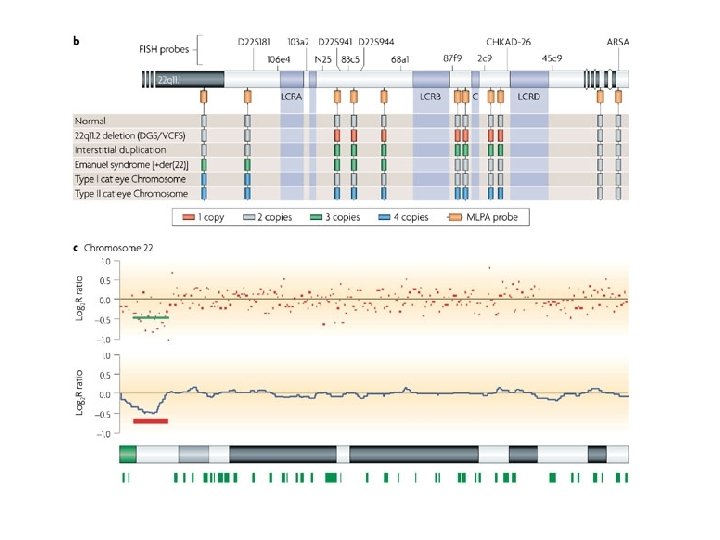
principali sindromi da delezione
FISH

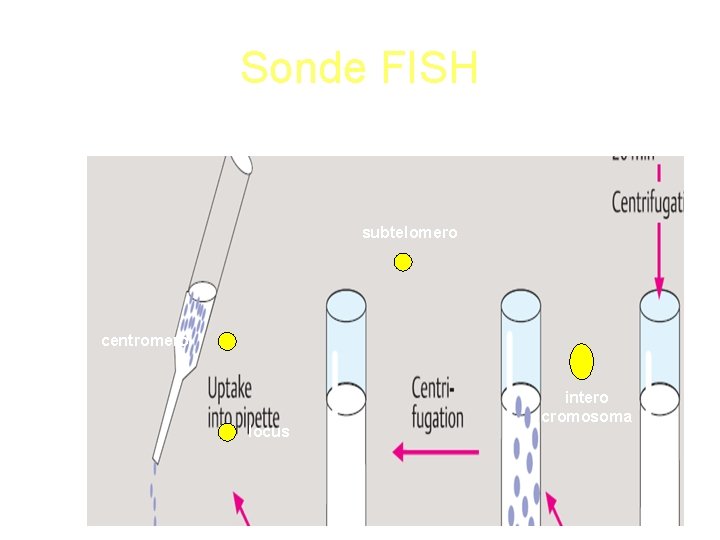
Sonde FISH subtelomero centromero locus intero cromosoma

PAINTING


Sindrome di Di. George

Di. George/velocardiofacciale La sindrome di Di. George del 22 q 11. 2 è la più frequente sindrome da microdelezione, con un incidenza di 1 su 4000— 5000 nati La delezione comprende 3 Mb ed almeno 30 geni

• Migrating neural crest cells make a contribution to the embryonic structures affected in Di. George syndrome. • The cartoon represents a human embryo at 4– 6 weeks gestation. • The migration of neural crest cells from the hindbrain to the branchial arch/pharyngeal pouch system and cardiac outflow tract is indicated by the arrows. • Examples of malformations associated with perturbation of this process are listed and these overlap substantially with those seen in 22 q 11 DS AAA, arch arteries; PDA, persistent ductus arteriosus; IAA, interrupted aortic arch.

Di. George • È caratterizzata da – Anomalie cardiache – T-cell deficit – palatoschisi – anomalie facciali – Ipocalcemia Mutazioni puntiformi del gene TBX 1 possono portare a questi 5 tratti fenotipici, ma non alle difficoltà nell’apprendimento che è invece frequente nella sindrome da delezione
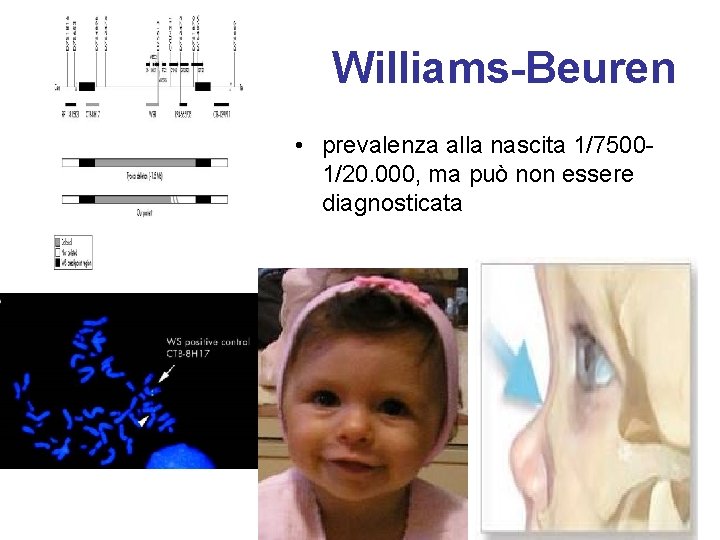
Williams-Beuren • prevalenza alla nascita 1/75001/20. 000, ma può non essere diagnosticata

Williams una delezione tipica

Williams genetica • delezione “de novo” • trasmissione autosomica dominante • delezione di 1. 6 MB da 21 geni contigui in eterozigosi a 7 q 11. 23 – gene dell’elastina – LIM kinase 1 (LIMK 1) – CLIP-115 che lega i microtubuli – Fattori di trascrizione GTF 2 IRD 1 – effetto posizionale su altri geni circostanti la delezione
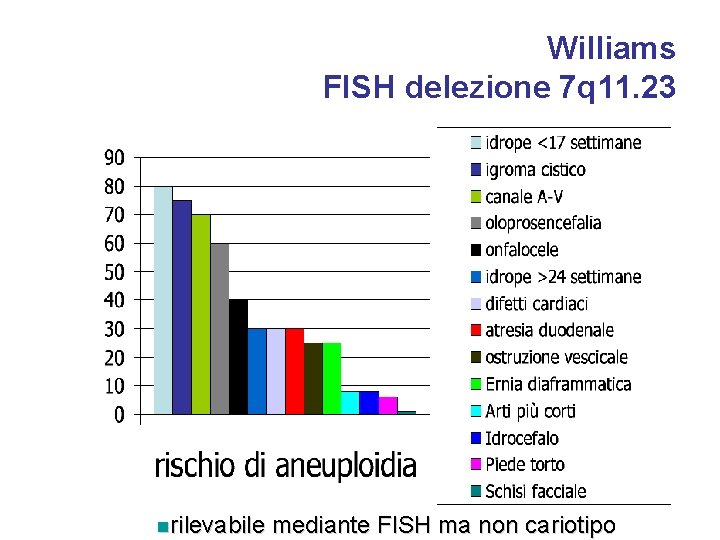
Williams FISH delezione 7 q 11. 23 nrilevabile mediante FISH ma non cariotipo

Williams comportamento • lieve o medio ritardo mentale (IQ tra 41 e 80) • scarsa capacità di concentrazione • ritardo nell’apprendimento del linguaggio e poi esagerata loquacità • personalità amichevole e affettuosa • danno facilmente confidenza anche a sconosciuti • ansietà, spesso preoccupati per il benessere altrui • ipersensibilità ai suoni • memoria visiva e uditiva spesso fuori dal comune • ricordano persone, luoghi e motivi musicali • predisposizione ad imparare le lingue e la musica

Williams aspetto e segni • Faccia da elfo • Occhi blu (77%) con pattern stellato dell’iride (74%) ma questo vale per i nordeuropei, strabismo (40%) • Naso con la punta bulbosa • bocca larga e guance piene • microdontia e micrognazia • Statura 10 cm in meno del normale • ipercalcemia • stenosi periferica delle arterie polmonari • stenosi aortica sopravalvolare
http: //www. wsf. org/family/photoalbum/wsfphoto. htm Williams foto
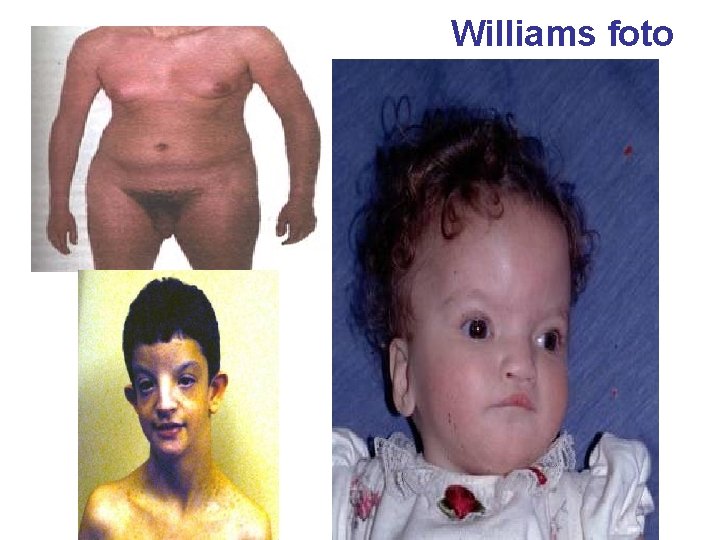
Williams foto

Wolf-Hirschhorn genetica • delezione “de novo” di circa 4 MB • le delezioni sono più frequenti nella linea germinale maschile • trasmissione autosomica dominante • Regione critica di 165 kb di molti geni contigui in eterozigosi a 4 p 16. 3

Wolf-Hirschhorn delezione a 4 p 16. 3

Wolf-Hirschhorn • • Scarso accrescimento Ritardo mentale, ipotonia Labbro leporino Conformazione ad elmo di guerriero greco

Sindrome 5 p- (cri du chat) 1: 50. 000 nati • Pianto acuto e flebile • Caratteristiche principali: – Ritardo di crescita – Microcefalia ed ipertelorismo – Ipotonia, diastasi dei retti – Deficit intellettivo e del linguaggio

Imprinting

Imprinting • Nelle cellule germinali primordiali l’imprinting viene cancellato del tutto e il DNA è demetilato • Successivamente nella linea germinale maschile si determina un pattern di imprinting che in alcuni loci è complementare a quello della linea germinale femminile • I cromosomi su cui avviene l’imprinting (7, 11, 15) manterranno questo pattern e lo riprodurranno ad ogni mitosi • Si potranno sempre distinguere l’espressione genica del cromosoma materno e paterno

Disomia uniparentale • Due copie dello stesso cromosoma sono ereditate dallo stesso genitore • Spesso questo avviene attraverso un fenomeno transitorio di trisomia, seguito dalla perdita del cromosoma singolo e mantenimento del cromosoma doppio

Angelman • 70% dei casi delezione della regione cromosomica 15 q 11 -q 13, che è soggetta al fenomeno dell'imprinting del cromosoma paterno • Il gene materno (l'unico espresso) può essere alterato con 4 meccanismi noti: – – delezione disomia uniparentale paterna difetti nell'imprinting mutazioni a carico del gene UBE 3 A (ubiquitin ligasi) • La diagnosi è clinica e il difetto genetico non si identifica nel 20% dei casi


Angelman • "happy puppet syndrome" si può identificare in Cucciolo (Dopey) "addormentato", il più giovane dei nani che non ha mai imparato a parlare • ritardo mentale con assenza del linguaggio, difficoltà nell'equilibrio, eccessivo buon umore
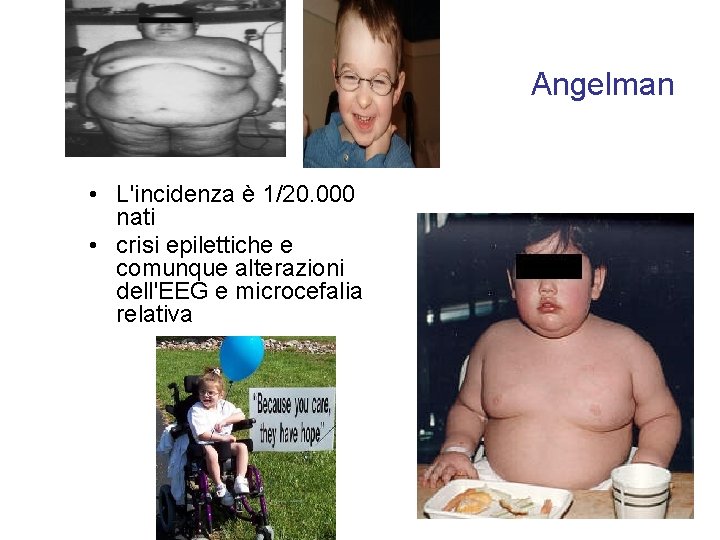
Angelman • L'incidenza è 1/20. 000 nati • crisi epilettiche e comunque alterazioni dell'EEG e microcefalia relativa

Prader-Willi • • • iperfagia>obesità eccessiva assunzione di liquidi reazioni abnormi ai sedativi acromicria, criptorchidismo insensibilità al dolore, lesioni cutanee sbalzi di umore
Prader-Willi 1/15. 000

Nomenclatura delle delezioni • Le delezioni sono designate con la sigla del che segue i numeri dei nucleotidi a monte e a valle della delezione separatida un segno _ – 82_83 del (o 82_83 del. TG) indica una delezione di TG nella sequenza ACTTTGTGCC (dove A è il nucleotide 76) che diventa ACTTTGCC

Cosa sono le distrofie muscolari? • Malattie degenerative progressive • Variazione dello spessore delle miofibrille con forti cambiamenti nella istologia del muscolo • indebolimento e degenerazione del tessuto muscolare in fibroso e adiposo • aree di necrosi con processi infiammatori
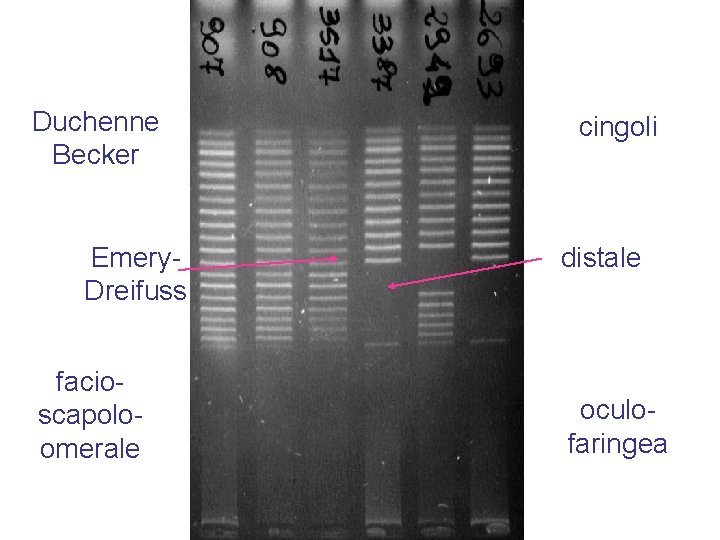
Duchenne Becker Emery. Dreifuss facioscapoloomerale cingoli distale oculofaringea

Distrofia muscolare Duchenne/Becker DMD Duchenne - 1/3, 500 maschi • Insorgenza -- Infanzia - tra 2 e 6 anni • Sintomi – Debolezza generalizzata e danno muscolare prima agli arti e al tronco, polpacci ingrossati • Progressione – Lenta ma inesorabile. Colpisce tutti i muscoli volontari. Sopravvivenza fino a 25 -30 anni BMD Becker - 1/10, 000 maschi • Insorgenza – Adolescenza o dopo • Sintomi – Identici alla DMD ma più attenuati. Vi è coinvolgimento cardiaco significativo • Progressione – Più lenta e più variabile della distrofia di Duchenne con buona aspettativa di vita

Le delezioni intrageniche del gene della distrofina mandano fuori cornice la lettura delle triplette quando gli esoni cancellati contenevano un numero di nucleotidi che non è multiplo esatto di tre (1, 2, 4, 5, 7, 8, 10, 11 ecc). Questo causa la distrofia di Duchenne.
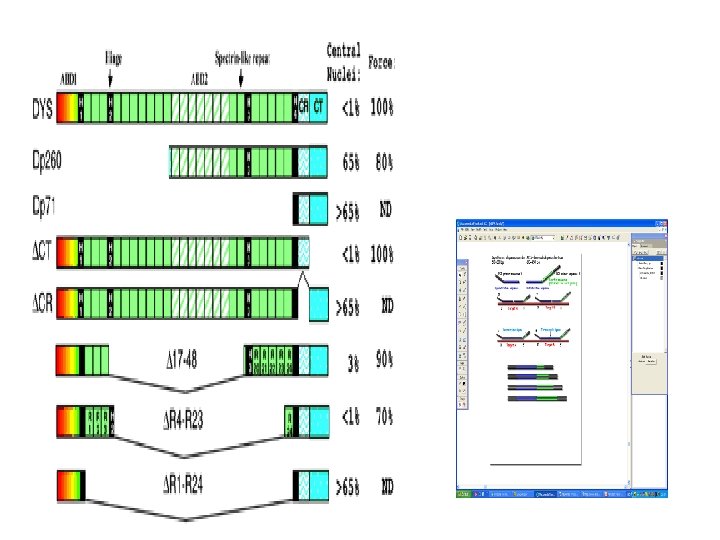
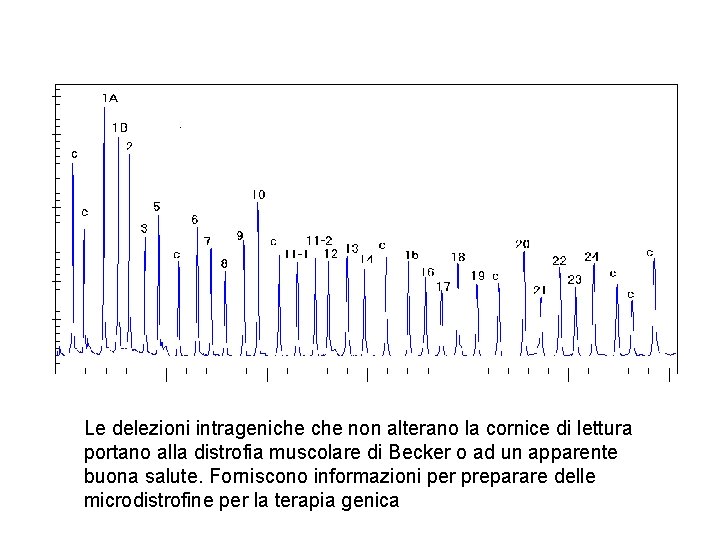
Le delezioni intrageniche non alterano la cornice di lettura portano alla distrofia muscolare di Becker o ad un apparente buona salute. Forniscono informazioni per preparare delle microdistrofine per la terapia genica

Nomenclatura delle delezioni • Le delezioni sono designate con la sigla del che segue i numeri dei nucleotidi a monte e a valle della delezione separatida un segno _ – 82_83 del (o 82_83 del. TG) indica una delezione di TG nella sequenza ACTTTGTGCC (dove A è il nucleotide 76) che diventa ACTTTGCC

MLPA probes

Hybridization 1. 2. The MLPA probemix is added to denatured genomic DNA The two parts of each probe hybridise to adjacent target sequences

ligation 3. Probes are ligated by a thermostable ligase

PCR amplification 4. A universal primer pair is used to amplify all ligated probes The PCR product of each probe has a unique length (130 480 bp)
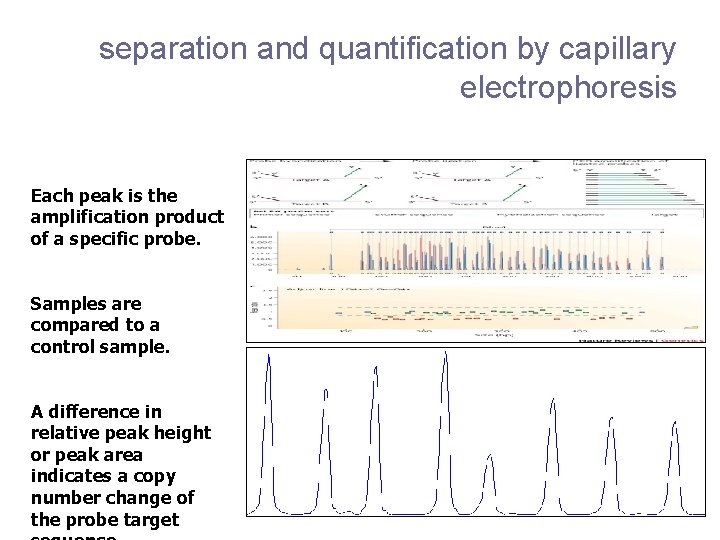
separation and quantification by capillary electrophoresis Each peak is the amplification product of a specific probe. Samples are compared to a control sample. A difference in relative peak height or peak area indicates a copy number change of the probe target


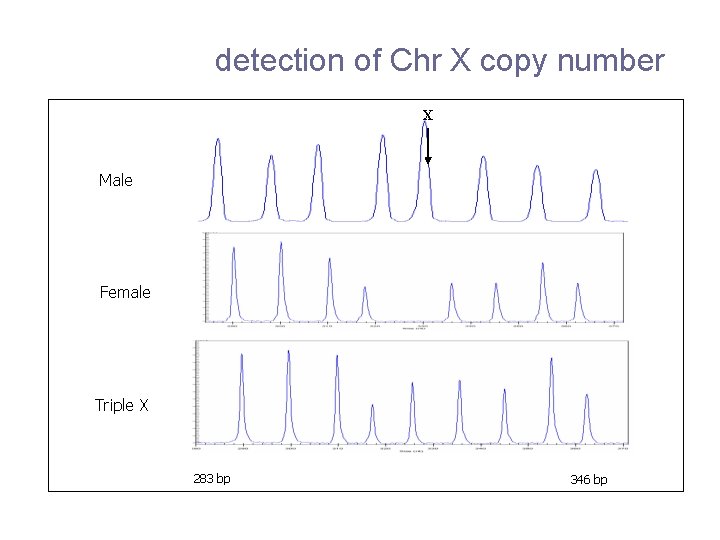
detection of Chr X copy number X Male Female Triple X 283 bp 346 bp
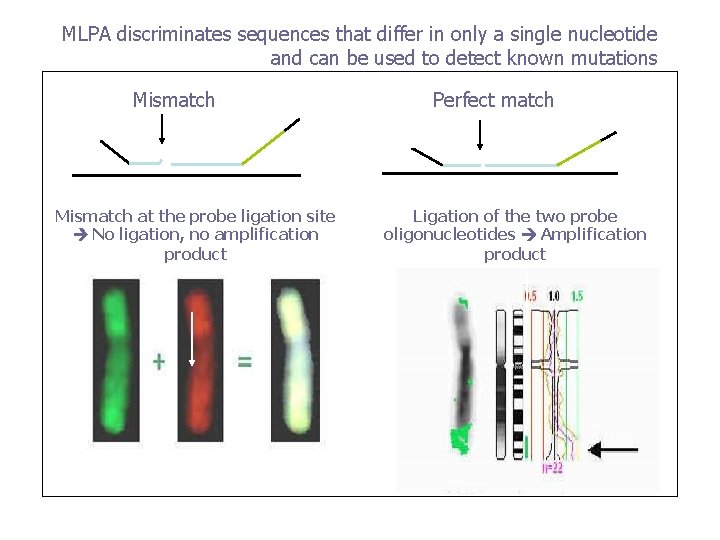
MLPA discriminates sequences that differ in only a single nucleotide and can be used to detect known mutations Mismatch at the probe ligation site No ligation, no amplification product Perfect match Ligation of the two probe oligonucleotides Amplification product
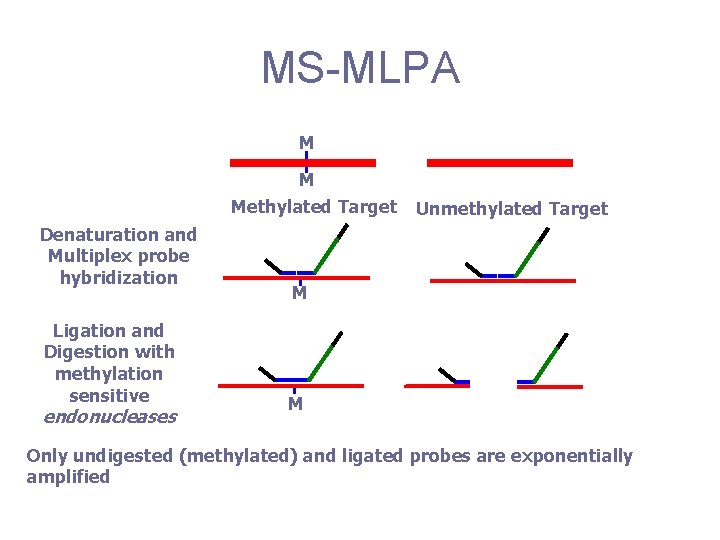
MS-MLPA M M Methylated Target Denaturation and Multiplex probe hybridization Ligation and Digestion with methylation sensitive endonucleases Unmethylated Target M M Only undigested (methylated) and ligated probes are exponentially amplified

La tecnica del CGH (comparative genomic hybridization) permette l’individuazione di sequenze delete o duplicate nel genoma da testare (red) mediante il confronto con un genoma di riferimento (green). Sono preparate due sonde fluorescenti di colore diverso che ibridano contemporaneamente sui cromosomi. Se in una regione cromosomica prevale il colore (green) relativo al genoma di controllo questo significa che il genoma da testare (red) ha una delezione in quella regione

- Slides: 148