Cours de Chimie Analytique JeanLuc Vialle jluc viallegmail











































































































- Slides: 125

Cours de Chimie Analytique Jean-Luc Vialle jluc. vialle@gmail. com 2009 -2010

Objectifs • Maitriser les techniques utilisées dans les domaines: - De l’agroalimentaire (lipides, glucides, protides) - Connexes à la production (environnement, culture, élevage) • Approfondir quelques techniques majeures et discriminatives

Sommaire • • • Panorama des techniques La Quantification et l’Echantillonnage La Chromatographie L’HPLC et La CPG L’ Absorption Atomique et L’ Absorption Moléculaire

Déroulement - Contrôle • • 5 Interventions: Cours 1, 5 TD + 0, 5 TD Projet 1 Projet (TP) 1 contrôle • Claroline: Chimie Analytique – Documents (cours + Power-Point) – Forum (Questions)

Chapitre N° 1 Panorama des techniques analytiques

Sommaire • Introduction Les environnements Recherche, R&D, Production • Contraintes des analyses Personnel, Matériel, Normatives, Economiques • Classifications des techniques Propriétés, Etat, Seuil, Cibles

I°) Introduction • Objectifs: Adéquation entre un‘produit’ et un cahier des charges et/ou une législation. • Moyens: Quantifications +/- précises de différents paramètres • Paramètres: Sensoriels, Physiques, Chimiques µ biologiques liés à la matrice, à la molécule

• Représentativité: Analyse, Echantillonage, Extraction, Conservation. • Adaptation de la méthode au résultat attendu • Ciblage des paramètres en fonction des objectifs et de l’environnement - Recherche et Développement - Production

11 L’environnement Recherche • Objectifs: • Mots Clefs: Structurale / Evolution Liés au produit Nature, Origine, Matrice, Etat, Pureté • Moyens: Techniques Lourdes disponibles en Centre de Recherche ou en externalisation • Obligations de moyens: Pas / peu de contraintes économiques et temporelle

12 L’environnement R&D • Objectifs: Quantification a) Centrée sur le produit + Niveau de détection 2 phases: b) Transposition en production : Contraintes normatives • • Moyens plus softs Techniques globales / discriminatives

13 L’environnement Production • 3 mots clefs: Simplicité - Durée - Coût • Nouvelles contraintes: Obligations - Références - Externalisation - Qualification • Techniques mises en œuvre : Liées à la valeur ajoutée du produit: Faible Globale Elevée Discriminative

II°) Contraintes des analyses • • Liées au personnel Liées au matériel Liées aux méthodes Liées à l’aspect économique et à l’aspect délai

21 Personnel compétent • Production : Faibles compétences Analyses simples (globales) Automatisation • Laboratoire d’analyse: Niveau de compétence + élevé Analyses discriminatives Automatisation • Laboratoire de recherche: Niveau de compétence très élevé Interprétation des analyses

22 Contraintes matérielles • Coût d’investissement: - Routine (Production) : 15. 000 Euros - Analyse discriminative: 15. 000 Euros par ligne d’analyse - Analyse structurale: Quelques centaines de milliers d’Euros par technique. • Coût de fonctionnement et de maintenance

23 Contraintes Normatives et Légales • Normes ISO, Afnor, Din, Asae… font références et sont incontournables si obligations légales • Méthodes officielles: AOAC pallient l’absence de normes • Méthodes interprofessionnelles Ex: Test de sédimentation de Zélény, saccharimétrique dans l’industrie sucrière, MS chez la pomme de terre. • Méthodes internes (propres à l’entreprise)

24 Contraintes économiques et temporelles • Liées à l’aspect légal ou marketting de l’analyse. • Liées à l’impact sur la production (Immobilisation) • Internalisation / Externalisation de l’analyse Impact sur le délai et sur le coût • Liées au volume d’activité de l’entreprise et à la valeur ajoutée de la production

• C < 15 Euros , D < 3 jours MS, p. H, Gravimétrie, Brix, tests simples • 15 < C < 50 Euros, D < 3 jours Titrimétrie, Complexiométrie, AA, Absorption moléculaire • 100 > C > 50 Euros, D < 3 jours Techniques chromatographiques internalisées, simples • C > 100 Euros, D > 1 semaine Analyse thermiques, structurales, analyses chromatographiques externalisées

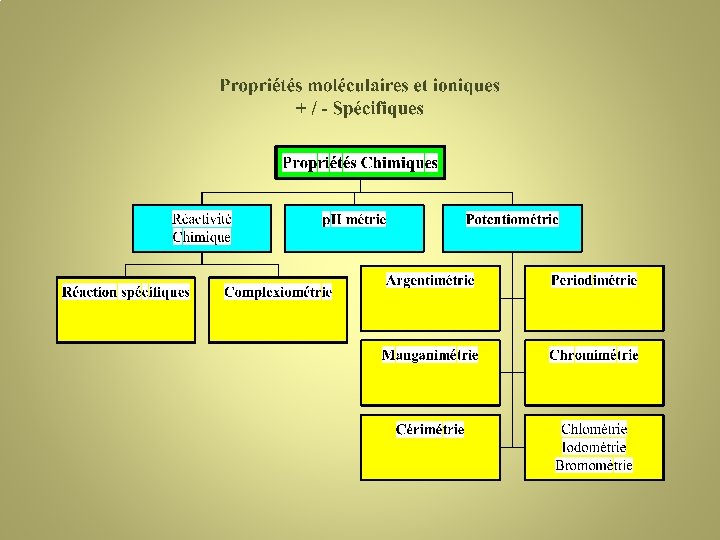
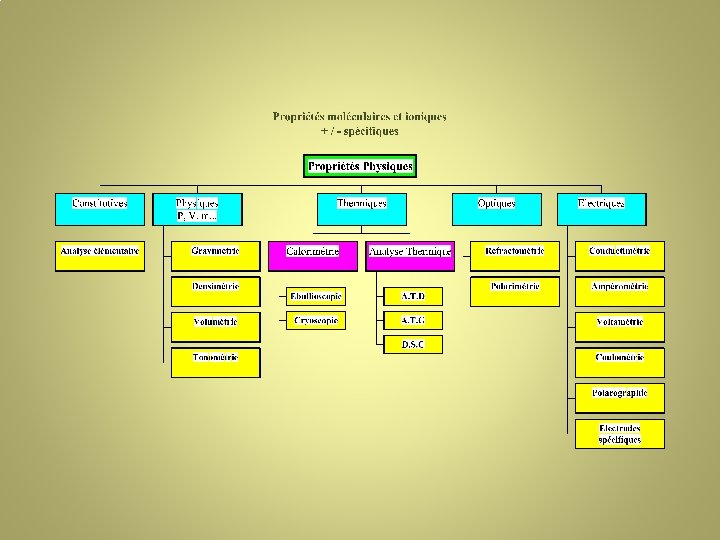
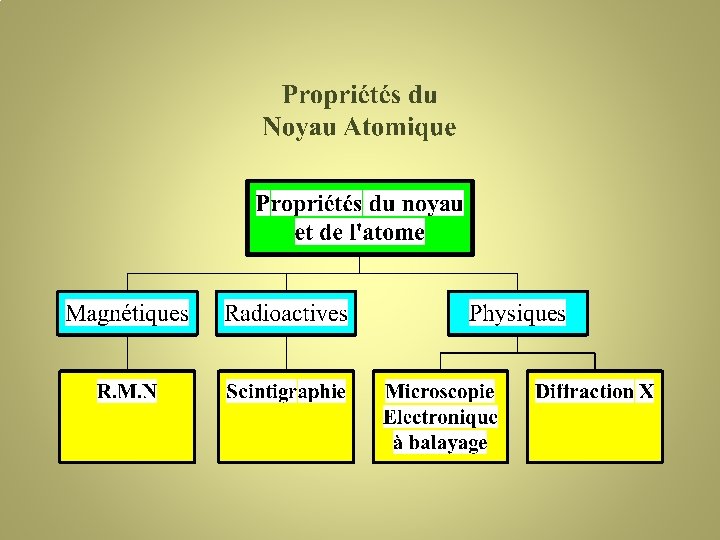
III°) Classifications des techniques • • • Selon les propriétés du soluté (matrice). Selon le caractère ‘destructif’. Selon l”état de la matière. Selon le seuil de détection Selon le caractère discriminant de l’analyse Selon la ‘cible’ visée dans la molécule

• Propriétés du soluté (matrice) Chimiques et µbiologiques - Physiques - Mécaniques - Thermiques - Optiques - Electriques - Magnétiques - Physico chimiques - Energétiques - Fragmentation • Caractère destructif / non destructif MEB, RX, RMN du solide, Near FTIR • Etat de la matière: S, L G • Seuil de détection: – 0, 1% (1000 ppm) Titrimétrie - Thermiques - IR - RMN - Gravimétrie - 1 ppm: AA, AM , Chromatographie… • Global / Discriminant: Titrimétrie / Séparatives

Classification selon la ‘cible’ • Molécule = atomes et ou de groupes fonctionnels liés entres eux par des électrons. • Atome = noyau + électrons • Propriétés physiques , chimiques +/- spécifiques et des Propriétés physicochimiques spécifiques Techniques Séparatives

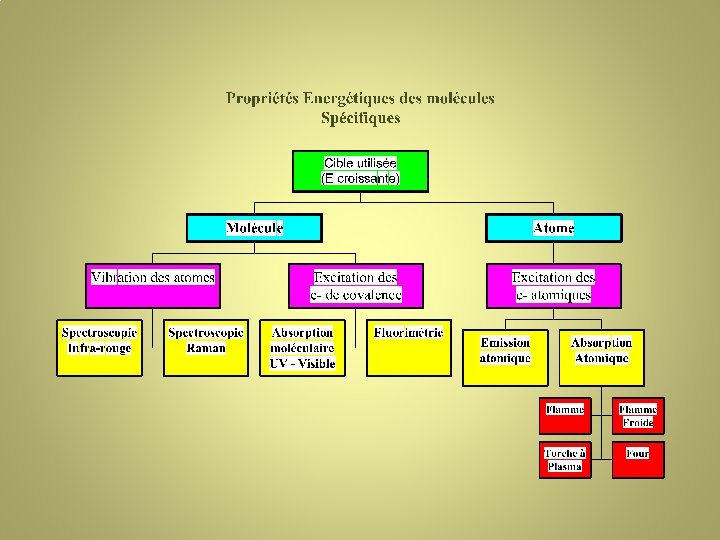
• Possibilité de la casser par apport d’énergie mécanique (chimique) analyse élémentaire , Spectrométrie de masse. • Possibilité de modification de la molécule par apport d’énergie sous forme thermique ATD, ATG, DSC, Fusion… • Possibilté d’action sur les molécules et ses atomes constitutifs par apport d’énergie sous forme lumineuse E = hc / En fonction de l’énergie apportée, on agit sur des cibles différentes: SAA, IR, Absorption moléculaire

• µ onde et ondes radio 3 106 nm Modification de la matrice • Infra-Rouge de 2500 à 1000 nm Vibration des atomes constitutifs des liaisons • Visible de 800 à 400 nm Excitation des electrons constitutifs des liaisons (les plus mobiles). Excitation des electrons atomiques • UV de 350 à 200 nm Excitation des électrons constitutifs des liaisons (les moins mobiles) • RX et rayons < 3 nm Arrachage des electrons constitutifs






Chapitre N° 2 La quantification

Sommaire • Introduction Les calculs d’incertitudes • Les méthodes ‘Absolues’ Methodes directes Dosages chimiques • Les méthodes comparatives Etalonnage interne et externe Les ajouts dosés • Conclusion

I°) Introduction • Analyse = Quantification • Structurale = Identification • Rappels sur les incertitudes Incertitudes absolues n x Incertitudes relatives x /x

II°) Les méthodes ‘absolues’ • Mesure de paramètre physiques Exemple Taux de cendres NF V 18 -101 • Méthodes basées sur l’application d’une loi simple Exemple ; L’amidon (3ème directive du JO du 23/11 1980) • Méthodes basées sur des réactions chimiques

• Acido-basique • Rédox • Complexiométrie - Précipitation • Conservation du nombre d’équivalents échangés • Méthodes à point final • Méthode directe: (NF T 60 -204) • Méthode en retour (NF V 18 -100)

III°) Méthodes comparatives • Etalonnage externe • Etalonnage interne • Méthode des ajouts dosés

31 Etalonnage externe • Pas de dépendance d’un facteur extérieur • Application au dosage du phosphore soluble dans les terres (NF X 31 -161) – Etalonnage – Exploitation des résultats – Avantages et inconvénients

32 Méthode de l’étalonnage interne • • • Domaine d’utilisation Principes Application à l’analyse des FAME (NF T 60 -234) Avantages et inconvénients Choix de l’étalon interne

33 Méthode des ajouts dosés • Analyse de traces • Application en absorption atomique • Application en chromatographie • Avantages et inconvénients

Chapitre N° 3 Introduction à la Chromatographie

Sommaire • • Introduction Aspect thermodynamique Aspect cinétique Facteurs liés à la chromatographie

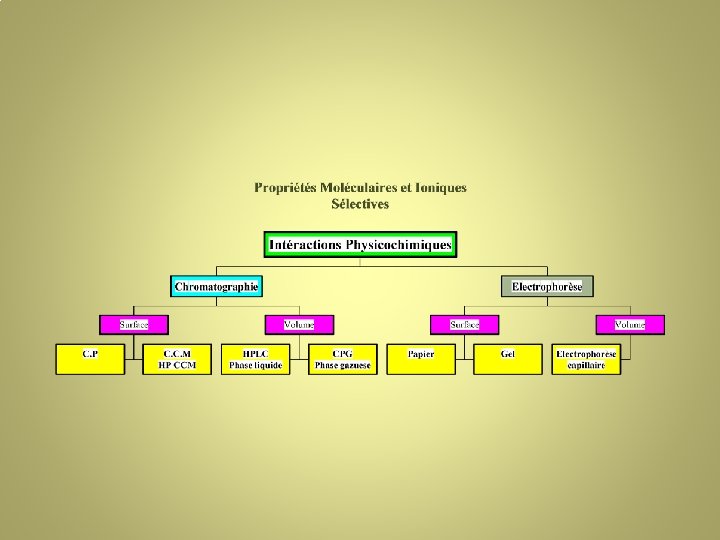
I°) Introduction • Technique séparative • Dualité Analytique / Préparative Lié à la valeur ajoutée • Les différents états de la matière solide – liquide – gaz – critique • Classification des techniques séparatives - Suivant les forces mises en jeu - Suivant l’état de la matière

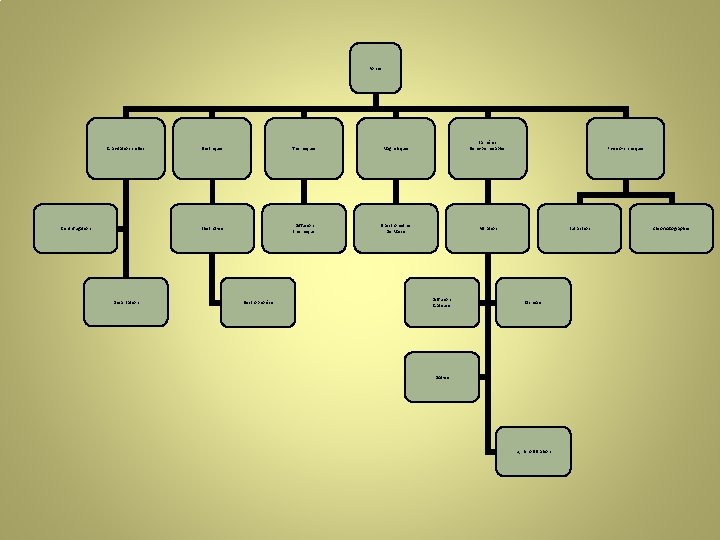
Forces Gravitationnnelles Centrifugation Décantation Electriques Thermiques Magnétiques Electrolyse Diffusion thermique Spectrométrie De Masse Electrophorèse Barrières Semi-perméables Physico-chimiques Filtration Diffusion Gazeuse Extraction Osmose Dialyse µ, nano filtration Chromatographie

Nature des phases Gaz - Liquide Gaz - Solide Liquide - Solide - Solide Diffusion Distillation µ filtration Chromatographie Tri Chromatographie Sonification Chromatographie Extraction Distillation Filtration Recristallisation Chromatographie

Un peu d’histoire… • Khrômatos = Couleur Graphikos = Tracé • 1903 Tswett: Ca. CO 3 Colonne ouverte • 1940 Martin et Synge : Théorie de la partition • 1950 Snyder: Théorie de l’adsorption • 1950 Martin et James CPG • 1960 CCM • 1970 HPLC et phase inverse • 1975 CPG Capillaire • 1985 HPLC en phase supercritique

Glossaire • • • Soluté: Espèce à séparer / à doser Solvant: Solubilise le soluté Eluant: Phase mobile Eluat: Phase mobile (+ soluté) Phase stationnaire: Phase immobilisée dans le système chromatographique

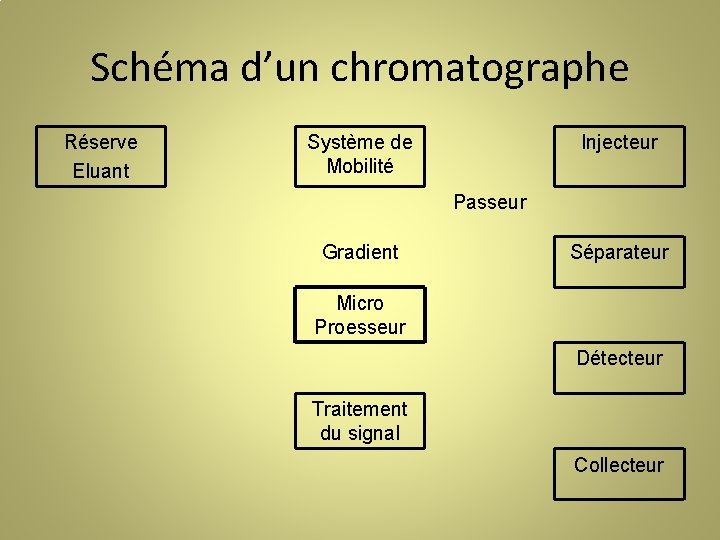
Schéma d’un chromatographe Réserve Eluant Système de Mobilité Injecteur Passeur Gradient Séparateur Micro Proesseur Détecteur Traitement du signal Collecteur

Classification des techniques chromatographiques • Suivant la technologie: Surface / Volume • Suivant la nature des phases: Phase mobile: Liquide ou Gazeuse (Critique) Phase stationnaire: Solide ou Liquide immobilisé

Récapitulatif Phase Mobile Phase Stationnaire Technologie Application Principe Partage Volume CPG G/L CPG G/S Adsorption Exclusion Surface CCM L/L Partage Volume HPLC L/L Partage Surface CP L/S Adsorption Exclusion Volume LC, HPLC L/S Adsorption Exclusion Liquide Gaz Solide Liquide Solide

II°) Aspect Thermodynamique Théorie des plateaux • Un soluté P qui se distribue entre les deux phases stationnaire et mobile = Equilibre K = [P]stat / [P]mob • K varie avec la force des interactions • Objectif: Multiplication du nombre d’équilibre : n • Ecoulement discontinu ; 1 plateau = 1 équilibre • y = fraction de P (stat) et x = fraction de P (mob) k’ = y/x = cste x + y = qo = 1 0 1 2 3 …. . p … n-2 n-1 n

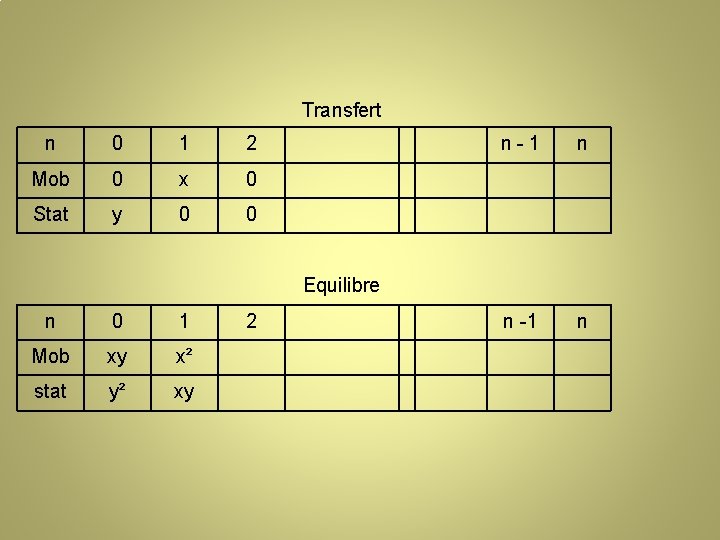
Evolution du soluté P Injection n 0 1 2 Stat. 1 0 0 Mob. 0 0 0 n-1 n n -1 n Equilibre n 0 Stat. y Mob. x 1 2

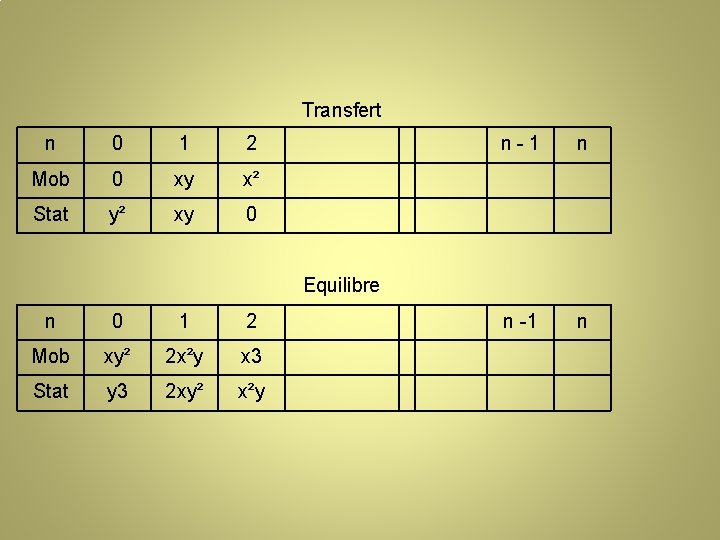
Transfert n 0 1 2 Mob 0 x 0 Stat y 0 0 n-1 n n -1 n Equilibre n 0 1 Mob xy x² stat y² xy 2

Transfert n 0 1 2 Mob 0 xy x² Stat y² xy 0 n-1 n n -1 n Equilibre n 0 1 2 Mob xy² 2 x²y x 3 Stat y 3 2 xy² x²y

Généralisation • Après n transferts: Le soluté se disperse suivant une loi du type (x + y)n • Facteur de capacité: k’ = y / x Grandeur caractéristique d’un soluté dans un système chromatographique donné • Qnp = f(n, p, q 0) Equation d’une Gaussienne Courbe à maximum

• Après n transferts, la phase mobile a parcourue une distance ln et l’extrémum se situe à une distance lp tel que lp / ln = 1 / (1+k’) • Soit en terme de vitesse vp / vn = 1 / (1+k’) • Soit t = Cste On mesure l Surface • Soit l = Cste Volume On mesure t

Quelques grandeurs fondamentales • Temps de rétention: Apparition de l’extrémum Tr = T 0 (1+k’) • Temps de rétention nulle: Soluté non retenu T 0 • Rf Rf = lp / l 0 • Efficacité : N = Nb de plateaux théoriques • HEPT: H = L / N

Séparation de plusieurs solutés • Sélectivité = k’ 2 / k’ 1 Traduit la différence d’affinité pour 1 et 2 • Résolution Rs Traduit la séparation entre deux pics chromatogaphiques

III°) Aspect Cinétique • Ecoulement Continu : Déformation des pics: • Transfert de système chromatographique et Transposition: Notion de grandeurs réduites (l, h et vitesse réduite) • Si l, h et la vitesse réduite sont constant, N est constant

Mécanismes de Dispersion • Knox (HPLC) • • • et Van Dempter (CPG) H = A + B / u + C u A = Anisotropie d’écoulement B = Diffusion longitudinale C = Résistance aux transferts de masse U = vitesse linéaire de la phase mobile Optimisation

IV°) Facteurs liés à la chromatographie • La température: Fondamental k’ est fonction de T Si T augmente k’ diminue • La composition de la phase mobile (HPLC - CCM) • Le débit de la phase mobile (u) • Loi de Darcy: Perte de charge dans un écoulement à travers un tube rempli

Chap N° 4 La CPG Sommaire • Introduction • Les phases stationnaires en colonne remplie • Transposition colonne remplie / colonne capillaire • L’injection • La détection • La dérivatisation

I°) Introduction • • • 1ère technique développée dès 1950 Simplicité de mise en œuvre Rapidité des analyses complexes Matériel disponible et peu onéreux Nombreuses applications : NF T 60 -234 FAME Carbowax 20 M DB 20 F. I. D NF T 60 -237 BHA et BHT DC 200 CP Sil 5 F. I. D

NF T 90 -120 Pc. B et Organo-chlorés OV 17 NF T 90 -121 Atrazine et Simazine DB 5 ECD Thermo ionique NF T 90 -125 COV halogénés Carbowax 1500 CPSil 5 ECD Nombreuses autres applications Permanents Catharomètre - Gaz Porapak - Solvants résiduels – Composés volatils Résidus d’incendies – Arômes – Huiles essentielles…. -

II°) Les phases stationnaires en colonne remplie • Colonne remplie = Tube + Support + Phase Liquide Imprégnée (Solide) • Tube: 2 m 1/8ème ‘’ Inox • Support: Diatomées P, W, G Granulométrie 80100 mesh (175 -150µm) Pertes de charge faibles (1 -2 bars) Taux d’imprégnation 10 - 30% Traitements: Tamisage, AW, TMCS

21 Les phases stationnaires • Les hydrocarbures ramifiés référence : Polarité nulle • Les Polysiloxanes et polysiloxanes substitués: R = CH 3, Phényl, Cyanopropyl… Polarité très faible (DB 1, 100% de CH 3) à très forte (CP Sil 88, 100% de cyanoéthyl) Référence en capillaire

• Les polyéthylènes glycols (carbowax 20 M, FFAP. . ) équivalence CP Wax, DB 20 • Les Polyesters: Polarités intermédiaires et fortes (DEGS, EGA…. ) • Les Adsorbants Tenax, Carbopack, Tamis moléculaires • Classification selon la polarité • Equivalence entre remplie et capillaire

22 Les indices de Kovat’s • Série homologue: log 10 Tr’ = an + b • Notion de droite de similitude: Prédiction de la rétention Approche d’identification • Application à la série des n alcanes Notion d’indice de rétention - - -

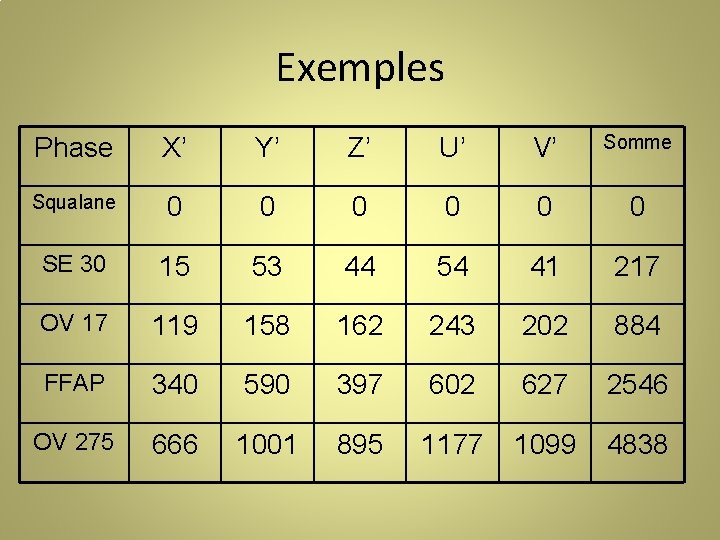
23 Classification suivant la polarité • Constantes de Mac Reynolds – Rohrschneider – 1 phase de référence : Squalane P = 0 – 5 solutés de référence: Benzène X’ n Butanol Y’ Me. COPr Z’ Nitropropane U’ Pyridine S’ Cste de Mac Reynods = Différence d’indice de rétention du soluté entre la phase et la référence Polarité = Somme des cstes de Mac Reynolds des cinq solutés (Existence de 3+2 autres solutés références)

Exemples Phase X’ Y’ Z’ U’ V’ Somme Squalane 0 0 0 SE 30 15 53 44 54 41 217 OV 17 119 158 162 243 202 884 FFAP 340 590 397 602 627 2546 OV 275 666 1001 895 1177 1099 4838

24 Choix raisonné des phases stationnaires • Classification des solutés en 5 catégories Liées à la polarité • Classification des phases en 4 catégories Liées à la polarité • Associations par catégories: - Apolaire – Apolaire - Polaire – Polaire - Moyennement polaire – Moyennement polaire

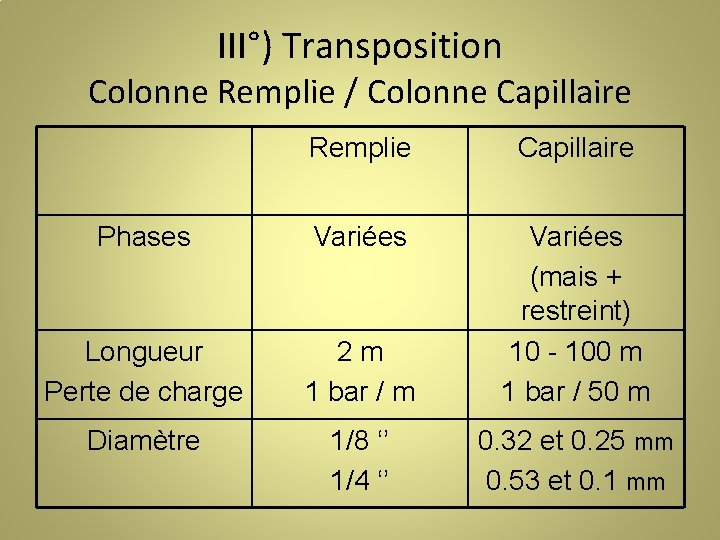
III°) Transposition Colonne Remplie / Colonne Capillaire Remplie Capillaire Phases Variées Longueur Perte de charge 2 m 1 bar / m Variées (mais + restreint) 10 - 100 m 1 bar / 50 m Diamètre 1/8 ‘’ 1/4 ‘’ 0. 32 et 0. 25 mm 0. 53 et 0. 1 mm

Classification • Colonnes de Golay: - COT et WCOT : Wall Coated Open Tubular - SCOT : Support Coated Open Tubular Layer Open Tubular - PLOT : Porous - Micropacked Columns • Perméabilité k importante : Efficacité importante et vitesses linéaires importantes soit tr faibles • B = VG/VL 2 à 10 x supérieur / remplie • B= dc / 4 ef et tr = t 0 (1 + K / B)

• Si B augmente : tr diminue ; possibilité de diminuer la température élevé: Analyses rapides : substances lourdes B faible: Substances volatiles B • Epaisseur du film: De l’ordre du micron • Tr augmente en f(Log e) e x 2 = Tr (-15°) • Films minces et films épais

• Films Minces: 0, 15 < e < 0, 5 µm Avantages: Meilleures performances Réduction du temps d’analyse Possibilité d’analyse de composés ‘lourds’ Inconvénients: Charges + faibles : restreint la possibilité d’analyse de traces - Interactions avec la surface • Films Epais: e > 1 µm Avantages: Analyses de traces Analyses de volatils Inconvénients Pb de Bleeding (e > 5µm) • Diamètre: Wide Bore = Remplie Narrow bore: Analyses courtes : Couplage GC / MS

IV°) L’injection • Colonne remplie: Injecteur à Septum Volume injecté: 0, 5 à 1 µl Gaz : 100 µl à 500 µl Head-Space (Statique et dynamique) • Colonne capillaires: Charges + faibles Utilisation de diviseurs - Split / Splitless - On column - Injecteur de verre

V°) La détection • 2 classes de détecteurs: I : Réponse proportionnelle à la concentration Catharomètre, E. C. D II : Réponse proportionnelle au débit massique: F. I. D , N. P. D • Sélectivité : Universels / Spécifiques • Quantité minimale détectable : variable de (110 ng) TCD à 0, 1 pg ECD (30 -100 pg) FID

• Catharomètre: Pont de Wheastone Universel Gaz permanents (I) • F. I. D: Combustion Universel (sauf incombustibles) Make-up (II) Notion de • E. C. D Spécifique: Capture d’électrons (I) Dérivés Halogénés • N. P. D Spécifique: Thermoionique Dérivés N et P (II)

VI°) La dérivatisation • Objectifs: Volatilisation des espèces Amélioration des analyses (trainées de pic) Amélioraion des résolutions • Méthodes: Estérification : Diazométhane, BF 3/CH 3 OH Silylation : TMCS / HMDS obtention d’éthers, d’esters silylés volatils: Pb H 2 O

Chapitre N° 5 La chromatographie Liquide L’adsorption Le Partage

Sommaire • La chromatographie d’adsorption Théorie de Snyder Facteurs liés à la phase stationnaire, la phase mobile et le soluté • Le Greffage • La chromatographie en phase inverse • La chaîne chromatographique

I°) Introduction • Le dosage de l’aflatoxine B 1 dans les aliments pour animaux (NF V 18 -200) Extraction Liquide / solide au CHCl 3 Purification Colonne ouverte de gel de silice (50 -200 µm) conditionnée dans CHCl 3 – Lavage à l’éther Désorption avec CHCl 3 / CH 3 OH (97/ 3) Chromatographie Monodimensionnelle sur silice: Phase mobile: CHCl 3 / Acétone (90/10) Ether / méthanol/ eau (96/3/1) Lecture visuelle / Fluorodensitométrique

II°) La chromatographie d’Adsorption • Supports solides polaires: Silice Caractère acide Alumine Caractère basique Utilisables en CCM, HPLC, colonne ouverte Principe: Formation de liaisons H entre le support et le soluté. (interactions)

• Phases mobiles : peu polaires • Applications analytiques: – Fonctionnalités Différentes – Isomères – Solutés peu et moyennement polaire • Applications en extraction (purification) Fixation des espèces plus polaires • Ordre d’élution: suivant l’ordre de polarité • Faible coût – Pb de la phase mobile

21 Mécanismes d’adsorption • Adsorption / désorption en surface • Equation de Snyder • log k’ = log Va + B*(E° - As °) + log (Wa/Vm) • k’ = facteur de capacité – Phase stationnaire: – Phase mobile: – Soluté: Va, Wa et Vm , B* B* , ° As et E°

Facteurs liés à la phase stationnaire • Va, Wa et Vm Liés à la taille des particules et au remplissage Peu d’actions Influence la transposition Surface / volume • B* Etat d’activité de l’adsorbant (0<B*<1) Séchage des plaques et conservation au dessicateur

Facteurs liés à la phase mobile • ° et B* • B* liée à la teneur en eau de la phase mobile Solvant isohydrique utilisation d’acide et de base pour réduire l’activité • °: Force éluante Série éluotropique si ° Augmente, alors Rf augmente (k’ diminue) Développement isocratique et en gradient de concentration. Utilisation de mélanges binaires et ternaires

Facteurs liés au soluté • As et E° • As: surface spécifique : Pas d’action si ce n’est une dérivatisation Changement de la nature du soluté et des interactions • E°: même remarque

III°) Le greffage • Adsorption Contraintes Activité du support Isohydrie de la phase mobile Limites 2 types de phase : Silice (alumine) échelle de polarité limitée problèmes de traînées de pics • 1970 Le greffage

II°) Le Greffage • Modification du support siliceux par greffage chimique d’espèces liquides: Si-OH Si-O-Si-R R= Alkyl (C 18, C 3, C 2) Phényl Amino alkyl Nitro alkyl Diols , Cyano…. • Notion de chromatographie de partage • Echelle de polarité inversée / Adsorption • End-Capping

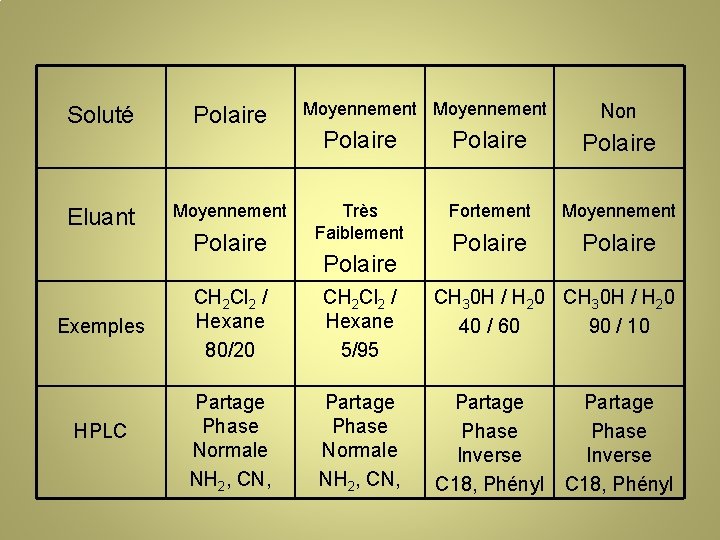
Soluté Eluant Exemples HPLC Polaire Moyennement Non Polaire Très Faiblement Fortement Moyennement Polaire CH 2 Cl 2 / Hexane 80/20 CH 2 Cl 2 / Hexane 5/95 CH 30 H / H 20 40 / 60 90 / 10 Partage Phase Normale NH 2, CN, Partage Phase Inverse C 18, Phényl

IV°) La Phase Inverse • Application : Dosage de 6 PAH (µ polluants) en phase aqueuse NFT 90 -115 : Fluoranthène, Benzofluoranthène b et k; Benzopyrène a; (10 ppb) Benzopérylène, Indénopyrène (50 ppb) • Extraction au cyclohexane - Concentration à 1 ml sous vide • Purification sur colonne d’alumine • Concentration à sec et reprise dans 1 ml de solvant: • Phase stationnaire: RP 18, Lichrosorb C 18 L = 250 mm Diam: ¼ ‘’ • Phase mobile: CH 3 -CN / H 2 O (85/15 ; 90/10) Débit: 1 ml mn-1 • Injection 20 µl • Fluorimétrie: Excitation 360 nm Emission > 420 nm

La phase stationnaire • Apolaire Lipophile = Hydrophobe • Nature du greffon: CH 3 -(CH 2)n-CH 2 si n augmente: La rétention augmente • Nombre de greffon: Plus le taux de greffage est élevé, plus la rétention est importante • Généralisation à la surface hydrocarbonée • Pratique: Entre 8 et 15 % de Carbone

La phase mobile • Base: H 20 + CH 3 OH ou H 20 + CH 3 CN Attention à la perte de charge (Darcy) • Utilisation éventuelle de modificateurs: THF, Acétone, CHCl 3… Attention à la détection • Influence de la teneur en eau : La rétention augmente avec la teneur en eau • Elution en mode isocratique : Composition de la phase mobile constante • Elution en mode gradient de concentration

Le soluté • Rétention Inverse à la polarité Plus le soluté est polaire, plus la rétention est faible. • Liée à l’hydrophobie: Cste de partage dans le système octanol / eau P • Rekker: log P = Somme fi + CM (somme kj) fi = Incréments CM = Cste = 0, 268 kj = effets de proximité log k’ = a log P + b

IV°) La chaîne chromatographique L’Injection • Couramment : 20 µl(1 à 50 µl) • Injection en boucle Etalonnage externe • Vanne d’injection Six Voies • Automatisation Passeurs automatiques

La détection - Généralités • Notion de dérive (1 heure) bruit à long terme (10 mn) bruit à court terme (1 mn) • Sensibilité: Pente de la courbe: Réponse = f (Concentration initiale) • Concentration minimale détectable: fois le bruit à court terme • Détection directe et différentielle n

Les différents Détecteurs Simples Détecteurs semi Informatifs Ultra violet Fluorimétrie Réfractométrie Diffusion de lumière UV multi lambda Fluorimètre programmable Electrochimique Conductimétrique Multi électrodes Détecteurs intelligents Spectométrie de Masse FT IR Barrette de diodes RMN

Dérivatisation pré et post colonne Dérivatisation Pré Colonne Simplicité Modification des conditions chromatographiques Ex: Acides aminés (OPA) Réactions reproductibles Possibilité de réactions secondaires Dérivatisation Post Colonne Sélectif Multi détection Exemple: Vitamine C Matériel plus sophistiqué Modification du pic chromatographique

VI°) Les autres techniques HPLC Technique Phase stationnaire Phase mobile Solutés Paire d’ions C 8, C 18 CH 3 CN, CH 3 OH, H 2 O Espèces ionisables Echange d’ions Résines échangeuses Tampons aqueux Ions minéraux cations et anions Exclusion Polymères poreux THF, Tampons aqueux Polymères hydrophiles et organiques Chirale cyclodextrines, Pirkle Aqueuses et organiques Enantiomères

Chapitre N° 6 L’absorption Moléculaire UV-Visible Et L’absorption atomique

L’absorption moléculaire Sommaire Introduction Détermination de l’indice Phénol NF T 90 -109 Détermination de As 3+ NF T 20 -054 Détermination du Fer total et du Fe 2+ NF T 90 -017 Détermination du Phosphore soluble NF X 31 -161 Le spectrophotomètre d’absorption moléculaire

Introduction • Absorption Atomique: Concerne les électrons atomiques (absorption et émission) • Absorption et Émission Moléculaire: Concerne les électrons des liaisons moléculaires, les électrons délocalisables ( ). • Mêmes concepts: Dualité Onde / Énergie E = h c / • Spectre de la lumière Domaine UV: 200 -350 nm Domaine Visible: 350 – 800 nm

• Complémentarité Absorption / Couleur Triangle des couleurs • Utilisation des propriétés d’absorptions pour une quantification • Nombreuses applications : Cations , Anions, Molécules Organiques • Sélectivité plus ou moins importante • Loi de Beer-Lambert: log 10 I 0/It = . l. C : Coefficient d’extinction molaire. Quantification par étalonnage externe

Détermination de l’indice phénol Eaux NF T 90 -109 • Principe Distillation des phénols en milieu acide (H 3 PO 4) en présence de Cu. SO 4(action bactérienne) (Entraînement à la vapeur) Enregistrement du spectre UV à 254 et 270 nm ( # 6000 et 1500) cuve quartz 1 cm Comparaison à un étalonnage externe • Applications: 0, 025 – 0, 5 mg/l

Dosage de l’arsenic Corps gras NF T 20 -054 • Principe Réduction de l’arsenic sous forme d’arsine As. H 3 par Zn en milieu HCl Absorption de l’arsine par le diéthyldithiocarbamate d’argent: Ag(DDTC) As. H 3 + 6 Ag(DDTC)…. 6 Ag + 3 H(DDTC) + As(DDTC)3 • Formation d’Argent colloïdal dispersé: Rouge – Violet • Mesure de la DO à 540 nm cuve 1 cm • Comparaison à un étalonnage externe • Application: masses de 1 à 20 µg d’Arsenic

Dosage du fer Eaux NF T 90 -017 • Fet = Fe dissous + Fe suspension • Formation d’un complexe coloré entre Fe 2+ et l’ortho phénanthroline (1 -10) Rouge –Orangé (510 nm) • Fer total: Oxydation par le peroxodisulfate Fe 3+ • Fer dissous: • Fe 2+ dissous • Applications Réduction par le chlorydrate d’hydroxylamine p. H # 4, 5 Fe 2+ Complexation (15 mn à l’obscurité) Réduction du Fe 3+ dissous Complexation directe 10 µg/l – 10 mg/l

Le phosphore soluble Sols NF X 31 -161 • Principe: Méthode de Joret-Hébert Extraction du phosphore soluble (sous toutes ses formes) par l’oxalate d’ammonium (p. H = 7) • Complexation du phosphore sous forme de complexe phosphomolybdique réduit avec le réactif sulfomolybdique (heptamolybdate d’ammonium, Acide ascorbique, thiosulfate de sodium, formol) • Développement chaud (100°C, 5 mn) d’une coloration violette • Mesure de la DO à 825 nm • Domaine d’application: 1 – 10 mg/l de P Expression du résultat en P 2 O 5 sols:

Le spectrophotomètre • • Source Monochromateur Fentes (Slit) Cuve Photomultiplicateur Amplificateur Calculateur

Sources et rayonnement incident • Lampes à décharge (lumière blanche) • Multi longueurs d’onde - Deutérium (Domaine UV) - Vapeur de mercure (Domaine visible) • Simple et double faisceaux • Sélecteur: Monochromateur • Fente (Slit): Permet de réguler l’énergie du rayon incident

Cuves • Cuves: - Plastique (jetables)Attention aux solvants organiques - Verre (domaine du visible) - Quartz (domaine UV) • A remplissage et à circulation (Cinétique – Passeurs automatiques) • Trajets optiques: 0, 1 à 5 cm fonction de la concentration et du coefficient d’extinction molaire • Zéro optique: Sur Blanc (0 d’absorbance)

Rayonnement transmis • Photomultiplicateur : Comptage des photons transmis: Travail en Absorbance (A) ou en Transmitance (T) • Amplificateur • Calculateur: Io, It, A (T), log 10(A), C • Restitution du spectre, des concentrations… • Gamme de linéarité de Beer-Lambert (Étalonnage externe)

L’absorption atomique Sommaire • • Introduction Principe de l’absorption et de l’émission Schéma général d’un spectromètre d’AA Les différentes parties du spectromètre La quantification Applications Analyse de traces

Introduction • Analyse de cations minéraux • Actuellement: Environ 60 éléments du tableau de Mendeleiev • Nombreuses applications: Métallurgie, Géologie, Environnement, Agriculture, Agro alimentaire… • Impératif: Mise en solution de l’échantillon Eaux NF T 90 -112 Flamme Eaux NF T 90 -119 Four Eaux NF T 90 -131 Flamme Froide Sols NF X 31 -151 Flamme

Principe • Atome = Noyau + électrons • Électrons: Gravitent autour du noyau (Champs électrostatique): Notion d’orbitales: Niveaux d’énergie quantifiés • État fondamental + Énergie électromagnétique: État excité (Passage de l’e- d’un niveau fondamental à un niveau supérieur) : Instable : Retour à l’état fondamental • Restitution calorifique: Absorption atomique • Restitution lumineuse: Émission atomique

• • • E = f (h, c et longueur d’onde) Notion de transitions spectrales Spectres de raies spécifiques à chaque élément Possibilité de dosage spécifique par éléments (Interférences) Équation de Boltzman: Ne = Cste x N 0 e-(E/k. T) Emission: Ne élevé Absorption: N 0 élevé Loi # Beer-Lambert A = I 0/It Log 10 A = K. l. C K = Coef. d’absorption monochromatique

Schéma général d’un spectromètre d’Absorption Atomique (Emission) • Une source de photons: Source d’émission • Une source d’atomes: Source d’atomisation • Un monochromateur: Sélecteur de radiations • Un détecteur: Photomultiplicateur + amplificateur

Source de photons • Tube à décharge à cathode creuse – Cathode : Élément à doser (sel) – Anode: Lame de Zirconium – Tube ‘rempli’ de gaz inerte (Ne, Ar) – Décharge : Tension 500 - 800 volts – Intensité = qqes m. A (suivant élément) • Obtention du spectre d’émission de l’élément à doser • Lampes mono élément et multi éléments

Générateurs d’atomes • Fonction de la nature des éléments à doser • Flamme: Cas général • Atomisation thermique: Détection plus basse • Flamme froide et générateurs d’hydrures: spécifique à certains éléments (Hg, As. . ) • Torche à plasma

Atomisation en flamme • Objectif: Transformer des espèces de la forme ionique à la forme atomique • Analyse d’échantillons liquides exempts de particules solides. • Capillaire: Transfert de l’échantillon vers la chambre de nébulisation • Nébuliseur: Formation d’un brouillard dans le comburant: Fines gouttelettes • Brûleur: Transformation des espèces à l’état atomique

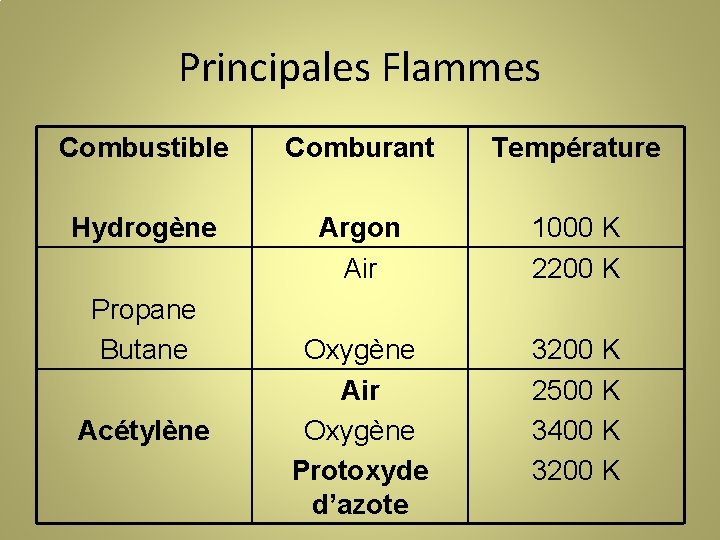
Principales Flammes Combustible Comburant Température Hydrogène Argon Air 1000 K 2200 K Oxygène Air Oxygène Protoxyde d’azote 3200 K 2500 K 3400 K 3200 K Propane Butane Acétylène

Autres Générateurs d’atomes • Atomisation électrothermique: Four - Séchage (# 100°C) - Décomposition thermique (100 à 1800°C) - Atomisation (1800 -2600°C) - Nettoyage Four (2800°C) • Générateur de mercure Hg. Cl 2 + Sn. Cl 2…. Hg° + Sn. Cl 4 • Générateurs d’hydrures As, Sb… Formations d’hydrures (As. H 3) + Flamme froide (1000°C)

Sélecteur de radiations et PM • Monochromateur: Sélection d’une longueur d’onde • Bande passante: 0, 05 à 0, 1 nm si spectre complexe sinon 0, 5 à 2 nm • Photomultiplicateur: Permet de compter les photons transmis • Amplificateur + calculateur

La quantification • Étalonnage externe (ajouts dosés) • Flamme: Mesure en continu à flux constant…. . Permet de minimiser les fluctuations de la flamme • Pb des interférences (chimiques, spectrales…) • Utilisation de modificateurs La. Cl 3, HNO 3. . • Réalisation de dilutions • Sensibilités: Flamme # ppm Four # ppb

Exemples d’Applications • Sols, Sédiments NF X 31 -151 - Calcination à 450°C Solubilisation (HF, HCLO 4) Evaporation et mise à sec eau régal(HCl/HNO 3) • Dosage par absorption atomique Co, Cr, Cu, Mn, Ni, Pb, Zn) - - - Reprise (Cd,

Eaux : Dosage du Hg par SAA sans flamme NF T 90 -113 • Minéralisation de l’échantillon par KMn. O 4 et K 2 S 2 O 8 à 95°C • Réduction par Sn. Cl 2 Obtention de Hg° • Entraînement sous argon • Mesure à 253, 7 nm Cuve à fenêtre • Limite de dosage 0, 5 µg/l

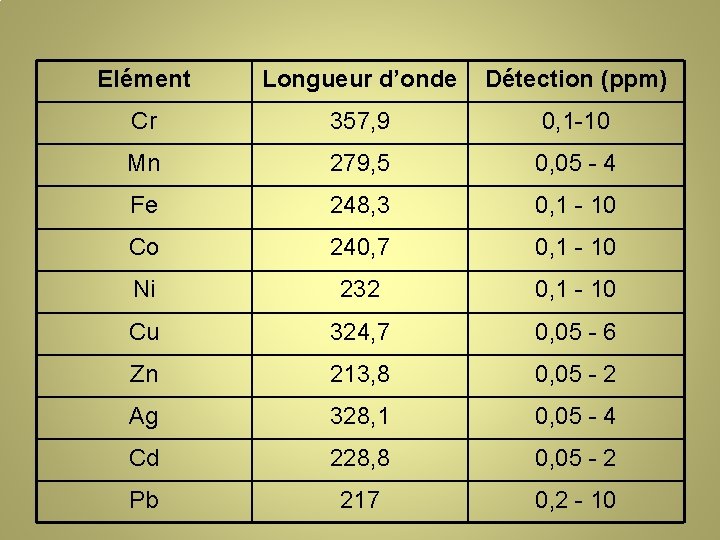
Eaux: Dosage de dix éléments métalliques (directe et indirecte) • NF T 90 -112 (Cr, Mn, Fe, Co, Ni, Cu, Zn, Ag, Cd et Pb) • Flammes air / acétylène - Oxydantes Fe, Ni, Cu, Mn - Réductrices Cr - Normales Co, Zn, Ar, Cd et Pb • Ex du plomb: 283, 3 nm et/ou 217 nm • Dosage direct

Elément Longueur d’onde Détection (ppm) Cr 357, 9 0, 1 -10 Mn 279, 5 0, 05 - 4 Fe 248, 3 0, 1 - 10 Co 240, 7 0, 1 - 10 Ni 232 0, 1 - 10 Cu 324, 7 0, 05 - 6 Zn 213, 8 0, 05 - 2 Ag 328, 1 0, 05 - 4 Cd 228, 8 0, 05 - 2 Pb 217 0, 2 - 10

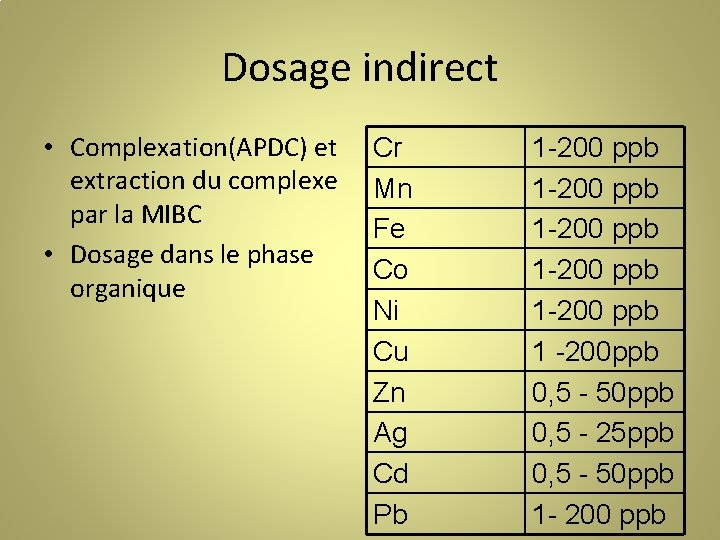
Dosage indirect • Complexation(APDC) et extraction du complexe par la MIBC • Dosage dans le phase organique Cr Mn Fe Co Ni Cu Zn Ag Cd Pb 1 -200 ppb 1 -200 ppb 1 -200 ppb 0, 5 - 50 ppb 0, 5 - 25 ppb 0, 5 - 50 ppb 1 - 200 ppb