Correction de lexercice dapplication Larbre de Diane Travail

Correction de l’exercice d’application L’arbre de Diane

Travail préalable à effectuer : Dans 500 m. L d’une solution de nitrate d’argent (Ag+(aq) + NO 3‑(aq)), de concentration c 0 = 0, 10 mol. L ‑ 1, on plonge un fil de cuivre Cu(s) dont la masse est égale à 10 g. Données : M(Cu) = 63, 5 g. mol-1 M(Ag) = 107, 9 g. mol-1 Lire l’énoncé en totalité Surligner les données

Attribuer à chaque valeur numérique une notation: • • • V = 500 m. L c 0 = 0, 10 mol. L‑ 1 m(Cu) = 10 g M(Cu) =63, 5 g. mol-1 M(Ag) = 107, 9 g. mol-1

1: Compléter l’équation modélisant la transformation chimique avec les nombres stœchiométriques convenables. Justifier le choix. 2 Ag+(aq) + Cu(s) → Cu 2+(aq) + Ag 2 (s) Ces nombres stoechiométriques sont nécessaires afin de respecter les lois de conservation (quantité de matière et charge) 0, 5

2: Les ions nitrate n’interviennent pas dans la transformation chimique : ce sont des ions spectateurs, ils n’apparaissent pas dans l’équation chimique. 1
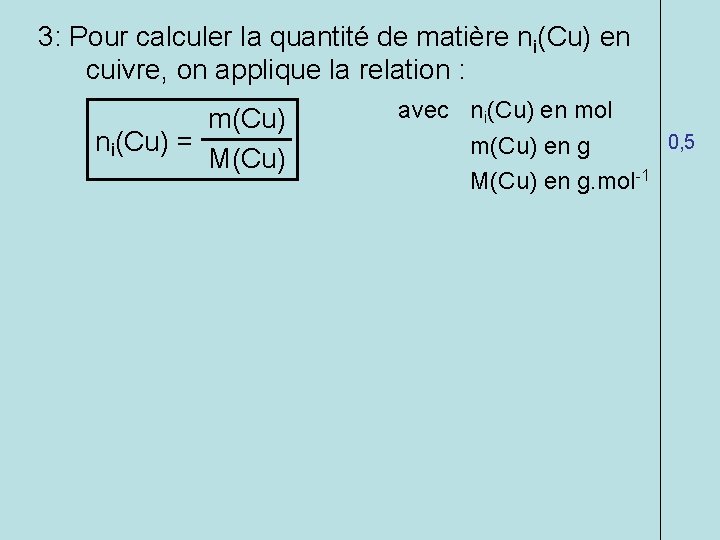
3: Pour calculer la quantité de matière ni(Cu) en cuivre, on applique la relation : m(Cu) ni(Cu) = M(Cu) avec ni(Cu) en mol 0, 5 m(Cu) en g M(Cu) en g. mol-1 4: On fait l’application numérique: 10 ni(Cu) = 63, 5 ni(Cu) = 0, 16 mol 0, 5

5: La concentration molaire (en mol. L-1) d’une espèce chimique dans une solution est la quantité de matière (en mol) de cette espèce chimique par unité de volume (en L) de la solution. 1

6: Expression de la quantité de matière en ions argent : ni(Ag+) = c 0. V avec ni(Ag+) en mol c 0 en mol. L‑ 1 V en L 0, 5

Pour calculer la quantité de matière initiale en ions argent Ag+, il faut convertir V en L : V = 0, 500 L 0, 5 On fait l’application numérique: ni(Ag+) = 0, 10 0, 500 ni(Ag+) = 5, 0 10 -2 mol 0, 5
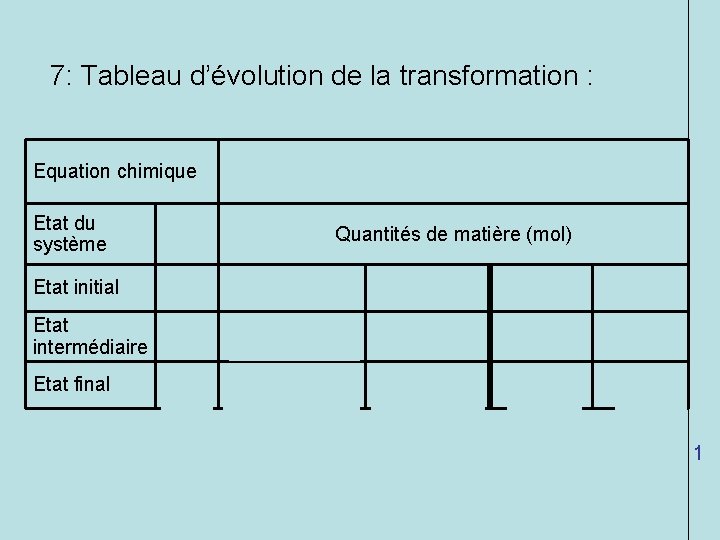
7: Tableau d’évolution de la transformation : Equation chimique 2 Ag+(aq) + Cu(s) → Cu 2+(aq)+ 2 Ag(s) Etat du système Etat initial Etat intermédiaire Etat final Quantités de matière (mol) xi = 0 ni(Ag+) ni(Cu) 0 0 x ni(Ag+) – 2 x ni(Cu) - x x 2 x xmax 2 xmax ni(Ag+) – 2 xmax ni(Cu) - xmax 1

8: A l’état final, un des deux réactifs est consommé, on a donc : 0, 5 Si l’ion argent est limitant: OU Si le cuivre est limitant: ni(Ag+) – 2 xmax = 0 n (Cu) – x = 0 i ni(Ag+) xmax = 2 xmax = 2, 5× 10 -2 mol max xmax = ni(Cu) xmax = 0, 16 mol 0, 5 Or le réactif limitant correspond au xmax le plus petit donc le réactif limitant est l’ion argent Ag+. 0, 5

9: D’après le tableau d’évolution, la quantité de matière en argent Ag à l’état final vaut: nf(Ag) = 2. xmax n f(Ag) = 2 × 2, 5 × 10 -2 f(Ag) = 5, 0 × 10 -2 mol n De plus, la masse d’argent Ag est donnée par la relation : mf(Ag) = n(Ag). M(Ag) 0, 5 mf(Ag) = 5, 0 × 10 -2 × 107, 9 mf(Ag) = 5, 4 g 0, 5

- Slides: 13