HIDROXIZI Definiie Clasificare Denumire HIDROXIZII BAZELE sunt compui

HIDROXIZI
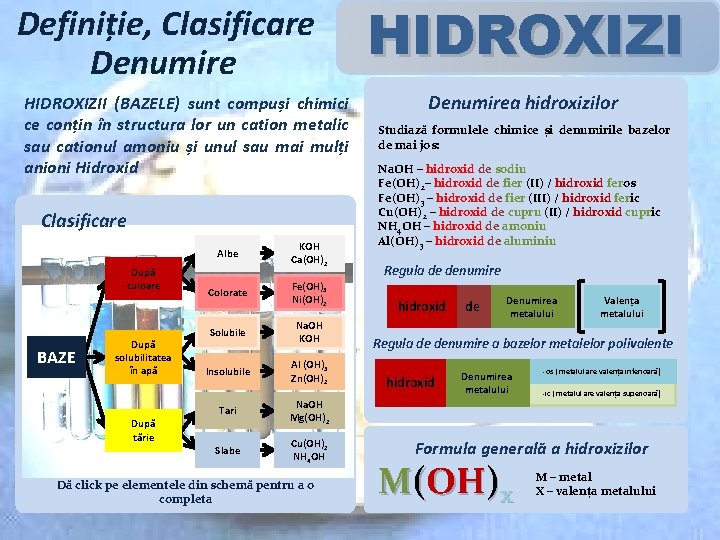
Definiție, Clasificare Denumire HIDROXIZII (BAZELE) sunt compuși chimici ce conțin în structura lor un cation metalic sau cationul amoniu și unul sau mai mulți anioni Hidroxid Clasificare Albe După culoare BAZE După solubilitatea în apă După tărie KOH Ca(OH)2 Colorate Fe(OH)3 Ni(OH)2 Solubile Na. OH KOH Insolubile Al (OH)3 Zn(OH)2 Tari Na. OH Mg(OH)2 Slabe Cu(OH)2 NH 4 OH Dă click pe elementele din schemă pentru a o completa HIDROXIZI Denumirea hidroxizilor Studiază formulele chimice și denumirile bazelor de mai jos: Na. OH – hidroxid de sodiu Fe(OH)2– hidroxid de fier (II) / hidroxid feros Fe(OH)3 – hidroxid de fier (III) / hidroxid feric Cu(OH)2 – hidroxid de cupru (II) / hidroxid cupric NH 4 OH – hidroxid de amoniu Al(OH)3 – hidroxid de aluminiu Regula de denumire hidroxid de Denumirea metalului Valența metalului Regula de denumire a bazelor metalelor polivalente hidroxid Denumirea metalului -os ( metalul are valența inferioară) -ic ( metalul are valența superioară) Formula generală a hidroxizilor M(OH)x M – metal X – valența metalului
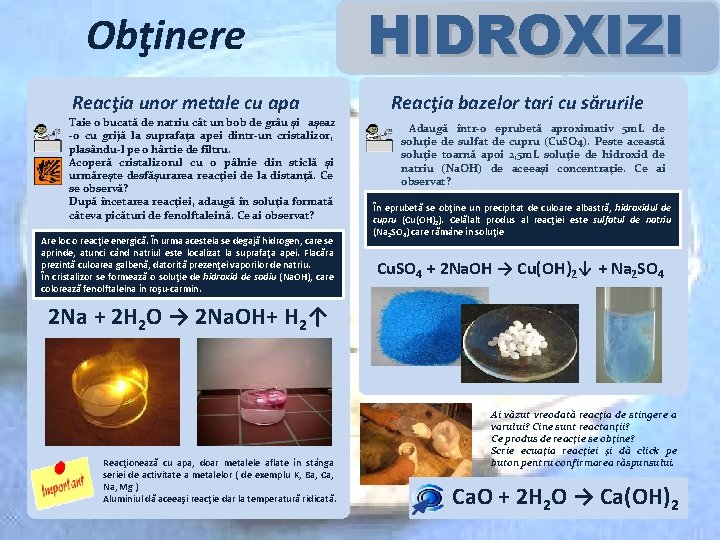
Obţinere Reacţia unor metale cu apa Taie o bucată de natriu cât un bob de grâu şi aşeaz -o cu grijă la suprafaţa apei dintr-un cristalizor, plasându-l pe o hârtie de filtru. Acoperă cristalizorul cu o pâlnie din sticlă şi urmăreşte desfăşurarea reacţiei de la distanţă. Ce se observă? După încetarea reacţiei, adaugă în soluţia formată câteva picături de fenolftaleină. Ce ai observat? Are loc o reacţie energică. În urma acesteia se degajă hidrogen, care se aprinde, atunci când natriul este localizat la suprafaţa apei. Flacăra prezintă culoarea galbenă, datorită prezenţei vaporilor de natriu. În cristalizor se formează o soluţie de hidroxid de sodiu (Na. OH), care colorează fenolftaleina în roşu-carmin. HIDROXIZI Reacţia bazelor tari cu sărurile Adaugă într-o eprubetă aproximativ 5 m. L de soluţie de sulfat de cupru (Cu. SO 4). Peste această soluţie toarnă apoi 2, 5 m. L soluţie de hidroxid de natriu (Na. OH) de aceeaşi concentraţie. Ce ai observat? În eprubetă se obţine un precipitat de culoare albastră, hidroxidul de cupru (Cu(OH)2). Celălalt produs al reacţiei este sulfatul de natriu (Na 2 SO 4) care rămâne în soluţie Cu. SO 4 + 2 Na. OH → Cu(OH)2↓ + Na 2 SO 4 2 Na + 2 H 2 O → 2 Na. OH+ H 2↑ Reacţionează cu apa, doar metalele aflate în stânga seriei de activitate a metalelor ( de exemplu K, Ba, Ca, Na, Mg ) Aluminiul dă aceeaşi reacţie dar la temperatură ridicată. Ai văzut vreodată reacţia de stingere a varului? Cine sunt reactanţii? Ce produs de reacţie se obţine? Scrie ecuaţia reacţiei şi dă click pe buton pentru confirmarea răspunsului. Ca. O + 2 H 2 O → Ca(OH)2

Proprietăți fizice Proprietăți chimice HIDROXIZI Proprietăți fizice q Sunt substanțe solide; q Culoarea bazelor poate fi: • albă (Na. OH, KOH, Ca(OH)2, Mg(OH)2); • colorată (Cu(OH)2 – albastru, Ni(OH)2 – verde, Fe(OH)3 – roșubrun); q Solubilitatea în apă este diferită: • bazele metalelor alcaline sunt ușor solubile; • bazele metalelor alcalino-pământoase sunt greu solubile; • bazele metalelor din grupele III – VIA şi ale metalelor tranziţionale sunt insolubile; q Soluţiile bazelor solubile sunt lunecoase la pipăit şi au acţiune distrugătoare asupra pielii (sunt caustice); q Soluţiile bazelor sunt bune conducătoare de electricitate (electroliţi). Acţiunea asupra indicatorilor Turnaţi soluţii de Na. OH şi Ca(OH)2 în două eprubete diferite. Adăugaţi în fiecare eprubetă 2 – 3 picături de turnesol. Ce observaţi? Repetaţi experimentul folosind soluţii de metiloranj şi fenolftaleină. TURNESOL METILORANJ FENOLFTALEINĂ Comportamentul indicatorilor în mediu bazic Hidroxizii colorează în albastru soluţia de turnesol, în galben pe cea de metiloranj şi în roşu – carmin pe cea de fenolftaleină

Proprietăți chimice Reacția bazelor cu oxizii acizi Introdu o soluție limpede de apă de var diluată, și adaugă apoi 3 – 4 picături de fenolftaleină. Apoi, suflă cu ajutorul unui pai în soluția obținută. Ce observi după un timp? Soluția de culoare roșie se decolorează, semn că hidroxidul de calciu a reacționat cu dioxidul de carbon din aerul expirat. Se obține carbonat de calciu, care se lasă la fundul paharului și apă. Ca(OH)2 + CO 2→Ca. CO 3↓ + H 2 O Reacția cu acizii (neutralizarea) A. Pune într-o capsulă 2 cm 3 de soluție de Na. OH și 2 cm 3 soluție de HCl. Încălzește până la evaporarea completă a apei. B. Filtrează conținutul fiecărei eprubete de la experimentul anterior. În 3 eprubete diferite, tratează precipitatele obținute cu soluție de HCl. A. După evaporarea completă a apei, rămân cristale de clorură de natriu. B. Și bazele insolubile reacționează cu acizii formând săruri solubile. Na. OH + HCl → Na. Cl + H 2 O Fe(OH)3 + 3 HCl → Fe. Cl 3 + 3 H 2 O Cu(OH)2+ 2 HCl → Cu. Cl 2 + 2 H 2 O Al(OH)3 + 3 HCl → Al. Cl 3 + 3 H 2 O HIDROXIZI Reacția bazelor cu sărurile solubile În trei eprubete ce conțin hidroxid de natriu, adaugă clorură ferică(Fe. Cl 3), sulfat de cupru (Cu. SO 4) și clorură de aluminiu (Al. Cl 3). Ce observi? Păstrează produșii obținuți pentru experimentul următor. În cele trei eprubete se obțin trei precipitate de culori diferite. Acestea sunt baze insolubile Fe. Cl 3 + 3 Na. OH →Fe(OH)3↓ + 3 Na. Cl Cu. SO 4+ 2 Na. OH →Cu(OH)2↓ + Na 2 SO 4 Al. Cl 3 + 3 Na. OH →Al(OH)3↓ + 3 Na. Cl Bazele reacționează cu unele săruri solubile, rezultând baze insolubile și săruri noi Descompunerea unor baze insolubile Încălzește puternic hidroxid de cupru (Cu(OH)2) într-o eprubetă. Ce se întâmplă? Hidroxidul de cupru de culoare albastră trece în oxid de cupru, de culoare neagră și vapori de apă. Cu(OH)2 →Cu. O + H 2 O
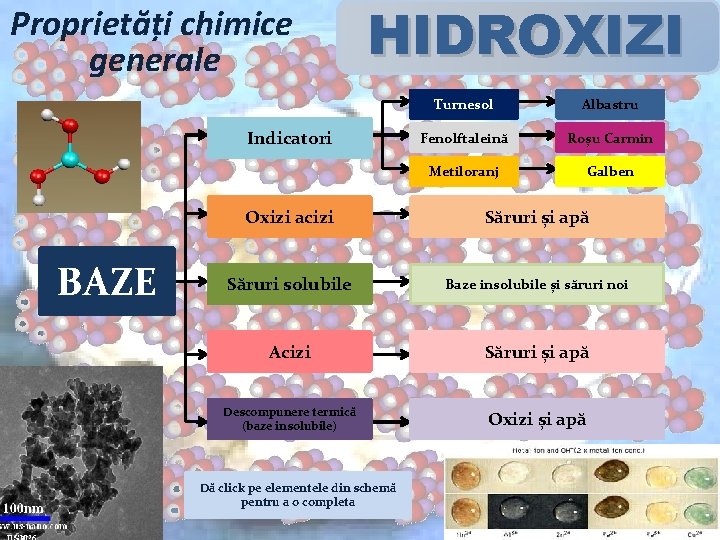
Proprietăți chimice generale HIDROXIZI Indicatori BAZE Turnesol Albastru Fenolftaleină Roșu Carmin Metiloranj Galben Oxizi acizi Săruri și apă Săruri solubile Baze insolubile și săruri noi Acizi Săruri și apă Descompunere termică (baze insolubile) Oxizi și apă Dă click pe elementele din schemă pentru a o completa

HIDROXIZI Utilizări Reactiv Obținerea săpunului Na. OH Sodă de rufe Mortar de var Rafinarea zahărului Ca(OH)2 Detergenți Mătase artificială Rafinarea petrolului Stropirea viței de vie Recunoașterea CO 2 KOH Văruirea caselor Săpun lichid Reactiv Uscarea gazelor Decapanți Dezinfectarea pomilor Pentru corectarea acidităţii aluatului pentru produsele de patiserie se foloseşte hidroxidul de sodiu (Na. OH).

HIDROXIZI Rebus 1 3 T D U I R N 2 O X E M I VERTICAL 10 9 4 V 6 5 C 7 S 8 M 11 D E N E T I 12 S O D A C A U S T I C A O R E R U L L A E L H M T C P C F R R O E O A A R I R U U L R B U G R L N R E A I I N N U O T N I J 1. Indicator care în mediu bazic devine albastru; 2. Material pentru construcții la care se utilizează hidroxidul de calciu; 3. Gaz incolor care tulbură apa de var (3 cuvinte); 4. Are formula chimică Ca. O; 5. Metal tranzițional, al cărui hidroxid prezintă culoarea albastră; 6. Metal component al varului stins; 7. Nemetal de culoare galbenă care reacționează cu hidroxizii alcalini; 8. Rezultă la reacția bazelor cu acizii; 9. Una dintre utilizările hidroxidului de sodiu; 10. Indicator care în mediu alcalin devine galben; 11. Metal tranzițional cu Z = 28; 12. Radical care intră în componența singurei baze ce nu conține cationi metalici. ORIZONTAL Denumirea tehnică a hidroxidului de sodiu ( 2 cuvinte).

HIDROXIZI Descoperă Răspunde în ordine la cele 12 întrebări și descoperă numele unui important chimist român și domeniile lui de activitate. Fiecare întrebare și variantele de răspuns se vor deschide, atunci când apăsați butonul corespunzător. Atenție! Aplicația nu funcționează corespunzător dacă răspundeți aleatoriu la întrebări! Întrebări 1 2 3 4 5 6 7 8 9 10 11 12 Întrebarea 11: Întrebarea 8: 3: Întrebarea 12: 10: 1: 2: 4: 5: 6: 7: 9: Într-un cristalizor cu 200 g apă se introduc 4 g Na. OH Sereacționează numește și potasă cu 3, 65 g. HCl. caustică: Culoarea 4, 6 g Na metalic. Concentrația soluției Culoarea Procentul Se Formula În. Nu reacțiile folosește Nu este fenolftaleinei rezultă Nu de generală utilizare de se Kla Sunt din dizolvă neutralizare obținerea baze potasa abaze: a hidroxizilor în sodei din înmediu apă: reacția: caustică mortarului: caustice: participă: bazic este: metiloranjului în soluția finală este: obținute este: a)Ca(OH) a) a)Ca(OH) Văruirea şi a)Acizii oxizii a) Nușise 22 cu a)portocaliu a) a)56, 00% CORECT! a) GRESIT! a) Cu(OH) Na. OH M roșie O 2 x formează soluție bazici 43 2 Al(OH) caselor Cu. SO b)b)Bazele b)CO Obținerea și 2 cu b) Ca. O b)roșu și HCl b) b)Ca(OH) b) b)69, 64% CORECT! GRESIT! b) galbenă M(OH) NH 3, 6% OH 4 2 x oxizii acizi săpunului Ca(OH) 2 c)c)c)Rafinarea Na. OH Acizii șiși c)Ca c)galben cu 37% H c)Mg(OH) c) c)Al(OH) c)39, 01% c) CORECT! GRESIT! c) albastră 2, M KOH EO bazele petrolului Ca. Oy x 2 32 N I C O L A T E C L U E Domeniile care au fost studiate de el includ: - Studii de rezistenţă a hârtiei şi a fibrelor lemnoase - Pigmenţi minerali - Uleiuri utilizate în pictură - Combustia gazelor Tot lui îi aparţin o serie de aparate de laborator păstrate în prezent la Universitatea din Bucureşti. Cele mai importante sunt apatatul pentru detectarea metanului si un altul pentru prepararea ozonului. A analizat chimia unui meteorit găsit în 1870 la Goalpara, India.
VĂ MULŢUMESC! BIBLIOGRAFIE: 1. Constantinescu, R. , Râpă, M. ”Chimie – manual pentru clasa a VIII-a”, Editura Sigma, București, 2000 2. Gheorghiu, C. , Panait, C. , ”Chimie – manual pentru clasa a VIII-a”, Editura Didactică și Pedagogică, București, 1995 3. Fătu, S. Stroe, F. , Stroe, C. ”Chimie – manual pentru clasa a VIII-a”, Editura Corint, București 4. Viu, F. , ”Pe urmele chimistului necunoscut”, Aplicaţie Powerpoint, www. didactic. ro, martie 2012. La realizarea materialului s-au folosit imagini de pe site-urile: www. visualphotos. com, www. public. asm. edu, www. imc. bme. hu, www. tulane. edu, www. dwb. unl. edu, www. wikipedia. org, www. sciencephoto. com, www. financiarul. ro, www. uups. ro, www. allex. ro, www. clever. ro, www. romchim. ro, www. bucataria. realitatea. net, www. muzeeinaerliber. ro, www. armaxgaz. infoconstruct. ro, www. vet_magazin. ro, www. hhoinfusion. com, www. faxmedia. ro Realizat de prof. Florin Viu Școala Gimnazială ”Ion Lovinescu” Rădășeni Noiembrie 2012
- Slides: 10