Colegio Andrs Bello Chiguayante IV UNIDAD QUMICA ORGNICA

Colegio Andrés Bello Chiguayante IV UNIDAD: QUÍMICA ORGÁNICA CAP 1: PROPIEDADES DEL CARBONO Jorge Pacheco R. Profesor de Biología y Química

QUÍMICA ORGÁNICA APRENDIZAJES ESPERADOS: • Identifican las características y propiedades del carbono que permiten la formación de una amplia variedad de moléculas. • Clasifican los hidrocarburos según el tipo de estructura que presentan. • Aplican las reglas de nomenclatura orgánica para nombrar y construir moléculas.

RECOMENDACIONES • ¡NO TE QUEDES ATRÁS! El curso avanza y es complejo ponerse al día. • ¡EJERCITA LOS PROBLEMAS! Todo el mundo necesita practicar y la resolución de los problemas te mostrará aspectos que necesites trabajar más. Ver vídeo
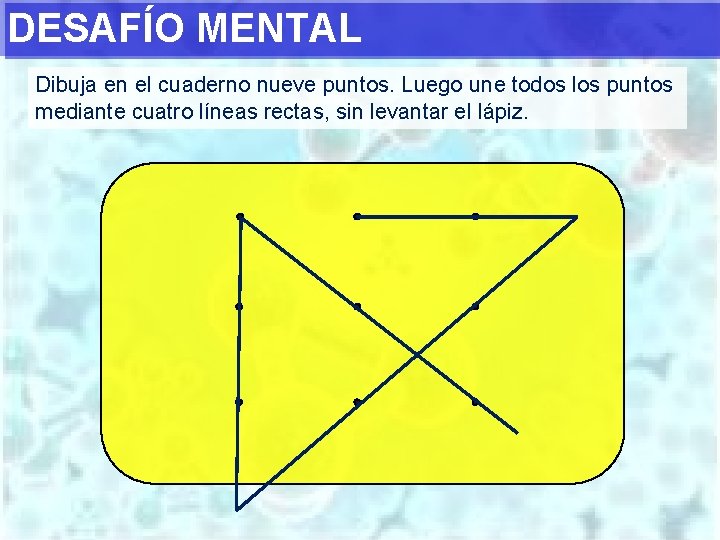
DESAFÍO MENTAL Dibuja en el cuaderno nueve puntos. Luego une todos los puntos mediante cuatro líneas rectas, sin levantar el lápiz.

PREGUNTAS PREVIAS • ¿Cuál es la configuración electrónica del Carbono (Z=6)? 2 2 2 1 s 2 s 2 p

PREGUNTAS PREVIAS • ¿Cuál es el período y familia del Carbono? 1 s 2 2 p 2 Período = 2 Familia = IV A

PREGUNTAS PREVIAS • ¿Cuál es la Estructura de Lewis del metano (CH 4) (C Z=6; H Z=1)? C Z= 6: 1 s 22 p 2 H Z= 1: 1 s 1 4 e x 1=4 1 e x 4=4 Total = 8 e H H C H H
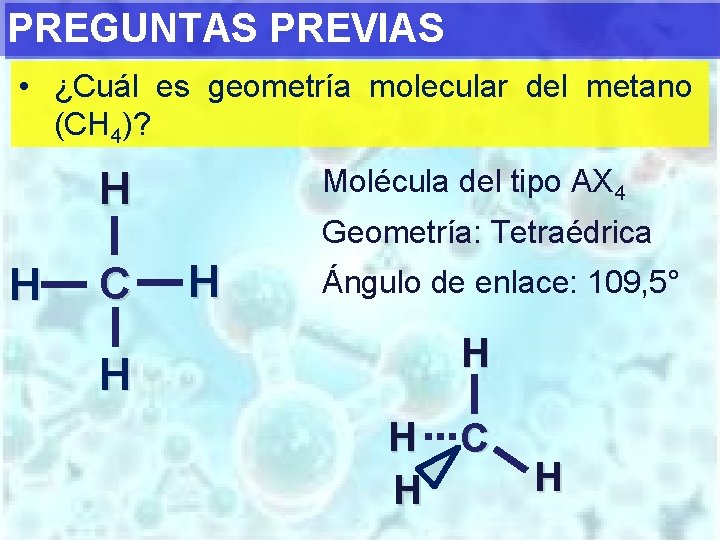
PREGUNTAS PREVIAS • ¿Cuál es geometría molecular del metano (CH 4)? Molécula del tipo AX 4 H H C H Geometría: Tetraédrica H Ángulo de enlace: 109, 5° H H C H H
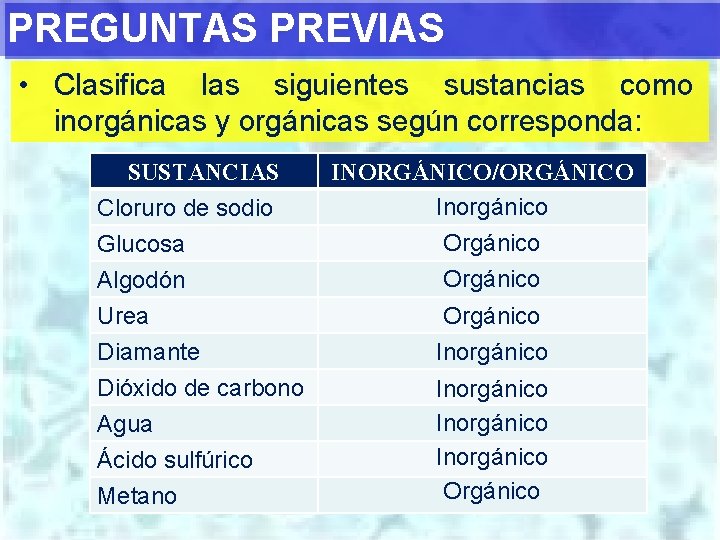
PREGUNTAS PREVIAS • Clasifica las siguientes sustancias como inorgánicas y orgánicas según corresponda: SUSTANCIAS Cloruro de sodio Glucosa Algodón Urea Diamante Dióxido de carbono Agua Ácido sulfúrico Metano INORGÁNICO/ORGÁNICO Inorgánico Orgánico Inorgánico Orgánico

PREGUNTAS PREVIAS • ¿Cuáles son los tipos de enlaces químicos? • Enlace Iónico • Enlace Covalente: Apolar, Polar y Dativo. • Enlace Metálico

PREGUNTAS PREVIAS • Nombra al menos tres fuerzas intermoleculares: • Puente de Hidrógeno. • Fuerzas de Van der Waals. • Unión dipolo-dipolo. Ver Vídeo
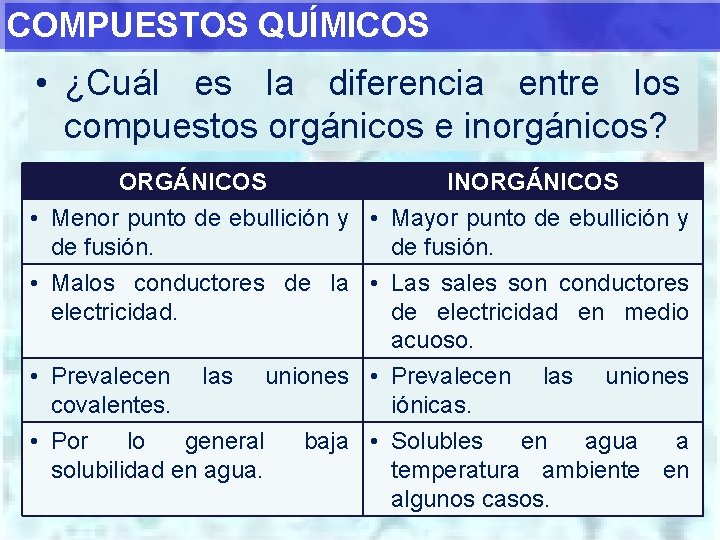
COMPUESTOS QUÍMICOS • ¿Cuál es la diferencia entre los compuestos orgánicos e inorgánicos? ORGÁNICOS INORGÁNICOS • Menor punto de ebullición y • Mayor punto de ebullición y de fusión. • Malos conductores de la • Las sales son conductores electricidad. de electricidad en medio acuoso. • Prevalecen las uniones covalentes. iónicas. • Por lo general baja • Solubles en agua a solubilidad en agua. temperatura ambiente en algunos casos.

¿QUÉ ES LA QUÍMICA ORGÁNICA? • Es una especialidad de la química dedicada al estudio de las estructuras, propiedades y reacciones que involucran a los compuestos que contienen al Carbono como átomo central de su estructura.

ORÍGEN DE LA QUÍMICA ORGÁNICA • Se remontan a los trabajos del químico sueco Jöns Jacob Berzelius, quien en el siglo XVIII postuló la teoría vitalista, que afirmaba que los compuestos orgánicos solo podían ser elaborados o sintetizados por los organismos vivos a través de una misteriosa “fuerza vital” que estos poseían.

APORTES ¿Cuál fue el aporte de Friedrich Wöhler al conocimiento de la química orgánica? Friedrich Wöhler, químico alemán, fue un precursor en el campo de la química orgánica, Wöhler es famoso por su síntesis del compuesto orgánico denominado urea a partir de un compuesto inorgánico conocido como cianato de amonio.

IDEAS GENERALES • Todos los compuestos considerados como orgánicos contienen Carbono. • Todo compuesto que posea carbono no necesariamente es orgánico (Ej. Diamante, grafito, dióxido de carbono) • Los compuestos de Carbono son mucho más numerosos que los compuestos conocidos del resto de los elementos.

ACTIVIDAD: RESPONDER 1. Menciona el(los) principal(es) aporte para el desarrollo de la química orgánica de: A) Friedrich Wöhler: B) Friedrich August Kekulé: 2. ¿Cuáles fueron las ideas del vitalismo?

LAS PROPIEDADES DEL CARBONO Ver Vídeo

PROPIEDADES DEL CARBONO • El Carbono no es abundante en la corteza terrestre (0, 027%) pero representa cerca del 20% en masa en los seres vivos. • Presenta cuatro formas alotrópicas: Grafito, diamante, fullereno y nanotubos de carbono. • El Carbono se une a otros átomos de C, H, O, S, N y P entre otros para formar una gran variedad de compuestos orgánicos diferentes. • El Carbono es tetravalente (posee cuatro electrones de valencia). • El Carbono posee gran capacidad para asociarse consigo mismo formando cadenas y anillos con ramificaciones.
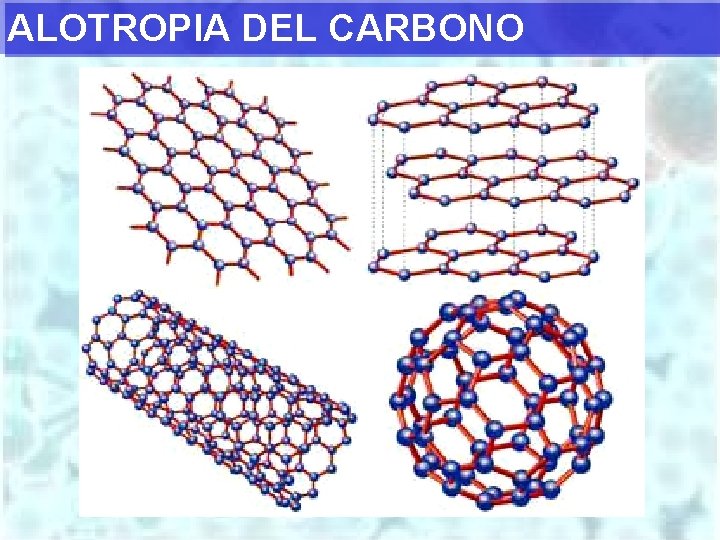
ALOTROPIA DEL CARBONO
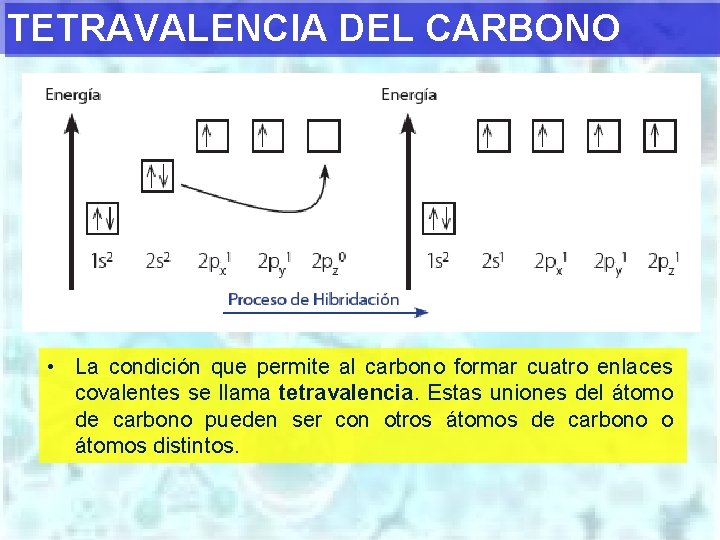
TETRAVALENCIA DEL CARBONO • La condición que permite al carbono formar cuatro enlaces covalentes se llama tetravalencia. Estas uniones del átomo de carbono pueden ser con otros átomos de carbono o átomos distintos.
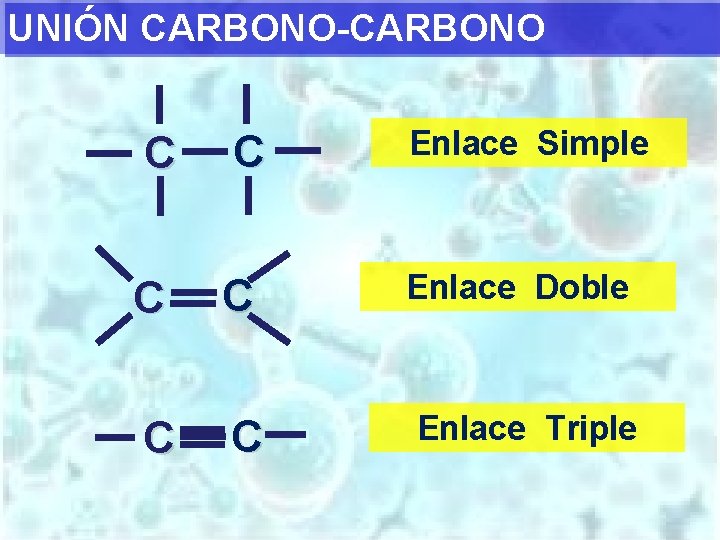
UNIÓN CARBONO-CARBONO Enlace Simple C C Enlace Doble C C Enlace Triple
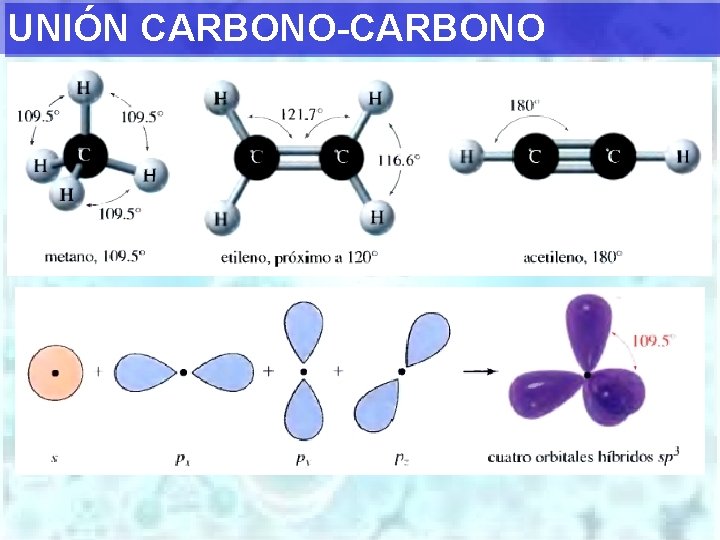
UNIÓN CARBONO-CARBONO
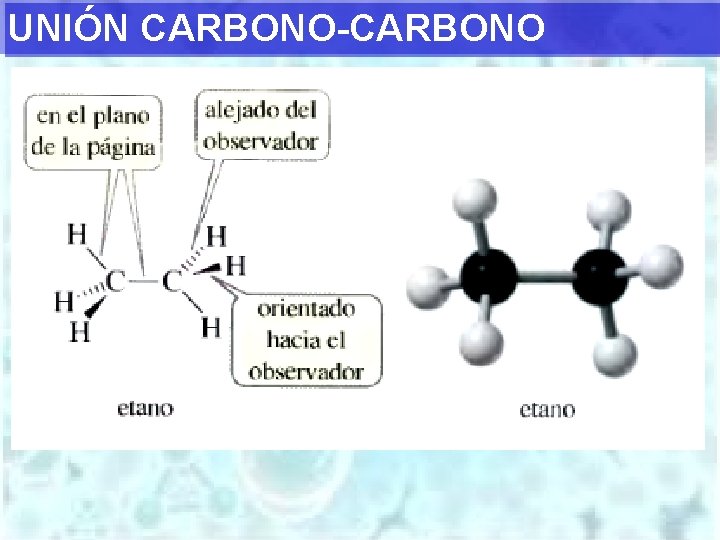
UNIÓN CARBONO-CARBONO
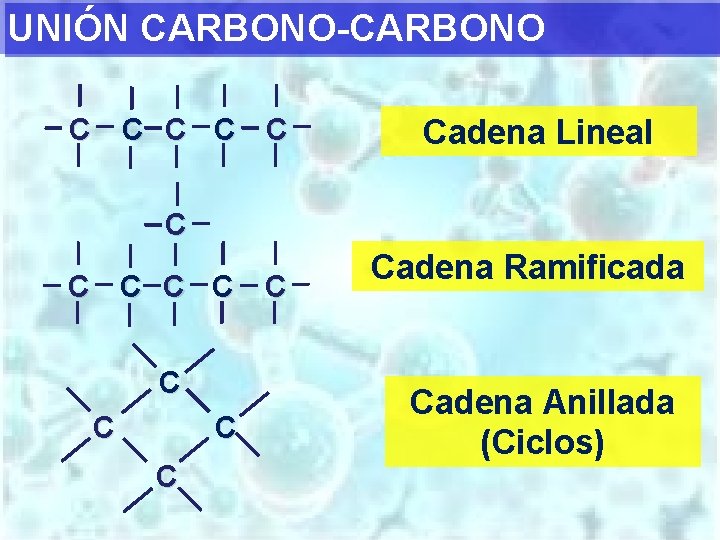
UNIÓN CARBONO-CARBONO C C Cadena Lineal C C Cadena Ramificada Cadena Anillada (Ciclos)

FUENTES DEL CARBONO • Carbono elemental: se presenta en dos tipo de cristales: Grafito y Diamante. • Carbón mineral: Es un mineral negro, que su origen se debe a la descomposición vegetal acumuladas desde épocas prehistóricas. • El Petróleo: Líquido de color generalmente negro, mezcla de hidrocarburos viscoso. • Productos vegetales y animales: síntesis de diversos compuestos orgánicos como el azúcar, almidones, aceites y ceras vegetales, etc.
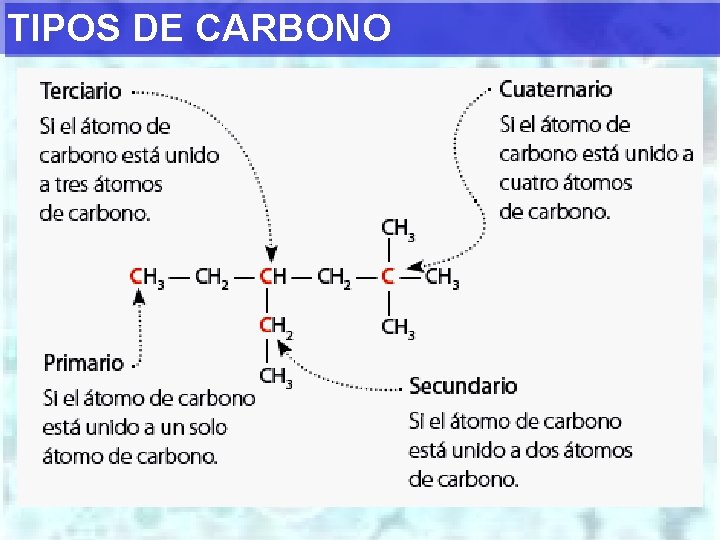
TIPOS DE CARBONO
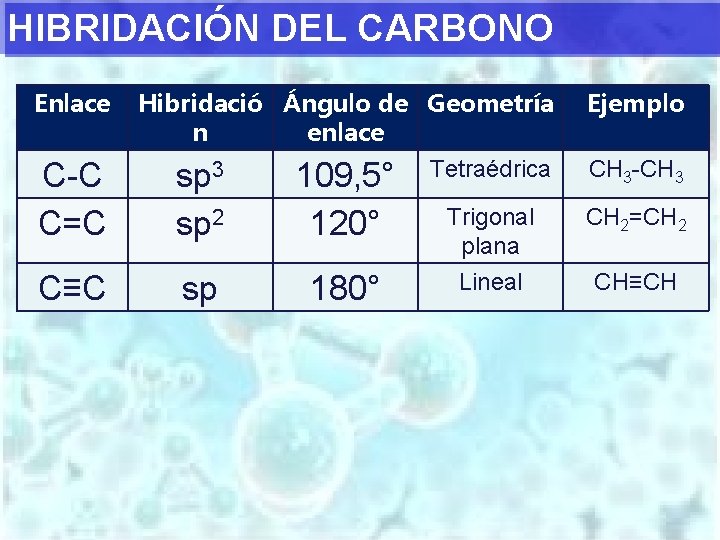
HIBRIDACIÓN DEL CARBONO Enlace Hibridació Ángulo de Geometría n enlace Ejemplo C-C C=C sp 3 sp 2 109, 5° 120° Tetraédrica CH 3 -CH 3 Trigonal plana CH 2=CH 2 C≡C sp 180° Lineal CH≡CH
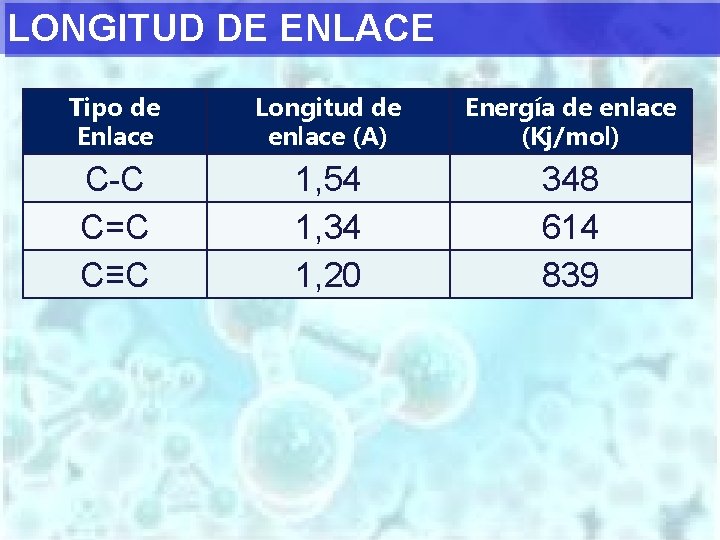
LONGITUD DE ENLACE Tipo de Enlace Longitud de enlace (A) Energía de enlace (Kj/mol) C-C C=C C≡C 1, 54 1, 34 1, 20 348 614 839
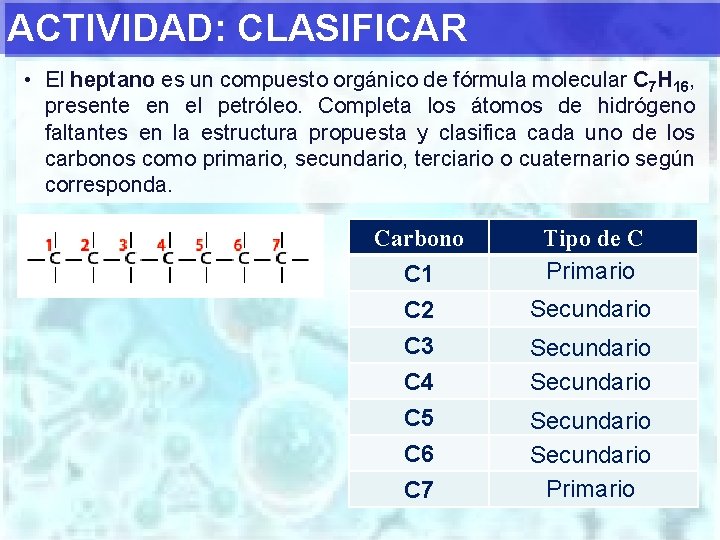
ACTIVIDAD: CLASIFICAR • El heptano es un compuesto orgánico de fórmula molecular C 7 H 16, presente en el petróleo. Completa los átomos de hidrógeno faltantes en la estructura propuesta y clasifica cada uno de los carbonos como primario, secundario, terciario o cuaternario según corresponda. Carbono C 1 C 2 C 3 C 4 C 5 C 6 C 7 Tipo de C Primario Secundario Secundario Primario
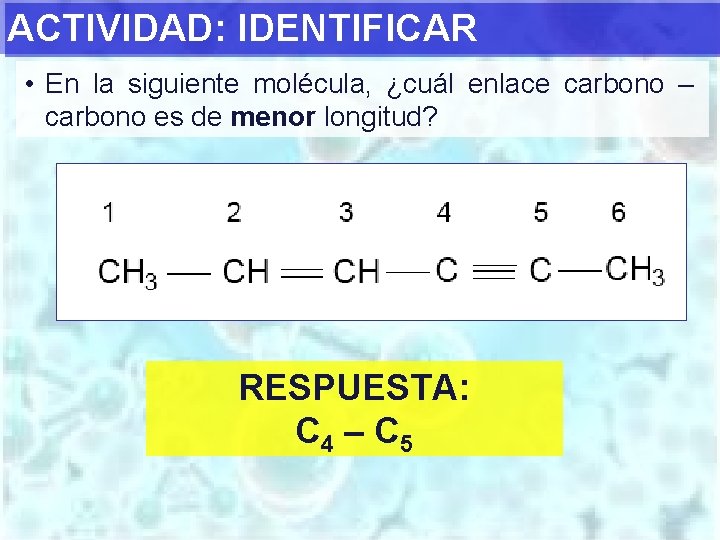
ACTIVIDAD: IDENTIFICAR • En la siguiente molécula, ¿cuál enlace carbono – carbono es de menor longitud? RESPUESTA: C 4 – C 5
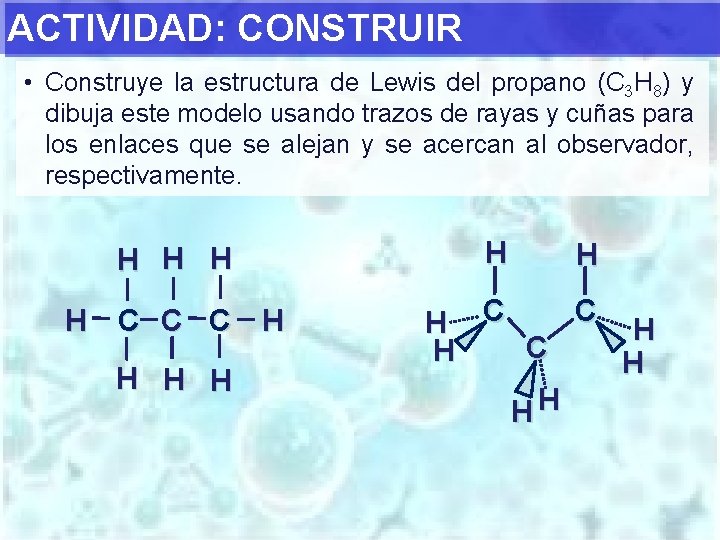
ACTIVIDAD: CONSTRUIR • Construye la estructura de Lewis del propano (C 3 H 8) y dibuja este modelo usando trazos de rayas y cuñas para los enlaces que se alejan y se acercan al observador, respectivamente. H H C C C H H H C H C H H HH

COMPUESTOS ORGÁNICOS • • • Hidrocarburos (C, H). Carbohidratos (C, H, O). Lípidos (C, H, O). Proteínas (C, H, O, N). Ácidos Nucleícos (C, H, O, N, P, S).

LOS HIDROCARBUROS

IDEAS GENERALES • ¿Qué son los Hidrocarburos? • Compuestos orgánicos simples debido a que están formados solo por átomos de carbono e hidrógeno. Los hidrocarburos se agrupan en dos grandes tipos: alifáticos y aromáticos.
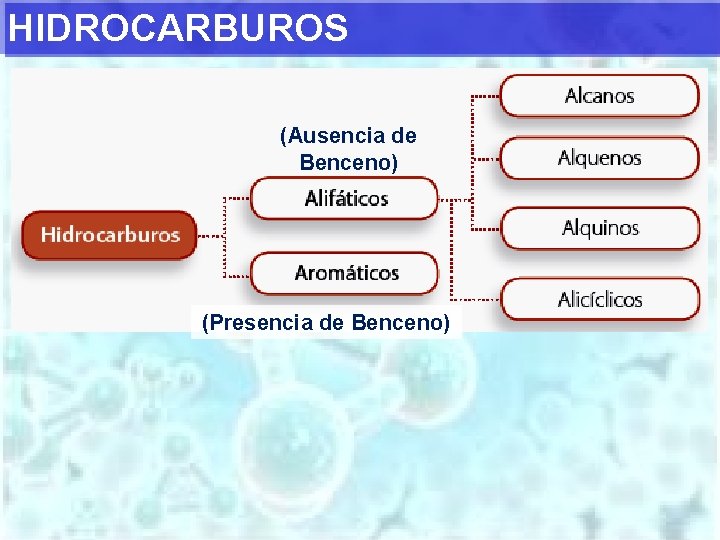
HIDROCARBUROS (Ausencia de Benceno) (Presencia de Benceno)

ALCANOS • Hidrocarburos formados exclusivamente por enlaces simples entre los átomos de carbono. • Poseen la capacidad máxima de unión con átomos de hidrógeno. Debido a esta particularidad, se les denomina hidrocarburos “saturados”. • Los puntos de ebullición y fusión aumentan gradualmente en función de las masas molares.
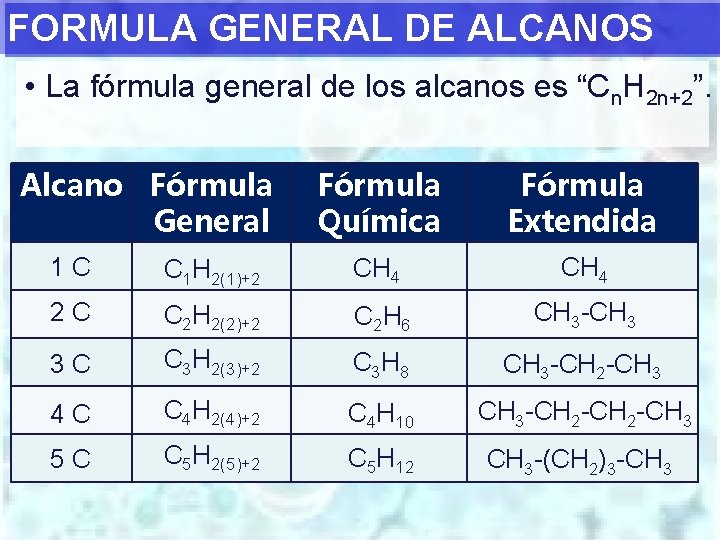
FORMULA GENERAL DE ALCANOS • La fórmula general de los alcanos es “Cn. H 2 n+2”. Alcano Fórmula General Fórmula Química Fórmula Extendida 1 C C 1 H 2(1)+2 CH 4 2 C C 2 H 2(2)+2 C 2 H 6 CH 3 -CH 3 3 C C 3 H 2(3)+2 C 3 H 8 CH 3 -CH 2 -CH 3 4 C C 4 H 2(4)+2 C 4 H 10 CH 3 -CH 2 -CH 3 5 C C 5 H 2(5)+2 C 5 H 12 CH 3 -(CH 2)3 -CH 3
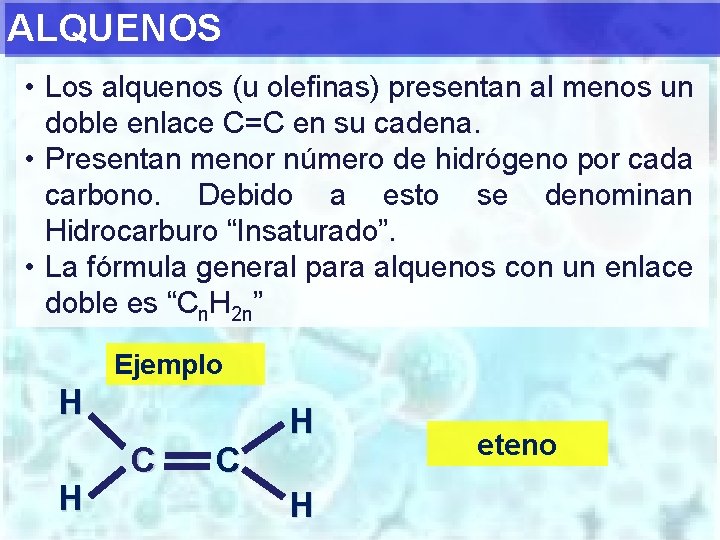
ALQUENOS • Los alquenos (u olefinas) presentan al menos un doble enlace C=C en su cadena. • Presentan menor número de hidrógeno por cada carbono. Debido a esto se denominan Hidrocarburo “Insaturado”. • La fórmula general para alquenos con un enlace doble es “Cn. H 2 n” Ejemplo H H H C C H eteno

ALQUINOS • Los alquinos presentan al menos un triple enlace C≡C en su cadena. • Presentan menor número de hidrógeno por cada carbono. Debido a esto se denominan Hidrocarburo “Insaturado”. • La fórmula general para alquinos con un enlace triple es “Cn. H 2 n-2” Ejemplo H C C H etino
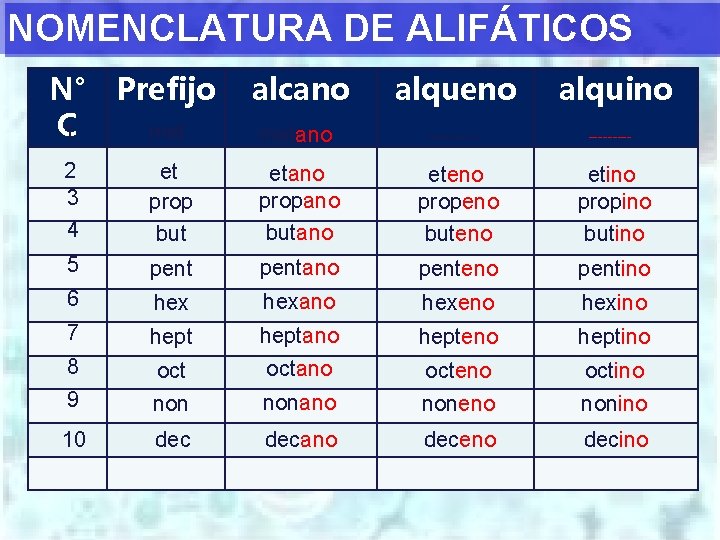
NOMENCLATURA DE ALIFÁTICOS N° Prefijo C 1 met alcano alqueno alquino metano --------- 2 3 4 et prop but etano propano butano eteno propeno buteno etino propino butino 5 pentano penteno pentino 6 hexano hexeno hexino 7 heptano hepteno heptino 8 octano octeno octino 9 nonano noneno nonino 10 decano deceno decino
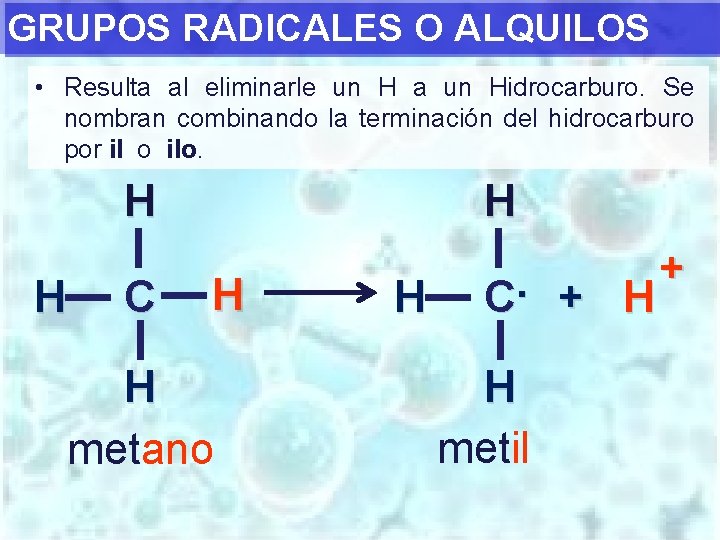
GRUPOS RADICALES O ALQUILOS • Resulta al eliminarle un H a un Hidrocarburo. Se nombran combinando la terminación del hidrocarburo por il o ilo. H H C H H H metano H C. + H H metil +
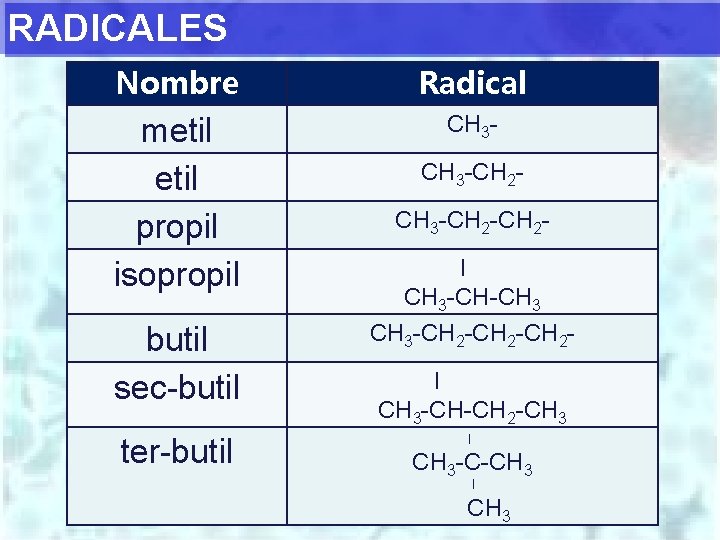
RADICALES Nombre Radical metil propil isopropil CH 3 -CH 2 CH 3 -CH 2 I CH 3 -CH-CH 3 butil sec-butil CH 3 -CH 2 -CH 2 - ter-butil I I CH 3 -CH-CH 2 -CH 3 -C-CH 3 I CH 3

REGLAS IUPAC 1. Para nombrar o construir la estructura de un hidrocarburo dependerá del número de carbonos presentes en la cadena principal y del tipo de enlace existente entre los carbonos. 2. Para cadenas ramificadas se debe identificar la cadena principal, luego enumerar los átomos de carbono. Si en la cadena principal solo existen enlaces simples C—C, la numeración debe considerar la posición más baja de los sustituyentes (grupos radicales). 3. Si la cadena principal posee insaturaciones, la numeración debe privilegiar la posición de los enlaces dobles o triples y, secundariamente, la ubicación de los sustituyentes si es que existen.

REGLAS IUPAC 4. Para nombrar a un hidrocarburo ramificado, se deben escribir los nombres de los sustituyentes en orden alfabético, además de su posición en la cadena principal. Si un mismo sustituyente se repite, debemos utilizar los prefijos di (dos), tri (tres) o tetra (cuatro) según corresponda. 5. La posición de las insaturaciones dentro de la cadena principal también debe ser registrada en el nombre del compuesto.
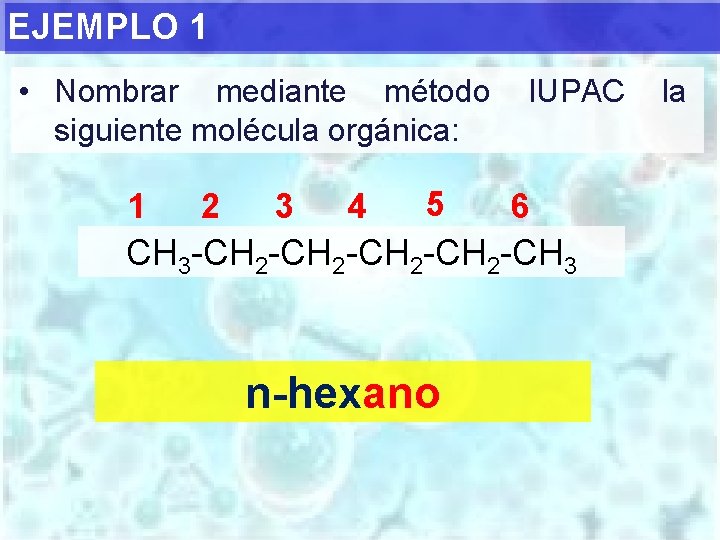
EJEMPLO 1 • Nombrar mediante método siguiente molécula orgánica: 1 2 3 4 5 IUPAC 6 CH 3 -CH 2 -CH 3 n-hexano la
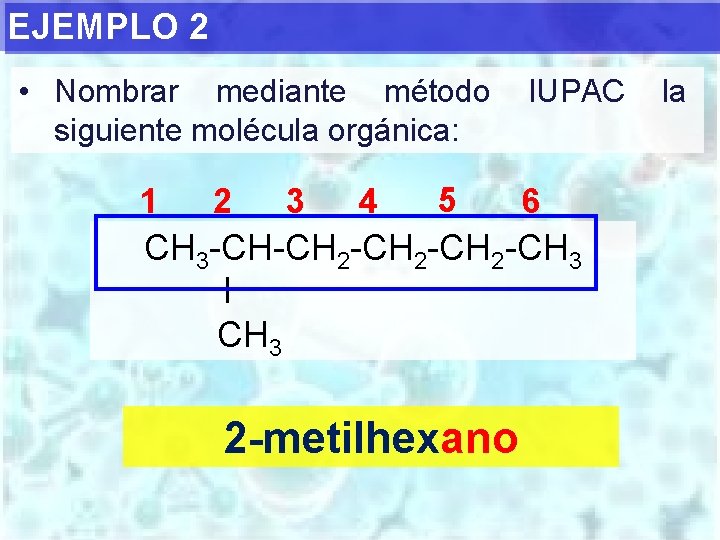
EJEMPLO 2 • Nombrar mediante método siguiente molécula orgánica: 1 2 3 4 5 IUPAC 6 CH 3 -CH-CH 2 -CH 3 I CH 3 2 -metilhexano la
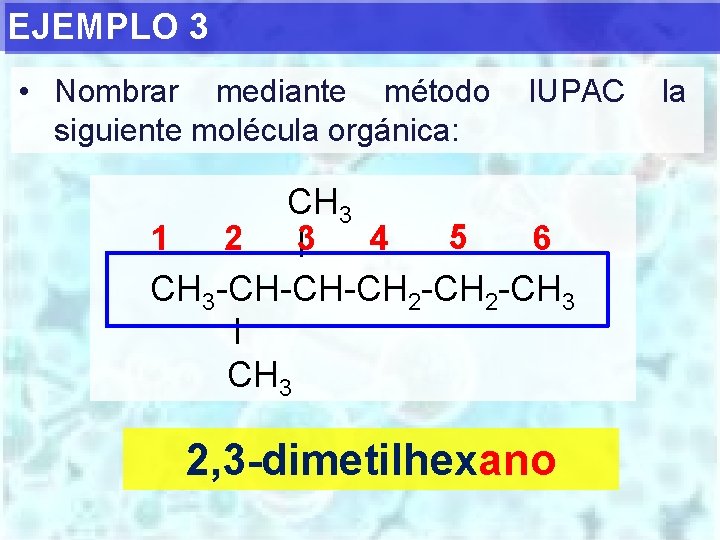
EJEMPLO 3 • Nombrar mediante método siguiente molécula orgánica: IUPAC CH 3 5 1 2 4 6 I 3 CH 3 -CH-CH-CH 2 -CH 3 I CH 3 2, 3 -dimetilhexano la
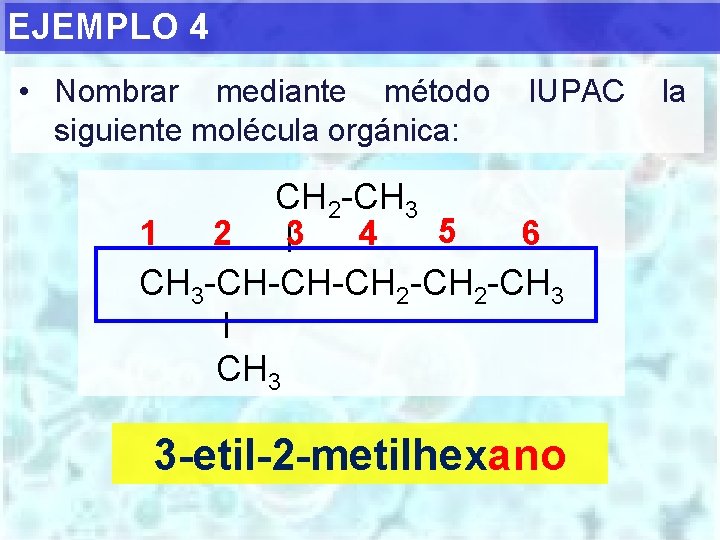
EJEMPLO 4 • Nombrar mediante método siguiente molécula orgánica: IUPAC CH 2 -CH 3 5 1 2 4 6 I 3 CH 3 -CH-CH-CH 2 -CH 3 I CH 3 3 -etil-2 -metilhexano la
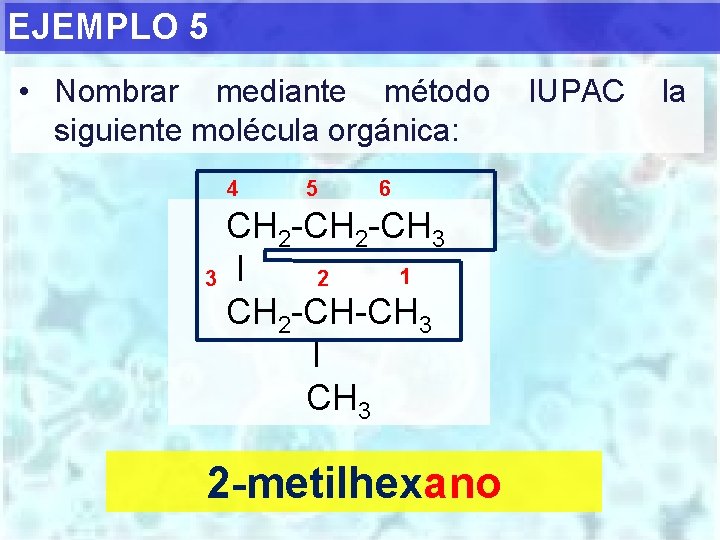
EJEMPLO 5 • Nombrar mediante método siguiente molécula orgánica: 4 5 6 CH 2 -CH 3 1 3 I 2 CH 2 -CH-CH 3 I CH 3 2 -metilhexano IUPAC la
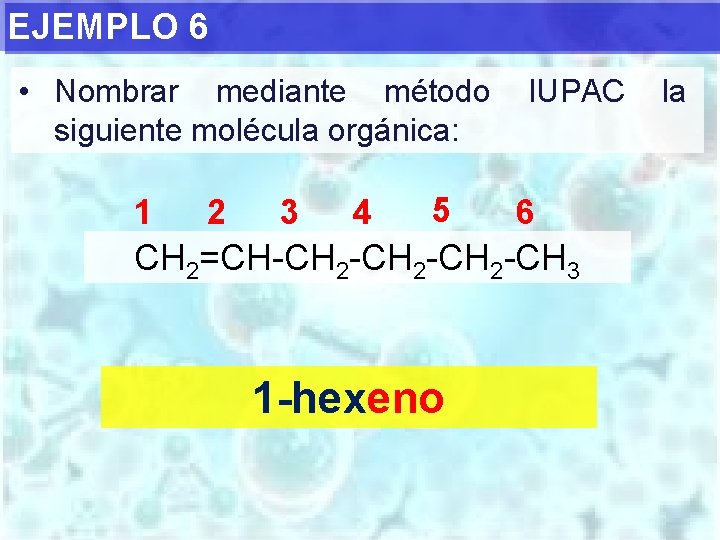
EJEMPLO 6 • Nombrar mediante método siguiente molécula orgánica: 1 2 3 4 5 IUPAC 6 CH 2=CH-CH 2 -CH 3 1 -hexeno la
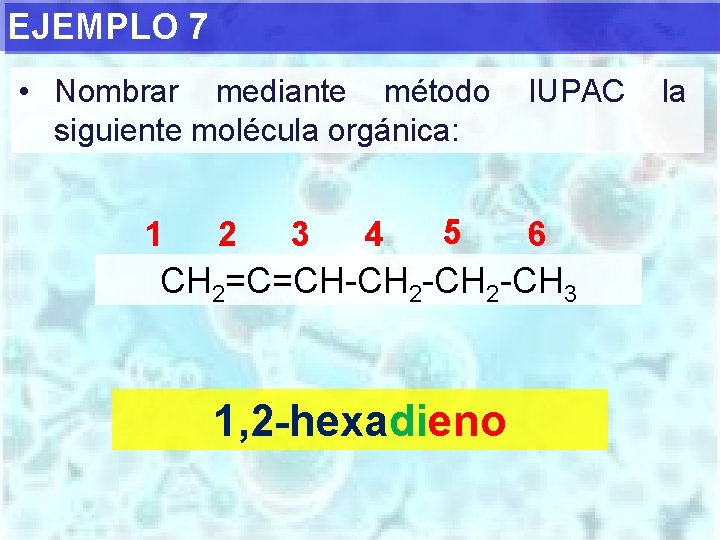
EJEMPLO 7 • Nombrar mediante método siguiente molécula orgánica: 1 2 3 4 5 IUPAC 6 CH 2=C=CH-CH 2 -CH 3 1, 2 -hexadieno la
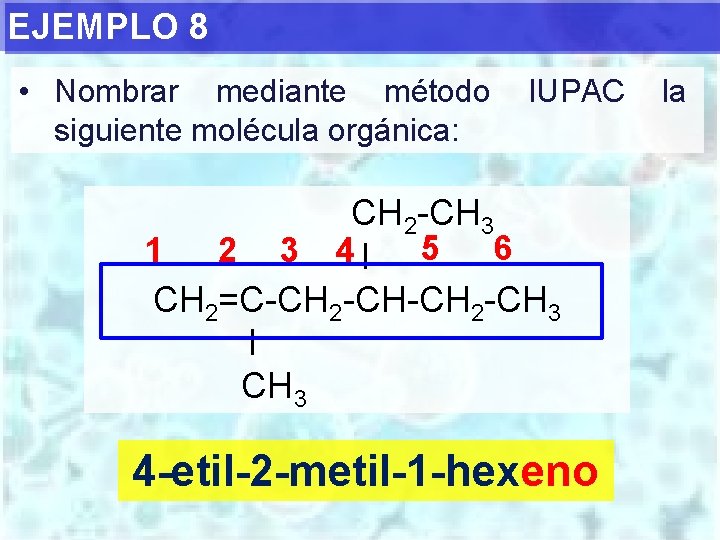
EJEMPLO 8 • Nombrar mediante método siguiente molécula orgánica: IUPAC CH 2 -CH 3 6 1 2 3 4 I 5 CH 2=C-CH 2 -CH 3 I CH 3 4 -etil-2 -metil-1 -hexeno la
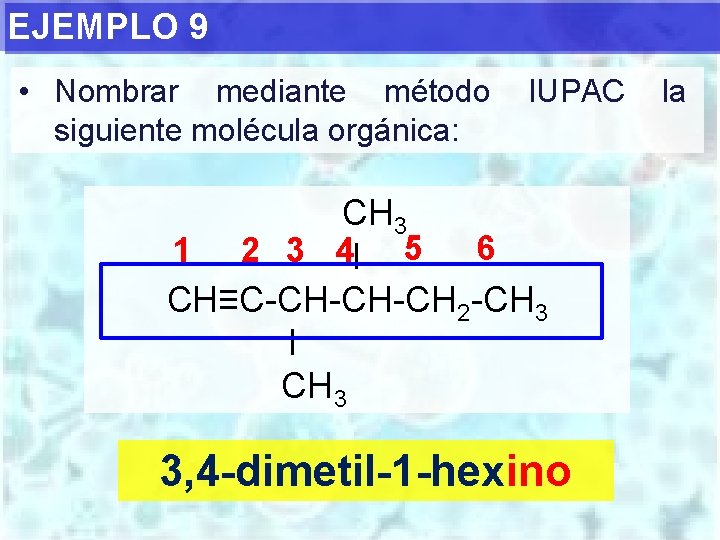
EJEMPLO 9 • Nombrar mediante método siguiente molécula orgánica: IUPAC CH 3 6 1 2 3 4 I 5 CH≡C-CH-CH-CH 2 -CH 3 I CH 3 3, 4 -dimetil-1 -hexino la
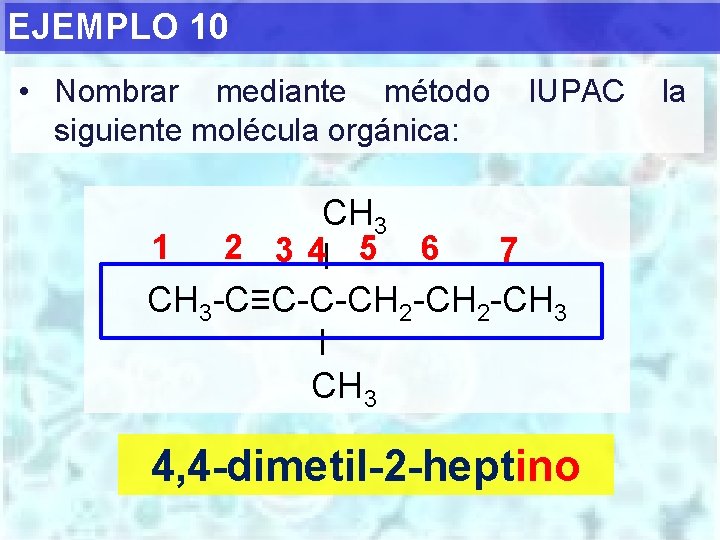
EJEMPLO 10 • Nombrar mediante método siguiente molécula orgánica: IUPAC CH 3 1 2 3 4 I 5 6 7 CH 3 -C≡C-C-CH 2 -CH 3 I CH 3 4, 4 -dimetil-2 -heptino la

EJEMPLO 11 • Desarrolla la fórmula extendida de 3, 3 -dimetilheptano: CH 3 I C H 3 - CH 2 - C - CH 2 -C H 3 I CH 3

EJEMPLO 12 • Desarrolla la fórmula extendida de 3, 4 -dimetil-1 -hepteno: CH 3 I C H 2= CH - CH 2 -C H 3 I CH 3

LOS ALICÍCLICOS

LOS ALICÍCLICOS • Los alicíclicos, que corresponden a cicloalcanos, cicloalquenos y cicloalquinos, forman cadenas cerradas. Alicíclicos Tipo de enlace cicloalcano Simple cicloalqueno Doble cicloalquino Triple Ejemplo
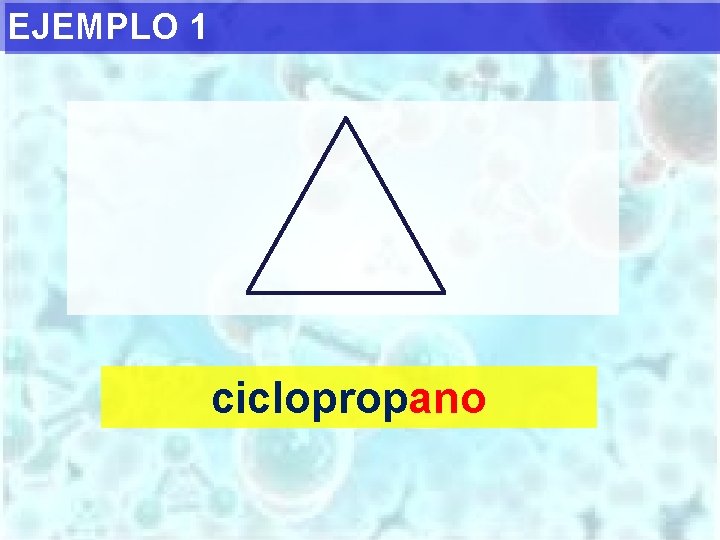
EJEMPLO 1 ciclopropano

EJEMPLO 2 ciclopropeno

EJEMPLO 3 ciclopropino
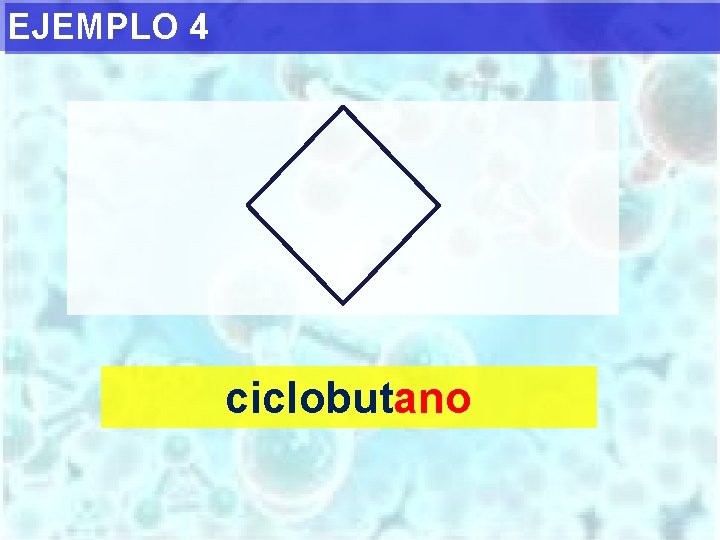
EJEMPLO 4 ciclobutano
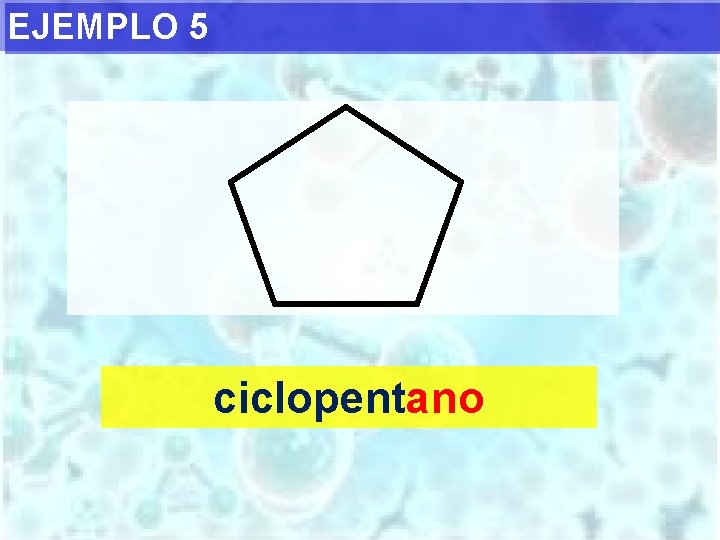
EJEMPLO 5 ciclopentano
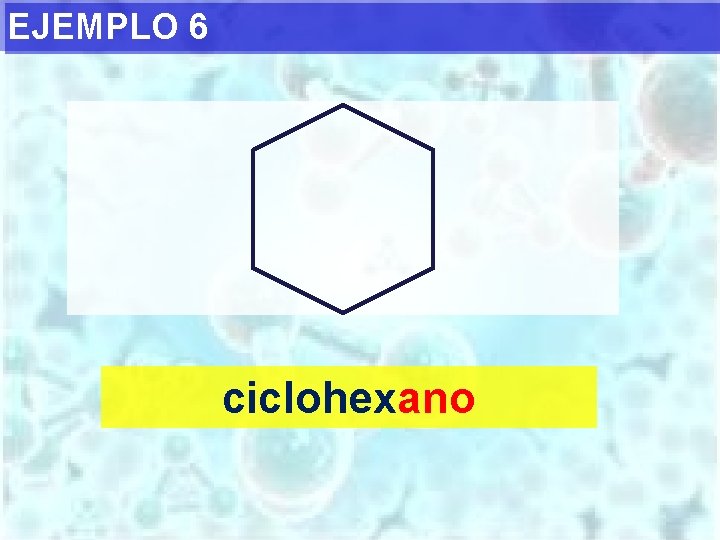
EJEMPLO 6 ciclohexano
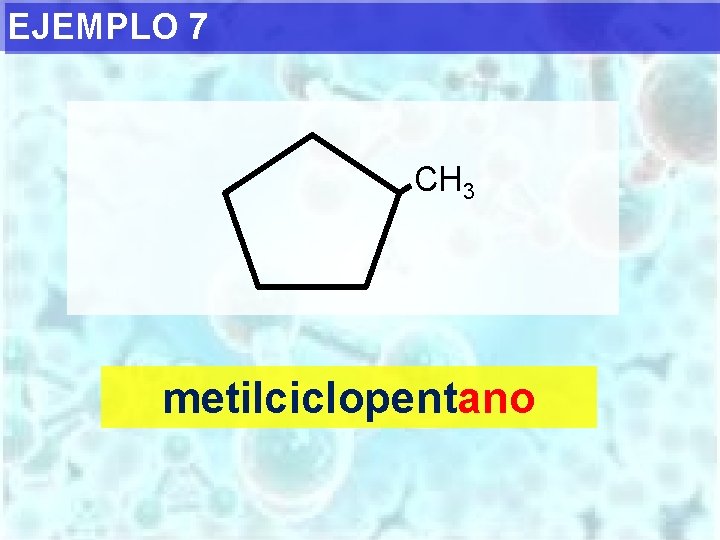
EJEMPLO 7 CH 3 metilciclopentano
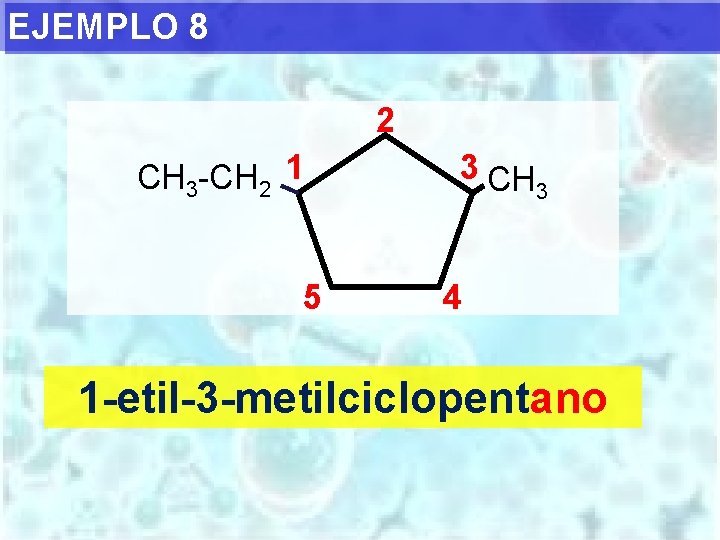
EJEMPLO 8 2 CH 3 -CH 2 1 5 3 CH 3 4 1 -etil-3 -metilciclopentano
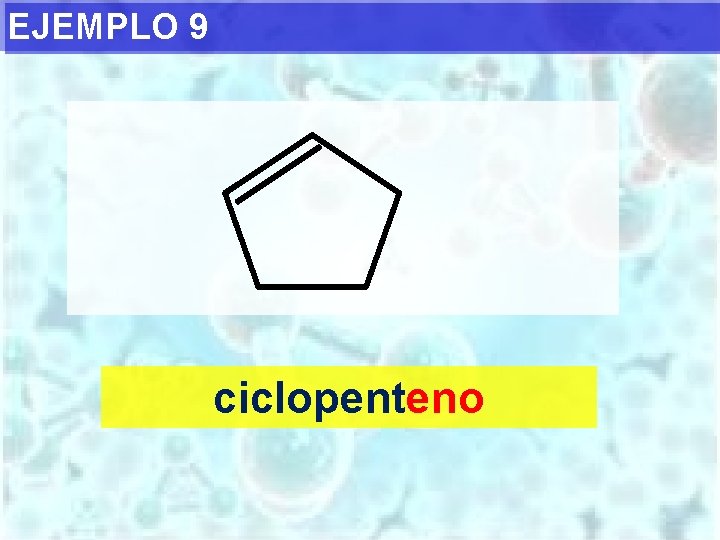
EJEMPLO 9 ciclopenteno
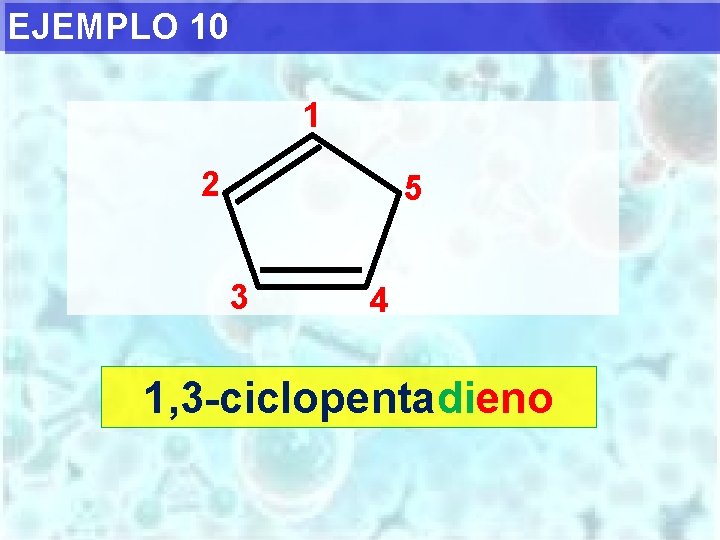
EJEMPLO 10 1 2 5 3 4 1, 3 -ciclopentadieno
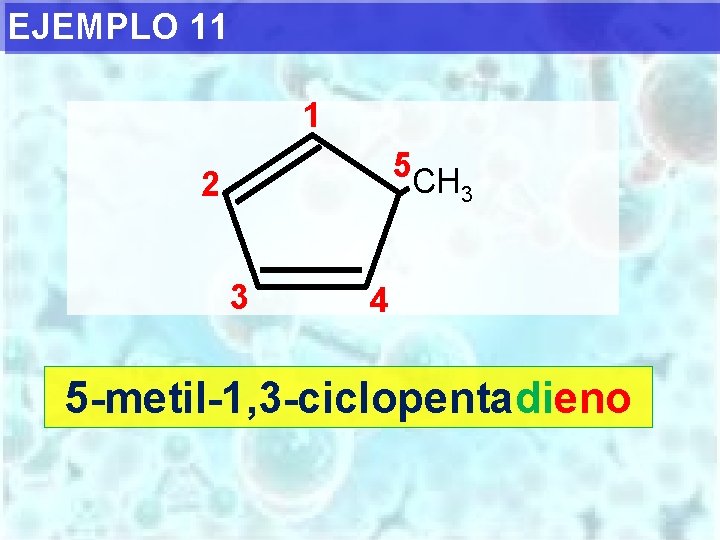
EJEMPLO 11 1 5 CH 2 3 3 4 5 -metil-1, 3 -ciclopentadieno
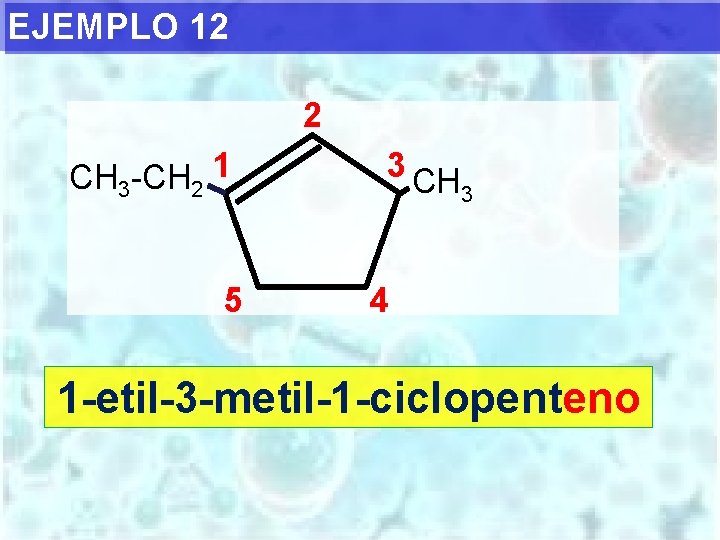
EJEMPLO 12 2 CH 3 -CH 2 1 5 3 CH 3 4 1 -etil-3 -metil-1 -ciclopenteno

EJERCICIOS • Desarrolla las fórmulas extendidas de las siguientes moléculas: A) 1 -etil-2 -metilciclopentano. B) 1 -etil-4 -metilciclohexano. C) isopropilciclohexano. D) 2 -metilciclopenteno. E) 3, 4 -dimetilciclohexeno. F) 3 -metilciclopentino.

LOS AROMÁTICOS
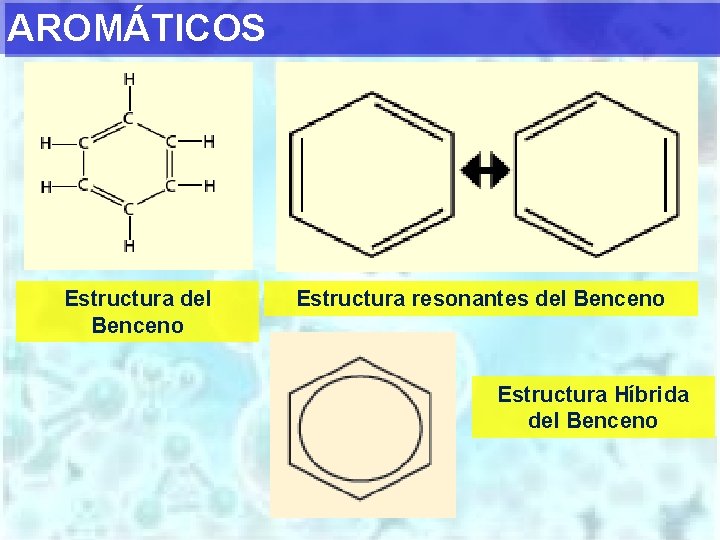
AROMÁTICOS Estructura del Benceno Estructura resonantes del Benceno Estructura Híbrida del Benceno
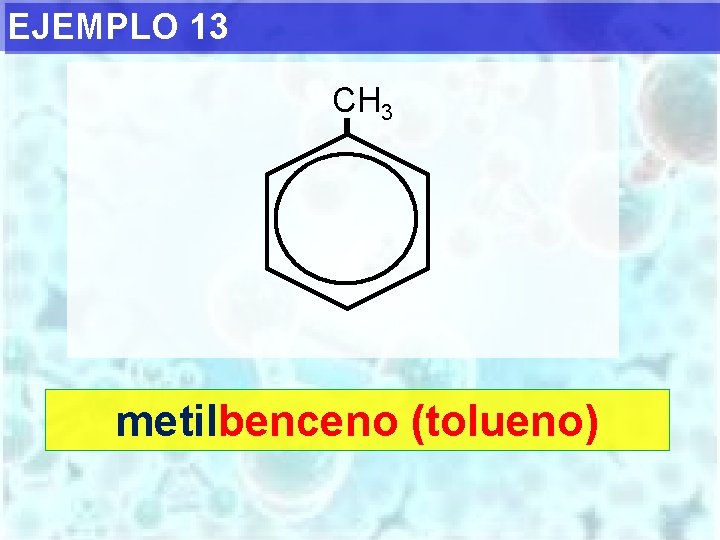
EJEMPLO 13 CH 3 metilbenceno (tolueno)
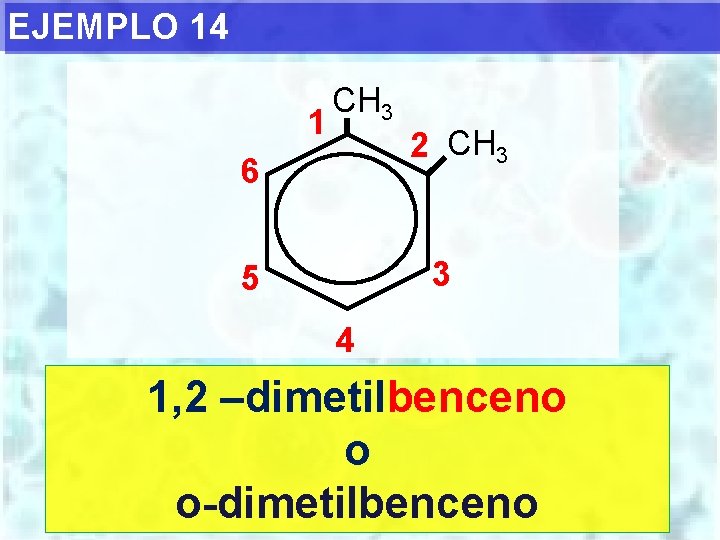
EJEMPLO 14 1 CH 3 6 2 CH 3 3 5 4 1, 2 –dimetilbenceno o o-dimetilbenceno
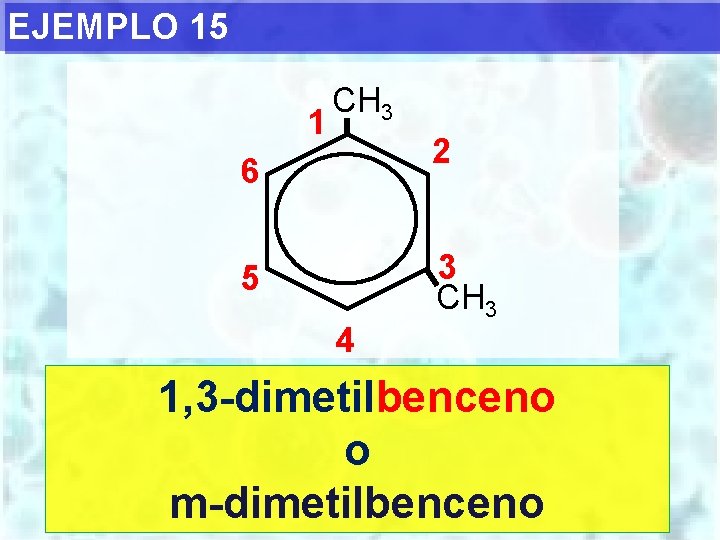
EJEMPLO 15 1 CH 3 2 6 5 4 3 CH 3 1, 3 -dimetilbenceno o m-dimetilbenceno
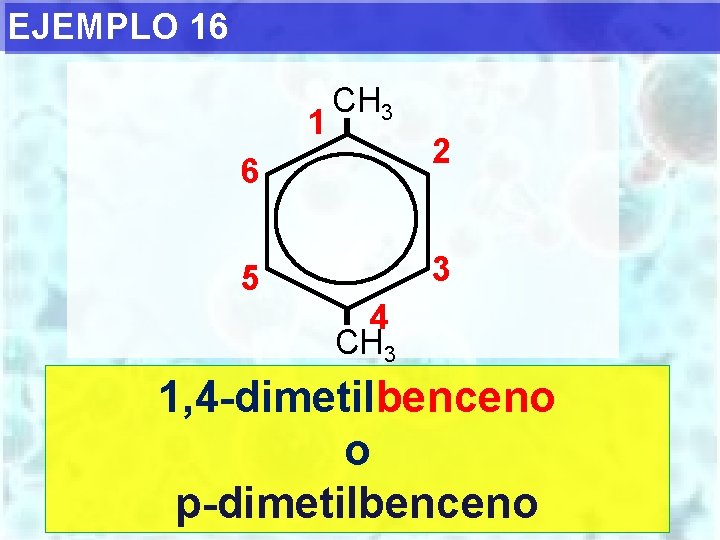
EJEMPLO 16 1 CH 3 2 6 3 5 4 CH 3 1, 4 -dimetilbenceno o p-dimetilbenceno
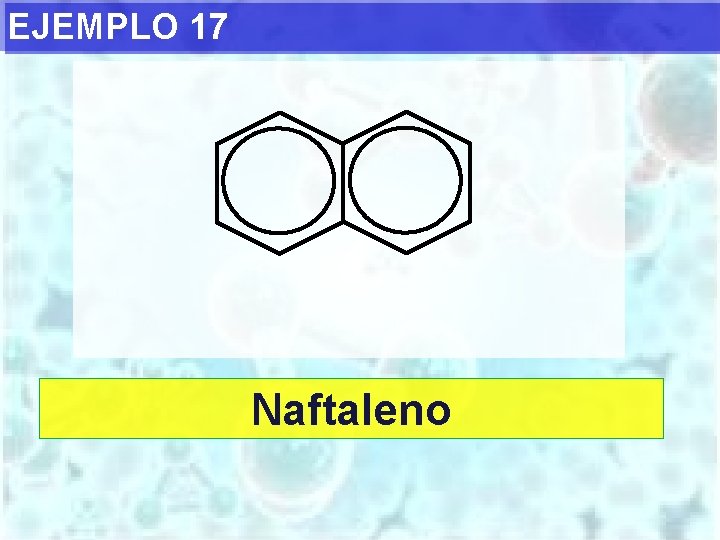
EJEMPLO 17 Naftaleno
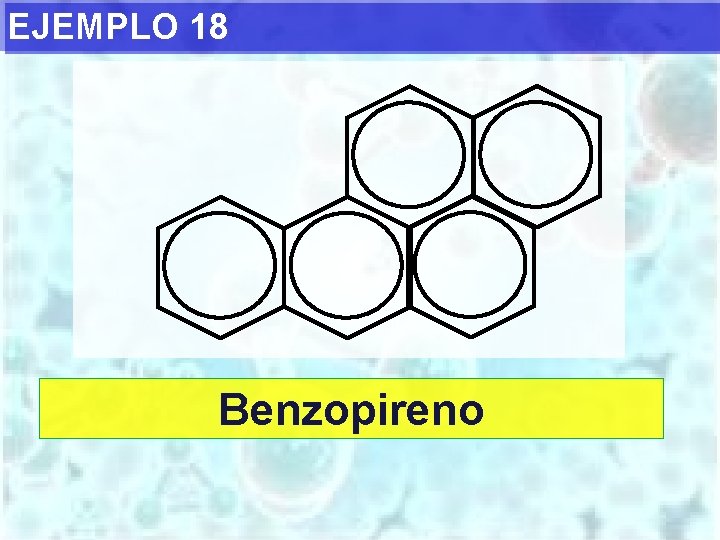
EJEMPLO 18 Benzopireno

EJERCICIOS • ¿Cuántos átomos de Hidrógeno contiene el compuesto aromático de la figura? • 8.
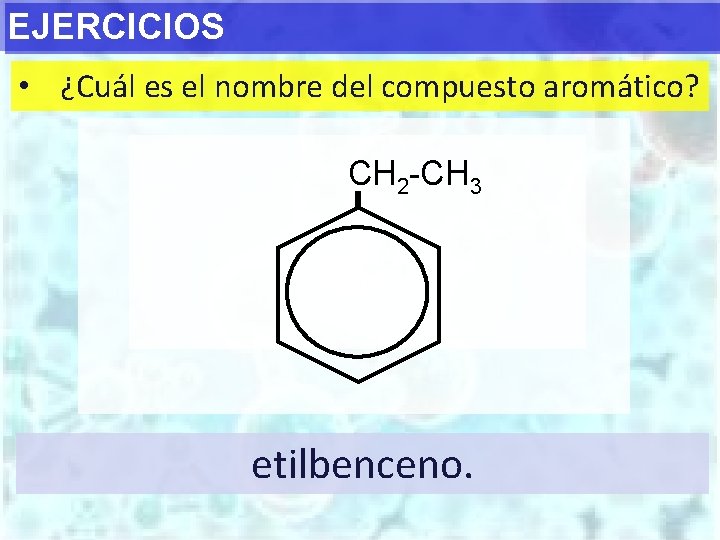
EJERCICIOS • ¿Cuál es el nombre del compuesto aromático? CH 2 -CH 3 etilbenceno.
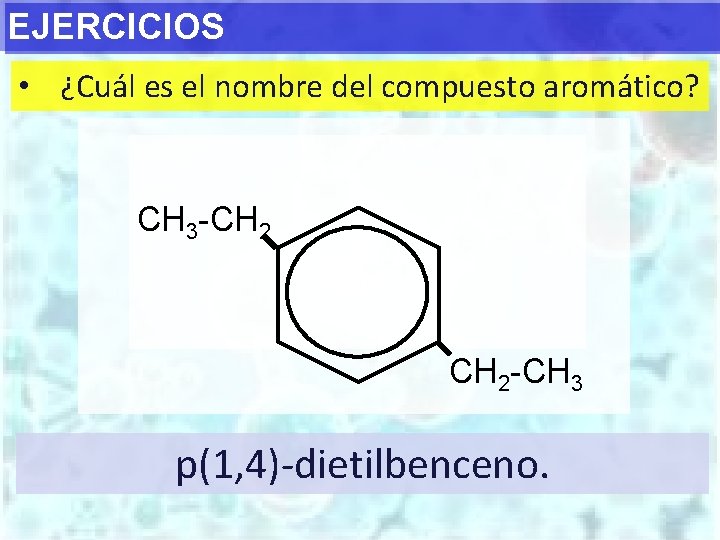
EJERCICIOS • ¿Cuál es el nombre del compuesto aromático? CH 3 -CH 2 -CH 3 p(1, 4)-dietilbenceno.

EJERCICIOS • Desarrolla las fórmulas extendidas de las siguientes moléculas: A) m-dietilbenceno. B) Isopropilbenceno. C) 1 -etil-3 -metilbenceno. D) 3 -metil-1 -hepteno. E) 4 -terbutil-2 -octino. F) 4, 4 -dimetil-1, 2 -hexadieno. G) 2 -metilciclohexeno.
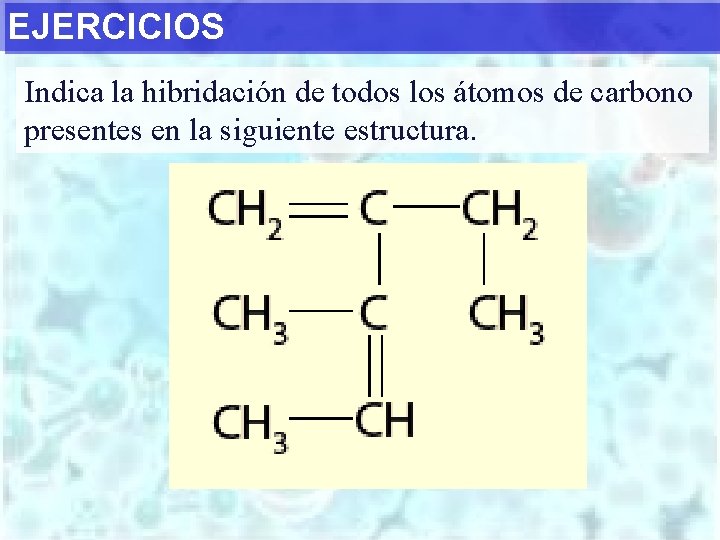
EJERCICIOS Indica la hibridación de todos los átomos de carbono presentes en la siguiente estructura.
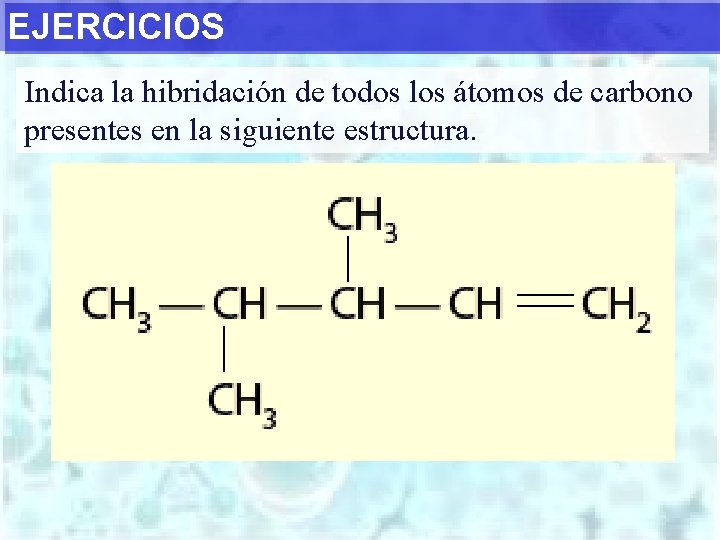
EJERCICIOS Indica la hibridación de todos los átomos de carbono presentes en la siguiente estructura.
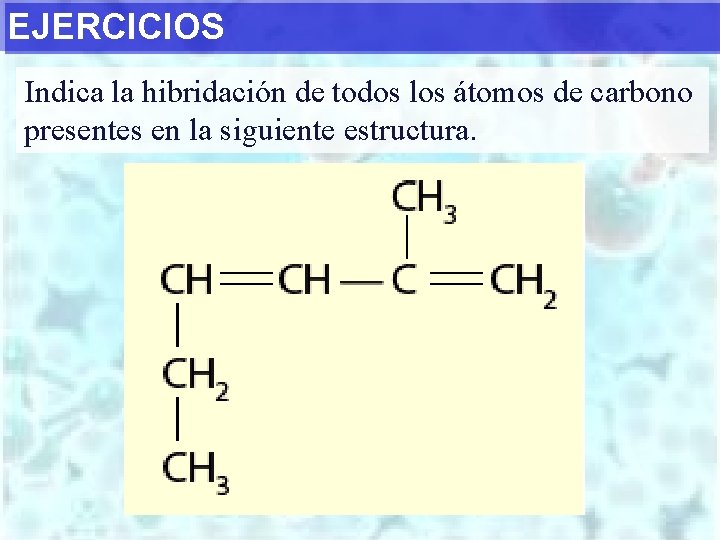
EJERCICIOS Indica la hibridación de todos los átomos de carbono presentes en la siguiente estructura.
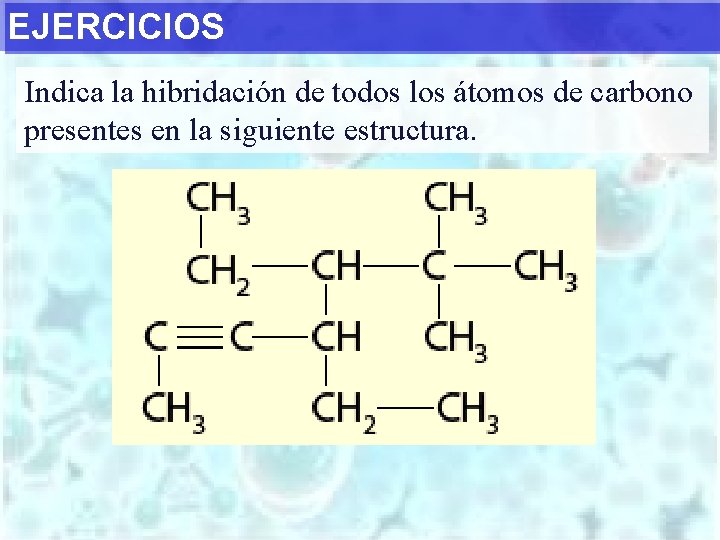
EJERCICIOS Indica la hibridación de todos los átomos de carbono presentes en la siguiente estructura.
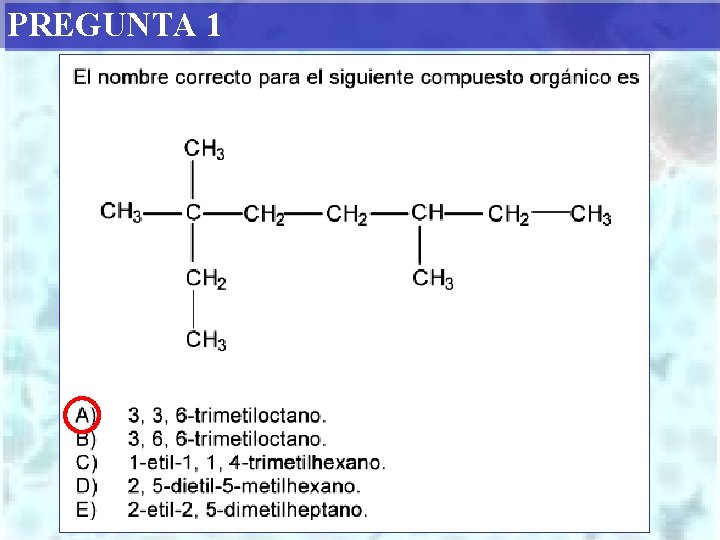
PREGUNTA 1

PREGUNTA 2

Colegio Andrés Bello Chiguayante Muchas Gracias Jorge Pacheco R. Profesor de Biología y Química

IDEAS GENERALES • ¿Qué es la Química Orgánica? • “Es la Química de los compuestos del Carbono”, el término Orgánica proviene del “derivados de organismo vivos”. Ejemplo: Azúcar, Urea, Almidón, Ceras, Aceites vegetales, etc.
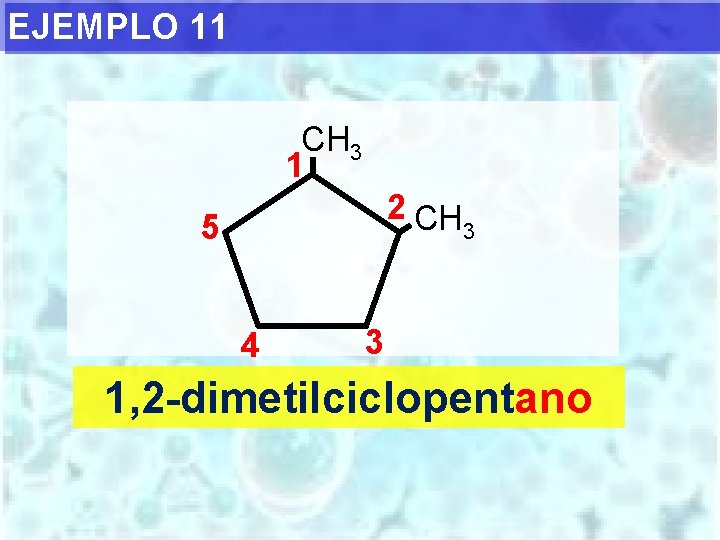
EJEMPLO 11 CH 3 1 2 CH 5 4 3 3 1, 2 -dimetilciclopentano
- Slides: 93