Qumica Geral 20182019 Professor Valentim Nunes Unidade Departamental


















- Slides: 20

Química Geral - 2018/2019 Professor Valentim Nunes, Unidade Departamental de Engenharia - Secção de Química email: valentim@ipt. pt Gabinete: J 207 Pág. Web: http: //www. docentes. ipt. pt/valentim/ensino/quimica 1. htm

Ferramentas básicas da Química (Termoquímica) Todas as reacções químicas obedecem a duas leis fundamentais: lei da conservação da massa (já estudada!) e lei da conservação da energia. Energia: conceito abstracto, definido normalmente como a capacidade para realizar trabalho. Ao contrário da massa, apercebemos-nos da energia através dos seus efeitos!

Formas de Energia cinética: energia do movimento Energia potencial: energia armazenada ou disponível como consequência da posição de um objecto. A energia química é uma forma de energia potencial armazenada nas substâncias químicas devido ás posições relativas e arranjo dos átomos nessas substâncias Energia radiante ou solar: provém do Sol e é a fonte de energia primária da Terra. Energia térmica: é a energia cinética associada ao movimento aleatório dos átomos e das moléculas (translaccionais, rotacionais e vibracionais)

Energia Lei da Conservação da Energia Embora a energia possa assumir formas diferentes e interconvertíveis, não pode ser criada ou destruída! A quantidade total de Energia do Universo permanece constante.

Variação de Energia em Reacções Químicas A variação de energia em reacções química é tão importante como as relações mássicas anteriormente derivadas. Por exemplo, quando queimamos propano num fogão doméstico é mais importante a energia térmica libertada do que os produtos da combustão! Quase todas as reacções químicas absorvem ou libertam energia, geralmente na forma de calor. Calor: é a transferência de energia térmica entre dois corpos que estão a temperaturas diferentes. O estudo do calor posto em jogo em reacções químicas chama-se Termoquímica.

Sistema & vizinhanças Numa reacção química os reagentes e produtos são o sistema. Um sistema é uma parte específica do Universo que nos interessa. O resto do Universo, fora do sistema designa-se por vizinhança. Tipos de sistemas: (a) aberto ; (b) fechado; (c) isolado

Entalpia Uma grande parte das transformações ocorre a pressão constante. Para quantificar o fluxo de calor para dentro ou para fora de um sistema a química utiliza o conceito de entalpia, H. A variação de entalpia, H, é a diferença entre a entalpia dos produtos e a entalpia dos reagentes: A variação de entalpia numa transformação é igual ao calor libertado ou absorvido quando esta ocorre a pressão constante!

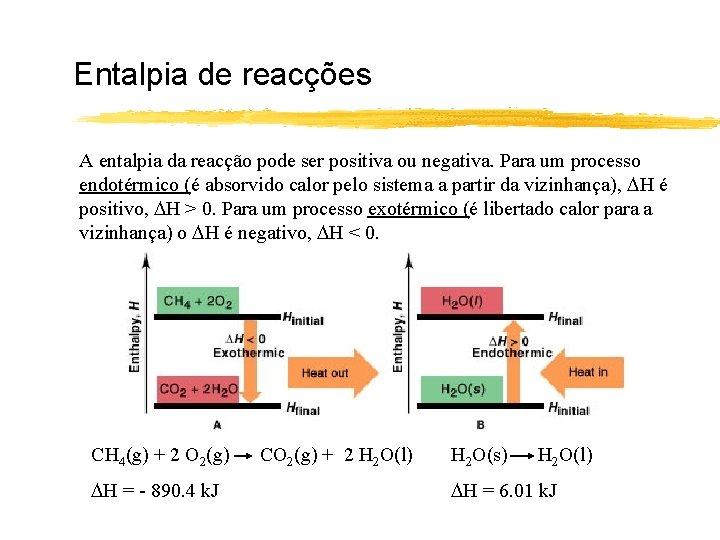
Entalpia de reacções A entalpia da reacção pode ser positiva ou negativa. Para um processo endotérmico (é absorvido calor pelo sistema a partir da vizinhança), H é positivo, H > 0. Para um processo exotérmico (é libertado calor para a vizinhança) o H é negativo, H < 0. CH 4(g) + 2 O 2(g) H = - 890. 4 k. J CO 2(g) + 2 H 2 O(l) H 2 O(s) H 2 O(l) H = 6. 01 k. J

Equações termoquímicas As equações termoquímicas mostram as variações de entalpia assim como as relações de massa. 1. Ao escrever equações termoquímicas devemos indicar os estados de agregação: CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) H = - 802. 4 k. J 2. Quando se inverte uma equação o valor de H permanece o mesmo, mas o sinal muda: H 2 O(l) H 2 O(s) H = - 6. 01 k. J 3. Se multiplicarmos ambos os lados de uma equação por um factor n então H deve vir multiplicado pelo mesmo factor: 2 H 2 O(s) 2 H 2 O(l) H = 2 6. 01 = 12. 02 k. J

Calorimetria O calor posto em jogo em processos físicos e químicos mede-se com um calorímetro. Calor específico, c: é a quantidade de calor necessária para elevar em 1 °C a temperatura de 1 g de substância; unidades: J. g-1. K-1 Capacidade calorífica, C: é a quantidade de calor necessária para elevar em 1 °C a temperatura de uma dada quantidade da substância. Se for um mole é a capacidade calorífica molar; unidades: J. mol-1. K-1 Q é a quantidade de calor, m é a massa, n é o número de moles e t é a variação de temperatura.

Calores específicos Subst. c / J. g-1. K-1 Al 0. 900 Au 0. 129 C(graf. ) 0. 720 C(diam) 0. 502 Cu 0. 385 Fe 0. 444 Hg 0. 139 H 2 O 4. 184 etanol 2. 460 Uma amostra de 466 g de água é aquecida de 8. 50 °C até 74. 60 °C. Qual a quantidade de calor absorvida pela água? Q = mc t Q = 466 g 4. 184 J. g-1. K-1 (74. 60 - 8. 50) K Q = 1. 29 105 J ou Q 130 k. J O sinal positivo indica que o calor é absorvido pela água.

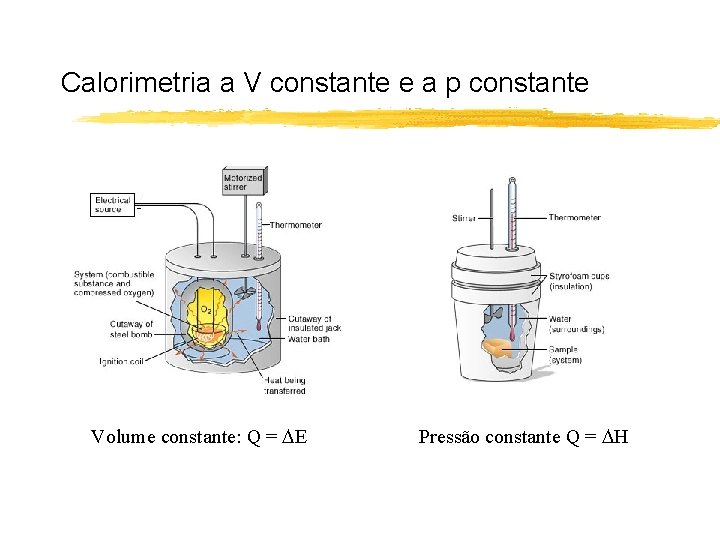
Calorimetria a V constante e a p constante Volume constante: Q = E Pressão constante Q = H

Alguns cálculos Não havendo perda de massa e calor para o exterior temos: Qsist = Qágua + Qbomba + Qreacção = 0 Qreacção = - (Qbomba + Qágua) Qágua = mágua 4. 184 J. g-1. K-1 t Qbomba = Cbomba t Fez-se a combustão de 1. 922 g de metanol num calorímetro de bomba a volume constante. A temperatura da água subiu 4. 20 °C. Calcular o calor molar de combustão do metanol sabendo que a capacidade calorífica da bomba mais a água é 10. 4 k. J/°C. Qreacção = - (10. 4 k. J. °C-1 4. 20 °C) = - 43. 68 k. J Qreacção = -43. 68 k. J 32 g. mol-1 (1/1. 922 g) - 727 k. J. mol-1

Outro exemplo Misturou-se 100 m. L de HCl 0. 5 M, com 100 m. L de Na. OH 0. 5 M, num calorímetro a pressão constante com capacidade calorífica, Cbomba = 335 J. K-1. A temperatura inicial das soluções era 22. 5 °C e a temperatura final da mistura foi 24. 9 °C. Calcular o calor da reacção de neutralização, por mole. Admitir que as soluções têm a densidade e calor específico da água. Qreacção = - (Qsol + Qbomba) Qsol = (100 g + 100 g) 4. 184 J. K-1. g-1 (24. 9 - 22. 5 ) K = 2. 01 103 J Qbomba = 335 J. K-1 (24. 9 - 22. 5 ) K = 804 J Qreacção = - (2. 01 103 + 804) J - 2. 81 k. J Qreacção = - 2. 81 k. J / 0. 05 mol -56. 2 k. J. mol-1

Entalpias de formação padrão A entalpia de formação padrão, H°f , é a variação de entalpia quando se forma um mole de composto a partir dos seus elementos à pressão de 1 bar ( 1 atm). Por convenção, a entalpia de formação padrão de qualquer elemento na sua forma mais estável é zero a qualquer temperatura. H°f(O 2) = 0; H°f (O 3) 0; H°f (C, grafite) = 0; H°f (C, diamante) 0 H 2(g) + 1/2 O 2(g) H 2 O(l) H°f = -286 k. J/mol 3/2 H 2(g) + 1/2 N 2(g) NH 3(g) H°f = - 46 k. J/mol 2 C(s) + H 2(g) C 2 H 2(g) H°f = + 227 k. J/mol

Entalpias de reacção padrão Uma vez conhecidos os valores das entalpias de formação padrão podemos calcular a entalpia de reacção padrão, H°r Para uma reacção acertada, a A + b B c. C+d. D H°r = c H°f (C) + d H°f (D) - a H°f (A) + b H°f (B) 4 NH 3(g) + 5 O 2(g) 4 NO (g) + 6 H 2 O(g) H°r = 4 H°f (NO) +6 H°f (H 2 O) - 4 H°f (NH 3) + 5 H°f (O 2) H°r = 4 90 +6 (- 286) - 4 (- 46) + 5 0 H°r - 1172 k. J

Lei de Hess Muitos compostos não podem ser preparados directamente a partir dos seus elementos. Como obter o H°f ? Método indirecto! Lei de Hess: Quando reagentes são convertidos em produtos, a variação de entalpia é a mesma quer a reacção se dê num passo ou numa série de passos.

Lei de Hess - outro exemplo Calcular a entalpia de formação padrão do metano, a partir das seguintes entalpias de reacção: C(grafite) + O 2(g) CO 2(g) H°r = -393. 5 k. J 2 H 2(g) + O 2(g) 2 H 2 O(g) H°r = -571. 6 k. J CH 4(g) + 2 O 2(g) CO 2(g) + 2 H 2 O(g) H°r = - 890. 4 k. J A reacção pretendida é: C(grafite) + 2 H 2(g) CO 2(g) + 2 H 2 O(g) C(grafite) + O 2(g) CH 4(g) + 2 O 2(g) CH 4(g) H°r = + 890. 4 k. J H°r = -393. 5 k. J 2 H 2(g) + O 2(g) 2 H 2 O(g) H°r = -571. 6 k. J _____________________________ C(grafite) + 2 H 2(g) CH 4(g) H°r = - 74. 7 k. J

Calores de solução O calor ou entalpia de solução, H°sol, é o calor libertado ou absorvido quando uma certa quantidade de soluto se dissolve numa dada quantidade de solvente. H 2 O Na. Cl(s) Na+(aq) + Cl-(aq) H°sol = ? H°sol = Urede + H°hidrat H°sol = 788 + ( - 784 ) k. J H°sol = 4 k. J. mol-1 Neste caso o processo é endotérmico!

Recomendações Finais A Termoquímica faz parte de um tema mais lato chamado Termodinâmica (irão estudar o assunto no 2º semestre do Curso e, provavelmente, apanham o mesmo Prof!) Utilizem estes “slides” em conjuntos com as vossa notas da lição! Complementem o vosso estudo com a leitura do Capítulo 6 do Chang (R. Chang, Química, 11ª ed. , Mc. Graw-Hill, Lisboa, 2013) Resolvam os exercícios da 1ª série! Boa semana!