Qumica Geral 20182019 Professor Valentim Nunes Unidade Departamental













- Slides: 20

Química Geral - 2018/2019 Professor Valentim Nunes, Unidade Departamental de Engenharia - Secção de Química email: valentim@ipt. pt Gabinete: J 207 Pág. Web: http: //www. docentes. ipt. pt/valentim/ensino/quimica 1. htm

O Estado Gasoso Substâncias que existem como gases: H 2, F 2, He, Xe. . Os compostos iónicos não são gases em condições PTN Os compostos moleculares podem ser gases (CO, CO 2, NH 3, CH 4), mas a maioria são líquidos ou sólidos. Ao serem aquecidos transformam-se mais facilmente em gases, vaporizando a temperaturas baixas.

Pressão de um gás A pressão é a força exercida por unidade de área. No Sistema Internacional a unidade é o Pascal (1 Pa = 1 N/m 2) 1 atm = 760 mm. Hg 1 atm = 101325 Pa

Pressão atmosférica ~32 km

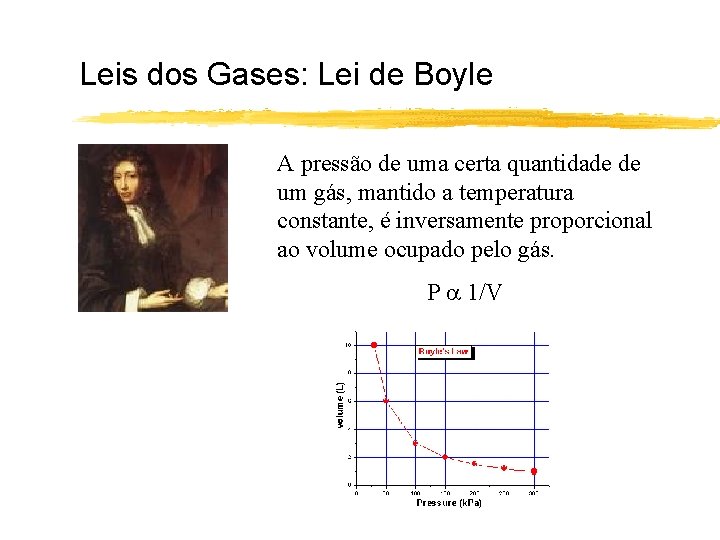
Leis dos Gases: Lei de Boyle A pressão de uma certa quantidade de um gás, mantido a temperatura constante, é inversamente proporcional ao volume ocupado pelo gás. P 1/V

Leis dos Gases: Lei de Charles e Gay-Lussac Volume/L A pressão constante, o volume ocupado por um gás é directamente proporcional à temperatura: V α T A volume constante, a pressão é directamente proporcional à temperatura: p α T. Temperatura/ºC

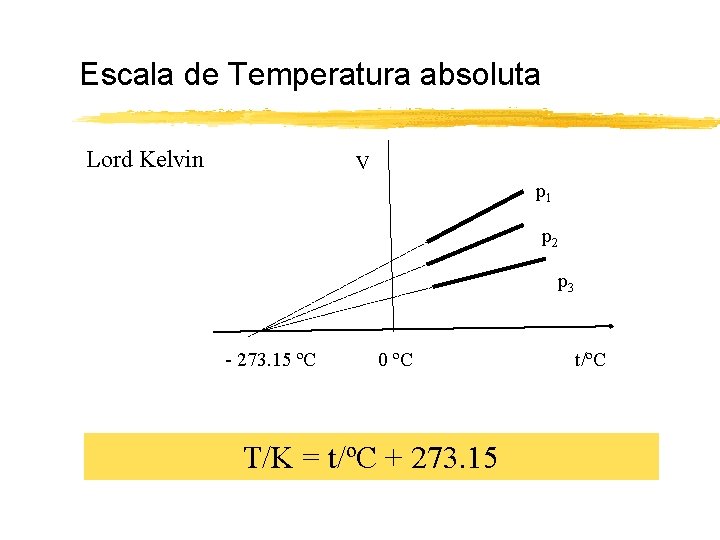
Escala de Temperatura absoluta Lord Kelvin V p 1 p 2 p 3 - 273. 15 ºC 0 ºC T/K = t/ºC + 273. 15 t/ºC

Leis dos Gases: Lei de Avogadro À mesma temperatura e pressão, o volume ocupado por um gás é directamente proporcional ao número de moles: V α n.

Equação dos Gases Perfeitos R = 8. 314 J. K-1. mol-1 R = 0. 0821 atm. L. K-1. mol-1 Qual o volume ocupado por um mole de gás perfeito em condições PTP? p. V = n. RT/p V = (1 mol × 0. 082 atm. L. mol-1. K-1 × 273. 15 K)/ 1 atm V 22. 414 L

Volumes molares de alguns gases a PTP

Cálculos de Densidade Rearranjando a equação dos gases perfeitos (ou gases ideais) obtemos: Calcular a densidade do brometo de hidrogénio (HBr) gasoso, em gramas por litro, a 733 mm. Hg e 46 ºC. ρ = (0. 964 atm × 80. 9 g. mol-1) / (0. 0821 atm. L. mol-1. K-1 × 319. 15 K) ρ 2. 98 g/L

Estequiometria envolvendo gases A azida de sódio (Na. N 3) é utilizada nos airbag de automóveis. Calcular o volume de azoto que se liberta quando reagem 60 g de azida a 21 ºC e quando a pressão é 823 mm. Hg. A reacção é: 2 Na. N 3(s) 2 Na(s) + 3 N 2(g) n azida = 60 g/65 g. mol-1 0. 92 mol n azoto = (3 mol azoto/ 2 mol azida) × 0. 92 mol azida 1. 38 mol de azoto V azoto = (1. 38 mol × 0. 082 atm. L. mol-1. K-1 × 294. 15 K)/(823/760) atm V azoto 30. 8 L

Lei de Dalton das pressões parciais A pressão total de uma mistura de gases é a soma das pressões que cada gás exerceria se ocupasse sozinho o mesmo volume.

Aplicando a Lei de Dalton PO 2 0. 2 atm valor “óptimo” para o nosso organismo! Ar contém aproximadamente 20% em oxigénio. Em profundidade, por exº, quando P = 2 atm: Utiliza-se hélio para diluir o oxigénio!

Teoria Cinética de Gases As leis ajudam a compreender o comportamento macroscópico dos gases, mas não explicam o que acontece à escala molecular! Moléculas percorrem grandes distâncias, sem interacções. Ocupam volume desprezável. Não existem forças atractivas nem repulsivas. Efectuam apenas colisões elásticas. E cinética = ½ mv 2 α T Ludwig Boltzmann

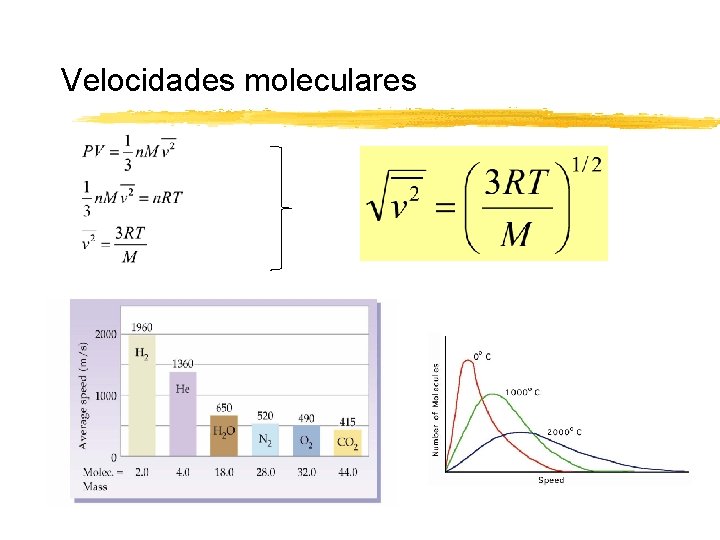
Velocidades moleculares

Lei de Graham da efusão A efusão consiste na passagem de moléculas de um gás através de um orifício à escala molecular. Qual o factor de separação entre o uranio-238 e uranio-235, necessário ao enriquecimento do urânio, a partir do hexafluoreto de urânio, UF 6 (g)? S = (238+6× 19/(235+6× 19))1/2 1. 004

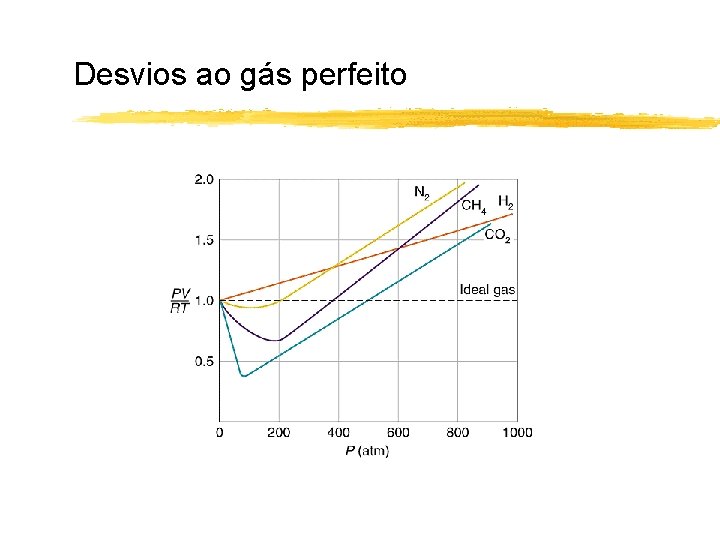
Desvios ao gás perfeito

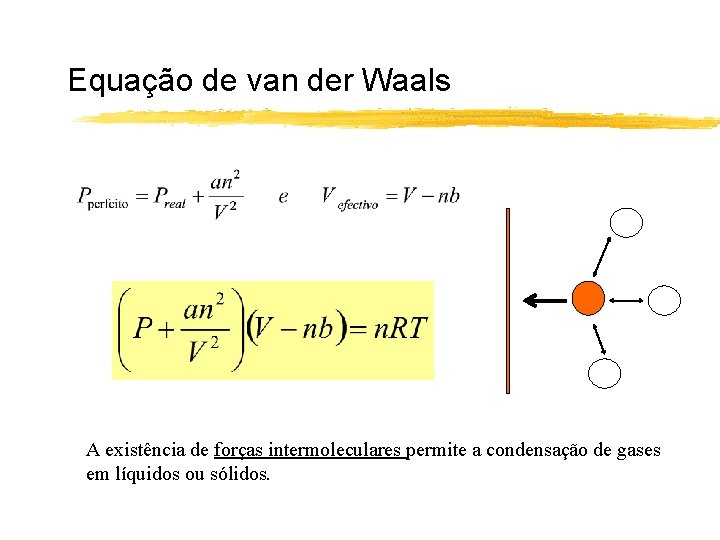
Equação de van der Waals A existência de forças intermoleculares permite a condensação de gases em líquidos ou sólidos.

Recomendações Finais Utilizem estes “slides” em conjuntos com as vossa notas da lição! Complementem o vosso estudo com a leitura do Capítulo 5 do Chang (R. Chang, Química, 11ª ed. , Mc. Graw-Hill, Lisboa, 2013) Resolvam os exercícios da 3ª série! Boa semana!