Qumica Fsica Cintica Qumica Valentim M B Nunes

Química Física Cinética Química Valentim M B Nunes Unidade Departamental de Engenharias Instituto Politécnico de Tomar, Outubro, 2019

Cinética Química A Cinética Química é o ramo da QUÍMICA FÍSICA que estuda a velocidade das reacções químicas. A velocidade de uma reacção química depende da temperatura, pressão, concentração dos reagentes, presença de catalisadores, etc.
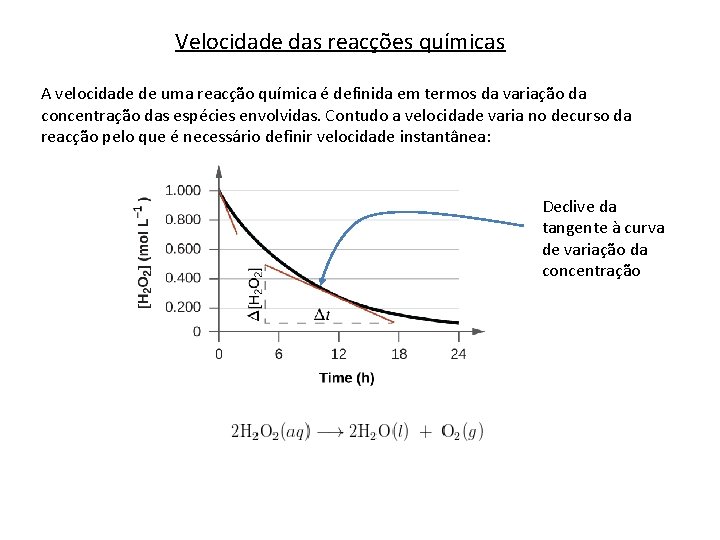
Velocidade das reacções químicas A velocidade de uma reacção química é definida em termos da variação da concentração das espécies envolvidas. Contudo a velocidade varia no decurso da reacção pelo que é necessário definir velocidade instantânea: Declive da tangente à curva de variação da concentração
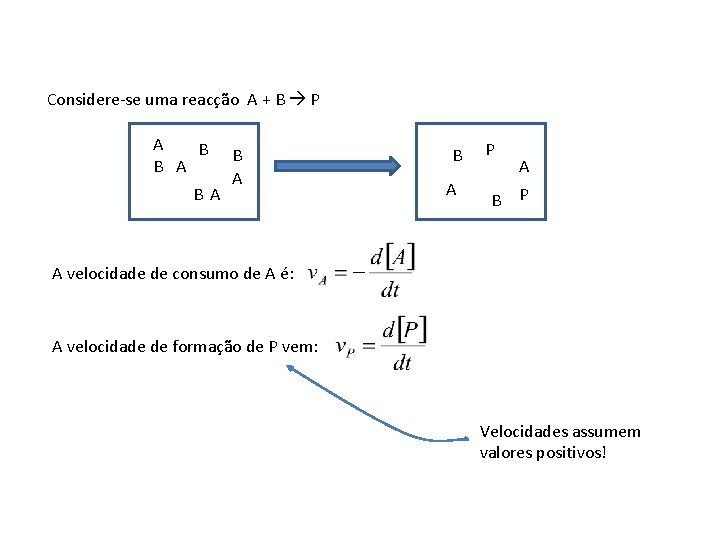
Considere-se uma reacção A + B P A B B A BA B A P A velocidade de consumo de A é: A velocidade de formação de P vem: Velocidades assumem valores positivos!

Para uma estequiometria mais complexa: A + 2 B 3 C + D Genericamente a velocidade da reacção é: onde J é o coeficiente estequiométrico da substância J, negativo para os reagentes e positivo para os produtos.

Leis de Velocidade Observação empírica: a velocidade de uma reacção química é geralmente proporcional à concentração molar dos reagentes elevada a uma potência simples. k – constante de velocidade Independente das concentrações Dependente da temperatura Uma equação deste tipo, determinada experimentalmente, é a Lei de velocidade da reacção. A lei de velocidade permite-nos calcular a velocidade de reacção para qualquer concentração de reagentes, e permite propor o mecanismo da reacção.

Ordem de Reacção A lei de velocidade permite classificar as reacções químicas. A classificação é baseada na ordem de reacção. A ordem de reacção em relação a cada espécie é a potência à qual é elevada a respectiva concentração. A ordem global da reacção é a soma das ordens de todos os componentes. Por exemplo: é de 1ª ordem em relação a A, 1ª ordem em relação a B e é de segunda ordem. Outro exemplo de uma reacção de 2ª ordem é: Na reacção: NO 2 (g) + CO (g) NO (g) + CO 2 (g) Esta reacção é de 2ª ordem em relação ao NO 2 e de ordem zero em relação ao CO.

Retomando: As ordens e são diferentes dos coeficientes estequiométricos. Se e forem iguais aos coeficientes estequiométricos, então a reacção dá-se num só passo reaccional.
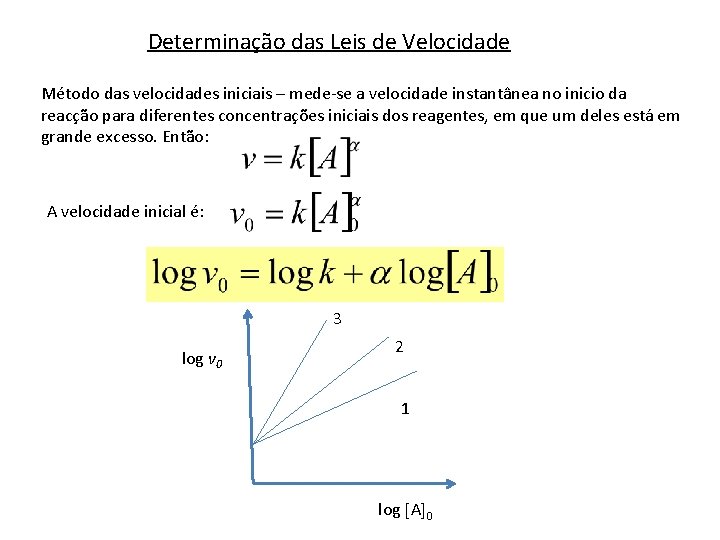
Determinação das Leis de Velocidade Método das velocidades iniciais – mede-se a velocidade instantânea no inicio da reacção para diferentes concentrações iniciais dos reagentes, em que um deles está em grande excesso. Então: A velocidade inicial é: 3 log v 0 2 1 log A 0

Métodos de Integração O método das velocidades pode não revelar totalmente a lei de velocidade. Uma alternativa são os métodos de integração. Consideremos uma reacção de 1ª ordem. A velocidade de consumo de A é:
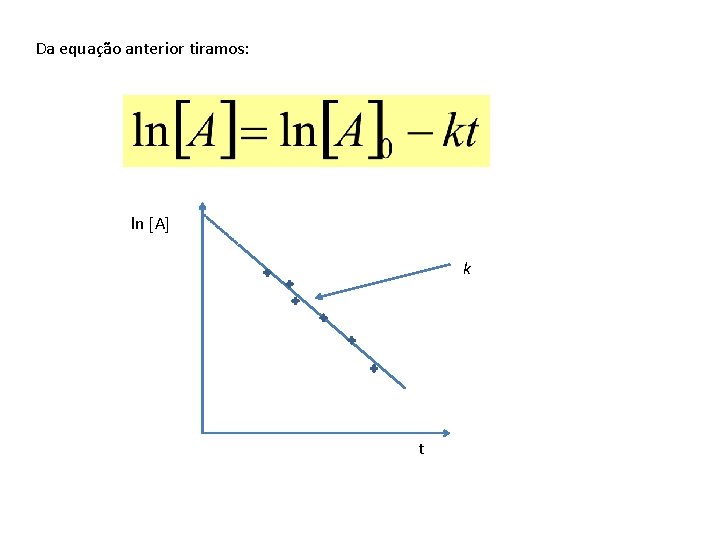
Da equação anterior tiramos: ln A k t
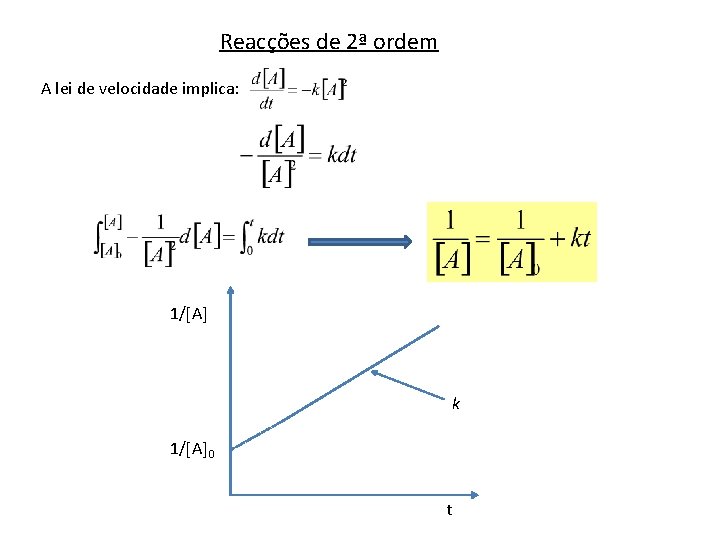
Reacções de 2ª ordem A lei de velocidade implica: 1/ A k 1/ A 0 t

Quando a reacção é de 2ª ordem, mas de 1ª ordem em relação a dois reagentes A e B então para o caso A + B P Sendo x o nº de moles que é consumido por unidade de tempo, temos: Mas:

Quando t = 0, x = 0, logo: Finalmente: Se a estequiometria for a A + b B P

Tempos de Meia-Vida Uma indicação útil da velocidade de uma reacção química é o tempo de meia vida, t 1/2 que é o tempo necessário para que a concentração de um reagente se reduza para metade. Considere-se uma reacção de 1ª ordem: Para t = t 1/2 temos A = A 0/2

Tempos de Meia-Vida - 2ª ordem Dependente da concentração inicial !

Reacções consecutivas de 1ª ordem A k 1 B k 2 C
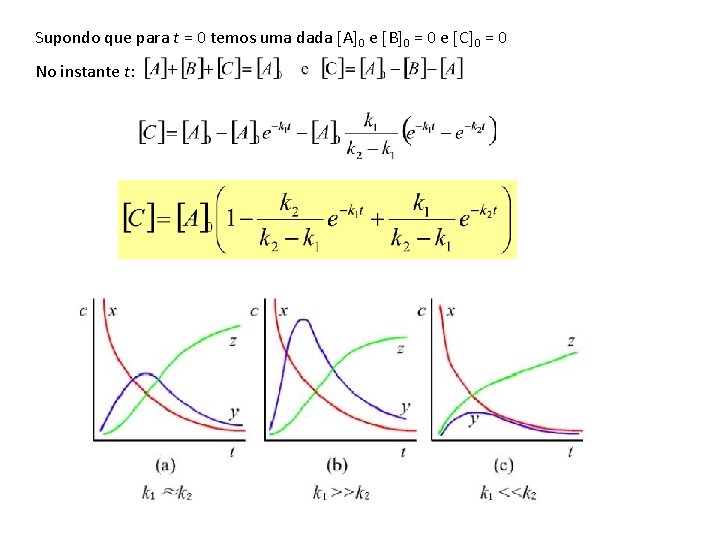
Supondo que para t = 0 temos uma dada A 0 e B 0 = 0 e C 0 = 0 No instante t:

No último caso, quando k 2 >> k 1 Depende apenas do coeficiente da 1ª reacção. A primeira reacção é muito lenta passo controlador da reacção. Em termos industriais é também importante saber quando é que a B é máxima isto é quando é que d B /dt = 0 Caso mais simples !


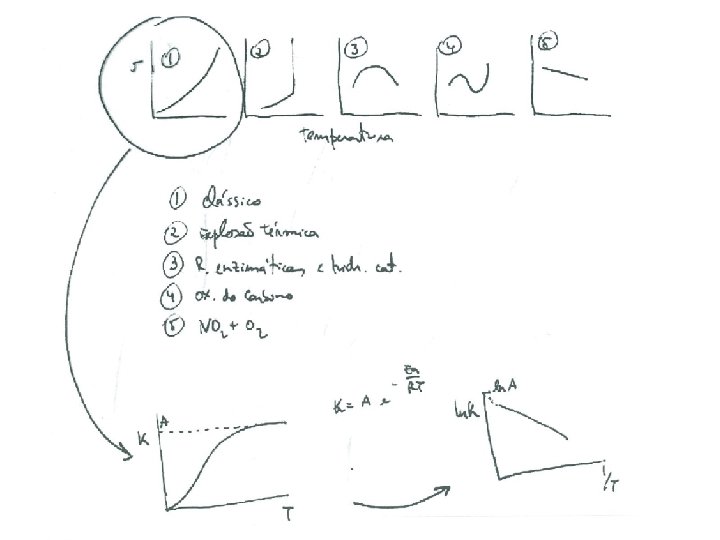
Dependência com a Temperatura Na maior parte das reacções químicas a velocidade aumenta com a temperatura. Uma observação empírica levou o químico sueco Svante Arrhenius a propor a seguinte equação, conhecida como Equação de Arrhenius. ln k - Ea /R 1/T

Se alargarmos muito o intervalo de temperaturas os pontos experimentais podem fugir um pouco da recta de Arrhenius. Uma outra equação é a equação de Kooij: Para qualquer processo temos: A – factor pré – exponencial Ea – Energia de activação

Mecanismo das Reacções elementares são aquelas que ocorrem num só passo. Exemplo: NO (g) + O 3(g) NO 2 (g) + O 2 (g) - bimolecular CH 2 CH 3 CH=CH 2 - unimolecular Molecularidade – nº de moléculas de reagente que intervêm no passo elementar. Nas reacções elementares a ordem é igual à molecularidade e as ordens parciais iguais aos coeficientes estequiométricos. Mecanismo reaccional – exº 2 NO (g) + 2 H 2 (g) N 2 (g) + 2 H 2 O (g) k 1 1º passo: 2 NO + H 2 N 2 + H 2 O 2 k 2 2º passo: H 2 O 2 + H 2 2 H 2 O k 2 >> k 1, 1º passo controla a reacção

Aproximação de Estado Estacionário Os intermediários de uma reacção têm concentração baixa e constante, I muito baixa e d I /dt 0 2 NO (g) + O 2 (g) 2 NO 2 (g) Mas a reacção ocorre em três passos: ka 1. NO + NO N 2 O 2 ka' 2. N 2 O 2 NO + NO kb 3. N 2 O 2 + O 2 NO 2 + NO 2 Aproximação de estado estacionário:

Daqui obtemos: Como ka’ >> kb O 2 , obtemos: Lei experimental

Mecanismo de Michaelis - Menten para a acção enzimática S E P Mecanismo: 1. Reacção bimolecular , E + S ES 2. Decomposição unimolecular, ES E + S 3. Formação unimolecular dos produtos, ES E + P

Mas, E + ES = E t, em que E t é a concentração total de enzima, logo E = E t - ES Como: Constante de Michaelis
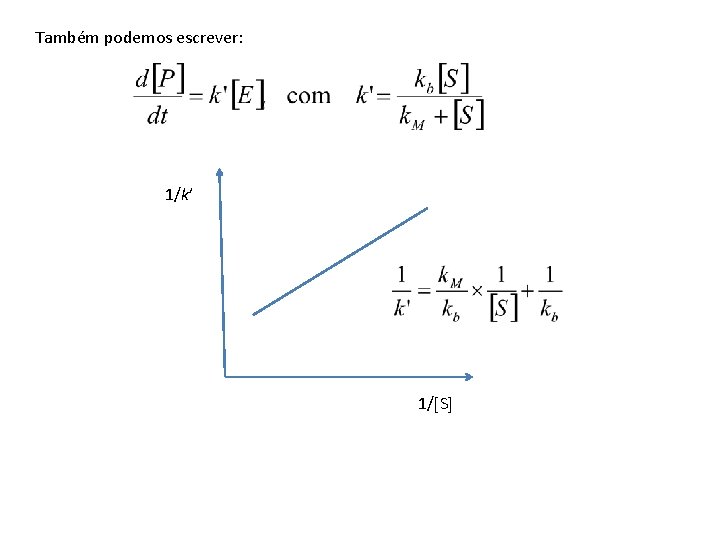
Também podemos escrever: 1/k’ 1/ S

Mecanismos de Reacções Complexas Reacções em Cadeia Br 2 (g) + H 2 g) 2 HBr (g) k 1 Iniciação: Br 2 2 Br (forma-se um radical de Br) k 2 Propagação: Br + H 2 HBr + H k 3 H + Br 2 HBr + Br k 4 Retardação: H + HBr H 2 + Br k 5 Terminação: Br + Br 2 Lei de velocidade observada: Complicado!
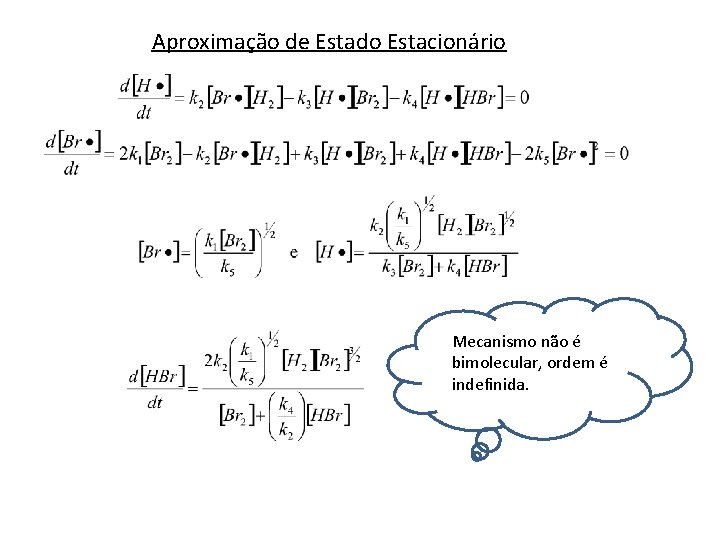
Aproximação de Estado Estacionário Mecanismo não é bimolecular, ordem é indefinida.
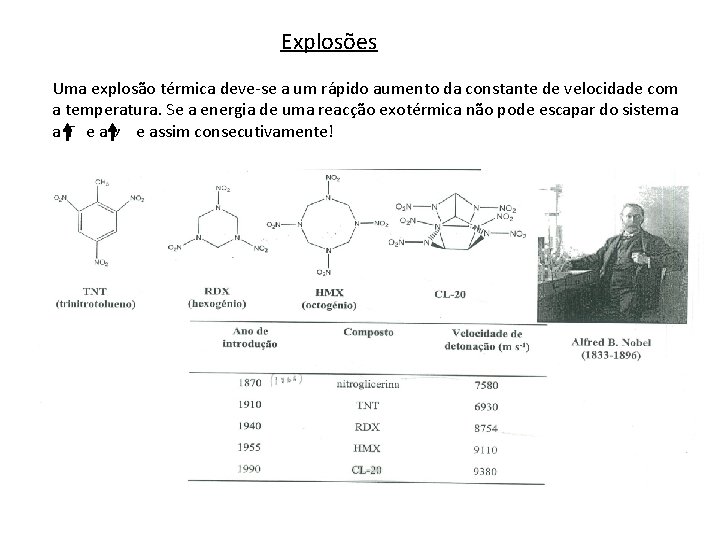
Explosões Uma explosão térmica deve-se a um rápido aumento da constante de velocidade com a temperatura. Se a energia de uma reacção exotérmica não pode escapar do sistema a T e a v e assim consecutivamente!
Reacções Fotoquímicas Muitas reacções podem ser iniciadas pela absorção de Luz. Por exemplo, a absorção de luz vermelha e azul pela clorofila e o subsequente uso de energia para a síntese de carbohidratos, a partir de CO 2 e H 2 O. Outro exemplo é a degradação do Ozono, designadamente pela acção dos CFC’s. Cl + O 3 Cl. O + O 2 Cl. O + M Cl 2 O 2 + M 2 O 3 3 O 2 Cl 2 O 2 + h 2 Cl + O 2 Estratosfera

Reacções de Polimerização em cadeia I 2 R M+ R M 1 v = ki I (rápido) onde I é o iniciador e M 1 é um radical monomérico M + M 1 M 2 M + M 2 M 3 M + Mn-1 Mn (propagação) v = kp M M Como as reacções de propagação são rápidas, a velocidade a que a concentração total dos radicais cresce é igual à velocidade do passo controlador, a iniciação. onde é a fracção de radicais R que iniciam a cadeia.

Mn + Mm Mn+m (terminação) v = kt M 2 independente do tamanho da cadeia A velocidade a que o monómero é consumido vem:

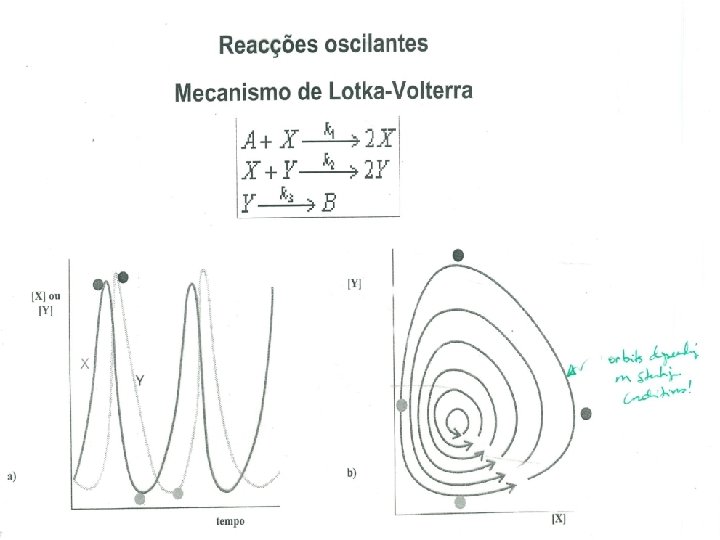
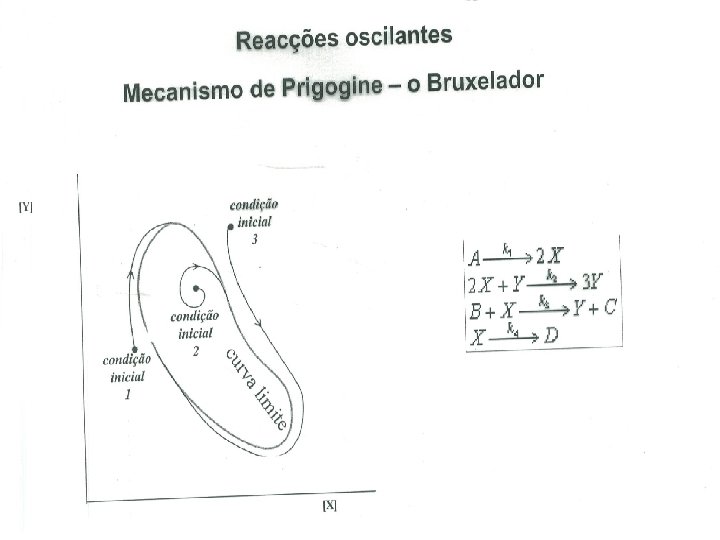
Autocatálise e Reacções Oscilantes O fenómeno de autocatálise consiste na catálise da reacção pelos produtos. A P v = k A P Uma consequência são as reacções oscilantes em que as concentrações de reagentes, intermediários e produtos variam periodicamente no espaço e no tempo. Exemplo é a reacção de Belousov-Zhabotinsky: Br. O 3 - + HBr. O 2 + H 3 O+ 2 Br. O 2 + 2 H 2 O 2 Br. O 2 + 2 Ce(III) + 2 H 3 O+ 2 HBr. O 2 + 2 Ce (IV) + 2 H 2 O
- Slides: 39