Enlace Qumico Qumica General con Laboratorio MI Frida

Enlace Químico Química General con Laboratorio MI Frida Karem Rivas Moreno

Tipos de Enlaces �Para la formación de compuestos, los átomos deben mantenerse unidos mediante un enlace químico, que es la fuerza que mantiene juntos a dos grupos de dos o más átomos y hace que funcionen como una unidad. �Iónico �Covalente (Simple, Polar y Coordinado) �Metálico �Por Puente de Hidrógeno

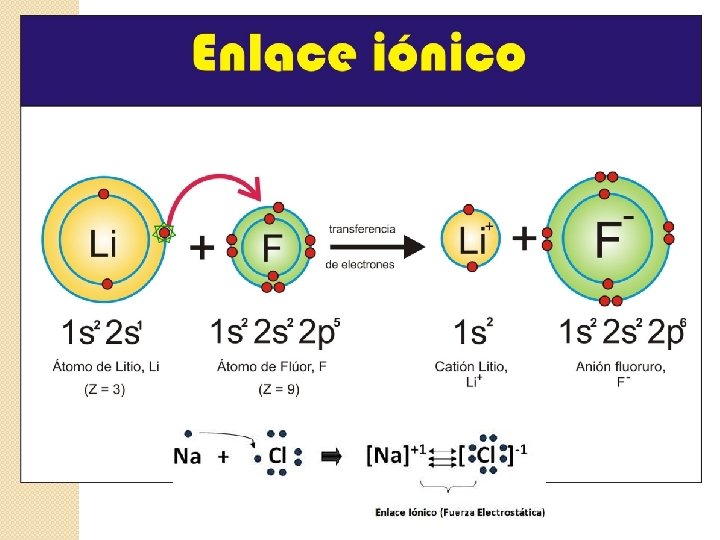
Enlace iónico Se forma al unir un metal (M) con un no metal (NM). El metal transfiere sus electrones al no metal. M + NM Características � Sólidos cristalinos, duros o frágiles � Solubles en agua y conductores de electricidad � Insolubles en solventes orgánicos � Elevados puntos de fusión y ebullición � Son inflamables Ejemplos: Sales, óxidos metálicos, carbonatos y bicarbonatos.

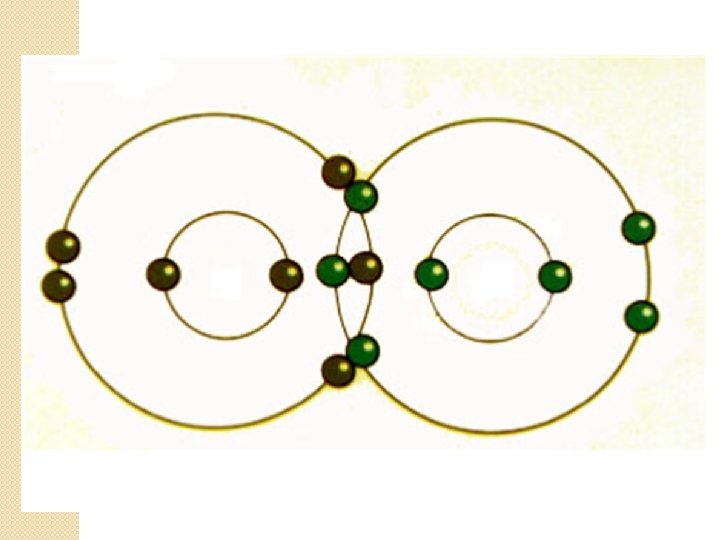
Enlace covalente simple Se forma entre no metales que comparten electrones. NM + NM Características: �Son insolubles en agua �Casi todos son combustibles �Puntos de fusión bajos �Enlace propio de los compuestos orgánicos �Ejemplos: agua, alcoholes, azúcares, grasas, aceites, perfumes, drogas y colorantes.

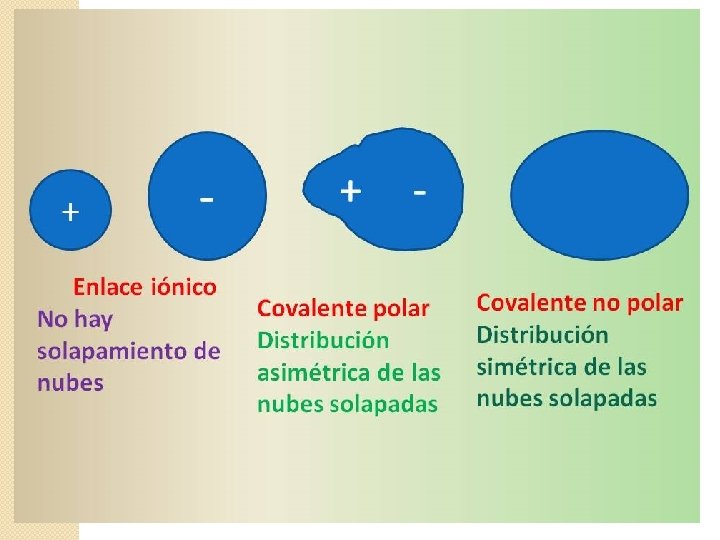
Enlace covalente polar Se forma entre no metales que comparten electrones, pero que tienen muy diferentes electronegatividades. NM + NM
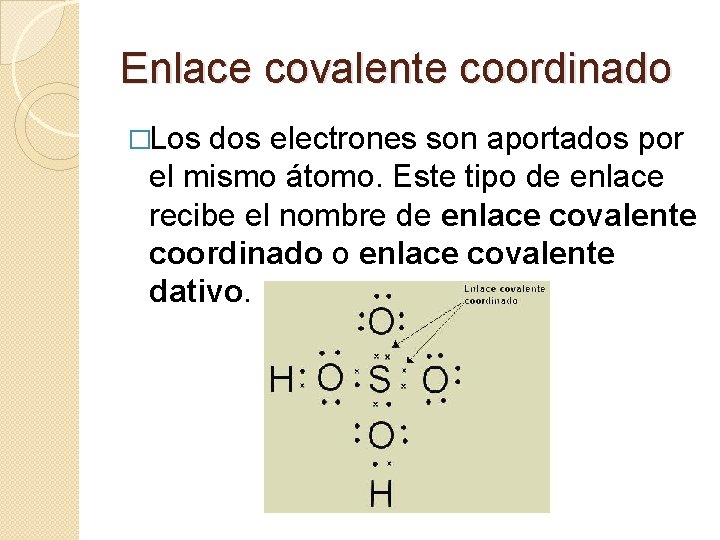
Enlace covalente coordinado �Los dos electrones son aportados por el mismo átomo. Este tipo de enlace recibe el nombre de enlace covalente coordinado o enlace covalente dativo.


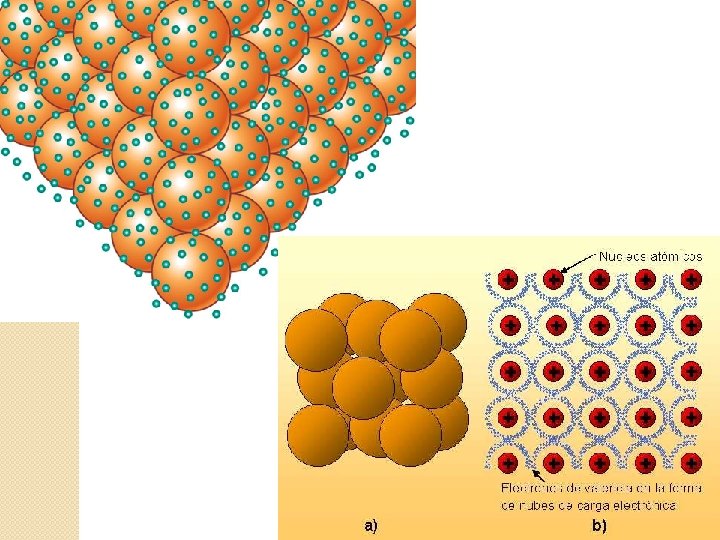
Enlace metálico Es la unión de los metales y aleaciones que forman cristales metálicos. Características: �Puntos de fusión y ebullición elevados. �Brillo metálico, dureza, maleabilidad, buena conductividad eléctrica y térmica. Ejemplos: Au, Na, Acero (hierro y carbón), bronce (Cu +Sn (3 -20%)+Zn, Al, Sb o P).

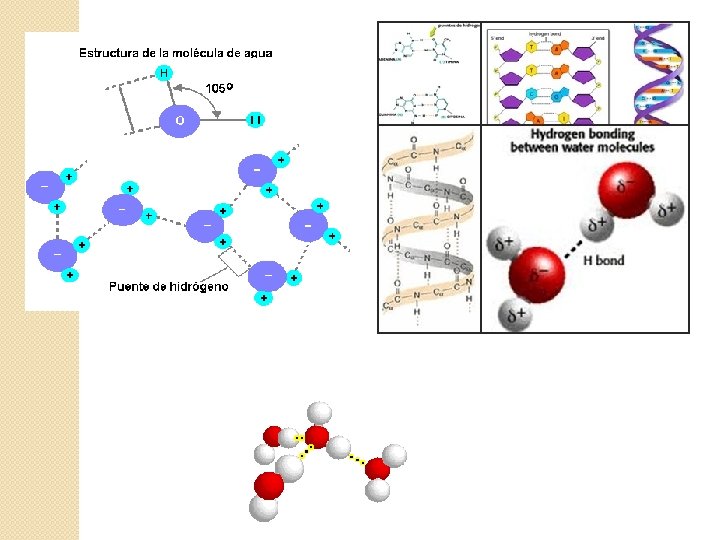
Enlace por puente de hidrógeno Atracción electrostática entre un protón combinado y otro átomo de gran electronegatividad y volumen pequeño. Características: �Puntos de fusión y ebullición elevados. �Líquidos de alto poder de disociación de los cristales iónicos. Ejemplos: H 2 O, HF, CH 3 OH, ADN

ESTRUCTURAS DE LEWIS Y REGLA DEL OCTETO
- Slides: 15