Colegio Andrs Bello Chiguayante UNIDAD DE NIVELACIN Captulo

Colegio Andrés Bello Chiguayante UNIDAD DE NIVELACIÓN: Capítulo 1: ESTEQUIOMETRÍA Jorge Pacheco R. Profesor de Biología y Química

CAPÍTULO 1: ESTEQUIOMETRÍA APRENDIZAJES ESPERADOS: • Aplican la información de una ecuación química en problemas relacionados con la estequiometria. • Identifican los factores que limitan la formación de un compuesto en una reacción química.
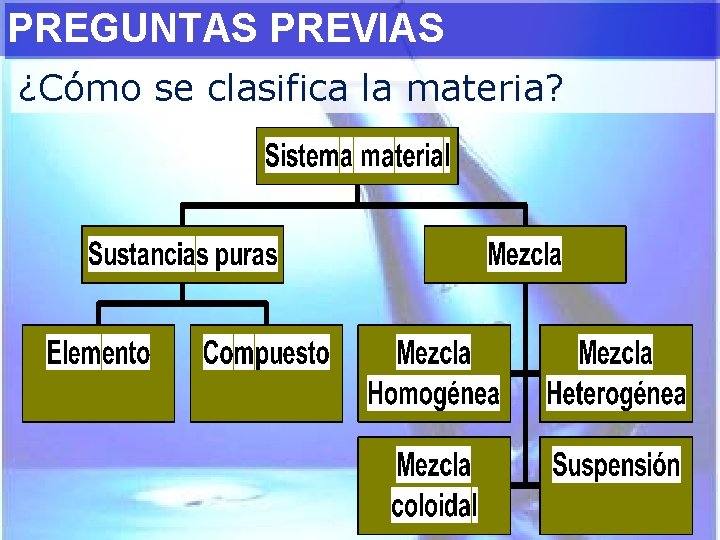
PREGUNTAS PREVIAS ¿Cómo se clasifica la materia?

PREGUNTAS PREVIAS ¿Cómo se clasifica la siguiente sustancia? ELEMENTO

PREGUNTAS PREVIAS ¿Cómo se clasifica la siguiente sustancia? MEZCLA HOMOGÉNEA

PREGUNTAS PREVIAS ¿Cómo se clasifica la siguiente sustancia? MEZCLA HETEROGÉNEA
PREGUNTAS PREVIAS ¿Cómo se clasifica la siguiente sustancia? COMPUESTO Cloruro de Sodio

PREGUNTAS PREVIAS ¿Qué es un cambio químico? Es un proceso en que, a partir de unas sustancias iniciales, llamadas reactivos, se obtienen unas sustancias finales distintas, llamadas productos.

PREGUNTAS PREVIAS ¿Qué es la Estequiometria? La Estequiometria(del griego “stoicheion”(elemento) y “metrón” (medida) es el cálculo de las relaciones cuantitativas entre reactivos y productos en el transcurso de una reacción química.

PREGUNTAS PREVIAS ¿Qué es un Estequiométrico? Coeficiente Es el número asignado a cada fórmula o símbolo químico que indica la cantidad de sustancias participantes en una ecuación química respetando la ley de la conservación de la masa.
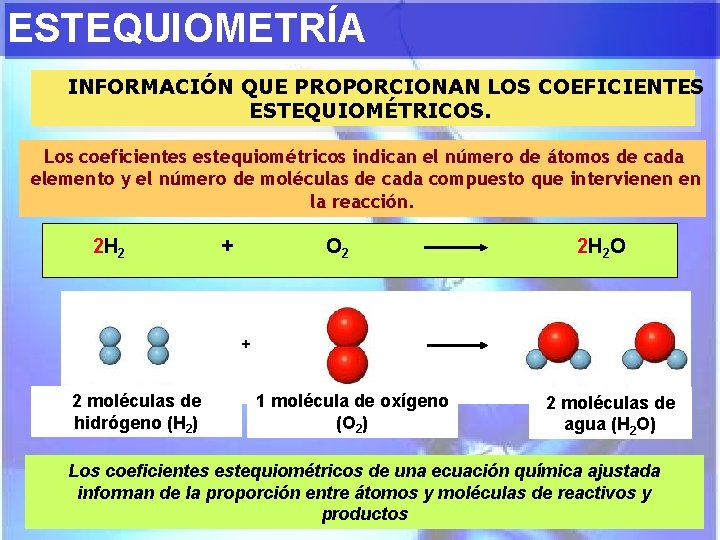
ESTEQUIOMETRÍA INFORMACIÓN QUE PROPORCIONAN LOS COEFICIENTES ESTEQUIOMÉTRICOS. Los coeficientes estequiométricos indican el número de átomos de cada elemento y el número de moléculas de cada compuesto que intervienen en la reacción. 2 H 2 + O 2 2 H 2 O + 2 moléculas de hidrógeno (H 2) 1 molécula de oxígeno (O 2) 2 moléculas de agua (H 2 O) Los coeficientes estequiométricos de una ecuación química ajustada informan de la proporción entre átomos y moléculas de reactivos y productos
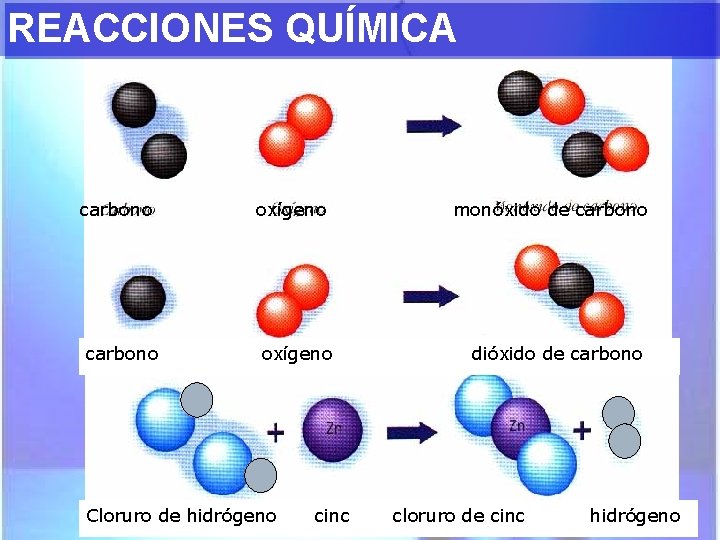
REACCIONES QUÍMICA carbono oxígeno Cloruro de hidrógeno cinc monóxido de carbono dióxido de carbono cloruro de cinc 12 hidrógeno

ACTIVIDAD: Al hacer reaccionar Hierro sólido (Fe) con Oxígeno gaseoso (O 2) en condiciones adecuadas, se obtiene Óxido de Hierro sólido (Fe 2 O 3). • Escribe la ecuación que representa la reacción: Fe (s) + O 2 (g) Fe 2 O 3 • Determina si la ecuación está balanceada: Fe = 1 Fe = 2 O = 3 (s)

BALANCE DE ECUACIONES QUÍMICAS 4 Fe (s) +3 O 2 (g) 2 Fe 2 O 3 (s) Fe = 1 x 4 = 4 Fe = 2 x 2 = 4 O = 2 x 3=6 O =3 x 2=6

TIPOS DE REACCIÓN QUÍMICA A) REACCIÓN DE COMBINACIÓN: • Tipo de reacción en las que se combinan dos reactivos, que pueden ser elementos o compuesto, para formar un solo producto, según la siguiente ecuación general: . Ejemplo: Reacción del aluminio metálico con oxígeno para formar el óxido de aluminio.

TIPOS DE REACCIÓN QUÍMICA B) REACCIÓN DE DESCOMPOSICIÓN: • En este tipo de reacción una sustancia se descompone o “rompe”, produciendo dos o más sustancias distintas, de acuerdo con el siguiente mecanismo general.

TIPOS DE REACCIÓN QUÍMICA C) REACCIÓN DE SUSTITUCIÓN SIMPLE: Tipo de reacción en donde un elemento reacciona con un compuesto para reemplazar uno de sus componentes, produciendo un elemento y un compuesto diferentes a los originales:

TIPOS DE REACCIÓN QUÍMICA D) REACCIÓN DE SUSTITUCIÓN DOBLE: • En este tipo de reacciones, dos compuestos intercambian sus elementos entre sí, produciendo dos compuestos distintos, de acuerdo al siguiente mecanismo general. AB + CD AD + CB

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química no balanceada identifica: el Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas (reactivos y productos) y masa en gramos. C 3 H 8 + 5 O 2 3 CO 2 + 4 H 2 O REACCIÓN DE SUSTITUCIÓN DOBLE 1 mol de C 3 H 8 6, 02 x 1023 moléculas de C 3 H 8 44 g 5 mol de O 2 3 mol de CO 2 3, 01 x 1024 moléculas de O 2 1, 81 x 1024 moléculas de CO 2 160 g 132 g 4 mol de H 2 O 2, 41 x 1024 moléculas de H 2 O 72 g
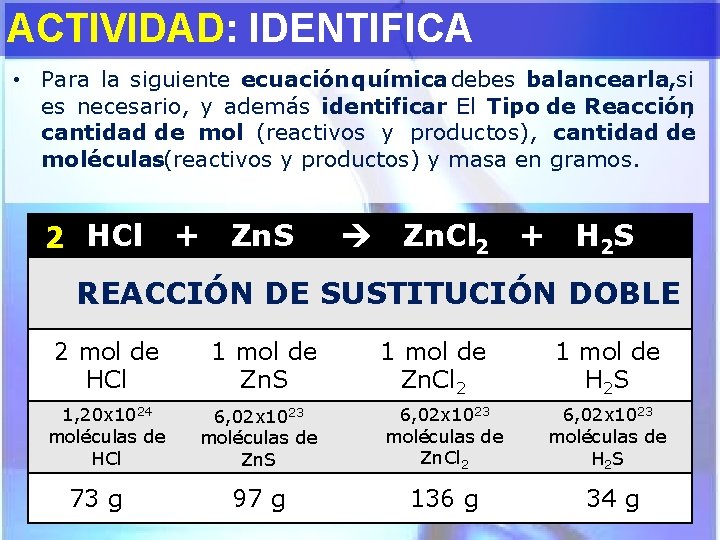
ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 HCl + Zn. S Zn. Cl 2 + H 2 S REACCIÓN DE SUSTITUCIÓN DOBLE 2 mol de HCl 1, 20 x 1024 moléculas de HCl 73 g 1 mol de Zn. S 1 mol de Zn. Cl 2 6, 02 x 1023 moléculas de Zn. S 6, 02 x 1023 moléculas de Zn. Cl 2 97 g 136 g 1 mol de H 2 S 6, 02 x 1023 moléculas de H 2 S 34 g

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 Al + 3 Br 2 2 Al. Br 3 REACCIÓN DE COMBINACIÓN 2 mol de Al 1, 20 x 1024 átomos de Al 54 g 3 mol de Br 2 2 mol de Al. Br 3 1, 81 x 1024 moléculas de Br 2 1, 20 x 1024 moléculas de Al. Br 3 480 g 534 g

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 H 2 O 2 2 H 2 O + O 2 REACCIÓN DE DESCOMPOSICIÓN 2 mol de H 2 O 2 1, 20 x 1024 moléculas de H 2 O 2 68 g 2 mol de H 2 O 1 mol de O 2 1, 20 x 1024 moléculas de H 2 O 6, 02 x 1023 moléculas de O 2 36 g 32 g
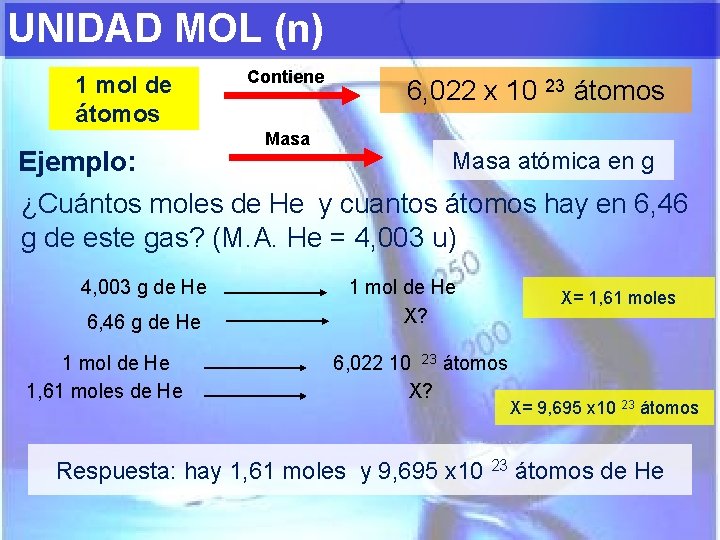
UNIDAD MOL (n) 1 mol de átomos Contiene 6, 022 x 10 23 átomos Masa atómica en g Ejemplo: ¿Cuántos moles de He y cuantos átomos hay en 6, 46 g de este gas? (M. A. He = 4, 003 u) 4, 003 g de He 6, 46 g de He 1 mol de He 1, 61 moles de He 1 mol de He X? 6, 022 10 23 átomos X? X= 1, 61 moles X= 9, 695 x 10 23 átomos Respuesta: hay 1, 61 moles y 9, 695 x 10 23 átomos de He

EJERCICIOS 1. ¿Qué cantidad de sustancia en unidad mol (n) de hierro existe en 25 g de hierro puro (Fe)? (M. A, Fe: 55, 65 u) 55, 65 g 1 mol Sabiendo que: X = = 25 g X mol 1 mol x 25 g 55, 65 g 0, 449 mol de Fe

EJERCICIOS 2. En el laboratorio un estudiante deberá manipular 5 g de Magnesio (Mg) durante un experimento de oxidación. ¿A qué cantidad de átomos de magnesio corresponde? (M. A. Mg: 24, 32 u) Sabiendo que: X 24, 32 g = 23 6, 02 x 10 átomos 6, 02 x 10 23 átomos 24, 32 g = X = 5 g X átomo x 5 g 1, 24 x 10 23 átomos de Mg

EJERCICIOS 3. ¿Qué masa en gramos presentará un átomo de carbono? (M. A. C: 12 u) Sabiendo que: X 6, 02 x 10 23 átomos = 12 g x 1 átomo 6, 02 x 10 23 átomos = X 1 átomo Xg = 1, 99 x 10 - 23 g

MASA MOLAR (M) • • • Masa en gramos de un mol de una sustancia. Se puede determinar al conocer la fórmula de la sustancia gracias a la suma consecutiva de todos sus componentes, al igual como se determina la masa molecular. La masa molar (en gramos) de cualquier sustancia es siempre numéricamente igual a su masa formular (uma).
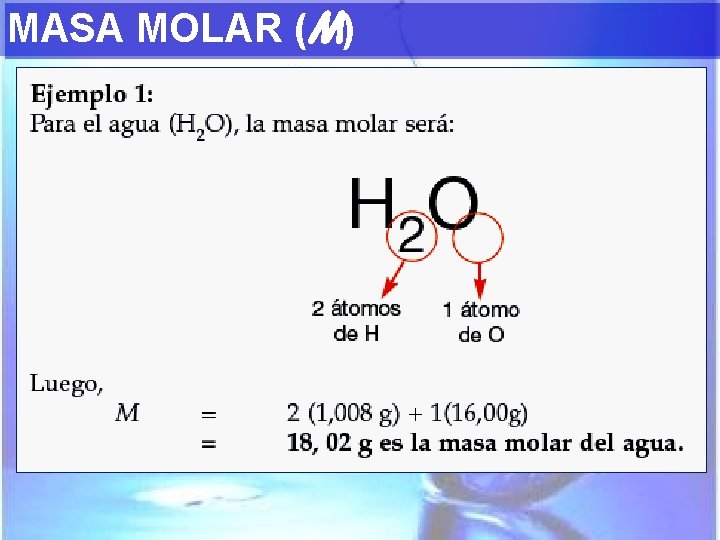
MASA MOLAR (M)

CONVERSIÓN MOL – GRAMO

EJEMPLO El sulfato de calcio (Ca. SO 4) es el principal ingrediente de la tiza utilizada antiguamente para escribir en la pizarra. ¿Cuál será el número de moles de sulfato de calcio que hay en un trozo de tiza de 14, 8 g? (M. A. Ca: 40 u; S: 32 u; O: 16 u)

PROBLEMA 1 El ácido acetilsalicílico C 9 H 8 O 4 es el principio activo de la aspirina. ¿Cuál es la masa en gramo de 0, 287 mol de ácido acetilsalicílico? (M. A. C: 12 u; H: 1 u; O: 16 u) M = [(9 x 12)+ (8 x 1) + (4 x 16)]g/mol = 180 g/mol n = m M m=nx. M m = 0, 287 molx 180 g/mol m = 51, 66 g

PROBLEMA 2 El hidróxido de sodio (Na. OH) es una sustancia que muchas dueñas de casa adquieren en ferreterías como soda cáustica y se utiliza para destapar cañerías. Si una señora compra 1 kg (1000 g)de dicha sustancia, ¿Cuántos moles de hidróxido de sodio adquirió? (M. A. Na: 23 u; O: 16 u; h: 1 u) M = [23 + 16 + 1]g/mol = 40 g/mol n n = = m M 1000 g 40 g/mol m = 25 mol de Na. OH
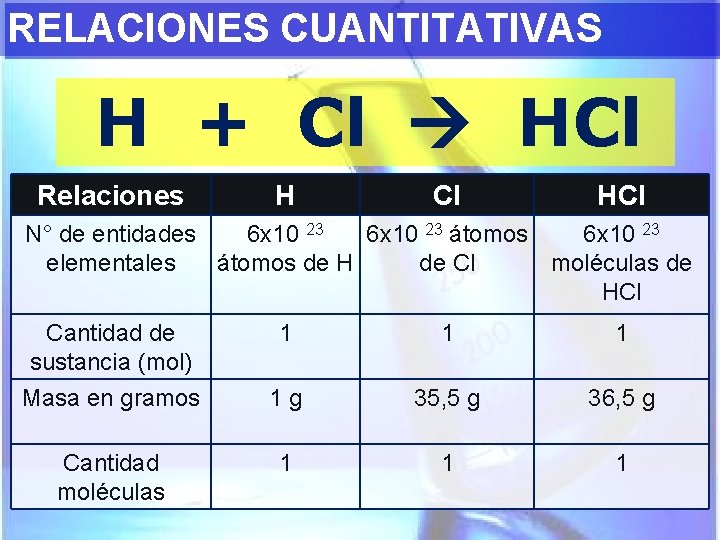
RELACIONES CUANTITATIVAS H + Cl HCl Relaciones H Cl HCl N° de entidades 6 x 10 23 átomos 6 x 10 23 elementales átomos de H de Cl moléculas de HCl Cantidad de sustancia (mol) 1 1 1 Masa en gramos 1 g 35, 5 g 36, 5 g Cantidad moléculas 1 1 1
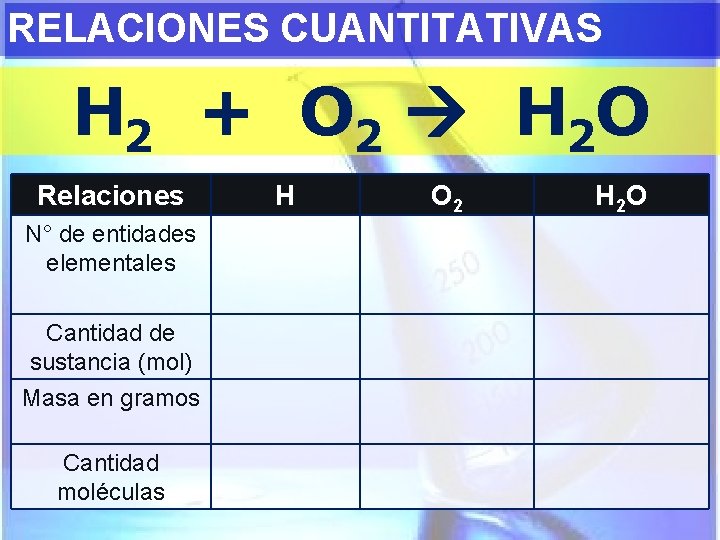
RELACIONES CUANTITATIVAS H 2 + O 2 H 2 O Relaciones N° de entidades elementales Cantidad de sustancia (mol) Masa en gramos Cantidad moléculas H O 2 H 2 O
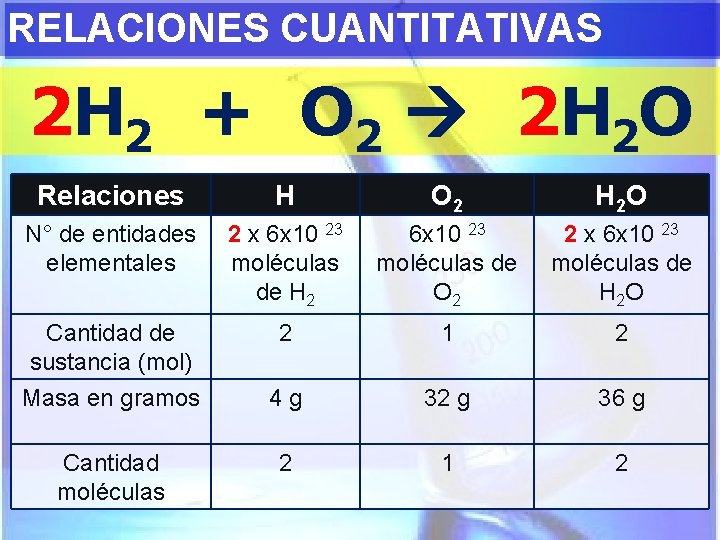
RELACIONES CUANTITATIVAS 2 H 2 + O 2 2 H 2 O Relaciones H O 2 H 2 O N° de entidades elementales 2 x 6 x 10 23 moléculas de H 2 6 x 10 23 moléculas de O 2 2 x 6 x 10 23 moléculas de H 2 O Cantidad de sustancia (mol) 2 1 2 Masa en gramos 4 g 32 g 36 g Cantidad moléculas 2 1 2

RELACIÓN MOLAR • La relación molar o método mol a mol, corresponde a la relación entre la cantidad de moles entre dos de las especies que participan en la reacción. Por ejemplo, si observamos la reacción de combinación del agua se tiene:

EJEMPLO 1 Paso 1: Determinar el número de moles de la sustancia inicial.

EJEMPLO 1 Paso 2: Determinar la relación molar de la sustancia deseada a la sustancia inicial. A partir de la cual es posible calcular la cantidad de moles que se formarán de CO 2. 1 mol de C 6 H 12 O 6 6 mol CO 2 Si: X = 2 mol de C 6 H 12 O 6 X mol CO 2 6 mol CO 2 x 2 mol de C 6 H 12 O 6 1 mol de C 6 H 12 O 6 = X = 12 mol de CO 2

EJEMPLO 1 Paso 3: Transformar el resultado a masa en gramos. La Masa Molar del CO 2 es 44 g/mol. m=nx. M m = 12 mol x 44 g/mol m = 528 g de CO 2 Respuesta: Se obtendrán 528 g de CO 2 al reaccionar 2 moles de glucosa (C 6 H 12 O 6)

REACTIVO LIMITANTE • En los procesos químicos existe un reactivo que limita la cantidad de productos que se pueden obtener durante una reacción, denominado reactivo limitante.

CONCEPTOS • Reactivo. Limitante: Reactivo que se consume primero en una reacción química. La cantidad máxima de producto que se forma depende de la cantidad de este reactivo. • Reactivo Excedente: Son los reactivos presentes en mayor cantidad que la necesaria para reaccionar con la cantidad de reactivo limitante.

EJEMPLO La reacción entre el aluminio y el óxido de hierro (III) puede producir temperaturas cercana a los 3000°C, lo que se utiliza para soldar metales: 2 Al + Fe 2 O 3 Al 2 O 3 + 2 Fe En un proceso se hicieron reaccionar 81 g de Al con 320 g de Fe 2 O 3. Determinar el reactivo limitante y la cantidad en gramos de Al 2 O 3 que se produce. n Al n Fe 2 O 3 = = 81 g 27 g/mol 320 g 160 g/mol n Al = n Fe 2 O 3 = 3 mol 2 mol
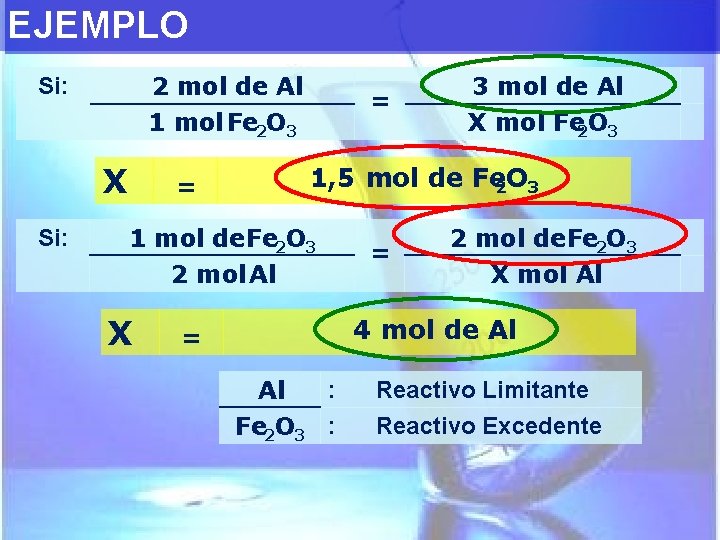
EJEMPLO 2 mol de Al 1 mol Fe 2 O 3 Si: X Si: = = 1, 5 mol de Fe 2 O 3 1 mol de Fe 2 O 3 2 mol Al X 3 mol de Al X mol Fe 2 O 3 = 2 mol de Fe 2 O 3 X mol Al 4 mol de Al = : Al Fe 2 O 3 : Reactivo Limitante Reactivo Excedente

EJEMPLO • La cantidad de Al 2 O 3 se determina con la cantidad de reactivo limitantes presente. Así, que: 2 mol de Al 1 mol Al 2 O 3 Si: X = m=nx. M m = = 3 mol de Al X mol Al 2 O 3 1, 5 mol de Al 2 O 3 m = 1, 5 mol x 102 g/mol 153 g de Al 2 O 3 Respuesta: Se producen 153 g de Al 2 O 3

Colegio Andrés Bello Chiguayante Muchas Gracias
- Slides: 45