Colegio Andrs Bello Chiguayante ESTEQUIOMETRA II Jorge Pacheco

Colegio Andrés Bello Chiguayante ESTEQUIOMETRÍA II Jorge Pacheco R. Profesor de Biología y Química

ESTEQUIOMETRÍA II APRENDIZAJESESPERADOS: • Aplican la información de una ecuación química. • Identifican los factores que limitan la formación de un compuesto en una reacción química. • Infieren el rendimiento real y teórico a partir de los datos estequiométricos de algunas reacciones químicas.
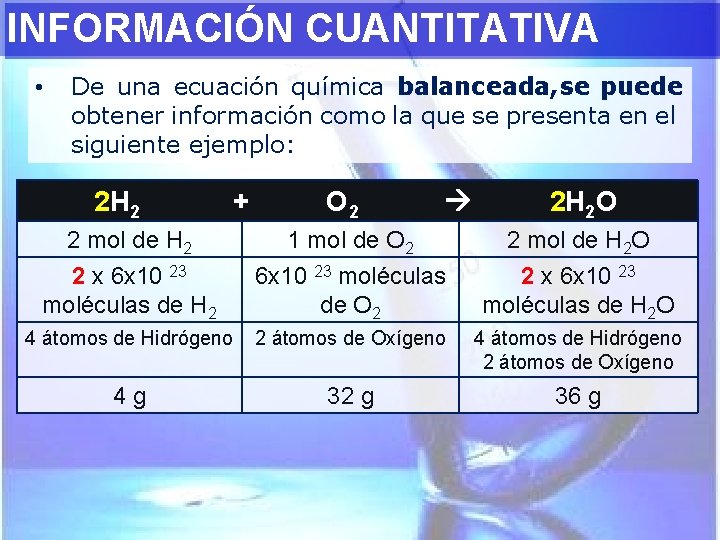
INFORMACIÓN CUANTITATIVA • De una ecuación química balanceada, se puede obtener información como la que se presenta en el siguiente ejemplo: 2 H 2 + O 2 2 H 2 O 2 mol de H 2 2 x 6 x 10 23 moléculas de H 2 1 mol de O 2 6 x 10 23 moléculas de O 2 2 mol de H 2 O 2 x 6 x 10 23 moléculas de H 2 O 4 átomos de Hidrógeno 2 átomos de Oxígeno 4 g 32 g 36 g

INFORMACIÓN CUANTITATIVA Balance de Ecuaciones Vídeo Reacciones Químicas

TIPOS DE REACCIÓN QUÍMICA A) REACCIÓN DE COMBINACIÓN: • Tipo de reacción en las que se combinan dos reactivos, que pueden ser elementos o compuesto, para formar un solo producto, según la siguiente ecuación general: . Ejemplo: Reacción del aluminio metálico con oxígeno para formar el óxido de aluminio.

TIPOS DE REACCIÓN QUÍMICA B) REACCIÓN DE DESCOMPOSICIÓN: • En este tipo de reacción una sustancia se descompone o “rompe”, produciendo dos o más sustancias distintas, de acuerdo con el siguiente mecanismo general.

TIPOS DE REACCIÓN QUÍMICA C) REACCIÓN DE SUSTITUCIÓN SIMPLE: Tipo de reacción en donde un elemento reacciona con un compuesto para reemplazar uno de sus componentes, produciendo un elemento y un compuesto diferentes a los originales:

TIPOS DE REACCIÓN QUÍMICA D) REACCIÓN DE SUSTITUCIÓN DOBLE: • En este tipo de reacciones, dos compuestos intercambian sus elementos entre sí, produciendo dos compuestos distintos, de acuerdo al siguiente mecanismo general. AB + CD AD + CB

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química no balanceada identifica: el Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas (reactivos y productos) y masa en gramos. C 3 H 8 + 5 O 2 3 CO 2 + 4 H 2 O REACCIÓN DE SUSTITUCIÓN DOBLE 1 mol de C 3 H 8 6, 02 x 1023 moléculas de C 3 H 8 44 g 5 mol de O 2 3 mol de CO 2 3, 01 x 1024 moléculas de O 2 1, 81 x 1024 moléculas de CO 2 160 g 132 g 4 mol de H 2 O 2, 41 x 1024 moléculas de H 2 O 72 g
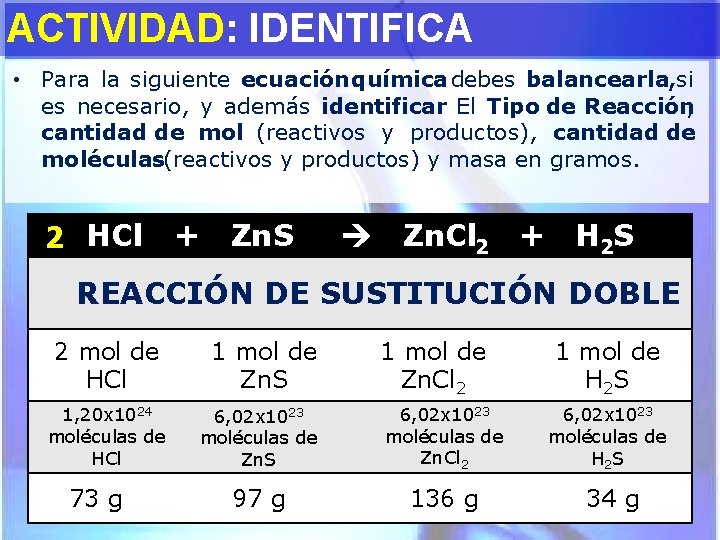
ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 HCl + Zn. S Zn. Cl 2 + H 2 S REACCIÓN DE SUSTITUCIÓN DOBLE 2 mol de HCl 1, 20 x 1024 moléculas de HCl 73 g 1 mol de Zn. S 1 mol de Zn. Cl 2 6, 02 x 1023 moléculas de Zn. S 6, 02 x 1023 moléculas de Zn. Cl 2 97 g 136 g 1 mol de H 2 S 6, 02 x 1023 moléculas de H 2 S 34 g

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 Al + 3 Br 2 2 Al. Br 3 REACCIÓN DE COMBINACIÓN 2 mol de Al 1, 20 x 1024 átomos de Al 54 g 3 mol de Br 2 2 mol de Al. Br 3 1, 81 x 1024 moléculas de Br 2 1, 20 x 1024 moléculas de Al. Br 3 480 g 534 g

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. Fe + Cu. SO 4 Cu + Fe. SO 4 REACCIÓN DE SUSTITUCIÓN SIMPLE 1 mol de Fe 6, 02 x 1023 átomos de Fe 56 g 1 mol de Cu. SO 4 1 mol de Cu 6, 02 x 1023 moléculas de Cu. SO 4 6, 02 x 1023 átomos de Cu 159, 5 g 63, 5 g 1 mol de Fe. SO 4 6, 02 x 1023 moléculas de Fe. SO 4 152 g

ACTIVIDAD: IDENTIFICA • Para la siguiente ecuación química debes balancearla, si es necesario, y además identificar : El Tipo de Reacción, cantidad de mol (reactivos y productos), cantidad de moléculas(reactivos y productos) y masa en gramos. 2 H 2 O 2 2 H 2 O + O 2 REACCIÓN DE DESCOMPOSICIÓN 2 mol de H 2 O 2 1, 20 x 1024 moléculas de H 2 O 2 68 g 2 mol de H 2 O 1 mol de O 2 1, 20 x 1024 moléculas de H 2 O 6, 02 x 1023 moléculas de O 2 36 g 32 g

ESTEQUIOMETRÍA, CÁLCULO A PARTIR DE REACCIONES QUÍMICAS

ESTEQUIOMETRÍA • Determinar la cantidad de “materiales” que serán empleados en la ejecución de una determinada tarea es un principio básico de eficienciaen toda profesión u oficio. Por ejemplo, un maestro albañil debe calcular la cantidad de arena, ripio y cemento necesaria para construir un piso o un muro, de lo contrario aumenta innecesariamente el costo del muro y tendrá que desperdiciar o botar lo que sobra. • Esta misma situación se aplica a la química; los científicos en los laboratorios de investigación o en laboratorios con fines industriales deben determinar la cantidad de materiales que necesitan para elaborar un determinado producto y así proceder a ejecutar las reacciones químicas que sean necesarias.

RELACIÓN MOLAR • La relación molar o método mol a mol, corresponde a la relación entre la cantidad de moles entre dos de las especies que participan en la reacción. Por ejemplo, si observamos la reacción de combinación del agua se tiene:

EJEMPLO 1 Paso 1: Determinar el número de moles de la sustancia inicial.

EJEMPLO 1 Paso 2: Determinar la relación molar de la sustancia deseada a la sustancia inicial. A partir de la cual es posible calcular la cantidad de moles que se formarán de CO 2. 1 mol de C 6 H 12 O 6 6 mol CO 2 Si: X = 2 mol de C 6 H 12 O 6 X mol CO 2 6 mol CO 2 x 2 mol de C 6 H 12 O 6 1 mol de C 6 H 12 O 6 = X = 12 mol de CO 2

EJEMPLO 1 Paso 3: Transformar el resultado a masa en gramos. La Masa Molar del CO 2 es 44 g/mol. m=nx. M m = 12 mol x 44 g/mol m = 528 g de CO 2 Respuesta: Se obtendrán 528 g de CO 2 al reaccionar 2 moles de glucosa (C 6 H 12 O 6)

EJEMPLO 2 Paso 1: Determinar el número de moles de la sustancia inicial. La Masa Molar del N 2 O es 44 g/mol. n = n m M n = = 8, 75 g 44 g/mol 0, 199 mol N 2 O

EJEMPLO 2 Paso 2: Determinar la relación molar de la sustancia deseada a la sustancia inicial. 10 mol de HNO 3 1 mol N 2 O Si: X = X mol de HNO 3 0, 199 mol N 2 O 10 mol de HNO 3 x 0, 199 mol de N 2 O 1 mol de N 2 O = 1, 99 mol de HNO 3

EJEMPLO 2 Paso 3: Transformar el resultado a masa en gramos. La Masa Molar del HNO 3 es 63 g/mol. m=nx. M m = 1, 99 mol x 63 g/mol m = 125, 37 g de HNO 3 Respuesta: Son necesarios 125, 37 g de HNO 3

EJERCICIOS 1. El metano se quema de acuerdo con la siguiente ecuación (M. A. C= 12, H=1; O=16). CH 4(g) + O 2(g) CO 2(g) + H 2 O(g) ¿Cuántos gramos de CO 2 se producen cuando se queman 8 g de CH 4? 2. ¿Qué masa de magnesio se necesita para que reaccione con 9, 27 g de nitrógeno? La ecuación que explica el proceso es (M. A. Mg= 24; N= 14). Mg(s) + N 2(g) Mg 3 N 2

REACTIVO LIMITANTE

REACTIVO LIMITANTE • En los procesos químicos existe un reactivo que limita la cantidad de productos que se pueden obtener durante una reacción, denominado reactivo limitante.

CONCEPTOS • Reactivo. Limitante: Reactivo que se consume primero en una reacción química. La cantidad máxima de producto que se forma depende de la cantidad de este reactivo. • Reactivo Excedente: Son los reactivos presentes en mayor cantidad que la necesaria para reaccionar con la cantidad de reactivo limitante.

EJEMPLO La reacción entre el aluminio y el óxido de hierro (III) puede producir temperaturas cercana a los 3000°C, lo que se utiliza para soldar metales: 2 Al + Fe 2 O 3 Al 2 O 3 + 2 Fe En un proceso se hicieron reaccionar 81 g de Al con 320 g de Fe 2 O 3. Determinar el reactivo limitante y la cantidad en gramos de Al 2 O 3 que se produce. n Al n Fe 2 O 3 = = 81 g 27 g/mol 320 g 160 g/mol n Al = n Fe 2 O 3 = 3 mol 2 mol

EJEMPLO 2 mol de Al 1 mol Fe 2 O 3 Si: X Si: = = 1, 5 mol de Fe 2 O 3 1 mol de Fe 2 O 3 2 mol Al X 3 mol de Al X mol Fe 2 O 3 2 mol de Fe 2 O 3 X mol Al = 4 mol de Al = Al Fe 2 O 3 : : R. L. R. E.

EJEMPLO • La cantidad de Al 2 O 3 se determina con la cantidad de reactivo limitantes presente. Así, que: 2 mol de Al 1 mol Al 2 O 3 Si: X = m=nx. M m = = 3 mol de Al X mol Al 2 O 3 1, 5 mol de Al 2 O 3 m = 1, 5 mol x 102 g/mol 153 g de Al 2 O 3 Respuesta: Se producen 153 g de Al 2 O 3

EJERCICIOS 1. Considerando la siguiente ecuación, ¿cuánto ácido sulfúrico en gramos (H 2 SO 4) se puede formar a partir de 5 mol de dióxido de azufre (SO 2) y 2 mol de oxígeno (O 2) (M. A. S= 32, H=1; O=16). 2 SO 2(g) + O 2(g) 2 H 2 O(g) + 2 H 2 SO 4(ac) 2. El proceso para la producción de amoniaco (NH 3) se representa mediante la siguiente ecuación balanceada: N 2(g) + 3 H 2(g) 2 NH 3(g). (M. A. N= 14, H= 1). A. ¿Cuántos g de NH 3 (amoniaco) se pueden obtener a partir de 100 g de N 2 y 100 g H 2. B. ¿Cuál el reactivo limitante y cuál el reactivo en exceso? C. Determina la cantidad de g de reactivo en exceso queda al final de la reacción.

RENDIMIENTO DE LA REACCIÓN • Rendimiento. Teórico: Es la cantidad calculada de producto que se puede obtener a partir de una determinada cantidad dada de reactivo, de acuerdo con la ecuación química. • Rendimiento. Real: Es la cantidad de producto que efectivamente se obtiene en una reacción. • Rendimiento. Porcentual: Corresponde a la relación real entre el rendimiento teórico y el real.

EJEMPLO • Se prepara bromuro de plata (Ag. Br) haciendo reaccionar 200 g de bromuro de magnesio (Mg. Br) con la cantidad adecuada de nitrato de plata (Ag. NO 3). ¿Cuál será el rendimiento porcentual de la reacción si se obtienen 375 g de bromuro de plata? Mg. Br 2 + 2 Ag. NO 3 Mg(NO 3)2 + 2 Ag. Br PASO 1: Sabiendo que la masa molecular de Mg. Br 2= 184, 13 g/mol, se calcula la cantidad de sustancia (mol) a la que equivalen 200 g de Mg. Br 2. n = 1, 09 moles.

EJEMPLO Paso 2: Determinar la relación molar de la sustancia deseada a la sustancia inicial. Si: 1 mol de Mg. Br 2 2 mol Ag. Br X = = 1, 09 mol de Mg. Br 2 X mol Ag. Br 2, 18 mol de Ag. Br Sabiendo que la masa molar del Ag. Br es 187, 8 g/mol, se obtiene que su masa es: m=nx. M m = 2, 18 mol x 187, 8 g/mol 409, 4 g de Ag. Br

EJEMPLO Paso 3: Para determinar el rendimiento de la reacción se compara el rendimiento real (375 g) con el teórico (409, 4 g). Rendimiento porcentual = Rendimiento real Rendimiento teórico x 100 = 375 g 409, 4 g x 100 Rendimiento porcentual = 91, 59 %

EJERCICIOS • En un experimento se obtuvieron 3, 43 g de SOCl 2. esta reacción tiene un rendimiento teórico de 5, 64 g de SOCl 2. considerando que la ecuación química es: SO 2 + PCl 5 SOCl 2 + POCl 3 Determina el rendimiento porcentual de la reacción. • El cloruro de calcio con nitrato de plata para producir un precipitado de cloruro de plata de acuerdo a la siguiente ecuación: Ca. Cl 2(ac) + Ag. NO 3(ac) Ag. Cl(s) + Ca(NO 3)2(ac) En un experimento se obtienen 1, 864 g de precipitado (sólido). Si el rendimiento teórico del cloruro de plata es 2, 45 g, ¿cuál es el rendimiento porcentual de la reacción?

Colegio Andrés Bello Chiguayante Muchas Gracias
- Slides: 36