GRAVIMETRIA ETAPAS DE UMA ANLISE QUMICA Definio do









- Slides: 14

GRAVIMETRIA

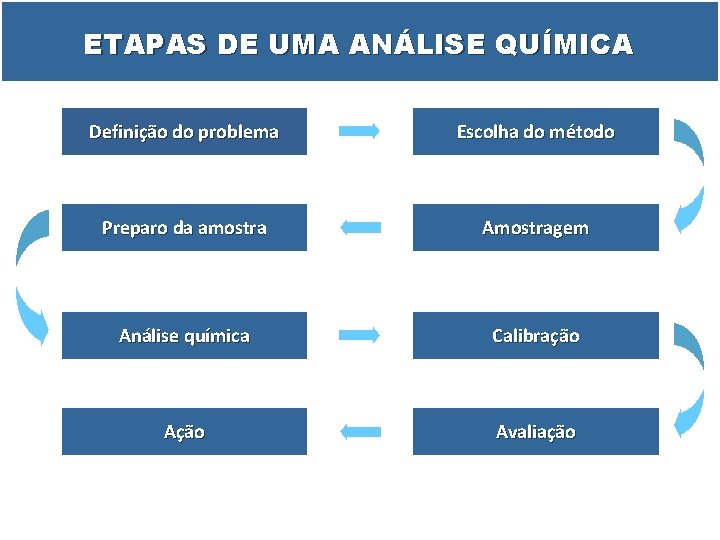
ETAPAS DE UMA ANÁLISE QUÍMICA Definição do problema Escolha do método Preparo da amostra Amostragem Análise química Calibração Avaliação

PRÁTICA 3 – G RAVIMETRIA Análise Gravimétrica – Determinação de água de cristalização em sais • Objetivo: Introdução da análise gravimétrica: determinação de água de cristalização em sólidos.

Procedimento • Preparo do cadinho (etapas já realizadas) – Colocar o cadinho de porcelana numerado em mufla e aquecer a 500°C por 30 min. – Retirar o cadinho da mufla, colocar em dessecador e esperar esfriar. – Pronto para o uso.

Cadinho de porcelana Mufla Dessecador

Procedimento • Análise química (a serem realizadas) – Pesar o cadinho em balança analítica. Anotar o número e a massa do cadinho (tara). – Pesar 0, 5000 g de um dos sais hidratados (Cu. SO 4. XH 2 O; KAl(SO 4)2. XH 2 O; Mg. SO 4. XH 2 O; Ba. Cl 2. XH 2 O) diretamente no cadinho. Anotar a massa. – Aquecer o cadinho contendo o sal novamente na mufla e aquecer durante 30 minutos a 500°C. – Retirar da mufla o cadinho contendo o resíduo do sal, colocar no dessecador e esperar esfriar. – Pesar o cadinho com o resíduo. Anotar o valor obtido.

Cálculos • Teor de água de cristalização no sal em g kg-1 • Número de mols de água de cristalização por mol do sal.

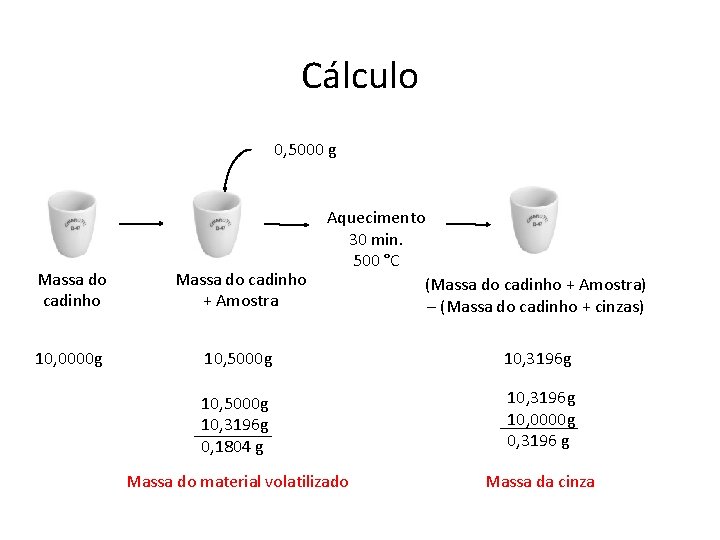
Cálculo 0, 5000 g Aquecimento 30 min. 500 °C (Massa do cadinho + Amostra) – (Massa do cadinho + cinzas) Massa do cadinho + Amostra 10, 0000 g 10, 5000 g 10, 3196 g 0, 1804 g 10, 3196 g 10, 0000 g 0, 3196 g Massa do material volatilizado Massa da cinza

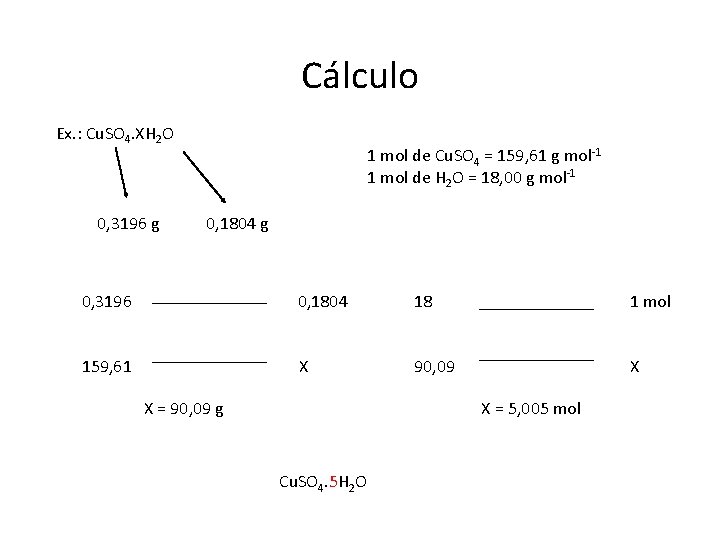
Cálculo Ex. : Cu. SO 4. XH 2 O 0, 3196 g 1 mol de Cu. SO 4 = 159, 61 g mol-1 1 mol de H 2 O = 18, 00 g mol-1 0, 1804 g 0, 3196 0, 1804 18 1 mol 159, 61 X 90, 09 X X = 90, 09 g X = 5, 005 mol Cu. SO 4. 5 H 2 O

ÁGUA DE CRISTALIZAÇÃO

Formas de ocorrência de água nos sólidos • • • Água de cristalização Água higroscópica ou de adsorção Água ocluída Água de embebição Água de constituição

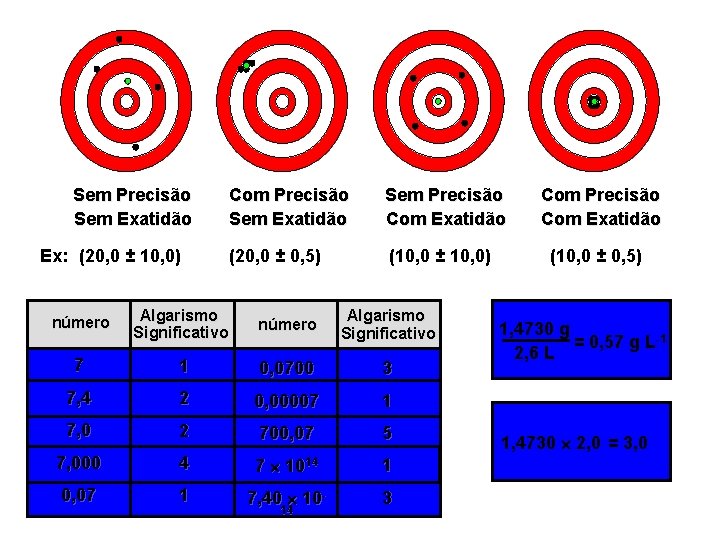
Erros em Química Analítica • Toda teoria envolve alguma incerteza – Erro absoluto ou relativo • Exatidão e Precisão • Tipos de erros – Sistemáticos e aleatórios • Representação do erro de uma medida experimental – Desvio padrão relativo

Sem Precisão Sem Exatidão Ex: (20, 0 ± 10, 0) Com Precisão Sem Exatidão Sem Precisão Com Exatidão (20, 0 ± 0, 5) (10, 0 ± 10, 0) número Algarismo Significativo 7 1 0, 0700 3 7, 4 2 0, 00007 1 7, 0 2 700, 07 5 7, 000 4 7 1014 1 0, 07 1 7, 40 10 - 3 14 Com Precisão Com Exatidão (10, 0 ± 0, 5) 1, 4730 g = 0, 57 g L-1 2, 6 L 1, 4730 2, 0 = 3, 0
