IMUNOLOKA NEREAKTIVNOSTTOLERANCIJA DEFINICIJA Nesposobnost organizma da imunoloki reaguje

IMUNOLOŠKA NEREAKTIVNOSTTOLERANCIJA

DEFINICIJA: • Nesposobnost organizma da imunološki reaguje na na • • nadražaj specifičnim Ag-om. Prirodna (urođena)-nastala u toku intrauterinog razvoja ploda Stečena – kasnije , u toku života Zavisi od: imunološke kompetencije i genetske konstitucije jedinke prirode Ag, njegove količine i načina aplikacije
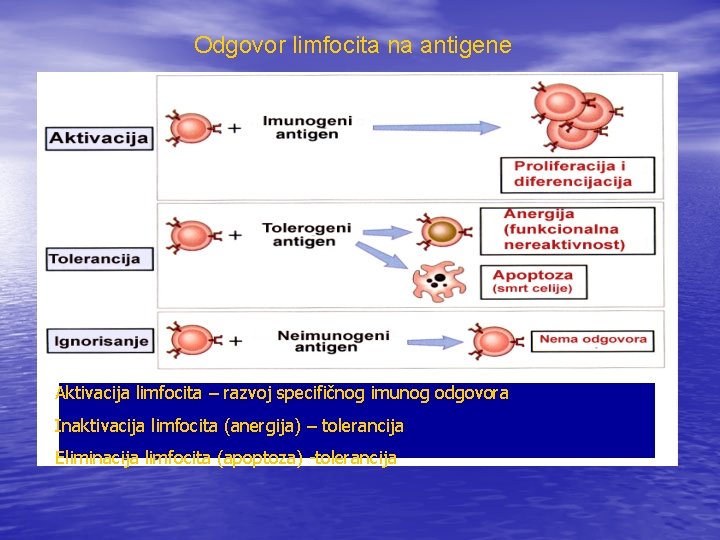
Odgovor limfocita na antigene Aktivacija limfocita – razvoj specifičnog imunog odgovora Inaktivacija limfocita (anergija) – tolerancija Eliminacija limfocita (apoptoza) -tolerancija

Vrste antigena • Imunogeni antigeni –su antigeni mikroorganizama, • • dovode do imunog odgovora Tolerogeni antigeni- sopstveni antigeni indukuju toleranciju u kojoj limfociti bivaju funkcionalno inakivisani ili ubijeni Ignorisanje –limfociti ne primećuju prisustvo najčešće sopstvenih antigena

Imunološka tolerancija ili specifična nereaktivost • stanje nastalo aktivnim procesom, • kontaktom imunološkog sistema sa dotičnim antigenom, • kada dolazi do pormena u specifičnom klonu limfocita u smislu njegove inaktivacije ili blokade delovanja

Imunološka tolerancija u užem smislu • • • centralna nereaktivnost, dolazi do inaktivacije specifičnog klona limfocita, izostaje njegovo sazrevanje i stvaranje efektora imunološke reakcije na sopstvene antigene u centralnim limfnim organima

Imunološka tolerancija u širem smislu • Periferna nereaktivnost • Ako je došlo do aktivacije spcifičnog klona limfocita i nastanka efektora imunološke reakcije, njihovo dalje stvaranje ili delovanje na sopstvene antigene u perifernim tkivima, zakočno raznim mehanizmima potiskivanja i imunoregulacijom

Nespecifična nereaktivnost • • • Odnosi se na sve ili većinu antigena i može biti posledica: naslednog poremećaja imunološke reaktivnosti -urođena ili primarna imunodeficijecija, sekundarna imunodeficijencija u toku neke bolesti, ili posle primene imunosupresiva

PRIRODNA (urođena) IMUNOLOŠKA TOLERANCIJA na sopstvene Ag • Razvuja se intrauterino • Kada imunološki sistem u svojoj nezreloj fazi • (prenanalno i perinatalno ) dođe u kontakt sa Ag umesto da nastane sepcifična stimulacija i aktivacija određenog klona limfocita, dolazi do njegove inaktivacije Ovakva reakcije je rezultat imunološke nezrelosti limfocita i APĆ.
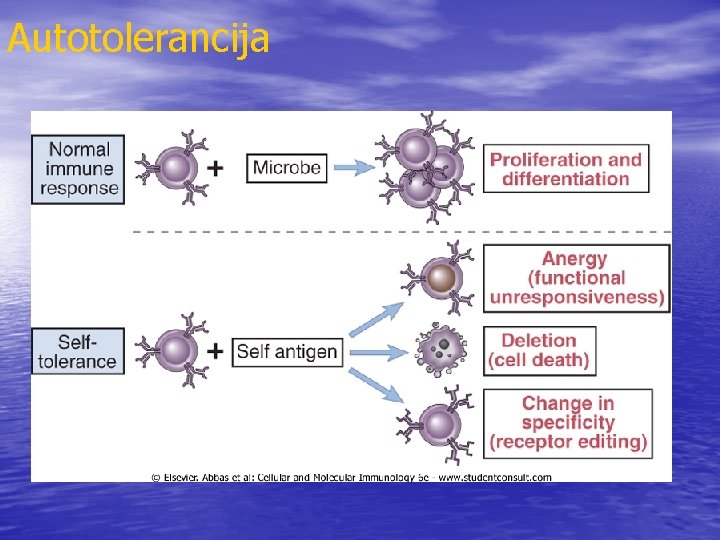
Autotolerancija

Autotolerancija- sopstveni antigeni normalno indukuju toleranciju Indukcija tolerancije limfocita na određeni Ag može biti korisna u sprečavanju ili kontroli neželjene imunološke reakcije: lečenje alergija lečenje autoimunih bolesti prevencija odbacivanja transplantiranih organa

Urođena tolerancija • Imunološki sistem in utero dolazi u dodir samo sa • • sopstvenim Ag-koji su izloženi i dostupni prepoznavanju od imunološkog sistema, ne dolazi u kontakt sa stranim Ag Razvija se tolerancija prema sopstvenim Ag

kako nastaje? • nastaje intrauterino procesom eliminacije klonova • • limfocita koji bi posnatalno reagovali sa sopstvenim Ag To je Burnetova teorija klonske selekcije: u toku sazrevanja iminološkog reagovanja i nereagovanja dolazi do pozitivne i negativne selekcije u timusu- važnu ulogu imaju timusne epitelne ćelije i druge APĆ.

Uloga timusa • • timusni epitel, timozin i timopoetin važni su u sticanju: imunološke kompetentnosti, imunološke reaktivnosti i prepoznavanju stranog i sopstvenog

Da je Intrauterino razvijanje tolerancije proces, dokazano I eksperimentalno • ako se u ranoj fazi intrauterinog razvoja odstrani neki organ, i čuva in vitro da bi se diferencirao, a zatim transplantira životinji u odraslom dobu , ona ga odbacuje kao stran, pošto se intrauterino nije razvila prirodna tolerancija

Indukovana tolerancija • inokulacijom solubilnih i korpuskularnih Ag • životinjama u toku intauterinog razvoja moguće je izaivati imunološku toleranciju na Ag u posnatalnom periodu Indukovana tolerancija na solubilne Ag traje kraće od korpuskularnih Ag, ali u oba slučaja za održavanje tolerancije neophodno je dodavati strane Ag

Sopstveni Ag • Sopstveni Ag zadovoljavaju uslov doživotne tolerancije: • Prisutni su in utero i dostupni su imunološkom aparatu za prepoznavanje i ostaju stalno prisutni u organizmu posnatalno

Imunološki sekvestrirana tkiva • Neka sopstvena tkiva anatomski su izolovana od • • • limforetikularnog sistema, nisu nikada u kontaktu sa cirkulacijom Ona se ne prihvataju kao sopstvena, na njih nije nastala prirodna tolerancija u toku intrauterinog razvoja To su: Ag uvealnog tkiva i očnog sočiva, mozga, tireoidne žlezde, majčinog mleka, spermatozoida posnatalno ako dođu u kontakt sa imunološkim sistemom nastaju autoimune bolesti

SPECIFIČNA TOLERANCIJA U ODRASLOM DOBU • Što je organizam imunološki zreliji u posnatalnom • • • periodu to je teže izazvati imunološku toleranciju Ona je moguća kod imunosuprimiranih I ako se radi o solubilnim Ag Facilitirajući efekat Ig. A i Ig. G 4 antitela koja ne vezuju Complement: vezuju se za receptore na površini ćelija alotransplantata i sprečavaju delovanje citotoksičnih T limfocita.

Faktori koji utiču na toleranciju • Zrelost imunološkog sistema obrnuto je strazmerna • • imunološkoj toleranciji Genetska konstitucija domaćina: osobe koje boluju od Wiskott-Aldrich-ovog sindroma ne reaguju na polisaharidne Ag Imunološka nereaktivnost je posledica odsustva odgovarajućih gena, jer ukupnu imunološku reaktivnost nadziru geni

Svojstva antigena • Da li će organizam reagovati na Ag imunim odgovorom ili • • • tolerancijom zavisi od: prirode Ag, odnosno strukuture Količine (doze Ag) Put njegovog unošenja

Priroda antigena • Što je veća imunogenost Ag , manja je mogućnost • • njegovog tolerogenog delovanja Rastorljive supstance, zaobilaze makrofage kao APĆlakše izazivaju toleranciju Agregirani, slepljeni molekuli ili čestice bolji su imunogeni, mikroorganizmi i njihovi produkti-teže dovode do tolerancije

Relativna molekulska masa • RMM i veličina Ag obrnuto su srazmerne njihovoj • • sposobnosti da dovedu do tolerancije Ag koji su polimeri, tj timus nezavisni teže dovode do tolerancije Kada se razgrade na monomere , postaju dobri tolerogeni (manja RMM i veličina, a specifičnost ostaje nepromenjena)

Tolerancija na Ag alotransplantata • Može se postići unošejem velikih doza mrtvih ćelija • dotičnog tkiva ili ćelijskih ekstrakata tog tkiva pre transplantacije tzv. preimunizacija Nasuprot tome preimunizacija živim ćelijama pojačava reakciju odbacivanja kalema

Način unošenja antigena • Intravensko unošenje solubilnih Ag pogoduje toleranciji • Limfociti bivaju izloženi prevelikoj dozi Ag, dolazi do • blokade receptora što dovodi do njihove inaktivacije Intradermalno i subkutano unošenje izaziva imunološku reakciju

Brzina zlučivanja Ag • Ag koji se brzo izlučuju iz organizma , lakše izazivaju • toleranciju Imunogeni koji su lako rastvorljivi ili sasvim nerastvorljivi ćešće izazivaju toleranciju

Doza antigena • Imunološka tolerancija velikih doza- veće od maksimalne • je imunološka paraliza, (prevelik nadražaj imunološkog klona limfocita , bez stvaranja ćelija memorije) Doza manja od minimalne- tolerancija malih doza

Celularne osnove tolerancije • Kod timus zavisnih Ag, dovoljno je da postoji tolerancija • • • samo jedne od dve vrste limfocita (T ili B limfociti) da bi se ispoljila tolerancija Lakše je postići toleranciju T limfocita od B limfocita Pri toleranciji malih doza, tolerantni su T limfociti, a pri toleranciji velikih doza tolerantni su i T i B limfociti (tolerancija na nosač i hapten) Tolerancija T limfocita nastaje ranije od B limfocita, nakon unošenja Ag i traje duže

Kompeticija antigena • Kompeticija raznih Ag dovodi do tolerancije na Ag • Ako se istovremeno ili nešto pre inokuliše drugi • imunološki nesrodan Ag nastaje tolerancija na prvi Ag Tolerancija izazvana ćelijama dugotrajna izazvana neživim materijama , serumskim proteinima se gubi

Održavanje tolerancije na sopstvene antigene • Tolerancija na sopstvene Ag je proces koji je aktivno • • • stečen ili naučen proces u kome su autoreaktivni limfociti eliminisani ili sprečeni da budu funkcionalno reaktivni na sopstvene Ag ili ostaju nereaktivni nakon antigenskog podsticaja to je tzv. Centralna tolerancija ona obezbeđuje da limfociti koji postignu funkcionalnu zrelost , napuste primarne limfatične organe i nasele periferna tkiva očišćeni od klonova koji bi mogli da reaguju na sopstvene Ag
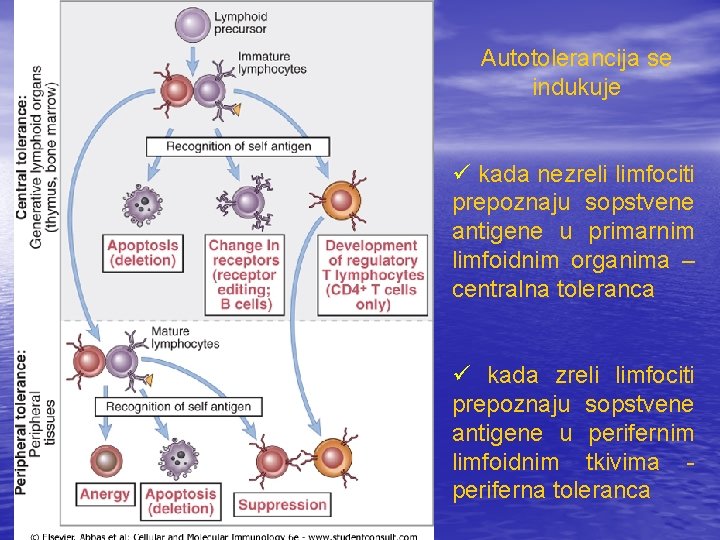
Autotolerancija se indukuje ü kada nezreli limfociti prepoznaju sopstvene antigene u primarnim limfoidnim organima – centralna toleranca ü kada zreli limfociti prepoznaju sopstvene antigene u perifernim limfoidnim tkivima periferna toleranca

Periferna tolerancija • Autoreaktivni limfociti koji izbegnu ovaj proces selekcije i • • nastave sa sazrevanjem, u perifernm tkivima, mogu da budu inaktivisani usled susreta sa sopstveim antigenima –destrukcijom-proces aktivisanja ćelijske smrti i klonskom anergijom tj. vezivanjem Ag za specifične receptore

Mehanizam nastanka T limfocitne tolerancije na sopstvene Ag • Centralna tolerancija na sopstvene Ag, • odigrava se u timusu , prilikom sazrevanja T ćelija, • negativnom selekcijom To je brisanje ili destrukcija klonova nezrelih T limfocita u timusu, koji su specifični za sopstvene Ag vezanih u kompleks sa HLA molekulima na površini timusnih ćelija
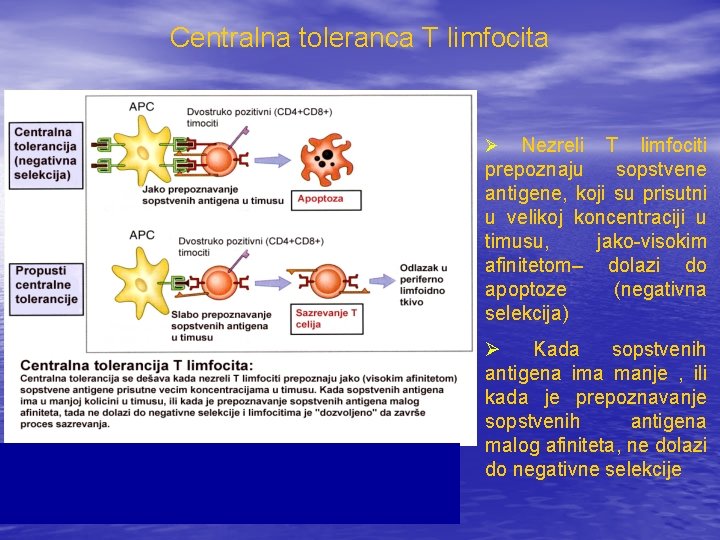
Centralna toleranca T limfocita Nezreli T limfociti prepoznaju sopstvene antigene, koji su prisutni u velikoj koncentraciji u timusu, jako-visokim afinitetom– dolazi do apoptoze (negativna selekcija) Ø Ø Kada sopstvenih antigena ima manje , ili kada je prepoznavanje sopstvenih antigena malog afiniteta, ne dolazi do negativne selekcije

Periferna ili ekstratimusna tolerancija T-ćelija neke autoreaktivne T-ćelije izbegnu negativnoj selekcji u timusu, dožive sazrevanje i dospeju u periferna tkiva u njima bivaju suprimirani ili dolazi do smrti autoreaktivnih limfocita

Periferna tolerancija T limfocita Indukuje se kada zreli T limfociti prepoznaju autoantigene u perifernom limfoidnom tkivu Mehanizmi periferne tolerancije su: 1. Funkcionalna inaktivacija (anergija) 2. Smrt autoreaktivnih limfocita 3. Aktivna supresija autoreaktivnih limfocita

Anergija • Anergija je funkcionalna inaktivacija T limfocita , kada • • prepoznaju antigen bez odgovarajućeg nivoa kostimulatora (drugih signala) koji su neophodni za potpunu aktivaciju T –limfocita. Za aktivaciju T-limfocita neophodna su dva signala: signal 1 je uvek antigen, signa 2 obezbeđuju kostimulatori na APĆ (B 7 proteini) Sigal 1 , bez odgovarajućeg signala 2 indukuje dugotrajnu anergiju T- ćelija ili odsustvo imunog odgovora

Delecija: smrt autoreaktivnih limfocita • Prepoznavanje sopstvenih antigena bez drugih signala indukuje apoptozu koja dovodi do eliminacije (delecije) autoreaktivnih limfocita

Aktivna supresija autoreaktivnih limfocita • Posle susreta sa antigenom, neki autoreaktivni T-limfociti • mogu da se razviju u regulatorne ćelije , čija je funkcija da spreče ili suprimiraju aktivnost drugih štetnih autoreaktivnih limfocita To su CD 4+ ćelije koje luče citokine: IL-10 koji sprečava aktivaciju limfocita i makrofaga

Tolerancija B-limfocita • Sopstveni polisaharidi, lipidi i nukleinske kiseline su T- nezavisni antigeni , njih ne prepoznaju T-limfociti. Ovi antigeni indukuju toleranciju B-limfocita da bi se sprečila produkcija autoantitela
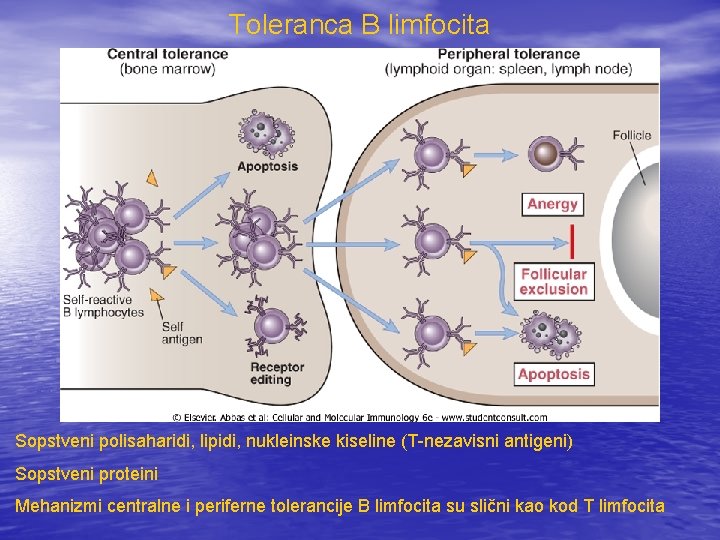
Toleranca B limfocita Sopstveni polisaharidi, lipidi, nukleinske kiseline (T-nezavisni antigeni) Sopstveni proteini Mehanizmi centralne i periferne tolerancije B limfocita su slični kao kod T limfocita

Centralna tolerancija B-limfocita • Kada nezreli B limfociti reaguju sanžno sa svojim • • antigenima u koštanoj srži, oni ili umiru (negativna selekcija) ili izmene specifičnost svog receptora
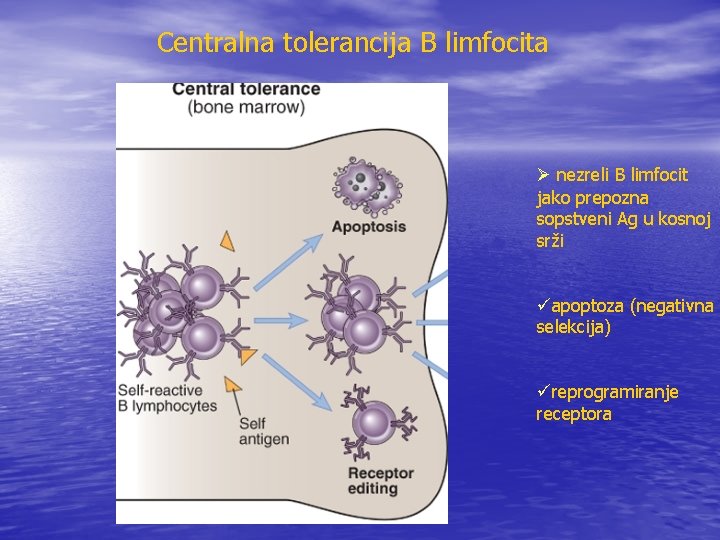
Centralna tolerancija B limfocita Ø nezreli B limfocit jako prepozna sopstveni Ag u kosnoj srži üapoptoza (negativna selekcija) üreprogramiranje receptora

Negativna selekcija B-limfocita • Negativna selekcije B-ćelija eliminiše limfocite koji imaju receptore visokog afiniteta za sopstvene membranske ili solubilne antigene prisutne u velikoj količini i široko rasprostranjene

Promena specifičnosti receptora • Nakon prepoznavanja sopstvenih antigena aktivira se rekombinacija imunoglobulinskih gena, tako da se eksprimira novi Ig laki lanac koji sa postojećim Ig teškim lancem daje nov receptor za antigen koji nije specifičan za sopstveni antigen

Periferna tolerancija B-ćelija • Kada zreli B-limfociti dođu u dodir sa visokim • • • koncentracijama sopstvenog antigena u perifernom limfnom tkivu, postaju anergični i ne mogu ponovo da odgovore na taj antigen. Ako B-ćelije prepoznaju neki antigen, a ne prime pomoć od T-ćelija (pošto njih nema ili su tolerantne), B ćelije postaju anergične. T-nezavisni antigeni mogu da aktiviraju B limfocite bez pomoći T –ćelija samo kada takvi antigeni pokreću jake signale u B-ćelijama. Anergične B- ćelije napuštaju limfne folikule i više se ne vraćaju u njih, dolazi do njihove apoptoze
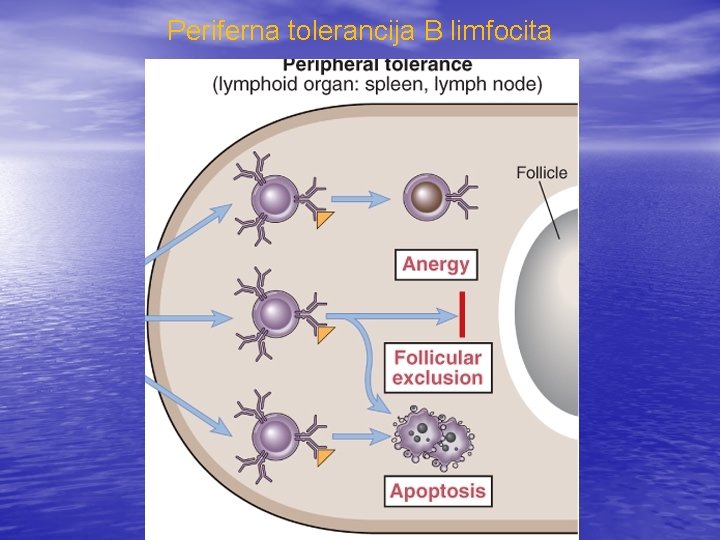
Periferna tolerancija B limfocita

• Pod normalnim uslovima tolerancija na sopstvene • proteine najefikasnije se održava preko tolerancije Tćelija. B limfociti koji su reaktivni na sopstvene Ag mogu da prežive i da sazru, ali neće proizvoditi autoantitela visokog afiniteta, niti dovesti do autoimune bolesti zbog postojanja tolerancije T-helper limfocita.
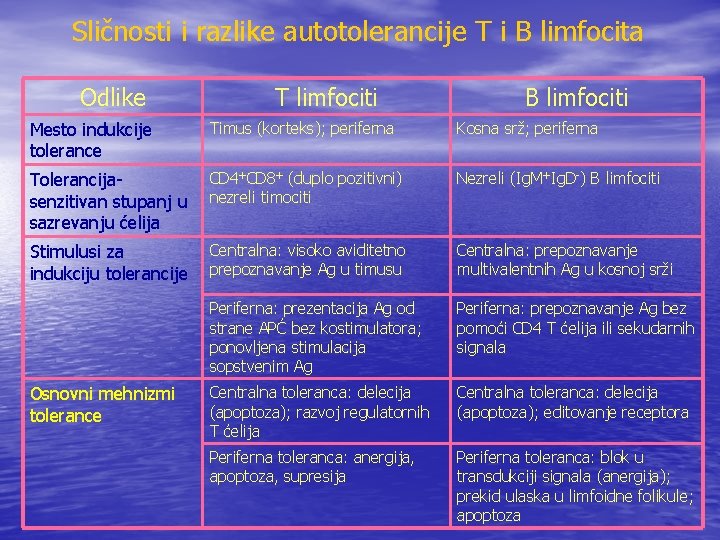
Sličnosti i razlike autotolerancije T i B limfocita Odlike T limfociti B limfociti Mesto indukcije tolerance Timus (korteks); periferna Kosna srž; periferna Tolerancijasenzitivan stupanj u sazrevanju ćelija CD 4+CD 8+ (duplo pozitivni) nezreli timociti Nezreli (Ig. M+Ig. D-) B limfociti Stimulusi za indukciju tolerancije Centralna: visoko aviditetno prepoznavanje Ag u timusu Centralna: prepoznavanje multivalentnih Ag u kosnoj srži Periferna: prezentacija Ag od strane APĆ bez kostimulatora; ponovljena stimulacija sopstvenim Ag Periferna: prepoznavanje Ag bez pomoći CD 4 T ćelija ili sekudarnih signala Centralna toleranca: delecija (apoptoza); razvoj regulatornih T ćelija Centralna toleranca: delecija (apoptoza); editovanje receptora Periferna toleranca: anergija, apoptoza, supresija Periferna toleranca: blok u transdukciji signala (anergija); prekid ulaska u limfoidne folikule; apoptoza Osnovni mehnizmi tolerance

Autoimuno reagovanje • Prisustvo antitela ili T-ćelija reaktivnih na sopstvene Ag • • može da bude uzrok nastanka autoimunih bolesti Kada zakažu mehanizmi koji su odgovorni za održavanje tolerancije na sopstveno Postoje prirodna autoantitela koja su niskog afiniteta vezivanja sa Ag, Ig. M klase, ne izazivaju oštećenja tkiva

IMUNODEFICIJENCIJE • To su stanja koja nastaju kao posledica slabljenja ili potpunog izostanka imunološke reakcije.

Imunodeficijencije • Mogu biti primarne i sekundarne • Primarne imunodeficijencije su izazvane genetskim • poremećajem-odnosno poremećajima koji su nastali u embrionalnom razvoju Sekundarne su posledica, tj prateća pojava drugih imunoloških i neimunoloških poremećaja i bolesti (malignih tumora, AIDS-a, zračenja, delovanja nekih lekova

Kategorije imunodeficijencije • • • Imunodeficijencije su svrstane u ćetiri kategorije: 1. deficijencije antitela tj. B limfocita 2. deficijencije celularnog reagovanja tj. T-limfocita 3. disfunkcija fagocita 4. deficijencije sistema komplementa

Bolesti izazvane deficitarnošću Blimfocita Karakterišu se smanjenjem količine imunogolbulina i to ili svih ili pojedinih klasa Težina kliničke slike zavisi od stepena deficijencije Bolest je teža kod hipogama-globulinemije, simptomi nastaju ranije u odnosu na selektivni nedostatak jedne klase imunoglobulina

Brutonova hipogama-globulinemija ili agama-globulinemija • Infantilna hipogama-globulinemija vezana za X • • • hromozom Nasleđuje se kao bolest vezana za X hromozom Prenosioci su žene Bolest se manifestuje kod muške dece, koja usled stalnih infekcija rano umiru Ženska dece bi mogla da obole ako oba X hromozoma nose ovo genetsko svojstvo Kod ove bolesti izrazito je smanjena koncentracija Ig. G AT (manja od 200 mg/dl), a ostale klase su potpuno odsutne

Patofiziološki mehanizam bolesti • Poremećaj je na nivou ćelija koje su preteča B-limfocita • • iz kojih nastaju B limfociti Područja B ćelija (timus nezavisne regije limfnih žlezda i slezina) su sa malo ćelija i bez germinativnih centara U prifernoj krvi uopšte nema B-limfocta i plazma ćelija T-limfociti su normalni i prisutni u perifernoj krvi Reakcje celularnog imunteta normalo se odigravaju

• Bolest se ispoljava nakon gubitka maminih Ig. G • • AT, nekoliko meseci po rođenju Deca oboljevaju od ponovljenih infekcija piogenim bakterijama Lećenjem –antibioticima i humanim gama globulinima produžava se žuvot ovakvoj deci

Selektivne deficijencije pojedinih klasa imunoglobulina • Radi se o poremećaju sinteze samo jedne klase • • imunoglobulina Najčešća je urođena deficijencija imunoglobulina A Ređe su selektivne deficijencija Ig. M i Ig. G AT

Selektivna imunodeficijencija imunoglobulina A • • Koncentracija Ig. A manja od 5 mg/dl Koncentracuja ostalih klasa imunoglobulina je normalna Celularni imunitet je očuvan Veća je učestalost rekurentnih pulmonalnih ifekcija, alergija i autoimunih bolesti

Selektivna deficijencija imunoglobulina A • Nije poznat tačan uzrok ove deficijencije • Smanjena je sinteza Ig. A ili smanjeno oslobađanje Ig. A • Moguće da je poremećaj u prekopčavanju B-limfocita, tj • • plazma ćelija od lućenja ig. M, preko Ig. G na Ig. A klasu antela pored serumskih Ig. A nedostaju i sekretorna Ig. A Prateće infekcije leče se prema protokolu za ta oboljenja

Selektivna deficijencija imunoglobulina M • • • Retko stanje, nema Ig. M AT Ostale klase prisutne u normalnom broju Celularni imunitet očuvan Bolest je verovatno nasledna i prisutna u oba pola Bolesnici sa ovom deficijencijom imaju češće autoimune bolesti i generalizovane infekcije raznim mikroorganizmima Daju se antibiotici u zavisnosti od infekcije

Selektivna deficijencija podklasa imunoglobulina G • Deficijencija nekih od 4 podklase Ig. G • Ostale klase imunoglobulina su prisutne u normalnim • koncentracjama Kod ovih bolesnika česte su rekurentne piogene infekcije pluća • Daju se humani gama globulini

Bolesti izazvane deficitarnošću T-ćelija • Radi se o celularnoj imunodeficijenciji koja dovodi do • poremećaja i B lifocitnog delovanja, jer nedostaje T-B kooperacije neophodna u humoralnom imunom odgovoru Ovakve osobe su osetljive na razne mikroorganizme smeštene intracelularno (posebno viruse)

Kongenitalna aplazija timusa-Di George -ov sindrom • Imunodeficijencija sa aplazijom timusa i • • • hipoparatireoidizmom Javlja se odmah po rođenju, nije nasledna bolest Poremečaj u embrionalnom razvoju, oko 12 nedelje, zahvaćena je 3 i 4 faringealna vreća iz njih se razvija timus i niz drugih organa, tako da se bolest manifestuje multiplim poremećajima(deformitet lica sa ribljim ustima, razmaknutim očima, mikrognatija, srčanim manama)

• Odmah po rođenju nastaje hipokalcemija rezistentna na • • • terapiju Izostaje T ćelijski imunitet Humoralni imunitet je poremećen usled izostanka kooperacije T i B limfocita Značajna je rana dijagnostika jer se stanje može popraviti transplantacijom fetalnog timusa

Hronična mukokutana kandidijaza • • • Nasledna deficitarnost –T limfocita Selektivnog tipa Nasleđuje se autosomno recesivno Selektivan poremećaj funkcije T-limfocita na Candida Ag (izostaju celularne reakcije) Obolele osobe pate od hronične infekcije izazvane Candidom(koža, nokti, sluzokoža) Ove infekcije ne prelaze u sistemsku kandidijazu

Udružene imunodeficijencije koje zahvataju T-ćelije i B-ćelije • Mogu biti potpune-kada se radi o naslednoj bolesti i • • obuhvata deficijenciju T i B ćelija tj. nedostatak celularnog i humoralnog imuniteta Terapija je transplantacija kostne srži Mogu biti delimične, kada se radi o promeni u broju i funkciji T-limfocita sa neurološkim poremečajem: imunodeficijencija sa ataksijom i teleangiektazijama (proširenje perifernih krvnih sudova)

Teška kombinovana imunodeficijencija T i B-ćelija • Nasledna bolest , poremećaj u diferecijaciji matičnih ćelija • • u limfocite B i T Pošto nema ni humoralnog ni celularnog imuniteta bolesnik umire do prve godine života, a bolest se otkriva nakon gubitka maminih Ig. G AT. Moguća je rekonstrukcija humoralnog i celularnog imuniteta transplantacijom kostne srži

Wiskott-Aldrichov sindrom • Imunodeficijencija usled povećanog katabolizma • • imunoglobulina Posledica-nizak nivo serumskih Ig. M AT Javlja se i trombocitopenija, ekscemi i sklonost ka infekcijama Bolest je nasledna i vezana za X hromozom Tokom života slabi i ćelijski imunitet

Stečene imunodeficijencije • Nastaju usled poremećaja imunog sistema koji se stiču u • • • toku života U sklopu nekih drugih bolesti i stanja: Tumora Infekcija Neadekvatne ishrane (malnutricije) Kao komplikacija terapije drugih bolesti i stanja(tzv. jatrogene imunodeficijencije)

SEKUNDARNE IMUNODEFICIJENCIJE (STEČENE) • Mogu biti prolazne: • posle akitnih virusni infekcija • • • trajne kod: kongenitalne rubele, Multiple rekurentne i perzistentne virusne infekcije Kod AIDS-a Kod malignih tumora i u toku njihovog lečenja Kod autoimunih bolesti

Klinički tok HIV infekcije • Akutna viremija, period kliničke latencije kada dolazi do neprekidnog propadanja CD 4+ T-ćelija i gubitka limfnog tkiva i na kraju AIDS-a sa teškom imunodeficijencijom praćenom oportunističkim infekcijama, pojavom nekih tumora, smanjenjem telesne mase , a ponekad i demencijom

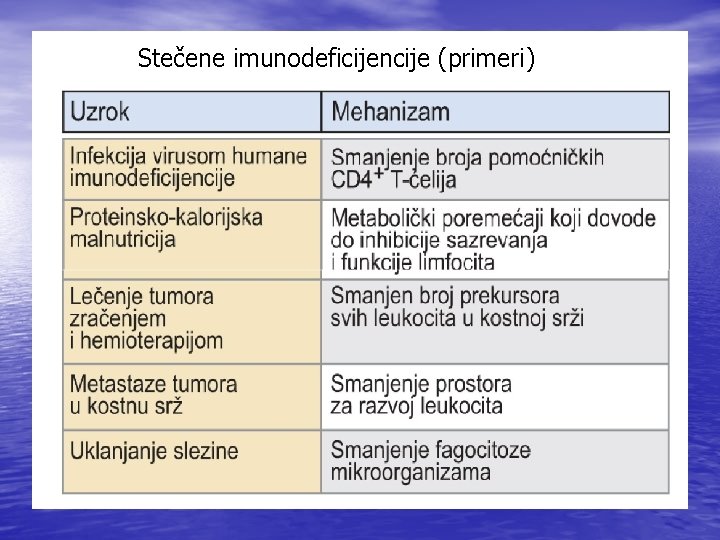
Stečene imunodeficijencije (primeri)

Imunodeficijencije-terapija • • • Kongenitalne (primarne): Imunoglobulini (kod poremećaja humoralnog imuniteta) Transplantacija kostne srži (oprez od GVHD) Genska terapija Profilaksa infekcija

Imunodeficijencije-terapija • Stečene imunodeficijencije (sekundarne): • Lečenje primarnog uzroka • Profilaksa infekcije


Autoimune bolesti Imuni odgovor protiv sopstvenih (autologih) antigena 1 -2% populacije pati od autoimunih bolesti Ø nastaje usled izostanka autotolerance ü primarnih nedostataka imunog sistema ü abnormalnosti sopstvenih Ag i njihovog prikazivanja limfocitim Ø Autoimunost-produkcija autoantitela i aktivacija autoreaktivnih T limfocita ØAutoimune bolesti - heterogene i multifaktorske, sopstveni Ag koji pokreću autoimunu reakciju, kao i ciljne ćelije/molekuli su često nepoznati Ø Bolest se često klinički manifestuje kasno posle započinjanja autoimune reakcije
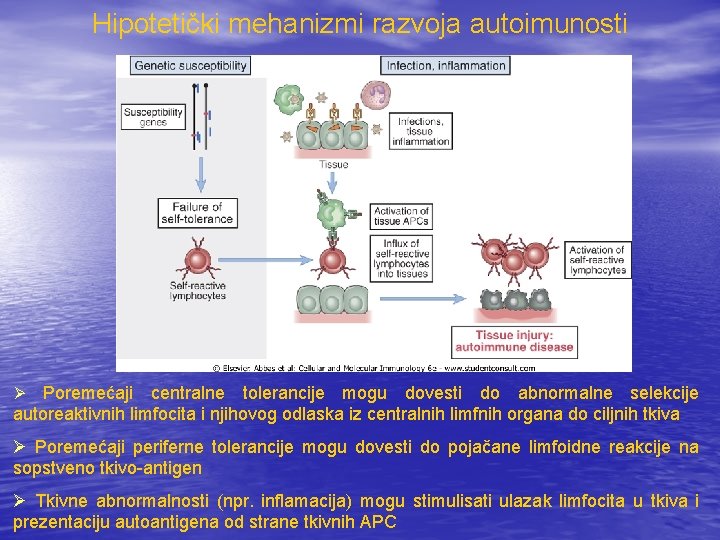
Hipotetički mehanizmi razvoja autoimunosti Poremećaji centralne tolerancije mogu dovesti do abnormalne selekcije autoreaktivnih limfocita i njihovog odlaska iz centralnih limfnih organa do ciljnih tkiva Ø Ø Poremećaji periferne tolerancije mogu dovesti do pojačane limfoidne reakcije na sopstveno tkivo-antigen Ø Tkivne abnormalnosti (npr. inflamacija) mogu stimulisati ulazak limfocita u tkiva i prezentaciju autoantigena od strane tkivnih APC

Imunološki činioci u autoimuim bolestima • Izostanak autotolerancije • Tolerancija na nivou T i B limfocita neće se uspostaviti ukoliko oštećenja tkiva izazovu otkrivanje sekvestriranih Ag na koje nije stvorena intrauterina imunološka tolerancija –stvaraju se autoantitela

Poremećaj regulacije limfocita Gubitak ili oštećenje subpopulacije T limfocita sa supresorskom funkcijom oni kontrolišu reakciju na autoantigene, nastaje spontana pojava anti- T autoantitela, ili dovodi do hiperfunkcije aktivisanih B-limfocita i pojačanog stvaranja antitela na timus nezavisne autoantigene

Autoimuni proces bi mogao da se indukuje na više načina: • Direktnom stimulacijom B ćelija- koje nisu tolerantne na • autoantigen, poliklonskim aktivatorima B-ćelija Prevazilaženjem T-ćelijske nereaktivnosti na sopstveno izmenom sopstvenih antigena: (Spajanjem sopstvenih antigena sa lekovima ili promena sopstvenih antigena pod dejstvom lekova i virusa), nosački deo izmenjenog antigena pokreće reakciju T pomagačkih limfocita (koji nisu tolerantni) , a oni aktivišu B-limfocite na sintezu autoantitela

Poliklonski aktivatori • • Aktivacija B-limfocita endogenim i egzogenim mitogenima-ploklonskim aktivatorima: različiti bakterijski produkti, virusi i njihov sastavni delovi, paraziti nastaju antinuklearna, antilimoficitna, antieritrocitna antitela, reumatoidni faktor (antitela protiv sopstvenih imunoglobulina G) Epstein Barr-virus je poliklonski aktivator B-limfocita, aktiviše ih direktno bez učestvovanja T-limfocita

Uloga makrofaga • Izmenjena funkcija makrofaga, koji su važni u fagocitozi i • uklanjanju imunih kompleksa, doprinosi da se imuni kompleksi pojavljuju u cirkulaciji i talože u tkivima Povećana ekspresija HLA antgena klase II na APĆ stimuliše jaku reakciju limfocita, • Virusne infekcije podstiču stvaranje interferona koji utiče na ekspresiju HLA antigena

Genetski činioci u autoimunim bolestima • Uočena je povezanost autoimunih bolesti sa određenim • • alelima HLA kompleksa : Reumatoidni artrirtis-HLA DR 4, SLE-HLA DR 2 i HLA DR 3
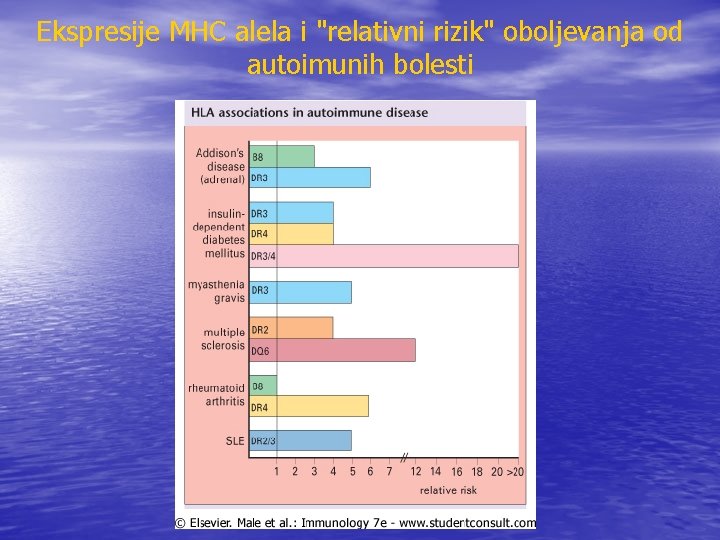
Ekspresije MHC alela i "relativni rizik" oboljevanja od autoimunih bolesti

Hormonalni činioci u autoimunim bolestima • Polni hormoni utiču na ekspresiju autoimunih bolesti • • akcelerirajući faktor Žene češće oboljevaju od SLE nego muškarci –zbog hronične stimulacije estrogenom Ovakav učinak polnih hormona nije prisutan kod svih autoimunih bolesti

Virusni činioci i druge infekcije u autoimuim bolestima • • Virusi i bakterije mogu da izazovu autoimunu bolest: Poliklonskom aktivacijom limfocita Razaranjem ćelije (CPE virusa) Oslobađanjem intracelularnih struktura u vanćelijske prostore Promenom u prepoznavanju (ugrađivanjem virusnih Ag u ćelijsku membranu) Antigenskom mimikrijom Ektopičnom indukcijom HLA antigena putem interferona
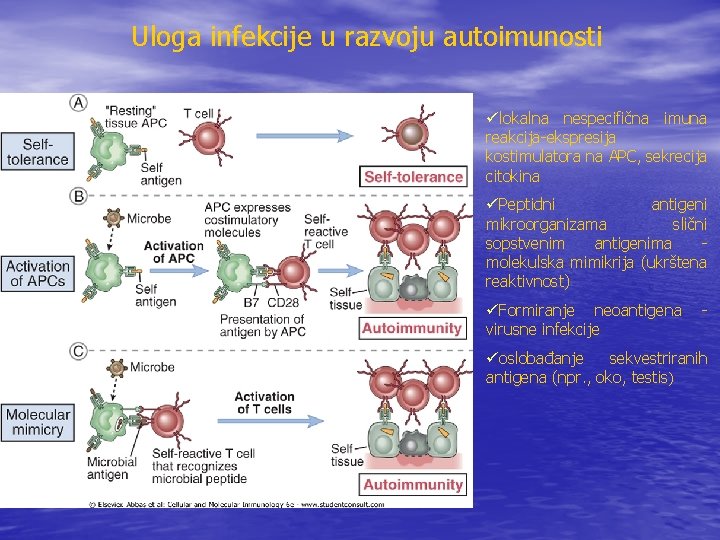
Uloga infekcije u razvoju autoimunosti ülokalna nespecifična imuna reakcija-ekspresija kostimulatora na APC, sekrecija citokina üPeptidni antigeni mikroorganizama slični sopstvenim antigenima molekulska mimikrija (ukrštena reaktivnost) üFormiranje neoantigena virusne infekcije - üoslobađanje sekvestriranih antigena (npr. , oko, testis)

Autoimune bolesti • Autoimuna oboljenja se dele na: • Autoimune bolesti usled menjanja sopstvenih antigena • Autimune bolesti nastale pojavom autoreaktivnih klonova koji reaguju na sopstvene nepromenjene antigene

Podela autoimunih bolesti • Organspecifične autoimune bolesti • Autoimuna reakcija upravljena protiv Ag koji se nalaze • • unutar određenih organa Sistemske ili organonespecifične autoimune bolesti Autoimuna reakcija upravljena protiv široko rasprostranjenih sopstvenih antigenskih determinanti

Patogenetski mehanizam autoimunih bolesti • 1. delovanje autoantitela na nepromenjene ili • promenjene strukture na površini sopstvenih ćelija ili u njihovoj unutrašnjosti Dolazi do razanja ćelija i tkiva uz pomoć komplementa ili putem antitelo zavisne celularne citotoksičnosti

• 2. stvaranjem imunih kompleksa u međućelijskoj tečnosti • • ili u krvotoku koji se talože , tu bivaju privučeni granulociti, monociti, dolazi do aktivacije komplementa i do ubijanja sopstvenih ćelija

• 3. delovanjem senzibilisanih T- limfocita koji lučenjem određenih citokina dovode do oštećenja tkiva ili privlače razne ćelije zapaljenja koje doprinose oštećenju tkiva

Organospecifične autoimune bolesti • • Autoimuna hemolitička anemija Autoimuna trobocitopenična purpura Autoimini tireoiditsi Gravesova bolest Autoimuni miksedem, atrofični gastritis, Autoimune endokrinopatije

• Myasthenia gravis-poremećaj neuromišićne transmisije • Multipla skleroza-brojna žarište demijelinizacije u • • • nervnom tkivu Sindrom Guillain Barre-akutni poliradikuloneuritis sa oštećenjima na perifernim živcima Sistemski lupus eritematodes-organonespecifično oboljenje Reumatoidni artritis sistemsko oboljenje sa oštećenjem lokomotornog aparata Sjogrenov sindrom-praćen suvoćom usne šupljine i očiju Sklerodermija-bolest vezivnog tkiva

Značaj određivanja autoantitela u autoimunim bolestima • • Prisustvo autoantitela je obeležje ovih bolesti Ona su monospecifična i visokog afiniteta Kod sistemskih autoimuih bolesti ona su brojna na intraćelijske proteine i nukleinske kiseline Kod organospecifičnih bolesti usmerena su protiv određenih tkivnih struktura
- Slides: 97