Hemija UGLJOVODONICI DEFINICIJA Ugljovodonici su organska jedinjenja sastavljena

















- Slides: 18

Hemija UGLJOVODONICI

DEFINICIJA �Ugljovodonici su organska jedinjenja sastavljena od ugljenika i vodonika

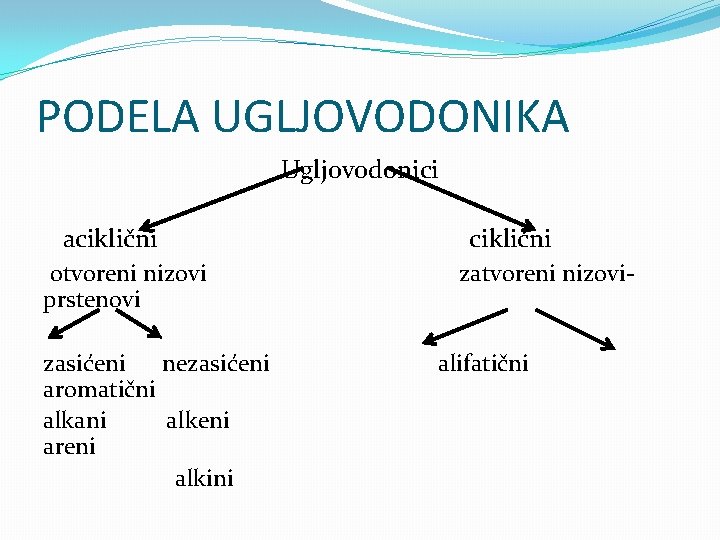
PODELA UGLJOVODONIKA Ugljovodonici aciklični otvoreni nizovi prstenovi zasićeni nezasićeni aromatični alkani alkeni areni alkini ciklični zatvoreni nizovi- alifatični

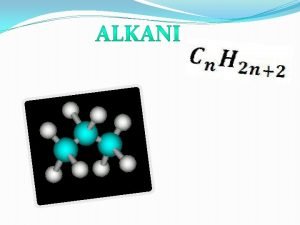
ALKANI �Zasićeni ugljovodonici kod kojih svaki C atom gradi 4 jednostruke veze OPŠTA FORMULA: Cn. H 2 n+2 n=1, 2, 3, 4. . . IZOMERI su jedinjenja iste molekulske formule a različitih osobina kao posledice različite strukture.

ALKANI �Hologi niz jedinjenja iste klase (iste funkcionalne grupe) koji se razlikuju za -CH 2 -grupu od prethodnog metan CH 4 heksan C 6 H 14 etan C 2 H 6 heptan C 7 H 16 propan C 3 H 8 oktan C 8 H 18 butan C 4 H 10 nonan C 9 H 20 pentan C 5 H 12 dekan C 10 H 22

IZOMERIJA ALKANA �Racionalne strukturne formule alkana �Etan CH 3−CH 3 �Propan CH 3−CH 2−CH 3 �Butan CH 3−CH 2−CH 3 �Izobutan CH 3−CH−CH 3 strukturna izomerija CH 3 IUPAC-ova nomenklatura 2 -metilpropan

IUPAC nomenklatura 1 2 3 4 5 CH 3−CH−CH 2−CH−CH 3 2, 4 -dimetilpentan ₁ ₂CH 3₃ ₄ CH 3−C−CH 2−CH 3 2, 2 -dimetilbutan

ALKENI �Nezasićeni ugljovodonici sa jednom dvostrukom vezom. OPŠTA FORMULA : Cn. H 2 n n=2, 3, 4, 5. .

ALKENI �Homologi niz i izomerija alkena Eten C 2 H 4 CH 2=CH 2 Propen C 3 H 6 CH 3−CH=CH 2 Buten C 4 H 8 CH 3 −CH 2−CH=CH 2 (1)- buten 1 2 3 4 CH 3−CH=CH−CH 3 2 -buten izomerija položaja dvostruke veze

IZOMERIJA ALKENA �Penten C 5 H 10 CH 3−CH 2−CH=CH 2 (1)-penten 1 2 3 4 5 CH 3−CH=CH−CH 2−CH 3 2 -penten 5 4 3 2 1 CH 3−CH 2−CH=CH−CH 3 2 -penten 1 2 3 4 CH 2=CH−CH−CH 3 3 -metil(1) buten CH 2=C−CH 2−CH 3 2 -metilbuten

ALKINI �Nezasićeni ugljovodonici sa jednom trostrukom vezom OPŠTA FORMULA Cn. H 2 n-2 n=2, 3, 4, 5. .

ALKINI �Homologi niz i izomerija alkina etin C 2 H 2 CH ≡CH PROPIN C 3 H 4 CH 3−C≡CH BUTIN C 4 H 6 CH 3−CH 2−C≡CH (1)butin CH 3−C≡C−CH 3 2 - butin

HEMIJSKA SVOJSTVA UGLJOVODONIKA Zasićeni ugljovodonici ALKANI slabo reaktivna jedinjenja. SUPSTITUCIJA: reakcija zamene jednog ili više H atoma drugim atomom ili atomskom grupom. CH 4 + Cl 2 CH 3 Cl + HCl hlormetan CH 3 Cl + Cl 2 CH 2 Cl 2 + HCl dihlormetan CH 2 Cl 2 + Cl 2 CHCl 3 + HCl trihlormetan CHCl 3 + Cl 2 CCl 4 + HCl tetrahlormetan

HEMIJSKA SVOJSTVA UGLJOVODONIKA �Nezasićeni ugljovodonici ALKENI I ALKINI reaktivni, teže da pređu u zasićene. �ADICIJA: zasićavanje dvostruke i trostruke veze do jednostrukih. Pri adiciji na svakom C atomu se stvara nova veza. C= C C− C

ADICIJA ALKENA �Adicija vodonika- hidrogenovanje �CH 2 = CH 2 + H 2 CH 3− CH 3 �Adicija broma- bromovanje �CH 2 = CH 2 + Br 2 CH 2 − CH 2 Br Br 1, 2 -dibrometan -Dokazna reakcija za nezasićenu vezu obezbojavanje bromne vode (smeđe).

ADICIJA ALKENA �Adicija HX CH 3−CH = CH 2 + HBr propen CH 3−CH−CH 3 Br 2 -brompropan Adicija vode ( u prisustvu sumporne kiseline) CH 3−CH = CH 2 + H 2 O CH 3−CH−CH 3 OH 2 -propanol (alkohol)

ADICIJA ALKINA �Kod alkina se adiraju DVA molekula reagensa na jedan molekul alkina. CH≡CH +H 2 CH 2= CH 2 +H 2 CH 3− CH 3 etin eten etan Br CH 3−C ≡ CH +HBr CH 3 −C= CH 2 + HBr CH 3− C −CH 3 propin Br Br 2 -brompropen 2, 2 dibrompropan

SAGOREVANJE UGLJOVODONIKA �Svi ugljovodonici sagorevaju do CO 2 i H 2 O uz oslobađanje toplote. � 2 C 2 H 6 + 7 O 2 4 CO 2 + 6 H 2 O �C 2 H 4 + 3 O 2 2 CO 2+2 H 2 O � 2 C 2 H 2 + 5 O 2 4 CO 2+2 H 2 O
 Svojstva kiselina
Svojstva kiselina Za sta se koristi spiritus
Za sta se koristi spiritus Lewisova teorija kiselina i baza
Lewisova teorija kiselina i baza Disocijacija kompleksnih soli
Disocijacija kompleksnih soli Mit o prometeju
Mit o prometeju Boja svinjske masti
Boja svinjske masti Benzen + 3cl2
Benzen + 3cl2 Heptan oktan nonan dekan
Heptan oktan nonan dekan Alifatični ugljovodonici
Alifatični ugljovodonici Ugljovodonik formula
Ugljovodonik formula Sagorevanje metana
Sagorevanje metana Halogenovanje metana
Halogenovanje metana Položajna izomerija
Položajna izomerija Heterociklicna jedinjenja
Heterociklicna jedinjenja Kalijum heksa cijano ferat 2
Kalijum heksa cijano ferat 2 Kiseline hemija
Kiseline hemija Kataliticka hidrogenizacija
Kataliticka hidrogenizacija Mezo jedinjenja
Mezo jedinjenja Hlorovanje
Hlorovanje