KISELOST I BAZNOST ORGANSKIH JEDINJENJA KLARA KAKUKA prof

KISELOST I BAZNOST ORGANSKIH JEDINJENJA KLARA KAKUČKA, prof. Hemije MAČVANSKA SREDNJA ŠKOLA

POJAM KISELOSTI I BAZNOSTI Arenijusova teorija: Kiseline su jedinjnja koja u vodenim rastvorima disosuju na H+ jone i kiselinske ostatke. H 2 SO 4→ 2 H+ + SO 42 Baze su jedinjenja koja u vodenim rastvorima disosuju na OH- jone i katjone metala. Mg(OH)2 → Mg 2+ + 2 OH Lewisova teorija: Kiseline su jedinjenja koja daju prazne orbitale i primaju elektronski par a baze daju elektronski par u stvaranju hemijske veze.

KISELOST ORGANSKIH JEDINJENJA Od organskih jedinjenjenja kisela su: v Alkini v Alkoholi v Fenoli v Karboksilne kiseline v I neka heterociklična jedinjenja

KISELOST ORGANSKIH JEDINJENJA Kiselo-bazna svojstva organskih jedinjenja • Bronsted-Lowry: kiseline su supstance koje mogu dati proton, a baze su supstance koje mogu primiti proton: HA + B → A-+ BH+ • Lewis: kiseline su supstance koji mogu primiti elektronski par, a baze mogu dati elektronski par nekoj kiselini: Kiselost i bazičnost su relativna svojstva molekula – određeno jedinjenje može biti prema nekom jedinjenju kiselina, a prema drugom baza (npr. H 2 O). HA+ H 20→ H 3 O+ + AB + H 2 O → HB+ + OH-
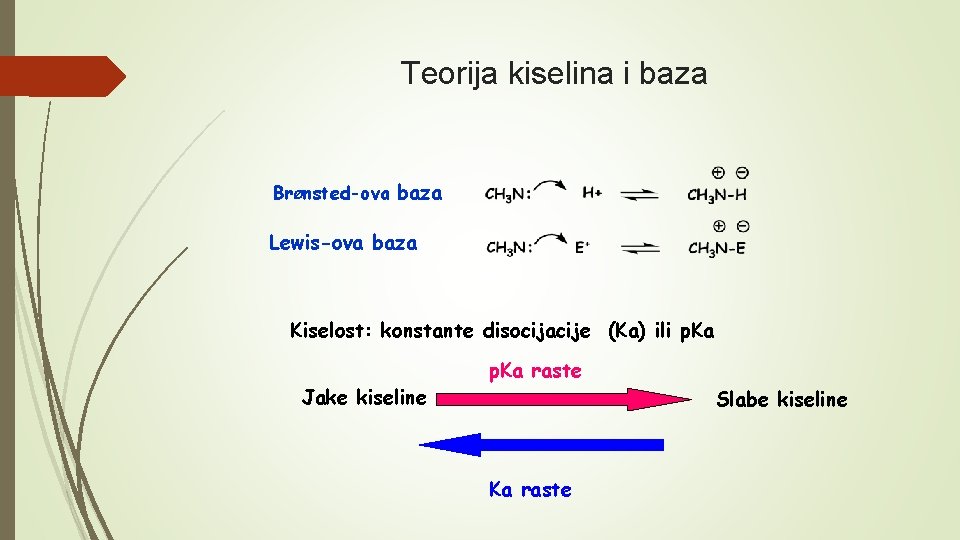
Teorija kiselina i baza BrØnsted-ova baza Lewis-ova baza Kiselost: konstante disocijacije (Ka) ili p. Ka Jake kiseline p. Ka raste Slabe kiseline Ka raste

KISELOST ORGANSKIH JEDINJENJA • jaka kiselina daje slabiju konjugiranu bazu i obrnuto • položaj kiselo-bazne ravnoteže pogoduje stvaranju slabije kiseline i slabije baze: jača kiselina + jača baza → slabija kiselina + slabija baza kiselost raste: -spuštanjem u vertikalnoj koloni periodnog sistema -s leva na desno u horizontalnom redu periodnog sistema -porastom elektronegativnosti induktivno djelovanje -polarizacija veze zbog delovanja susedne polarne veze ili grupe –induktivno delovanje elektronegativnih atoma povećava kiselost

KISELOST ORGANSKIH JEDINJENJA prostorna delovanja -prostorno međudelovanje različitih grupa (stabilizacija konjugovane baze ili kiseline solvatacijom ili međumolekulskom vodičnom vezom) Stabolizacija solvatacijom A-H + Sol: kiselina rastvarač → A: - + konjug baza Sol-H+ konjug kiselina

KISELOST ORGANSKIH JEDINJENJA delovanje rezonancije -delokalizacija elektronskog para uzrokuje veću kiselost karboksilnih kiselina u odnosu na alkohole (konjugirana baza karboksilne kiseline srazmerno je jače stabilizovana rezonancijom u pooređenju sa alkoksidnim anjonom kod alkohola):

Kiselost alkina Vodonikov atom na trostruko vezanom ugljeniku je kiselog karaktera Alkini su vrlo slabe organske kiseline Kiselost alkina: nespareni elektronski par aniona alkina je u sp-orbitali(50% skaraktera) koja je bliža jezgru, pa je stabilniji u odnosu na anione alkena (u sp 2 orbitali, 33% s-karaktera) i akana (u sp 3 orbitali, 25% s-karaktera) što alkinima daje veću kiselost H─ C≡ C─ H +2 Ag+ → + Ag─ C≡ C─ Ag + + H 2
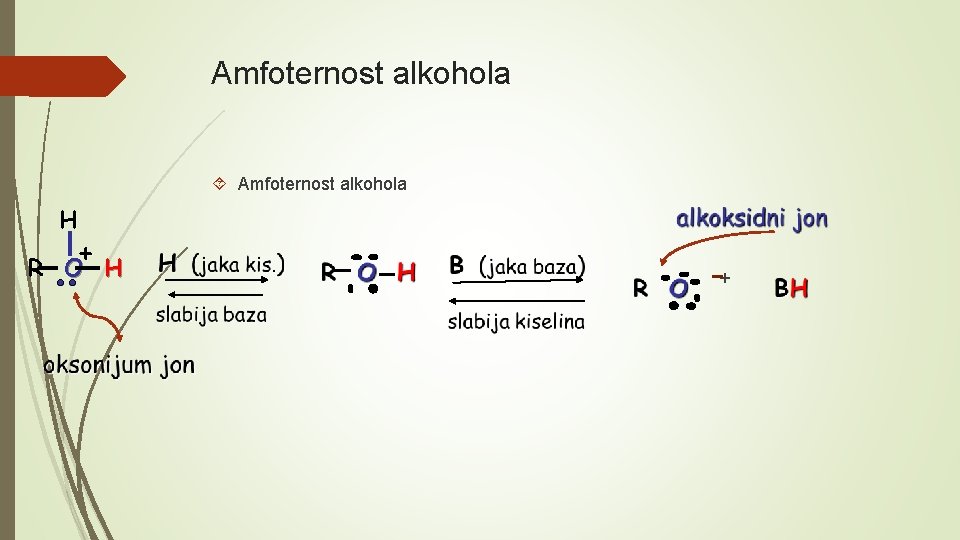
Amfoternost alkohola H + R O H +
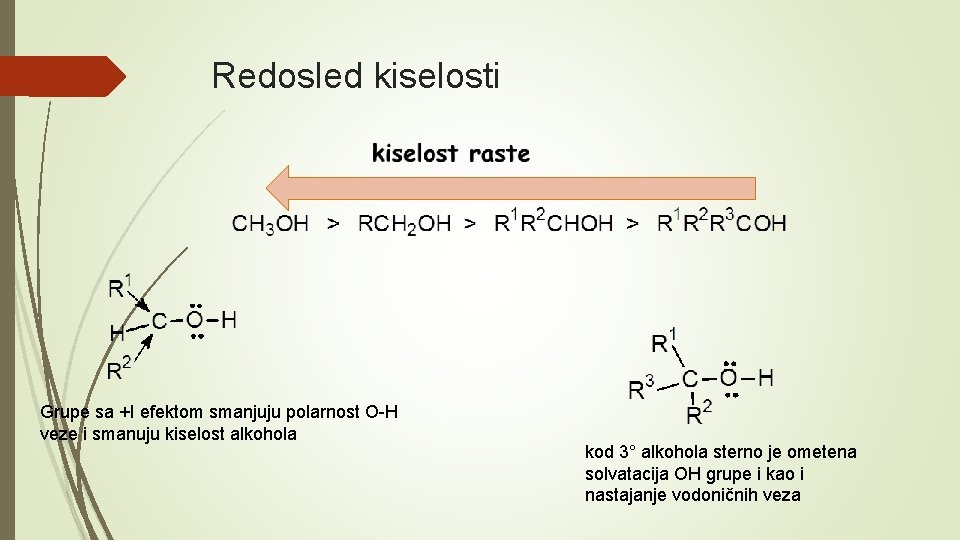
Redosled kiselosti Grupe sa +I efektom smanjuju polarnost O-H veze i smanuju kiselost alkohola kod 3° alkohola sterno je ometena solvatacija OH grupe i kao i nastajanje vodoničnih veza
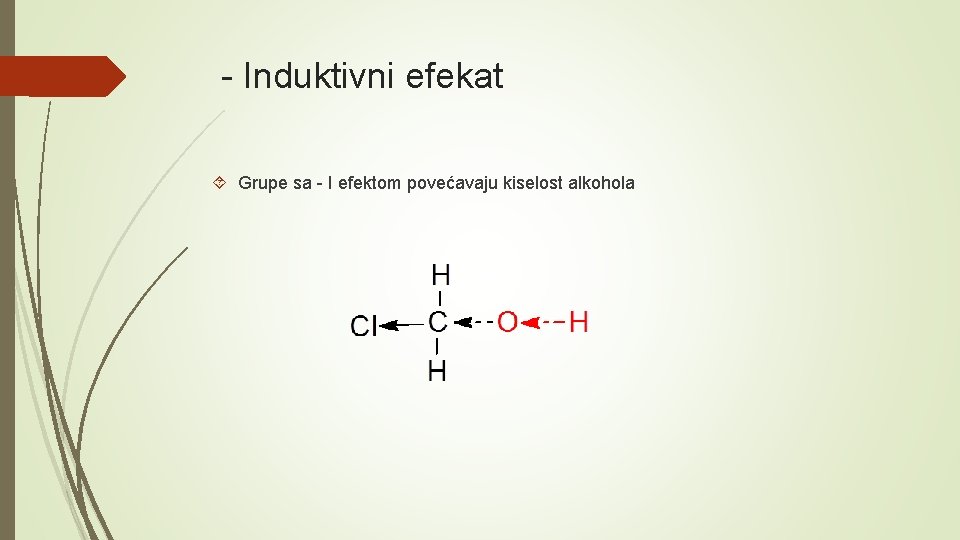
- Induktivni efekat Grupe sa - I efektom povećavaju kiselost alkohola
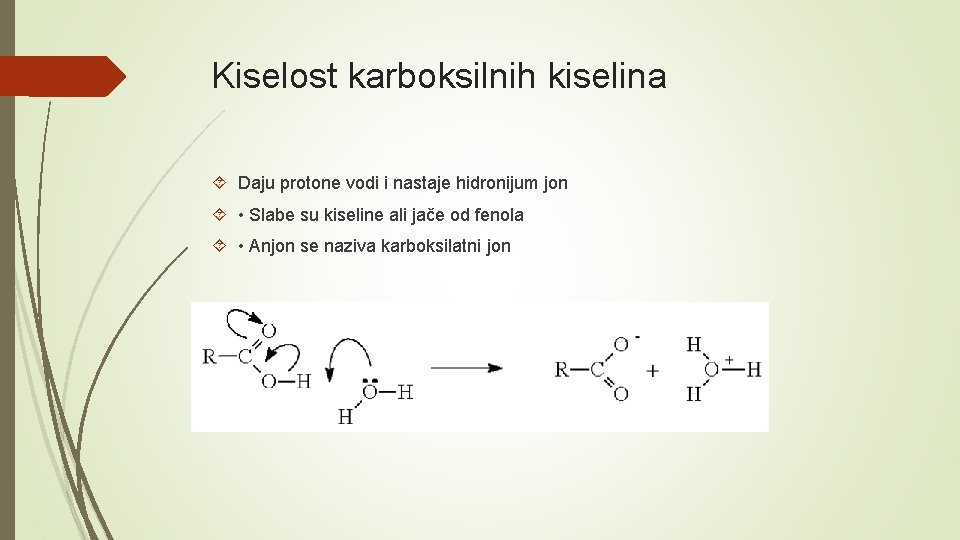
Kiselost karboksilnih kiselina Daju protone vodi i nastaje hidronijum jon • Slabe su kiseline ali jače od fenola • Anjon se naziva karboksilatni jon
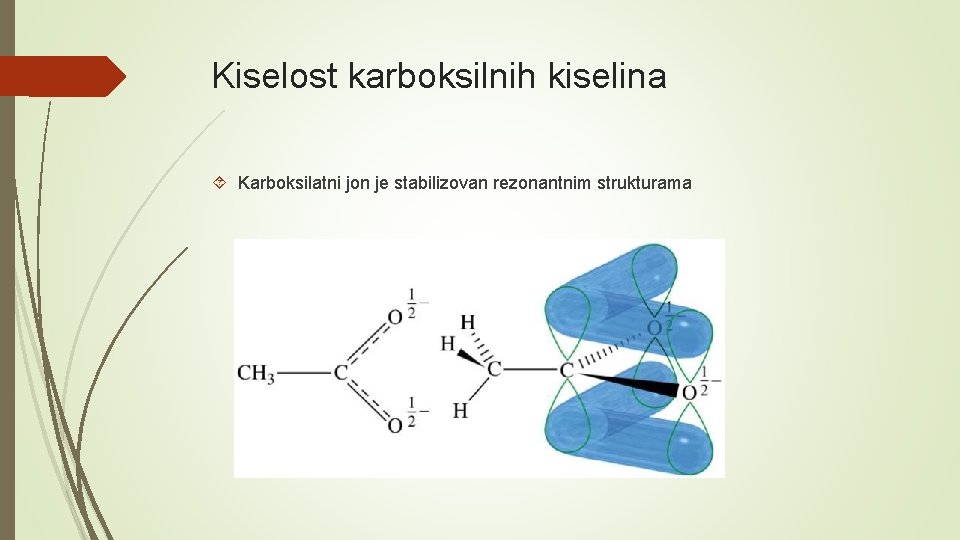
Kiselost karboksilnih kiselina Karboksilatni jon je stabilizovan rezonantnim strukturama
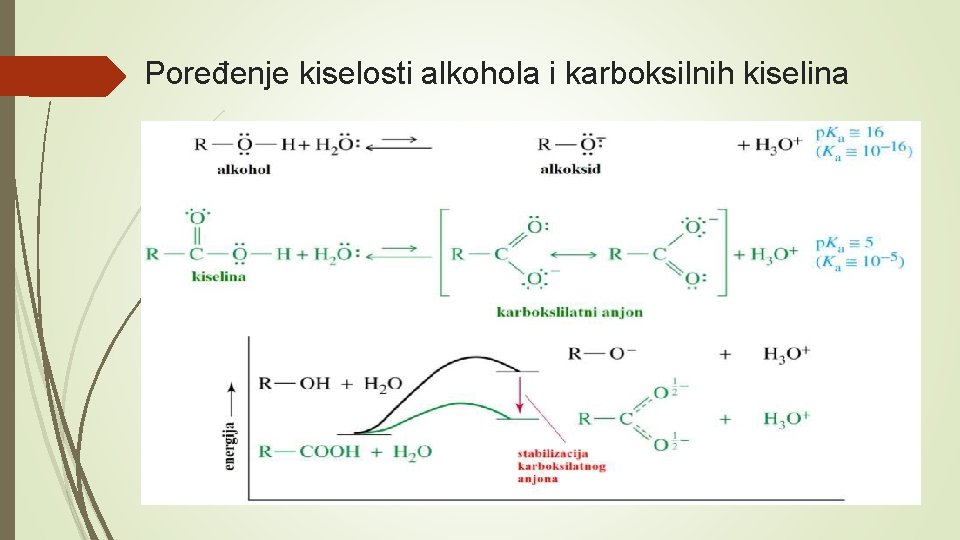
Poređenje kiselosti alkohola i karboksilnih kiselina
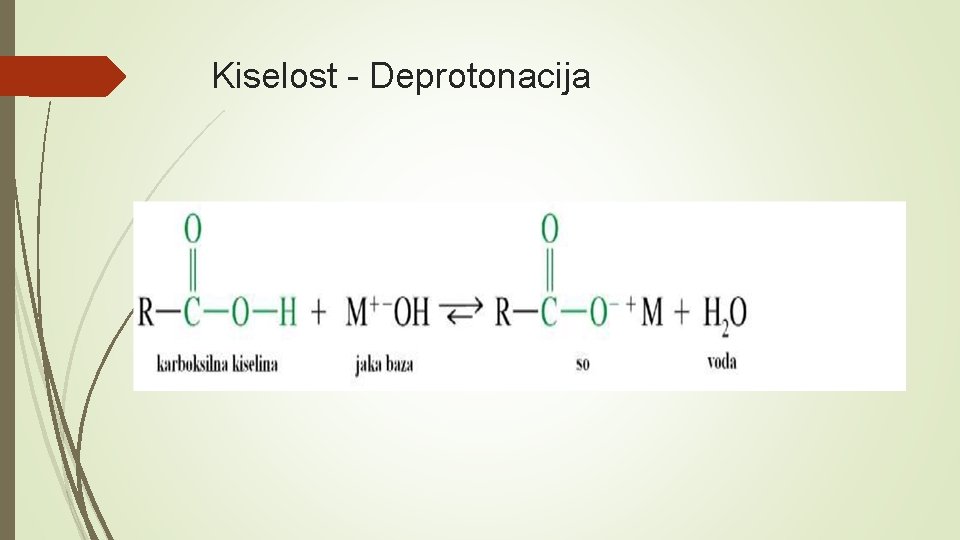
Kiselost - Deprotonacija

Građenje soli RCOOH + Na. OH→ RCOONa + H 2 O CH 3 COOH + Na. OH →CH 3 COONa + H 2 O
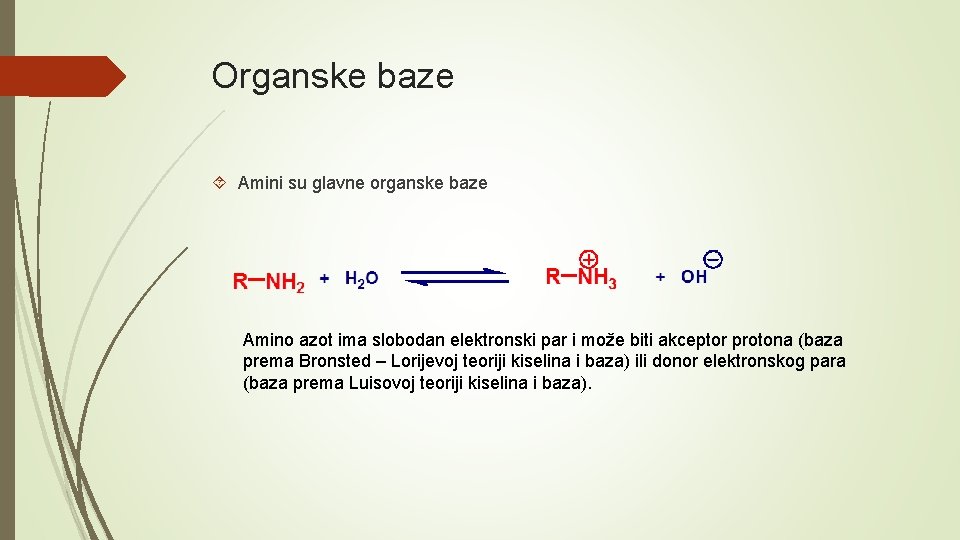
Organske baze Amini su glavne organske baze Amino azot ima slobodan elektronski par i može biti akceptor protona (baza prema Bronsted – Lorijevoj teoriji kiselina i baza) ili donor elektronskog para (baza prema Luisovoj teoriji kiselina i baza).
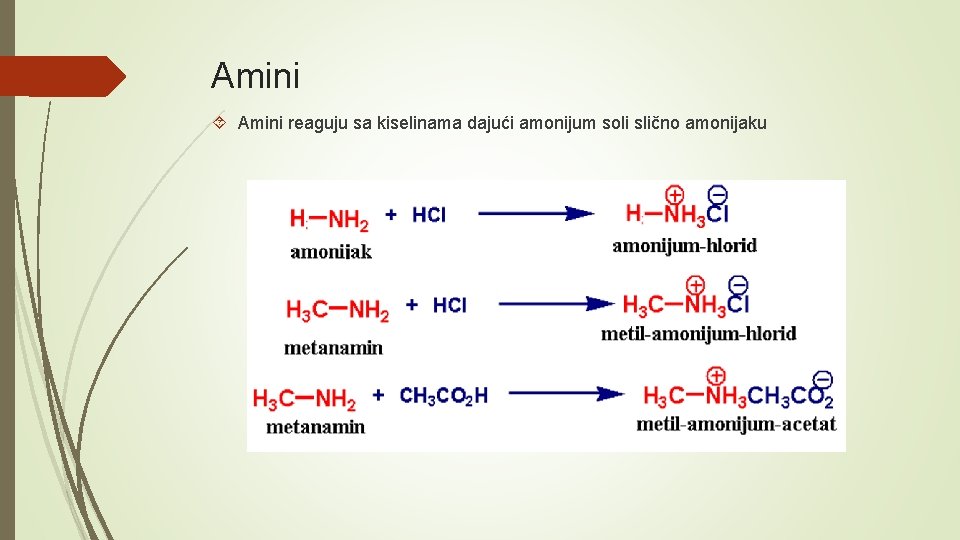
Amini reaguju sa kiselinama dajući amonijum soli slično amonijaku
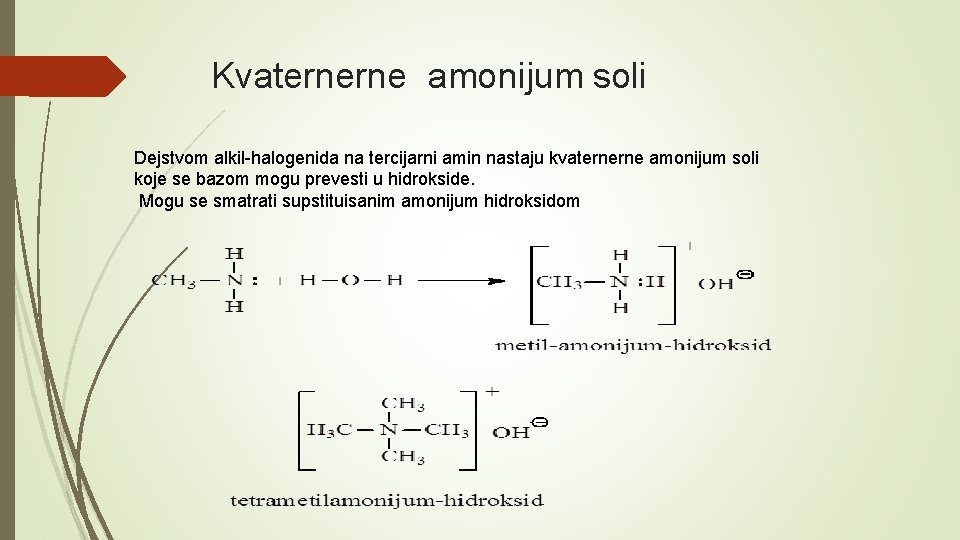
Kvaternerne amonijum soli Dejstvom alkil-halogenida na tercijarni amin nastaju kvaternerne amonijum soli koje se bazom mogu prevesti u hidrokside. Mogu se smatrati supstituisanim amonijum hidroksidom
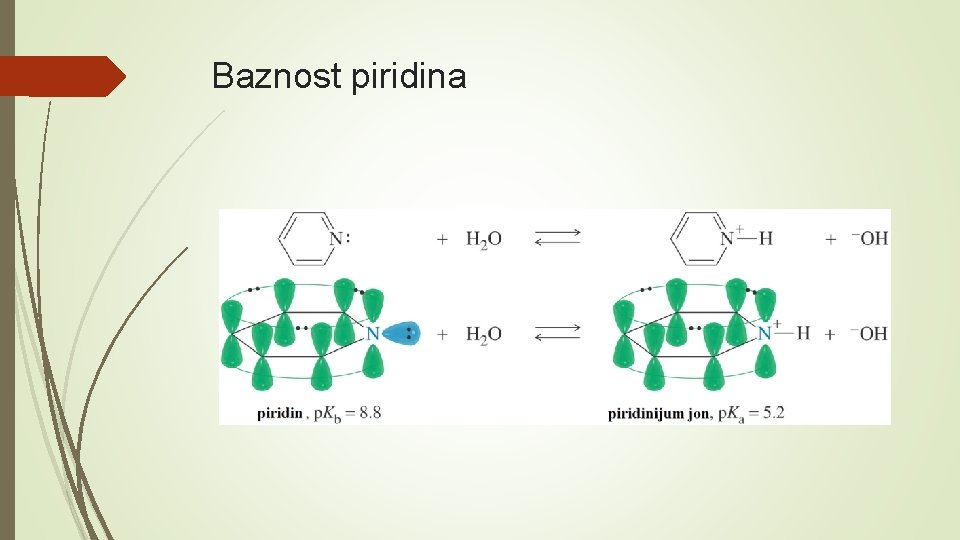
Baznost piridina
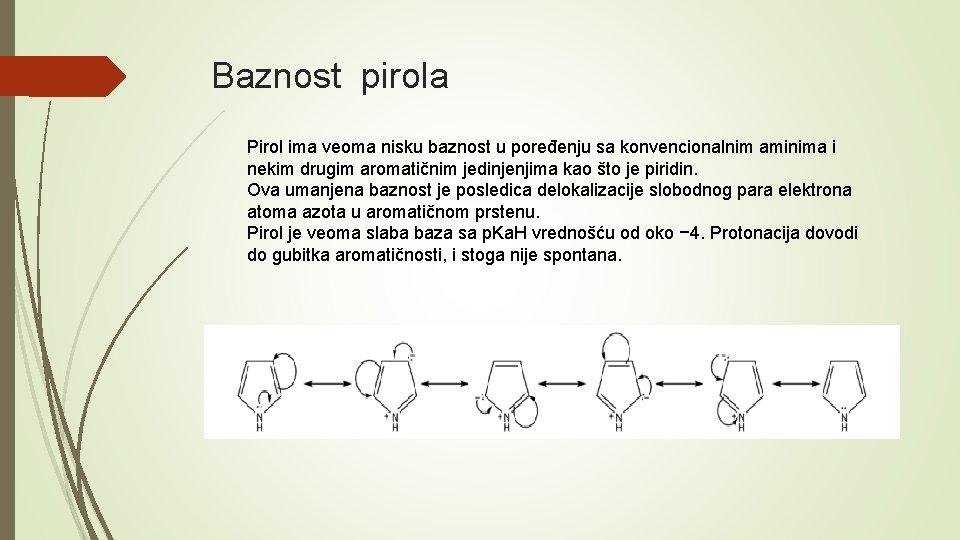
Baznost pirola Pirol ima veoma nisku baznost u poređenju sa konvencionalnim aminima i nekim drugim aromatičnim jedinjenjima kao što je piridin. Ova umanjena baznost je posledica delokalizacije slobodnog para elektrona atoma azota u aromatičnom prstenu. Pirol je veoma slaba baza sa p. Ka. H vrednošću od oko − 4. Protonacija dovodi do gubitka aromatičnosti, i stoga nije spontana.

Kiselost tiola Tioli su kiseliji od alkohola i u vodenim rastvorima daju proton vodi: C 2 H 5 SH + H 2 O ⇄ C 2 H 5 S- + H 3 O+ Reaguju sa vodenim rastvorima jakih baza dajući soli: C 2 H 5 SH + Na. OH → C 2 H 5 S- Na+ + H 2 O Soli teških metala (Pb, Hg, Cu, Cd i Ag) su nerastvorne vodi. Ime merkaptan (lat. mercurium captans, oteta živa) potiče od lakoće stvaranja nerastvornih živinih soli.
- Slides: 23