10 Aomatini ugljovodonici Struktura benzena Aromatinost Nomenklatura Fizike

10 -Aomatični ugljovodonici • • • Struktura benzena Aromatičnost Nomenklatura Fizičke osobine Reakcije benzena Elektrofilna aromatična supstitucija (EAS) 1

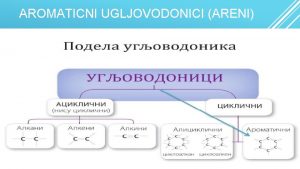
Aromati-areni (Ar) • Aroma, grčki – miris • Aromati - (prvobitno značenje, mirisne supstance izolovane iz prirodnog materijala) • Aromati –(aktuelno zančenje, supstance za koje su karakteristične: 1. elektrofilne i nukleofilne supstitucione reakcije uprkos nezasićenosti, 2. delokalizacija -elektrona, 3. položaj signala u NMR (nuklearna magnetna rezonanca) spektrima 2

Benzen: • izolovan iz gasa za osvetljenje (1825, Michael Faraday) • Dobijen iz benzoeve kiseline – (prvobitno ime benzin) i određena molekulska formula C 6 H 6 (1834, Eilhardt Mitscherlich) • Iz katrana uglja (1845, August W. von Hofmann) – industrijski • Od 1950. industrijski iz nafte • Za dobijanje stirena (polistirenski polomeri) 3
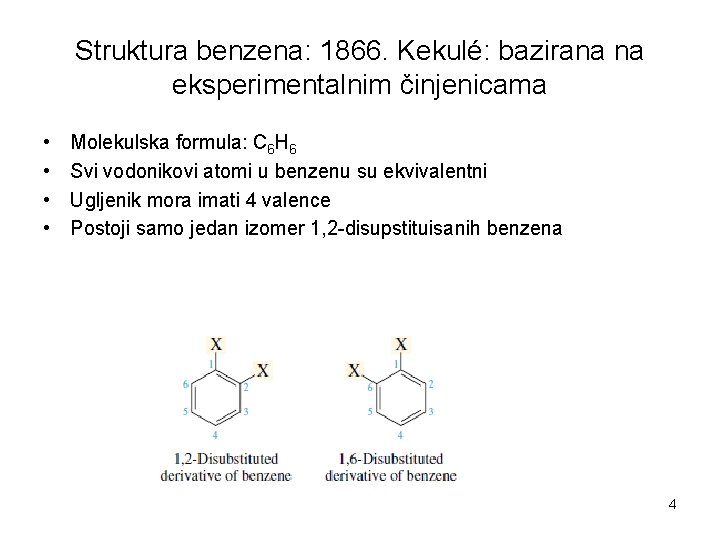
Struktura benzena: 1866. Kekulé: bazirana na eksperimentalnim činjenicama • • Molekulska formula: C 6 H 6 Svi vodonikovi atomi u benzenu su ekvivalentni Ugljenik mora imati 4 valence Postoji samo jedan izomer 1, 2 -disupstituisanih benzena 4
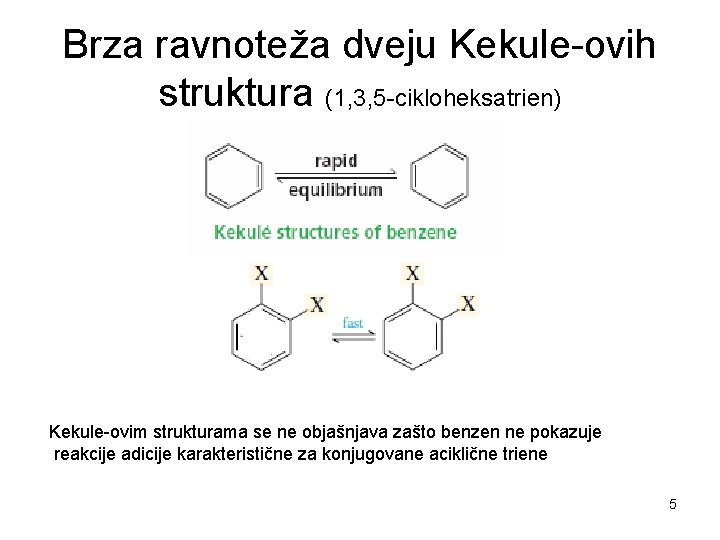
Brza ravnoteža dveju Kekule-ovih struktura (1, 3, 5 -cikloheksatrien) Kekule-ovim strukturama se ne objašnjava zašto benzen ne pokazuje reakcije adicije karakteristične za konjugovane aciklične triene 5

6

Sve C-C veze su iste dužine, 140 pm Sve C-H veze iste dužine, 108 pm Uglovi 1200 planaran 7
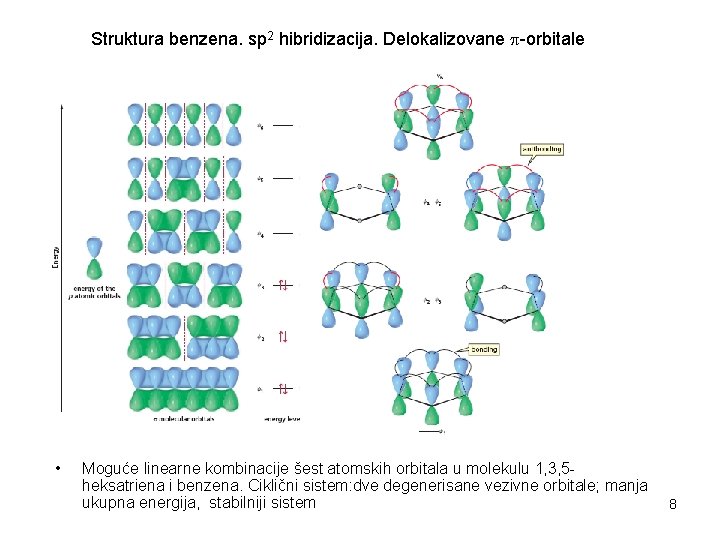
Struktura benzena. sp 2 hibridizacija. Delokalizovane -orbitale • Moguće linearne kombinacije šest atomskih orbitala u molekulu 1, 3, 5 heksatriena i benzena. Ciklični sistem: dve degenerisane vezivne orbitale; manja ukupna energija, stabilniji sistem 8

Energetski dijagram -orbitala 1, 3, 5 -heksatriena i benzena 9
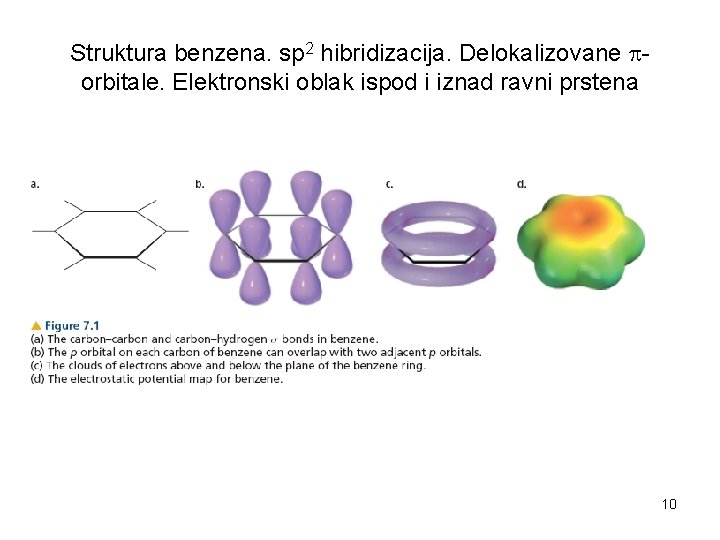
Struktura benzena. sp 2 hibridizacija. Delokalizovane orbitale. Elektronski oblak ispod i iznad ravni prstena 10
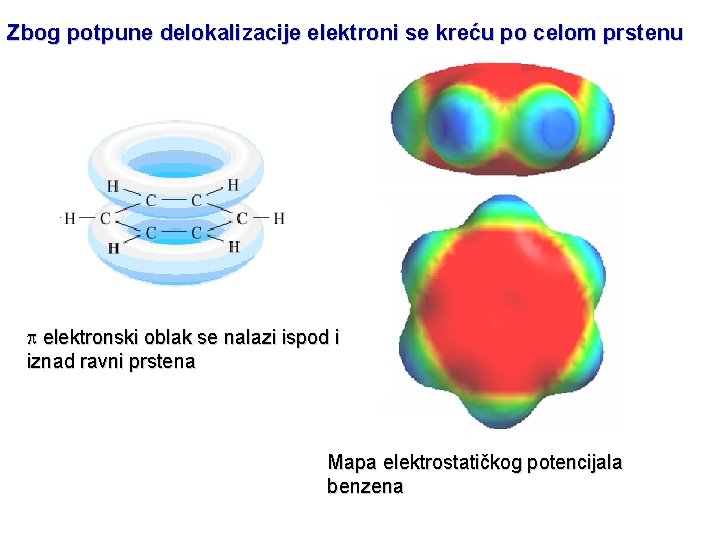
Zbog potpune delokalizacije elektroni se kreću po celom prstenu elektronski oblak se nalazi ispod i iznad ravni prstena Mapa elektrostatičkog potencijala benzena
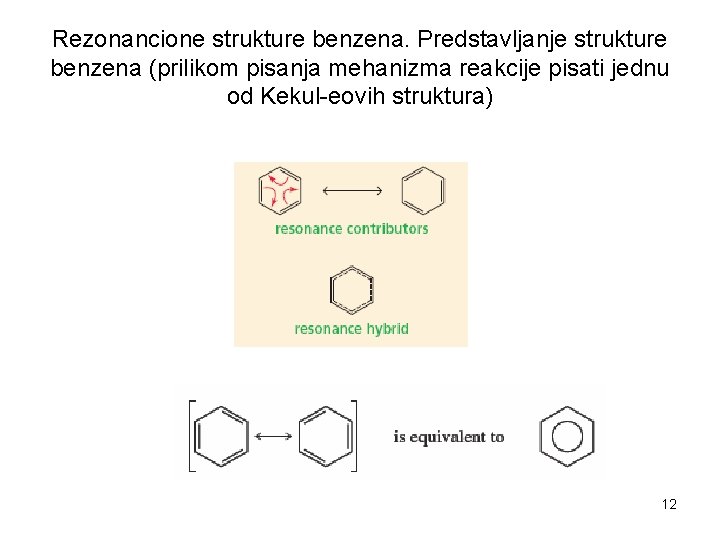
Rezonancione strukture benzena. Predstavljanje strukture benzena (prilikom pisanja mehanizma reakcije pisati jednu od Kekul-eovih struktura) 12

Frost-Musulin-ov metod određivanja energetskih nivoa molekulskih orbitala u monocikličnim konjugovanim ugljovodonicima Energetski nivoi MO cikličnih konjugovanih ugljovodonika se nalaze na dodirnim tačkama upisanih pravilnih poligona sa n temena u krugu poluprečnika 2 i vrhom na dole. Energija elektrona u p AO se označava sa α. Energija vezivne MO, koja nastaje iz dve p AO, se označava sa α + , a antivezivne sa α - . Dakle, je promena u energiji kada se elektron delokalizuje na dva C atoma. Kako vezivna MO može sadržavati dva elektrona, to je sistem od dva elektrona u vezivnoj MO, za 2 stabilniji od sistema sa dva elektrona u dve p AO. 13

Struktura grafita. Paralelni slojevi kondenzovanih prstenova sličnih benzenu 14

Struktura fulerena. Ima 60 C sp 2 atoma povezanih u petočlane i šestočlane prstenove. Nije aromatičan, podleže adicionim reakcijama. Delokalizacija je ograničena zbog preklapanja nehibridizovanih p orbitala pod uglom. 15

Struktura ‘’nanotube-a’’. Krajevi su polovina fulerena a središnji oblik valjka formiraju šestočlani prstenovi. Svi C atomi su sp 2 hibridizovani. 16
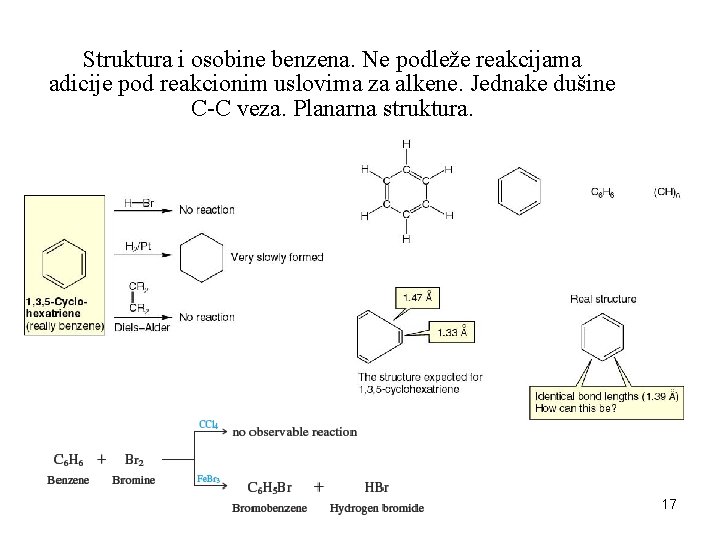
Struktura i osobine benzena. Ne podleže reakcijama adicije pod reakcionim uslovima za alkene. Jednake dušine C-C veza. Planarna struktura. 17
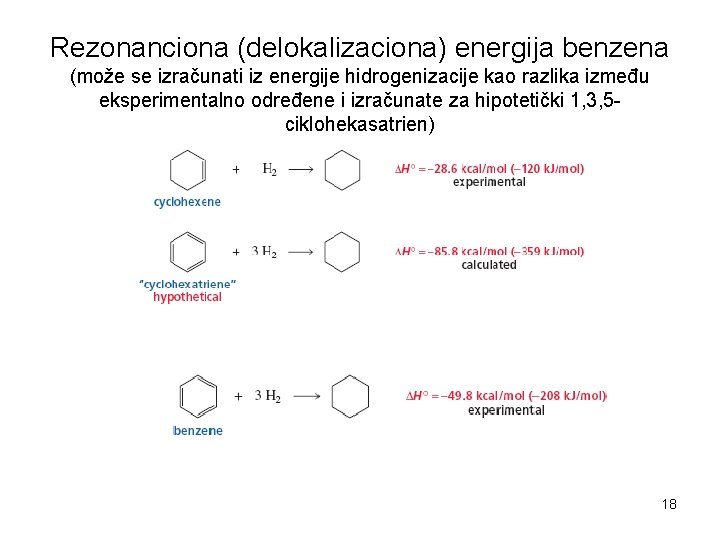
Rezonanciona (delokalizaciona) energija benzena (može se izračunati iz energije hidrogenizacije kao razlika između eksperimentalno određene i izračunate za hipotetički 1, 3, 5 ciklohekasatrien) 18
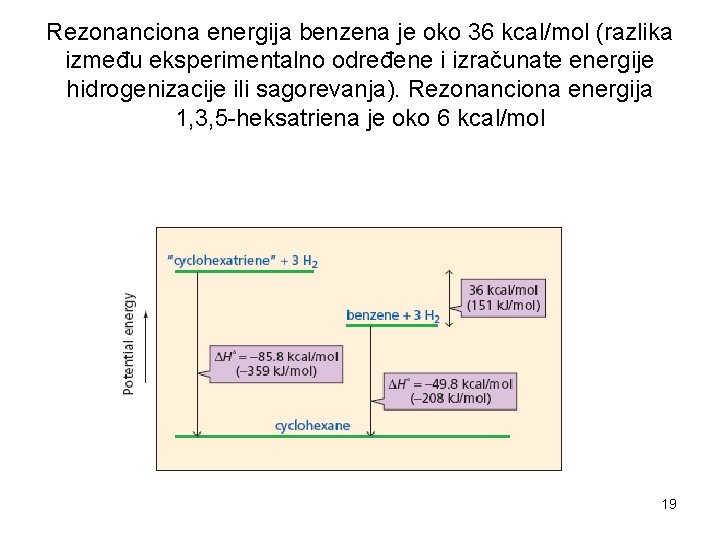
Rezonanciona energija benzena je oko 36 kcal/mol (razlika između eksperimentalno određene i izračunate energije hidrogenizacije ili sagorevanja). Rezonanciona energija 1, 3, 5 -heksatriena je oko 6 kcal/mol 19

Aromatične su strukture koje w Imaju cikličnu strukturu w Potpuno su konjugovane w Planarne (svi atomi u prstenu su sp 2 -hibridizovani) w Imaju Hückel-ov broj elektrona: (4 n + 2) -elektrona (gde je n = 0, 1, 2, 3. . . ) 20

Relativna stabilnost cikličnih i acikličnih poliena delokalizaciona energijaja/e– 0. 37 0. 41 1. 0 a 0. 24 0. 21 0. 0 aa 0. 41 a 0. 17 0. 12 0. 0 0. 31 aa aa 0. 33 a aromatični: stabilniji od otvorenog niza, energija delokalizacije veća od acikličnog analoga antiaromatični: manje stabilni od otvorenog niza, energija delokalizacije manja od acikličnog analoga nearomatični: ~približna stabilnost kao otvoreni niz, energije delokalizacije približne u cikličnom 21 i acikličnom

D. Aromatični (Hückel-ovi 4 n+2 sistemi) Ciklični, planarni, konjugovani sistemi (na svakom atomu u prstenu imaju praznu, polupopunjnu ili popunjenu p orbitalu) sa 4 n+2 elektrona poseduju specijalnu (aromatičnu) stabilnost. Karakteristike : • Termodinamička stabilnost • reaktivnost (elektrofilna aromatična supstitucija umesto adicije karakteristične za alkene otvorenog niza) • spektroskopske karakteristike 22

Posledica delokalizacije: kiselost ciklopentadiena (H atom vezan za sp 3 C atom je kiseliji od H atoma vezanog za sp 2 C i H atom u etanu zbog aromatičnosti ciklopentadienilnog anjona). 23

Elektronska delokalizacija u ciklopentadienil-anjonu H H – • • H • • – H H H H • • H H H – • • H H H • • – H H H
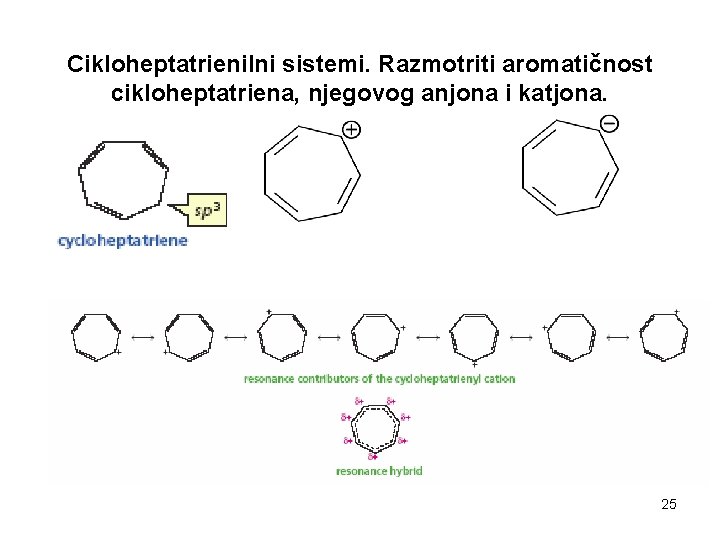
Cikloheptatrienilni sistemi. Razmotriti aromatičnost cikloheptatriena, njegovog anjona i katjona. 25
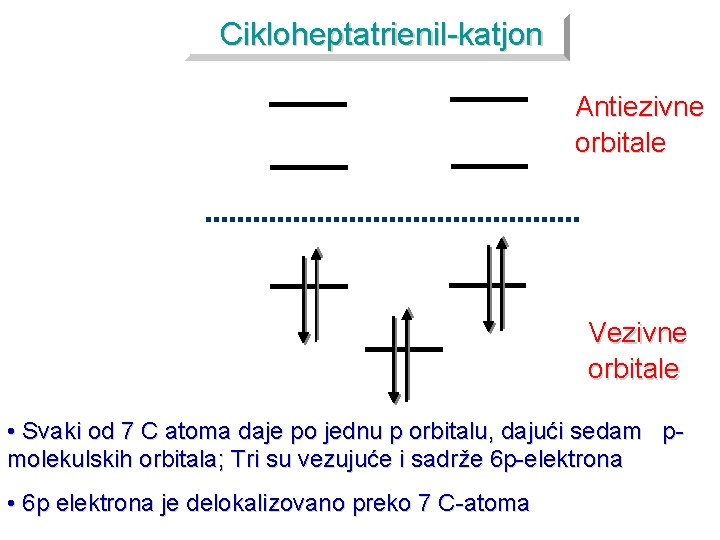
Cikloheptatrienil-katjon Antiezivne orbitale Vezivne orbitale • Svaki od 7 C atoma daje po jednu p orbitalu, dajući sedam pmolekulskih orbitala; Tri su vezujuće i sadrže 6 p-elektrona • 6 p elektrona je delokalizovano preko 7 C-atoma
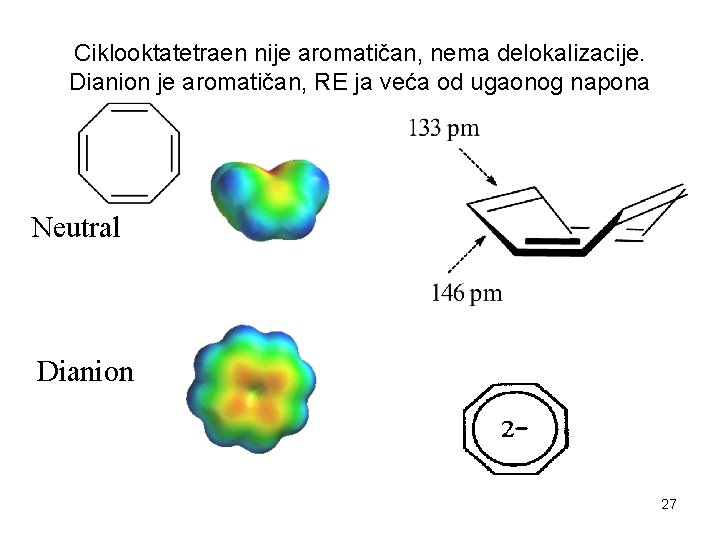
Ciklooktatetraen nije aromatičan, nema delokalizacije. Dianion je aromatičan, RE ja veća od ugaonog napona Neutral Dianion 27
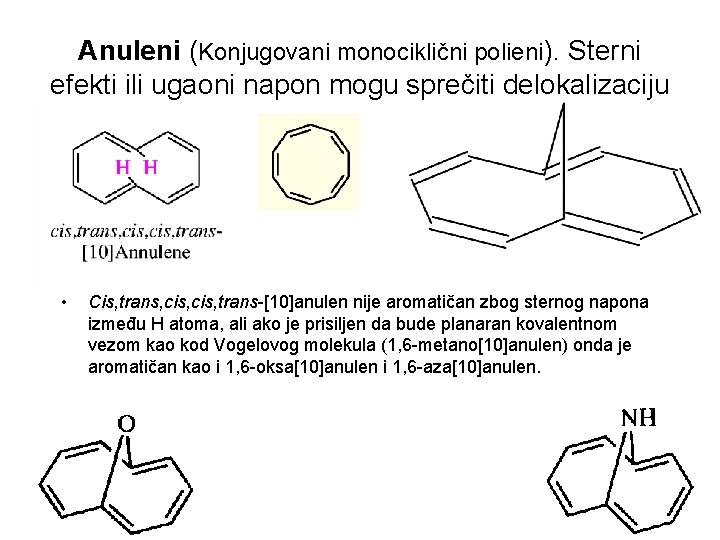
Anuleni (Konjugovani monociklični polieni). Sterni efekti ili ugaoni napon mogu sprečiti delokalizaciju • Cis, trans, cis, trans-[10]anulen nije aromatičan zbog sternog napona između H atoma, ali ako je prisiljen da bude planaran kovalentnom vezom kao kod Vogelovog molekula (1, 6 -metano[10]anulen) onda je aromatičan kao i 1, 6 -oksa[10]anulen i 1, 6 -aza[10]anulen. 28
![[10]-Anulen sve-cis ciklodekapentaen vrlo reaktivan Trebalo bi da bude aromatičan na osnovu Hückel-ovog pravila [10]-Anulen sve-cis ciklodekapentaen vrlo reaktivan Trebalo bi da bude aromatičan na osnovu Hückel-ovog pravila](http://slidetodoc.com/presentation_image/53754e8f425662c752f37829781f4c7a/image-29.jpg)
[10]-Anulen sve-cis ciklodekapentaen vrlo reaktivan Trebalo bi da bude aromatičan na osnovu Hückel-ovog pravila ali. . . Kad su sve veze CIS kod planarnog sistema se javlja značajan ugaoni napon Pravilni desetougao ima uglove od 144 o
![[10]-Anulen Cis, trans, cis, trans ciklodekapentaen Uvođenjem dve trans C=C veze slabi ugaoni napon [10]-Anulen Cis, trans, cis, trans ciklodekapentaen Uvođenjem dve trans C=C veze slabi ugaoni napon](http://slidetodoc.com/presentation_image/53754e8f425662c752f37829781f4c7a/image-30.jpg)
[10]-Anulen Cis, trans, cis, trans ciklodekapentaen Uvođenjem dve trans C=C veze slabi ugaoni napon ali se između vodonika sa trans veza javlja van der Waals-ove interakcije. Molekul odstupa od planarne geometrije što ograničava mogućnost stabilizacije prstena preko elektronske delokalizacije
![[16]-Anulen 16 elektrona ne zadovoljavaju Hückel-ovo pravilo Naizmenične kraće (134 pm) i duže veze [16]-Anulen 16 elektrona ne zadovoljavaju Hückel-ovo pravilo Naizmenične kraće (134 pm) i duže veze](http://slidetodoc.com/presentation_image/53754e8f425662c752f37829781f4c7a/image-31.jpg)
[16]-Anulen 16 elektrona ne zadovoljavaju Hückel-ovo pravilo Naizmenične kraće (134 pm) i duže veze (146 pm) veze Prema Hückel-u anuleni sa 4 n -elektronima nisu aromatični (antiaromatični).
![[18]-Anulen 18 elektrona zadovoljava Hückel-ovo pravilo, n=4 [18]-Anulen je dovoljno prostran, tako da njegovi [18]-Anulen 18 elektrona zadovoljava Hückel-ovo pravilo, n=4 [18]-Anulen je dovoljno prostran, tako da njegovi](http://slidetodoc.com/presentation_image/53754e8f425662c752f37829781f4c7a/image-32.jpg)
[18]-Anulen 18 elektrona zadovoljava Hückel-ovo pravilo, n=4 [18]-Anulen je dovoljno prostran, tako da njegovi unutrašnji H atomi ne deluju jedan na drugi, nije narušena planarnost. C-C veze su od 137 -143 pm (slične vezama kod benzena) Rezonanciona energija je oko 418 k. J/mol

Aromatičnost benzenoidnih ugljovodonika • Naftalen (aromatičan) • 61 kcal/mol 33

Naftalen Konjugovani sistem je proširen u odnosu na benzen. Dodatna 4 elekrtona se efikasno preklapaju sa onima na benzenovom prstenu. Dužina veza neznatno odstupa od onih kod benzena, ali se znatno razlikuju od jednostrukih i dvostrukih. Orbitalna predstava naftalena pokazuje prošireno preklapanje p-orbitala.
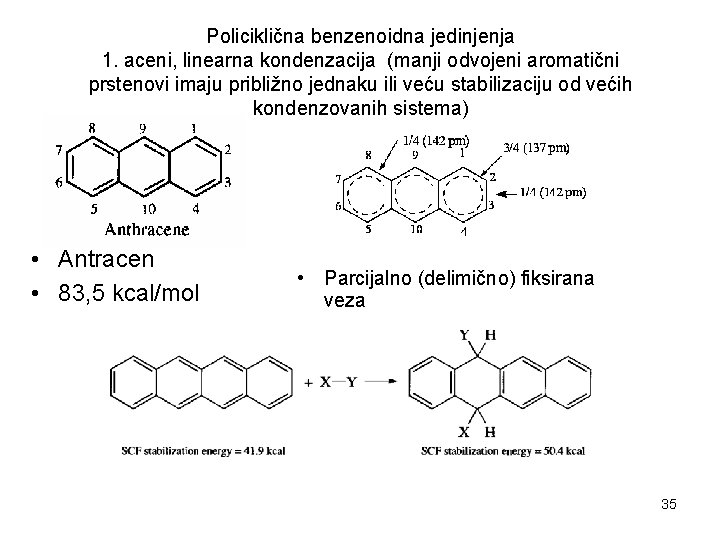
Policiklična benzenoidna jedinjenja 1. aceni, linearna kondenzacija (manji odvojeni aromatični prstenovi imaju približno jednaku ili veću stabilizaciju od većih kondenzovanih sistema) • Antracen • 83, 5 kcal/mol • Parcijalno (delimično) fiksirana veza 35

Antracen ne može da se prikaže pomoću samo jedne Lewis-ove strukture u kojoj sva tri prstena odgovaraju Kekulé-vim formulama Antracen ima četiri rezonantne strukture, i to samo dve sa dva aromatična benzenova prstena. Rezonanciona energija = 347 k. J/mol

angularna kondenzacija • Fenantren • 91, 3 kcal/mol • • • C 9 -C 10 Kao izolovana dvoguba veza Ekstremna fiksacija veza 37

fenantren Fenantren ima pet rezonantnih struktura, i to jednu sa sva tri aromatična benzenova prstena, i tri sa dva zbog čega je stabilniji od antracena. Rezonanciona energija = 381 k. J/mol
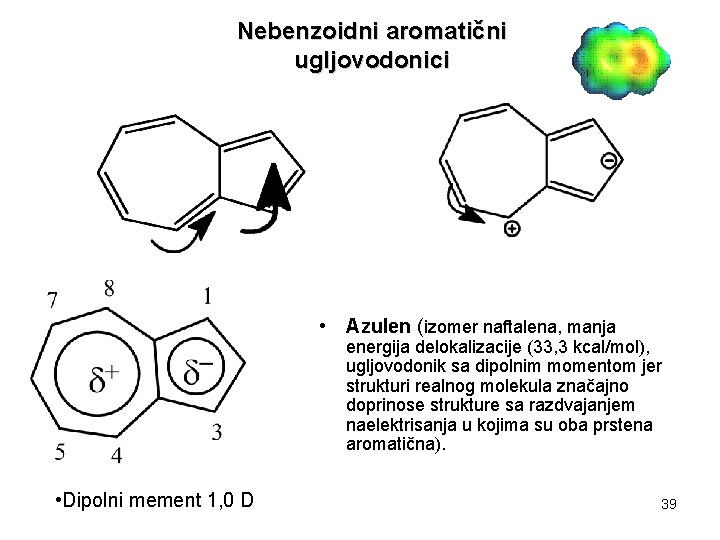
Nebenzoidni aromatični ugljovodonici • Azulen (izomer naftalena, manja energija delokalizacije (33, 3 kcal/mol), ugljovodonik sa dipolnim momentom jer strukturi realnog molekula značajno doprinose strukture sa razdvajanjem naelektrisanja u kojima su oba prstena aromatična). • Dipolni mement 1, 0 D 39
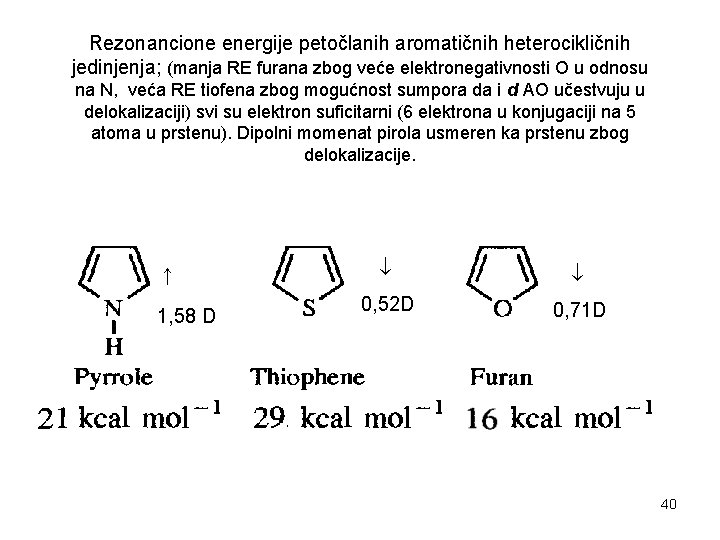
Rezonancione energije petočlanih aromatičnih heterocikličnih jedinjenja; (manja RE furana zbog veće elektronegativnosti O u odnosu na N, veća RE tiofena zbog mogućnost sumpora da i d AO učestvuju u delokalizaciji) svi su elektron suficitarni (6 elektrona u konjugaciji na 5 atoma u prstenu). Dipolni momenat pirola usmeren ka prstenu zbog delokalizacije. ↑ 1, 58 D 0, 52 D 0, 71 D 40

• 1. 58 D, pozitivan kraj dipola na azotu, elektron suficitaran, elektronska gustina na svim atomima veća od 1 41
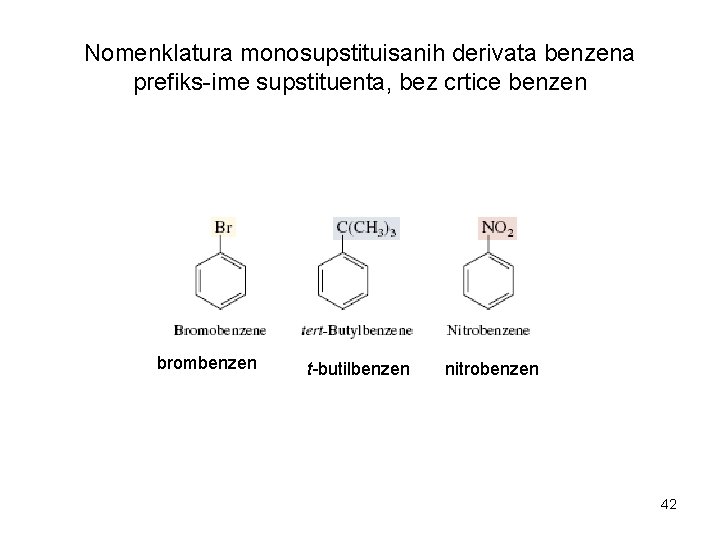
Nomenklatura monosupstituisanih derivata benzena prefiks-ime supstituenta, bez crtice benzen brombenzen t-butilbenzen nitrobenzen 42
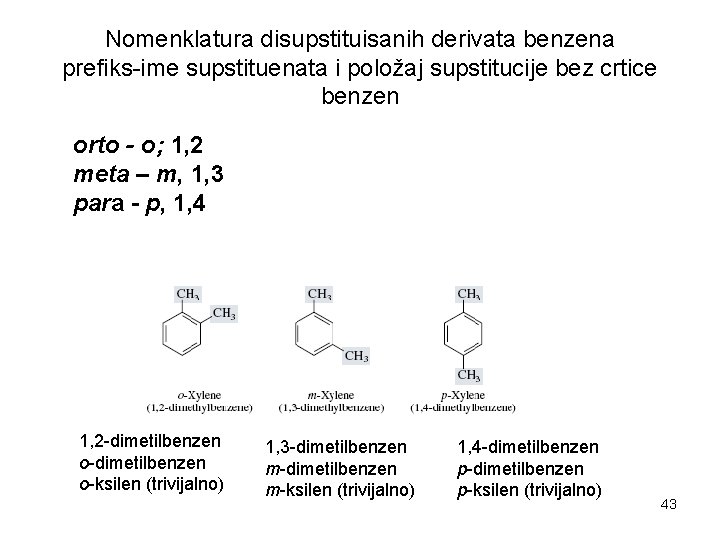
Nomenklatura disupstituisanih derivata benzena prefiks-ime supstituenata i položaj supstitucije bez crtice benzen orto - o; 1, 2 meta – m, 1, 3 para - p, 1, 4 1, 2 -dimetilbenzen o-ksilen (trivijalno) 1, 3 -dimetilbenzen m-ksilen (trivijalno) 1, 4 -dimetilbenzen p-ksilen (trivijalno) 43

Sistemska i trivijalna imena monosupstituisanih derivata benzena koji se često pojavljuju u literaturi struktura sistemsko ime benzenkarbaldehid NH 2 trivijalno ime benzaldehid benzenkarboksilna kiselina vinilbenzen benzoeva kiselina stiren Metil-fenil-keton acetofenon benzenol fenol metoksibenzen anizol aminobenzenamin anilin
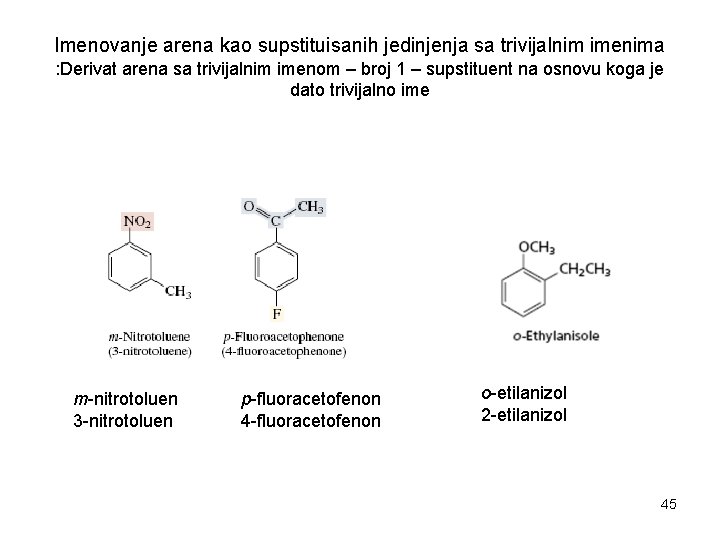
Imenovanje arena kao supstituisanih jedinjenja sa trivijalnim imenima : Derivat arena sa trivijalnim imenom – broj 1 – supstituent na osnovu koga je dato trivijalno ime m-nitrotoluen 3 -nitrotoluen p-fluoracetofenon 4 -fluoracetofenon o-etilanizol 2 -etilanizol 45
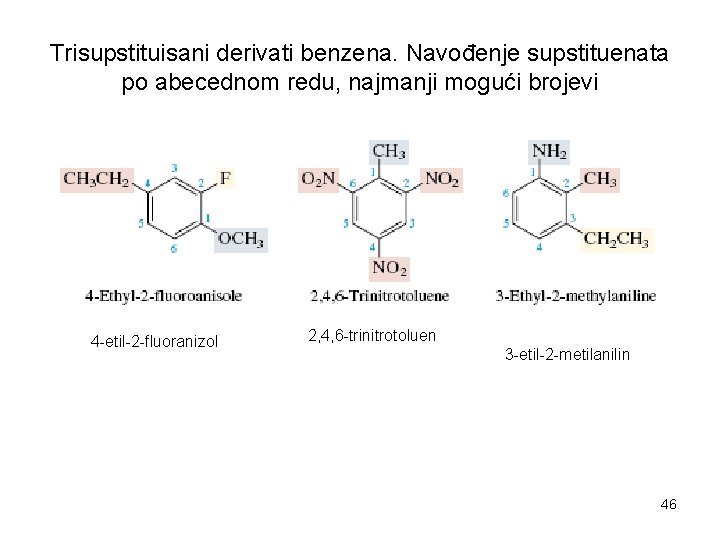
Trisupstituisani derivati benzena. Navođenje supstituenata po abecednom redu, najmanji mogući brojevi 4 -etil-2 -fluoranizol 2, 4, 6 -trinitrotoluen 3 -etil-2 -metilanilin 46
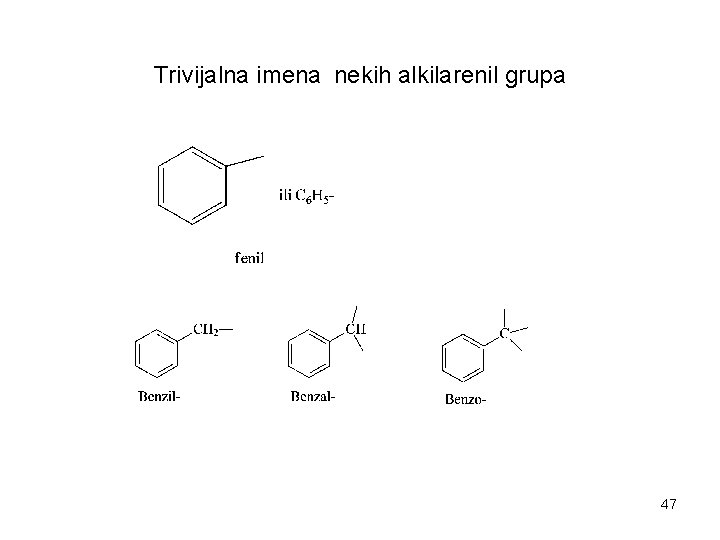
Trivijalna imena nekih alkilarenil grupa 47
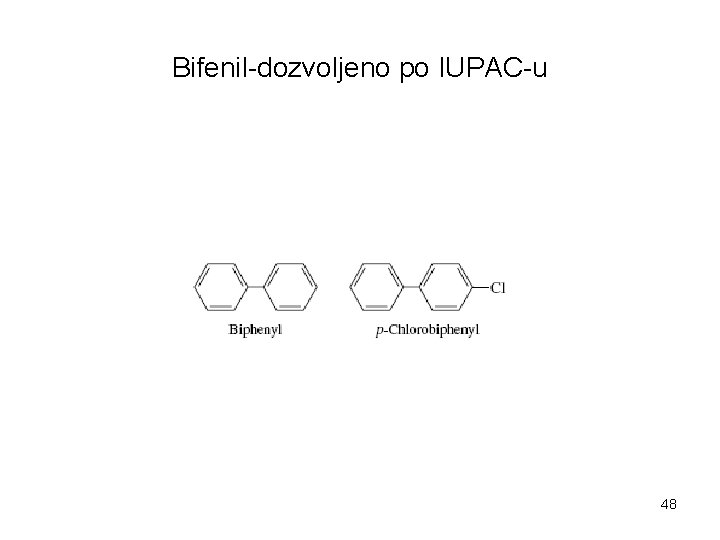
Bifenil-dozvoljeno po IUPAC-u 48
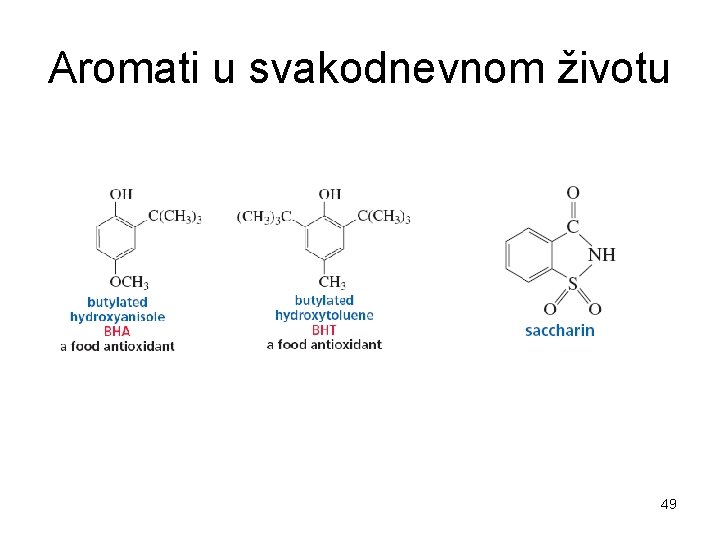
Aromati u svakodnevnom životu 49
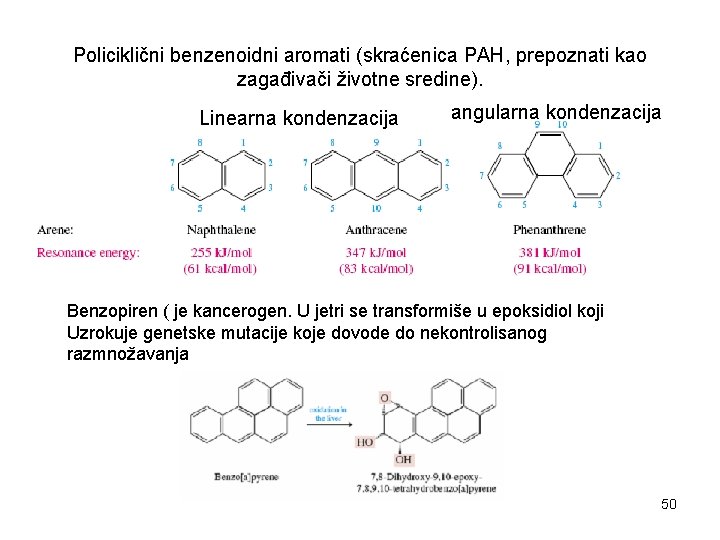
Policiklični benzenoidni aromati (skraćenica PAH, prepoznati kao zagađivači životne sredine). Linearna kondenzacija angularna kondenzacija Benzopiren ( je kancerogen. U jetri se transformiše u epoksidiol koji Uzrokuje genetske mutacije koje dovode do nekontrolisanog razmnožavanja 50
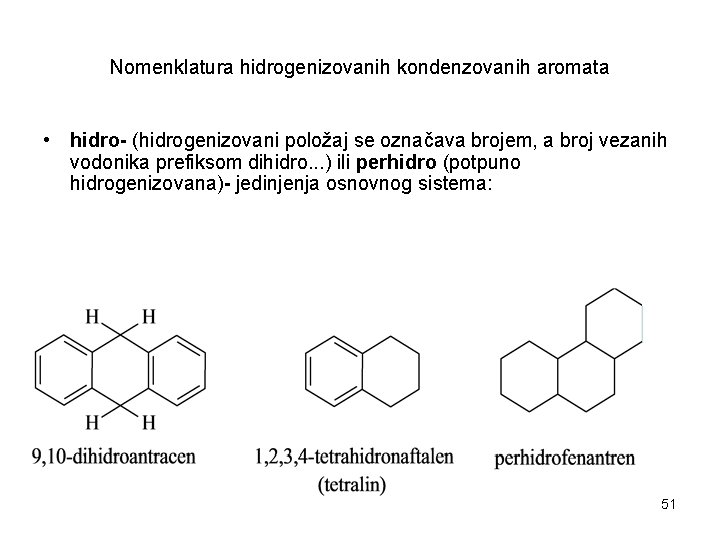
Nomenklatura hidrogenizovanih kondenzovanih aromata • hidro- (hidrogenizovani položaj se označava brojem, a broj vezanih vodonika prefiksom dihidro. . . ) ili perhidro (potpuno hidrogenizovana)- jedinjenja osnovnog sistema: 51

Fizičke osobine arena • Nepolarni • Nerastvorni u vodi • Manje gustine od vode • London-ove sile • Dobri rastvarači • Benzen izaziva leukemiju • Toluen umesto benzena( sličnu sposobnost rastvaranja, a nije kancerogen) 52

Fizičke osobine izomernih disupstituisanih benzena • što je jedinjenje simetričnije, ima višu tačku topljenja i manju rastvorljivost izomer t. t. o-ksilen -25 C m-ksilen -48 C p-ksilen +13 C 53
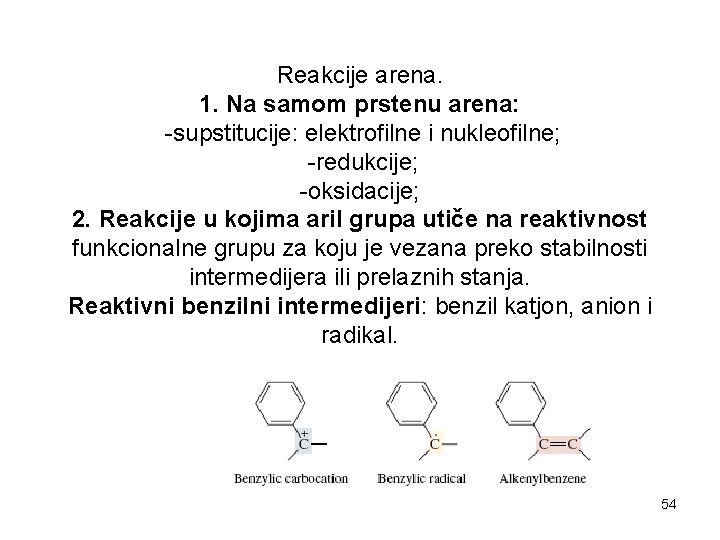
Reakcije arena. 1. Na samom prstenu arena: -supstitucije: elektrofilne i nukleofilne; -redukcije; -oksidacije; 2. Reakcije u kojima aril grupa utiče na reaktivnost funkcionalne grupu za koju je vezana preko stabilnosti intermedijera ili prelaznih stanja. Reaktivni benzilni intermedijeri: benzil katjon, anion i radikal. 54
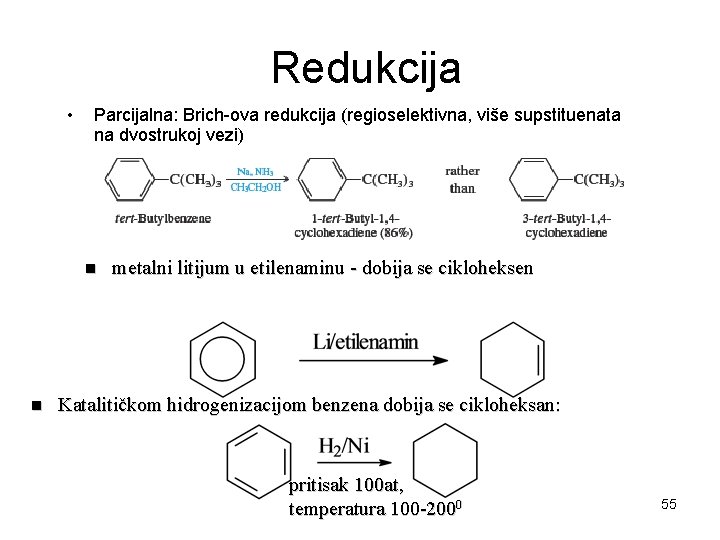
Redukcija • Parcijalna: Brich-ova redukcija (regioselektivna, više supstituenata na dvostrukoj vezi) n n metalni litijum u etilenaminu - dobija se cikloheksen Katalitičkom hidrogenizacijom benzena dobija se cikloheksan: pritisak 100 at, temperatura 100 -2000 55

Oksidacija alkilarena-samo ako postoji benzilni H koji omogućava nastajanje reaktivnog intermedijera 56
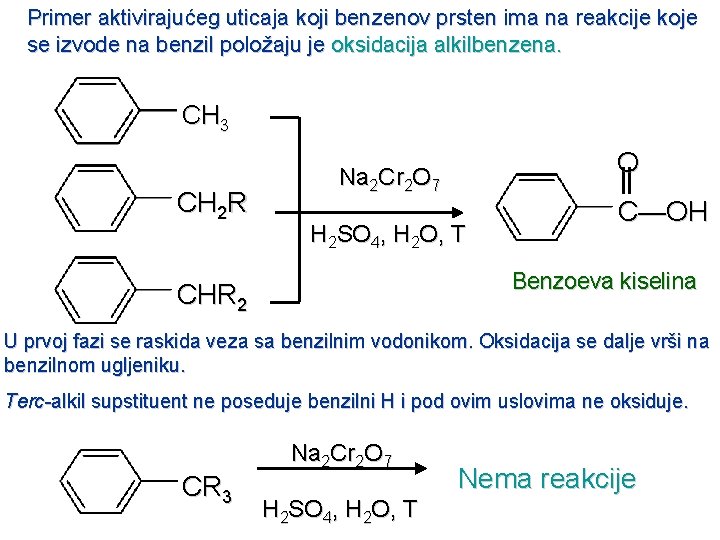
Primer aktivirajućeg uticaja koji benzenov prsten ima na reakcije koje se izvode na benzil položaju je oksidacija alkilbenzena. CH 3 CH 2 R O Na 2 Cr 2 O 7 H 2 SO 4, H 2 O, T C—OH Benzoeva kiselina CHR 2 U prvoj fazi se raskida veza sa benzilnim vodonikom. Oksidacija se dalje vrši na benzilnom ugljeniku. Terc-alkil supstituent ne poseduje benzilni H i pod ovim uslovima ne oksiduje. Na 2 Cr 2 O 7 CR 3 H 2 SO 4, H 2 O, T Nema reakcije

Kada su dve alkil grupe prisutne na benzenovom prstenu obe se oksiduju. O C—OH CH(CH 3)2 Na 2 Cr 2 O 7 H 2 SO 4, H 2 O, T CH 3 p-izopropiltoluen C—OH O (45%) p-benzendikarboksilna kiselina (tereftalna kiselina)
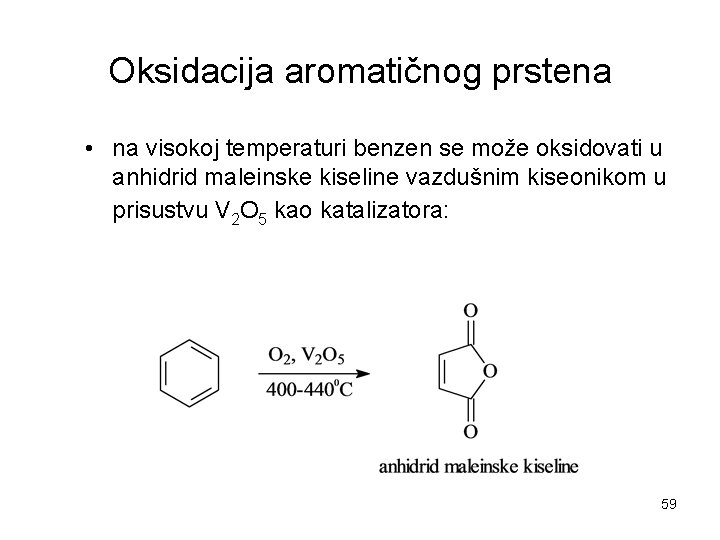
Oksidacija aromatičnog prstena • na visokoj temperaturi benzen se može oksidovati u anhidrid maleinske kiseline vazdušnim kiseonikom u prisustvu V 2 O 5 kao katalizatora: 59

Oksidacija aromatičnog prstena • Naftalen se oksiduje u anhidrid ftalne kiseline: n Ftalanhidrid se takođe može dobiti i oksidacijom o-ksilena: 60
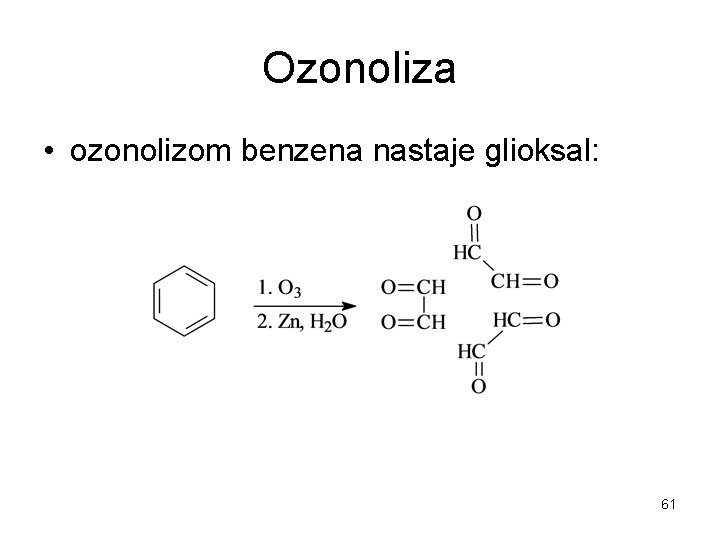
Ozonoliza • ozonolizom benzena nastaje glioksal: 61
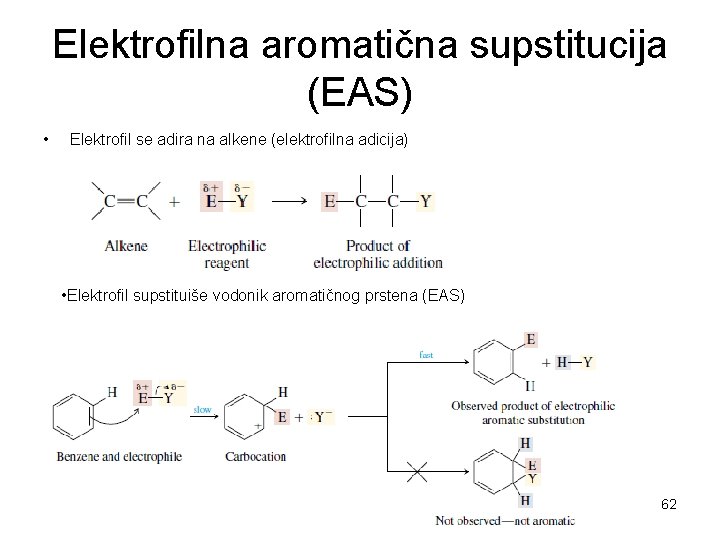
Elektrofilna aromatična supstitucija (EAS) • Elektrofil se adira na alkene (elektrofilna adicija) • Elektrofil supstituiše vodonik aromatičnog prstena (EAS) 62

Zašto supstitucija a ne adicija? Adicija na arene je endergoni proces (proizvod je termodinamički manje stabilan od reaktanta). Adicioni proizvod nema aromatičnu strukturu. Supstitucioni je aromatičan (ima stabilnost približnu stabilnosti reaktanta). 63
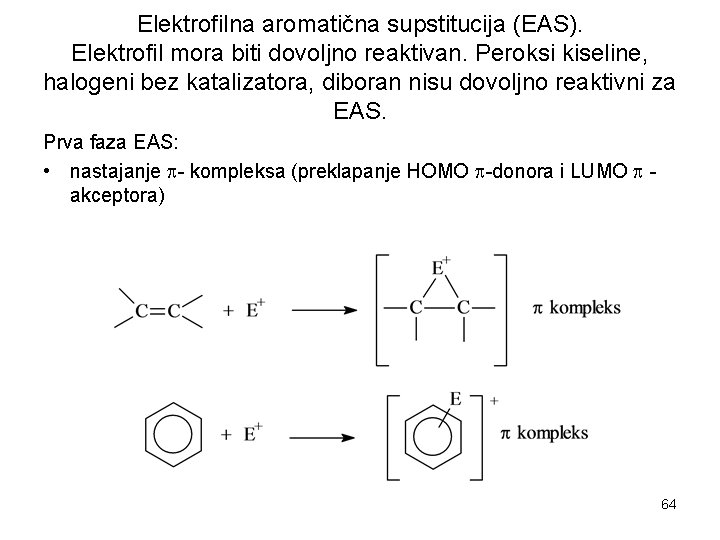
Elektrofilna aromatična supstitucija (EAS). Elektrofil mora biti dovoljno reaktivan. Peroksi kiseline, halogeni bez katalizatora, diboran nisu dovoljno reaktivni za EAS. Prva faza EAS: • nastajanje - kompleksa (preklapanje HOMO -donora i LUMO akceptora) 64
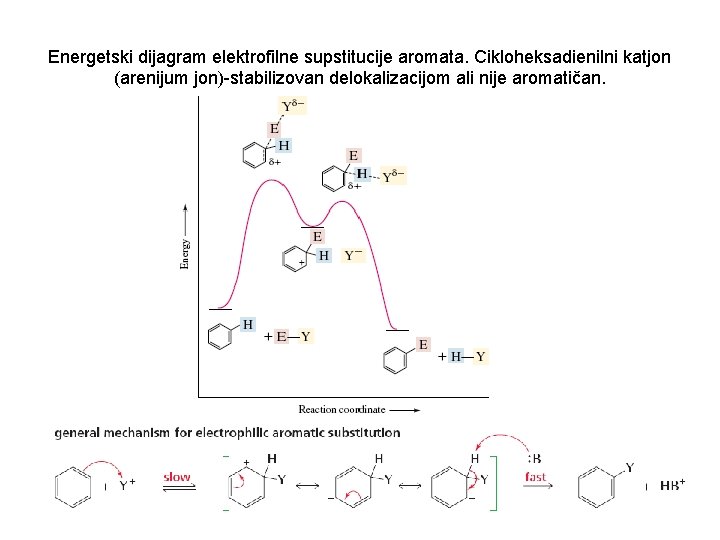
Energetski dijagram elektrofilne supstitucije aromata. Cikloheksadienilni katjon (arenijum jon)-stabilizovan delokalizacijom ali nije aromatičan. 65
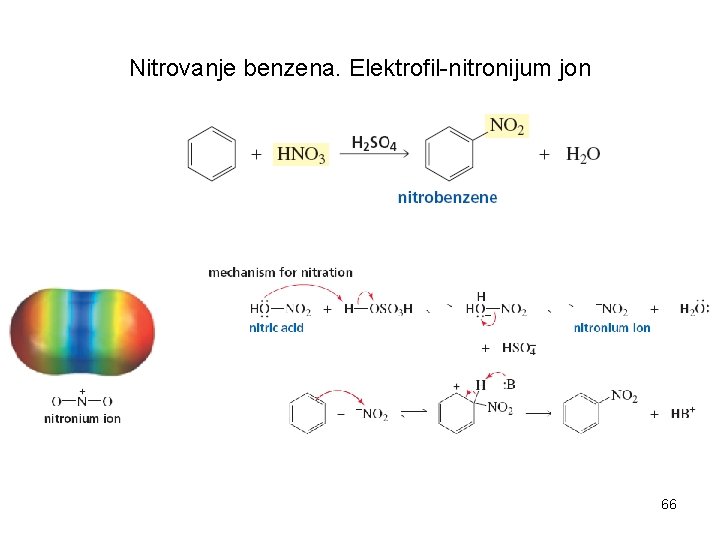
Nitrovanje benzena. Elektrofil-nitronijum jon 66
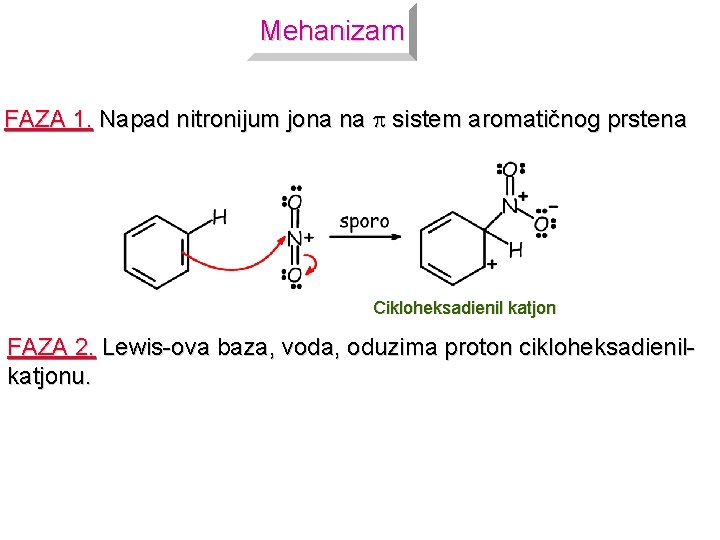
Mehanizam FAZA 1. Napad nitronijum jona na sistem aromatičnog prstena Cikloheksadienil katjon FAZA 2. Lewis-ova baza, voda, oduzima proton cikloheksadienilkatjonu.
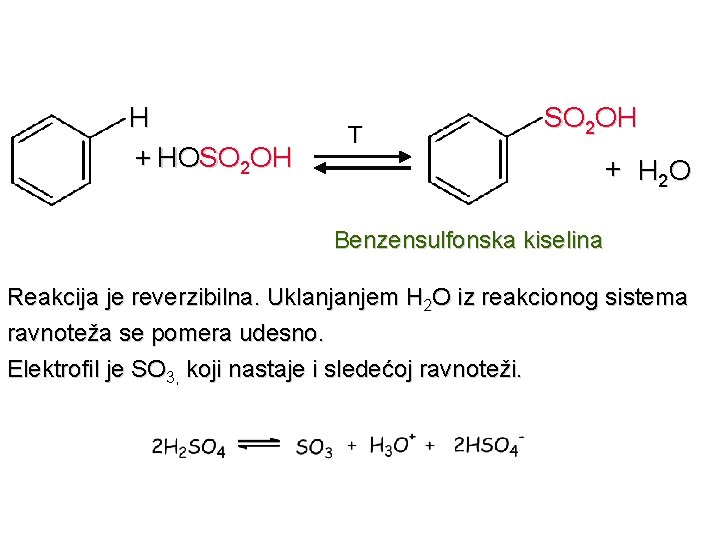
H + HOSO 2 OH T SO 2 OH + H 2 O Benzensulfonska kiselina Reakcija je reverzibilna. Uklanjanjem H 2 O iz reakcionog sistema ravnoteža se pomera udesno. Elektrofil je SO 3, koji nastaje i sledećoj ravnoteži.
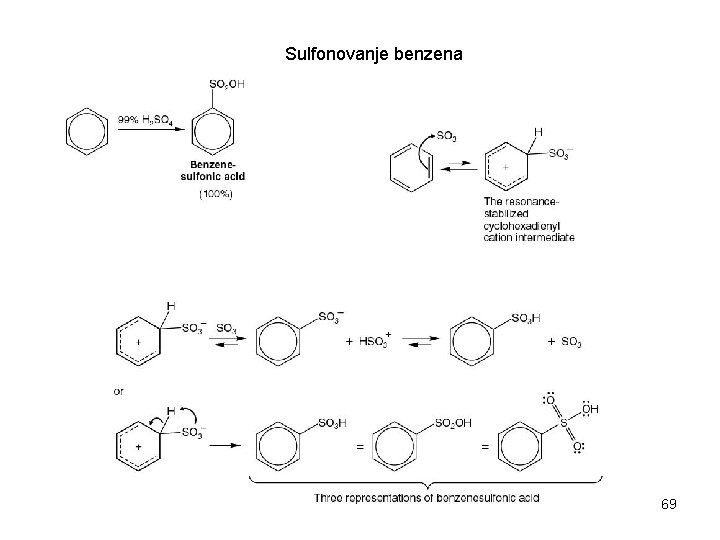
Sulfonovanje benzena 69
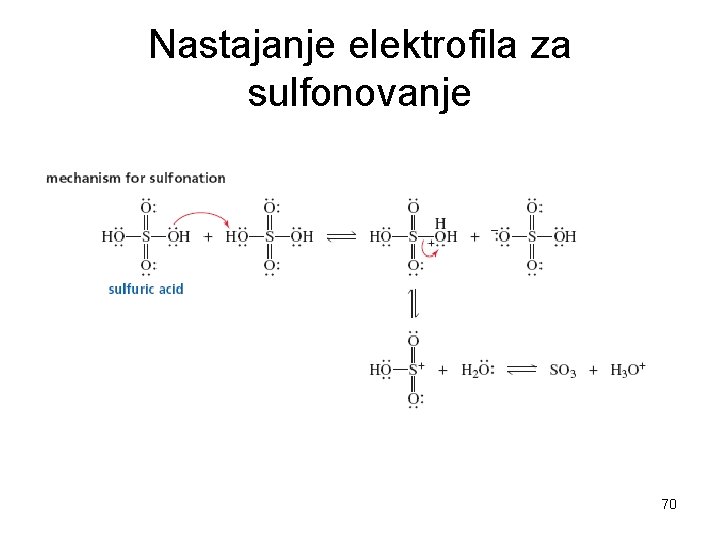
Nastajanje elektrofila za sulfonovanje 70

Reakcija je mnogo brža kada se koristi pušljiva H 2 SO 4 (8% SO 3 u konc. H 2 SO 4). H + SO 3 H 2 SO 4 SO 2 OH Benzensulfonska kiselina I u ovom slučaju elektrofil je sumpor(VI)-oksid (SO 3). • • – • Zbog jakog elektron-privlačnog • + O • • S • • O • • dejstva tri kiseonikova atoma, sumpor iz SO 3 je dovoljno elektrofilan da napadne benzen.
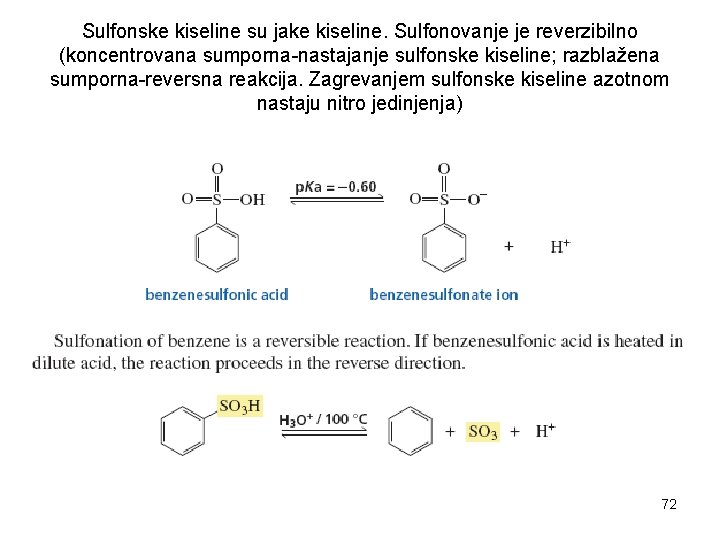
Sulfonske kiseline su jake kiseline. Sulfonovanje je reverzibilno (koncentrovana sumporna-nastajanje sulfonske kiseline; razblažena sumporna-reversna reakcija. Zagrevanjem sulfonske kiseline azotnom nastaju nitro jedinjenja) 72
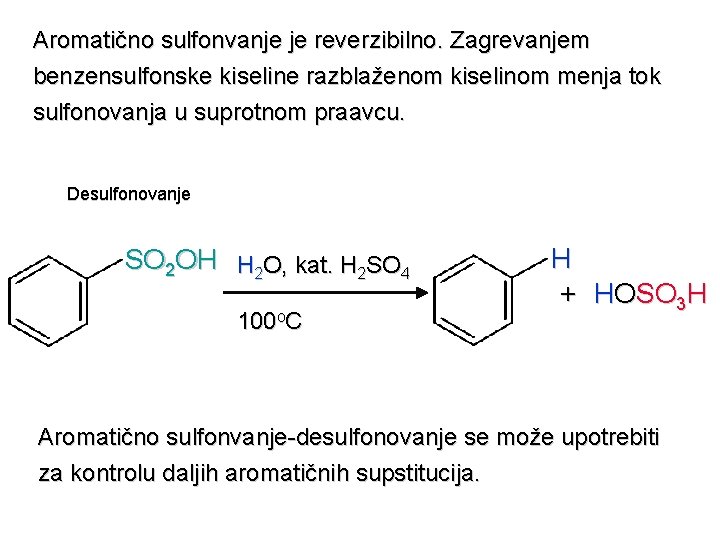
Aromatično sulfonvanje je reverzibilno. Zagrevanjem benzensulfonske kiseline razblaženom kiselinom menja tok sulfonovanja u suprotnom praavcu. Desulfonovanje SO 2 OH H 2 O, kat. H 2 SO 4 100 o. C H + HOSO 3 H Aromatično sulfonvanje-desulfonovanje se može upotrebiti za kontrolu daljih aromatičnih supstitucija.
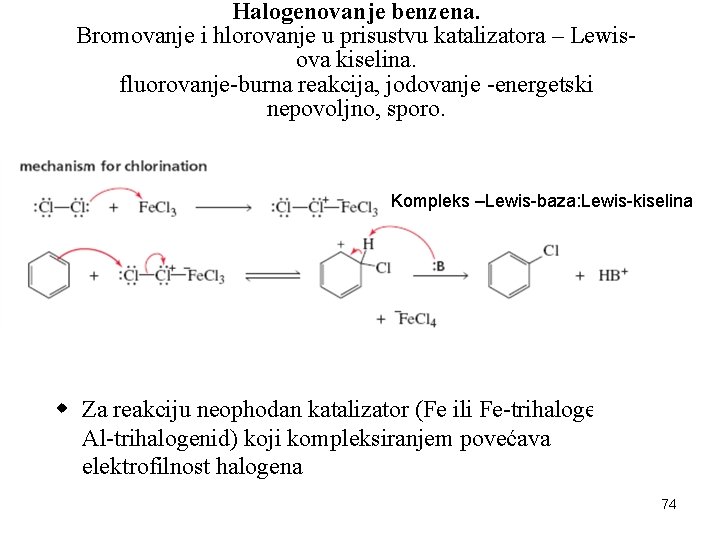
Halogenovanje benzena. Bromovanje i hlorovanje u prisustvu katalizatora – Lewisova kiselina. fluorovanje-burna reakcija, jodovanje -energetski nepovoljno, sporo. Kompleks –Lewis-baza: Lewis-kiselina w Za reakciju neophodan katalizator (Fe ili Fe-trihalogenidi ili Al-trihalogenid) koji kompleksiranjem povećava elektrofilnost halogena 74
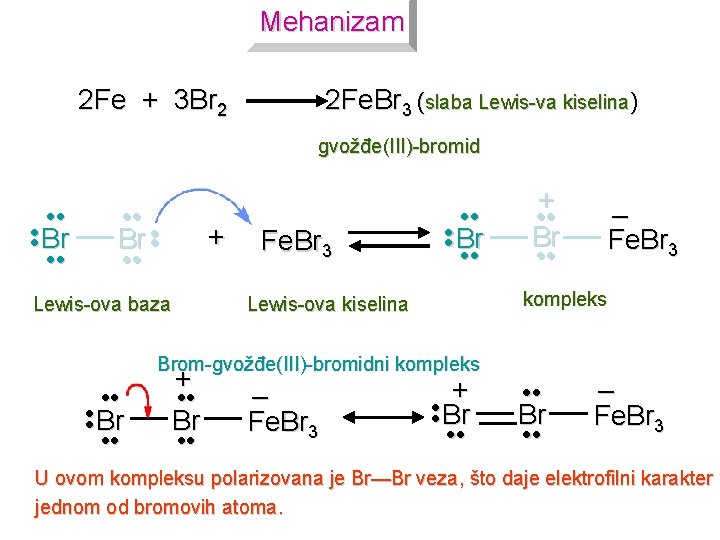
Mehanizam 2 Fe + 3 Br 2 2 Fe. Br 3 (slaba Lewis-va kiselina) gvožđe(III)-bromid • • Br • • + Lewis-ova baza Fe. Br 3 • • Br • • + • • Br • • kompleks Lewis-ova kiselina Brom-gvožđe(III)-bromidni kompleks • • Br • • + • • Br • • – Fe. Br 3 U ovom kompleksu polarizovana je Br—Br veza, što daje elektrofilni karakter jednom od bromovih atoma.
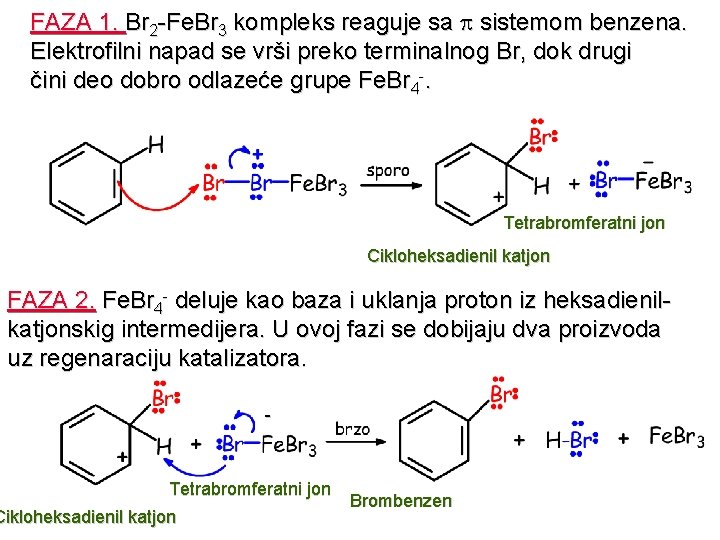
FAZA 1. Br 2 -Fe. Br 3 kompleks reaguje sa sistemom benzena. Elektrofilni napad se vrši preko terminalnog Br, dok drugi čini deo dobro odlazeće grupe Fe. Br 4 -. Tetrabromferatni jon Cikloheksadienil katjon FAZA 2. Fe. Br 4 - deluje kao baza i uklanja proton iz heksadienilkatjonskig intermedijera. U ovoj fazi se dobijaju dva proizvoda uz regenaraciju katalizatora. - Tetrabromferatni jon Cikloheksadienil katjon Brombenzen

Aromatično hlorovanje i jodovanje • hlor i jod (ali ne i fluor, jer je jako reaktivan, reakcija je veoma egzotermna) mogu dati supstitucione proizvode na benzenu • hlorovanje zahteva Fe. Cl 3, mehanizam je identičan bromovanju • Reakcija sa jodom je endotermna i pri normalnim uslovima nije moguća. Jod se mora oksidacijom prevesti u aktivniji I+ (pomoću Cu 2+ ili peroksidom) : baza

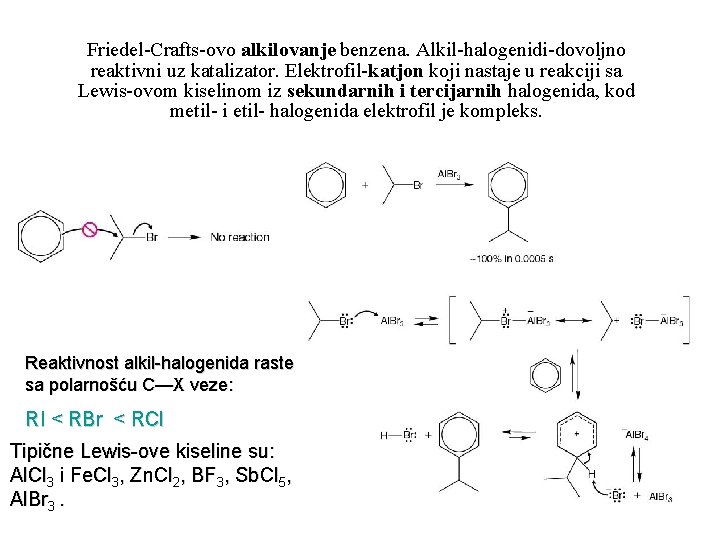
Friedel-Crafts-ovo alkilovanje benzena. Alkil-halogenidi-dovoljno reaktivni uz katalizator. Elektrofil-katjon koji nastaje u reakciji sa Lewis-ovom kiselinom iz sekundarnih i tercijarnih halogenida, kod metil- i etil- halogenida elektrofil je kompleks. Reaktivnost alkil-halogenida raste sa polarnošću C—X veze: RI < RBr < RCl Tipične Lewis-ove kiseline su: Al. Cl 3 i Fe. Cl 3, Zn. Cl 2, BF 3, Sb. Cl 5, Al. Br 3. 79
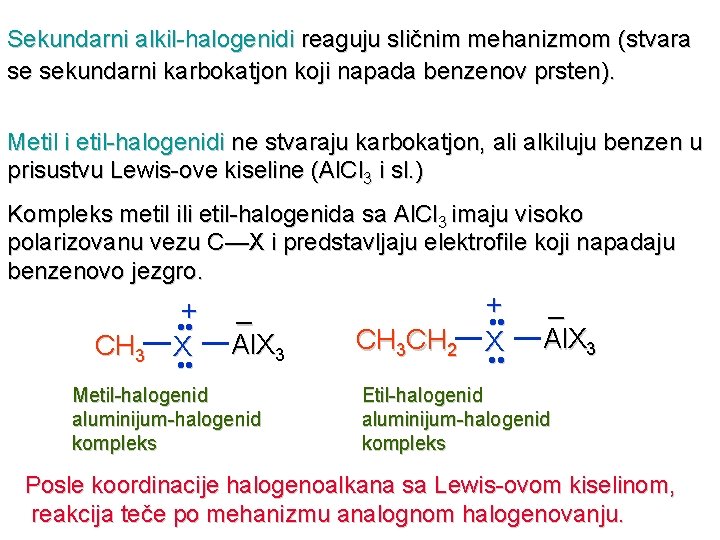
Sekundarni alkil-halogenidi reaguju sličnim mehanizmom (stvara se sekundarni karbokatjon koji napada benzenov prsten). Metil i etil-halogenidi ne stvaraju karbokatjon, ali alkiluju benzen u prisustvu Lewis-ove kiseline (Al. Cl 3 i sl. ) Kompleks metil ili etil-halogenida sa Al. Cl 3 imaju visoko polarizovanu vezu C—X i predstavljaju elektrofile koji napadaju benzenovo jezgro. CH 3 + • • X • • – Al. X 3 Metil-halogenid aluminijum-halogenid kompleks CH 3 CH 2 + • • X • • – Al. X 3 Etil-halogenid aluminijum-halogenid kompleks Posle koordinacije halogenoalkana sa Lewis-ovom kiselinom, reakcija teče po mehanizmu analognom halogenovanju.
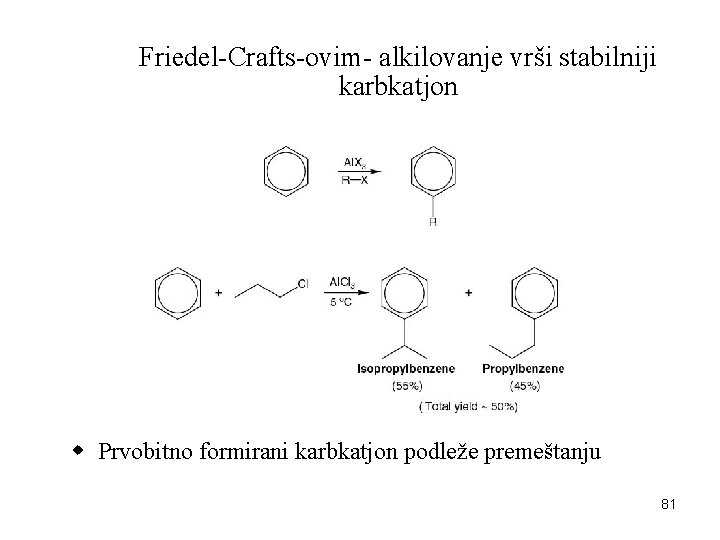
Friedel-Crafts-ovim- alkilovanje vrši stabilniji karbkatjon w Prvobitno formirani karbkatjon podleže premeštanju 81
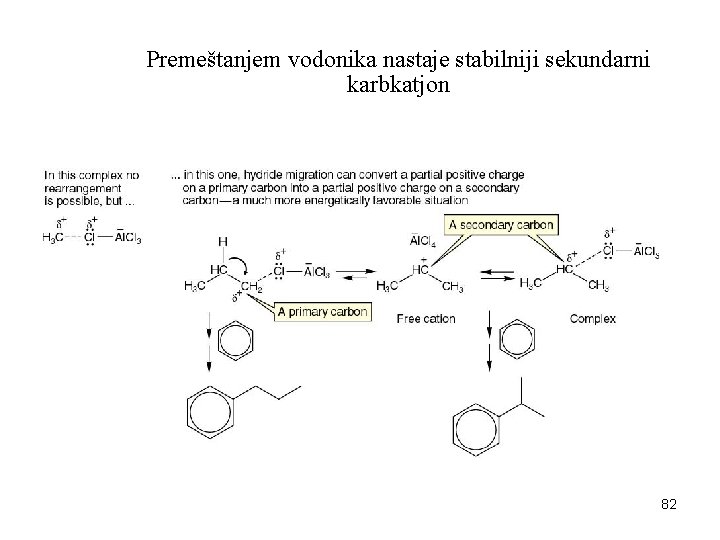
Premeštanjem vodonika nastaje stabilniji sekundarni karbkatjon 82

Iz primarnog karbkatjona premeštanjem vodonika nastaje t -karbkatjon 83
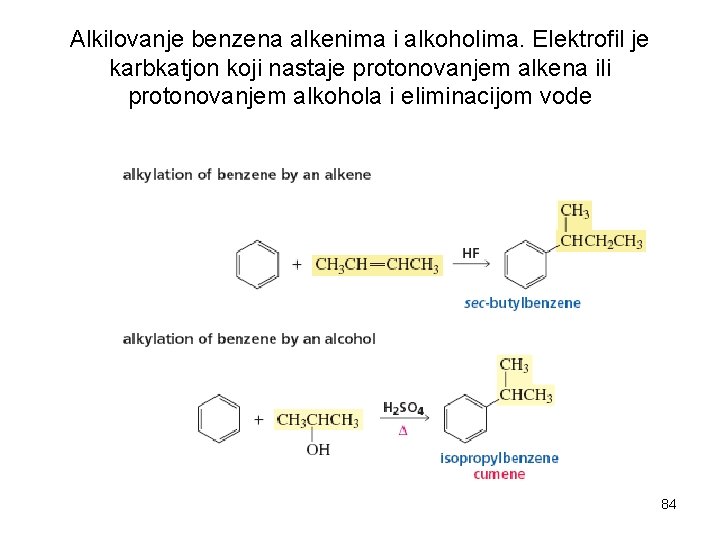
Alkilovanje benzena alkenima i alkoholima. Elektrofil je karbkatjon koji nastaje protonovanjem alkena ili protonovanjem alkohola i eliminacijom vode 84
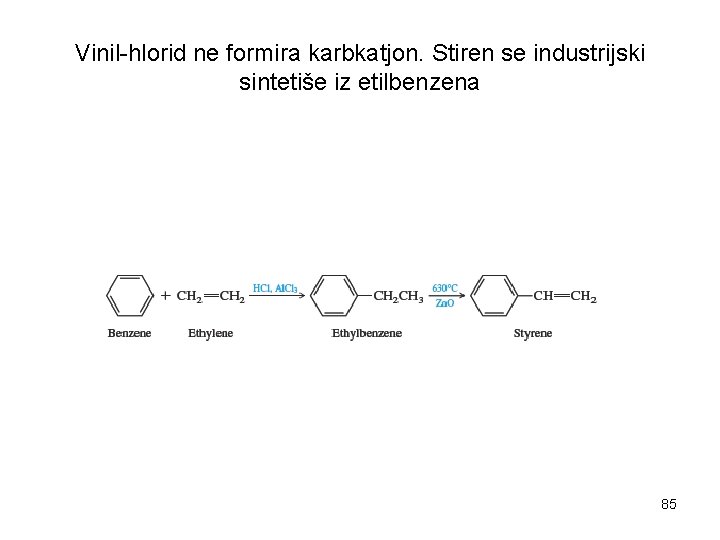
Vinil-hlorid ne formira karbkatjon. Stiren se industrijski sintetiše iz etilbenzena 85

Ograničenja Friedel-Crafts-ovog alkilovanja – postoji mogućnost polisupstitucije; – moguće je preuređivanje alkil-grupe; – ne mogu se upotrebiti aril-halogenidi zbog manje reaktivnosti; – aromatični prstenovi sa smanjenom reaktivnošću (zbog prisustva dezaktivirajućeg supstituenta) ne podležu reakciji i – aromatični prstenovi koji imaju –NH 2, -NHR ili –NR 2 grupu ne podležu Friedel-Crafts-ovom alkilovanju jer grade kompleks sa Lewis-ovim kiselinama sa pozitivnom šaržom na azotu što dezaktivira prsten.
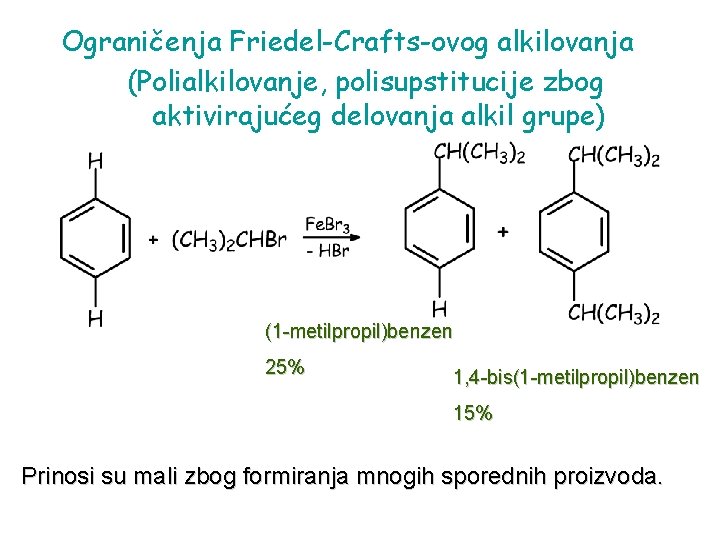
Ograničenja Friedel-Crafts-ovog alkilovanja (Polialkilovanje, polisupstitucije zbog aktivirajućeg delovanja alkil grupe) (1 -metilpropil)benzen 25% 1, 4 -bis(1 -metilpropil)benzen 15% Prinosi su mali zbog formiranja mnogih sporednih proizvoda.

88


Friedel-Crafts-ovo acilovanje (alkanoilovanje). Acilhalogenid ili anhidrid uz katalizator 90
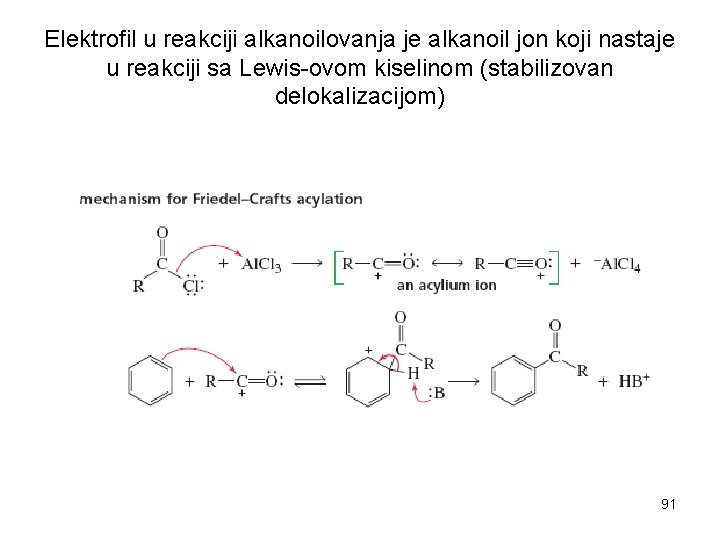
Elektrofil u reakciji alkanoilovanja je alkanoil jon koji nastaje u reakciji sa Lewis-ovom kiselinom (stabilizovan delokalizacijom) 91

Acil-katjon nastaje u reakciji alkanoil-halogenida sa auminijum-hloridom. Propanoil-hlorid Propanoil-katjon Lewis-ova kiselina-Levis-ova baza kompleks Tetrahloraluminijum jon Najveći deo pozitivne šarže je skoncentrisano na karbonilnom ugljeniku. Acilijum jon ne podleže premeštanju.

Za reakciju acilovanja potrebno je dodati Lewis-ovu kiselinu u višku. Gradi kompleks sa nastalim ketonom 93
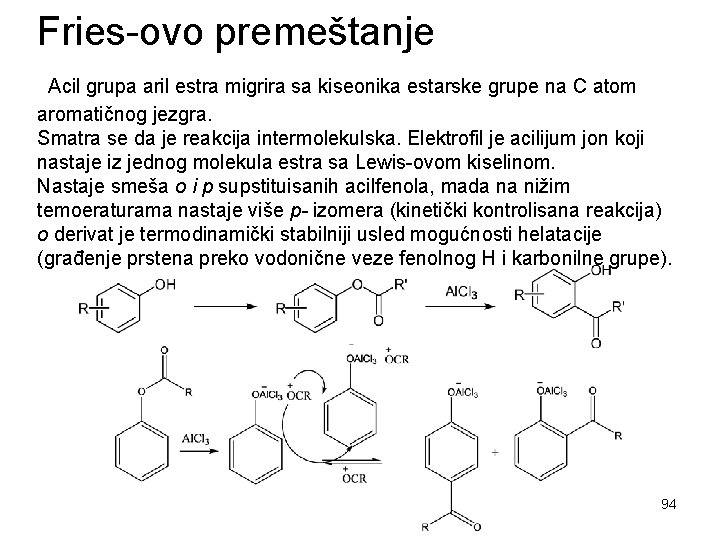
Fries-ovo premeštanje Acil grupa aril estra migrira sa kiseonika estarske grupe na C atom aromatičnog jezgra. Smatra se da je reakcija intermolekulska. Elektrofil je acilijum jon koji nastaje iz jednog molekula estra sa Lewis-ovom kiselinom. Nastaje smeša o i p supstituisanih acilfenola, mada na nižim temoeraturama nastaje više p- izomera (kinetički kontrolisana reakcija) o derivat je termodinamički stabilniji usled mogućnosti helatacije (građenje prstena preko vodonične veze fenolnog H i karbonilne grupe). 94

Karakteristike Friedel-Crafts-ovog acilovanja ØAcil grupa dezaktivira jezgro (privlači elektrone), pa se reakcija zaustavlja na monosupstituciji ØPri acilovanju ne dolazi do preuređivanja ØOd dobijenih ketona redukcijom se mogu dobiti aromatični alkoholi ili čak ugljovodonici
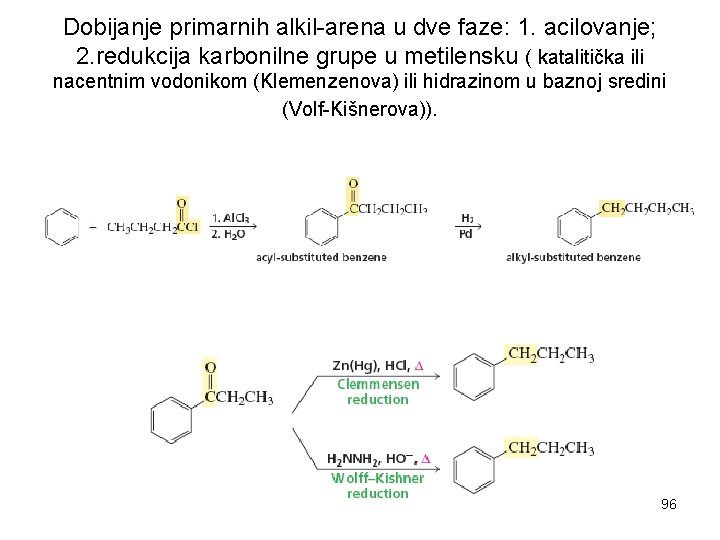
Dobijanje primarnih alkil-arena u dve faze: 1. acilovanje; 2. redukcija karbonilne grupe u metilensku ( katalitička ili nacentnim vodonikom (Klemenzenova) ili hidrazinom u baznoj sredini (Volf-Kišnerova)). 96
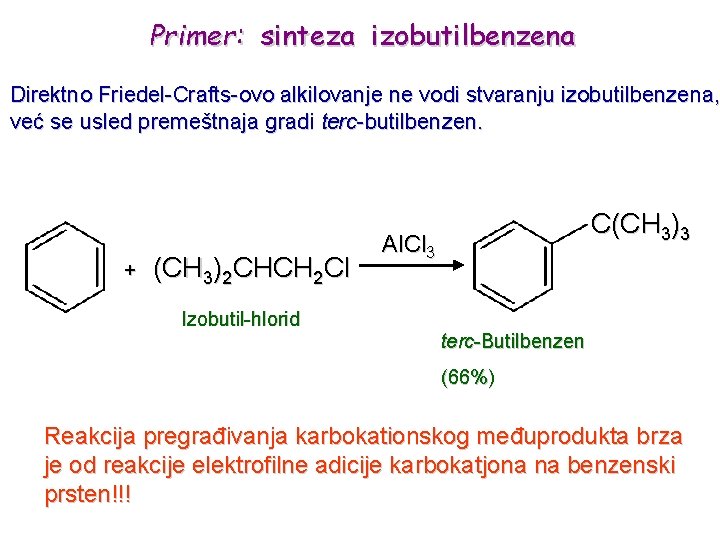
Primer: sinteza izobutilbenzena Direktno Friedel-Crafts-ovo alkilovanje ne vodi stvaranju izobutilbenzena, već se usled premeštnaja gradi terc-butilbenzen. + (CH 3)2 CHCH 2 Cl Izobutil-hlorid C(CH 3)3 Al. Cl 3 terc-Butilbenzen (66%) Reakcija pregrađivanja karbokationskog međuprodukta brza je od reakcije elektrofilne adicije karbokatjona na benzenski prsten!!!
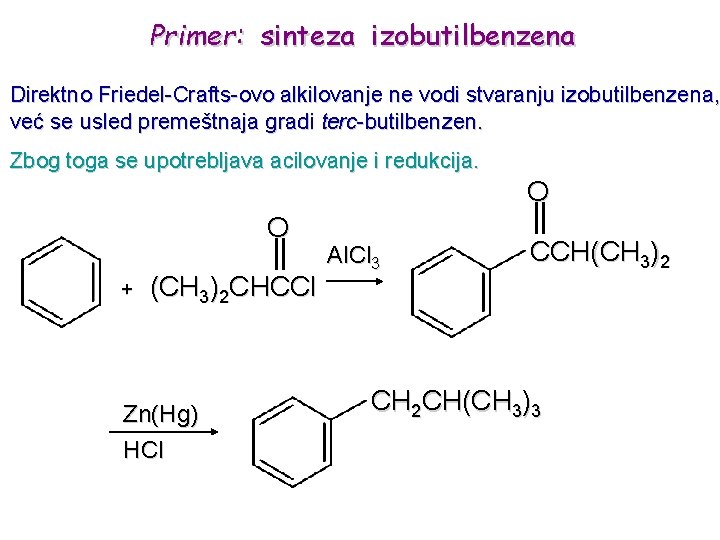
Primer: sinteza izobutilbenzena Direktno Friedel-Crafts-ovo alkilovanje ne vodi stvaranju izobutilbenzena, već se usled premeštnaja gradi terc-butilbenzen. Zbog toga se upotrebljava acilovanje i redukcija. O O + (CH 3)2 CHCCl Zn(Hg) HCl Al. Cl 3 CCH(CH 3)2 CH 2 CH(CH 3)3
- Slides: 98