Metoda valentnih struktura VB Kekulov opis benzena Dvije
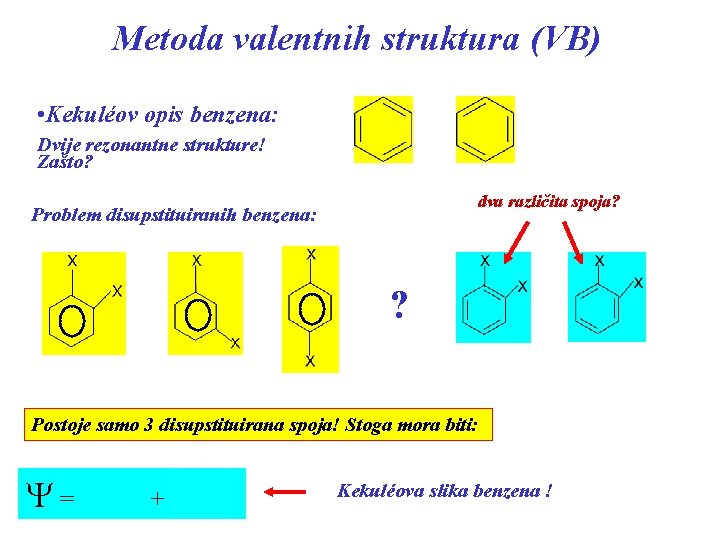
Metoda valentnih struktura (VB) • Kekuléov opis benzena: Dvije rezonantne strukture! Zašto? dva različita spoja? Problem disupstituiranih benzena: ? Postoje samo 3 disupstituirana spoja! Stoga mora biti: Y= + Kekuléova slika benzena !

Metoda valentnih struktura (VB) Y= Kekuléova slika benzena ! + Ostali opisi benzena Y= Y= + + Dewarov prikaz Clausov prikaz, etc. Gornji prikazi su bili odbačeni radi postojanja dugih veza kroz prostor!

Metoda valentine struktura Heitler i London 1 r 2 Primjer molekule vodika: (jezgre atoma (protoni) A i B i elektroni 1 i 2!) r. A 1 Hamiltonijan sustava: A r. A 2 r. B 1 r. B 2 R B H 1 H 2 V (ovisi o elektronu 1) (ovisi o elektronu 2) (ovisi o oba elektrona) Za R je V 0 ! Separacija varijabli!
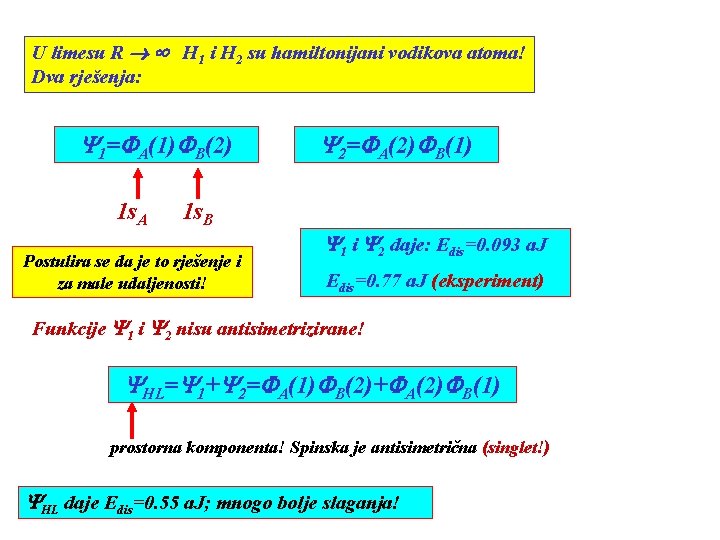
U limesu R H 1 i H 2 su hamiltonijani vodikova atoma! Dva rješenja: Y 1=FA(1)FB(2) 1 s. A Y 2=FA(2)FB(1) 1 s. B Postulira se da je to rješenje i za male udaljenosti! Y 1 i Y 2 daje: Edis=0. 093 a. J Edis=0. 77 a. J (eksperiment) Funkcije Y 1 i Y 2 nisu antisimetrizirane! YHL=Y 1+Y 2=FA(1)FB(2)+FA(2)FB(1) prostorna komponenta! Spinska je antisimetrična (singlet!) YHL daje Edis=0. 55 a. J; mnogo bolje slaganja!

VB funkcije prostorna VB funkcija spinska komponenta (singlet) Pokusna valna funkcija (nenormirana prostorna - vezna i nevezna): Coulombski integral; Q > 0 destabilizirajući efekt! Integral izmjene; J < 0 daje 90% kemijske veze (energije) Prekrivanje orbitala FA i FB Ukupno prekrivanje
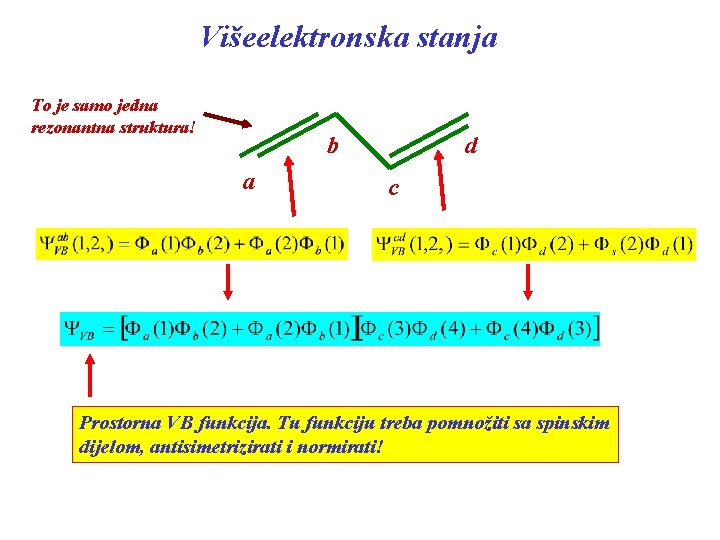
Višeelektronska stanja To je samo jedna rezonantna struktura! b a d c Prostorna VB funkcija. Tu funkciju treba pomnožiti sa spinskim dijelom, antisimetrizirati i normirati!
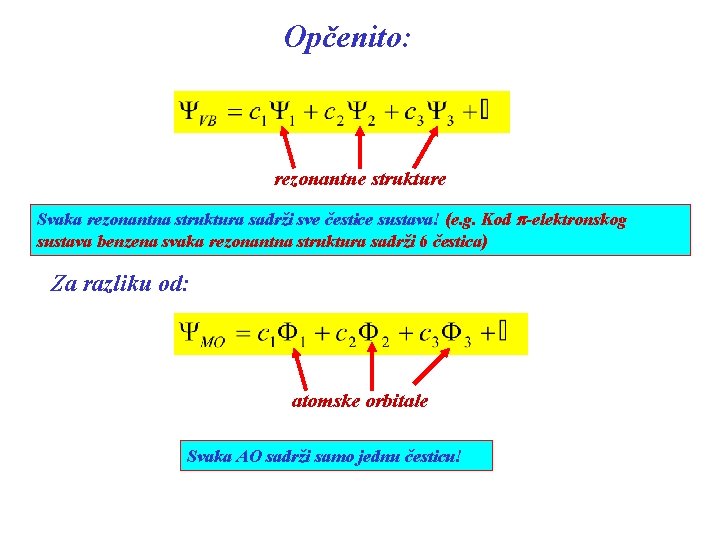
Opčenito: rezonantne strukture Svaka rezonantna struktura sadrži sve čestice sustava! (e. g. Kod p-elektronskog sustava benzena svaka rezonantna struktura sadrži 6 čestica) Za razliku od: atomske orbitale Svaka AO sadrži samo jednu česticu!
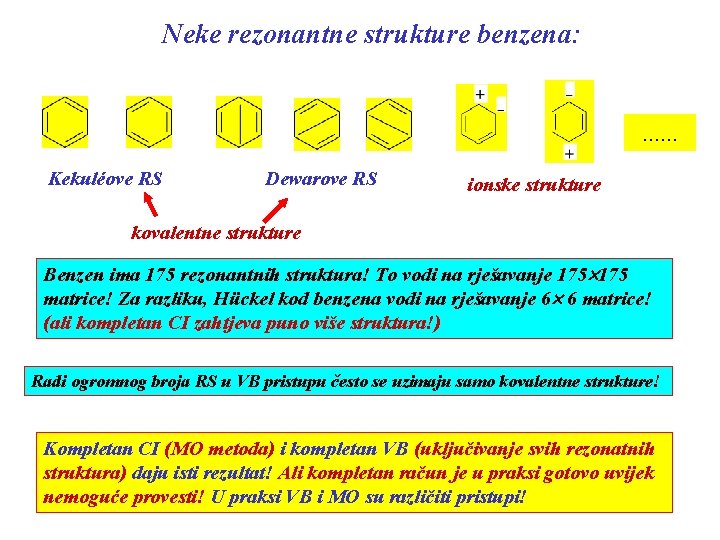
Neke rezonantne strukture benzena: . . . Kekuléove RS Dewarove RS ionske strukture kovalentne strukture Benzen ima 175 rezonantnih struktura! To vodi na rješavanje 175 matrice! Za razliku, Hückel kod benzena vodi na rješavanje 6 6 matrice! (ali kompletan CI zahtjeva puno više struktura!) Radi ogromnog broja RS u VB pristupu često se uzimaju samo kovalentne strukture! Kompletan CI (MO metoda) i kompletan VB (uključivanje svih rezonatnih struktura) daju isti rezultat! Ali kompletan račun je u praksi gotovo uvijek nemoguće provesti! U praksi VB i MO su različiti pristupi!
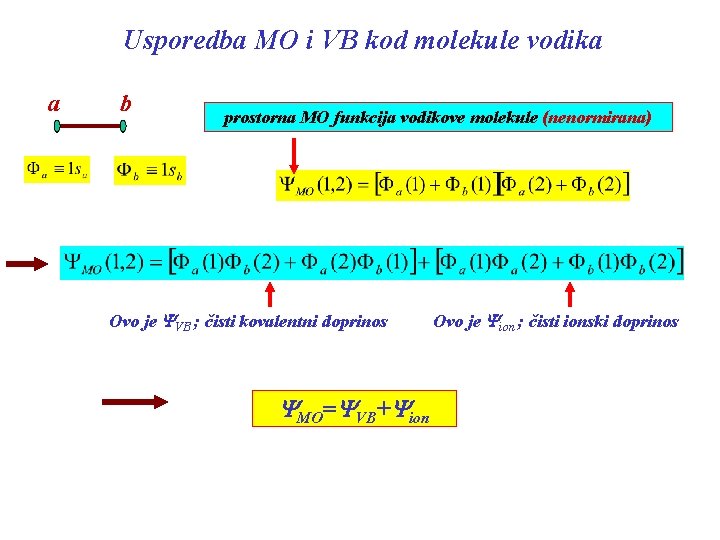
Usporedba MO i VB kod molekule vodika a b prostorna MO funkcija vodikove molekule (nenormirana) Ovo je YVB ; čisti kovalentni doprinos YMO=YVB+Yion Ovo je Yion ; čisti ionski doprinos
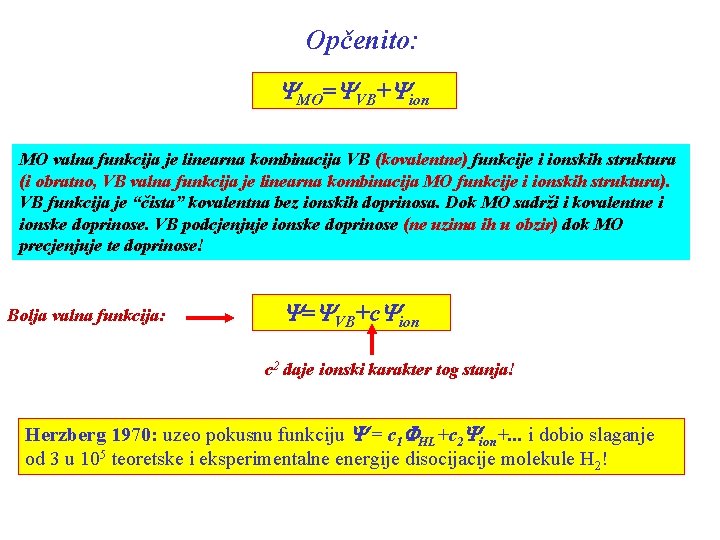
Opčenito: YMO=YVB+Yion MO valna funkcija je linearna kombinacija VB (kovalentne) funkcije i ionskih struktura (i obratno, VB valna funkcija je linearna kombinacija MO funkcije i ionskih struktura). VB funkcija je “čista” kovalentna bez ionskih doprinosa. Dok MO sadrži i kovalentne i ionske doprinose. VB podcjenjuje ionske doprinose (ne uzima ih u obzir) dok MO precjenjuje te doprinose! Bolja valna funkcija: Y=YVB+c. Yion c 2 daje ionski karakter tog stanja! Herzberg 1970: uzeo pokusnu funkciju Y = c 1 FHL+c 2 Yion+. . . i dobio slaganje od 3 u 105 teoretske i eksperimentalne energije disocijacije molekule H 2!

Pitanja VB metoda • • Kako je Kekulé predstavio molekulu benzena? Zašto? Koja su bila druga predložena rješenja za tu molekulu? Zašto nisu bila prihvaćena? • Objasnite osnovnu ideju VB pristupa na primjeru H 2 molekule! • Kako izgleda potpuna normirana dvoelektronska VB valna funkcija? • Koje su energije vezne i nevezne dvoelektronske VB funkcije? • Koji doprinos stabilizira VB vezu? • Kako izgleda višeelektronska VB valna funkcija (jedna rezonantna struktura)? • Kako se u VB slici prikazuje osnovno pelektronsko stanje molekule benzena? Molekule vodika? Koje strukture doprinose tome stanju? • Usporedite VB i MO pristup! • Što bi dobili kada bi u MO CI pristupu uzeli u obzir sve moguće konfiguracije i u VB pristupu uzeli u obzir sve moguće kovalentne i sve moguće ionske strukture?
- Slides: 11