Uvod u laboratorijski rad NOMENKLATURA NEORGANSKIH JEDINJENJA Profesor

Uvod u laboratorijski rad NOMENKLATURA NEORGANSKIH JEDINJENJA Profesor dr. Dragica Minić

IUPAC organizacija u The International Union of Pure and Applied Chemistry (IUPAC) je međunarodna ne-vladina organizacija ustanovljena 1919 radi podrške razvoja moderne hemije. u Nacionalna hemijska društva su članovi IUPAC-a. u IUPAC je priznat je autoritet za razvijanje standarda za imenovanje hemijskih elemenata i njihovih jedinjenja preko Međudevizionog komiteta za nomenklaturu i simbole (IUPAC nomenklatura). u Član je Internacionalnog naučnog konzilijuma (International Council for Science, ICSU).

Istorijski pregled u 1782. Francuski hemičar Louis-Bernard Guyton de Morveau [Guyton de Morveau L. B. , J. Phys. 19(1782) 310] Publikovao je svoje preporuke u obliku “konstantnog metoda davanja naziva”. u 1787. Sistem su preradili Berthollet, de Fourcoy and Lavoisier: [Guyton de Morveau, L. B. Lavoisier A. L. , Berthollet C. L. , de Fourcroy A. F. u Methode de Nomenclature Chimique, Paris (1787)] u 1801. Promocija sistema data je u priručniku koji je dugo posle autorovog pogubljenja na giljotini 1794. bio u upotrebi: [Lavoisier A. L. , Traite Elementaire de Chemie (3. ed. Paris: Deterville (1801)]

Prva strana Lavoazjeve “Chymical Nomenclature”

u 1811 Berzelius je sistem adapatirao za primenu na nemačkom govornom području: [Berzelius J. J. , J. Phys. 73 (1811) 248] Preporuke Guyton-a su se odnosile samo na nomenklaturu neorganskih jedinjenja, što nikako nije moglo da zadovolji opšti razvoj organske hemije koji je doveo do boljeg razumevanja strukture organskih jedinjenja sredinom devetnaestog veka i nametnuo potrebu razvoja nomenklature organskih jedinjenja. u 1892 U Ženevi održana je međunarodna konferencija nacionalnih hemijskih društava gde su prihvaćani predlozi za uvođenje standardizacije [Bull. Soc. Chim. (Paris) 3(7), xiii. (1982)]

Učesnici Ženevske konferencije 1892

u 1913. osnovan je Savet međunarodne zajednice hemijskih društava [Council of the International Associacion of Chemical Societies] čiji je rad prekinuo I. svetski rat u 1919. osnovana je Međunarodna zajednica za čistu i primenjenu hemiju [International Union of Pure and Applied Chemistry, IUPAC] u 1921 IUPAC formira komisije za sledeće nomenklature, koje postoje i danas: organsku neorgansku biohemijsku Pored upustva za nomenklaturu IUPAC daje standarde i za internacionalno pisanje: npr. aluminum, sulphur, itd

IUPAC nomenklatura neorganskih jedinjenja u IUPAC nomenklatura neorganskih jedinjenja je sistematsko imenovanje neorganskih hemijskih jedinjenja kako je preporučeno od strane International Union of Pure and Applied Chemistry (IUPAC) u Prema ovoj nomenklaturi, svako jedinjenje treba da ime iz koga nedvosmisleno može da bude određena formula, odnosno svako ime označava samo jednu supstancu. u Ime treba da sadrži informacije kako o sastavu tako i o strukturi jedinjenja. u Pravila za imenovanje organskih i neorganskih jedinjenja sadržana su u sledećim dokumentima:

u u u u 1. Plava knjiga –organska jedinjenja [Nomenclature of Organic Chemistry, Oxford: Pergamon Press 1979, A Guide to IUPAC, Nomenclature of Organic Compounds, Recommendations 1993, Oxford: Blackwell Scientific Publications, 1993] 2. Crvena knjiga –neorganska jedinjenja [Nomenclature of Inorganic Compounds, Recommendations 1990, Oxford: Blackwell Scientific Publications, 1990] 3. Zelena knjiga [Quantities, Units Oxford: Blackwell –simboli i fizičke veličine and Symbols in Physical Chemistry (2. ed. ) Scientific Publications, 1993] 4. Zlatna knjiga –tehnički termini u hemiji [Compendium of Chemical Terminology IUPAC Recommendations (2. ed. ), Oxford: Blackwell Scientific Publications, 1997]

u 5. Slična literatura postoji za biohemiju, analitičku hemiju i hemiju mikromolekula: u [Biochemical Nomenclature and related Documents, London: Portland Press, 1992] u [Compendium of Analytical Nomenclature, definite Rules 1997 (3. ed. ) Oxford: Blackwell Scientific Publications, 1998] u [Compendium of macromolecular Nomenclature, Oxford: Blackwell Scientific Publications, 1991]

u Sistematsko određivanje imena mora da odražava strukturu i sastav: 1. Jednoatomski anjoni imaju sufiks id, H- = hidrid 2. Ime jedinjanja koja sadrže katjon i anjon sadrže prvo ime katjona a zatim ime anjona, Na. Cl =natrijum-hlorid 3. Naelektrisanje katjona koji imaju više pozitivnih naelektrisanja se stavlja u zagradu bakar(I)=kupro i bakar(II)=kupri.

4. Poliatomski anjoni koji sadrže više atoma kiseonika sadrže sufiks it za niži i at za viši sadržaj kiseonika, NO 2 -=nitrit i NO 22 -=nitrat. Za 4 atoma kiseonika koriste se još i prefiksi hipo i per, Cl. O-= hipohlorit 5. i Cl. O 4 -= perhlorat. Prefiks bi- se koristi za označavanje prisustva jednog vodoničnog jona, Na. HCO 3= natrijum-bikarbonat ili sada Na. HCO 3 =natrijum vodonik karbonat

Periodni sistem elemenata Elementi u periodnoj tablici se dele u četiri kategorije: metali (leva strana), prelazni elementi (u sredini), nemetali (desna strana), lantanidi i aktinidi

u Broj atoma svakog elementa u molekulu (ili formulskoj jedinki) označava se grčkim prefiksom: Prefiks u Broj atoma mono-* 1 di 2 tri 3 tetra 4 penta 5 heksa 6 hepta 7 okta 8 nona 9 deka 10 * Prefiks mono- se retko koristi; kada nema prefiksa ispred imena elementa pretpostavlja se da je u molekulu ili formulskoj jedinki prisutan jedan atom tog elementa.

Binarna jedinjenja koja sadrže dva nemetala u Binarna jedinjenja su ona koja sadrže dva hemijska elementa, npr dva nemetala na kraju imena drugog po redu elementa binarnog jedinjenja stavlja se nastavak –id BCl 3 =bor-trihlorid, SO 2 =sumpor-dioksid, N 2 O 4 =diazot-tetroksid, CO =ugljen-monoksid, PCl 5 = fosfor-pentahlorid.

Binarna jedinjenja koja sadrže metal i nemetal u Nomenklatura ovih jedinjenja zavisi od toga da li metal koji je prisutan u jedinjenju ima konstantno naelektrisanje ili promenljivo naelektrisanje. u Katjoni sa konstantnim naelektrisanjem su sledeći: Li+, Na+, K+, Rb+, Cs+, Ag+, Mg 2+, Ca 2+, Sr 2+, Ba 2+, Zn 2+, Cd 2+, Al 3+ Svi drugi metali imaju promenljivo naelektrisanje.

u Ime metala ide kao prvo, a zatim sledi ime nemetala sa nastavkom -id, u Primeri binarnih jedinjenja koja sadrže metal i nemetal: KCl = kalijum-hlorid Mg. O = magnezijum-oksid Na 2 S = natrijum-sulfid Ca. H 2 = kalcijum-hidrid Li. Br = litijum-bromid

u Kod binarnih jedinjenja nemetala i metala promenljivog naelektrisanja mora se naznačiti naelektrisanje datog metalnog jona na jedan od dva sledeća načina: u I. Posle naziva metala u zagradu se stavlja rimski broj koji predstavlja naelektrisanje metalnog jona: Cu. Cl 2 = bakar (II) hlorid, Fe. O= gvoždje (II) oksid Fe 2 O 3= gvoždje (III) oksid u II. Na ime metala dodaje se nastavak (sufiks) –o, za jon manjeg naelektrisanja, ili nastavak –i, za jon većeg naelektrisanja: Cu 1+ = kupro jon Fe 2+= fero jon Pb 2+ = plumbo jon Hg 2 2+ = merkuro jon Sn 2+ = stano jon Cu 2+ = kupri jon Fe 3+ = feri jon Pb 4+ = plumbi jon Hg 2+ = merkuri jon Sn 4+ = stani jon

Ternarna i viša jedinjenja u Ternarna jedinjenja sastavljena su od tri tipa atoma (tj. uključuju tri hemijska elementa), metalni jon, višeatomski jon ili oksihalogen jon. Negativni višeatomski joni sa imenom koje sadrži sufiks –at imaju jedan kiseonikov atom više od onih sa sufiksom –it: NH 4+ Amonijum jon CO 32 - Karbonatni jon HCO 3 - Bikarbonatni jon CN- Cijanidni jon C 2 O 42 - Oksalatni jon CH 3 COO- Acetatni jon

Cl. O- Hipohloritni jon Cl. O 2 - Hloritni jon Cl. O 3 - Hloratni jon Cl. O 4 - Perhloratni jon Cr. O 42 - Hromatni jon Cr 2 O 72 - Dihromatni jon OH- Hidroksidni jon NO 2 - Nitritni jon NO 3 - Nitratni jon Mn. O 4 - Permanganatni jon PO 43 - Fosfatni jon HPO 42 - Vodonik fosfatni jon

u Za metale sa promenljivim naelektrisanjem koriste se sufiksi -o ili –i. Formula jedinjenja Na. NO 2 Ime jedinjenja natrijum-nitrit Na. NO 3 natrijum-nitrat Na. HSO 3 natrijum-vodonik sulfit (natrijum-bisulfit) Cu 3(PO 4)2 bakar (II) fosfat (kupri-fosfat) Cu. CN bakar (I) cijanid (kupro-cijanid) Ba(CH 3 COO)2 barijum acetat Ag. Cl. O 4 srebro-perhlorat Fe 2(Cr. O 4)3 gvoždje (III) hromat (feri-hromat)

Kiseline u Kiselina je jedinjenje koje sadrži vodonik i koje daje vodonične (H+) jone kada se rastvori u vodi. u Ovo je Arrhenius-ova definicija, koja je ograničena na rastvore koji sadrže vodu kao rastvarač. u Preciznije, prema Bronsted-Lowry- konceptu, kiselina je supstanca koja je donor (davalac) vodoničnih jona , tj. protona nekoj drugoj supstanciji. Poslednja definicija važi za bilo koji rastvarač koji se koristi za pripremu rastvora kiseline.

u Formule i imena nekih kiselina Formula Naziv HF Fluorovodonična kiselina HCl Hlorovodonična kiselina HBr Bromovodonična kiselina HNO 3 Azotna kiselina CH 3 COOH Sirćetna kiselina H 2 SO 3 Sumporasta kiselina H 2 SO 4 Sumporna kiselina
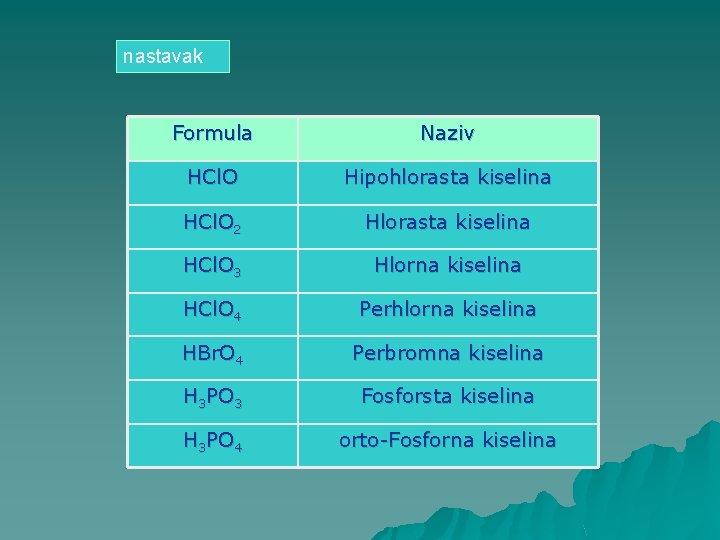
nastavak Formula Naziv HCl. O Hipohlorasta kiselina HCl. O 2 Hlorasta kiselina HCl. O 3 Hlorna kiselina HCl. O 4 Perhlorna kiselina HBr. O 4 Perbromna kiselina H 3 PO 3 Fosforsta kiselina H 3 PO 4 orto-Fosforna kiselina

Baze Baza je, prema Arrhenius-ovom konceptu, supstanca koja daje hidroksidne jone (OH-) kada se rastvori u vodi. Prema Bronsted-Lowry konceptu, baza je supstanca koja može da primi vodonikov jon (proton) od neke druge supstancije. Kažemo da su baze akceptori protona. u Imena baza završavaju se sa –id: Li. OH litijum-hidroksid Ba(OH)2 barijum-hidroksid.

Soli su jedinjenja koja nastaju kada se jedan ili više vodonikovih jona u kiselini zameni drugim katjonom ili kada se jedan ili više hidroksidnih jona u bazi zameni drugim anjonom. u Osnovni tipovi soli su: binarna jedinjenja sastavljena od metalnog katjona i nemetalnog anjona Na. Cl natrijum-hlorid u ternarna i viša jedinjenja koja su sačinjena od metalnog katjona ili amonijumovog jona i negativnog višeatomskog jona: Na. NO 3 natrijum-nitrat (NH 4)2 SO 4 amonijum-sulfat

Kristalohidrati u Poseban tip soli (kristalnih jedinjenja) koje sadrže definisanu količinu hemijski vezane vode, i koje se pri zagrevanju razlažu otpuštajući vodu, nose naziv kristalohidrati ili hidrati. Mg. SO 4 · 7 H 2 O magnezijum sulfat heptahidrat. Grčki prefiksi dati pokazuju broj molekula vode: Mg. SO 4. 2 H 2 O magnezijum sulfat dihidrat, Mg. SO 4. 3 H 2 O magnezijum sulfat trihidrat.

Revizija IUPAC-ove nomenklature za neorganska jedinjenja 2005. Izvršena je revizija nomenklature Prema ovoj reviziji nema više apsolutno ispravnog imena za jedno jedinjenje. - Svako ime koje nedvosmisleno označava jedinjenje je korektno ime (voda, karbonil, cijano) Postoje dva načina opisa jedinjenja prema: - sastavu i prema substituentima

Prema sastavu: Molekul se opisuje preko jezgra kao kod kompleksa. 1. Jezgro(a) molekula je atom najniže elektronegativnosti. Ovaj elemenat definiše osnovno ime jedinjenja: ako je jedinjenje negativno naelektrisano sadrži prefiks id ako nije prisutan drugi atom i at u drugom slučaju 2. Okolni atomi i grupe se opisuju kao ligandi sa sufiksom o, identične grupe sadrže prefikse tri-, tetra- ili bis 3. Zatim se navode oznake za naelektrisanje, funkciju radikala, kristalizaciona voda, premoštavajući ili koordinirani ligandi.
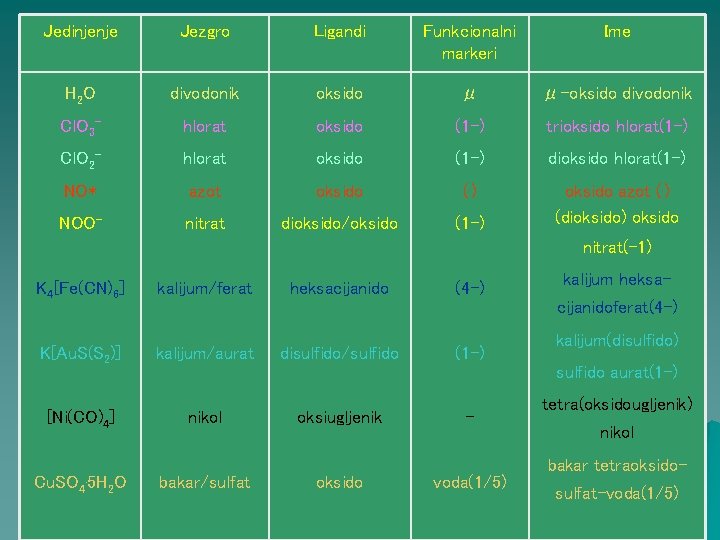
Jedinjenje Jezgro Ligandi Funkcionalni markeri Ime H 2 O divodonik oksido μ μ-oksido divodonik Cl. O 3 - hlorat oksido (1 -) trioksido hlorat(1 -) Cl. O 2 - hlorat oksido (1 -) dioksido hlorat(1 -) NO* azot oksido (. ) NOO- nitrat dioksido/oksido (1 -) oksido azot (. ) (dioksido) oksido nitrat(-1) K 4[Fe(CN)6] kalijum/ferat K[Au. S(S 2)] kalijum/aurat [Ni(CO)4] nikol Cu. SO 4 . 5 H 2 O heksacijanido (4 -) kalijum heksacijanidoferat(4 -) disulfido/sulfido (1 -) kalijum(disulfido) sulfido aurat(1 -) bakar/sulfat oksiugljenik oksido - voda(1/5) tetra(oksidougljenik) nikol bakar tetraoksidosulfat-voda(1/5)

u Prema supstituentima Uopštava se nomenklatura organskih jedinjenja prateći osnovna pravila: 1. Svim elementima se dodaje nastavak an na bazno ime a nezasićene veze se ispunjavaju atomima vodonika: oksidan atom kiseonika vezan za vodonik (H 2 O voda) dioksidan lanac dva atoma kiseonika vezan sa atomima vodonika (H 2 O 2 vodonik peroksid)

BH 3 Al. H 3 Ga. H 3 In. H 3 Tl. H 3 boran aluman galan indigan talan CH 4 Si. H 4 Ge. H 4 Sn. H 4 Pb. H 4 metan silan german stanan plumban NH 3 PH 3 As. H 3 Sb. H 3 Bi. H 3 azan fosfan arsan stiban bizmutan H 2 O H 2 Se H 2 Te H 2 Po oksidan sulfan selan telan polan HF HBr HAt fluoran broman astatan HCl HI hloran jodan
- Slides: 32