Aldehidi i ketoni Struktura i nomenklatura Opta formula














































- Slides: 57

Aldehidi i ketoni Ü Struktura i nomenklatura Opšta formula aldehida: RCHO Opšta formula ketona RCOR'. Grupe R i R' mogu biti alifatične ili aromatične. Obe grupe jedinjenja sadrže karbonilnu grupu, >C=O, pa se često nazivaju jednim imenom karbonilna jedinjenja

Ü Zbog sličnosti u strukturi aldehidi i ketoni pokazuju i sličnost kod većine svojih karakteristika Ü Međutim, činjenica da aldehidi imaju jedan H-atom vezan za karbonilnu grupu, dok su kod ketona za karbonilnu grupu vezana dva C-atoma, ima za posledicu: (1) lako oksidovanje aldehida u odnosu na ketone, kod kojih je oksidacija vrlo otežana, (2) veću reaktivnost aldehida u odnosu na ketone prema reakciji nukleofilne adicije, koja je karakteristična za karbonilna jedinjenja.

Ü Struktura karbonilne grupe Veza >C=O je vrlo polarizovana Dipolni moment aldehida i ketona je stoga prilično veliki i kreće se od 2, 3 -2, 8 D Ova činjenica u velikoj meri utiče na fizičke i hemijske osobine aldehida i ketona

Nomenklatura Ü Aldehidi Trivijalna imena izvode se iz trivijalnih imena odgovarajućih karboksilnih kiselina, tj. kiselina sa istim brojem C-atoma. Korenu latinskog imena kiseline dodaje se reč aldehid. – Primer: Formaldehid i acetaldehid - odgovarajuće kiseline su "mravlja" (acidum formicum) i sirćetna (acidum aceticum)

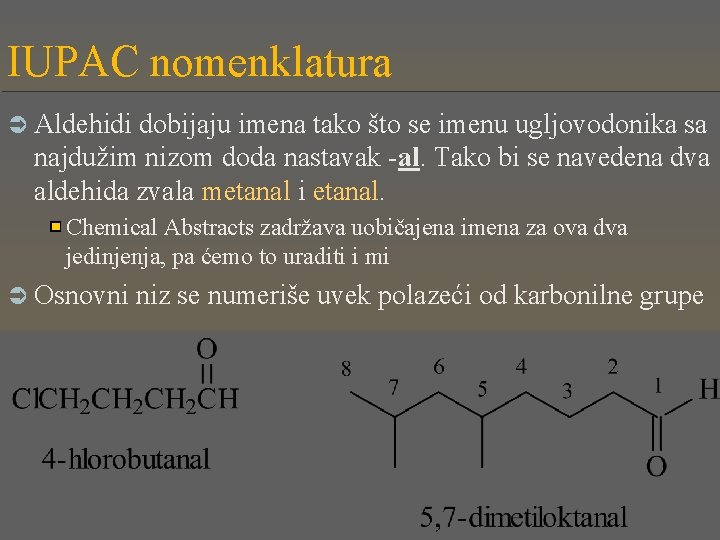
IUPAC nomenklatura Ü Aldehidi dobijaju imena tako što se imenu ugljovodonika sa najdužim nizom doda nastavak -al. Tako bi se navedena dva aldehida zvala metanal i etanal. Chemical Abstracts zadržava uobičajena imena za ova dva jedinjenja, pa ćemo to uraditi i mi Ü Osnovni niz se numeriše uvek polazeći od karbonilne grupe

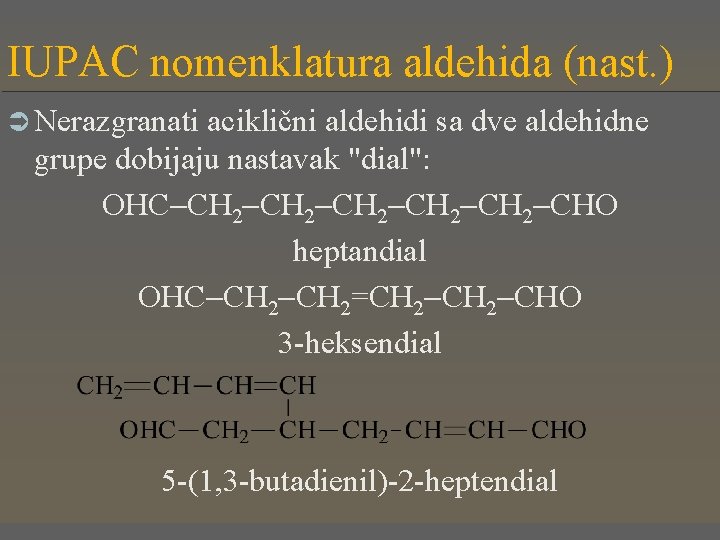
IUPAC nomenklatura aldehida (nast. ) Ü Nerazgranati aciklični aldehidi sa dve aldehidne grupe dobijaju nastavak "dial": OHC CH 2 CH 2 CHO heptandial OHC CH 2=CH 2 CHO 3 -heksendial 5 -(1, 3 -butadienil)-2 -heptendial

IUPAC nomenklatura aldehida (nast. ) Ü Aciklični polialdehidi, koji imaju više od dve aldehidne grupe vezane za nerazgranati niz, imenuju se dodatkom nastavka –trikarbaldehid, tetrakarbaldehid, itd. na ime osnovnog, najdužeg niza s najvećim brojem aldehidnih grupa Ü Ovom prilikom ime i numerisanje glavnog niza ne uključuje aldehidne grupe (koje se smatraju supstituentima), a numerisanje se vrši prema osnovnim načelima za nezasićene i/ili supstuisane ugljovodonike.

IUPAC nomenklatura aldehida (nast. ) 1, 2, 5 -pentantrikarbaldehid Ü Alternativno, ovakva jedinjenja mogu dobijati imena dodatkom prefiksa "formil" imenu diala koji uključuje glavni niz. Tako bi ime jedinjenja iz prethodnog primera po ovoj nomenklaturi bilo 3 formilheptandial

IUPAC nomenklatura aldehida (nast. ) Ü Ovakav način imenovanja aldehidne grupe primenjuje se i kada je u acikličnom jedinjenju prisutna, pored aldehidne, i grupa koja ima prednost pri navođenju, npr. trimetilamonijum-grupa u sledećem primeru: (6 -formilheksil)trimetilamonijum-jodid

IUPAC nomenklatura aldehida (nast. ) Ü Ako se u razgranatom polialdehidu jedna ili više aldehidnih grupa nalazi na krajevima bočnih nizova, osnovu imena takvog jedinjenja čini ime najdužeg niza sa najvećim brojem aldehidnih grupa, iza kojeg sledi sufiks –dial, -trikarbaldehid, itd. , a bočni lanci s aldehidnim grupama imenuju se kao formilalkilgrupe: 3 -(formilmetil)heptandial

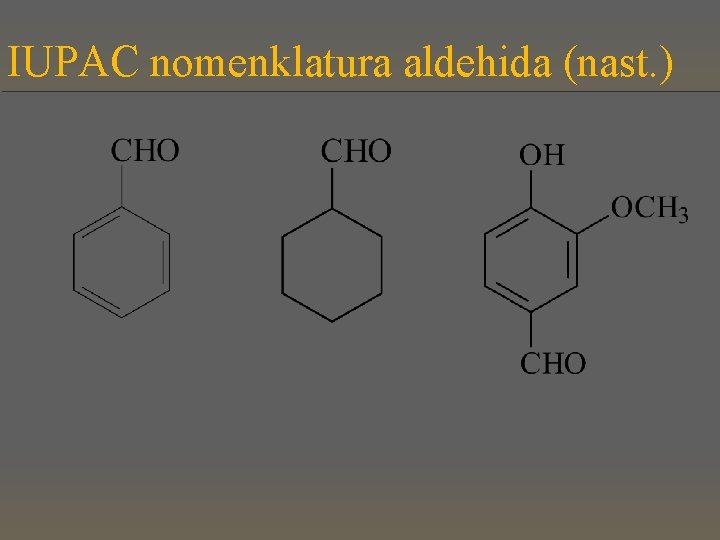
IUPAC nomenklatura aldehida (nast. ) 3 -(2 -formiletil)-1, 2, 6 -heksantrikarbaldehid Ü Kod cikličnih jedinjenja, kada je aldehidna grupa direktno vezana za C-atom prstena, imena se grade dodatkom sufiksa -karbaldehid, -dikarbaldehid, itd. imenu cikličnog sistema.

IUPAC nomenklatura aldehida (nast. )

Nomenklatura ketona Trivijalna imena izvode se iz naziva kiselina koje pirolizom daju keton. CH 3 COCH 3 - aceton, izvodi se iz dva molekula sirćetne kiseline Ü Radikal-funkcijsko imenovanje - imenima alkil grupa dodaje se reč keton Npr. CH 3 COCH 2 CH 3 je etilmetilketon Ü Po IUPAC sistemu koristi se nastavak on, a položaj karbonilne grupe mora se naznačiti brojem, osim ako je naziv i bez broja potpuno nedvosmislen Položaj karbonilne funkcije u najdužem nizu označava se takvim numerisanjem da karbonilna grupa dobije najmanji mogući broj Ü

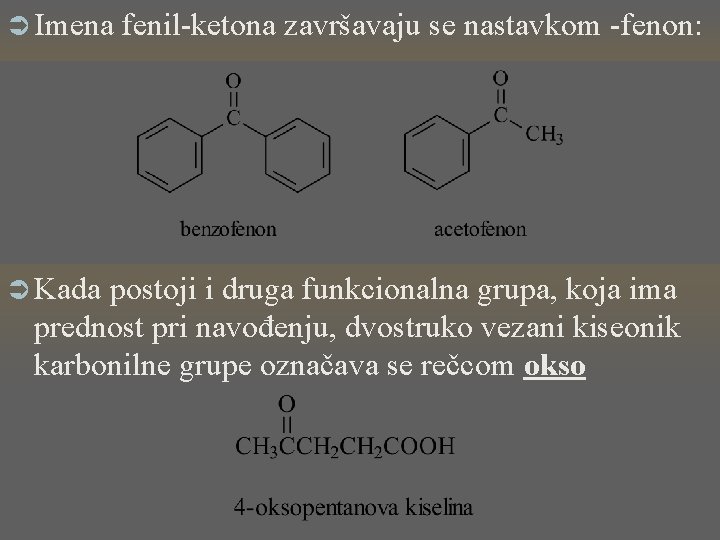
Ü Imena Ü Kada fenil-ketona završavaju se nastavkom -fenon: postoji i druga funkcionalna grupa, koja ima prednost pri navođenju, dvostruko vezani kiseonik karbonilne grupe označava se rečcom okso

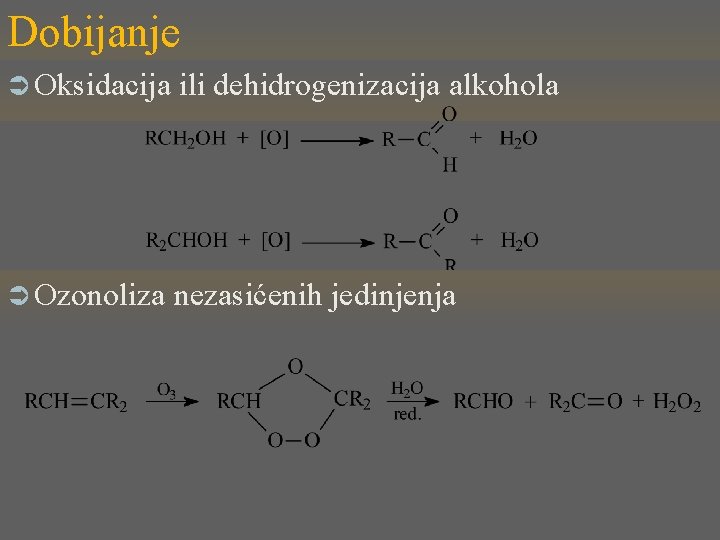
Dobijanje Ü Oksidacija ili dehidrogenizacija alkohola Ü Ozonoliza nezasićenih jedinjenja

Dobijanje aldehida i ketona Ü Piroliza Ü Ako karboksilnih kiselina se radi sa smešom organskih kiselina mogu se dobiti mešoviti ketoni, a ako se upotrebi smeša mravlje i neke druge organske kiseline mogu se dobiti aldehidi

Dobijanje aldehida i ketona Ü Adicija vode na alkine Adicijom vode na acetilen nastaje acetaldehid. Svi ostali alkini adiraju vodu po Markovnikovljevom pravilu adicije dajući ketone. Ü Friedel-Crafts-ovo acilovanje

Dobijanje aldehida i ketona Ü Reakcija Grignard-ovih reagenasa i alkil-kadmijumovih jedinjenja sa acil-hloridima Ü Alkil-kadmijumova jedinjenja, dobijena iz Grignardovog reagensa u reakciji sa suvim Cd. Cl 2, takođe supstituišu halogen acil-halogenida alkil-grupom

Fizičke osobine Ü Polarnost molekula uzrokuje dipol-dipol interakcije, zbog čega imaju više tačke ključanja od nepolarnih jedinjenja iste molekulske mase Ü Ne grade intermolekulske vodonične veze, jer je kod njih vodonik vezan samo za ugljenik. Zbog toga imaju niže tačke ključanja nego odgovarajući alkoholi ili karboksilne kiseline Ü Niži aldehidi i ketoni su u priličnoj meri rastvorni u vodi, pre svega zbog vodoničnih veza sa molekulima vode. Granica rastvorljivosti je na oko 5 C-atoma Ü Aldehidi i ketoni imaju karakterističan miris i ukus i uveliko su odgovorni, zajedno sa isparljivim masnim kiselinama, za ukus i kiselost - užeglost ustajale hrane Ü C 8 - C 14 normalni aldehidi koriste se za parfeme

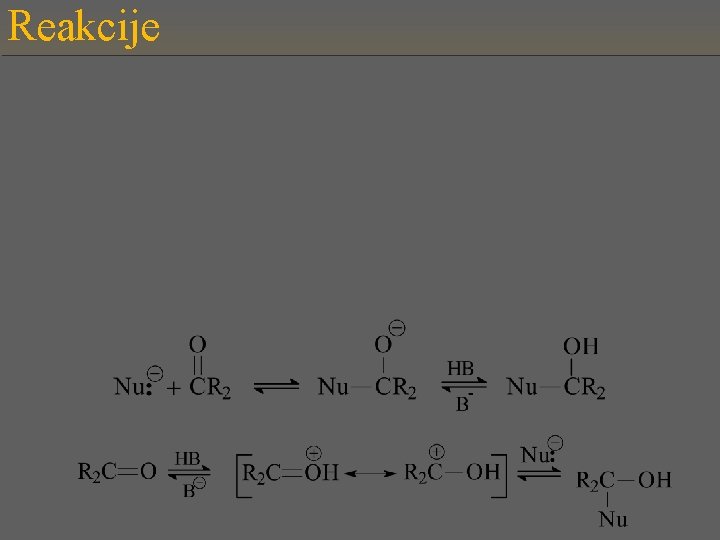
Reakcije

Ü Red reaktivnosti karbonilnih jedinjenja jeste: formaldehid ostali aldehidi ketoni Ü Veliki broj reakcija kojima aldehidi i ketoni podležu mogu se grupisati prema ukupnom reakcionom efektu na: proste adicije sa gubitkom vode oksidacija i redukcija različiti testovi i reakcije za dokazivanje aldehida i ketona

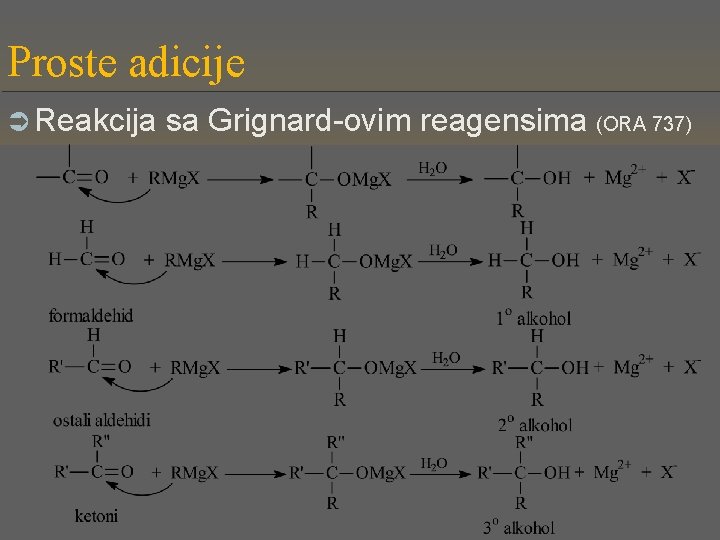
Proste adicije Ü Reakcija sa Grignard-ovim reagensima (ORA 737)

Ü Cijanovodonik Anhidrovani HCN se adira na aldehide i ketone dajući hidroksicijanide (cijanhidrini ) Ü Natrijum-bisulfit Kada se mućkaju sa zasićenim vodenim rastvorom natrijum-bisulfita većina aldehida i metil-ketona lako grade slabo rastvorna bisulfitna adiciona jedinjenja, kod kojih se vodonik adira na kiseonik, a natrijum-bisulfitna grupa na ugljenik karbonilne grupe

Ü Ove reakcije su reversne, pa se karbonilno jedinjenje može regenerisati sa bilo kojim reagensom koji ireverzibilno reguje sa bisulfitom. Mogu se upotrebiti i kiseline i baze.

Adicija hidroksi jedinjenja Ü Voda (ORA 710) jedinjenja koja imaju dve hidroksilne grupe na istom Catomu retko se mogu izolovati u slobodnom stanju Ipak, ona mogu biti postojana u vodenom rastvoru Kada se aldehidi rastvore u vodi, mogu postojati u znatnijoj količini u hidratisanom obliku. Ovo naročito važi za formaldehid, čiji vodeni rastvor sadrži skoro isključivo metandiol

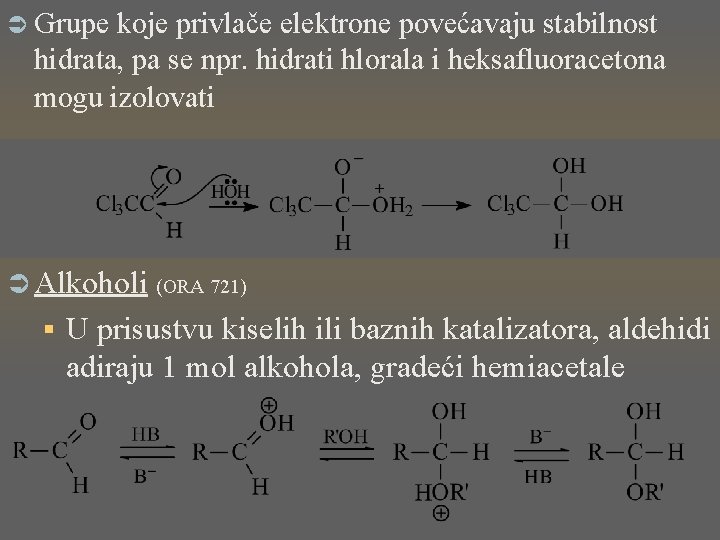
Ü Grupe koje privlače elektrone povećavaju stabilnost hidrata, pa se npr. hidrati hlorala i heksafluoracetona mogu izolovati Ü Alkoholi § (ORA 721) U prisustvu kiselih ili baznih katalizatora, aldehidi adiraju 1 mol alkohola, gradeći hemiacetale

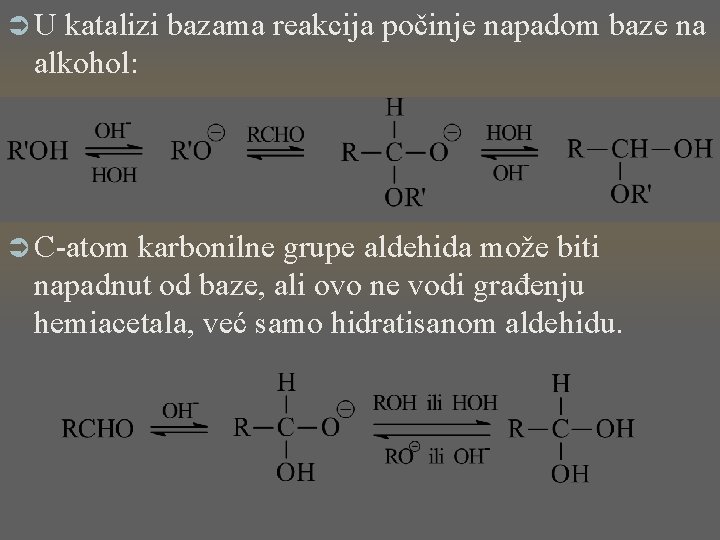
ÜU katalizi bazama reakcija počinje napadom baze na alkohol: Ü C-atom karbonilne grupe aldehida može biti napadnut od baze, ali ovo ne vodi građenju hemiacetala, već samo hidratisanom aldehidu.

Ü Sa viškom alkohola i kiselim katalizatorom eliminiše se voda i gradi acetal Ü Baze ne mogu da katalizuju građenje acetala, zato što uklanjanje protona iz hidroksilne grupe može da pomeri ravnotežu reakcije nazad, u pravcu dobijanja početnog alkohola i aldehida Ü Građenje acetala može se iskoristiti da se zaštiti aldehidna grupa za vreme dok se na drugim funkcionalnim grupama vrše reakcije kao što su oksidacija ili redukcija. Kada se reakcija završi, alkoksilne grupe se mogu ukloniti kiselom hidrolizom.

Adicija acetilena Ü Acetilidni anjon je jak nukleofil i lako napada karbonilnu grupu dajući alkinole

Ciklična trimerizacija Ü Alifatični aldehidi, ali ne i ketoni, podležu kiselo katalizovanoj adiciji dajući ciklične trimere

Aldolna adicija ÜU prisustvu razblaženih vodenih rastvora baza i kiselina, aldehidi i ketoni koji imaju najmanje jedan -vodonikov atom podležu reakcijama međusobne adicije

Ü Sa ketonima je ravnoteža pomerena toliko ulevo, da treba upotrebiti specijalne reagense (barijumpernitrid, Ba 3 N 4, i bazni Al 2 O 3) ili specijalnu aparaturu (Soxhlet-ov ekstraktor) da bi se dobile značajne količine proizvoda. 4 -hidroksi-4 -metil-2 -pentanon

Adicija sa gubitkom vode Ü Adicija amonijaka (ORA 726) Dobijeni intermedijer je nestabilan i gubi vodu dajući aldimin, RCH=NH, koji se polimerizuje u ciklični trimer

Ü Adicija derivata amonijaka Jedinjenja tipa H 2 N Z, koja se strukturno izvode iz amonijaka, pa se zato smatraju njegovim derivatima, reaguju sa aldehidima i ketonima na tipičan način i daju jedinjenja karakteristične strukture:

Adicija hidroksilamina Ü Aldehidi i ketoni adiraju hidroksilamin, hidroksilni derivat amonijaka, H 2 N-OH, dajući nestabilni početni proizvod, koji eliminacijom vode daje stabilan monomolekulski proizvod poznat kao oksim RCH = O + H 2 N-OH RCH = N-OH + H 2 O aldoksim

Ü Oksimi dobijaju imena tako što se imenu aldehida ili ketona iz kojih su nastali doda reč oksim. Tako, npr. , oksim nastao iz acetaldehida, CH 3 CH=N-OH, naziva se acetaldehid-oksim, iz acetona aceton-oksim, a iz etil-metil-ketona, CH 3(CH 3 CH 2)C=N-OH, etil-metilketon-oksim. Ü Aldehid ili keton može biti regenerisan iz svog oksima kiselo katalizovanom izmenom sa viškom nekog reaktivnijeg aldehida ili ketona, npr. HCHO, acetona itd. Ü Oksimi su obično kristalna jedinjenja i stoga su korisni derivati za identifikaciju aldehida i ketona.

Supstituisani hidrazini Ü Najčešće upotrebljavani hidrazini su: fenilhidrazin, C 6 H 5 NHNH 2, i supstituisani fenilhidrazini, naročito 2, 3 -dinitrofenilhidrazin, pri čemu nastaju proizvodi poznati kao fenilhidrazoni i semikarbazid, H 2 NNHCONH 2, pri čemu su proizvodi poznati kao semikarbazoni

Oksidacija Ü Vazduhom (autooksidacija) Aldehidi spadaju u supstance koje se lako spontano oksiduju. Lančana reakcija se inicira prisustvom slobodnih radikala

Oksidacija drugim oks. sredstvima Ü Aldehidi se lako oksiduju u kiseline čak i slabim oksidacionim sredstvima Ü Najčešće se koriste HNO 3, hromna kiselina ili KMn. O 4 Ü Ketoni su prilično stabilni prema oksidaciji, ali se i oni mogu oksidovati

Test za razlikovanje aldehida od ketona Ü Zbog lakoće oksidacije aldehida u onosu na ketone, moguće je izabrati takvo oksidaciono sredstvo koje napada samo aldehide, a ne ketone, i da se ova reakcija upotrebi kao test za razlikovanje aldehida od ketona. U ovu svrhu obično se upotrebljava Tollens-ov reagens, amonijačni rastvor Ag 2 O

Redukcija Ü Katalitička redukcija. Aldehidi daju primarne alkohole, a ketoni sekundarne (ORA 740) Ü Redukcija pomoću metalnih hidrida. Najčešće se koriste Li. Al. H 4 u etarskom rastvoru ili Na. BH 4 u vodi ili etanolu

Redukcija u glikole i pinakole Ü na površini amalgamisanog magnezijuma adsorpcija karbonilnih grupa prenos jednog elektrona na C-atom

Redukcija >C=O u >CH 2 grupu Ü Clemmensen-ova redukcija Reakcijom nekog aldehida ili ketona sa amalgamisanim cinkom u prisustvu HCl zamenjuje se kiseonik sa dva vodonikova atoma RCOR + 2 Zn + 4 HCl RCH 2 R + H 2 O + 2 Zn. Cl 2

Ü Wolff-Kishner-ova redukcija Hidrazoni ili semikarbazoni aldehida ili ketona raspadaju se na povišenoj temperaturi, naročito u prisustvu baza, dajući ugljovodonik i N 2

Intermolekulska oksidacija i redukcija Ü Moguće je da se istovremeno vrše i oksidacija i redukcija između dva molekula aldehida, tako da se jedan oksiduje, a drugi redukuje (Cannizzaro-va reakcija) Ü Cannizzaro-va reakcija je ograničena na aldehide koji nemaju -vodonik, kao što su formaldehid ili trimetil-acetaldehid

Različiti testovi i reakcije Ü Schiff-fuksin aldehidni reagens Fuksin je reagens mrko-ljubičaste boje u vodenom rastvoru može se obezbojiti pomoću SO 2 u prisustvu aldehida mrko-ljubičasta boja se opet pojavljuje pošto sve ono što uklanja SO 2 iz reakcije (alkalije, amini, itd. ) regeneriše boju, ova reakcija nije specifična za aldehide Kada takve smetnje ne postoje, reagens služi za razlikovanje aldehida od ketona.

fuksin-hidrohlorid

Supstitucija kiseonika halogenom Ü Kada aldehidi ili ketoni reaguju sa PCl 5 ili PBr 5, kiseonik karbonilne grupe supstituišu dva atoma halogena. Ü Pošto se u ovoj reakciji gradi intermedijerni karbkatjon, postoje i uslovi za konkurentnu reakciju eliminacije, pri čemu može nastati halogenalken:

Građenje soli atomi na -ugljenikovom atomu u odnosu na karbonilnu grupu su dovoljno kiseli da reaguju s alkalnim metalima i grade soli. Tako npr. , aceton reaguje sa metalnim Na i izdvaja vodonik. Ü Vodonikovi

Halogenovanje i haloformska reakcija Ü katalizovano je i kiselinama i bazama Ü brzina reakcije zavisi od koncentracije karbonilnog jedinjenja i od koncentracije kiseline ili baze, ali je nezavisna od koncentracije ili vrste halogena. Ü kiselo katalizovana reakcija započinje protonovanjem kiseonika karbonilne grupe.

ÜU baznoj katalizi početna faza reakcije je uklanjanje protona sa -ugljenikovog atoma Ü Ako je karbonilna grupa vezana za metil-grupu, kao kod acetaldehida ili acetona, dobija se trihalogenski proizvod. Ü U prisustvu baze, dolazi do raskidanja veze i proizvodi reakcije su odgovarajući haloform i karboksilatni anjon.

Aromatični aldehidi i ketoni Ü Dobijanje Hidroliza dihalogenida Ü Reimer-Tieman-ova je samo sa fenolima reakcija. Ova reakcija izvedena

Reakcije aromatičnih aldehida Ü Halogenovanje aldehidne grupe Kako aromatični aldehidi nemaju -vodonik i kako se aromatični prsten ne susptituiše u odsustvu specijalnog katalizatora, moguće je izvršiti direktnu supstituciju Hatoma aldehidne grupe, pri čemu kao proizvod nastaje acilhalogenid

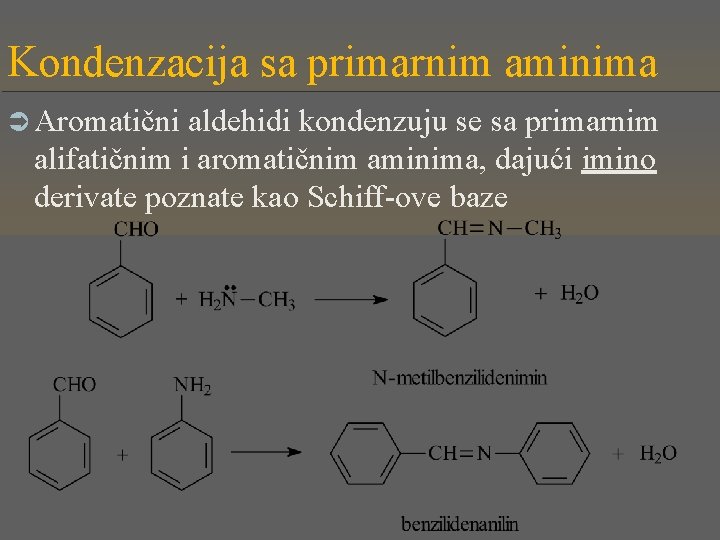
Kondenzacija sa primarnim aminima Ü Aromatični aldehidi kondenzuju se sa primarnim alifatičnim i aromatičnim aminima, dajući imino derivate poznate kao Schiff-ove baze

Aldolne kondenzacije sa alifatičnim aldehidima i ketonima Ü Aromatični aldehidi se kondenzuju sa drugim aldehidima i ketonima koji imaju dva -vodonikova atoma Ü intermedijerni aldoli gube molekul vode, jer je uvedena dvoguba veza konjugovana i sa karbonilnom grupom i sa aromatičnim prstenom. Ü Kondenzacije aldehida izvode se u prisustvu 10% Na. OH i poznate su kao Claisen-ove reakcije.

Perkin-ova sinteza Ü Perkin je otkrio tip aldolne kondenzacije anhidrida kiselina i aromatičnih aldehida Ü Kao katalizator obično se upotrebljava natrijumova so one kiseline čiji se anhidrid koristi Ü Krajnji proizvod je , -nezasićena kiselina.

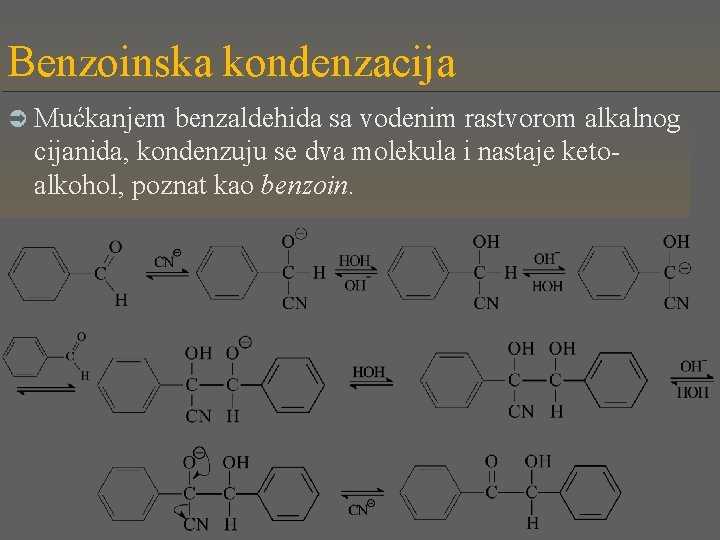
Benzoinska kondenzacija Ü Mućkanjem benzaldehida sa vodenim rastvorom alkalnog cijanida, kondenzuju se dva molekula i nastaje ketoalkohol, poznat kao benzoin.