Uvod u laboratorijski rad NOMENKLATURA NEORGANSKIH JEDINJENJA Profesor

Uvod u laboratorijski rad NOMENKLATURA NEORGANSKIH JEDINJENJA Profesor dr. Dragica Minić

IUPAC organizacija u The International Union of Pure and Applied Chemistry (IUPAC) je međunarodna nevladina organizacija ustanovljena 1919 radi podrške razvoju moderne hemije. u Nacionalna hemijska društva su članovi IUPAC-a.

u u IUPAC je priznat je autoritet za razvijanje standarda za imenovanje hemijskih elemenata i njihovih jedinjenja preko Međudevizionog komiteta za nomenklaturu i simbole (IUPAC nomenklatura). Član je Internacionalnog naučnog konzilijuma (International Council for Science, ICSU)
Istorijski pregled u 1782. Francuski hemičar Louis-Bernard Guyton de Morveau Publikovao je svoje preporuke za davanje naziva u hemiji pod nazivom “Konstantni metod zadavanja naziva”. [Guyton de Morveau L. B. , J. Phys. 19(1782) 310]

u 1787. Sistem su preradili Berthollet, de Fourcroy and Lavoisier: [Guyton de Morveau, L. B. Lavoisier A. L. , Berthollet C. L. , de Fourcroy A. F. ] Methode de Nomenclature Chimique, Paris (1787)] u 1801. Promocija sistema data je u priručniku koji je dugo posle autorovog pogubljenja na giljotini 1794. bio u upotrebi: [Lavoisier A. L. , Traite Elementaire de Chemie (3. ed. Paris: Deterville (1801)]

Prva strana Lavoazjeve “Chymical Nomenclature”

u 1811 Berzelius je sistem adapatirao za primenu na nemačkom govornom području: [Berzelius J. J. , J. Phys. 73 (1811) 248] Preporuke Guyton-a su se odnosile samo na nomenklaturu neorganskih jedinjenja, što nikako nije moglo da zadovolji opšti razvoj organske hemije koji je doveo do boljeg razumevanja strukture organskih jedinjenja sredinom devetnaestog veka i nametnuo potrebu razvoja nomenklature organskih jedinjenja.

u 1892. u Ženevi je održana međunarodna konferencija Nacionalnih hemijskih društava gde su prihvaćani predlozi za uvođenje standardizacije naziva u hemiji [Bull. Soc. Chim. (Paris) 3(7), XIII. (1982)]

Učesnici Ženevske konferencije 1892

u u 1913. osnovan je Savet međunarodne zajednice hemijskih društava [Council of the International Associacion of Chemical Societies] čiji je rad prekinuo I. svetski rat 1919. osnovana je Međunarodna zajednica za čistu i primenjenu hemiju [International Union of Pure and Applied Chemistry, skraceno IUPAC]

u 1921 IUPAC formira komisije za sledeće nomenklature, koje postoje i danas: organsku neorgansku biohemijsku Pored upustva za nomenklaturu IUPAC daje standarde i za internacionalno pisanje naziva: npr. aluminum, sulphur, itd.

IUPAC nomenklatura neorganskih jedinjenja u IUPAC nomenklatura neorganskih jedinjenja je sistematsko imenovanje neorganskih hemijskih jedinjenja kako je preporučeno od strane International Union of Pure and Applied Chemistry (IUPAC)

u Prema ovoj nomenklaturi, svako jedinjenje treba da ime iz koga nedvosmisleno može da bude određena formula, odnosno svako ime treba da označava samo jednu supstancu. u Ime treba da sadrži informacije kako o sastavu tako i o strukturi jedinjenja. u Pravila za imenovanje organskih i neorganskih jedinjenja sadržana su u sledećim dokumentima:

u u 1. Plava knjiga –organska jedinjenja [Nomenclature of Organic Chemistry, Oxford: Pergamon Press 1979, A Guide to IUPAC, Nomenclature of Organic Compounds, Recommendations 1993, Oxford: Blackwell Scientific Publications, 1993] 2. Crvena knjiga–neorganska jedinjenja [Nomenclature of Inorganic Compounds, Recommendations 1990, Oxford: Blackwell Scientific Publications, 1990]

u u 3. Zelena knjiga–simboli i fizičke veličine [Quantities, Units and Symbols in Physical Chemistry (2. ed. ) Oxford: Blackwell Scientific Publications, 1993] 4. Zlatna knjiga–tehnički termini u hemiji [Compendium of Chemical Terminology IUPAC Recommendations (2. ed. ), Oxford: Blackwell Scientific Publications, 1997]

u 5. Slična literatura postoji za biohemiju, analitičku hemiju i hemiju makromolekula: u [Biochemical Nomenclature and related Documents, London: Portland Press, 1992] u [Compendium of Analytical Nomenclature, definite Rules 1997 (3. ed. ) Oxford: Blackwell Scientific Publications, 1998] u [Compendium of macromolecular Nomenclature, Oxford: Blackwell Scientific Publications, 1991]

u Sistematsko određivanje imena mora da odražava strukturu i sastav: 1. Jednoatomski anjoni imaju sufiks id, H- = hidrid 2. Ime jedinjanja koja sadrže katjon i anjon sadrže prvo ime katjona a zatim ime anjona, Na. Cl =natrijum-hlorid 3. Naelektrisanja katjona koji imaju više pozitivnih naelektrisanja se stavljaju u zagrade bakar(I)=kupro i bakar(II)=kupri.

4. Poliatomski anjoni koji sadrže više atoma kiseonika sadrže sufiks it za niži i at za viši sadržaj kiseonika: NO 2 -=nitrit i NO 3 -=nitrat. Za kiseonike koriste se još i prefiksi hipo i per: Cl. O-= hipohlorit 5. i Cl. O 4 -= perhlorat. Prefiks bi- se koristi za označavanje prisustva jednog vodoničnog jona, Na. HCO 3= natrijum-bikarbonat ili sada Na. HCO 3 =natrijum vodonik karbonat
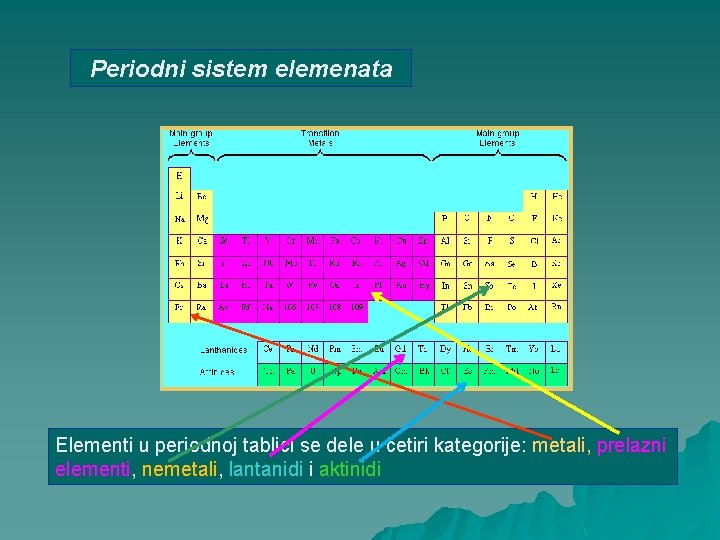
Periodni sistem elemenata Elementi u periodnoj tablici se dele u četiri kategorije: metali, prelazni elementi, nemetali, lantanidi i aktinidi

u Broj atoma svakog elementa u molekulu (ili formulskoj jedinki) označava se grčkim prefiksom: Prefiks mono-* ditritetrapentaheksaheptaoktanonadeka- Broj atoma 1 2 3 4 5 6 7 8 9 10 * Prefiks mono- se retko koristi; kada nema prefiksa ispred imena elementa pretpostavlja se da je u molekulu ili formulskoj jedinki prisutan jedan atom tog elementa.

Binarna jedinjenja koja sadrže dva nemetala u Binarna jedinjenja su ona koja sadrže dva hemijska elementa, npr dva nemetala; na kraju imena drugog po redu elementa binarnog jedinjenja stavlja se nastavak –id BCl 3 =bor-trihlorid, SO 2 =sumpor-dioksid, N 2 O 4 =diazot-tetroksid, CO =ugljen-monoksid, PCl 5 = fosfor-pentahlorid.

Binarna jedinjenja koja sadrže metal i nemetal u Nomenklatura ovih jedinjenja zavisi od toga da li metal koji je prisutan u jedinjenju ima konstantno naelektrisanje ili promenljivo naelektrisanje. u Katjoni sa konstantnim naelektrisanjem su sledeći: Li+, Na+, K+, Rb+, Cs+, Ag+, Mg 2+, Ca 2+, Sr 2+, Ba 2+, Zn 2+, Cd 2+, Al 3+ Svi drugi metali imaju promenljivo naelektrisanje.

u Ime metala ide kao prvo, a zatim sledi ime nemetala sa nastavkom -id, u Primeri binarnih jedinjenja koja sadrže metal i nemetal: KCl = kalijum-hlorid Mg. O = magnezijum-oksid Na 2 S = natrijum-sulfid Ca. H 2 = kalcijum-hidrid Li. Br = litijum-bromid

u Kod binarnih jedinjenja nemetala i metala promenljivog naelektrisanja mora se naznačiti naelektrisanje datog metalnog jona na jedan od dva sledeća načina: u I. Posle naziva metala u zagradu se stavlja rimski broj koji predstavlja naelektrisanje metalnog jona: Cu. Cl 2 = bakar(II) hlorid, Fe. O= gvoždje(II) oksid Fe 2 O 3= gvoždje(III) oksid u II. Na ime metala dodaje se nastavak (sufiks) –o, za jon manjeg naelektrisanja, ili nastavak –i, za jon većeg naelektrisanja: Cu 1+ = kupro jon Fe 2+= fero jon Pb 2+ = plumbo jon Hg 2 2+ = merkuro jon Sn 2+ = stano jon Cu 2+ = kupri jon Fe 3+ = feri jon Pb 4+ = plumbi jon Hg 2+ = merkuri jon Sn 4+ = stani jon

Ternarna i viša jedinjenja u Ternarna jedinjenja sastavljena su od tri ili više atoma obično uključuju tri hemijska elementa: metalni jon, višeatomski jon ili oksi-halogen jon. NH 4+ Amonijum jon CO 32 - Karbonatni jon HCO 3 - Bikarbonatni jon CN- Cijanidni jon C 2 O 42 - Oksalatni jon CH 3 COO- Acetatni jon

Negativni višeatomski joni sa imenom koje sadrži sufiks –at imaju jedan kiseonikov atom više od onih sa sufiksom –it: Cl. O- Hipohloritni jon Cl. O 2 - Hloritni jon Cl. O 3 - Hloratni jon Cl. O 4 - Perhloratni jon Cr. O 42 - Hromatni jon Cr 2 O 72 - Dihromatni jon OH- Hidroksidni jon NO 2 - Nitritni jon NO 3 - Nitratni jon Mn. O 4 - Permanganatni jon PO 43 - Fosfatni jon HPO 42 - Vodonik fosfatni jon

u Za metale sa promenljivim naelektrisanjem koriste se sufiksi - o ili – i. Formula jedinjenja Na. NO 2 Ime jedinjenja natrijum-nitrit Na. NO 3 natrijum-nitrat Na. HSO 3 natrijum-vodonik sulfit (natrijum-bisulfit) Cu 3(PO 4)2 bakar (II) fosfat (kupri-fosfat) Cu. CN bakar (I) cijanid (kupro-cijanid) Ba(CH 3 COO)2 barijum acetat Ag. Cl. O 4 srebro-perhlorat Fe 2(Cr. O 4)3 gvoždje (III) hromat (feri-hromat)

Kiseline u Kiselina je jedinjenje koje sadrži vodonik i koje daje vodonične (H+) jone kada se rastvori u vodi. u Ovo je Arrhenius-ova definicija, koja je ograničena na rastvore koji sadrže vodu kao rastvarač. u Preciznije, prema Bronsted-Lowry- konceptu, kiselina je supstanca koja je donor (davalac) vodoničnih jona , tj. protona nekoj drugoj supstanci. Poslednja definicija važi za bilo koji rastvarač koji se koristi za pripremu rastvora kiseline.

u Formule i imena nekih kiselina Formula Naziv HF Fluorovodonična kiselina HCl Hlorovodonična kiselina HBr Bromovodonična kiselina HNO 3 Azotna kiselina CH 3 COOH Sirćetna kiselina H 2 SO 3 Sumporasta kiselina H 2 SO 4 Sumporna kiselina

nastavak Formula Naziv HCl. O Hipohlorasta kiselina HCl. O 2 Hlorasta kiselina HCl. O 3 Hlorna kiselina HCl. O 4 Perhlorna kiselina HBr. O 4 Perbromna kiselina H 3 PO 3 Fosforsta kiselina H 3 PO 4 orto-Fosforna kiselina

Baze Baza je, prema Arrhenius-ovom konceptu, supstanca koja daje hidroksidne jone (OH-) kada se rastvori u vodi. Prema Bronsted-Lowry konceptu, baza je supstanca koja može da primi vodonikov jon (proton) od neke druge supstance. Kažemo da su baze akceptori protona. u Imena baza završavaju se sa –id: Li. OH litijum-hidroksid Ba(OH)2 barijum-hidroksid.

Soli su jedinjenja koja nastaju kada se jedan ili više vodonikovih jona u kiselini zameni drugim katjonom ili kada se jedan ili više hidroksidnih jona u bazi zameni drugim anjonom. u Osnovni tipovi soli su: binarna jedinjenja sastavljena od metalnog katjona i nemetalnog anjona Na. Cl natrijum-hlorid u ternarna i viša jedinjenja koja su sačinjena od metalnog katjona ili amonijumovog jona i negativnog višeatomskog jona: Na. NO 3 natrijum-nitrat (NH 4)2 SO 4 amonijum-sulfat

Kristalohidrati u Poseban tip soli (kristalnih jedinjenja) koje sadrže definisanu količinu hemijski vezane vode, i koje se pri zagrevanju razlažu otpuštajući vodu, nose naziv kristalohidrati ili hidrati. Mg. SO 4 · 7 H 2 O magnezijum sulfat heptahidrat. Grčki prefiksi pokazuju broj molekula vode: Mg. SO 4. 2 H 2 O magnezijum sulfat dihidrat, Mg. SO 4. 3 H 2 O magnezijum sulfat trihidrat.

Revizija IUPAC-ove nomenklature za neorganska jedinjenja 2005. Izvršena je revizija nomenklature Prema ovoj reviziji nema više apsolutno ispravnog imena za jedno jedinjenje. - Svako ime koje nedvosmisleno označava jedinjenje je korektno ime (voda, karbonil, cijano) Postoje dva načina opisa jedinjenja prema: - sastavu i prema substituentima

Prema sastavu: Molekul se opisuje preko jezgra kao kod kompleksa. 1. Jezgro(a) molekula je atom najniže elektronegativnosti. Ovaj elemenat definiše osnovno ime jedinjenja: ako je jedinjenje negativno naelektrisano sadrži prefiks id ako nije prisutan drugi atom i at u drugom slučaju 2. Okolni atomi i grupe se opisuju kao ligandi sa sufiksom o, identične grupe sadrže prefikse tri-, tetra- ili bis 3. Zatim se navode oznake za naelektrisanje, funkciju radikala, kristalizaciona voda, premoštavajući ili koordinirani ligandi.
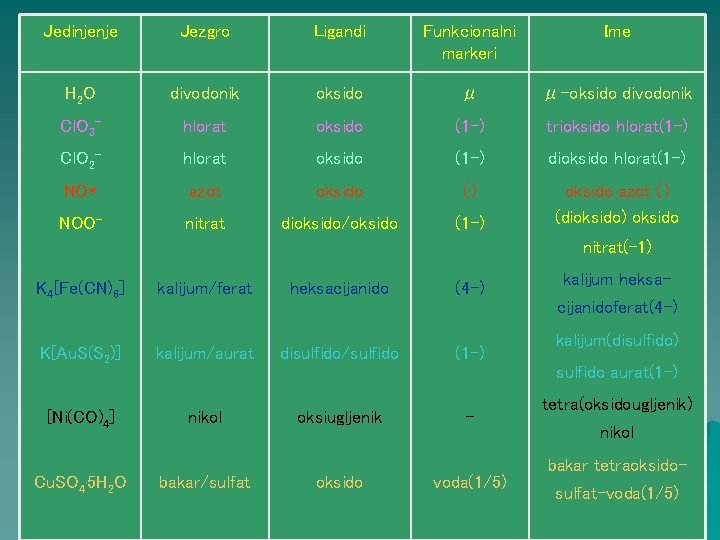
Jedinjenje Jezgro Ligandi Funkcionalni markeri Ime H 2 O divodonik oksido μ μ-oksido divodonik Cl. O 3 - hlorat oksido (1 -) trioksido hlorat(1 -) Cl. O 2 - hlorat oksido (1 -) dioksido hlorat(1 -) NO* azot oksido (. ) NOO- nitrat dioksido/oksido (1 -) oksido azot (. ) (dioksido) oksido nitrat(-1) K 4[Fe(CN)6] kalijum/ferat K[Au. S(S 2)] kalijum/aurat [Ni(CO)4] nikol Cu. SO 4 . 5 H 2 O heksacijanido (4 -) kalijum heksacijanidoferat(4 -) disulfido/sulfido (1 -) kalijum(disulfido) sulfido aurat(1 -) bakar/sulfat oksiugljenik oksido - voda(1/5) tetra(oksidougljenik) nikol bakar tetraoksidosulfat-voda(1/5)

u Prema supstituentima Uopštava se nomenklatura organskih jedinjenja prateći osnovna pravila: 1. Svim elementima se dodaje nastavak an na bazno ime a nezasićene veze se ispunjavaju atomima vodonika: oksidan atom kiseonika vezan za vodonik (H 2 O voda) dioksidan lanac dva atoma kiseonika vezan sa atomima vodonika (H 2 O 2 vodonik peroksid)

BH 3 Al. H 3 Ga. H 3 In. H 3 Tl. H 3 boran aluman galan indigan talan CH 4 Si. H 4 Ge. H 4 Sn. H 4 Pb. H 4 metan silan german stanan plumban NH 3 PH 3 As. H 3 Sb. H 3 Bi. H 3 azan fosfan arsan stiban bizmutan H 2 O H 2 Se H 2 Te H 2 Po oksidan sulfan selan telan polan HF HBr HAt fluoran broman astatan HCl HI hloran jodan
- Slides: 38