FENOLI Areni supstituisani hidroksi grupama Nomenklatura IUPAC benzenoli

FENOLI • Areni supstituisani hidroksi grupama Nomenklatura: • IUPAC – benzenoli • Staro (trivijalno) ime – karbolna kiselina • Supstituisani fenoli: fenoli, benzendioli i benzentrioli • Fenoli koji sadrže karboksilnu ili sulfonsku funkcionalnu grupu zovu se hidroksibenzoeva ili hidroksisulfonska kiselina • Metil supstituisani fenoli zovu se još i krezoli
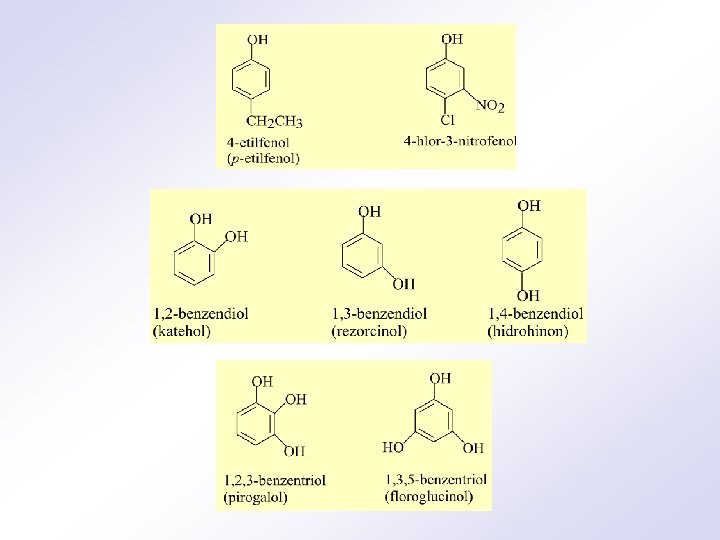

OH OH OH COOH SO 3 H 4 -hidroksibenzensulfonska kiselina OH COOH 2 -hidroksibenzoeva kiselina (salicilna kiselina) 3 -hidroksibenzoeva kiselina OH OH CH 3 2 -metilfenol (o-krezol) 3 -metilfenol (m-krezol) CH 3 4 -metilfenol (p-krezol)
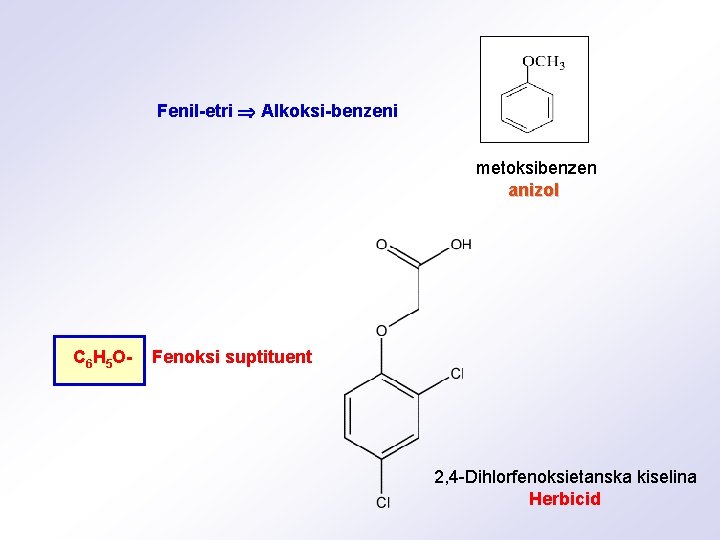
Fenil-etri Alkoksi-benzeni metoksibenzen anizol C 6 H 5 O- Fenoksi suptituent 2, 4 -Dihlorfenoksietanska kiselina Herbicid

FIZIČKE OSOBINE: • Bezbojni, igličasti kristali karakterističnog mirisa • Tt = 430 C • Rastvorljivost u vodi: 9 g/100 g Fenoli imaju visoke temperature ključanja zbog vodoničnih veza! Jedinjenje Tk (70 mm. Hg) Rastvorljivost u vodi (g/100 g H 2 O) o-nitrofenol 100 0, 2 m-nitrofenol 194 1, 35 p-nitrofenol raspada se 1, 69 • Najvažnija primena: dobijanje polimera – fenolnih smola • Vodeni rastvori fenola i metilfenola koriste se kao dezifekciona sredstva • Fenol je otrovan, izaiziva opekotine na koži, • 1 g izaziva smrt, • Lako se apsorbuje kroz kožu.

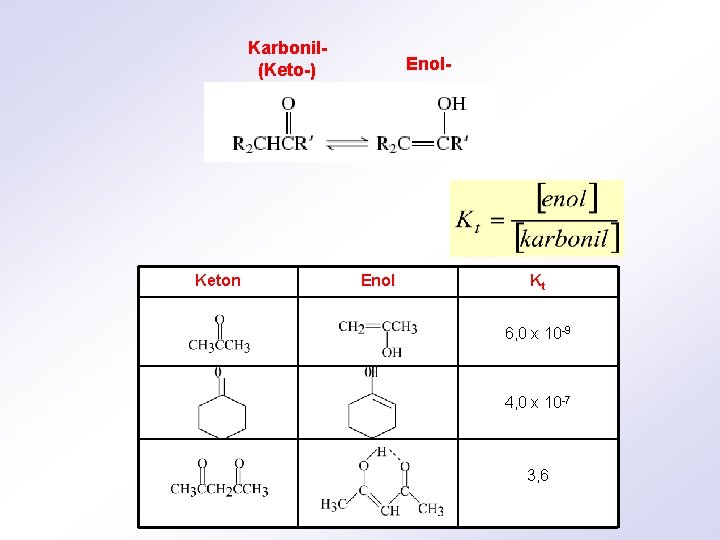
Karbonil(Keto-) Keton Enol- Enol Kt 6, 0 x 10 -9 4, 0 x 10 -7 3, 6

STRUKTURA I KISELOST FENOLA: Enolni oblik zbog očuvanja aromatičnog karaktera
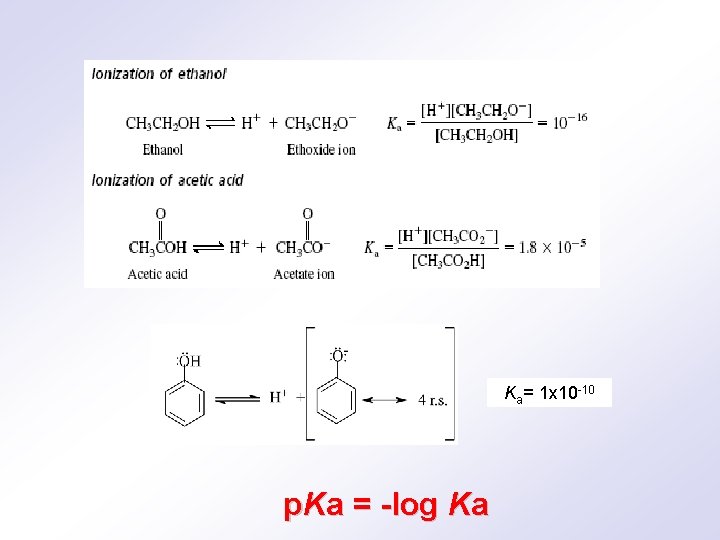
Ka= 1 x 10 -10 p. Ka = -log Ka
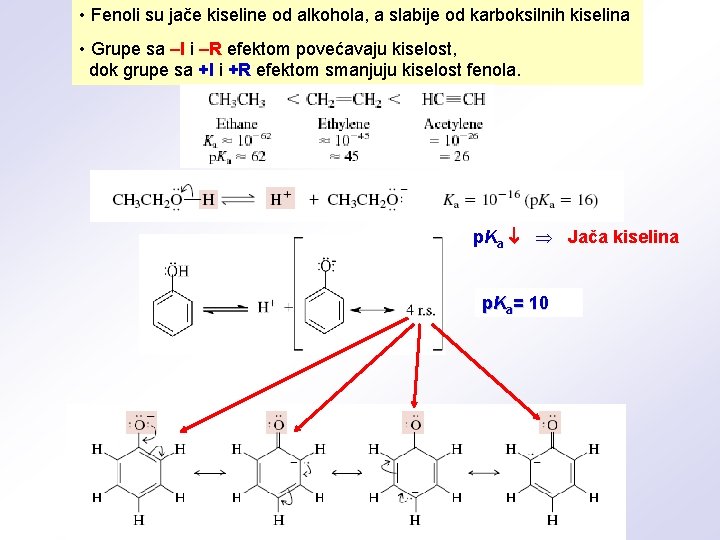
• Fenoli su jače kiseline od alkohola, a slabije od karboksilnih kiselina • Grupe sa –I i –R efektom povećavaju kiselost, dok grupe sa +I i +R efektom smanjuju kiselost fenola. p. Ka Jača kiselina p. Ka= 10
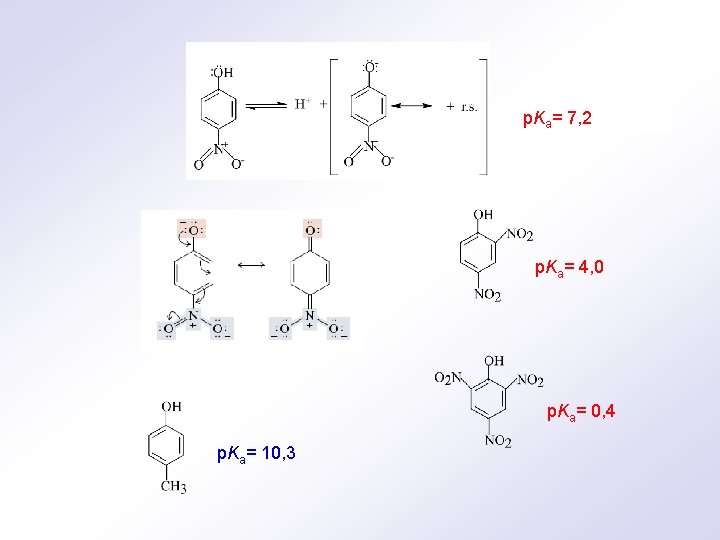
p. Ka= 7, 2 p. Ka= 4, 0 p. Ka= 0, 4 p. Ka= 10, 3
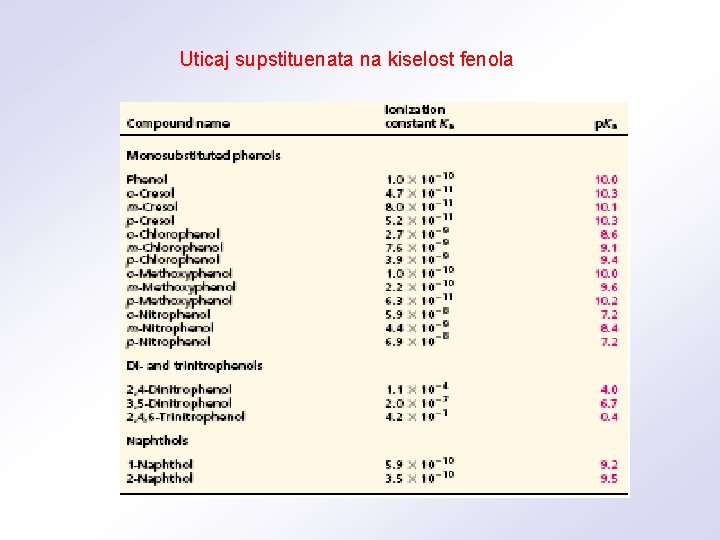
Uticaj supstituenata na kiselost fenola
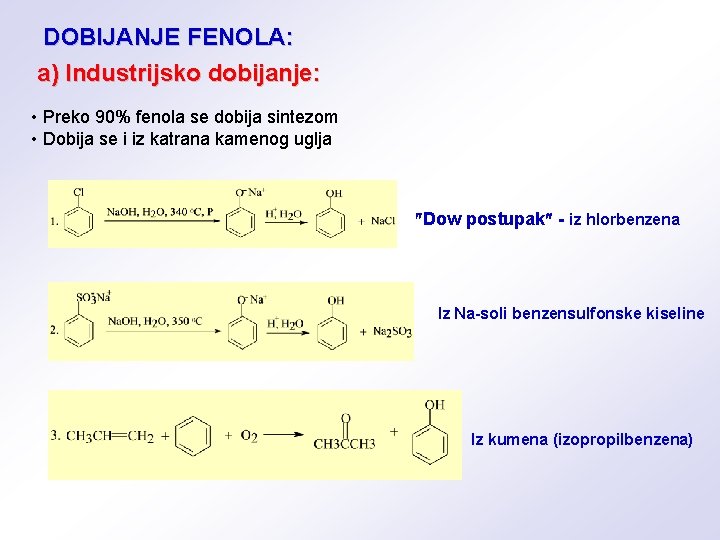
DOBIJANJE FENOLA: a) Industrijsko dobijanje: • Preko 90% fenola se dobija sintezom • Dobija se i iz katrana kamenog uglja Dow postupak - iz hlorbenzena Iz Na-soli benzensulfonske kiseline Iz kumena (izopropilbenzena)
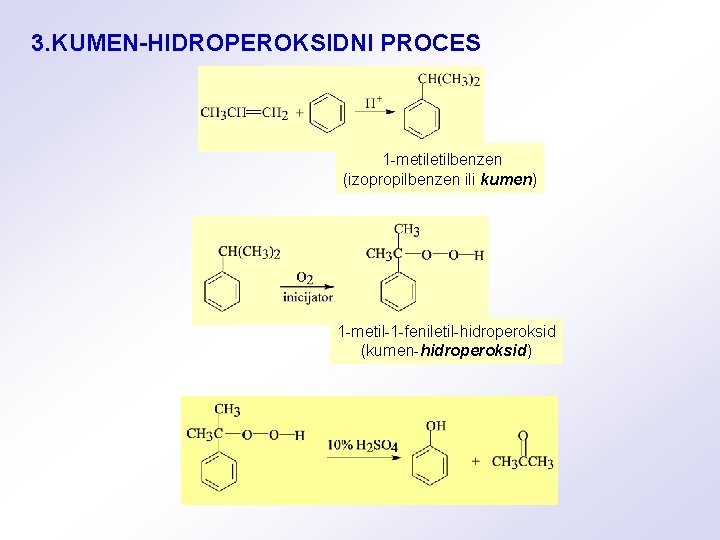
3. KUMEN-HIDROPEROKSIDNI PROCES 1 -metilbenzen (izopropilbenzen ili kumen) 1 -metil-1 -feniletil-hidroperoksid (kumen-hidroperoksid)
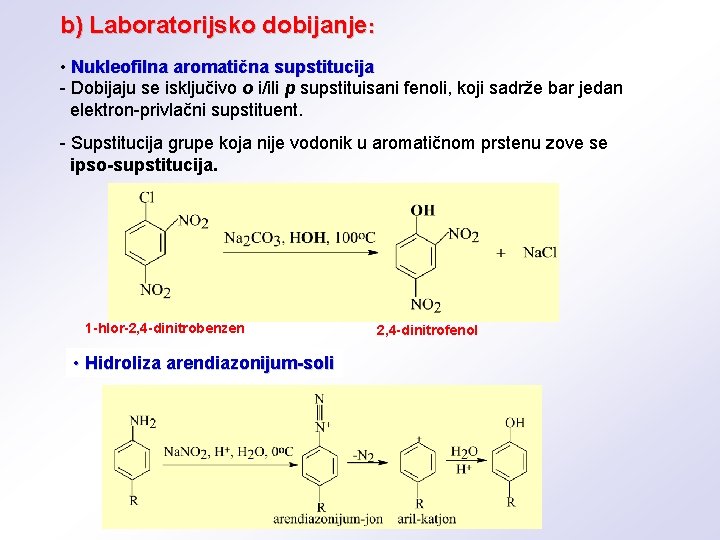
b) Laboratorijsko dobijanje: • Nukleofilna aromatična supstitucija - Dobijaju se isključivo o i/ili p supstituisani fenoli, koji sadrže bar jedan elektron-privlačni supstituent. - Supstitucija grupe koja nije vodonik u aromatičnom prstenu zove se ipso-supstitucija. 1 -hlor-2, 4 -dinitrobenzen • Hidroliza arendiazonijum-soli 2, 4 -dinitrofenol
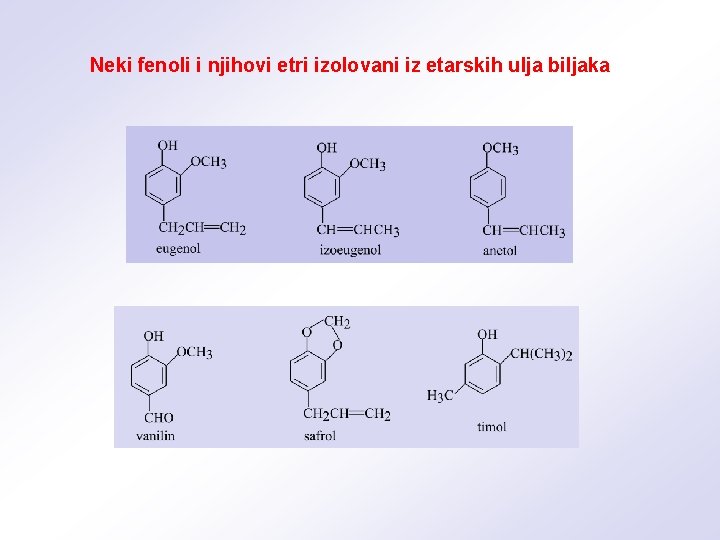
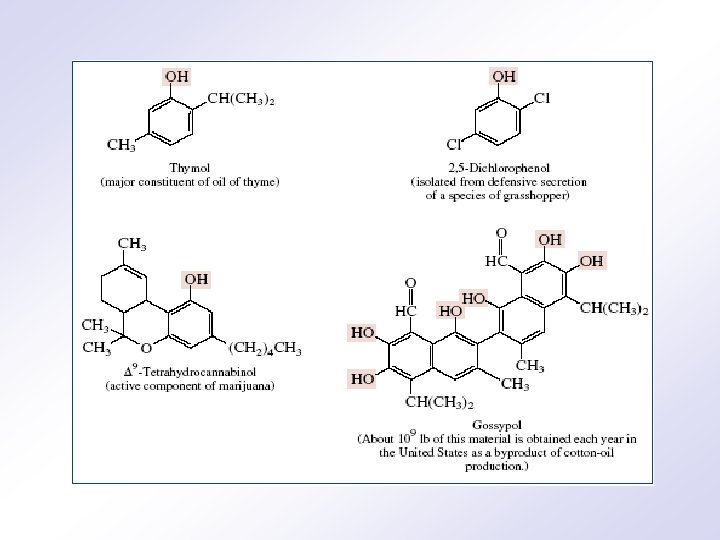
Neki fenoli i njihovi etri izolovani iz etarskih ulja biljaka
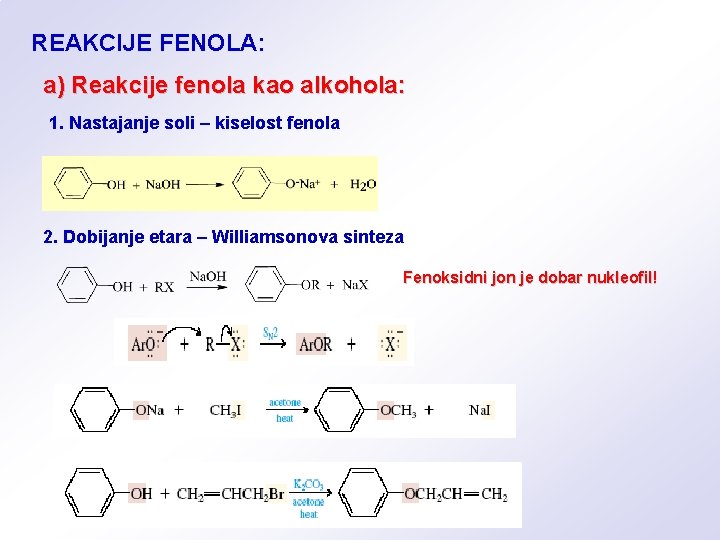
REAKCIJE FENOLA: a) Reakcije fenola kao alkohola: 1. Nastajanje soli – kiselost fenola 2. Dobijanje etara – Williamsonova sinteza Fenoksidni jon je dobar nukleofil!
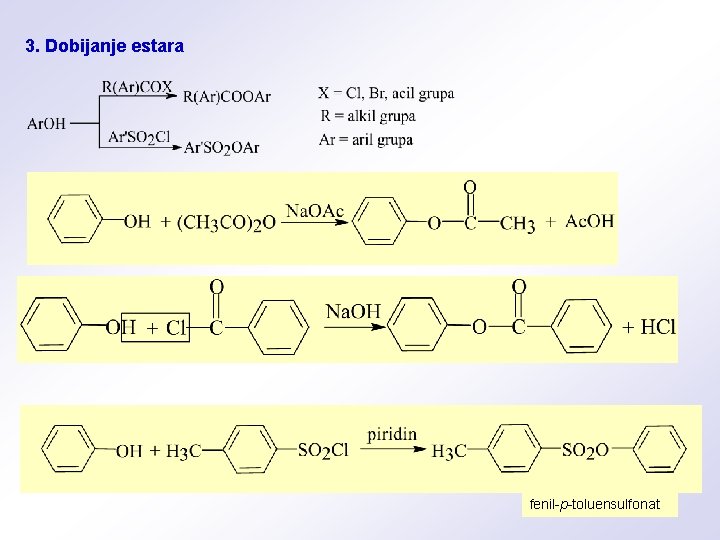
3. Dobijanje estara fenil-p-toluensulfonat
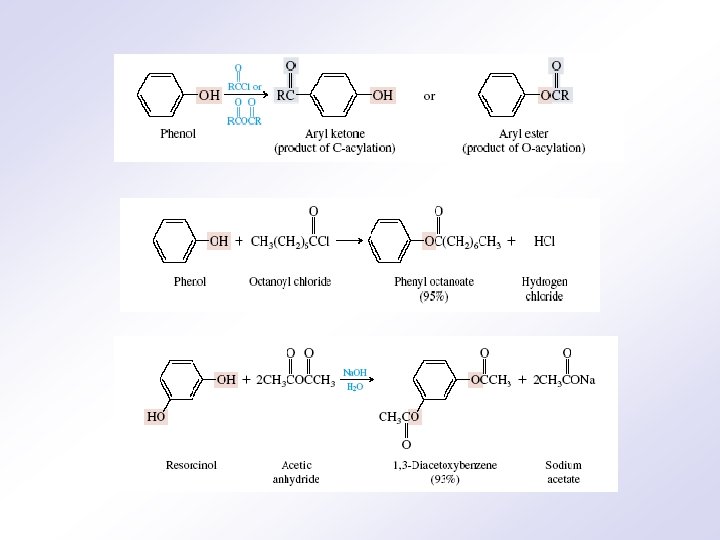
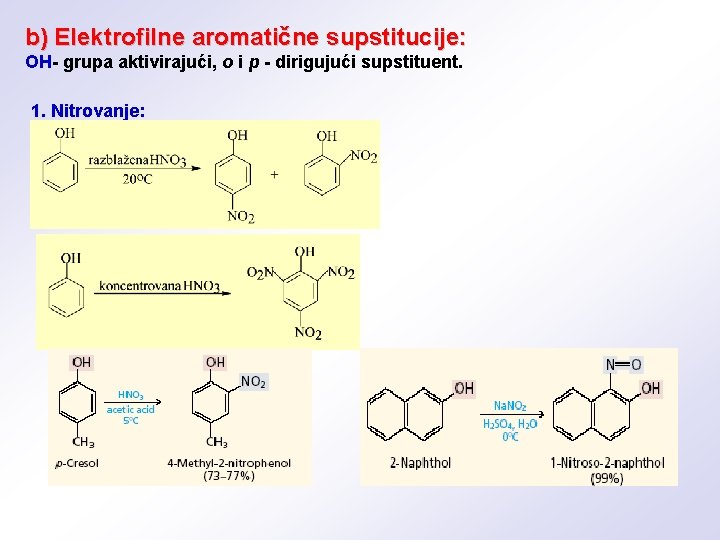
b) Elektrofilne aromatične supstitucije: OH- grupa aktivirajući, o i p - dirigujući supstituent. 1. Nitrovanje:
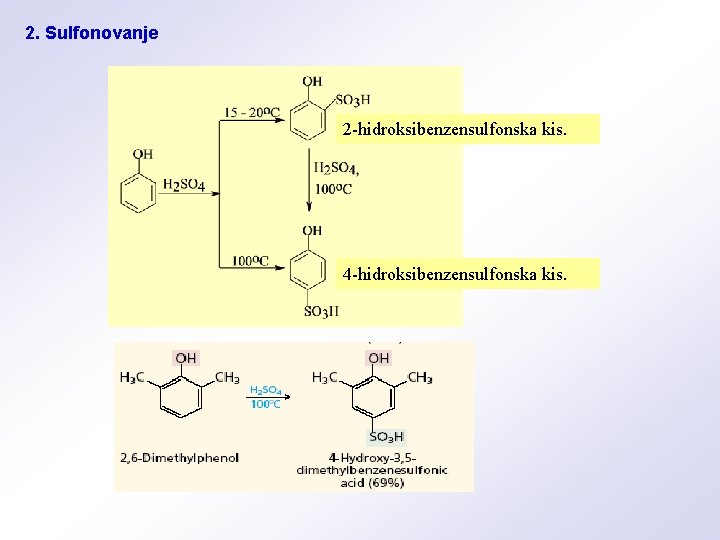
2. Sulfonovanje 2 -hidroksibenzensulfonska kis. 4 -hidroksibenzensulfonska kis.
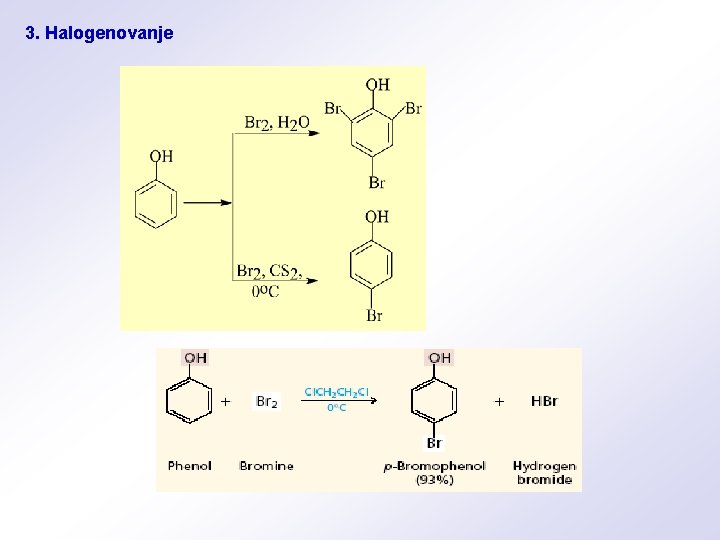
3. Halogenovanje
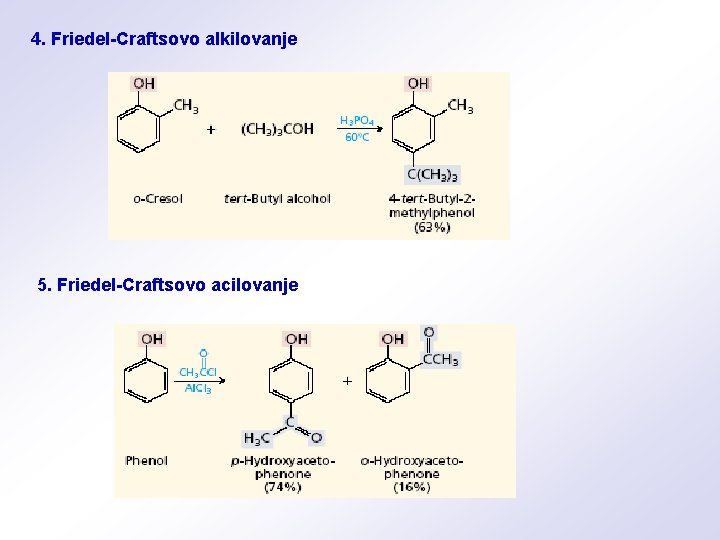
4. Friedel-Craftsovo alkilovanje 5. Friedel-Craftsovo acilovanje
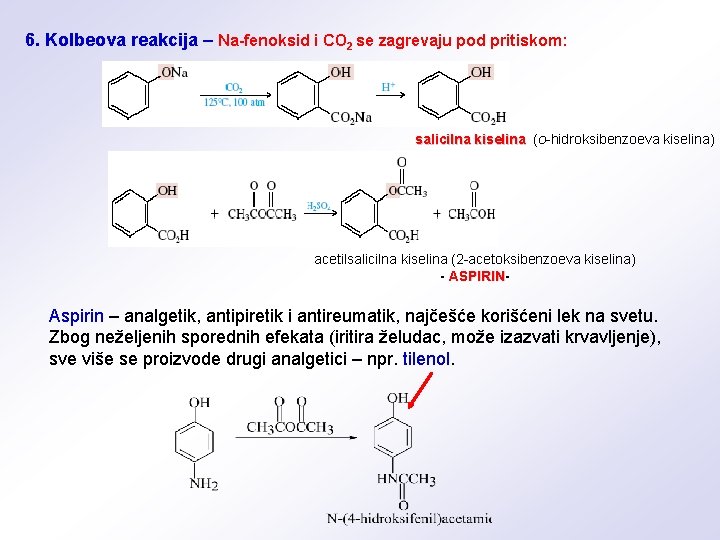
6. Kolbeova reakcija – Na-fenoksid i CO 2 se zagrevaju pod pritiskom: salicilna kiselina (o-hidroksibenzoeva kiselina) acetilsalicilna kiselina (2 -acetoksibenzoeva kiselina) - ASPIRIN Aspirin – analgetik, antipiretik i antireumatik, najčešće korišćeni lek na svetu. Zbog neželjenih sporednih efekata (iritira želudac, može izazvati krvavljenje), sve više se proizvode drugi analgetici – npr. tilenol.
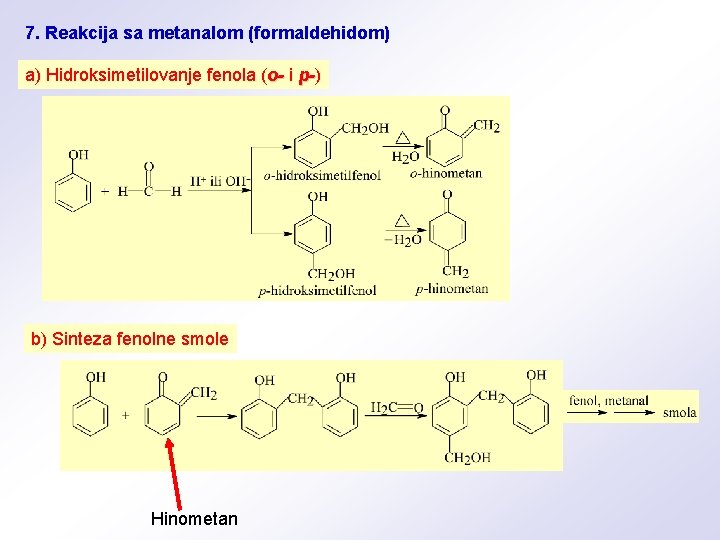
7. Reakcija sa metanalom (formaldehidom) a) Hidroksimetilovanje fenola (o- i p-) p- b) Sinteza fenolne smole Hinometan
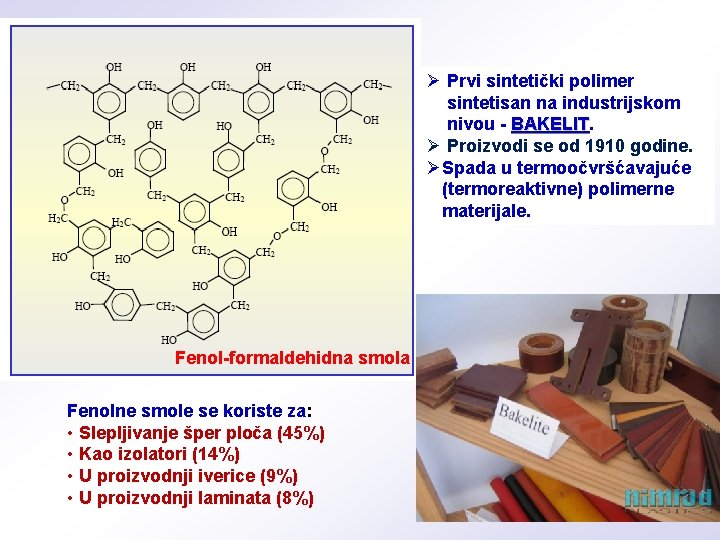
Ø Prvi sintetički polimer sintetisan na industrijskom nivou - BAKELIT Ø Proizvodi se od 1910 godine. ØSpada u termoočvršćavajuće (termoreaktivne) polimerne materijale. Fenol-formaldehidna smola Fenolne smole se koriste za: • Slepljivanje šper ploča (45%) • Kao izolatori (14%) • U proizvodnji iverice (9%) • U proizvodnji laminata (8%)
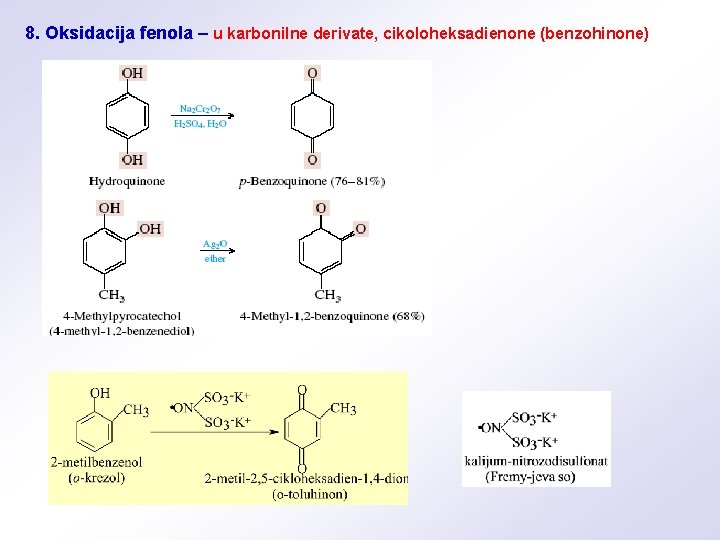
8. Oksidacija fenola – u karbonilne derivate, cikoloheksadienone (benzohinone)
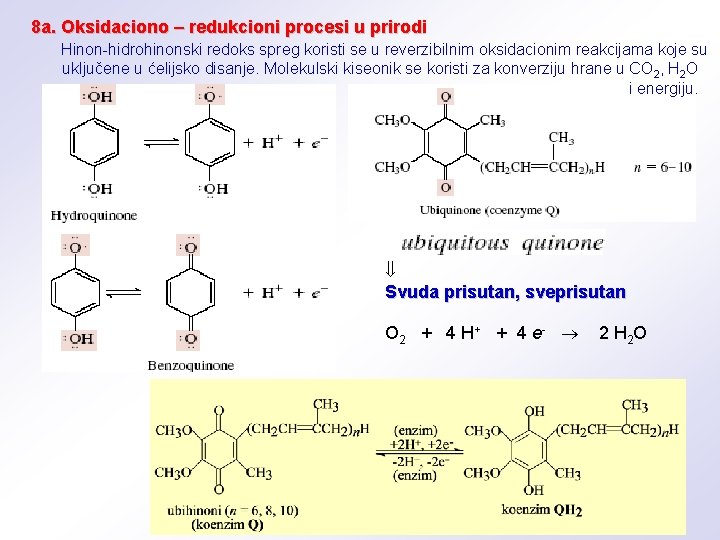
8 a. Oksidaciono – redukcioni procesi u prirodi Hinon-hidrohinonski redoks spreg koristi se u reverzibilnim oksidacionim reakcijama koje su uključene u ćelijsko disanje. Molekulski kiseonik se koristi za konverziju hrane u CO 2, H 2 O i energiju. Svuda prisutan, sveprisutan O 2 + 4 H + + 4 e- 2 H 2 O
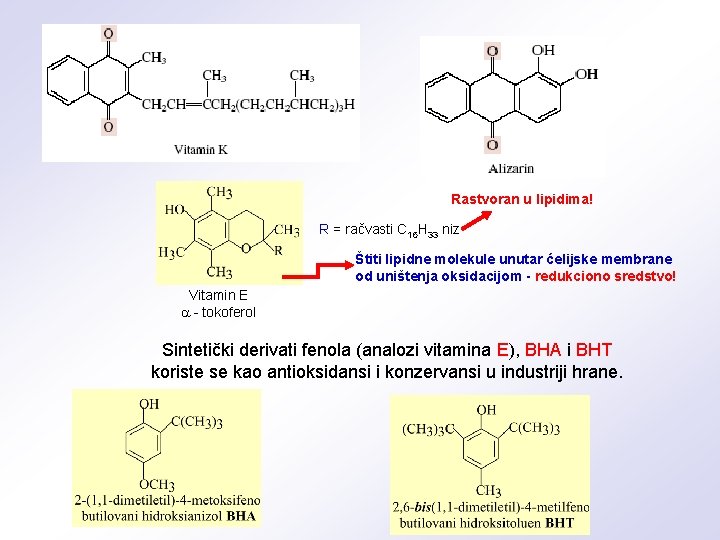
Rastvoran u lipidima! R = račvasti C 16 H 33 niz Štiti lipidne molekule unutar ćelijske membrane od uništenja oksidacijom - redukciono sredstvo! Vitamin E - tokoferol Sintetički derivati fenola (analozi vitamina E), BHA i BHT koriste se kao antioksidansi i konzervansi u industriji hrane.
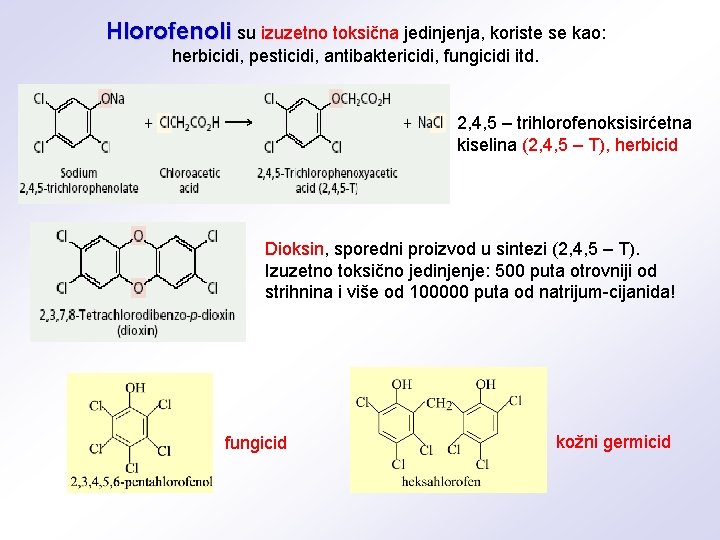
Hlorofenoli su izuzetno toksična jedinjenja, koriste se kao: herbicidi, pesticidi, antibaktericidi, fungicidi itd. 2, 4, 5 – trihlorofenoksisirćetna kiselina (2, 4, 5 – T), herbicid Dioksin, sporedni proizvod u sintezi (2, 4, 5 – T). Izuzetno toksično jedinjenje: 500 puta otrovniji od strihnina i više od 100000 puta od natrijum-cijanida! fungicid kožni germicid
Nomenklarura Prirodni i sintetički fenoli Fizičke osobine FENOLI Reakcije: Kao alkohola, EAS, oksidacije Struktura i kiselost Dobijanje: Industrijsko, laboratorijsko
- Slides: 33