Fenole v Budowa fenoli v Homologi fenolu v

Fenole v Budowa fenoli v Homologi fenolu v Otrzymywanie fenolu v Dysocjacja elektrolityczna fenolu v Nitrowanie fenoli v Alkilowanie fenoli v Halogenowanie fenoli v Fenolany, estry fenoli, wykrywanie fenolu
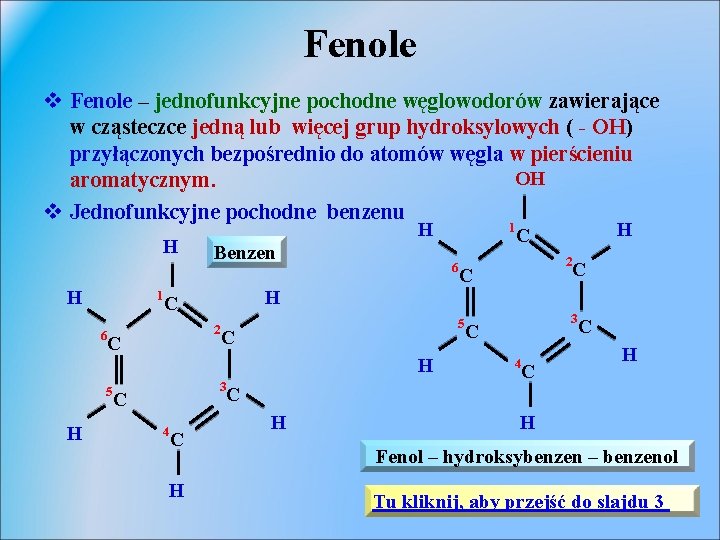
Fenole v Fenole – jednofunkcyjne pochodne węglowodorów zawierające w cząsteczce jedną lub więcej grup hydroksylowych ( - OH) przyłączonych bezpośrednio do atomów węgla w pierścieniu OH aromatycznym. v Jednofunkcyjne pochodne benzenu H H 1 6 H Benzen 6 2 C H 3 C 4 C H 2 C 5 H C C 1 3 C 4 C C H H Fenol – hydroksybenzen – benzenol Tu kliknij, aby przejść do slajdu 3
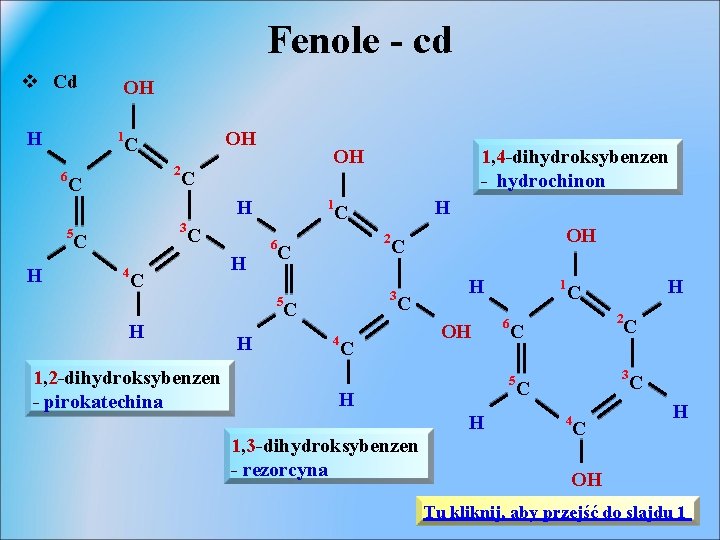
Fenole - cd v Cd H OH 1 6 OH C 2 C OH C H 5 H 3 C 4 1, 4 -dihydroksybenzen - hydrochinon C C 1 6 H H 1, 2 -dihydroksybenzen - pirokatechina H 2 C 5 H C 3 C 4 OH C C C H OH 1 6 H H 1, 3 -dihydroksybenzen - rezorcyna 2 C 5 H C C 3 C 4 C C H OH Tu kliknij, aby przejść do slajdu 1
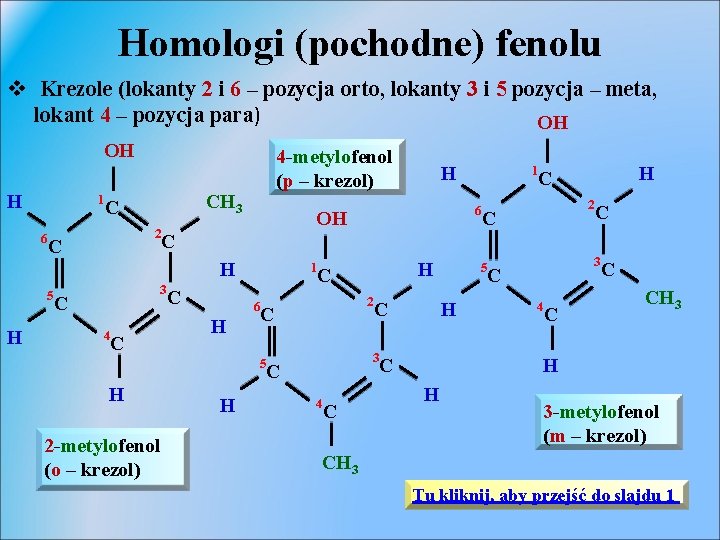
Homologi (pochodne) fenolu v Krezole (lokanty 2 i 6 – pozycja orto, lokanty 3 i 5 pozycja – meta, lokant 4 – pozycja para) OH OH H 1 6 CH 3 C 2 C 4 -metylofenol (p – krezol) H 4 C C 1 6 H 2 -metylofenol (o – krezol) H H C 2 C 5 H H C 2 C C C 3 C 1 6 OH H 5 H C 4 C H C 3 5 3 C 4 C C CH 3 H C H 3 -metylofenol (m – krezol) CH 3 Tu kliknij, aby przejść do slajdu 1
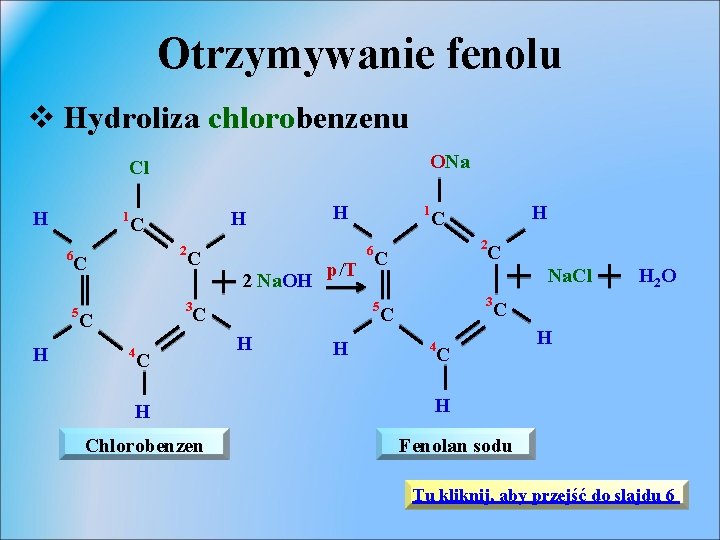
Otrzymywanie fenolu v Hydroliza chlorobenzenu ONa Cl H 1 6 H C 2 C 5 H 2 Na. OH C 4 p/T H Chlorobenzen H H H C 2 C 5 C C 1 6 C 3 H C Na. Cl 3 C 4 H 2 O C C H H Fenolan sodu Tu kliknij, aby przejść do slajdu 6
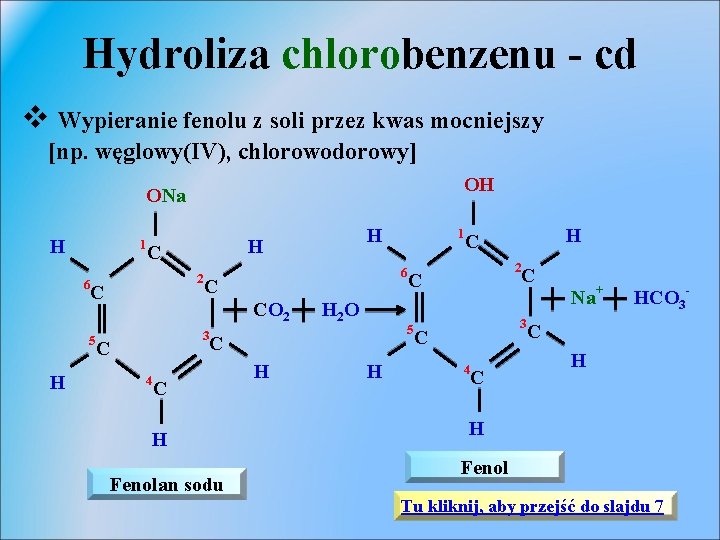
Hydroliza chlorobenzenu - cd v Wypieranie fenolu z soli przez kwas mocniejszy [np. węglowy(IV), chlorowodorowy] OH ONa H 1 6 5 H H C 2 C C 3 4 H 2 O H Fenolan sodu H H H C 2 C 5 C C 1 6 CO 2 C H C 3 C 4 C Na+ HCO 3 - C H H Fenol Tu kliknij, aby przejść do slajdu 7
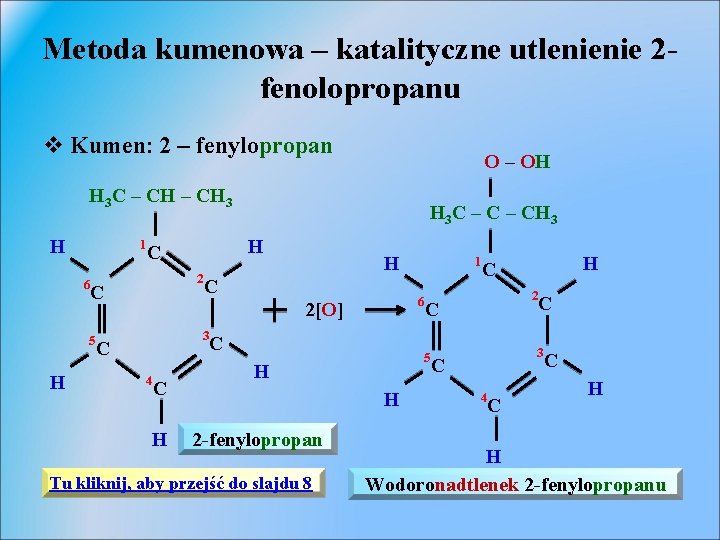
Metoda kumenowa – katalityczne utlenienie 2 fenolopropanu v Kumen: 2 – fenylopropan O – OH H 3 C – CH 3 H 1 6 5 H H C 2 C H 3 C – CH 3 H C 6 2[O] 3 C 4 C H Tu kliknij, aby przejść do slajdu 8 H C 2 C 5 H 2 -fenylopropan 1 C 3 C 4 C C H H Wodoronadtlenek 2 -fenylopropanu
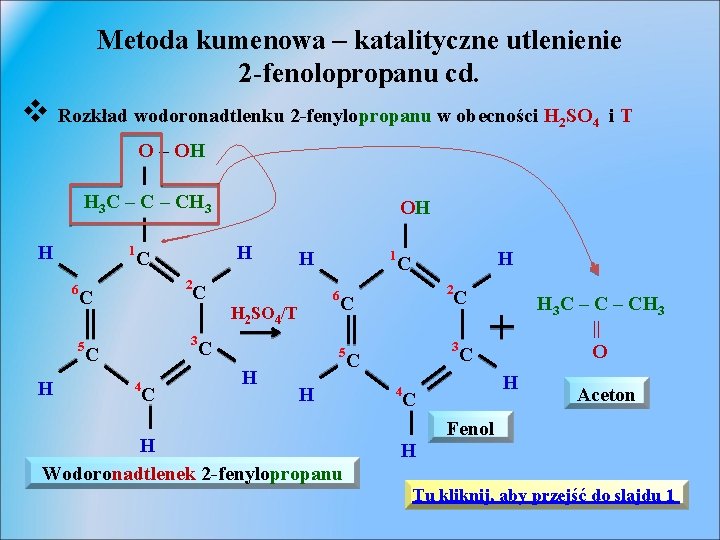
Metoda kumenowa – katalityczne utlenienie 2 -fenolopropanu cd. v Rozkład wodoronadtlenku 2 -fenylopropanu w obecności H 2 SO 4 i. T O – OH H 3 C – CH 3 H 1 6 5 H H C 2 C OH H C 6 H 2 SO 4/T 3 C 4 C 1 C 2 C 5 H H C H H Wodoronadtlenek 2 -fenylopropanu C 3 C 4 H 3 C – CH 3 || O C H C Aceton Fenol H Tu kliknij, aby przejść do slajdu 1
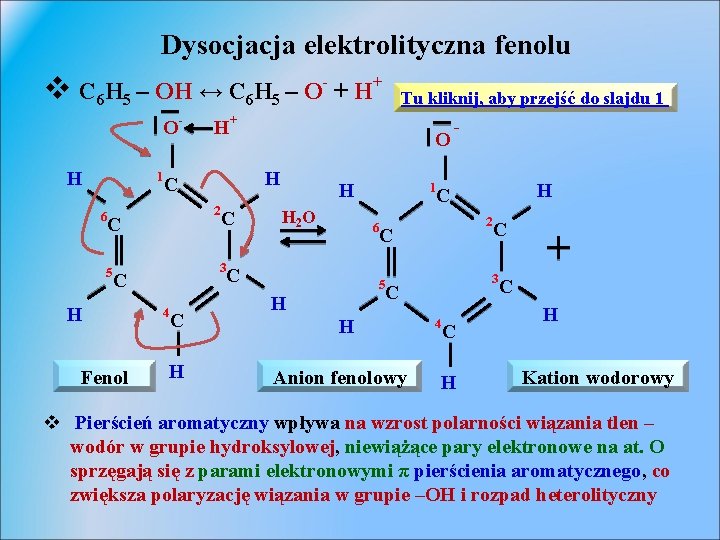
Dysocjacja elektrolityczna fenolu v C 6 H 5 – OH ↔ C 6 H 5 – O- + H+ O H 1 6 - 5 Fenol C 3 4 C H O H 2 C H H+ C C Tu kliknij, aby przejść do slajdu 1 H H 2 O 1 6 C 2 Anion fenolowy C 3 C H H C C 5 H - 4 C H Kation wodorowy v Pierścień aromatyczny wpływa na wzrost polarności wiązania tlen – wodór w grupie hydroksylowej, niewiążące pary elektronowe na at. O sprzęgają się z parami elektronowymi π pierścienia aromatycznego, co zwiększa polaryzację wiązania w grupie –OH i rozpad heterolityczny
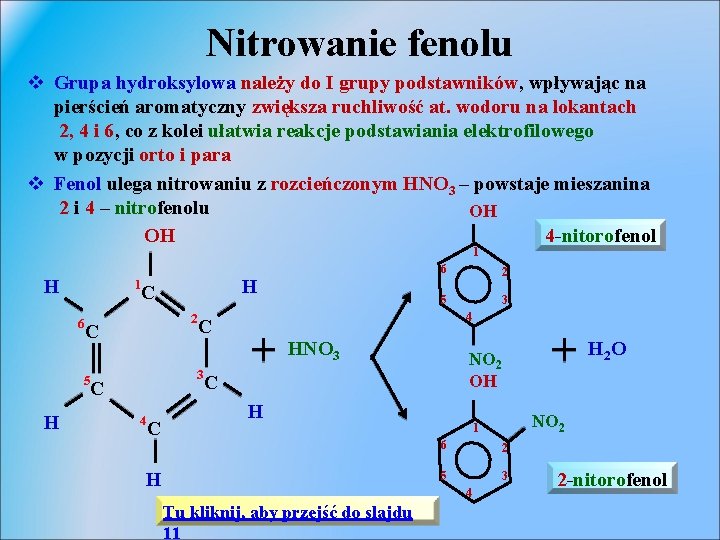
Nitrowanie fenolu v Grupa hydroksylowa należy do I grupy podstawników, wpływając na pierścień aromatyczny zwiększa ruchliwość at. wodoru na lokantach 2, 4 i 6, co z kolei ułatwia reakcje podstawiania elektrofilowego w pozycji orto i para v Fenol ulega nitrowaniu z rozcieńczonym HNO 3 – powstaje mieszanina 2 i 4 – nitrofenolu OH OH 4 -nitorofenol 1 H 1 6 H 2 C 5 H C 6 2 5 3 4 C HNO 3 3 C 4 C C H H NO 2 1 6 2 5 3 4 Tu kliknij, aby przejść do slajdu 11 H 2 O NO 2 OH 2 -nitorofenol
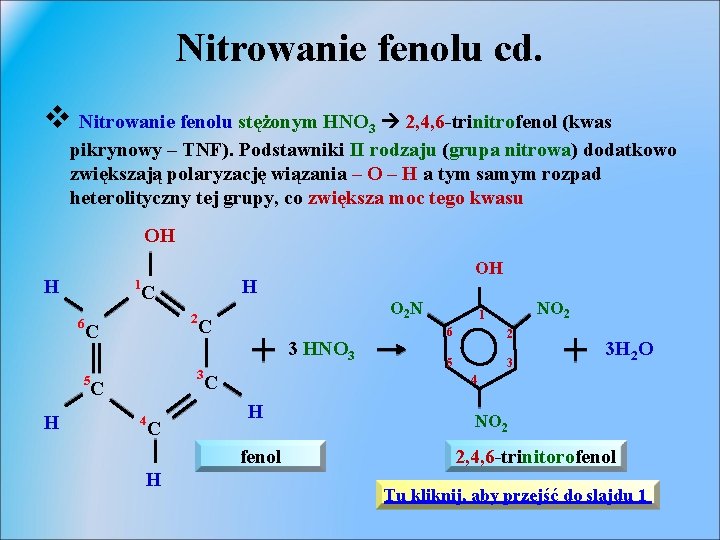
Nitrowanie fenolu cd. v Nitrowanie fenolu stężonym HNO 3 2, 4, 6 -trinitrofenol (kwas pikrynowy – TNF). Podstawniki II rodzaju (grupa nitrowa) dodatkowo zwiększają polaryzację wiązania – O – H a tym samym rozpad heterolityczny tej grupy, co zwiększa moc tego kwasu OH H 1 6 5 H H C 2 C OH O 2 N C 3 HNO 3 3 C 4 C C 6 2 5 3 3 H 2 O 4 H fenol H NO 2 1 NO 2 2, 4, 6 -trinitorofenol Tu kliknij, aby przejść do slajdu 1
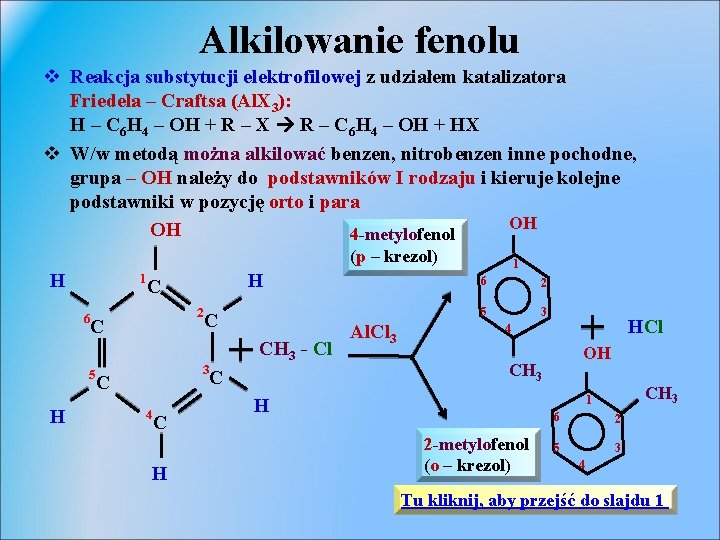
Alkilowanie fenolu v Reakcja substytucji elektrofilowej z udziałem katalizatora Friedela – Craftsa (Al. X 3): H – C 6 H 4 – OH + R – X R – C 6 H 4 – OH + HX v W/w metodą można alkilować benzen, nitrobenzen inne pochodne, grupa – OH należy do podstawników I rodzaju i kieruje kolejne podstawniki w pozycję orto i para OH OH 4 -metylofenol (p – krezol) H 1 6 H 2 C 5 H C C 3 C 4 C H CH 3 - Cl C Al. Cl 3 1 6 2 5 3 HCl 4 OH CH 3 1 H 2 -metylofenol (o – krezol) 6 2 5 3 4 Tu kliknij, aby przejść do slajdu 1
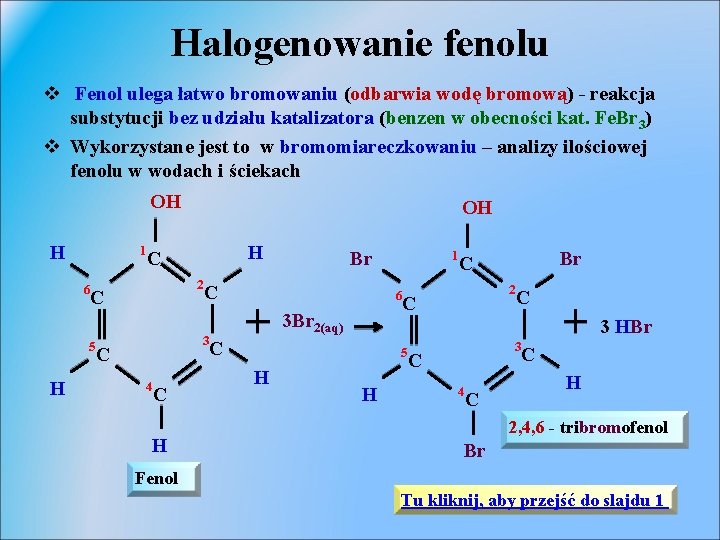
Halogenowanie fenolu v Fenol ulega łatwo bromowaniu (odbarwia wodę bromową) - reakcja substytucji bez udziału katalizatora (benzen w obecności kat. Fe. Br 3) v Wykorzystane jest to w bromomiareczkowaniu – analizy ilościowej fenolu w wodach i ściekach OH H 1 6 H H C 2 C 5 OH C 3 C 4 C H Br 1 6 3 Br 2(aq) 2 C C 3 HBr C 5 H Br C H 3 C 4 C C H 2, 4, 6 - tribromofenol Br Fenol Tu kliknij, aby przejść do slajdu 1

Fenolany, estry fenolu, wykrywanie fenolu v Fenole reagują z zasadami, powstają sole fenolany, które ulegają hydrolizie anionowej, odczyn wodnego roztworu fenolanów jest zasadowy Ø C 6 H 5 -OH + Na. OH ↔ C 6 H 5 -ONa + H 2 O Ø C 6 H 5 -O- + Na+ + H 2 O ↔ C 6 H 5 -OH + Na+ + OH Ø C 6 H 5 -O- + H 2 O ↔ C 6 H 5 -OH + OH v Fenole w reakcji z kwasami karboksylowymi tworzą estry O H+ // v CH 3 – COOH + HO – C 6 H 5 ↔ CH 3 – C - O – C 6 H 5 + H 2 O kwas etanowy + fenol ↔ etanian fenylu + woda v Fenol w reakcji z solami żelaza(III) daje związek kompleksowy barwy niebieskofioletowej lub czerwonej
- Slides: 14