Fenole Budowa fenoli Homologi fenolu Nazewnictwo fenoli Waciwoci

Fenole Budowa fenoli Homologi fenolu Nazewnictwo fenoli Właściwości chemiczne i fizyczne Zastosowanie
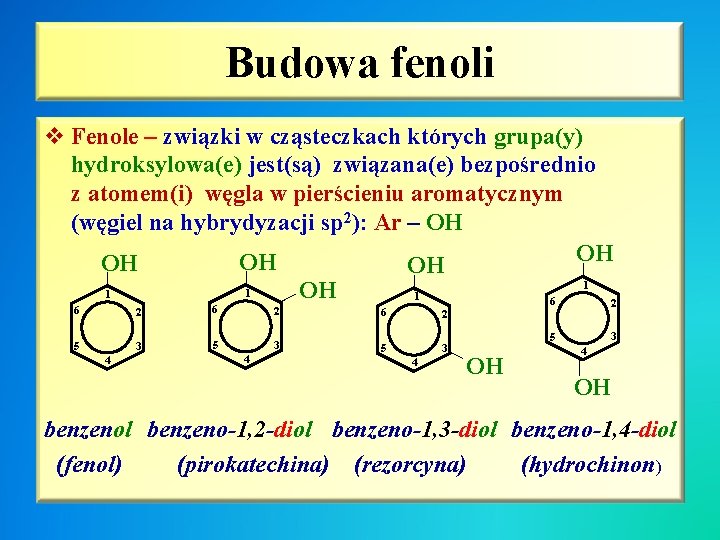
Budowa fenoli v Fenole – związki w cząsteczkach których grupa(y) hydroksylowa(e) jest(są) związana(e) bezpośrednio z atomem(i) węgla w pierścieniu aromatycznym (węgiel na hybrydyzacji sp 2): Ar – OH OH OH | | OH 1 1 | | 6 2 6 2 5 3 5 3 4 4 4 2 3 5 | 6 OH 4 | OH benzenol benzeno-1, 2 -diol benzeno-1, 3 -diol benzeno-1, 4 -diol (fenol) (pirokatechina) (rezorcyna) (hydrochinon)
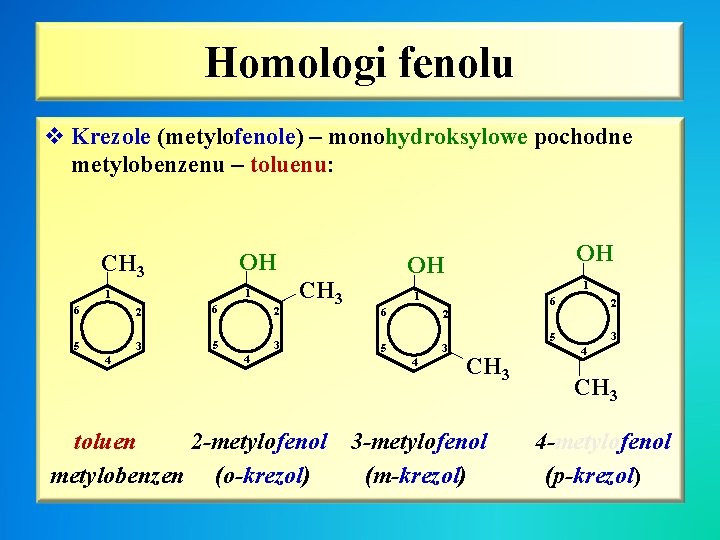
Homologi fenolu v Krezole (metylofenole) – monohydroksylowe pochodne metylobenzenu – toluenu: OH CH 3 | | 2 6 2 5 3 4 toluen 2 -metylofenol metylobenzen (o-krezol) 1 1 6 6 2 5 3 4 2 3 5 | 6 4 CH 3 | | | 1 1 OH OH CH 3 3 -metylofenol (m-krezol) 4 | CH 3 4 -metylofenol (p-krezol)

Otrzymywanie fenolu C 6 H 5 -OH v Naturalnym źródłem jest smoła pogazowa otrzymywana w procesie koksowania węgla kamiennego. v Na skalę przemysłową fenole otrzymuje się w hydrolizie zasadowej halogenków arylowych (Ar – X) w podwyższonej temp. , ciśnieniu i obecności katalizatora Ø C 6 H 5 – Cl + 2 Na. OH(aq) C 6 H 5 – ONa + Na. Cl + H 2 O chlorofenolan sodu Ø fenolan sodu podaje rozkładowi kwasem HCl lub wodą nasycaną CO 2 Ø C 6 H 5 – ONa + HCl C 6 H 5 – OH + Na. Cl Ø C 6 H 5 – ONa + CO 2 + H 2 O C 6 H 5 – OH + Na. HCO 3
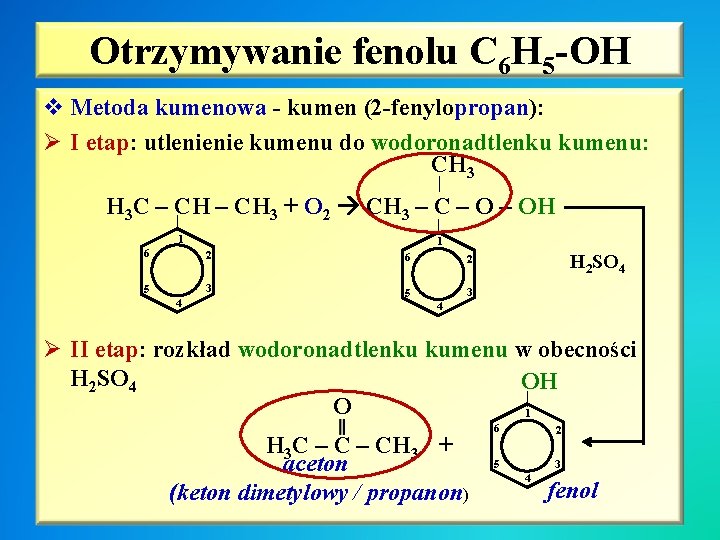
Otrzymywanie fenolu C 6 H 5 -OH v Metoda kumenowa - kumen (2 -fenylopropan): Ø I etap: utlenienie kumenu do wodoronadtlenku kumenu: CH 3 | H 3 C – CH 3 + O 2 CH 3 – C – OH | | 1 6 5 4 1 2 6 3 5 H 2 SO 4 2 3 4 Ø II etap: rozkład wodoronadtlenku kumenu w obecności H 2 SO 4 OH | O 1 H 3 C – CH 3 + aceton (keton dimetylowy / propanon) 6 2 5 3 4 fenol

Właściwości fizyczne fenolu v Fenol: Ø substancja stała, krystaliczna, bezbarwna, pod wpływem tlenu różowieje, higroskopijna, o charakterystycznej nieprzyjemnej woni, Ø toksyczny, ma właściwości żrące, w zimnej wodzie rozpuszcza się słabo, w temp. 70 o. C rozpuszcza się bez ograniczeń, Ø wodny roztwór fenolu wykazuje słaby odczyn kwasowy, co wskazuje, że ulega dysocjacji elektrolitycznej, Ka ≈ 1, 3 ٠ 10 -10: ü C 6 H 5 – OH + H 2 O ↔ C 6 H 5 – O- + H 3 O+ Ø dysocjacja jest efektem oddziaływania pierścienia aromatycznego na polaryzację wiązania O – H i jego osłabienie, to z kolei umożliwia odszczepienie kationu H+.

Właściwości chemiczne fenolu v Reakcja z metalami – powstają fenolany i wypierany jest wodór: Ø 2 C 6 H 5 – OH + 2 Na 2 C 6 H 5 – ONa + H 2 fenolan sodu Ø 2 C 6 H 5 – OH + Mg (C 6 H 5 – O)2 Mg + H 2 fenolan magnezu v Reakcja z wodnymi roztworami zasad – reakcje zobojętniania: Ø 2 C 6 H 5 – OH + Ca(OH)2 (C 6 H 5 – O)2 Ca + 2 H 2 O fenolan wapnia Ø C 6 H 5 – OH + KOH C 6 H 5 – OK + H 2 O fenolan potasu v Fenol jest wypierany z fenolanów przez mocniejsze kwasy, nawet prze kwas węglowy(IV). v Reakcje z kwasami karboksylowymi – powstają estry.

Właściwości chemiczne fenolu v Reakcje fenolu na pierścieniu aromatycznym: Ø fenol daje takie same reakcje jak benzen, Ø grupa – OH należy do podstawników I rodzaju i w reakcjach substytucji, oraz nitrowania kieruje kolejne podstawniki w pozycje orto i para: v Reakcja substytucji wodoru na pierścieniu aromatycznym bromem – powstaje 2, 4, 6 -tribromofenol i bromowodór. v Reakcja nitrowania (reakcja zachodzi nawet z rozcieńczonym HNO 3), produktem jest mieszanina o-nitrofenolu i p-nitrofenolu. . v Wykrywanie fenolu – z Fe. Cl 3 fenol tworzy związek kompleksowy barwy niebieskofioletowej.

Zastosowanie fenolu v Substrat wyjściowy do produkcji: Ø tworzyw sztucznych, żywic – żywica fenyloformaldehydowa, stosowana do produkcji farb, barwników, lakierów, Ø produkcja materiałów wybuchowych - kwas pikrynowy (2, 4, 6 -trinitrofenol): ü substancja stała w postaci żółtych płatków, o silnych właściwościach kwasowych i gorzkim smaku, nierozpuszczalna w wodzie, miesza się z alkoholem, eterem, toksyczna, ü jest silnym materiałem wybuchowym, wybucha powyżej temp. topnienia Tt = 123 o. C lub w zetknięciu z metalami i ich tlenkami lub w skutek uderzenia.

Zastosowanie fenolu v Substrat wyjściowy do produkcji – cd. : Ø krezole nie wykazują tak silnych właściwości toksycznych jak fenol, ü zachowują właściwości (bakteriobójcze) dezynfekujące, stąd zastosowanie są do produkcji mydeł krezolowych (lizol), stosowanych jako środki dezynfekcyjne.
- Slides: 10