Valenn elektrony a chemick vazba Ve vnj energetick

Valenční elektrony a chemická vazba • Ve vnější energetické hladině se nacházejí valenční elektrony, které se mohou podílet na tvorbě chemické vazby. • Valenční elektrony často znázorňujeme pomocí teček kolem značky prvku (= Lewisova struktura). • Existují tři základní typy chemické vazby: - Iontová vazba, založená na elektrostatickém přitahování opačně nabitých iontů (Na. Cl) - Kovalentní vazba, která vzniká sdílením jednoho nebo více valenčních elektronů (Cl 2) - Kovová vazba, u které jsou valenční elektrony sdíleny více atomy v krystalické mřížce kovu (Ag)

Zápis valenčních elektronů v Lewisově symbolice

Iontová vazba • Ve sloučenině s iontovou vazbou existují kladně a záporně nabité ionty (kationty a anionty), které si navzájem kompenzují náboj – sloučenina musí být elektroneutrální. • Sloučeniny s iontovou vazbou jsou typicky soli, tvořící za běžných podmínek krystaly s vysokou teplotou tání. • Iontovou vazbu lze chápat jako kombinaci neutrálních atomů, při které dojde k transferu jednoho nebo více elektronů od jednoho atomu k druhému (popř. k několika).
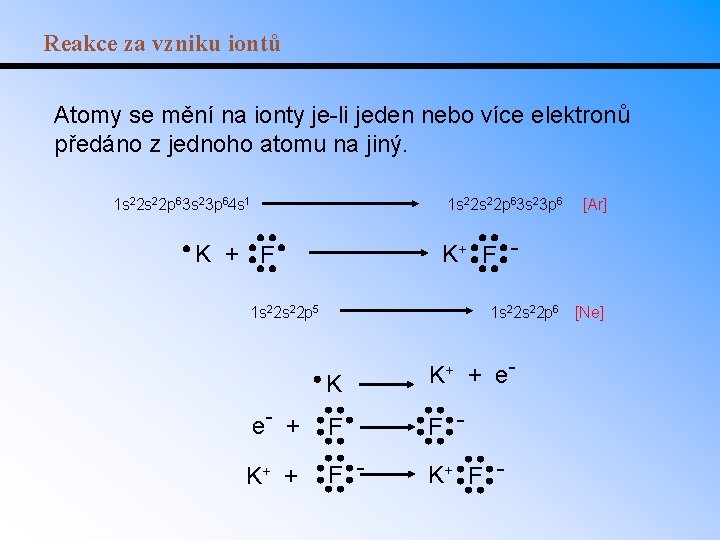
Reakce za vzniku iontů Atomy se mění na ionty je-li jeden nebo více elektronů předáno z jednoho atomu na jiný. 1 s 22 p 63 s 23 p 64 s 1 1 s 22 p 63 s 23 p 6 [Ar] K+ F - K + F 1 s 22 p 5 1 s 22 p 6 [Ne] K K+ + e- e- + F F - K+ + F - K+ F -

Oktetové pravidlo • Elektronová konfigurace mnoha iontů odpovídá konfiguraci vzácného plynu. • Oktetové pravidlo: Prvky hlavní skupiny (s a p) přijímají, ztrácejí nebo sdílí elektrony tak, aby dosáhly valenčního oktetu (osm elektronů ve zcela zaplněné valenční slupce). • Např. elektronová konfigurace obou částic v KCl je: – K+ má konfiguraci [Ar] – Cl má konfiguraci [Ar] • Další elektrony v atomu se obvykle chemické vazby neúčastní. • Oktetové pravidlo je zvláště důležité u sloučenin s nekovy.

Energie iontové vazby • Když se přiblíží draslíkový a chlorový atom, dojde k výměně elektronu: K(g) K+(g) + e Ei = +418 k. J Cl(g)+ e Cl (g) Eea = 349 k. J K(g)+Cl(g) K+(g) + Cl (g) E = + 69 k. J • Pozitivní energie E reakce není energeticky přípustná (neproběhne samovolně). • Hybnou silou procesu tudíž musí být tvorba krystalické tuhé fáze: K+(g) + Cl (g) KCl(s)

Bornův-Haberův cyklus a mřížková energie • Celková energetická změna při vzniku krystalické fáze může být určena z Bornova-Haberova cyklu, který zahrnuje všechny postupné kroky při vzniku krystalu z prvků. Např. pro krystalický KCl najdeme: 1. Sublimace draslíku 2. Disociace chloru 3. Ionizace draslíku (Ei) 4. Vznik Cl- aniontu (Eea) 5. Vznik tuhého KCl Suma reakcí a energií • Celková energie 434 k. J/mol potvrzuje že jde o energeticky výhodný proces. • Energie 5. kroku je (záporná) mřížková energie. • Mřížková energie: energie potřebná k rozrušení iontové vazby a sublimaci iontů (je vždy kladná). Př. : Určete mřížkovou energii Ba. Cl 2 je-li sublimační entalpie Ba 150. 9 k. J/mol, jeho 1. a 2. ionizační energie 502, resp. 966 k. J/mol. Slučovací entalpie Ba. Cl 2(s) z prvků je 806. 06 k. J/mol.
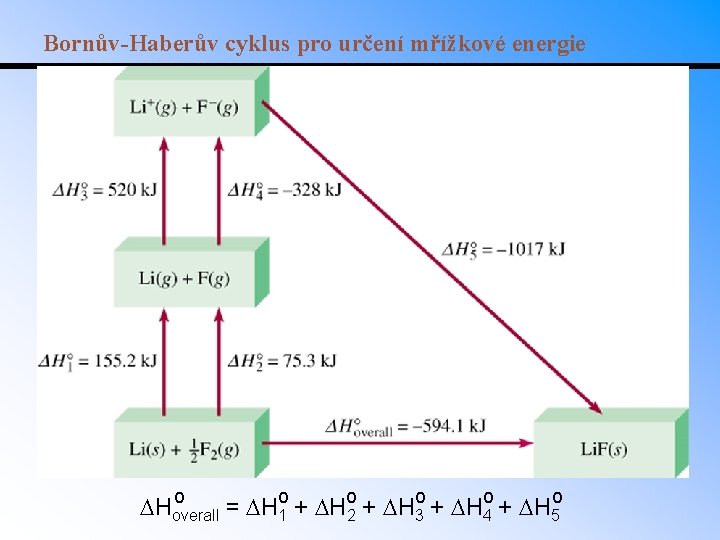
Bornův-Haberův cyklus pro určení mřížkové energie o Hoverall = Ho 1 + Ho 2 + H 3 o + H 4 o + H 5 o

Kovalentní vazba • Odpudivé síly mezi elektrony mohou být překonány přitažlivými silami elektronů a dvou atomových jader. • Stabilní vazba vznikne v uspořádání s nejnižší energií (nižší než odpovídá dvěma separovaným atomům). • Pevnost kovalentní vazby: • Porušení vazby zvýší celkovou energii systému, k tomuto účelu tedy musí být energie dodána zvenčí. H - H (g) 2 H(g) H = 432 k. J • Látky s iontovou vs. kovalentní vazbou – Iontové látky mají vysoký bod tání a varu a za běžných podmínek bývají krystalické; – Sloučeniny s kovalentní vazbou mají obvykle nižší bod tání a varu protože přitažlivé síly mezi molekulami jsou relativně slabé.

Možnosti vzniku kovalentní vazby • Oktet může být zaplněn sdílenými elektrony každého atomu nebo jeden z atomů může poskytnout oba vazebné elektrony. Př. : H+ + NH 3 koordinačně-kovalentní vazba • Pokud atomy tvořící vazbu nemají k dispozici dostatek elektronů, může vzniknout násobná vazba. – O=O – N N • Násobné vazby jsou kratší a silnější než vazby jednoduché.

Lewisovy struktury víceatomových molekul • Procedura u komplikovanějších molekul: – Určit celkový počet valenčních elektronů každého atomu. – Shromáždit atomy kolem centrálního atomu (tj. atomu s nejnižší elektronegativitou). – Naplnit oktet u atomů vázaných na centrální atom. – Naplnit oktet u centrálního atomu přiřazením zbylých elektronů do nevazebných elektronových párů, případně doplnit násobné vazby.
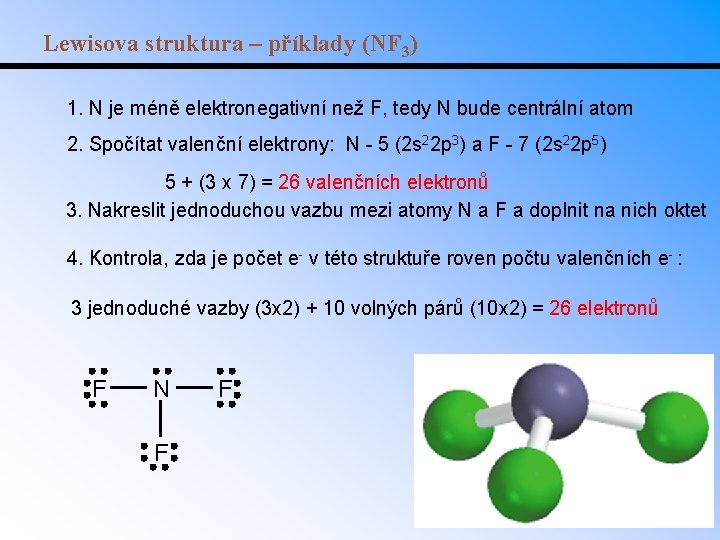
Lewisova struktura – příklady (NF 3) 1. N je méně elektronegativní než F, tedy N bude centrální atom 2. Spočítat valenční elektrony: N - 5 (2 s 22 p 3) a F - 7 (2 s 22 p 5) 5 + (3 x 7) = 26 valenčních elektronů 3. Nakreslit jednoduchou vazbu mezi atomy N a F a doplnit na nich oktet 4. Kontrola, zda je počet e- v této struktuře roven počtu valenčních e- : 3 jednoduché vazby (3 x 2) + 10 volných párů (10 x 2) = 26 elektronů F N F F

Lewisova struktura – příklady (CO 32 -) 1. C je méně elektronegativní než O, tedy C bude centrální atom 2. Spočítat valenční elektrony: C - 4 (2 s 22 p 2) a O - 6 (2 s 22 p 4), náboj - 2 4 + (3 x 6) + 2 = 24 valenčních elektronů 3. Nakreslit jednoduchou vazbu mezi atomy C a O a doplnit na nich oktet 4. Kontrola, zda je počet e- v této struktuře roven počtu valenčních e- : 3 jednoduché vazby (3 x 2) + 10 volných párů (10 x 2) = 26 elektronů O C O O

Lewisova struktura – příklady (CO 32 -) 1. C je méně elektronegativní než O, tedy C bude centrální atom 2. Spočítat valenční elektrony: C - 4 (2 s 22 p 2) a O - 6 (2 s 22 p 4), náboj - 2 4 + (3 x 6) + 2 = 24 valenčních elektronů 3. Nakreslit jednoduchou vazbu mezi atomy C a O a doplnit na nich oktet 4. Kontrola, zda je počet e- v této struktuře roven počtu valenčních e- : 3 jednoduché vazby (3 x 2) + 10 volných párů (10 x 2) = 26 elektronů 5. Příliš mnoho elektronů: doplnit násobnou vazbu a znovu zkontrolovat počet e 2 jednoduché vazby (2 x 2) = 4 1 dvojná vazby = 4 O C O 8 volných párů (8 x 2) = 16 O celkem = 24

Struktura a formální náboje • Formální náboj (atomu) je hypotetický náboj za předpokladu rovnoměrného sdílení elektronů v chemické vazbě. Volné elektronové páry patří k příslušnému atomu. • Znalost formálních nábojů umožňuje odhadnout pravděpodobnou strukturu a umístění násobných vazeb: – Formální náboje by měly být co nejbližší nule. – Případné záporné formální náboje by měly být u atomů s nejvyšší a kladné u atomů s nejnižší elektronegativitou.
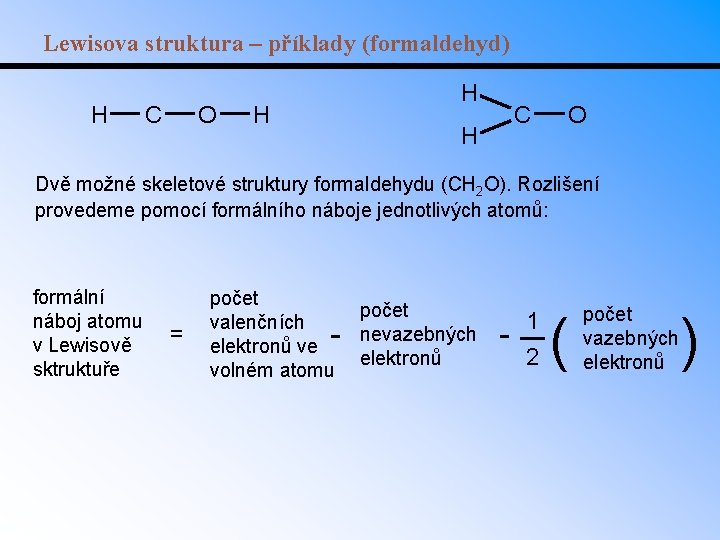
Lewisova struktura – příklady (formaldehyd) H C O H H C H O Dvě možné skeletové struktury formaldehydu (CH 2 O). Rozlišení provedeme pomocí formálního náboje jednotlivých atomů: formální náboj atomu v Lewisově sktruktuře = počet valenčních elektronů ve volném atomu - počet nevazebných elektronů - 1 2 ( počet vazebných elektronů )

Lewisova struktura – příklady (formaldehyd) H -1 +1 C O formální náboj atomu v Lewisově sktruktuře = H C – 4 e. O – 6 e 2 H – 2 x 1 e 12 e- počet valenčních elektronů ve volném atomu - 2 jednoduché v. (2 x 2) = 4 1 dvojná v. = 4 2 volné páry (2 x 2) = 4 celkem = 12 počet nevazebných elektronů formální náboj na C = 4 -2 - ½ x 6 = -1 formální náboj na O = 6 -2 - ½ x 6 = +1 - 1 2 ( počet vazebných elektronů )
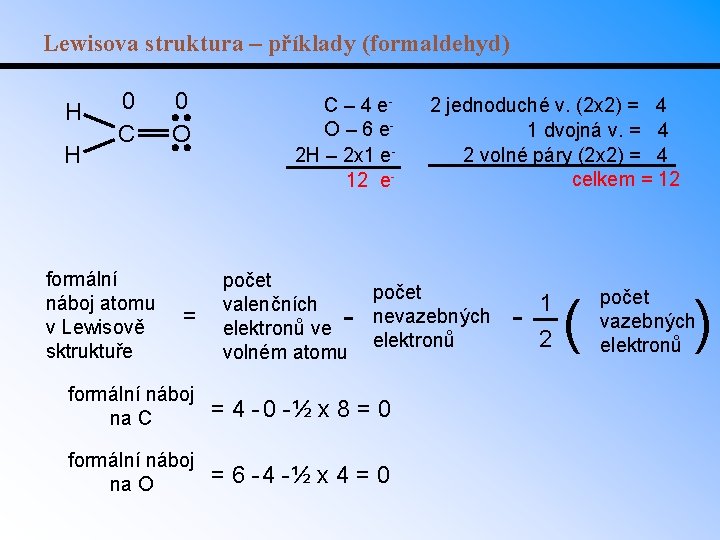
Lewisova struktura – příklady (formaldehyd) H H 0 C formální náboj atomu v Lewisově sktruktuře 0 O = C – 4 e. O – 6 e 2 H – 2 x 1 e 12 e- počet valenčních elektronů ve volném atomu - 2 jednoduché v. (2 x 2) = 4 1 dvojná v. = 4 2 volné páry (2 x 2) = 4 celkem = 12 počet nevazebných elektronů formální náboj na C = 4 - 0 - ½ x 8 = 0 formální náboj na O = 6 -4 - ½ x 4 = 0 - 1 2 ( počet vazebných elektronů )
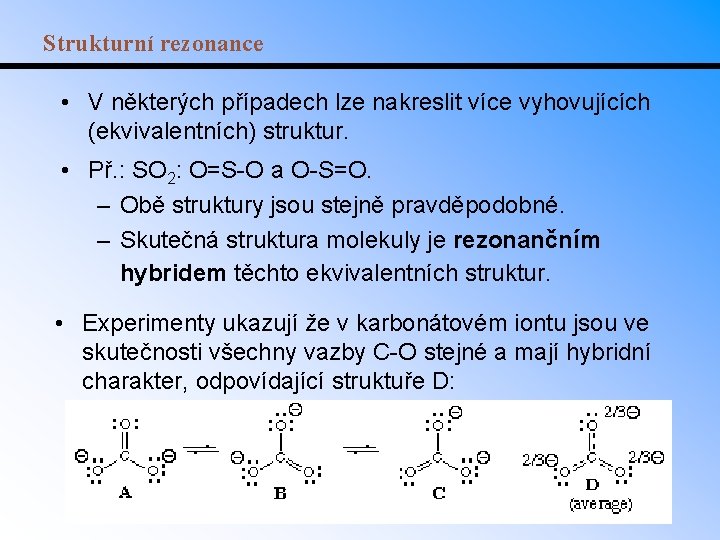
Strukturní rezonance • V některých případech lze nakreslit více vyhovujících (ekvivalentních) struktur. • Př. : SO 2: O=S-O a O-S=O. – Obě struktury jsou stejně pravděpodobné. – Skutečná struktura molekuly je rezonančním hybridem těchto ekvivalentních struktur. • Experimenty ukazují že v karbonátovém iontu jsou ve skutečnosti všechny vazby C-O stejné a mají hybridní charakter, odpovídající struktuře D:
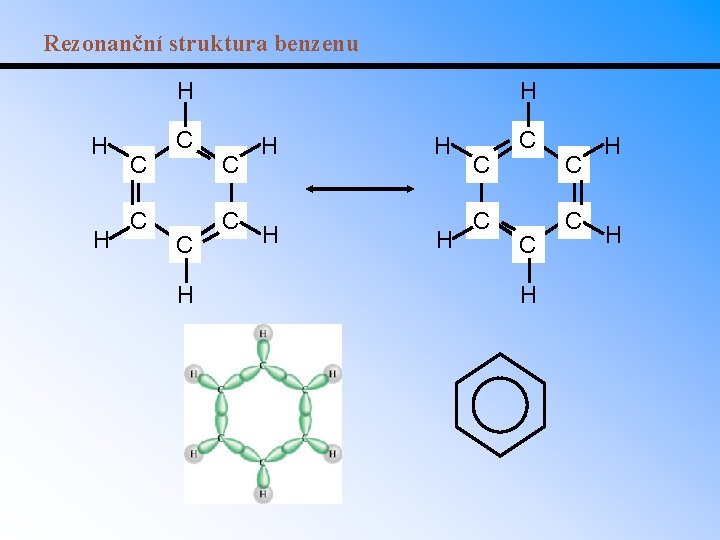
Rezonanční struktura benzenu H H H H C C C C H H

Výjimky z oktetového pravidla • Ačkoli mnoho molekul splňuje oktetové pravidlo, existují výjimky kdy centrální atom má jiný počet elektronů než 8. – Je-li centrální atom nekov ze třetí nebo vyšší periody, může být kolem shromážděno až 12 elektronů. – Tyto prvky mají nezaplněnou podslupku “d”, kterou mohou využít k vazbě.
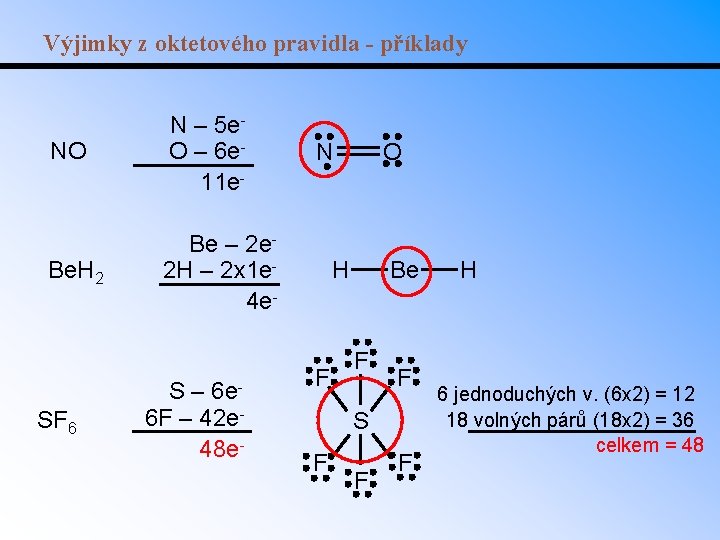
Výjimky z oktetového pravidla - příklady NO N – 5 e. O – 6 e 11 e- Be. H 2 Be – 2 e 2 H – 2 x 1 e 4 e- SF 6 S – 6 e 6 F – 42 e 48 e- N O H F Be F F S F F F H 6 jednoduchých v. (6 x 2) = 12 18 volných párů (18 x 2) = 36 celkem = 48

Disociační energie vazby • Disociační energie chemické vazby, D – energie potřebná k rozrušení jednoho molu příslušných vazeb v izolovaných molekulách v plynné fázi. • Disociační energie vazby je vždy kladná (k rozrušení vazby je nutné energii dodat). • Z vazebných energií lze odhadnout energetické změny neznámých reakcí vhodnou kombinací dílčích dějů a jim odpovídajících energetických změn (Hessův zákon).

Použití disociačních energií vazeb • Př. : Odhadněte slučovací teplo H 2 O(g) z vazebných energií: H 2(g) + ½ O 2(g) H 2 O(g) = ? Hodnoty vazebných energií z tabulek: H – H (g) 2 H(g) ½ O=O (g) O(g) H 1 = 432 k. J H 2 = 494/2 = 247 k. J 2 H(g) + O(g) H – O – H (g) 2 H 3 = 2*459 k. J H 2(g) + ½ O 2(g) H 2 O(g) H = 239 k. J experimentální hodnota H = 241. 8 k. J

Použití disociačních energií vazeb • Mezi dílčí procesy je často nezbytné zařadit fázovou změnu protože některé reaktanty nebo produkty nejsou plynné fázi. • Př. : Vypočítejte slučovací entalpii CCl 4(l). C(s) + 2 Cl 2(g) CCl 4(l) = ? • Dílčí reakce a jim odpovídající energie: C(s) 2 Cl – Cl(g) C(g) + 4 Cl(g) CCl 4(g) C(g) 4 Cl(g) CCl 4(l) C(s) + 2 Cl 2(g) CCl 4(l) H 1 = 715 k. J H 2 = 480 H 3 = 1308 H 4 = 43 H = 156 k. J exp. = 139 k. J
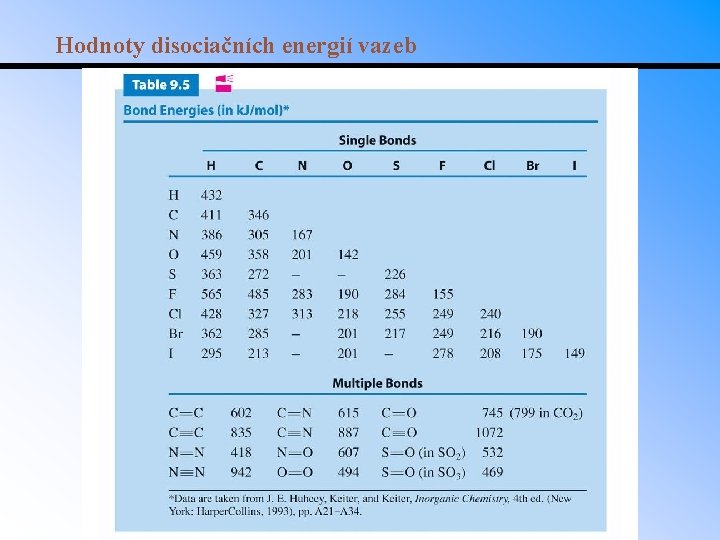
Hodnoty disociačních energií vazeb
- Slides: 26