TRATAMIENTO DE LAS NUSEAS Y VMITOS INDUCIDOS POR




























































- Slides: 79

TRATAMIENTO DE LAS NÁUSEAS Y VÓMITOS INDUCIDOS POR QUIMIOTERAPIA Eugenio Saigí Grau

N y V por QT en pacientes con cáncer • Aproximadamente 70%– 80% de pacientes con QT experimentan nauseas y vómitos • Las N y V representan uno de los efectos indeseables más frecuentes referidos por los pacientes sometidos a quimioterapia 1. Wiser W, Berger A. Oncology. 2005; 19: 637.

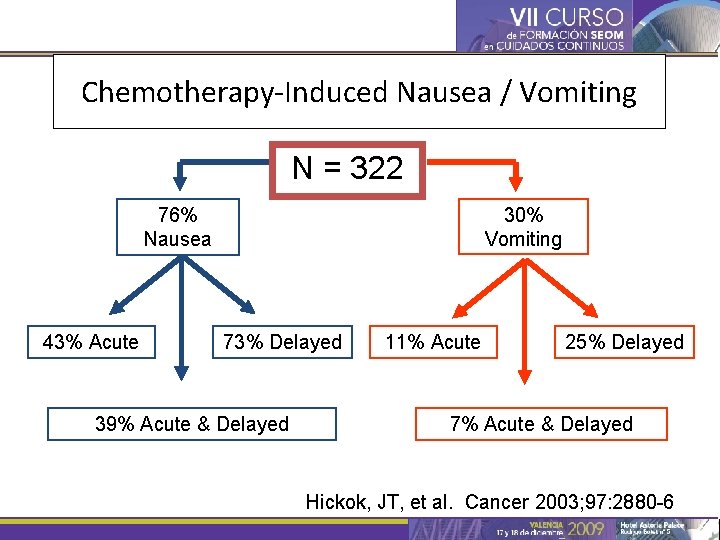
Chemotherapy-Induced Nausea / Vomiting N = 322 30% Vomiting 76% Nausea 43% Acute 73% Delayed 39% Acute & Delayed 11% Acute 25% Delayed 7% Acute & Delayed Hickok, JT, et al. Cancer 2003; 97: 2880 -6

C o n s e c u e n c • • Complicaciones metabólicas Deterioro nutricional y anorexia Lesiones mecánicas (Mallory-Weiss…. ) Dehiscencia de heridas Efectos psíquicos indeseables Deterioro del estado general y calidad de vida Interrupción del tratamiento NCCN Practice Guidelines in Oncology–Version 1. 2007. Antiemesis, MS-1.

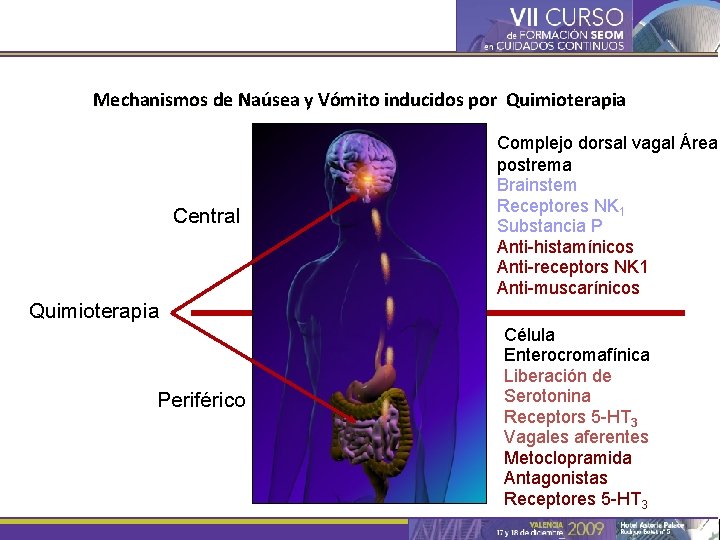
Mechanismos de Naúsea y Vómito inducidos por Quimioterapia Central Complejo dorsal vagal Área postrema Brainstem Receptores NK 1 Substancia P Anti-histamínicos Anti-receptors NK 1 Anti-muscarínicos Quimioterapia Periférico Célula Enterocromafínica Liberación de Serotonina Receptors 5 -HT 3 Vagales aferentes Metoclopramida Antagonistas Receptores 5 -HT 3

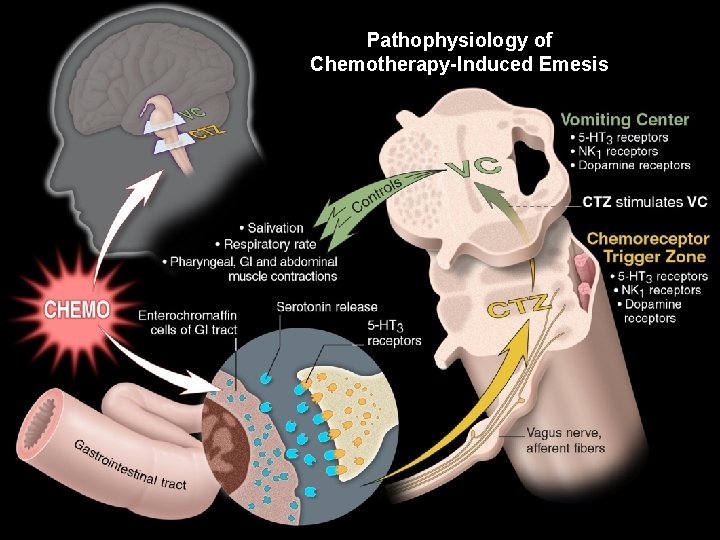
Pathophysiology of Chemotherapy-Induced Emesis

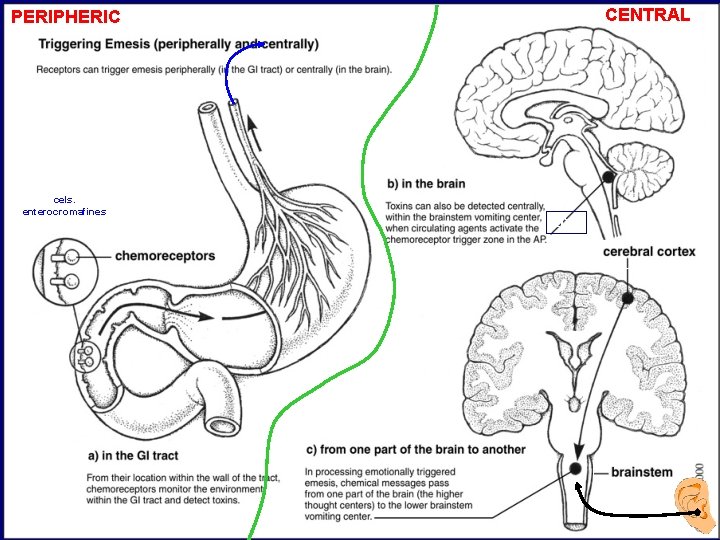
CENTRAL PERIPHERIC Fisiopatología de las náuseas y la emesis PERIFERICO CENTRAL • ZDQ • Centros vómito cels. enterocromafines ZDQ cels. enterocromafines quimiorreceptores TOXINAS, FARMACOS, acidosis, isquemia, aferencias vagales serotonina TOXINAS, IRRITANTES, obstrucción, isquemia ZDQ Zona desencadenante quimiorreceptora (fuera de BHE) estímulos corticales, náuseas, cinetosis, hipertensión IC ZDQ

Factores de riesgo de N/V inducidos por QTP Específicos del paciente Antecedentes de emesis Edad joven Sexo femenino Mayor ansiedad adversos Expectativa de efectos hospitalaria con náuseas Compañero de habitación Cantidad de sueño Baja ingestión de alcohol y vómitos Específicos del tratamiento Fármacos con mayor potencial emetógeno Regímenes combinados Quimioterapia en dosis altas Régimen y vía de administración Na. VIQ: náuseas y vómitos inducidos por quimioterapia Tomado de Berger AM, Clark-Snow RA. En Cancer: Principles and Practice of Oncology. 7 th ed. Philadelphia: Lippincott Williams & Wilkins, 2004: 2515– 2523; Antiemetic Subcommittee Ann Oncol 1998; 9: 811– 819.

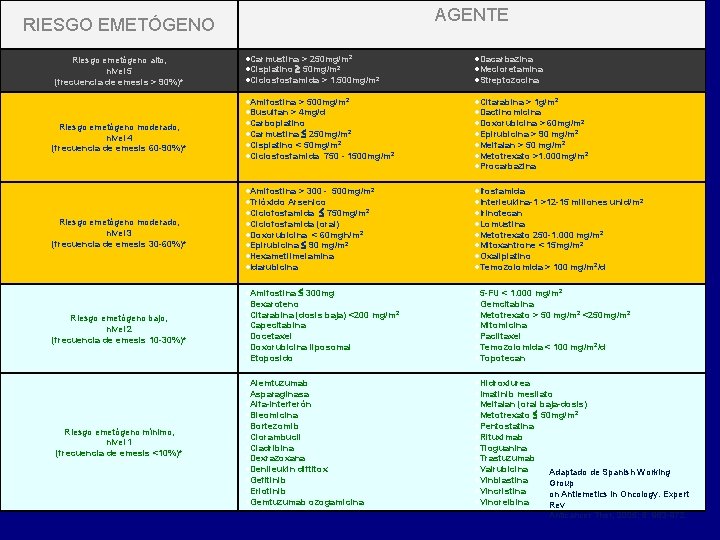
AGENTE RIESGO EMETÓGENO Riesgo emetógeno alto, nivel 5 (frecuencia de emesis > 90%)* Riesgo emetógeno moderado, nivel 4 (frecuencia de emesis 60 -90%)* Riesgo emetógeno moderado, nivel 3 (frecuencia de emesis 30 -60%)* Riesgo emetógeno bajo, nivel 2 (frecuencia de emesis 10 -30%)* Riesgo emetógeno mínimo, nivel 1 (frecuencia de emesis <10%)* Carmustina > 250 mg/m 2 Cisplatino 50 mg/m 2 Ciclosfosfamida > 1. 500 mg/m 2 Dacarbazina Mecloretamina Streptozocina Amifostina > 500 mg/m 2 Busulfan > 4 mg/d Carboplatino Carmustina 250 mg/m 2 Cisplatino < 50 mg/m 2 Ciclosfosfamida 750 - 1500 mg/m 2 Citarabina > 1 g/m 2 Dactinomicina Doxorubicina > 60 mg/m 2 Epirubicina > 90 mg/m 2 Melfalan > 50 mg/m 2 Metotrexato >1. 000 mg/m 2 Procarbazina Amifostina > 300 - 500 mg/m 2 Trióxido Arsenico Ciclofosfamida 750 mg/m 2 Ciclofosfamida (oral) Doxorubicina < 60 mgh/m 2 Epirubicina 90 mg/m 2 Hexametilmelamina Idarubicina Ifosfamida Interleukina-1 >12 -15 millones unid/m 2 Irinotecan Lomustina Metotrexato 250 -1. 000 mg/m 2 Mitoxantrone < 15 mg/m 2 Oxaliplatino Temozolomida > 100 mg/m 2/d Amifostina 300 mg Bexaroteno Citarabina (dosis baja) <200 mg/m 2 Capecitabina Docetaxel Doxorubicina liposomal Etoposido 5 -FU < 1. 000 mg/m 2 Gemcitabina Metotrexato > 50 mg/m 2 <250 mg/m 2 Mitomicina Paclitaxel Temozolomida < 100 mg/m 2/d Topotecan Alemtuzumab Asparaginasa Alfa-interferón Bleomicina Bortezomib Clorambucil Cladribina Dexrazoxana Denileukin diftitox Gefitinib Erlotinib Gemtuzumab ozogamicina Hidroxiurea Imatinib mesilato Melfalan (oral baja-dosis) Metotrexato 50 mg/m 2 Pentostatina Rituximab Tioguanina Trastuzumab Valrubicina Adaptado de Spanish Working Vinblastina Group Vincristina on Antiemetics in Oncology. Expert Vinorelbina Rev Anticancer Ther, 2005; 5: 963 -972.

NIVEL EMETÓGENO DE LA POLIQUIMIOTERAPIA Los fármacos del nivel I no añaden emetogenicidad. Añadir uno o más fármacos del nivel 2 aumenta la emetogenicidad de la combinación en UN GRADO SUPERIOR al del fármaco más emetógeno por separado. Añadir fármacos del nivel 3 o 4 incrementa la emetogenicidad en UN NIVEL POR CADA FÁRMACO AÑADIDO.

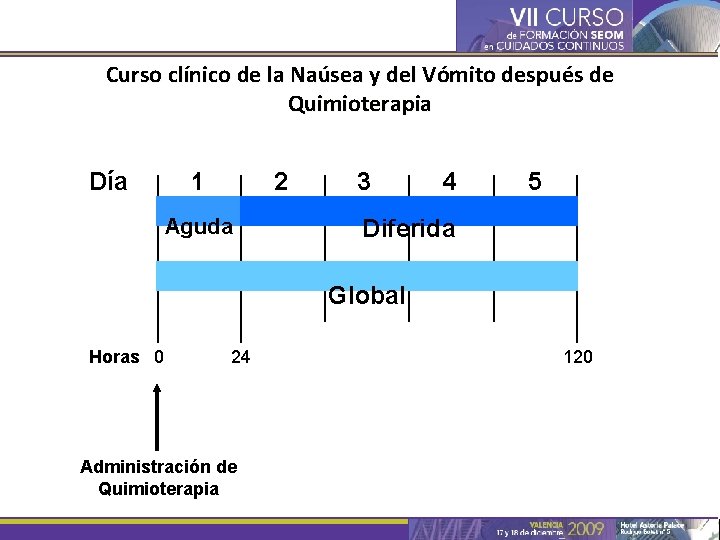
Tipos de Na. VIQ TIPO INICIO Y DURACIÓN Emesis aguda En las primeras 24 horas de la quimioterapia Emesis retrasada Al menos 24 horas después de la quimioterapia; puede durar hasta 7 días Emesis anticipada Antes del segundo o sucesivos ciclos de quimioterapia, pero debe comenzar durante o después de la quimioterapia en cualquier ciclo de tratamiento Tomado de Berger AM, Clark-Snow RA. En Cancer: Principles and Practice of Oncology. 7 th ed. Philadelphia: Lippincott Williams & Wilkins, 2004: 2515– 2513; Antiemetic Subcommittee Ann Oncol 1998 ; 9: 811– 819.

Curso clínico de la Naúsea y del Vómito después de Quimioterapia Día 1 2 Aguda 3 4 5 Diferida Global Horas 0 24 Administración de Quimioterapia 120

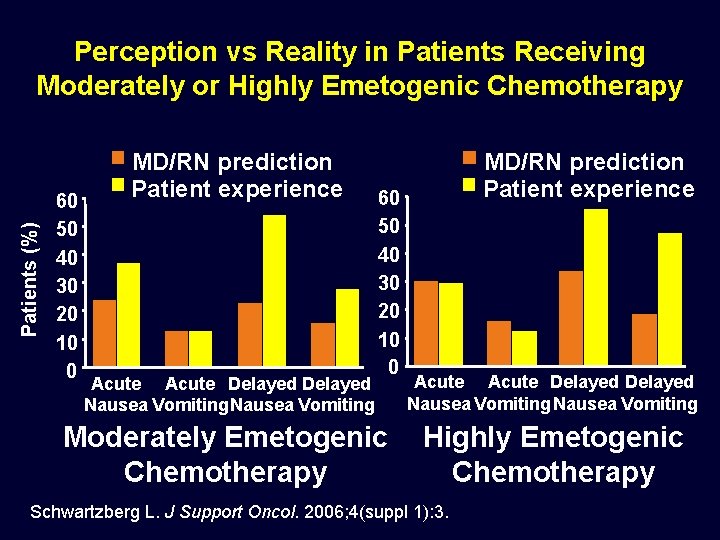
Patients (%) Perception vs Reality in Patients Receiving Moderately or Highly Emetogenic Chemotherapy 60 50 40 30 20 10 0 MD/RN prediction Patient experience Acute Delayed Nausea Vomiting 60 50 40 30 20 10 0 Moderately Emetogenic Chemotherapy MD/RN prediction Patient experience Acute Delayed Nausea Vomiting Highly Emetogenic Chemotherapy Schwartzberg L. J Support Oncol. 2006; 4(suppl 1): 3.

Objetivos del tratamiento antiemético • Principal: – Prevenir las NVIQ de la forma más completa posible. • Relacionados: – Aportar un tratamiento que sea lo más cómodo posible para los pacientes y el personal sanitario. – Minimizar el impacto de las NVIQ sobre la calidad de vida relacionada con la salud. – Reducir la hospitalización, el uso global de recursos sanitarios y los costes asociados. – Eliminar los posibles efectos adversos del tratamiento. Berger AM, Clark-Snow RA. In Cancer: Principles and Practice of Oncology. 7 th ed. Philadelphia: Lippincott Williams & Wilkins, 2004: 2515– 2523; Gralla RJ et al J Clin Oncol 1999; 17(9): 2971– 2994.

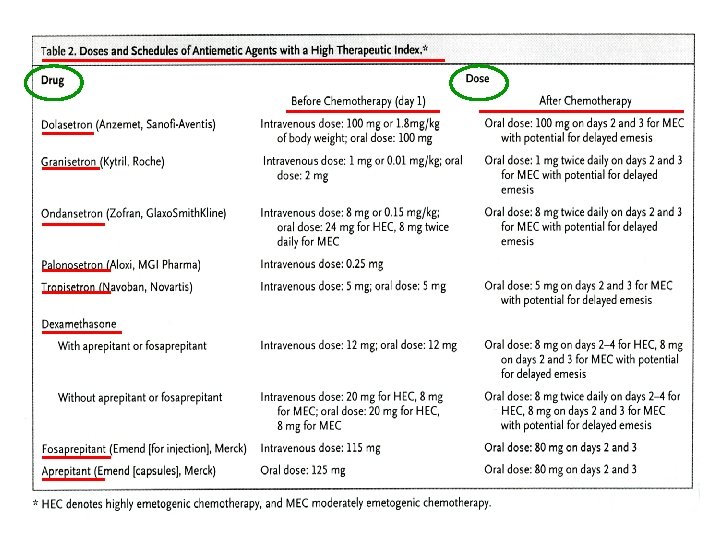
Fármacos antieméticos 1. Antagonistas de 5 HT 3 • ondansetrón, granisetrón, tropisetrón, dolasetrón y palonosetrón 2. Antidopaminérgicos (D 2) • fenotiazinas: proclorperazina, clorpromazina, tietilperazina • butiroferonas: haloperidol, droperidol (domperidona) • benzamidas: metoclopramida (mixto periférico + central) 3. Glucocorticoides • dexametasona, metilprednisolona 4. Antihistamínicos (H 1) • difenhidramina 5. Otros • benzodiazepinas: midazolán, lorazepam, diazepam • cannabinoides: -THC, dronabinol • antagonistas 5 HT 4: cisaprida 6. Antagonistas NK 1 • aprepitant.





Caso clínico • Paciente de 42 a. , con antecedentes de Hipertiroidismo tratado con I radioactivo, Hepatitis A a los 10 a. , Exéresis Hemangioma parotídeo. Menarquia a los 12 a. . Menstruante. No alergias conocidas. • Profesión : Neuróloga.

Caso clínico • Historia oncológica : Autopalpación de nódulo mamario en UCE mama izquierda. – MX /ECO : Área densa en MX con ECO que visualiza nódulo sólido de 7 mm. – RMN : Área de captación patológica de 5 -6 cm. – BAG : Carcinoma infiltrante de bajo grado – Estudio de extensión negativo. – Valoración en Comité : Se decide Mastectomia radical. Paciente de acuerdo.

Caso clínico • Resultado AP : C. Ductal Infiltrante , grado II, de 4 cm. . Infiltración focal del pezón. Presencia de carcinoma intraductal en conductos galactóforos. Afectación de 1/14 ganglios axilares. R. Hormonales positivos Ki 67 con índice proliferativo medio. ERB-2 negativo. • ESTADIO : p. T 2 N 1 a M 0.

Caso clínico • Valoración de tratamiento quimioterápico adyuvante : Se propone tratamiento con esquema secuencial de Epirrubicina / Ciclofosfamida (EC a dosis de 90 y 600 mg/m 2) por 4 ciclos , seguido de 4 ciclos de Docetaxel (100 mg/m 2) por 4 ciclos y posteriormente Hormonoterapia.

V a l o r a c i ó n • Reducción del riesgo de la recidiva esperado con este régimen de tratamiento • Toxicidades esperables – Neutropenia, alopecia, toxicidad cardiaca, mucositis, fatiga, y nauseas y vómitos

Caso clínico • La paciente inicia quimioterapia con esquema EC. • PREGUNTA 1 : ¿Qué esquema antiemético se aconsejaría para la emesis aguda? – Dexa, 5 -HT 3, Aprepitant – Dexa, 5 -HT 3, Aprepitant +/- Loracepan – Ninguno de los anteriores

Caso clinico • PREGUNTA 2 : Y para la emesis diferida? – Dexa, Aprepitant, dias 2 -3 – Dexa o Aprepitant, días 2 -3 – Dexa o 5 -HT 3, días 2 -3 – En cualquier caso añadir Loracepan

Factores de riesgo de N/V inducidos por QTP Específicos del paciente Antecedentes de emesis Edad joven Sexo femenino Mayor ansiedad adversos Expectativa de efectos hospitalaria con náuseas Compañero de habitación Cantidad de sueño Baja ingestión de alcohol y vómitos Específicos del tratamiento Fármacos con mayor potencial emetógeno Regímenes combinados Quimioterapia en dosis altas Régimen y vía de administración Na. VIQ: náuseas y vómitos inducidos por quimioterapia Tomado de Berger AM, Clark-Snow RA. En Cancer: Principles and Practice of Oncology. 7 th ed. Philadelphia: Lippincott Williams & Wilkins, 2004: 2515– 2523; Antiemetic Subcommittee Ann Oncol 1998; 9: 811– 819.

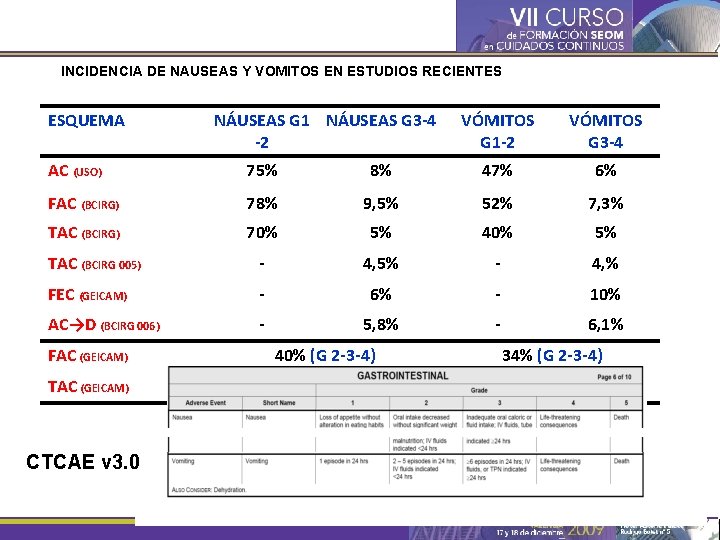
INCIDENCIA DE NAUSEAS Y VOMITOS EN ESTUDIOS RECIENTES ESQUEMA NÁUSEAS G 1 NÁUSEAS G 3 -4 -2 VÓMITOS G 1 -2 VÓMITOS G 3 -4 AC (USO) 75% 8% 47% 6% FAC (BCIRG) 78% 9, 5% 52% 7, 3% TAC (BCIRG) 70% 5% 40% 5% TAC (BCIRG 005) - 4, 5% - 4, % FEC (GEICAM) - 6% - 10% AC→D (BCIRG 006) - 5, 8% - 6, 1% FAC (GEICAM) 40% (G 2 -3 -4) 34% (G 2 -3 -4) TAC (GEICAM) 39% (G 2 -3 -4) 28% (G 2 -3 -4) CTCAE v 3. 0











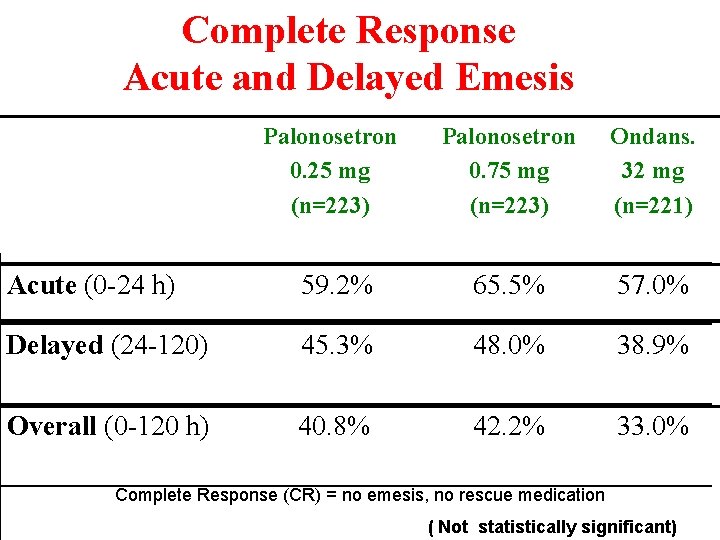
A PHASE III, DOUBLE-BLIND, RANDOMIZED TRIAL OF PALONOSETRON COMPARED WITH ONDANSETRON IN PREVENTING CHEMOTHERAPY-INDUCED NAUSEA AND VOMITING FOLLOWING HIGHLY EMETOGENIC CHEMOTHERAPY Aapro MS et al. Ann Oncol 2006; 17: 1441 -449

Complete Response Acute and Delayed Emesis Palonosetron 0. 25 mg (n=223) Palonosetron 0. 75 mg (n=223) Ondans. 32 mg (n=221) Acute (0 -24 h) 59. 2% 65. 5% 57. 0% Delayed (24 -120) 45. 3% 48. 0% 38. 9% Overall (0 -120 h) 40. 8% 42. 2% 33. 0% Complete Response (CR) = no emesis, no rescue medication ( Not statistically significant)



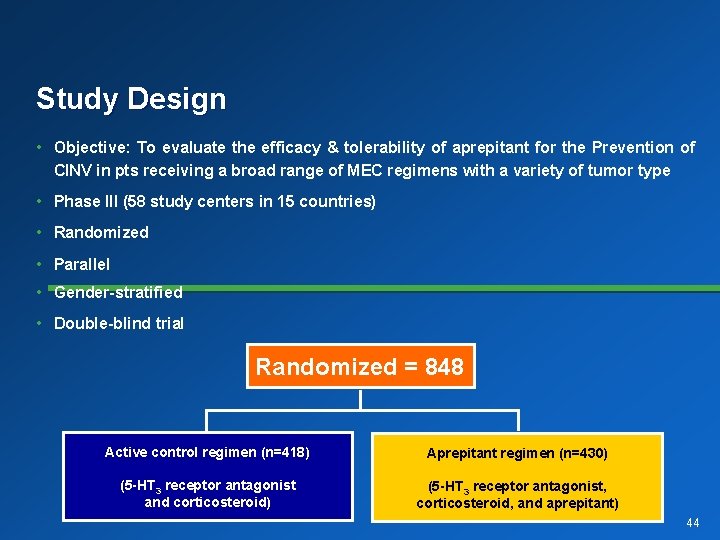
PN 130: RESULTS OF APREPITANT FOR THE PREVENTION OF CHEMOTHERAPY-INDUCED NAUSEA AND VOMITING ASSOCIATED WITH A BROAD RANGE OF MODERATELY EMETOGENIC CHEMOTHERAPIES (MEC) AND TUMOR TYPES Bernardo L. Rapoport 1, Karin Jordan 2, Judith A. Boice 3, Arlene Taylor 4, Carole Brown 4, James S. Hardwick 4, Alexandra Carides 4, Timothy Webb 5, and Hans-Joachim Schmoll 2 1. Medical Oncology Center of Rosebank, Johannesburg, South Africa 2. Departments of Internal Medicine and Oncology/Hematology, Martin-Luther. University of Halle-Wittenberg, Halle/Saale, Germany 3. Merck Research Laboratories, Rahway, PA 4. Merck Research Laboratories, Upper Gwynedd, PA 5. Genesis Cancer Center, Hot Springs, AR

Study Design • Objective: To evaluate the efficacy & tolerability of aprepitant for the Prevention of CINV in pts receiving a broad range of MEC regimens with a variety of tumor type • Phase III (58 study centers in 15 countries) • Randomized • Parallel • Gender-stratified • Double-blind trial Randomized = 848 Active control regimen (n=418) Aprepitant regimen (n=430) (5 -HT 3 receptor antagonist and corticosteroid) (5 -HT 3 receptor antagonist, corticosteroid, and aprepitant) 44

Endpoints • Primary – To determine the proportion of patients reporting No Vomiting during the five days (120 hours) following initiation of chemotherapy • Key Secondary – To determine the Overall Complete Response (no emetic episodes and no administration of rescue therapy) during the five days (120 hrs) following the initiation of chemotherapy • Tolerability – To evaluate the safety and tolerability of the Aprepitant Regimen for Chemotherapy Induced Nausea and Vomiting (CINV) 45

Treatment Regimens Active control regimen Day 1 Day 2 Day 3 Ondansetron 16 mg PO* Aprepitant 80 mg PO Dexamethasone 20 mg PO Aprepitant 125 mg PO Aprepitant with Ondansetron control 16 mg PO* regimen Dexamethasone 12 mg PO Placebo for aprepitant in the active control regimen was used to maintain blinding. All medications were given orally. * 8 mg PO bid. PO=by mouth; bid=twice daily. 46

Chemotherapy Regimens* • AC – Cyclophosphamide + doxorubicin or epirubicin ± other LEC agents • Non AC – – – – – Carboplatin + other LEC agents Carboplatin + doxorubicin + 5 FU Oxaliplatin ± other LEC agents Oxaliplatin + irinotecan, epirubicin or raltitrexed ± other LEC agents Cyclophosphamide + methotrexate or mitoxantrone ± 5 FU Doxorubicin + decarbazine or ifosfamide Doxorubicin ± other LEC agents Irinotecan ± 5 FU or raltitrexed * Regimens may have also included minimally emetogenic chemotherapy as well as antibody targeted therapies (bevacizumab, trastuzumab, 47 rituximab)

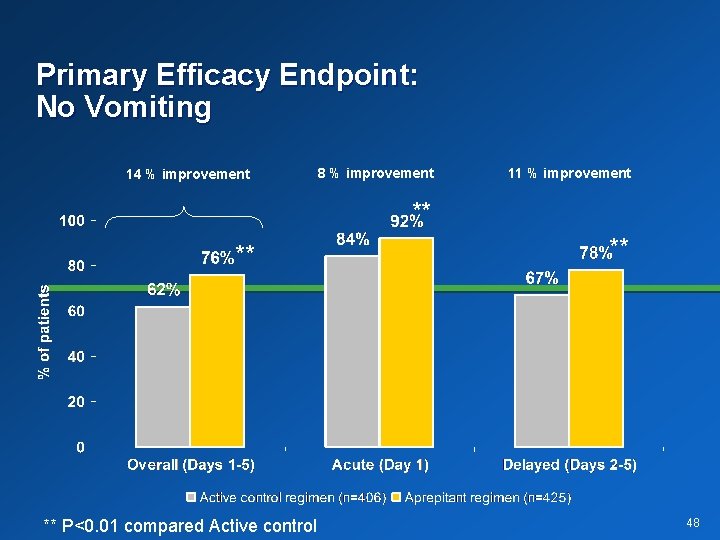
Primary Efficacy Endpoint: No Vomiting 14 % improvement 8 % improvement 11 % improvement ** ** ** P<0. 01 compared Active control ** 48

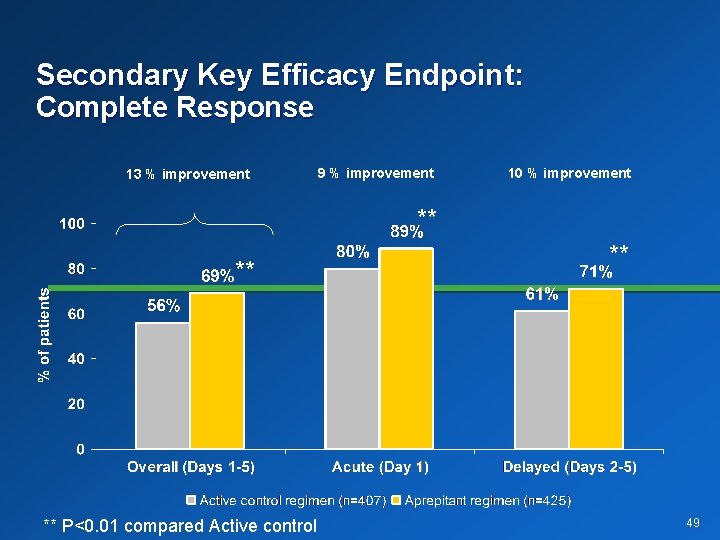
Secondary Key Efficacy Endpoint: Complete Response 13 % improvement 9 % improvement 10 % improvement ** ** ** P<0. 01 compared Active control ** 49

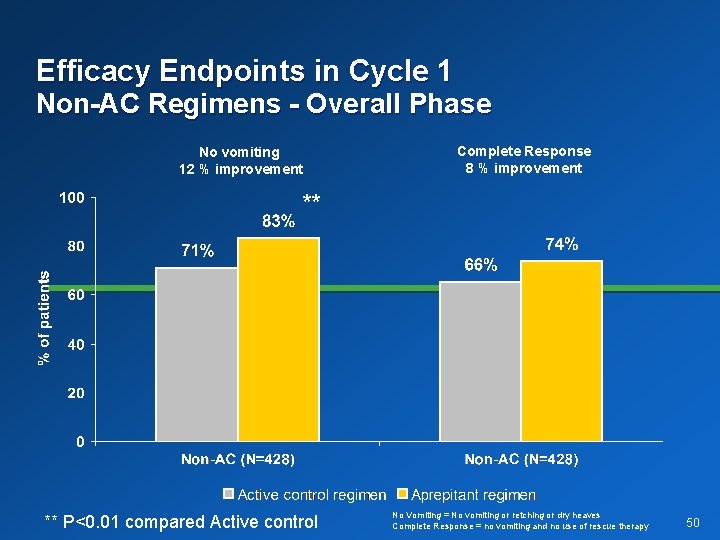
Efficacy Endpoints in Cycle 1 Non-AC Regimens - Overall Phase Complete Response 8 % improvement No vomiting 12 % improvement ** ** P<0. 01 compared Active control No Vomiting = No vomiting or retching or dry heaves Complete Response = no vomiting and no use of rescue therapy 50

Conclusions • Aprepitant regimen significantly improved prevention of CINV for pts receiving a broad range of MEC regimens & tumor types • Aprepitant regimen was superior than the active control regimen endpoints across all phases (acute, delayed and overall): – No Vomiting – Complete Response • Active in AC- and non-AC- based MEC • Aprepitant was well tolerated 51

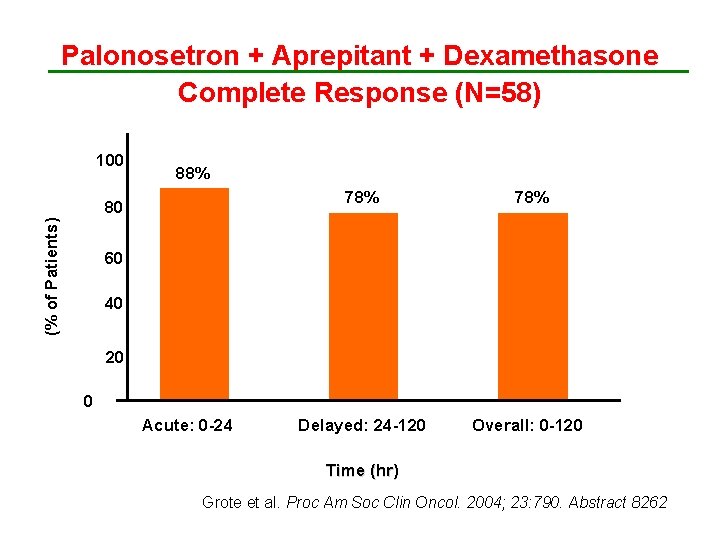
COMBINATION THERAPY FOR CHEMOTHERAPY-INDUCED NAUSEA AND VOMITING IN PATIENTS RECEIVING MODERATELY EMETOGENIC CHEMOTHERAPY: PALONOSETRON, DEXAMETHASONE, AND APREPITANT Grote T et al. J Support Oncol 2006; 4: 403 -8

Palonosetron + Aprepitant + Dexamethasone Complete Response (N=58) 100 88% (% of Patients) 80 78% Delayed: 24 -120 Overall: 0 -120 60 40 20 0 Acute: 0 -24 Time (hr) Grote et al. Proc Am Soc Clin Oncol. 2004; 23: 790. Abstract 8262

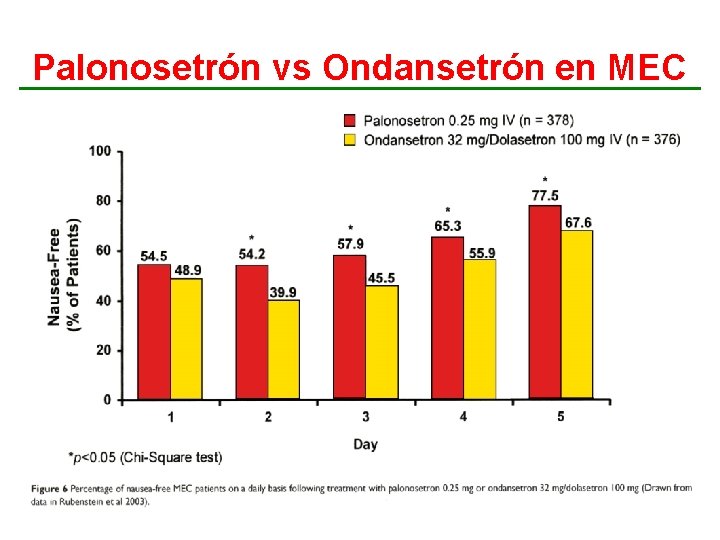
Palonosetrón vs Ondansetrón en MEC


Caso clínico • La paciente fue tratada con un régimen antiemético con Dexa, Aprepitant y 5 -HT 3. Tras primer ciclo presenta nausea grado I. • Pregunta 3 : Hay que tener en cuenta posibles interacciones del Aprepitant con otros fármacos? – Sí, el Aprepitant puede ser inductor o inhibidor del citocromo P 450 ( inhibidor enzima 3 A 4 – CYP 3 A 4 o inductor CYP 2 C 9). – Debido a ello puede interferir con diversos fármacos tanto con quimioterápicos como con otros fármacos. – Sólo debe tenerse en cuenta reducir la dosis de dexametasona. – Las dos primeras respuestas son correctas.

Aprepitant Metabolism § metabolized in the liver through the P 450 enzyme system § primarily metabolized by the CYP 3 A 4 isozyme § Some drug-drug interactions may be more significant for oral medications (first pass effect)

Aprepitant: Impact on CYP 450 § Aprepitant is primarily metabolized by the CYP 3 A 4 isoenzyme § Aprepitant inhibits CYP 3 A 4 (as early as 1 hr after first dose) § Induces its own metabolism upon dosing for 2 weeks (autoinduction) via CYP 3 A 4 § Aprepitant induces CYP 2 C 9 Shadle CR, et al. J Clin Pharmacol 2004

Interacciones medicamentosas: efecto de EMEND® sobre la farmacocinética de otros fármacos Característica de aprepitant Importancia clínica ● Aprepitant puede aumentar las concentraciones plasmáticas de los fármacos administrados al mismo tiempo que se metabolicen a través de CYP 3 A 4 ● Reducir las dosis de corticosteroides orales en aproximadamente un 50% cuando se administren junto con aprepitant ● Considerar los posibles efectos de las mayores concentraciones plasmáticas de midazolam u otras benzodiazepinas metabolizadas a través de CYP 3 A 4 (p. ej. , alprazolam, triazolam) cuando se administren junto con aprepitant ● No usar aprepitant junto con pimozida, terfenadina, astemizol, ni cisaprida ● Se aconseja precaución cuando aprepitant se administre con antineoplásicos administrados por vía oral metabolizados principal o parcialmente a través de CYP 3 A 4 (por ejemplo etopósido, vinolrebina) ● Puede disminuir las concentraciones plasmáticas de los fármacos administrados al mismo tiempo que se metabolicen a través de CYP 3 A 4 ● La eficacia de los anticonceptivos hormonales puede disminuir durante la administración de aprepitant y los 28 días siguientes; por tanto, deben usarse métodos anticonceptivos alternativos o de refuerzo durante el tratamiento y en los 2 meses siguientes a la última dosis de aprepitant

Interacciones medicamentosas: efecto de EMEND® sobre la farmacocinética de otros fármacos (cont. ) Característica de aprepitant Importancia clínica ● Puede disminuir las concentraciones plasmáticas de los fármacos administrados al mismo tiempo que se metabolicen por la CYP 2 C 9 al ser un inductor moderado del mismo. ● La administración conjunta de aprepitant con warfarina da lugar a una disminución del tiempo de protrombina, comunicado como coeficiente internacional normalizado (INR, International Normalised Ratio). En pacientes en tratamiento crónico con warfarina, el INR debe vigilarse estrechamente durante el tratamiento con aprepitant y durante 2 semanas después de cada ciclo de 3 días de aprepitant ● Considerar los posibles efectos de las menores concentraciones plasmáticas de tolbutamida

Interacciones medicamentosas: efecto de otros fármacos sobre la farmacocinética de EMEND® Característica de aprepitant Importancia clínica ● Los fármacos que inhiben o inducen fuertemente la CYP 3 A 4 pueden aumentar o reducir las concentraciones plasmáticas de aprepitant, respectivamente ● La administración de aprepitant con medicamentos que inhiben la actividad de CYP 3 A 4 (p. ej, ketoconazol) debe abordarse con precaución ya que la combinación provoca elevación de la concentración plasmática de aprepitant. ● La administración constante de aprepitant con medicamentos que inducen fuertemente la actividad de CYP 3 A 4 (p. ej, rifampicina) debe evitarse ya que la combinación provoca reducciones en las concentraciones plasmáticas de aprepitant lo que podría provocar disminución de la eficacia de aprepitant.

Aprepitant: Drug Interactions Antineoplastic agents commonly metabolized through CYP 3 A 4: • paclitaxel • ifosfamide • imatinib • etoposide • vinorelbine • docetaxel • irinotecan • vinblastine • vincristine

Caso clínico • Tras administración del segundo ciclo de EC, la paciente presenta N y V grado III diferida. PREGUNTA 4 ¿Cómo tratar la emesis diferida o continuada? – Añadir un nuevo Agente antiemético – Pueden ser necesarios múltiples agentes concurrentes utilizando pautas y vias de administración alternativas. – En caso de controlarse debe mantenerse en los próximos ciclos la medicación de forma pautada. – Puden considerarse los canabinoides si no hay respuesta a la terapia convencional. – Todas las respuestas son correctas

Delayed Symptoms Some patients experience delayed symptoms (24 hours or more after chemotherapy), and the risk of nausea and vomiting increases during multiple cycles of therapy

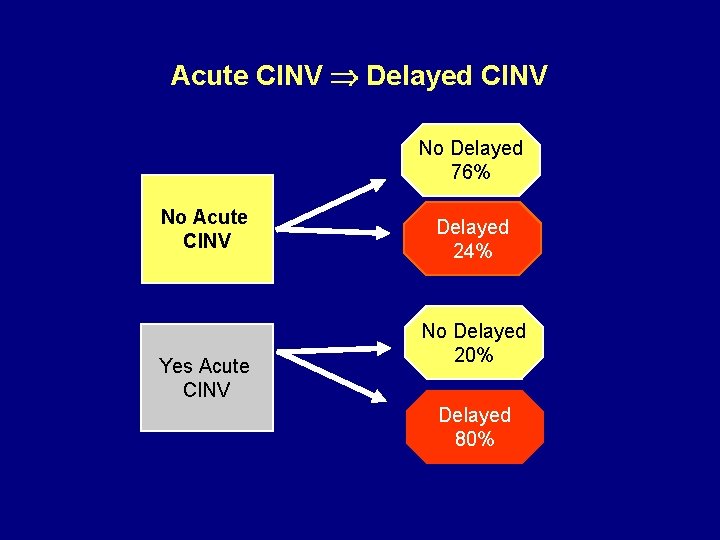
Acute CINV Delayed CINV No Delayed 76% No Acute CINV Yes Acute CINV Delayed 24% No Delayed 20% Delayed 80%

Delayed CINV Is More Prevalent Than Acute CINV l Delayed emesis is 2. 5 times more prevalent than acute emesis l For moderately emetogenic chemotherapy l – Delayed nausea exceeds acute nausea by 16% – Delayed emesis exceeds acute emesis by 15% For highly emetogenic chemotherapy – Delayed nausea exceeds acute nausea by 27% – Delayed emesis exceeds acute emesis by 38% Grunberg SM, et al. Cancer. 2004; 100: 2261.

CINV with delayed nausea l About half of all patients experience moderate to severe delayed nausea and vomiting even in this era of better agents l Fewer than half of patients with moderate to severe CINV after cycle 1 get an adjustment of regimen before cycle 21 l Association of CINV with fatigue, “down time” is quite strong 2 l Nausea causes greater QOL impact than vomiting 3 1. Dibble SL, et al. Oncol Nurs Forum. 2003; 30: E 40. 2. Dibble SL, et al. Oncol Nurs Forum. 2004; 31: E 1. 3. Bloechl-Daum B, et al. J Clin Oncol. 2006; 24: 4472.

Options for Breakthrough CINV l Additional agents should be from a different drug class than initial therapy l Possible options include dopamine antagonists, metoclopramide, butyrophenones, cannabinoids, corticosteroids, or agents such as lorazepam NCCN Practice Guidelines in Oncology – Version 1. 2007. Antiemesis, MS-1.


Caso clínico • Tras control de la emesis diferida con tratamiento que requiere dexa, 5 -HT -3, haloperidol, rehidratación, la paciente prosigue tratamiento. Antes del 4 ciclo, presenta nauseas anticipatorias. • Pregunta 5 : Sobre las N y V anticipatorios – No dependen de la emesis aguda o diferida – Deben tratarse con un régimen antiemético superior al utilizado en la pauta previa – Son muy poco frecuentes y de escasa relevancia clínica. – Deben tratarse con técnicas psicológicas, de relajación y uso de ansiolíticos. – Todas las respuestas son correctas

Anticipatory Nausea and Vomiting l Anticipatory nausea occurs in 29% of chemotherapy patients 1, 2 l Anticipatory vomiting occurs in 11% of chemotherapy patients 1, 2 l Anticipatory nausea and vomiting – Mostly on the basis of classic or Pavlovian conditioning 3 1. Roscoe JA, et al. J Pain Symptom Manage. 2000; 20: 113. 2. Morrow GR, et al. Support Care Cancer. 1998; 6: 244. 3. Reesal RT, et al. Can J Psychiatr. 1990; 35: 80.

Anticipatory nausea and vomiting l Still occurs in about 25% of patients in spite of new antiemetics l Prevention is key: lower incidence when initial CINV is well managed l Memory? Anxiety? Lorazepam, cannabinoids may reduce incidence l Treat before chemotherapy l Training measures: visualization, acupressure?

COMITÉ VIII : Nota: El mejor enfoque para la emesis anticipatoria es el mejor control posible de la emesis aguda y tardía December 2005 Multinational Association of Supportive Care in Cancer © MASCC 2007


COMITÉ VIII: Guías de práctica clínica para el manejo de las náuseas y los vómitos anticipatorios en pacientes que reciben quimioterapia o RT Las náuseas y los vómitos anticipatorios deben ser manejados mediante técnicas psicológicas. Nivel de confianza MASCC: alto Nivel de consenso MASCC: alto ----------------------------------------- Una alternativa o adición a las técnicas psicológicas es el uso de benzodiazepinas Nivel de confianza MASCC: moderado Nivel de consenso MASCC: alto December 2005 Multinational Association of Supportive Care in Cancer © MASCC 2007

Conclusiones

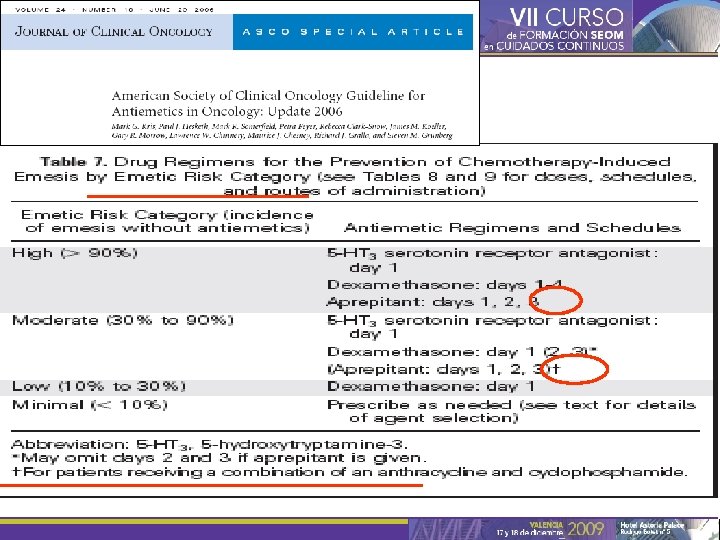
RECOMENDACIONES ( según riesgo emetógeno) ALTO: Emesis aguda: anti 5 HT 3 + corticoesteroide + aprepitant (IA) Emesis retardada: corticoesteroide + aprepitant (IIA) MODERADO: Emesis aguda (AC): anti 5 HT 3 + corticoest. + aprepitant (IIA) Emesis aguda (otros): anti 5 HT 3 + corticoesteroides (IA) Emesis retardada (AC): aprepitant o corticoesteroide (IIA), Emesis retardada (otros): corticoesteroide oral (IIA) o anti 5 HT 3 (IIB) BAJO: Corticoesteroide (III, IV D) para emesis aguda; no prevenir la diferida. MÍNIMO: No de rutina, si no hay antecedentes (V y consenso D)


Muchas gracias por su atención