ACTUALIZACION DEL TRATAMIENTO ANTIRRETROVIRAL Macarena Bonilla Porras Residente

ACTUALIZACION DEL TRATAMIENTO ANTIRRETROVIRAL Macarena Bonilla Porras Residente III Servicio de Farmacia. Hospital Severo Ochoa

TERAPIA ACTUAL

GRUPOS ACTUALES n n n INHIBIDORES DE LA TRANSCRIPTASA INVERSA ¨ ANÁLOGOS DE NUCLEOSIDOS ¨ ANÁLOGOS DE NUCLEOTIDOS ¨ NO ANÁLOGOS DE NUCLEOSIDOS INHIBIDORES DE LA PROTEASA INHIBIDORES DE LA FUSION

INHIBIDORES DE LA TRANSCRIPTASA INVERSA ANÁLOGOS DE NUCLEOSIDOS n n n n n RETROVIR® - AZT - ZIDOVUDINA VIDEX® - dd. I - DIDANOSINA HIVID® - dd. C - ZALCITABINA ZERIT® - d 4 T - ESTAVUDINA EPIVIR® - 3 TC - LAMIVUDINA ZIAGEN® - ABC - ABACAVIR TRIZIVIR® AZT + 3 TC + ABC COMBIVIR® AZT + 3 TC VIREAD® - TDF – TENOFOVIR (PMPA) (análogo de nucleótido)

INHIBIDORES DE LA TRANSCRIPTASA INVERSA ANÁLOGOS DE NUCLEOSIDOS EN DESARROLLO n n AMDOXOVIR ESTAMPIDINA DPC 817 ALOVUDINA

INHIBIDORES DE LA TRANSCRIPTASA INVERSA NO ANÁLOGOS DE NUCLEOSIDOS n SUSTIVA® - EFAVIREZ n VIRAMUNE® - NEVIRAPINA n RESCRIPTOR® - DELAVIRDINA

INHIBIDORES DE LA TRANSCRIPTASA INVERSA NO ANÁLOGOS DE NUCLEOSIDOS EN DESARROLLO n n n CAPRAVIRINA (ENSAYO FASE II-III) EMVIRINE (MKC 442) DPC-083 TMC 120 TMC 125

INHIBIDORES PROTEASA n n n AGENERASE® - AMPRENAVIR CRIXIVAN® - INDINAVIR KALETRA® - LOPINAVIR/RITONAVIR VIRACEPT® - NELFINAVIR NORVIR® - RITONAVIR FORTOVASE/INVIRASE® - SAQUINAVIR
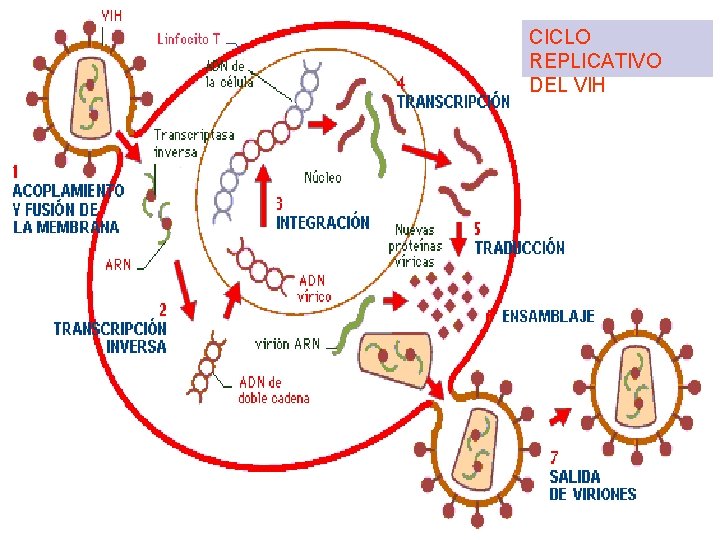
CICLO REPLICATIVO DEL VIH
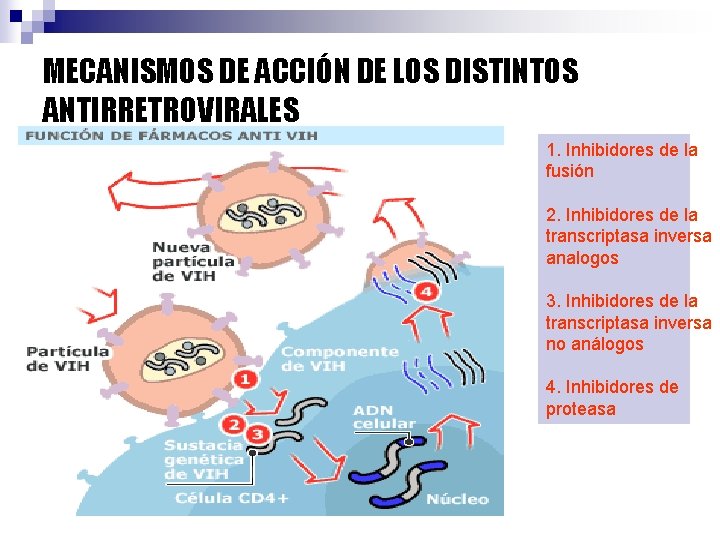
MECANISMOS DE ACCIÓN DE LOS DISTINTOS ANTIRRETROVIRALES 1. Inhibidores de la fusión 2. Inhibidores de la transcriptasa inversa analogos 3. Inhibidores de la transcriptasa inversa no análogos 4. Inhibidores de proteasa

OBJETIVOS DEL TRATAMIENTO ANTIRRETROVIRAL DE GRAN ACTIVIDAD (TARGA) 1. Desde 1996 2. Se basa en la asociación de análogos de la Tx inversa + no análogos o IP 3. Permite incidencia eventos oportunistas disminución morbi-mortalidad

¿POR QUÉ SE SIGUEN DESARROLLANDO NUEVOS FÁRMACOS? ADHERENCIA Elevado nº de pastillas debido a: - la limitada abs intestinal - alta tasa de unión a prot plasmáticas - t 1/ 2 corto - problemas formulación

¿POR QUÉ SE SIGUEN DESARROLLANDO NUEVOS FÁRMACOS? TOXICIDAD FRACASO TERAPÉUTICO - Alteraciones metabólicas aumento de colesterol, triglicéridos y resistencia a la insulina - Alteraciones morfológicas distribución anormal del tejido adiposo síndrome de lipodistrofia (desgaste de la grasa periférica y adiposidad central)
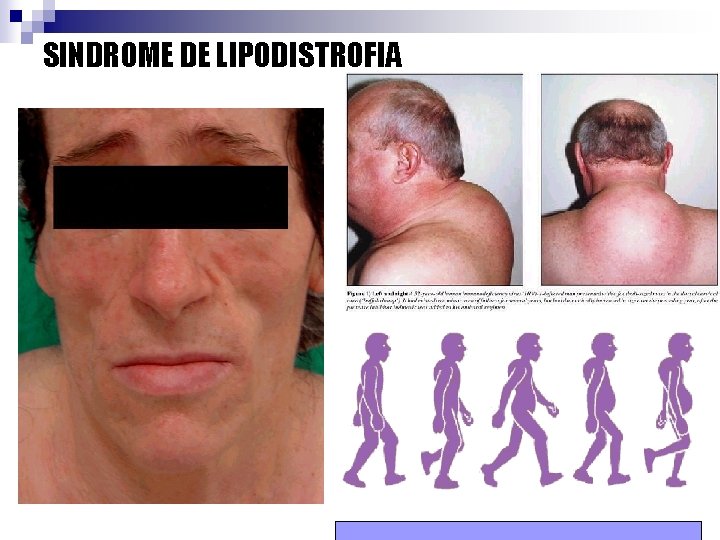
SINDROME DE LIPODISTROFIA

SIMPLIFICACIÓN DEL TRATAMIENTO

OBJETIVOS n n Eliminar restricciones dietéticas nº pastillas la frecuencia de tomas evitar la progresión de trastornos metabólicos y morfológicos OBJETIVO FINAL MANTENER EL ÉXITO VIROLÓGICO E INMU FACILITANDO LA ADHERENCIA Y MEJORANDO LA CALIDAD DE VIDA D
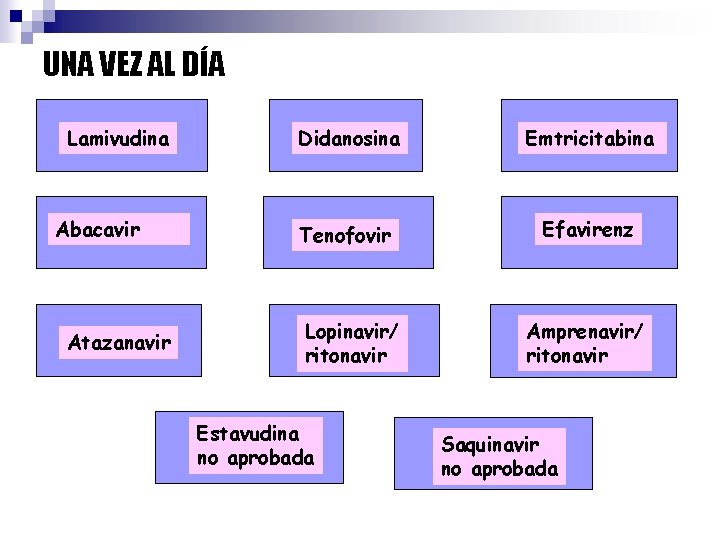
UNA VEZ AL DÍA Lamivudina Abacavir Atazanavir Didanosina Emtricitabina Tenofovir Efavirenz Lopinavir/ ritonavir Estavudina no aprobada Amprenavir/ ritonavir Saquinavir no aprobada

VENTAJAS n n n Poder administrar el tratamiento en una sola toma lo que facilita el cumplimiento terapéutico Facilitar su adm en forma de tratamientos directamente observados Facilidad para adaptarse al estilo de vida del paciente DESVENTAJAS Infradosificación si el paciente pierde una o más dosis de medicación aunque los fcos que pueden utilizarse QD tienen T ½ de 24 -50 h por lo que el olvido de una dosis es menos trascendente que aquellos fcos diseñados inicialmente para BID.
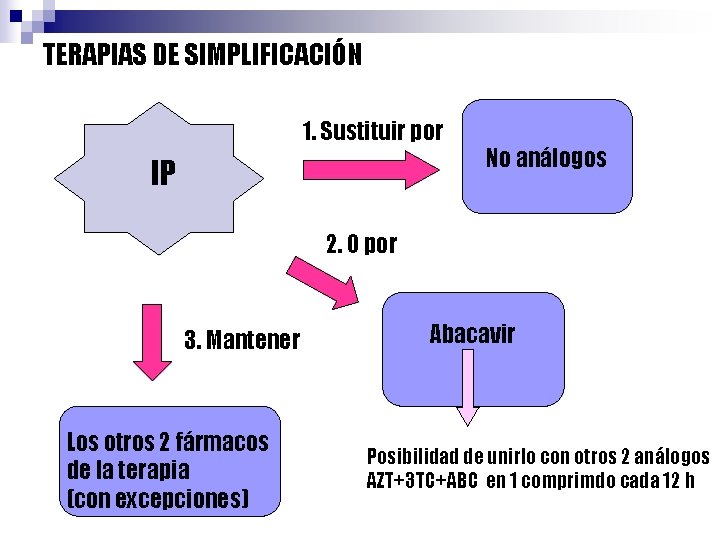
TERAPIAS DE SIMPLIFICACIÓN 1. Sustituir por IP No análogos 2. O por 3. Mantener Los otros 2 fármacos de la terapia (con excepciones) Abacavir Posibilidad de unirlo con otros 2 análogos AZT+3 TC+ABC en 1 comprimdo cada 12 h

n Excepciones La combinación tenofovir + lamivudina junto abacavir o didanosina se asocia con gran nº de fracasos virológicos con selección de resistencias Tampoco se recomienda asociar estavudina y didanosina con otro análogo ya que los riesgos de toxicidad mitocondrial y fracaso virológico son elevados

NUEVOS INHIBIDORES DE LA TX INVERSA ANALOGOS DE NUCLEOSIDOS EMTRIVA® - EMTRICITABINA – FTC Autorización EMEA: 24 Octubre 2003
FOTO CAJA EMTRIVA Presentaciones Emtriva® cápsulas duras 200 mg C/30 (pvl envase 150. 36 €) Emtriva® solución oral 10 mg/ml (conservar en nevera) HSVO---- 2 PACIENTES

MECANISMO DE ACCIÓN n Análogo del nucleósido citosina con actividad frente n a transcriptasa inversa. Es similar a 3 TC aunque su actividad in vitro es mayor. Se metaboliza a 5´-trifosfato-emtricitabina Es un inhibidor competitivo de la TI dando lugar a una interrupción de la cadena de ADN n

INDICACIONES n n Tratamiento de adultos y niños infectados por el VIH 1 en combinación con otros antirretrovirales La indicación se basa en estudios con pacientes naive y pretratados control virológico estable No existe experiencia en pac que no responde al tto actual o a múltiples regímenes anteriores. FTC en estudios en fase III en pacientes naive se mostró superior a d 4 T(estavudina) en combinación con didanosina y efavirenz pero inferior a 3 TC(lamivudina)

EFECTIVIDAD- ensayos en pac naive n n n FTC-201 (Montana) FTC-302 FTC-301 ACTG-5015 FTC-203 (ensayo en pediatría) EFECTIVIDAD- ensayos de cambio de 3 TC a FTC • FTC - 303 • FTC - 350

POSOLOGIA n n Dosis: 200 mg / 24 h en adultos y adolescentes > 33 kg. Dosis niños: 6 mg/kg/24 h Sólo administrar en forma de solución oral hasta 24 ml, por su baja biodisponibilidad se recomienda que en niños de > 33 kg se administren las cápsulas. ¨ No se recomienda adm a lactantes < 4 meses ¨ no se conoce su efecto en el embarazo ¨ n Se puede administrar sin restricciones dietéticas (con o sin alimentos).

REACCIONES ADVERSAS n n n n En sangre: ANEMIA En el metabolismo: ↑ TG ↑ GLC En SNC: CEFALEA, INSOMNIO GI: DIARREAS, NAUSEAS Hepatobiliares: ↑ TRANSAMINASAS En piel: EXANTEMA, PRURITO Musculoesqueléticas: ↑ CK Otras: DOLOR

CONTRAINDICACIONES Y PRECAUCIONES n n n Hipersensibilidad Ajuste de dosis en IR (no existen datos sobre IH). FTC se elimina por filtración glomerular y secreción tubular activa No existen datos sobre IH. Se está evaluando su actividad clínica frente VHB Acidosis láctica especial precaución en pac con alt hepáticas y mujeres obesas Lipodistrofia

INTERACCIONES Precaución en fármacos que se eliminen por vía renal n No inhibe cit P 450 n No interacciona con indinavir, estavudina, zidovudina, famciclovir y tenofovir No combinarlos n FTC Y 3 TC son fcos muy similares no hay experiencia sobre la coadministración de análogos de citidina ( lamivudina o zalcitabina) n

RESISTENCIA n n Los virus resistentes a emtricitabina (mutación M 184 V/I) mostraron resistencia cruzada a lamivudina pero sensibilidad a otros análogos. Los virus resistentes a zidovudina, zalcitabina, didanosina y no análogos son sensibles a emtricitabina. Lamivudina es un fármaco de barrera genética baja, su utilización en una primera linea de tto la inutiliza (en caso de fracaso virológico para tto sucesivos) Sin embargo, la escasa resistencia cruzada de la lamivudina la convierte en una alternativa útil en el rescate cuando no se ha utilizado anteriormente

VENTAJAS n Administración 1 vez al día n No presenta restricciones alimentarias n Su larga vida media justifica la permisividad del olvido de una dosis

DESVENTAJAS n n No se aconseja cambiar a FTC cuando el paciente ha respondido a 3 TC + TNF + IP o no análogo No ha demostrado actividad en pac que están fracasando en su tto actual o con múltiples regímenes

TRUVADA® EMTRICIBAINA - TENOFOVIR Aprobada por FDA agosto 2004
Indicado en combinación con otros antirretrovirales para el tratamiento de la infección VIH-1 en adultos Emtricitabina 200 mg + tenofovir 300 mg

TRUVADA n n n Se adm 1 vez al día con o sin alimentos Necesita ajuste de dosis en pac con alt renal En pac con alt hepática la farmacocinética no se ve afectada No se establecido su seguridad en niños Hay que tener en cuenta la interacción entre dd. I y tenofovir Pac que toman LPV/RTV o ATZ/RTV + Truvada deben ser monitorizados

RESULTADOS PRELIMINARES ESTUDIO GS-934 A LAS 24 SEMANAS n Sustiva® (efavirenz) ¨ n 1 vez al día Combivir® (zidovudina+lamivudina) ¨ n 2 veces al día . Respuesta virológica mayor. Menor abandono del tto Sustiva® (efavirenz) ¨ n 1 vez al día Truvada® (emtricitabina+tenofovir) ¨ 1 vez al día

KIVEXA® EPZICOM® LAMIVUDINA- ABACAVIR Epzicom Aprobado por la FDA agosto 2004 Kivexa Aprobado por la EMEA 17 diciembre 2004
EPIVIR + ZIAGEN COMBINATION KIVEXA lamivudina 300 mg + abacavir 600 mg 1 vez al día con o sin alimentos

INDICACIONES n n Terapia de combinación antirretroviral para el tto de adultos y adolescentes > 12 años infectados por el VIH La demostración del beneficio de Kivexa adm 1 vez al día se basa principalmente en estudios realizados en pacientes naive asintomáticos

REACCIONES ADVERSAS n n ACIDOSIS LÁCTICA PANCREATITIS DISFUNCIÓN MITOCONDRIAL: Trastornos hematológicos y metabólicos REACCIÓN DE HIPERSENSIBILIDAD Aparece fiebre y/o erupción, signos y síntomas respiratorios (tos, disnea), síntomas GI (vómitos, diarrea, dolor abdominal) ¨ Empeoran al continuar el tto y ponen en peligro la vida del paciente ¨

NUEVOS INHIBIDORES PROTEASA REYATAZ® - ATAZANAVIR TIPRANAVIR TELZIR® - LEXIVA® - FOSAMPRENAVIR
Aprobado FDA junio 2003 Aprobado EMEA marzo 2004 HSVO - 15 PACIENTES

PRESENTACIONES n n REYATAZ 100 MG cápsulas duras - blister - 60 cápsulas REYATAZ 150 MG cápsulas duras - blister - 60 cápsulas REYATAZ 200 MG cápsulas duras - blister - 60 cápsulas REYATAZ 50 MG/1. 5 G polvo oral (no disponible) COSTE 300 mg ATV/100 mg RTV PVL= 468 € pac/mes 400 mg LPV/100 mg RTV PVL= 379 € pac/mes

MECANISMO DE ACCIÓN n Es un inhibidor de la proteasa del VIH-1. Inhibe el procesamiento específico del virus de las proteínas víricas Gag-Pol en céls infectadas n Previene de este modo la formación de viriones maduros y la infección de otras células

INDICACIONES TERAPÉUTICAS Tratamiento de pacientes adultos infectados por el VIH-1 previamente tratados y en combinación con otros fármacos antirretrovirales Los datos son insuficientes para una dosis de tto en pacientes naive No se espera eficacia en pacientes con cepas resistentes a múltiples IP (> 4 mutaciones) La elección de REYATAZ se basa en los datos de resistencia viral individual y el historial del tratamiento de los pacientes

EFICACIA EN PAC NAIVE n Estudio AI 424 -007 n Estudio AI 424 -008 (ATZ y NFV tuvieron respuestas similares Sanne I, et al. Results of a phase 2 clinical trial at 48 weeks: a dose-ranging, safety, and efficacy comparative trial of ATZ at three doses in combination with dd. I and d 4 T in antiretroviral-naive subjects. J Acquir Immune Defic Syndr 2003; 32(1): 18 -29 cuando cada uno se combinó con 2 análogos) n n Estudio AI 424 -044 (seguimiento del anterior) Estudio AI 424 -034 (compara ATZ con EFV cada uno combinado con AZT y 3 TC, en la semana 48 los resultados virológicos fueron comparables)

EFICACIA EN PACIENTES PRETRATADOS n n El ATZ fue inferior a LPV/RTV pero cdo se comparó ATZ/RTV con LPV/RTV o SQV/RTV se obtuvieron resultados similares Estudio AI 424009 Estudio AI 424 -043 Estudio AI 424 -045 (La combinación ATZ + RTV posee una actividad antirretroviral similar y menos efectos hiperlipemiantes que otros regímenes que contienen IP potenciados con RTV)

POSOLOGIA - FARMACOCINÉTICA n n n Dosis ¨ 400 mg ATZ + 100 mg RTV/ 24 h (CON EFAVIRENZ) ¨ 300 mg ATZ + 100 mg RTV/ 24 h Farmacocinética ¨ t 1/2 = 4 -7 horas BD= 68% ¨ Administrar con alimentos para disminuir la variabilidad inter- e intra- sujeto Metabolismo ¨ Vía citocromo P 450 CYP 3 A 4

SITUACIONES ESPECIALES n INSUFICIENCIA RENAL (IR) ¨ no existen datos suficientes ¨ se espera que el impacto sobre la IR sea el mínimo ¨ no es necesario ajustar la dosis n INSUFICIENCIA HEPÁTICA (IH) ¨ se metaboliza ppalmente en hígado ¨ se espera que las cc aumenten en pac con IH moderada o grave ¨ utilizar con precaución en pac con IH leve

n Embarazo ¨ No existen estudios adecuados ¨ En animales no existe toxicidad selectiva durante el desarrollo o efectos sobre la función reproductora ¨ Debe adm en embarazo beneficio > riesgo ¨ Se desconoce si produce hiperbilirrubinemia fisiológica en embarazo o kernicterus en neonato y lactantes n Lactantes, bebes, niños y adolescentes ¨ la eficacia y seguridad no ha sido establecida en esta población

CONTRAINDICACIONES + Hipersensibilidad + Insuficiencia hepática moderada a grave + Rifampicina + Fcos sustratos del CYP 3 A 4 (ergotamina, quinidina …) + Hierba de San Juan

REACCIONES ADVERSAS ¨ Cefalea , dolor abdominal, nauseas, diarrea ¨ Rash ¨ Provoca menor elevación de lípidos en sangre comparado con otros IP. U otras alteraciones metabólicas como resistencia a la insulina ¨ Menor relación con lipodistrofia ¨ Elevación de la bilirrubina plasmática (efecto dosis dependiente relacionado con la inhibición de la UDP- glucuronosil transferasa). Ictericia 6%. No obliga a suspender el fármaco.

INTERACCIONES n ATZ + RTV-------------------- DIDANOSINA ¨ n ATZ ------------- ANTICONCEPTIVOS ORALES ¨ n Uso no recomendado ATZ -------------SIMVATATINA/LOVASTATINA ¨ n Evitar el uso concomitante ATZ + RTV --------- FCOS INDUCTORES CYP 3 A 4 ¨ n Tomar 2 horas después de la adm de ATZ No administrar ATZ --------------------------TENOFOVIR

INTERACCIONES n ATZ ---------------------------INDINAVIR ¨ n ATZ + RTV -------------------- EFAVIRENZ ¨ n No administrar por hiperbilirrubinemia ↑ dosis a 400 mg ATZ + 100 mg RTV con 600 mg de EFV ATZ + RTV --------------------OMEPRAZOL ¨ ↓ AUC, Cmin y Cmáx plasmática de ATZ ¨ No administrar concomitantemente

RESISTENCIAS PACIENTES NAIVE Aparece por selección de cambios específicos y no compromete la sensibilidad a otros IP La sustitución I 50 L es la mutación característica No existe resistencia cruzada ATZ- amprenavir PACIENTES PRETRATADOS Se produce por acumulación de sustituciones de resistencia primaria y secundaria Existe resistencia cruzada de alto grado cuando hay > 5 mutaciones.

VENTAJAS TERAPÉUTICAS MEJOR TOLERANCIA GI n NO INDUCE ALTERACION LIPIDOS (incluso puede revertir las alteracionesproducidas por otros IP(nelfinavir) (AI 424 -044) n MEJOR POSOLOGÍA : único IP con dosis 1 diaria SQV+RTV suponen 9 cáps. Cáps más pequeñas n BAJA RESISTENCIA n CEPAS VIRALES RESISTENTES A 1 O 2 IP MANTIENEN SENSIBILIDAD A ATZ n ES UNA ALTERNATIVA A LPV/RTV * n * Haas DW, et al. Therapy with atazanavir plus saquinavir in patients failing active antiretrovira randomized comparative pilot trial. AIDS 2003; 17: 1339 -1349

DESVENTAJAS TERAPÉUTICAS -Mayor incidencia de hiperbilirrubinemia asintomática a expensas de bilirrubina indirecta sin hepatotoxicidad -Debe tomarse con comidas -Falta de datos de pac pediátricos -Gran nº de interacciones con otros antirretrovirales - Mayor coste

TIPRANAVIR - TPV Precio aprox: 600 euros HSVO ---- 2 PACIENTES

TIPRANAVIR (IP) n n Estructura química no peptídica resto IP Dosis ¨ 500 mg TPV/ 200 mg RTV cada 12 h Farmacocinética ¨ Elevada unión proteínas plasmáticas ¨ Baja BD oral por ello formulación en cáps con p. a. Emulsionado (SEDDS) ¨ debe adm con alimentos Metabolismo ¨ Vía citocromo P 450 ( por ello adm con dosis bajas de ritonavir). Puede necesitar ajuste de dosis en insuficiencia hepática

TIPRANAVIR n n Efectos adversos ¨ GI: diarrea en un 94% cede espontáneamente al continuar el tto o con antidiarreicos. ¨ nauseas, vómitos y dolor abdominal; > si se asocia con ritonavir ¨ rash ¨ ↑ transaminasas y bilirrubina Interacciones ¨ Se metaboliza por CYP 3 A 4

TIPRANAVIR (IP) n Eficacia ¨ Especialmente indicado para pacientes pretratados. Tiene eficacia contra cepas con resistencias a otros IP n Resistencias ¨ necesita de 15 a 20 mutaciones para reducir su eficacia ¨ se requieren múltiples cambios en la proteasa para que se pierda la sensibilidad a tipranavir ¨ Gran utilidad en pac con fracaso previo a otros IP (relacionado con su estructura no peptídica)

TELZIR® - LEXIVA® FOSAMPRENAVIR Aprobado por la EMEA 12 julio 2004

TELZIR® 700 mg / C 60 Comprimidos con película HSVO ------ 4 PACIENTES

MECANISMO DE ACCIÓN n n Es el precursor de amprenavir y en el que se convierte durante la absorción Inhibe la proteasa del VIH-1 impidiendo la formación del virus maduro y la infección de nuevas células

INDICACIONES n n En combinación con RTV a dosis bajas está indicado para el tto de adultos infectados por VIH-1 en combinación con otros agentes antirretrovirales En pac tratados previamente de forma moderada con antirretrovirales FOS/RTV no ha demostrado ser tan eficaz como LPV/RTV En pac tratados previamente de forma intensiva no se ha estudiado el uso de FOS/RTV En pac tratados previamente con IP la elección debe basarse en resistencia viral y antecedentes de tto

ESTUDIOS QUE PERMITIERON SU APROBACION n APV 20001 n APV 30001 -30002 n APV 30003 estudio en fase II que evalúa la eficacia, seguridad y tolerabilidad de FOS frente APV estudio en fase III en pac naive que evalúan la eficacia de FOS con o sin RTV estudio en fase III en pac previamente tratados que evalúa la eficacia de FOS/RTV en régimen de 1 o 2 veces al día Actualmente se lleva a cabo el ensayo FOS-GW 433908 programa de a expandido de fosamprenavir/ritonavir para pacientes VIH

EFICACIA n n n En pac naive TELZIR con RTV proporciona una supresión virológica comparable a nelfinavir En pac pretratados TELZIR con RTV proporciona supresión virológica durante 48 semanas aunque no ha demostrado ser tan eficaz como LPV/RTV En pac naive se ha demostrado que la potenciación con RTV evita la aparición de mutaciones frente a IP

POSOLOGIA n DOSIS solo debe adm con RTV a dosis bajas ¨ ¨ n NIÑOS Y ADOLESCENTES ¨ n No se considera necesario ajustar la dosis ALTERACIÓN HEPÁTICA ¨ n No se ha establecido seguridad ni eficacia ALTERACIÓN RENAL ¨ n 700 mg FOS + 100 mg RTV / 12 h Con o sin alimentos Utilizar con precaución en pac con alt hepática leve y contraindicado en pac con alt hepática moderada-grave EMBARAZO ¨ No existe experiencia clínica

CONTRAINDICACIONES n n Hipersensibilidad Alteración hepática grave No adm con fármacos con estrecho márgen terapéutico sustratos del cit P 450 No adm con rifampicina ni hipérico

REACCIONES ADVERSAS n n n Molestias GI: diarrea Cefalea, mareos, fatiga Erupción cutánea ↑ AST, ALT, lipasa y TG lipodistrofia

INTERACCIONES n n Sustratos de CYP 3 A 4 con estrecho margen terapéutico Rifampicina Hipérico Usar con precaución con nevirapina

VENTAJAS n n n Ha sido diseñado para optimizar el uso de amprenavir la ingesta de comp. Mayor BD y mejor formulación Se adm con RTV : 700 mg FOS/100 mg RTV 2 veces al día Como característica diferencial con otros IP puede adm con o sin comidas

DESVENTAJAS n n n Mismo perfil de toxicidad que otros IP El tamaño de las pastillas es grande como el resto de IP Datos limitados sobre resistencias cruzadas

CONCLUSION SOBRE NUEVOS IP Inhibidores de la proteasa vs efavirenz EFAVIRENZ SE ADM 1 VEZ AL DIA HACEN FALTA ESTUDIOS COMPARATIVOS DIRECTOS, existen pocos estudios que comparen IP potenciados con regímenes que contienen EFV. Estudio FOCUS (SQV+RTV vs EFV siendo favorable a EFV). Estudio CLASS ( muestra superioridad en la supresión del ARN viral en el grupo de EFV en comparación con AMP + RTV)

INHIBIDORES DE LA FUSIÓN FUZEON® ENFUVIRTIDA – T 20 Aprobado EMEA: 27 mayo 2003

PVFenvase = 1586 euros HSVO---- 5 PACIENTES FUZEON® 90 MG/ML 60 VIALES/60 DILUYENT 60 JERINGAS DE 3 ML DE CARGA(para la dil 60 JERINGAS DE 1 ML Y AGUJAS SC ( para el medicamento) / 180 TOALLITAS/ CONTENE BIOLÓGICO/VIDEO/GUÍA DE ADM.

MECANISMO DE ACCIÓN n n n Primer representante de la familia de inhibidores de la fusión. Bloquea la entrada del virus en la célula huesped. Es un péptido sintético análogo a residuos del segmento transmembrana de la gp 41 n Enfuvirtida interfiere en el cambio de conformación de la gp 41 impidiendo que la membrana del virus entre en contacto con la célula y por tanto la fusión viral con la célula diana

INDICACIONES n En combinación con otros fármacos antirretrovirales tto de pac infectados por VIH-1 que hayan recibido tto previo sin éxito con al menos un medicamento de las siguientes clases: IP, análogos y no análogos o que hayan mostrado intolerancia a ttos antirretrovirales previos.

POSOLOGIA n n 90 mg subcutáneo / 12 h en abdomen, brazo o muslo (evitar cara externa de mmii y mmss) 2 mg/kg en niños / 12 h ( la experiencia se basa en un nº muy limitado de niños) n n n INSUFICIENCIA RENAL: no existen estudios INSUFICIENCIA HEPÁTICA: no existen estudios EMBARAZO: no existen estudios

EFECTOS ADVERSOS n Relacionados con el punto de inyección dolor eritema y prurito induración n n No asociado a alt en distribución de grasa, metabolismo de glc y lípidos La neumonía bacteriana fue más frecuente con T 20 INTERACCIONES No se esperan interacciones con fármacos que se metabolicen vía cit P 450

VENTAJAS n Generalmente es aceptable en pacientes con limitado nº de alternativas. Se valora esta opción en el 2º, 3º o 4º fracaso según el nº de fcos activos queden como opciones INCONVENIENTES n n Necesidad de adquirir el hábito de preparación y adm del fármaco. Para la disolución del polvo pueden ser necesarios 45 min El momento optimo para su prescripción implica valorar su incomodidad de adm y el coste

OTROS INHIBIDORES DE LA ENTRADA
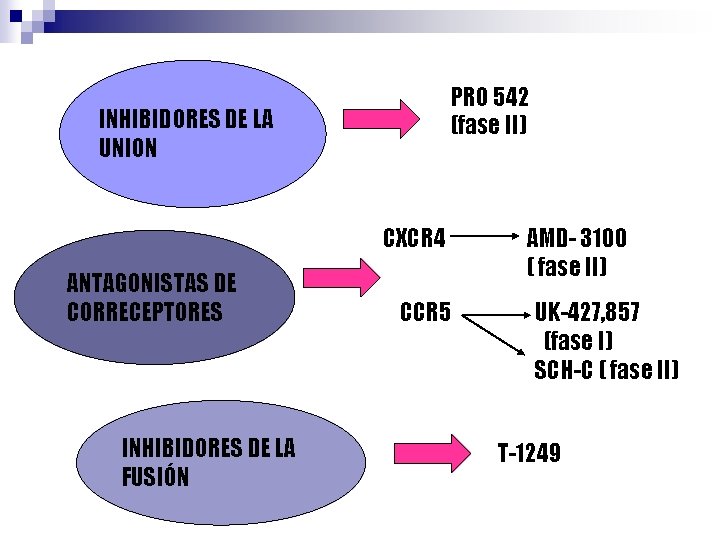
PRO 542 (fase II) INHIBIDORES DE LA UNION CXCR 4 ANTAGONISTAS DE CORRECEPTORES INHIBIDORES DE LA FUSIÓN CCR 5 AMD- 3100 ( fase II) UK-427, 857 (fase I) SCH-C ( fase II) T-1249

INTERACCIÓN DIDANOSINA-TENOFOVIR

EN DICIEMBRE 2002 n n Se observó que cdo se adm didanosina junto con tenofovir existe un aumento medio del área bajo la curva (AUC) de didanosina del 44 -60%. Didanosina 250 mg en ayunas + tenofovir produjo un AUC ~ al de didanosina 400 mg sólo en ayunas. Se recomienda utilizar didanosina 250 mg cuando se adm tenofovir Dosificación de Videx EC cuando se coadministra con Tenofovir DF- Actualización a diciemb Departamento científico Bristol-Myers Squibb

DESCENSO DE CD 4 n n ↓ CD 4 pac dd. I + TDF a pesar de suspensión virológica. Estudio 302 pac. 50% ↓ CD 4 > 100 en 48 sem. Recomendación: ↓ dd. I de 400 mg a 250 mg cdo se adm con TDF ¿DEBIDO A MUTACIONES? ¿DEBIDO A TOXICIDAD CELULAR? . Negredo E. et al. CD 4 cell count decline in patients receiving didanosine and tenofovir- based regimens despite undetectable viral load. AIDS 2004 Feb 20; 18(3): 459 -63. Leon A, et al. Early virological failure in treatment-naive HIV-infected adults receiving didanosine and tenofovir plus efavirenz or nevirapine. AIDS 2005 Jan 28; 19(2): 213 -5. Kakuda TN et al. CD 4 cell decline with didanosine and tenofovir and failure of triple nucleoside/nucleotide regimens may be related. AIDS. 2004 Dec 3; 18(18): 2442 -4. No abstract available.

VACACIONES TERAPEUTICAS

n n Existen estudios para evaluar la interrupción estructurada (o supervisada) del tratamiento (IST) Comprenden estrategias de tto intermitente en pacientes con replicación viral controlada Objetivo determinar si varios ciclos de interrupción pueden reducir la duración de la exposición al tto sin comprometer el recuento de CD 4 Riesgo aparición de resistencias Editorial técnico. Farmacia Hospitalaria. Suplemento vol 28

DOBLE POTENCIACIÓN

n n n Nueva estrategia terapéutica a base de IP que combina la eficacia de 2 Ips potenciados simultáneamente con una minidosis de RTV Principalmente lopinavir, atazanavir y fosamprenavir con saquinavir “Algunos datos sugieren que en pac con fracaso virológico exhiben mejoras inmunológicas y virológicas bastante superiores en tratamientos con dos IP que con 1 IP”

BIBLIOGRAFÍA n n n n n Ficha técnica EMEA: informes de aprobación Recomendaciones de 2004 del Grupo de EEUU de la International AIDS Society. Tratamiento de la infección por VIH en adultos. JAMA 2004 Jul; 292(2): 251 -265 Goldsmith DR, Perry CM. Atazanavir. Drugs 2003; 63 (16)-1679 -95 Inhibidores de la fusión. Número 1 may-jun 2004 Cahn P. Emtricitabine: a new nucleoside analogue for once-daily antiretroviral therapy. Expert Opinion on Investigational Drugs 2004; 13(1): 55 -68 Guardiola, Soriano. Tratamiento de la infección por VIH-SIDA. Fármacos y combinaciones. Ed. Publicaciones Permanyer. Sexta edición. Rivero A. Tratamiento antirretroviral anuario 2004. Edimsa. Tercer seminario de Atención Farmacéutica. Jornadas de actualización terapéutica en el tratamiento antirretroviral.
- Slides: 91