5 Metalle 5 2 der metallische Zustand Intermetallische























































































































- Slides: 150

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Ionenverbindungen und kovalente Verbindungen sind meist stöchiometrisch zusammengesetzt - bei Verbindungen zwischen Metallen ist das Gesetz der konstanten Proportionen häufig nicht erfüllt, - die Zusammensetzung kann innerhalb weiter Grenzen schwanken: + Beispiel Messing, Schwankungsbreite von Cu 0, 34 Zn 0, 66 - Cu 0, 42 Zn 0, 58

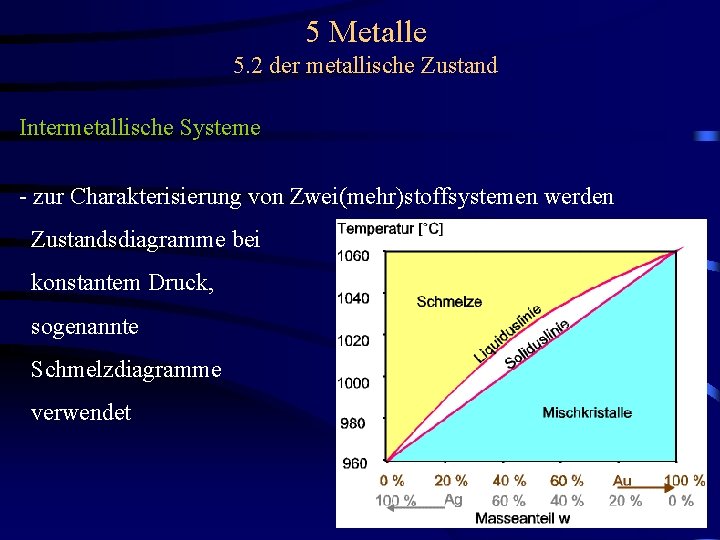
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - zur Charakterisierung von Zwei(mehr)stoffsystemen werden Zustandsdiagramme bei konstantem Druck, sogenannte Schmelzdiagramme verwendet

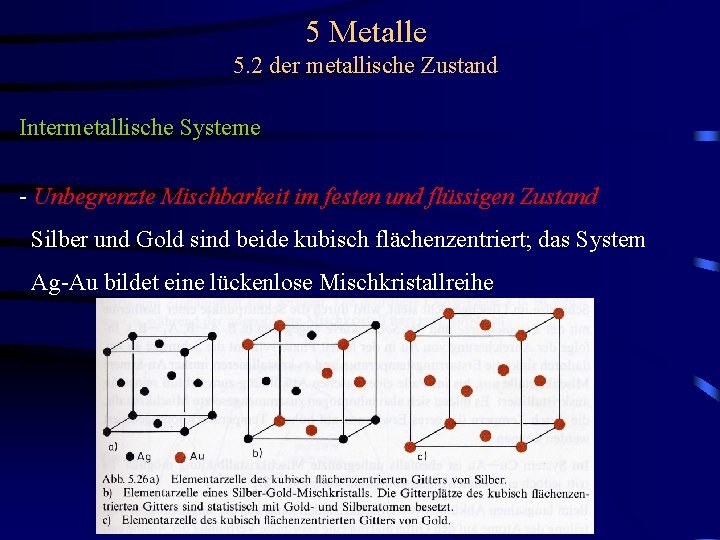
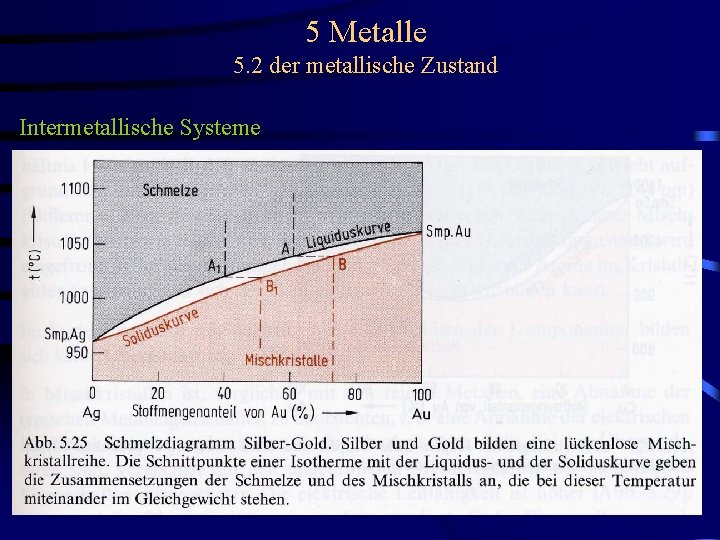
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Unbegrenzte Mischbarkeit im festen und flüssigen Zustand Silber und Gold sind beide kubisch flächenzentriert; das System Ag-Au bildet eine lückenlose Mischkristallreihe

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - zur Charakterisierung von Zwei(mehr)stoffsystemen werden Zustandsdiagramme bei konstantem Druck, sogenannte Schmelzdiagramme verwendet

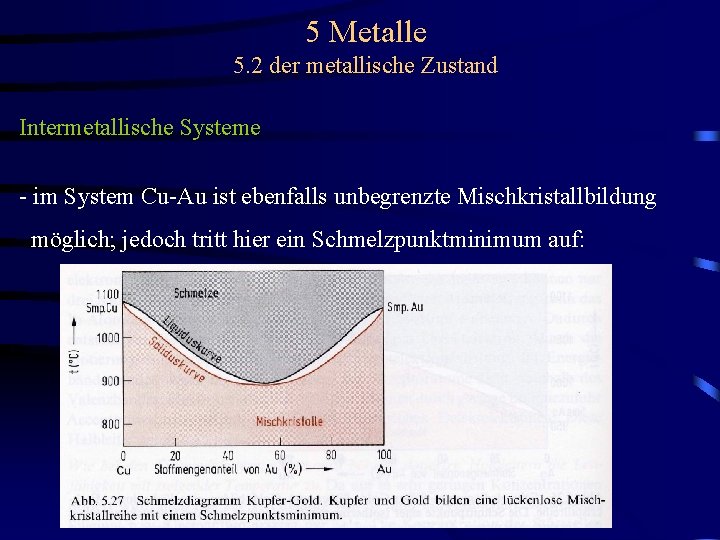
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - im System Cu-Au ist ebenfalls unbegrenzte Mischkristallbildung möglich; jedoch tritt hier ein Schmelzpunktminimum auf:

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - im System Cu-Au existieren Überstrukturen, die sich durch relativ höhere elektrische Leitfähigkeit auszeichnen:

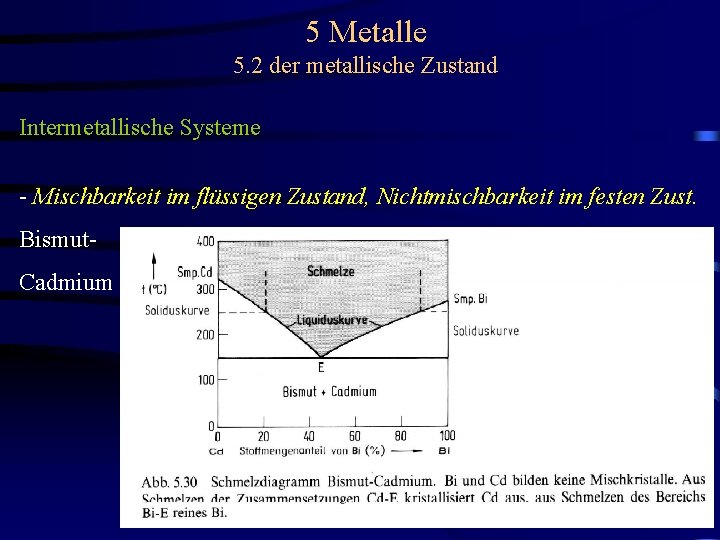
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Mischbarkeit im flüssigen Zustand, Nichtmischbarkeit im festen Zust. Bismut. Cadmium

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - unbegrenzte Mischbarkeit im flüssigen Zustand, begrenzte Mischbarkeit im festen Zustand Kupfer. Silber

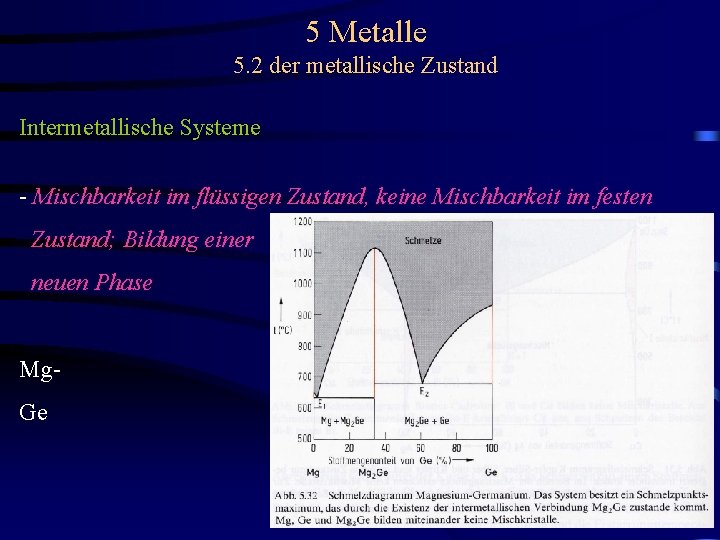
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Mischbarkeit im flüssigen Zustand, keine Mischbarkeit im festen Zustand; Bildung einer neuen Phase Mg. Ge

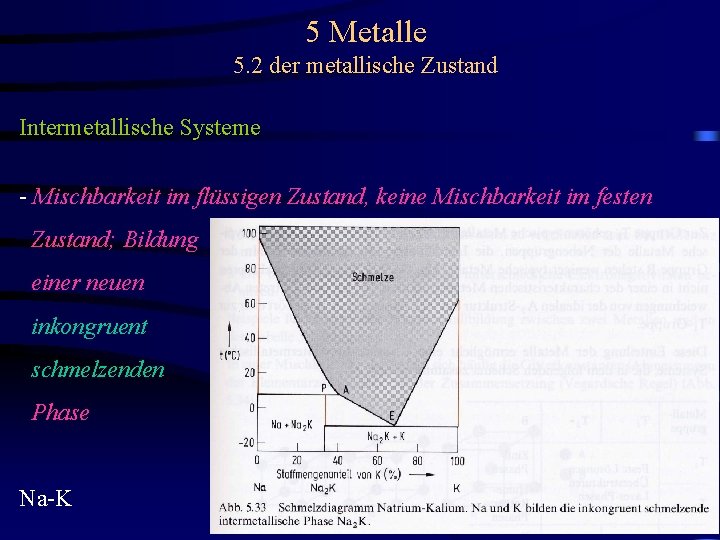
5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Mischbarkeit im flüssigen Zustand, keine Mischbarkeit im festen Zustand; Bildung einer neuen inkongruent schmelzenden Phase Na-K

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme - Nichtmischbarkeit im festen und flüssigen Zustand Eisen-Blei

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme- häufige intermetallische Phasen - Metalle können ihrer Stellung im PSE nach in 3 Gruppen eingeteilt werden: T 1, T 2 und B

5 Metalle 5. 2 der metallische Zustand Intermetallische Systeme- häufige intermetallische Phasen - Metalle können ihrer Stellung im PSE nach in 3 Gruppen eingeteilt werden: T 1, T 2 und B - hierdurch wird eine Klassifizierung der intermetallischen Systeme möglich:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Einleitung - alle Nebengruppenelemente sind Metalle - außer den s-Elektronen der äußersten Schale sind auch d-Elektronen der zweitäußersten Schale an chemischen Bindungen beteiligt - die meisten Ionen haben unvollständig besetzte d-Niveaus

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Einleitung - alle Nebengruppenelemente sind Metalle - außer den s-Elektronen der äußersten Schale sind auch d-Elektronen der zweitäußersten Schale an chemischen Bindungen beteiligt - die meisten Ionen haben unvollständig besetzte d-Niveaus - Die Ionen sind häufig gefärbt und neigen zur Komplexbildung

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Einleitung - alle Nebengruppenelemente sind Metalle - außer den s-Elektronen der äußersten Schale sind auch d-Elektronen der zweitäußersten Schale an chemischen Bindungen beteiligt - die meisten Ionen haben unvollständig besetzte d-Niveaus - Die Ionen sind häufig gefärbt und neigen zur Komplexbildung - durch WW paramagnetischer Momente der Ionen kann kollektiver Magnetismus entstehen - viele nichtstöchiometrische Verbindungen

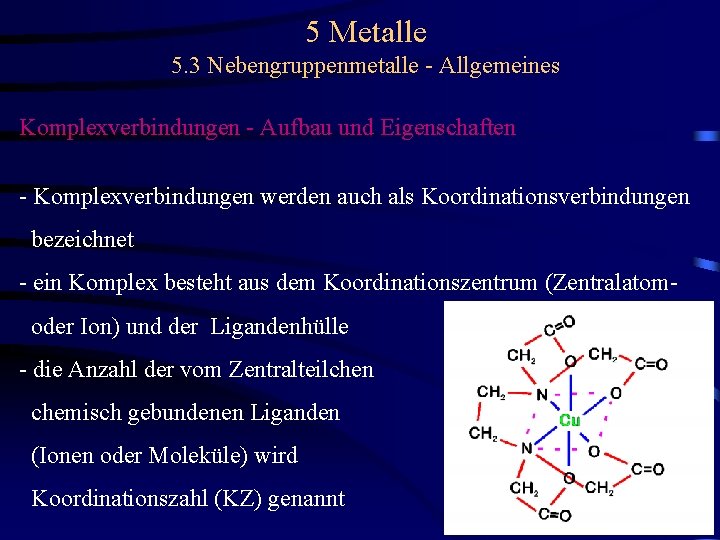
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - Komplexverbindungen werden auch als Koordinationsverbindungen bezeichnet - ein Komplex besteht aus dem Koordinationszentrum (Zentralatomoder Ion) und der Ligandenhülle - die Anzahl der vom Zentralteilchen chemisch gebundenen Liganden (Ionen oder Moleküle) wird Koordinationszahl (KZ) genannt

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - Beispiele für Komplexverbindungen

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - Komplexe sind an ihren typischen Eigenschaften und Reaktionen zu erkennen: + Farbe + elektrolytische Eigenschaften + Ionenreaktionen (z. B. „Maskierung“)

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - Komplexe sind an ihren typischen Eigenschaften und Reaktionen zu erkennen: - Komplexe mit einem Koordinationszentrum sind einkernige Komplexe; mehrkernige Komplexe besitzen mehrere Koordinationszentren:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - Komplexe sind an ihren typischen Eigenschaften und Reaktionen zu erkennen: - Komplexe mit einem Koordinationszentrum sind einkernige Komplexe; mehrkernige Komplexe besitzen mehrere Koordinationszentren - einzähnige Liganden besetzen im Komplex nur eine Koordinationsstelle, mehrzähnige dagegen mehrere:

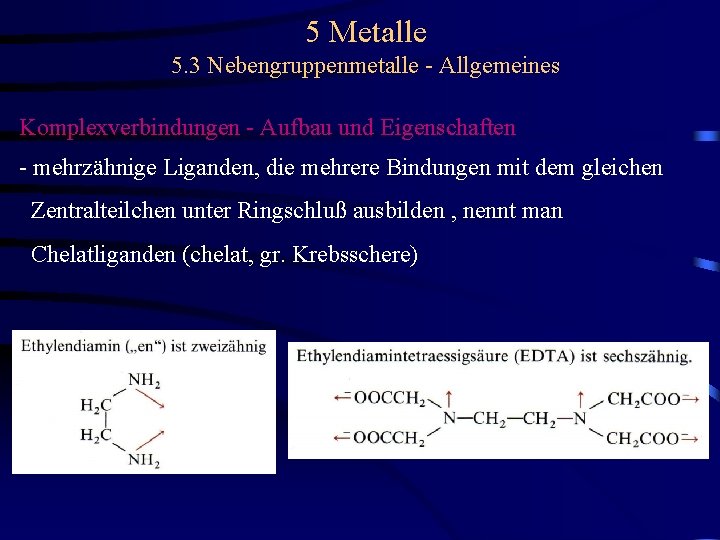
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - mehrzähnige Liganden, die mehrere Bindungen mit dem gleichen Zentralteilchen unter Ringschluß ausbilden , nennt man Chelatliganden (chelat, gr. Krebsschere)

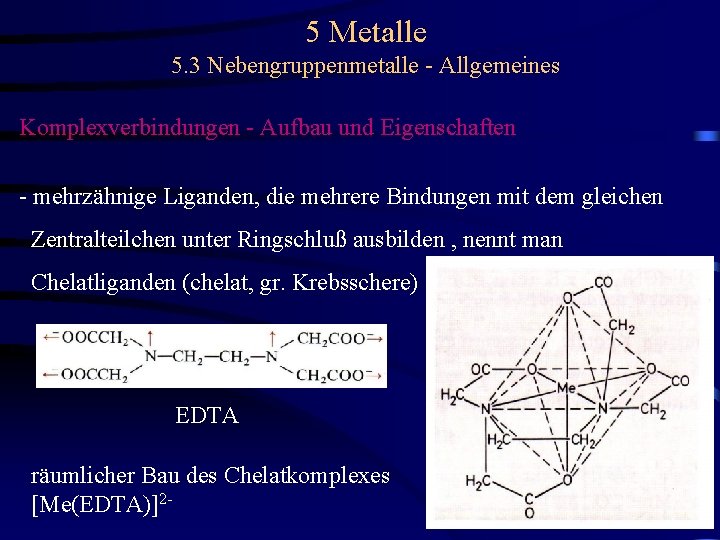
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Aufbau und Eigenschaften - mehrzähnige Liganden, die mehrere Bindungen mit dem gleichen Zentralteilchen unter Ringschluß ausbilden , nennt man Chelatliganden (chelat, gr. Krebsschere) EDTA räumlicher Bau des Chelatkomplexes [Me(EDTA)]2 -

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Nomenklatur - zuerst wird der Name der Liganden, dann der des Zentralatoms angegeben - anionische Liganden werden durch ein angehängtes o gekennzeichnet

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Nomenklatur - zuerst wird der Name der Liganden, dann der des Zentralatoms angegeben - anionische Liganden werden durch ein angehängtes o gekennzeichnet - die Ligandenanzahl wird mit den griechischen Präfixen mono, di, tri, tetra, penta, hexa, hepta, octa bezeichnet:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Nomenklatur - zuerst wird der Name der Liganden, dann der des Zentralatoms angegeben - anionische Liganden werden durch ein angehängtes o gekennzeichnet - die Ligandenanzahl wird mit den griechischen Präfixen mono, di, tri, tetra, penta, hexa, hepta, octa bezeichnet - in negativ geladenen Komplexen endet der Name auf -at:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Nomenklatur - zuerst wird der Name der Liganden, dann der des Zentralatoms angegeben - anionische Liganden werden durch ein angehängtes o gekennzeichnet - die Ligandenanzahl wird mit den griechischen Präfixen mono, di, tri, tetra, penta, hexa, hepta, octa bezeichnet - in negativ geladenen Komplexen endet der Name auf -at: - bei verschiedenen Liganden ist die Reihenfolge alphabetisch:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - häufige Kordinationszahlen in Komplexen sind 2, 4 und 6 - die räumliche Anordnung ist dann linear (2), tetraedrisch oder quadratisch-planar (4) und oktaedrisch (6) - für die meisten Komplexe gibt es bei wechselnden Liganden Komplexe mit unterschiedlicher Koordination + z. B. kann Ni 2+ oktaedrisch, tetraedrisch und quadratisch-planar koordiniert sein

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - für die meisten Komplexe gibt es bei wechselnden Liganden Komplexe mit unterschiedlicher Koordination + z. B. kann Ni 2+ oktaedrisch, tetraedrisch und quadratisch-planar koordiniert sein - andere Ionen bevorzugen dagegen bestimmte Koordinationen: + Cr 3+, Co 3+ und Pt 4+ die oktaedrische, + Pt 2+ und Pd 2+ die quadratisch-planare und + Ag+, Cu+ und Au+ die lineare Koordination

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen räumlicher Bau, Stereoisomerie

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen räumlicher Bau, Stereoisomerie

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen räumlicher Bau, Stereoisomerie

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen räumlicher Bau, Stereoisomerie

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - Komplexe, dieselbe chemische Zusammensetzung und Ladung, aber einen verschiedenen räumlichen Aufbau haben, sind stereoisomer - man unterscheidet die folgenden Arten der Stereoisomerie:

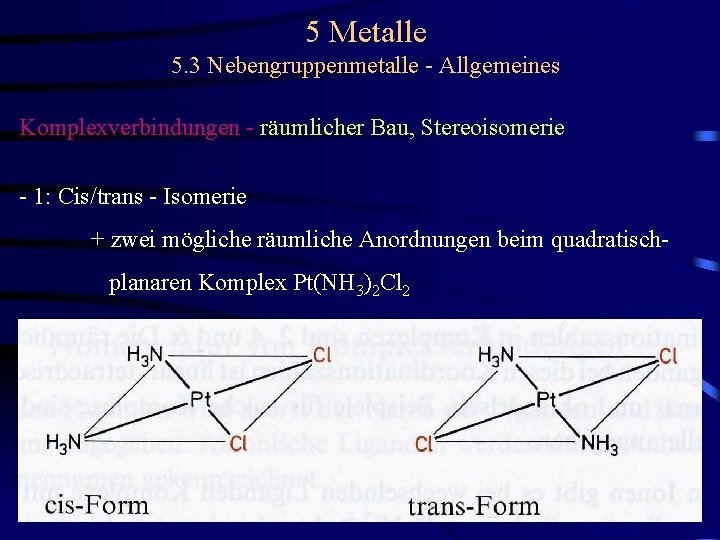
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 1: Cis/trans - Isomerie + zwei mögliche räumliche Anordnungen beim quadratischplanaren Komplex Pt(NH 3)2 Cl 2

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 1: Cis/trans - Isomerie + auch möglich bei oktaedrischen Komplexen; Beispiel [Cr(NH 3)4 Cl 2]+

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 1: Cis/trans - Isomerie + zwei mögliche räumliche Anordnungen beim quadratischplanaren Komplex Pt(NH 3)2 Cl 2 + auch möglich bei oktaedrischen Komplexen; Beispiel [Cr(NH 3)4 Cl 2]+ + bei tetraedrischen Komplexen ist keine cis/trans-Isom. mögl.

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 2: Optische Isomerie (Spiegelbildisomerie) + bei tetraedrischer Koordination mit 4 verschiedenen Liganden treten zwei Formen auf, die sich nicht zur Deckung bringen lassen

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 2: Optische Isomerie (Spiegelbildisomerie) + bei tetraedrischer Koordination mit 4 verschiedenen Liganden treten zwei Formen auf, die sich nicht zur Deckung bringen lassen

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 2: Optische Isomerie (Spiegelbildisomerie) + bei tetraedrischer Koordination mit 4 verschiedenen Liganden treten zwei Formen auf, die sich nicht zur Deckung bringen lassen

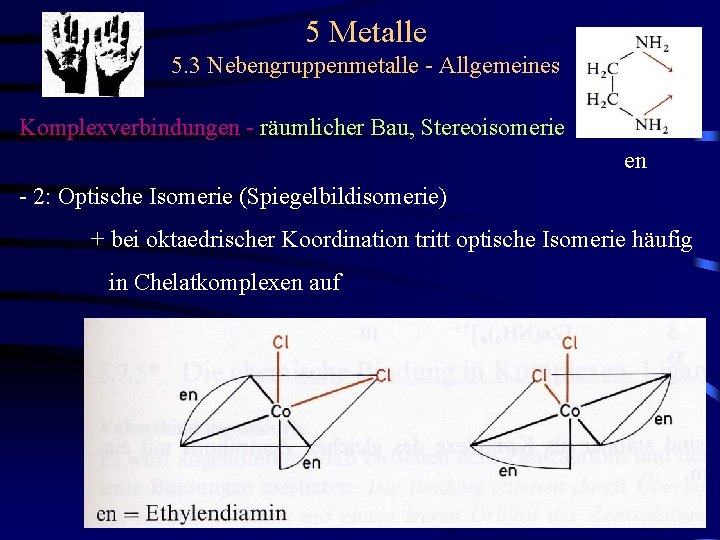
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie en - 2: Optische Isomerie (Spiegelbildisomerie) + bei oktaedrischer Koordination tritt optische Isomerie häufig in Chelatkomplexen auf

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 2: Optische Isomerie (Spiegelbildisomerie) + bei tetraedrischer Koordination mit 4 versch. Liganden treten zwei Formen auf, die sich nicht zur Deckung bringen lassen + bei oktaedrischer Koordination tritt optische Isomerie häufig in Chelatkomplexen auf + optische Isomere bezeichnet man auch als enantiomorph oder enantiomer; sie besitzen bis auf eine Ausnahme gleiche phys. Eigenschaften: Polarisiertes Licht wird entgegenges. gedreht

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 3: Salzisomerie + tritt auf, wenn Liganden wie CN- oder NO 2 - durch verschiedene Atome an das Zentralteilchen gebunden sind Beispiel:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 4: Koordinationsisomerie + tritt auf bei Verbindungen, bei denen Anionen und Kationen Komplexe sind: Beispiel:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - räumlicher Bau, Stereoisomerie - 5: Ionenisomerie + in einer Verbindung kann ein Ion als Ligand im Komplex oder außerhalb des Komplexes gebunden sein: Beispiel: + ein spezieller Fall der Ionenisomerie ist die Hydratisomerie:

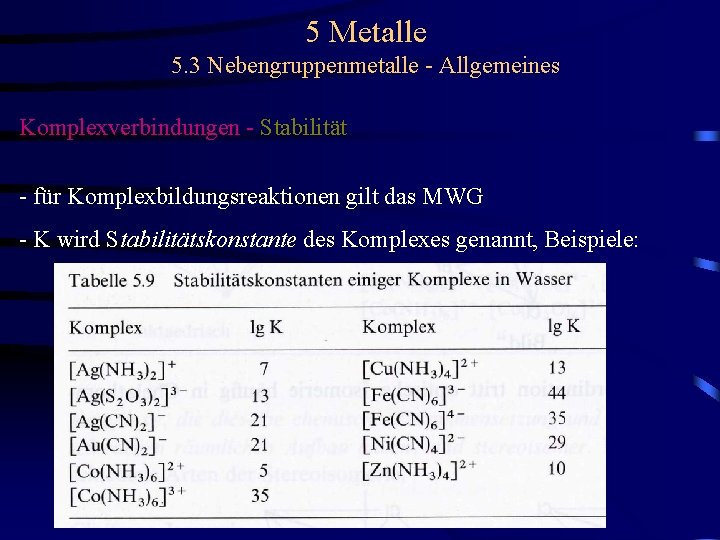
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Stabilität - für Komplexbildungsreaktionen gilt das MWG: - K wird Stabilitätskonstante des Komplexes genannt

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Komplexverbindungen - Stabilität - für Komplexbildungsreaktionen gilt das MWG - K wird Stabilitätskonstante des Komplexes genannt, Beispiele:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - Kohlenmonoxid bildet mit dem einsamen Elektronenpaar am Kohlenstoffatom eine dative s-Bindung Ligand Metall

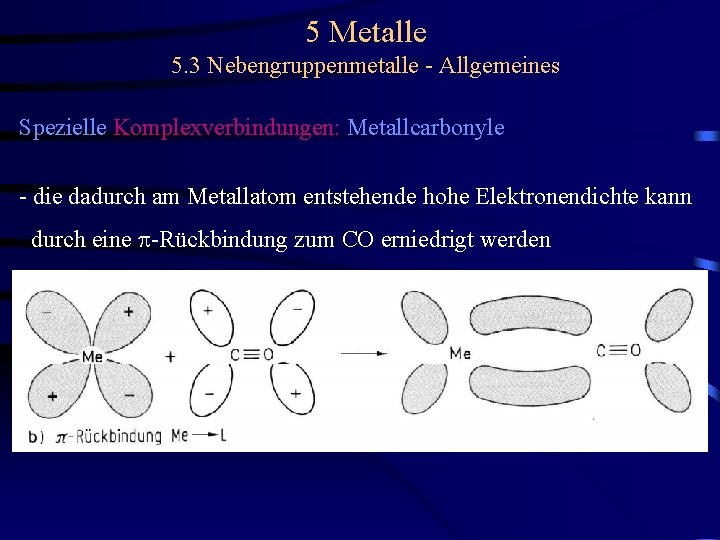
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - die dadurch am Metallatom entstehende hohe Elektronendichte kann durch eine p-Rückbindung zum CO erniedrigt werden

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - Kohlenmonoxid bildet mit dem einsamen Elektronenpaar am Kohlenstoffatom eine dative s-Bindung Ligand Metall - die dadurch am Metallatom entstehende hohe Elektronendichte kann durch eine p-Rückbindung zum CO erniedrigt werden - die resultierende Bindung besitzt zwei mesomere Formeln

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - die Zusammensetzung der meisten Carbonyle kann mit der 18 -Elektronenregel (Edelgasregel) vorhergesagt werden: + Anzahl der Valenzelektronen des Metallatoms + Anzahl der von den Liganden für s-Bindungen stammenden Elektronen = 18 + es wird die Valenzelektronenkonfiguration des nächsthöheren Edelgases erreicht

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - die Zusammensetzung der meisten Carbonyle kann mit der 18 -Elektronenregel (Edelgasregel) vorhergesagt werden:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - die Zusammensetzung der meisten Carbonyle kann mit der 18 -Elektronenregel (Edelgasregel) vorhergesagt werden - die kristallinen Carbonyle sublimieren im Vakuum - die bei RT flüssigen Carbonyle sind flüchtig, leicht entzündlich und sehr giftig!

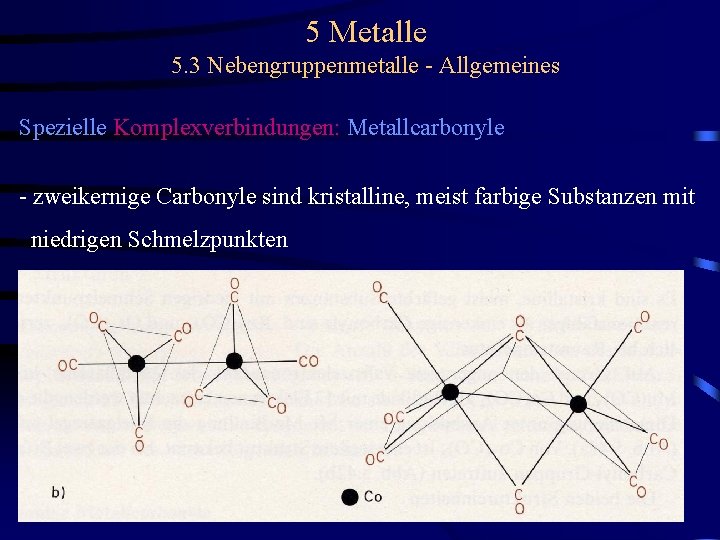
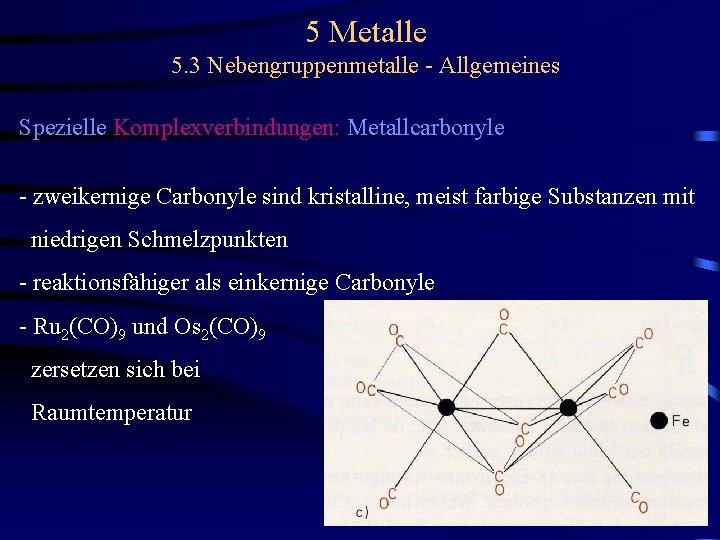
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - zweikernige Carbonyle sind kristalline, meist farbige Substanzen mit niedrigen Schmelzpunkten - reaktionsfähiger als einkernige Carbonyle - Ru 2(CO)9 und Os 2(CO)9 zersetzen sich bei Raumtemperatur

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - zweikernige Carbonyle sind kristalline, meist farbige Substanzen mit niedrigen Schmelzpunkten

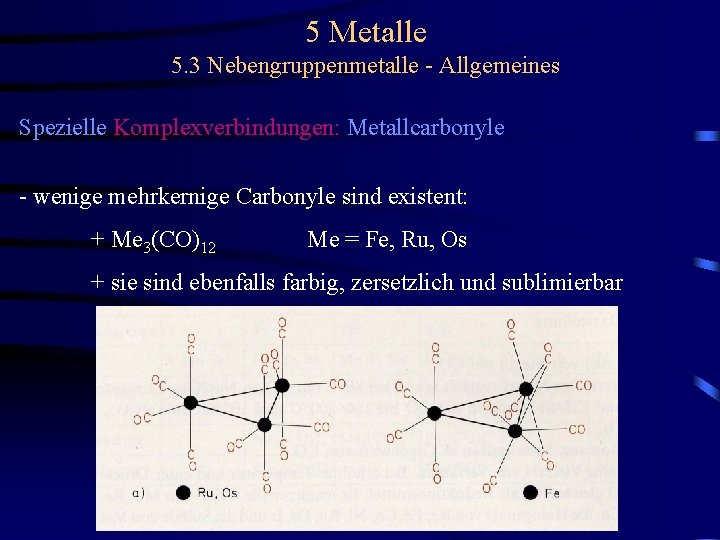
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - zweikernige Carbonyle sind kristalline, meist farbige Substanzen mit niedrigen Schmelzpunkten - reaktionsfähiger als einkernige Carbonyle - Ru 2(CO)9 und Os 2(CO)9 zersetzen sich bei Raumtemperatur - wenige mehrkernige Carbonyle sind existent: + Me 3(CO)12 Me = Fe, Ru, Os + sie sind ebenfalls farbig, zersetzlich und sublimierbar

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - zweikernige Carbonyle sind kristalline, meist farbige Substanzen mit niedrigen Schmelzpunkten - reaktionsfähiger als einkernige Carbonyle - Ru 2(CO)9 und Os 2(CO)9 zersetzen sich bei Raumtemperatur

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - wenige mehrkernige Carbonyle sind existent: + Me 3(CO)12 Me = Fe, Ru, Os + sie sind ebenfalls farbig, zersetzlich und sublimierbar

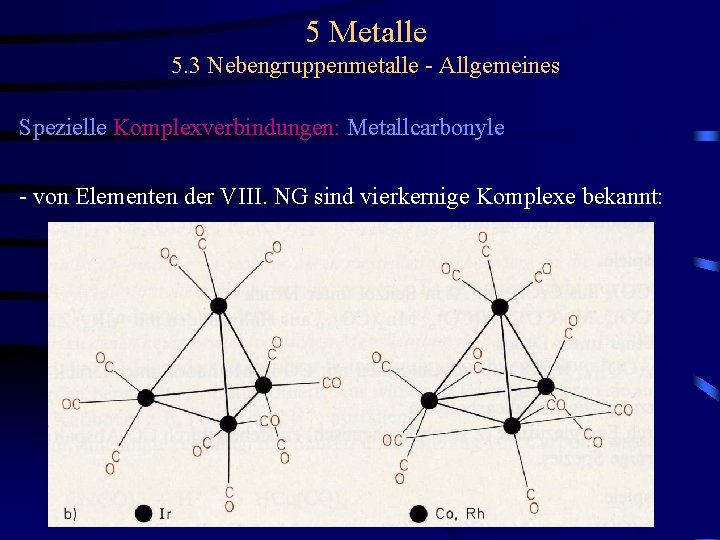
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: Metallcarbonyle - von Elementen der VIII. NG sind vierkernige Komplexe bekannt:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die Bindung Ligand Metall wird bei diesen Komplexen von den p-Elektronen organischer Verbindungen errichtet. - wie bei den Metallcarbonylen werden auch diese komplexe durch eine p-Rückbindung stabilisiert - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein

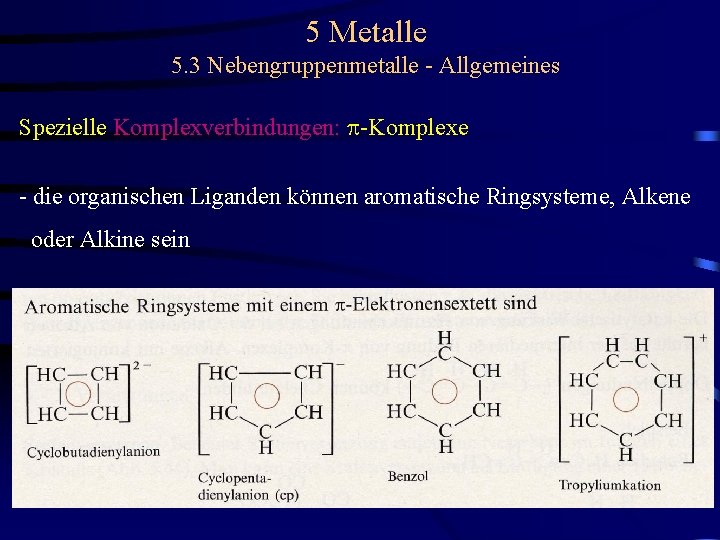
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein

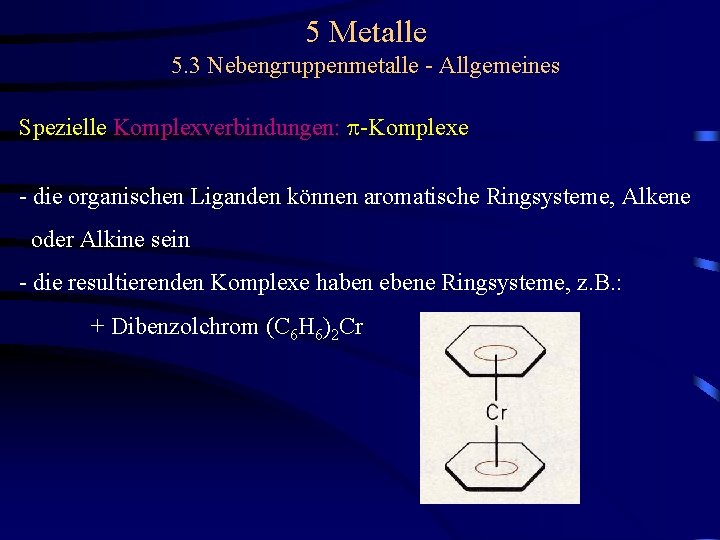
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein - die resultierenden Komplexe haben ebene Ringsysteme, z. B. : + Dibenzolchrom (C 6 H 6)2 Cr

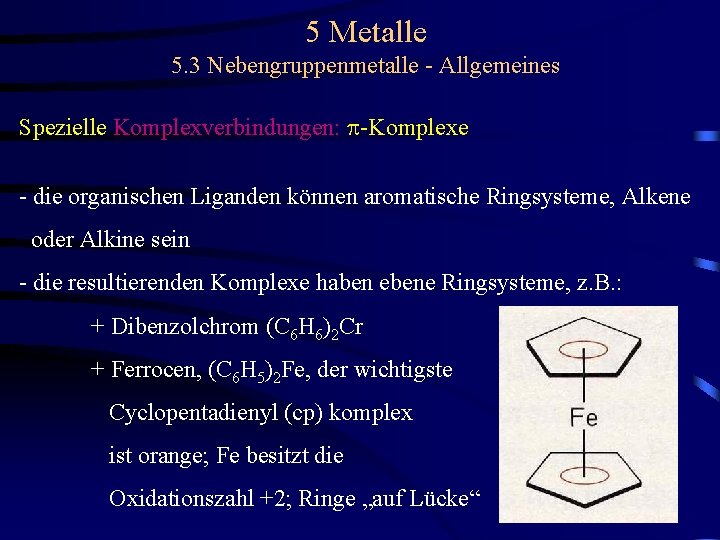
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein - die resultierenden Komplexe haben ebene Ringsysteme, z. B. : + Dibenzolchrom (C 6 H 6)2 Cr + Ferrocen, (C 6 H 5)2 Fe, der wichtigste Cyclopentadienyl (cp) komplex ist orange; Fe besitzt die Oxidationszahl +2; Ringe „auf Lücke“

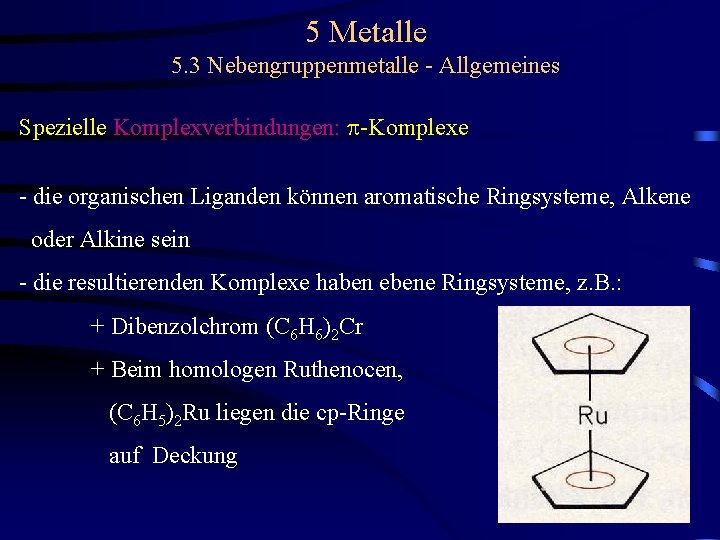
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein - die resultierenden Komplexe haben ebene Ringsysteme, z. B. : + Dibenzolchrom (C 6 H 6)2 Cr + Beim homologen Ruthenocen, (C 6 H 5)2 Ru liegen die cp-Ringe auf Deckung

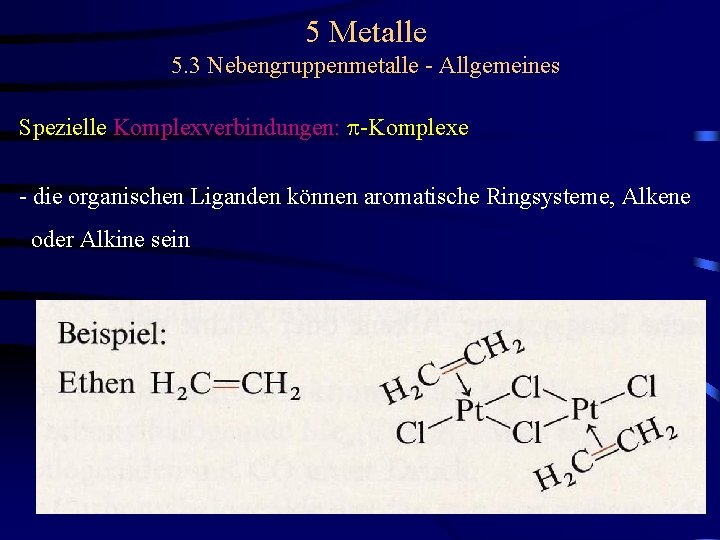
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein

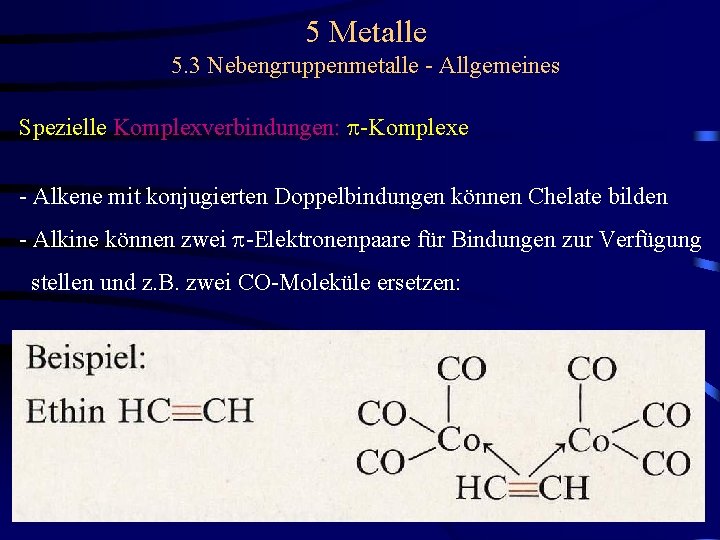
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - die organischen Liganden können aromatische Ringsysteme, Alkene oder Alkine sein - die katalytische Wirkung von Platinverbindungen bei der Oxidation von Alkenen beruht auf der intermediären Bildung von p-Komplexen - Alkene mit konjugierten Doppelbindungen können Chelate bilden:

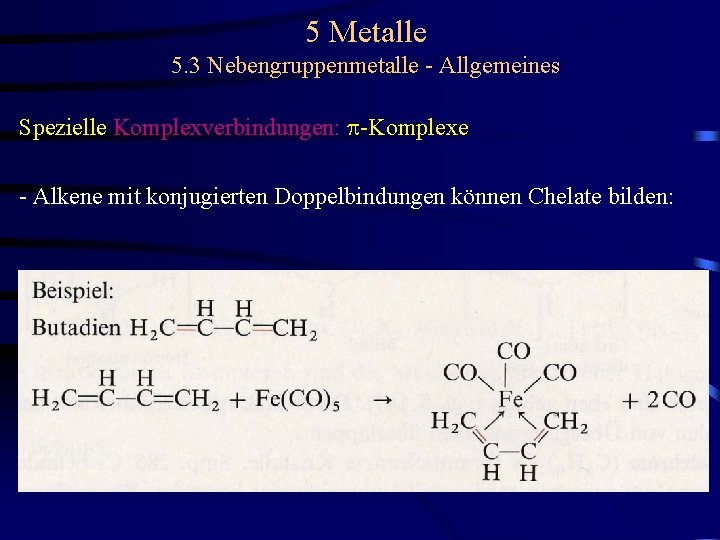
5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - Alkene mit konjugierten Doppelbindungen können Chelate bilden:

5 Metalle 5. 3 Nebengruppenmetalle - Allgemeines Spezielle Komplexverbindungen: p-Komplexe - Alkene mit konjugierten Doppelbindungen können Chelate bilden - Alkine können zwei p-Elektronenpaare für Bindungen zur Verfügung stellen und z. B. zwei CO-Moleküle ersetzen:

5 Metalle 5. 4 die 1. Nebengruppe Gruppeneigenschaften Cu

5 Metalle 5. 4 die 1. Nebengruppe Gruppeneigenschaften Ag Cu

5 Metalle 5. 4 die 1. Nebengruppe Gruppeneigenschaften Ag Cu Au

5 Metalle 5. 4 die 1. Nebengruppe Gruppeneigenschaften -

5 Metalle 5. 4 die 1. Nebengruppe Gruppeneigenschaften - die Metalle der 1. NG werden auch als Münzmetalle bezeichnet - aufgrund der Elektronenkonfiguration Auftreten in der Ox-stufe +1, daneben auch +2 und +3 möglich, seltener +4, +5 - stabilste Ox-stufen für Cu +2, für Ag +1, für Au +3 - zu den Alkalimetallen besteht nur formale Ähnlichkeit : d 10 - Konfiguration schirmt Kernladung nicht so wirkungsvoll ab wie eine Edelgaskonfiguration, daher Ionisierungsenergien größer edlerer Charakter

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - alle Münzmetalle kristallisieren kubisch-flächenzentriert mit hohen Schmelzpunkten - Kupfer ist hellrot, zäh und dehnbar - Cu besitzt nach Ag die höchste elektrische Leitfähigkeit

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - alle Münzmetalle kristallisieren kubisch-flächenzentriert mit hohen Schmelzpunkten - Kupfer ist hellrot, zäh und dehnbar - Cu besitzt nach Ag die höchste elektrische Leitfähigkeit - mit Sauerstoff bildet sich an der Oberfläche eine fest haftende Schicht von Cu 2 O

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - mit Sauerstoff bildet sich an der Oberfläche eine fest haftende Schicht von Cu 2 O - an CO 2 - und SO 3 - haltiger Luft bilden sich fest haftende Deckschichten von basischem Carbonat Cu 2 CO 3(OH)2 und Cu 2 SO 4(OH)2

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - mit Sauerstoff bildet sich an der Oberfläche eine fest haftende Schicht von Cu 2 O - an CO 2 - und SO 3 - haltiger Luft bilden sich fest haftende Deckschichten von basischem Carbonat Cu 2 CO 3(OH)2 und Cu 2 SO 4(OH)2 - Cu ist toxisch für niedere Organismen (Bakterien, Algen, Pilze „Hausmittel“ Pfennig in Blumenvase, Kupfernagel in Nachbars Baum)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu wird von konz. Schwefelsäure und Salpetersäure, nicht aber von Salzsäure gelöst

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu ist ein recht häufiges Metall, am häufigsten sind Sulfide - wichtige Kupfermineralien sind Kupferkies Cu. Fe. S 2, Kupferglanz Cu 2 S, Bornit Cu 5 Fe. S 4, Covellin Cu. S, Rotkupfererz Cu 2 O, Malachit Cu 2(OH)2 CO 3, Azurit Cu 3(OH)2(CO 3)2

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - Ausgangspunkt der Kupferherstellung ist der Kupferkies Cu. Fe. S 2 - zunächst wird der Eisenanteil in das Oxid überführt - danach erfolgt eine Röst-Reaktion

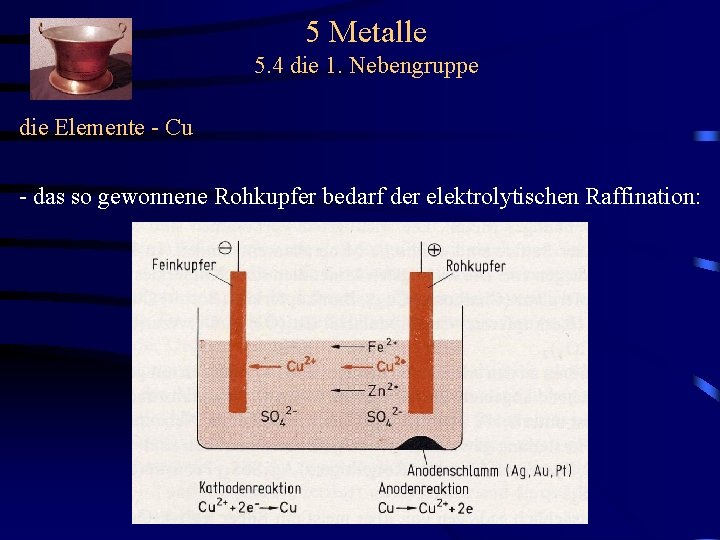
5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - das so gewonnene Rohkupfer bedarf der elektrolytischen Raffination:

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - das so gewonnene Rohkupfer bedarf der elektrolytischen Raffination - nach Eisen und Aluminium ist Kupfer das wichtigste Gebrauchsmetall - breite Verwendung aufgrund hoher thermischer (Wärmetauscher) und elektrischer (Elektroindustrie) Leitfähigkeit sowie der guten Korrosionsbeständigkeit (Schiffbau, chemischer Apparatebau, Braukessel)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - wichtige Kupferlegierungen sind Messing (Cu-Zn)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - wichtige Kupferlegierungen sind Messing (Cu-Zn) , Bronze (Cu-Sn)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Cu - wichtige Kupferlegierungen sind Messing (Cu-Zn) , Bronze (Cu-Sn) oder Neusilber (Alpaka, 60% Cu, 20% Ni, 20% Zn)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag - Silber ist ein weißglänzendes, weiches, dehnbares Metall - es besitzt die höchste thermische und elektrische Leitfähigkeit aller Metalle

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag - Silber ist ein weißglänzendes, weiches, dehnbares Metall - es besitzt die höchste thermische und elektrische Leitfähigkeit aller Metalle - wird von O 2 nicht angegriffen - mit H 2 S bildet sich in Gegenwart von Sauerstoff schwarzes Ag 2 S

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag wird nur von oxidierenden Säuren wie Salpetersäure und konz. Schwefelsäure gelöst - in Gegenwart von O 2 löst es sich auch unter Komplexbildung in Cyanidlösungen - Silber ist wie Cu für Mikroorganismen toxisch; Silbersalze finden bei der Wassersterilisation Verwendung

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag (Silber) gehört wie Au (Gold) zu den seltenen Elementen, Lagerstätten mit gediegenem Silber sind weitgehend abgebaut

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag (Silber) gehört wie Au (Gold) zu den seltenen Elementen, Lagerstätten mit gediegenem Silber sind weitgehend abgebaut - in sulfidischen Erzen ist Ag - meist unter 0, 1% - enthalten; daher wird Ag als Nebenprodukt bei der Pb- und Cu-Herstellung gewonnen - wichtige Silbermineralien sind Silberglanz (Argentit) Ag 2 S, Pyrargyrit Ag 3 Sb. S 3 und Proustit Ag 3 As. S 3

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag - Silber fällt als Nebenprodukt bei der Kupferraffination an - aus seinen Erzen wird Silber durch Cyanidlaugerei gewonnen:

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag - Silber ist für die meisten Verwendungen zu weich, daher wird es für den Gebrauch legiert (Ag-Gehalt wird auf 1000 Gewichtsteile bez. ) - Verwendungen: + Münzen + Versilberungen + Elektronik

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Ag - Silber ist für die meisten Verwendungen zu weich, daher wird es für den Gebrauch legiert (Ag-Gehalt wird auf 1000 Gewichtsteile bez. ) - Verwendungen: + Spiegel + Gebrauchsgegenstände + Fotoindustrie

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Gold ist „goldgelb“, das geschmeidigste und duktilste Metall + zu einer Dicke von 0, 00001 mm auswalzbar! - 70% der Leitfähigkeit des Silbers - chemisch inert, wird nur von Königswasser und in GG von O 2 von CN- angegriffen Gold + HCl Königswasser

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Gold kommt hauptsächlich gediegen vor, aber meist mit Ag legiert - Gold in Primärlagerstätten heißt Berggold Goldnugget, AUS

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Gold kommt hauptsächlich gediegen vor, aber meist mit Ag legiert - Gold in Primärlagerstätten heißt Berggold - Nach Gesteinsverwitterung weggeschmemmtes Gold lagert sich im Flußsand in Form von Goldstaub oder Goldkörnern als Seifenoder Waschgold ab und kann dort durch „Waschen“ gewonnen werden

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Nach Gesteinsverwitterung weggeschmemmtes Gold lagert sich im Flußsand in Form von Goldstaub oder Goldkörnern als Seifenoder Waschgold ab und kann dort durch „Waschen“ gewonnen werden Altertum, l. Rheingoldwäscher, r.

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Nach Gesteinsverwitterung weggeschmemmtes Gold lagert sich im Flußsand in Form von Goldstaub oder Goldkörnern als Seifenoder Waschgold ab und kann dort durch „Waschen“ gewonnen werden Brasilien, l. Ekuador, r.

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - aus seinen Erzen wird Gold wie Silber durch Cyanidlaugerei gew. - beim Amalgamverfahren wird aus feingemahlenem Gestein Gold mit Quecksilber als Amalgam abgetrennt, das Hg wird danach destillativ abgetrennt - Effektivität bei der Cyanidlaugerei 95 %, beim Amalgamverfahren 65 % - Au entsteht als Nebenprodukt der Pb- oder Cu-Herstellung Umweltrisiken der Cyanidlaugerei hier die vergiftete Theis (H/ROM)

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Gold findet Verwendung als Münz- (meist mit 10% Cu) oder als Schmuckmetall

5 Metalle 5. 4 die 1. Nebengruppe die Elemente - Au - Gold findet Verwendung als Münz- (meist mit 10% Cu) oder als Schmuckmetall, der Au-Gehalt wird auf 1000 Gewichtsteile bezogen oder in „Karat“ ausgedrückt: 24 Karat 100 % Au 18 Karat 75 % Au, 750 er Gold - Au wird ebenso wie Ag in der Elektronik verwendet - Weißgold ist eine Legierung mit Cu, Ni, Ag (1/4 bis 1/3 Au)

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften Zn

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften Cd Zn

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften Cd Zn Hg

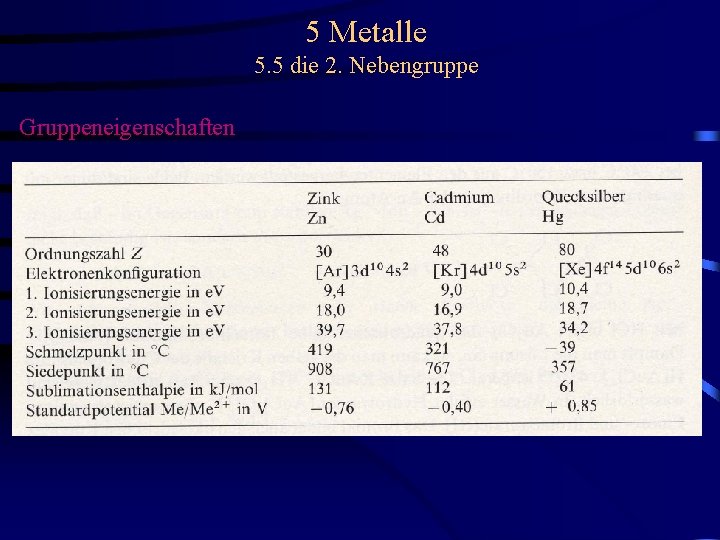
5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften - alle Elemente treten in der Oxadationsstufe +2 auf - Verbindungen höherer Oxidationsstufen sind bisher nicht isoliert worden - die Oxidationsstufe +1 ist nur für Hg von Bedeutung (als Hg 22+) - die Elemente bilden nur Verbdg. mit voll besetzten Unterschalen keine Übergangselemente - die Ionen Me 2+ und Hg 22+ sind daher farblos - ähnlich den Übergangselemente gibt es jedoch mit Ausnahme von Carbonylen zahlreiche Komplexe

5 Metalle 5. 5 die 2. Nebengruppe Gruppeneigenschaften - Zink und Cadmium sind sich chemisch recht ähnlich, Hg ist edler - Hg 22+ ist stärker polarisierbar und bildet kovalente Verbindungen - analoge Zn- und Cd- Verbdg. sind besser löslich als die Hg-Verbdg. - Hg 22+ - Komplexe sind stabiler als die von Zn 2+ und Cd 2+ - Zn 2+ - Ionen sind tetraedrisch- Cd 2+ - Ionen oktaedrisch koordiniert - für Hg(II) ist (ähnlich Cu(I), Ag(I) und Au(I)) die lineare Koordination typisch - geringe Ähnlichkeit zu Elementen der 2. HG (Ausn. Zn 2+ Mg 2+ )

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zink ist ein bläulich - weißes Metall; hochrein ist es duktil - oberhalb 200 °C und verunreinigt ist es spröde - der Dampf besteht aus Zn - Atomen - Zn ist ein unedles Metall alchemistisches Symbol

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zink ist ein bläulich - weißes Metall; hochrein ist es duktil - oberhalb 200 °C und verunreinigt ist es spröde - der Dampf besteht aus Zn - Atomen - Zn ist ein unedles Metall, - jedoch wird es durch Schutzschichten aus Oxid, Carbonat bzw. Hydroxid passiviert - Zn löst sich auch in Laugen (amphoter) unter Wasserstoffentwicklung und Bildung von Hydroxokomplexen

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zink kommt in der Natur nicht elementar vor - die wichtigsten Zinkerze sind Zinkblende Zn. S und Zinkspat Zn. CO 3 Zinkblende Zinkspat

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zink kommt in der Natur nicht elementar vor - die wichtigsten Zinkerze sind Zinkblende Zn. S und Zinkspat Zn. CO 3 - Zink wird thermisch oder elektrolytisch dargestellt; zunächst erfolgt die Röstung von Zinkerz:

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zink wird thermisch oder elektrolytisch dargestellt; zunächst erfolgt die Röstung von Zinkerz: -

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zinkverwendungen : + Dächer, Dachrinnen + Trockenbatterien

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn - Zinkverwendungen: + Dächer, Dachrinnen + Trockenbatterien + Zn-Staub als Reduktionsmittel + Zinküberzüge (Feuerverzinken o. galvanisch) + Legierungen (Messing)

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn einige Reaktionen des Zinks: - alle wichtigen Zinkverbindungen enthalten Zink in der Oxidationsstufe +2 - Zinkoxid entsteht durch Entwässerung von Zn(OH)2, durch thermische Zersetzung von Zn. CO 3 oder durch Oxidation von Zinkdampf an der Luft dargestellt:

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn einige Reaktionen des Zinks: - die Darstellung von Zinkhalogeniden kann durch Auflösen von Zn in Halogenwasserstoffsäuren erfolgen: - das technisch wichtigste Zinksalz Zn. SO 4 wird technisch durch Auflösen von Zinkschrott in verdünnter Schwefelsäure hergestellt

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Zn einige Reaktionen des Zinks: - Zinksulfid Zn. S kann aus den Elementen dargestellt werden Zn + S Zn. S

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Cd - Cadmium ist ein silberweißes Metall, edler und duktiler als Zink - beständig an der Luft, schwerlöslich in nichtoxidierenden Säuren, leicht in verdünnter Salpetersäure - von Laugen wird Cd nicht gelöst - Cadmium ist stark toxisch; sowohl die Aufnahme löslicher Cadmiumsalze als auch die Inhalation von Cadmiumdämpfen ist gefährlich

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Cd - Cadmium kommt wie Zink nicht elementar vor - Cd ist in den meisten Zinkerzen mit 0, 2 - 0, 4% enthalten; daher wird es als Nebenprodukt bei der Zinkherstellung gewonnen - Cadmiumminerale spielen für die technische Erzeugung keine Rolle - Cd-Verwendungen: + in wiederaufladbaren Batterien

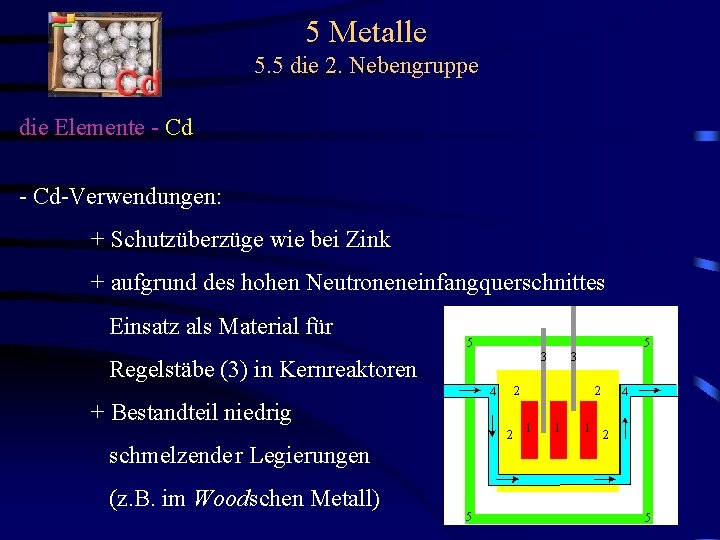
5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Cd-Verwendungen: + Schutzüberzüge wie bei Zink + aufgrund des hohen Neutroneneinfangquerschnittes Einsatz als Material für Regelstäbe (3) in Kernreaktoren + Bestandteil niedrig schmelzender Legierungen (z. B. im Woodschen Metall)

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Cd einige Reaktionen des Cadmiums: - Cd(OH)2 löst sich in Säuren und in sehr starken Basen als [Cd(OH)4]2 - in NH 3 löst sich Cd(OH)2 unter Bildung von [Cd(NH 3)4]2+ - die Cd-Halogenide Cd. X 2 bilden mit Halogenidionen die Komplexe Cd. X 3 - und Cd. X 42 - Cd. S (Cadmiumgelb wird als gelbes Pigment verw. , Cd. Se als rotes Pigment

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Cd einige Reaktionen des Cadmiums: - Cd(OH)2 löst sich in Säuren und in sehr starken Basen als [Cd(OH)4]2 - in NH 3 löst sich Cd(OH)2 unter Bildung von [Cd(NH 3)4]2+ - die Cd-Halogenide Cd. X 2 bilden mit Halogenidionen die Komplexe Cd. X 3 - und Cd. X 42 - Cd. S (Cadmiumgelb wird als gelbes Pigment verw. , Cd. Se als rotes Pigment - Cd. S ist photoleitend Belichtungsmesser

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - Quecksilber (engl. mercury)

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - Quecksilber ist ein silberglänzendes Metall, das bei -39 °C erstarrt - hoher Dampfdruck; der Dampf besteht aus Hg-Atomen - Hg-Dämpfe sind sehr giftig und verursachen chronische Vergiftungen; verschüttetes Hg ist deshalb sofort mit Zinkstaub (Amalgambildung) oder Iodkohle (Reduktion zu Hg. I 2) unschädlich zu machen

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - Quecksilber ist ein edles Metall und unterscheidet sich in seinen Rkn von Zink und Cadmium - wird von Salpeter- nicht aber von Salz- oder Schwefelsäure gelöst - bei RT ist Hg beständig gegen O 2, Wasser, CO 2, SO 2, HCl, H 2 S, NH 3 - reagiert mit Halogenen und Schwefel, ab 300 °C mit O 2 Hg. O Hg + 0, 5 O 2

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - das einzige für die Gewinnung von Quecksilber bedeutende Mineral ist der Zinnober Hg. S - Quecksilber erhält man hieraus durch Rösten: - Hg entweicht dampfförmig und wird kondensiert

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - Quecksilber findet vielseitige Verwendung: + Füllung in wiss. Geräten (Thermometer, Barometer) + Hg-Dampflampen (hoher UV-Anteil)

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg - Quecksilber findet vielseitige Verwendung: + Füllung in wiss. Geräten (Thermometer, Barometer) + Hg-Dampflampen (hoher UV-Anteil) + Kathodenmaterial für die Chloralkalielekrolyse + Extraktionsmittel bei der Goldgewinnung + als Silberamalgam in der Zahnmedizin

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg einige Reaktionen des Quecksilbers: - wichtig ist das Disproportionierungsgleichgewicht - die dadurch eingeschränkte Stabilität von Hg(I)-Verbindungen zeigt sich exemplarisch in folgenden Rkn:

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg einige Reaktionen des Quecksilbers: - beim Erhitzen an der Luft auf 300 - 350 °C erhält man orthorhomb. rotes Hg. O, das oberhalb 400 °C wieder zerfällt - es ist polymer aus Zickzackketten aufgebaut:

5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg einige Reaktionen des Quecksilbers: - beim Erhitzen an der

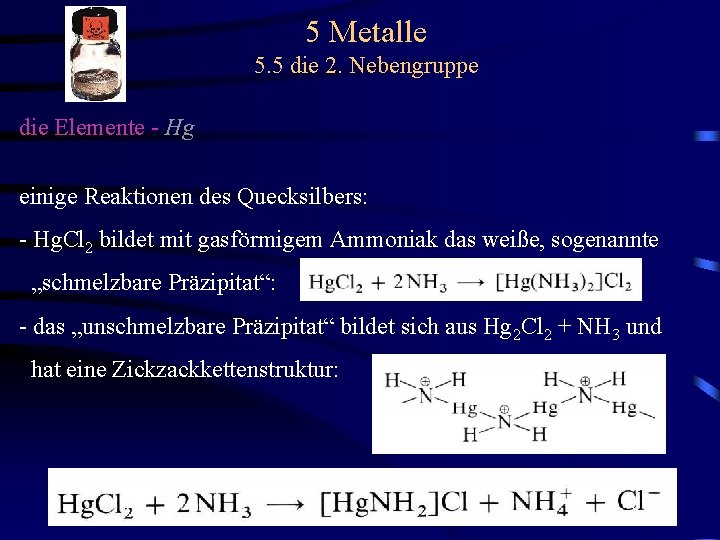
5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg einige Reaktionen des Quecksilbers: - Hg. Cl 2 bildet mit gasförmigem Ammoniak das weiße, sogenannte „schmelzbare Präzipitat“: - das „unschmelzbare Präzipitat“ bildet sich aus Hg 2 Cl 2 + NH 3 und hat eine Zickzackkettenstruktur:

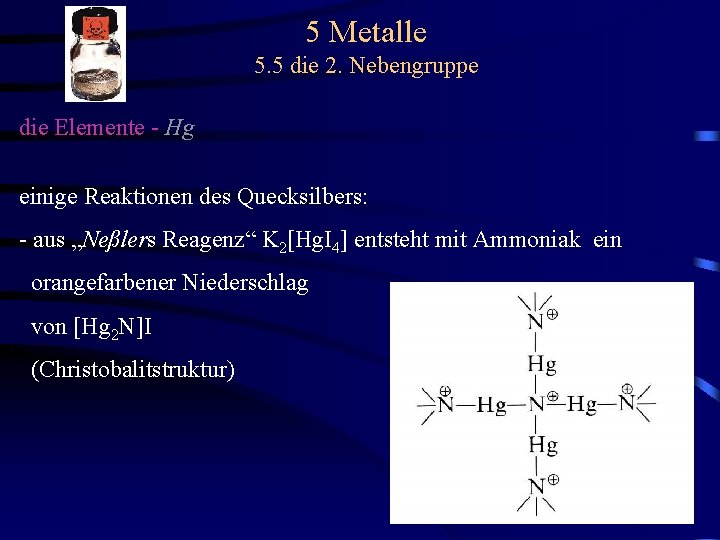
5 Metalle 5. 5 die 2. Nebengruppe die Elemente - Hg einige Reaktionen des Quecksilbers: - aus „Neßlers Reagenz“ K 2[Hg. I 4] entsteht mit Ammoniak ein orangefarbener Niederschlag von [Hg 2 N]I (Christobalitstruktur)

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften Sc

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften Y Sc

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften Y Sc La

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften - aufgrund ihrer Elektronenkonfiguration treten die Elemente der 3. NG ausschließlich in der Oxidationsstufe +3 auf - die Me 3+ - Ionen besitzen Edelgaskonfiguration und sind farblos - Eigenschaften ähneln mehr denen der 2. HG denn denen der 2. NG - es bestehen Ähnlichkeiten zur Chemie des Aluminiums

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften - aufgrund ihrer Elektronenkonfiguration treten die Elemente der 3. NG ausschließlich in der Oxidationsstufe +3 auf - die Me 3+ - Ionen besitzen Edelgaskonfiguration und sind farblos - Eigenschaften ähneln mehr denen der 2. HG denn denen der 2. NG - es bestehen Ähnlichkeiten zur Chemie des Aluminiums - insbesondere Scandium ist wie Al amphoter - zusammen mit den Lanthanoiden werden Scandium, Yttrium und Lanthan als Seltenerdmetalle bezeichnet

5 Metalle 5. 6 die 3. Nebengruppe Gruppeneigenschaften - die Metalle sind unedel und reaktionsfreudig - Zunahme der Ionenradien bewirkt Zunahme der Basizität der Hydroxide: + Sc(OH)3 ist amphoter + La(OH)3 eine ziemlich starke Base - Fluoride, Sulfate, Oxalate und Carbonate sind schwerlöslich - geringe Neigung zur Komplexbildung - Actinium Ac ist radioaktiv und kommt als radioaktives Zerfallsprodukt vor

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - in elementarem Zustand kristallisieren Sc, Y und La in typischen Metallstrukturen - es sind silberweiße, duktile Metalle - Sc und Y sind Leichtmetalle Lanthan

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - in elementarem Zustand kristallisieren Sc, Y und La in typischen Metallstrukturen - es sind silberweiße, duktile Metalle - Sc und Y sind Leichtmetalle - die Elemente der NG 3 sind unedler als Al und reagieren dementsprechend mit Säuren unter Wasserstoffentwicklung - in der Atmosphäre und in Wasser sind sie beständig, da sich passivierende Deckschichten bilden

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - entgegen ihrem Namen sind Sc, Y und La nicht selten, sondern ebenso häufig wie Blei und Zink - die Anreicherung in Lagerstätten ist allerdings gering - die wenigen wichtigen Mineralien sind: + Thortveitit (Y, Sc)2[Si 2 O 7]

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - entgegen ihrem Namen sind Sc, Y und La nicht selten, sondern ebenso häufig wie Blei und Zink - die Anreicherung in Lagerstätten ist allerdings gering - die wenigen wichtigen Mineralien sind: + Thortveitit (Y, Sc)2[Si 2 O 7] + Gadolinit Be 2 Y 2 Fe[Si 2 O 8]O 2 + Xenotim YPO 4 - La kommt als Begleiter der Lanthanoiden, vor allem des Cers, vor

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - alle Metalle können durch Reduktion der Fluoride mit Ca oder Mg hergestellt werden: - Mg-Sc - Legierungen werden in der Kerntechnik als Neutronenfilter verwendet - in Magnetspeichern erhöht Dotierung mit Sc 2 O 3 eine schnelle Ummagnetisierung - Rohre aus Yttrium dienen in der Kerntechnik als Brennstabummantel.

5 Metalle 5. 6 die 3. Nebengruppe die Elemente - große Mengen Yttriumverbindungen werden in der Farbfernsehtecnik als Farbkörper (rote Fluoreszenz) verwendet - flüssiges Lanthan dient zur Plutoniumextraktion aus geschmolzenem Uran - eine Co. Y - Legierung dient als hervorragendes Material für Permanentmagnete

5 Metalle 5. 6 die 3. Nebengruppe die Elemente einige Reaktionen von Sc, Y und La - Scandiumverbindungen ähneln den Aluminiumverbindungen - Sc. F 3 ist schwerlöslich in Wasser, Sc. Cl 3 Sc. Br 3 und Sc. I 3 sind hygroskopisch und leichtlöslich - mit Halogeniden bilden sich die Halogenokomplexe [Sc. F 6]3(Kryolith-Analoga!) und [Sc. Cl 6]3 - Sc(OH)3 ist eine schwache Base und weniger amphoter als Al(OH)3, in Na. OH-Lösungen löst es sich unter Bildung von Na 3[Sc(OH)6]

5 Metalle 5. 6 die 3. Nebengruppe die Elemente einige Reaktionen von Sc, Y und La - Yttriumverbindungen ähneln den Scandiumverbindungen - Yttriumhydroxid ist stärker basisch und stärker löslich als Sc(OH)3 - La. F 3 ist in Wasser schwerlöslich, es existieren die Fluorokomplexe [La. F 4]- und [La. F 6]3 - La 2 O 3 wird durch Erhitzen von La(OH)3 oder durch Verbrennen von Lanthan erhalten