Thermodynamik Wdh letzte Stunde 2 4 Reale Gase








- Slides: 27

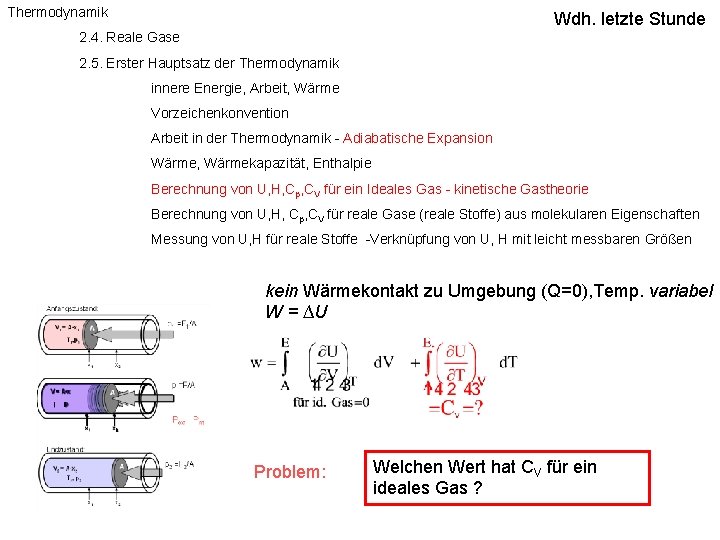
Thermodynamik Wdh. letzte Stunde 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen kein Wärmekontakt zu Umgebung (Q=0), Temp. variabel W = ∆U Problem: Welchen Wert hat CV für ein ideales Gas ?

Thermodynamik Wdh. letzte Stunde 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen kein Wärmekontakt zu Umgebung (Q=0), Temp. variabel W = ∆U

Thermodynamik Wdh. letzte Stunde 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen kein Wärmekontakt zu Umgebung (Q=0), Temp. variabel W = ∆U Problem: wie groß ist T 2? Ansatz: liefert: für ideales Gas

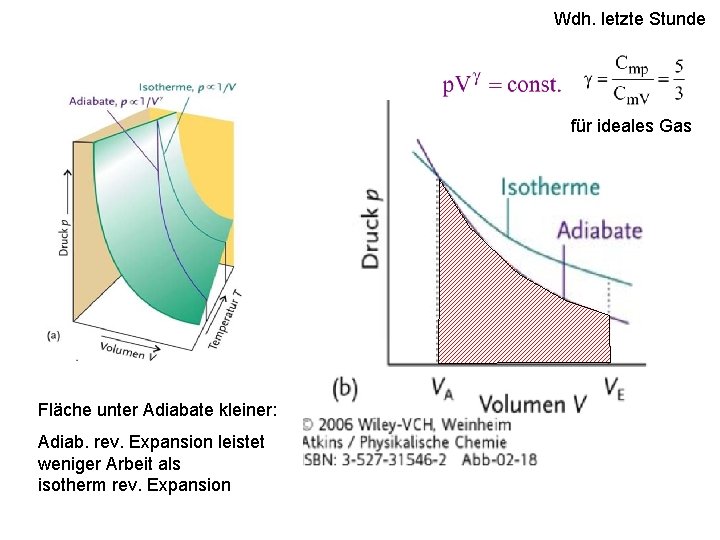
Wdh. letzte Stunde für ideales Gas Fläche unter Adiabate kleiner: Adiab. rev. Expansion leistet weniger Arbeit als isotherm rev. Expansion

Thermodynamik Wdh. letzte Stunde 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen

Thermodynamik Wdh. letzte Stunde 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen

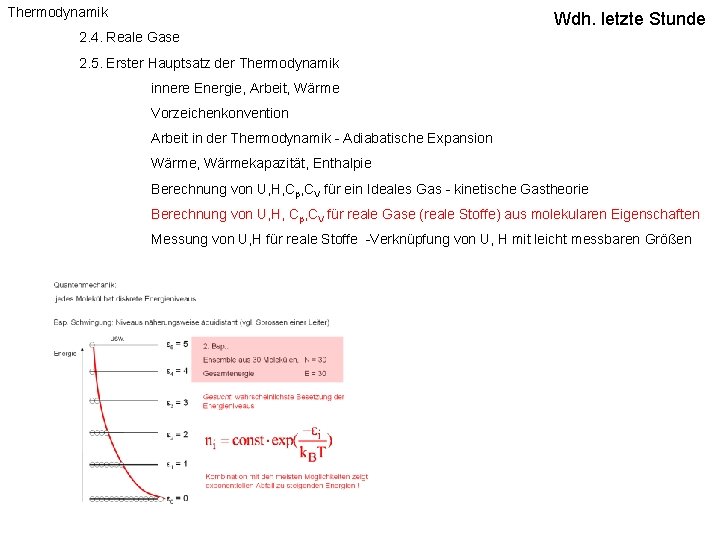
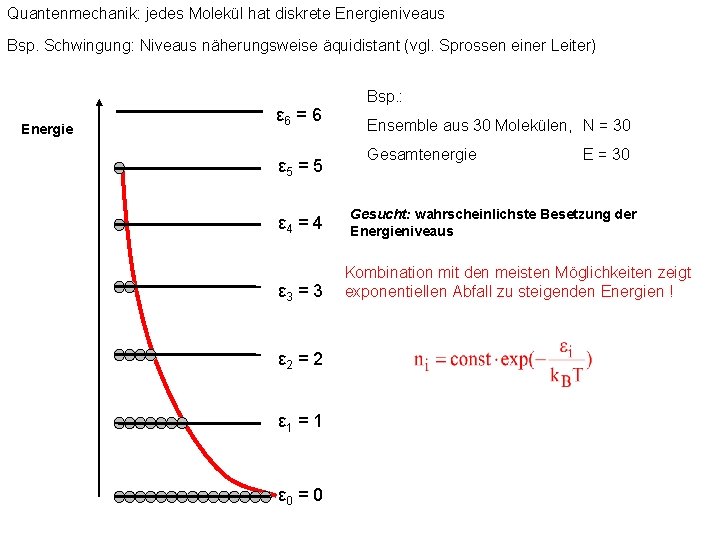
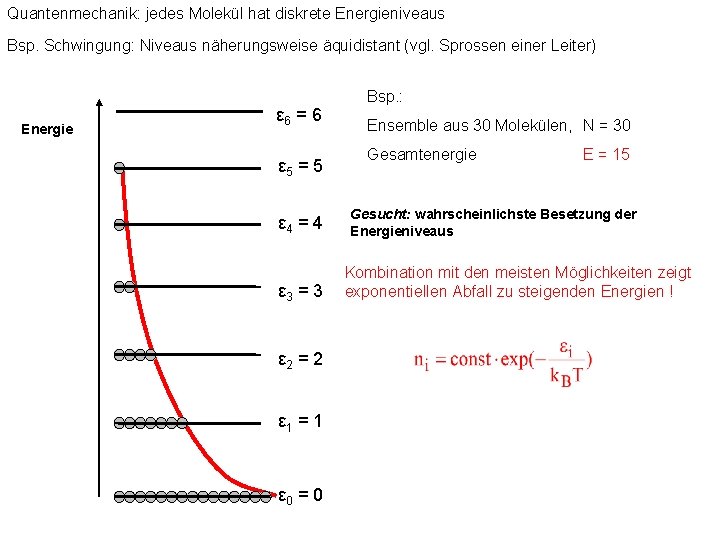
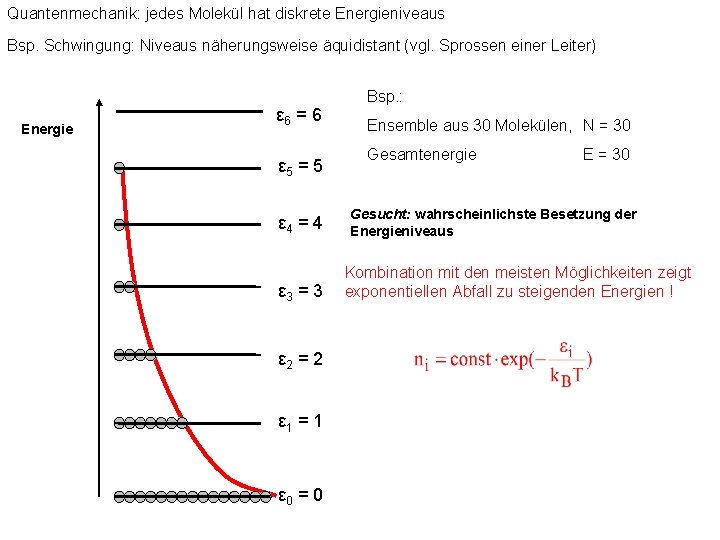
Quantenmechanik: jedes Molekül hat diskrete Energieniveaus Bsp. Schwingung: Niveaus näherungsweise äquidistant (vgl. Sprossen einer Leiter) Energie ε 6 = 6 ε 5 = 5 ε 4 = 4 ε 3 = 3 ε 2 = 2 ε 1 = 1 ε 0 = 0 Bsp. : Ensemble aus 30 Molekülen, N = 30 Gesamtenergie E = 30 Gesucht: wahrscheinlichste Besetzung der Energieniveaus Kombination mit den meisten Möglichkeiten zeigt exponentiellen Abfall zu steigenden Energien !

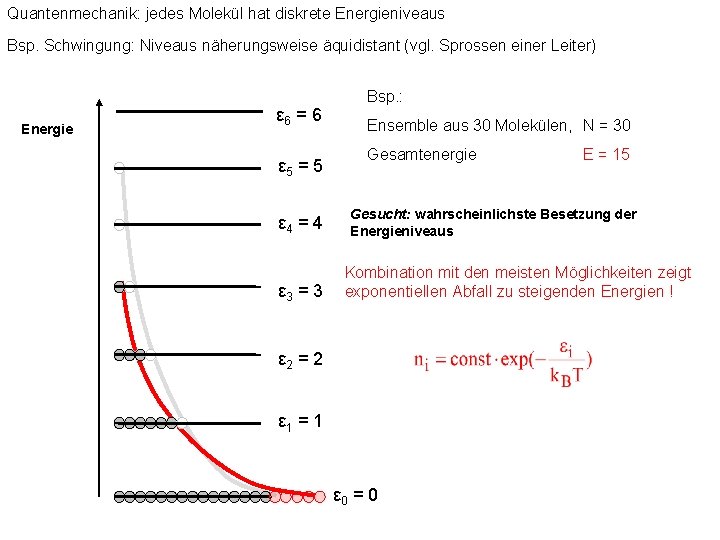
Quantenmechanik: jedes Molekül hat diskrete Energieniveaus Bsp. Schwingung: Niveaus näherungsweise äquidistant (vgl. Sprossen einer Leiter) Energie ε 6 = 6 ε 5 = 5 ε 4 = 4 ε 3 = 3 ε 2 = 2 ε 1 = 1 ε 0 = 0 Bsp. : Ensemble aus 30 Molekülen, N = 30 Gesamtenergie E = 15 Gesucht: wahrscheinlichste Besetzung der Energieniveaus Kombination mit den meisten Möglichkeiten zeigt exponentiellen Abfall zu steigenden Energien !

Quantenmechanik: jedes Molekül hat diskrete Energieniveaus Bsp. Schwingung: Niveaus näherungsweise äquidistant (vgl. Sprossen einer Leiter) Energie ε 6 = 6 ε 5 = 5 ε 4 = 4 ε 3 = 3 Bsp. : Ensemble aus 30 Molekülen, N = 30 Gesamtenergie E = 15 Gesucht: wahrscheinlichste Besetzung der Energieniveaus Kombination mit den meisten Möglichkeiten zeigt exponentiellen Abfall zu steigenden Energien ! ε 2 = 2 ε 1 = 1 ε 0 = 0

Quantenmechanik: jedes Molekül hat diskrete Energieniveaus Bsp. Schwingung: Niveaus näherungsweise äquidistant (vgl. Sprossen einer Leiter) Energie ε 6 = 6 ε 5 = 5 ε 4 = 4 ε 3 = 3 ε 2 = 2 ε 1 = 1 ε 0 = 0 Bsp. : Ensemble aus 30 Molekülen, N = 30 Gesamtenergie E = 30 Gesucht: wahrscheinlichste Besetzung der Energieniveaus Kombination mit den meisten Möglichkeiten zeigt exponentiellen Abfall zu steigenden Energien !

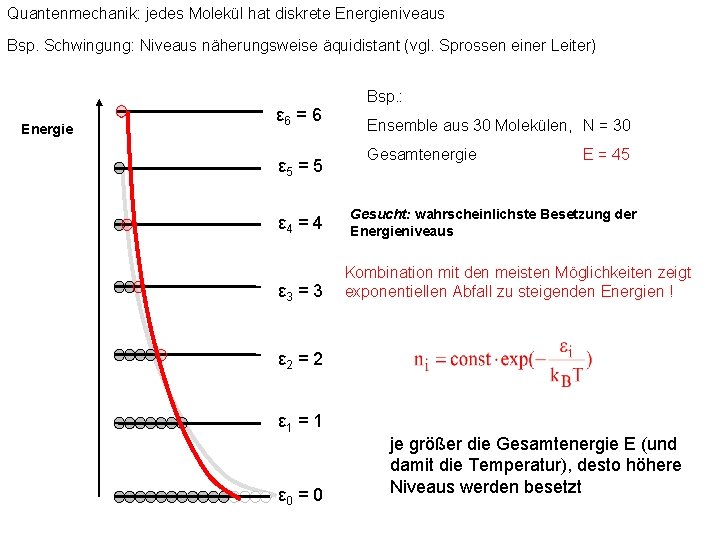
Quantenmechanik: jedes Molekül hat diskrete Energieniveaus Bsp. Schwingung: Niveaus näherungsweise äquidistant (vgl. Sprossen einer Leiter) Energie ε 6 = 6 ε 5 = 5 ε 4 = 4 ε 3 = 3 Bsp. : Ensemble aus 30 Molekülen, N = 30 Gesamtenergie E = 45 Gesucht: wahrscheinlichste Besetzung der Energieniveaus Kombination mit den meisten Möglichkeiten zeigt exponentiellen Abfall zu steigenden Energien ! ε 2 = 2 ε 1 = 1 ε 0 = 0 je größer die Gesamtenergie E (und damit die Temperatur), desto höhere Niveaus werden besetzt


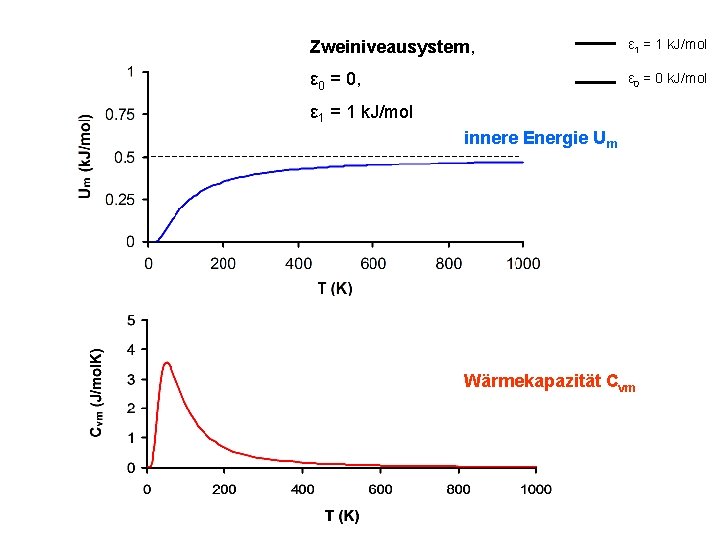
Zweiniveausystem, ε 1 = 1 k. J/mol ε 0 = 0, ε 0 = 0 k. J/mol ε 1 = 1 k. J/mol innere Energie Um Wärmekapazität Cvm

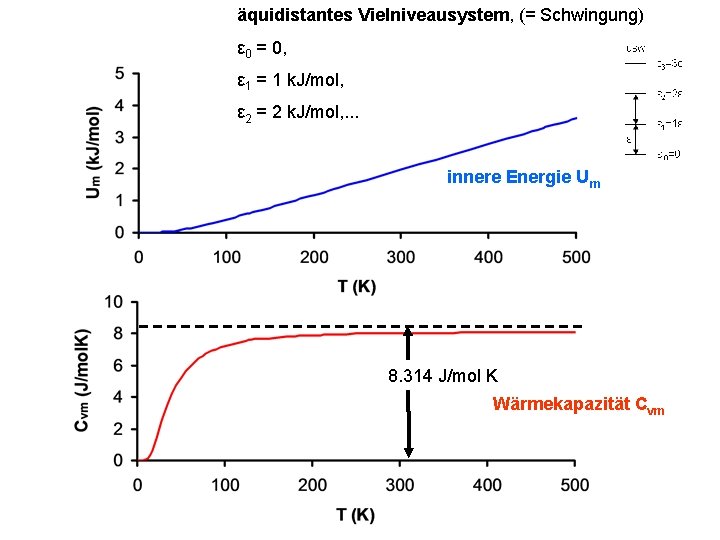
äquidistantes Vielniveausystem, (= Schwingung) ε 0 = 0, ε 1 = 1 k. J/mol, ε 2 = 2 k. J/mol, . . . innere Energie Um 8. 314 J/mol K Wärmekapazität Cvm

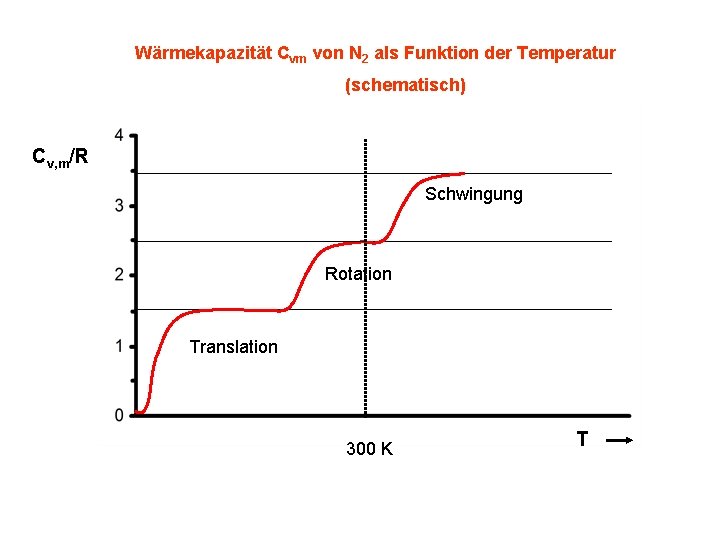
Wärmekapazität Cvm von N 2 als Funktion der Temperatur (schematisch) Cv, m/R Schwingung Rotation Translation 300 K T

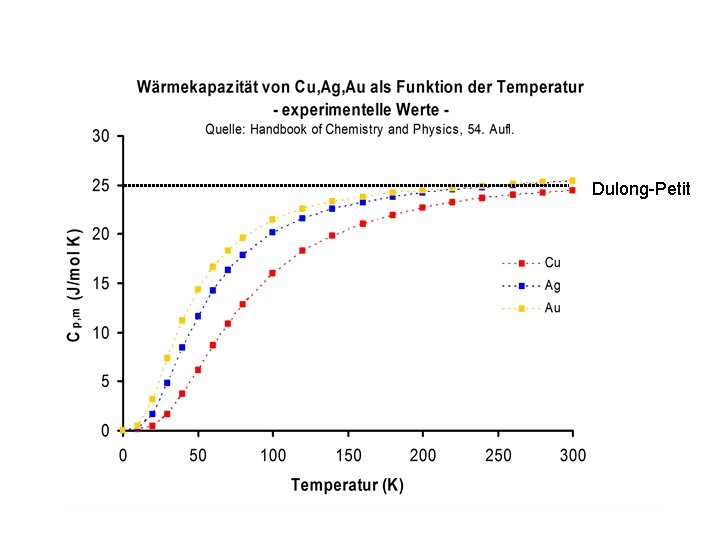
Regel von Dulong-Petit: molare Wärmekapazität vieler Festkörper bei Raumtemperatur: ≈3 R (≈ 25 J/mol K) experimentelle Werte (Atkins, 3. Aufl. , Tabelle 2. 12. ) Eisen 25. 1 J/mol K 3. 02 R Kupfer 24. 4 J/mol K 2. 93 R Silber 25. 4 J/mol K 3. 06 R Gold 25. 4 J/mol K 3. 06 R Phosphor (weiß) 23. 8 J/mol K 2. 86 R Antimon 3. 03 R 25. 2 J/mol K

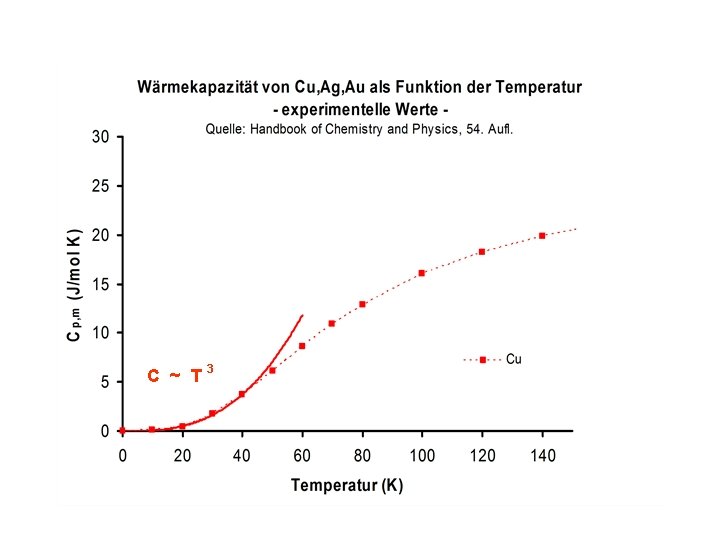
Dulong-Petit

C ~ T 3

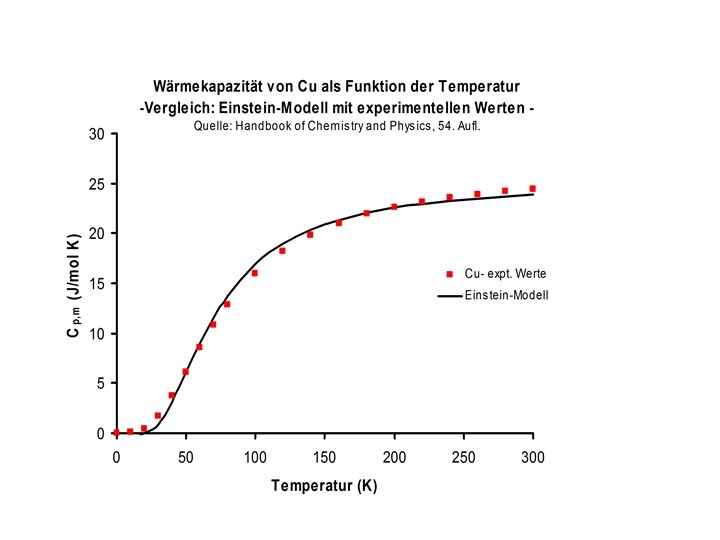
Einstein-Modell des Festkörpers Atome schwingen um ihre Gitterplätze mit einer festen Frequenz



Thermodynamik 2. 4. Reale Gase 2. 5. Erster Hauptsatz der Thermodynamik innere Energie, Arbeit, Wärme Vorzeichenkonvention Arbeit in der Thermodynamik - Adiabatische Expansion Wärme, Wärmekapazität, Enthalpie Berechnung von U, H, Cp, CV für ein Ideales Gas - kinetische Gastheorie Berechnung von U, H, Cp, CV für reale Gase (reale Stoffe) aus molekularen Eigenschaften Messung von U, H für reale Stoffe -Verknüpfung von U, H mit leicht messbaren Größen

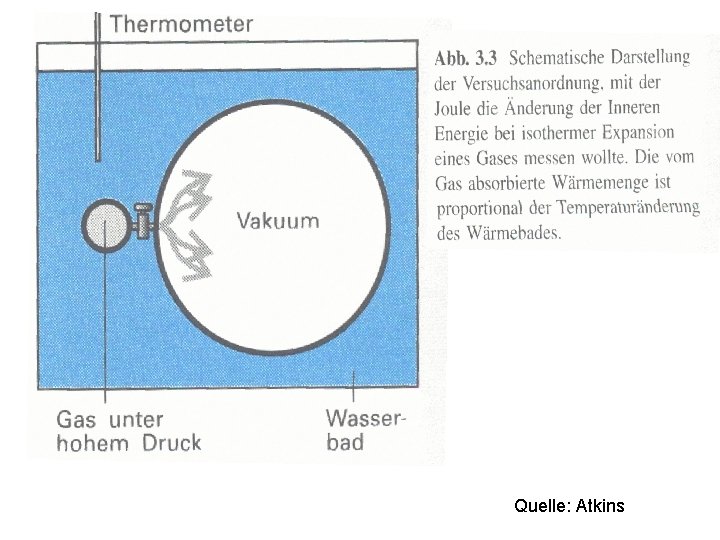
Quelle: Atkins

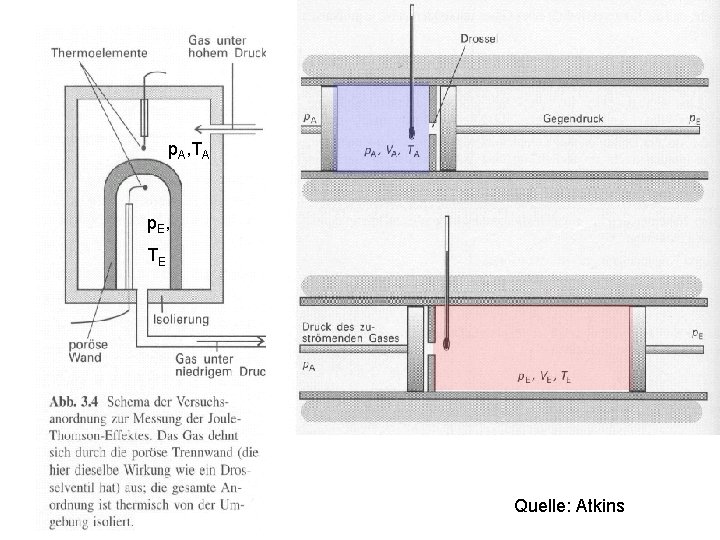
p. A, TA p. E, TE Quelle: Atkins

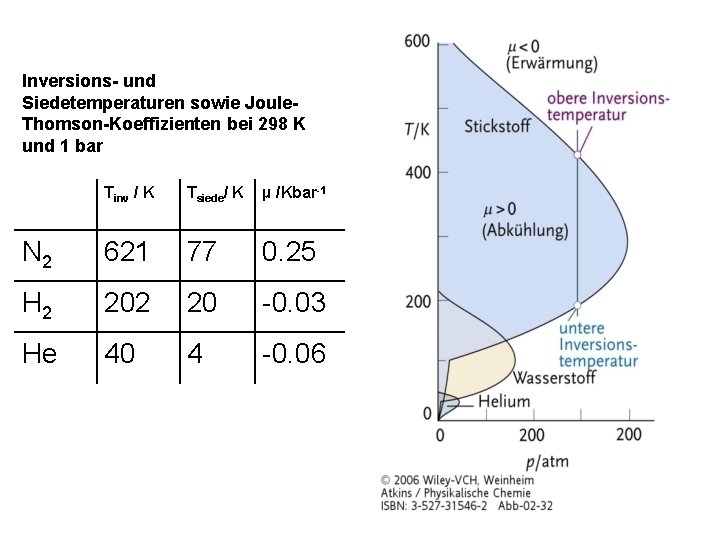
Inversions- und Siedetemperaturen sowie Joule. Thomson-Koeffizienten bei 298 K und 1 bar Tinv / K Tsiede/ K µ /Kbar-1 N 2 621 77 0. 25 H 2 20 -0. 03 He 40 4 -0. 06

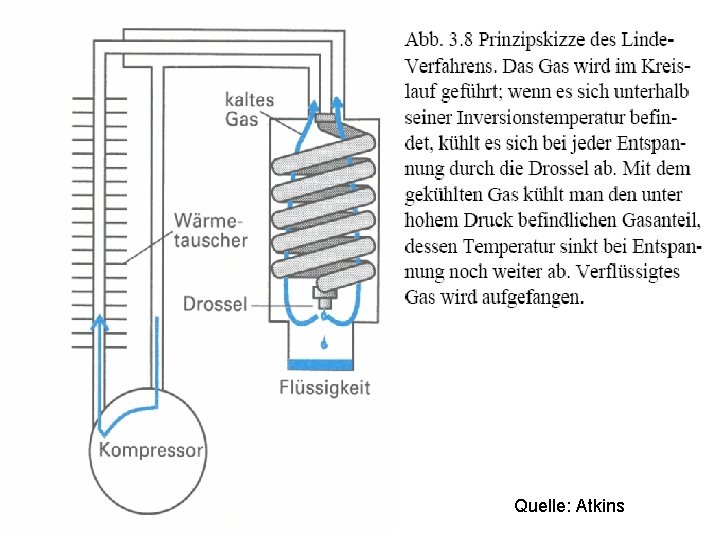
Quelle: Atkins

Thermischer Ausdehnungskoeffizient Joule-Thomson. Koeffizient Isotherme Kompressibilität 1/T 1/p 3/2 R 0 5/2 R 0 0 3/2 R R 5/2 R ideales Gas