ENZYME Teil 1 Grundlagen und Substratbestimmungen Metastabiler Zustand

ENZYME Teil 1: Grundlagen und Substratbestimmungen

Metastabiler Zustand Beispiel: Glucose-6 -Phosphat + H 2 O • Glucose + Pi [Glc 6 P] [H 20] K= = 1. 135 x 10 -3 [Glc] [Pi] Gleichgewicht stark auf Seite von Glc + Pi • DGo‘ = - 4. 02 kcal mol-1 (Exergonische Reaktion) Reaktion läuft freiwillig ab! ABER: Beim Lösen von Glc 6 P in Wasser passiert aber scheinbar nichts!
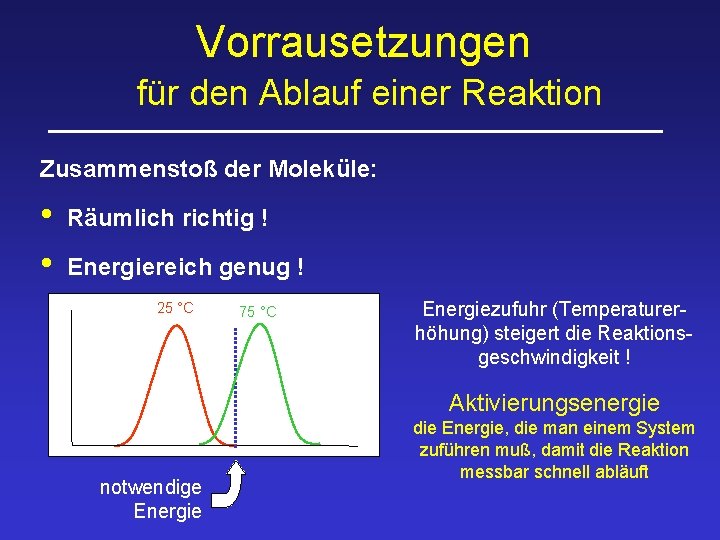
Vorrausetzungen für den Ablauf einer Reaktion Zusammenstoß der Moleküle: • • Räumlich richtig ! Energiereich genug ! 25 °C 75 °C Energiezufuhr (Temperaturerhöhung) steigert die Reaktionsgeschwindigkeit ! Aktivierungsenergie notwendige Energie die Energie, die man einem System zuführen muß, damit die Reaktion messbar schnell abläuft
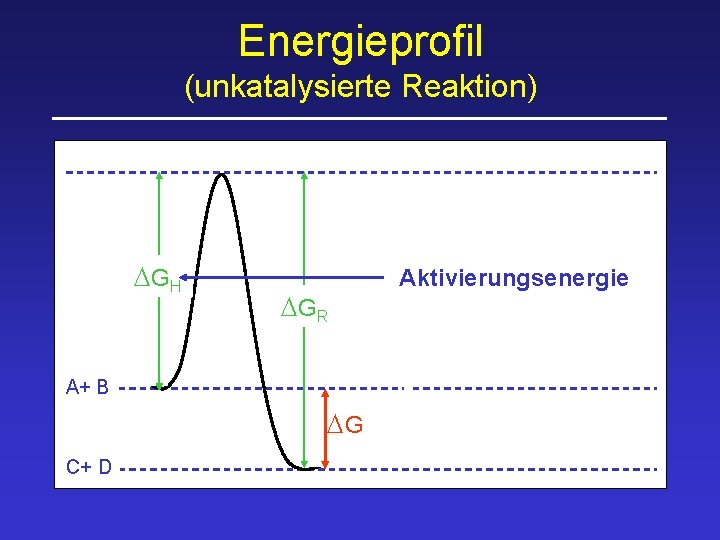
Energieprofil (unkatalysierte Reaktion) DGH DGR A+ B DG C+ D Aktivierungsenergie
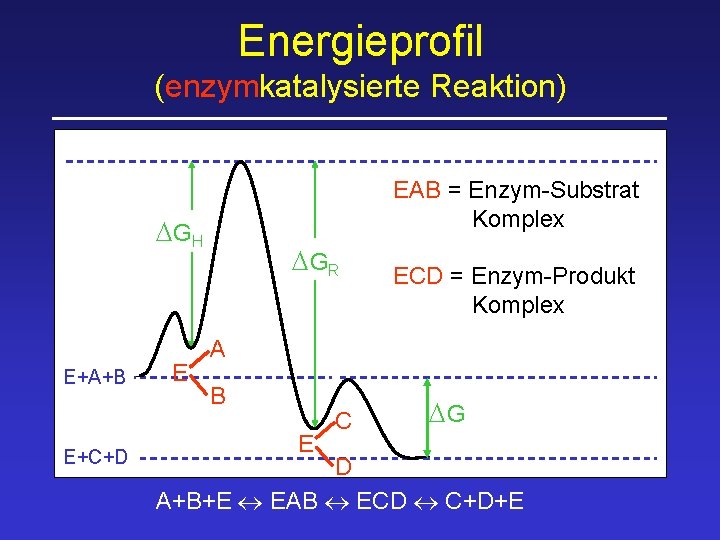
Energieprofil (enzymkatalysierte Reaktion) EAB = Enzym-Substrat Komplex DGH E+A+B E+C+D E DGR ECD = Enzym-Produkt Komplex A B E C DG D A+B+E EAB ECD C+D+E

Enzymkatalysierte Reaktionen benötigen geringere Aktivierungsenergie, weil: • • • Nährungseffekt räumlich richtige Ausrichtung der Substrate durch Bindung an Enzym Milleueffekt optimale Bedingungen für Reaktion am Enzym (p. H, Solvatisierung, etc) Konformationsstreckungseffekt durch Substratbindung Gestaltänerung des Enzyms (Übergangszustand)

Enzymkatalysierte Reaktionen • Gleichgewicht • Hin- und Rückreaktion Ein Enzym verändert die Geschwindigkeit einer Reaktion in Richtung des Gleichgewichts. Das Gleichgewicht selbst kann aber nicht verändert werden! Wenn das Gleichgewicht einer Reaktion stark auf einer Seite liegt spricht man von einer nicht umkehrbaren Reaktion. Ein Enzym kann eine Reaktion in beide Richtungen beschleunigen. Die Reaktion läuft aber immer in Richtung Gleichgewicht ab.

Was sind Enzyme sind Biokatalysatoren, die Aktivierungsenergie einer Reaktion herabsetzen können! Unterschiede zu anderen Katalysatoren sind: • • • Spezifität für die Substrate (Gruppen) und Reaktionen Kapazität sehr hohe Effizienz (Beschleunigung bis zu 1014 -fach) Regulation Aktivität kann an Umweltbedingungen angepasst werden.

Regulation von Enzymen • • Proteinsynthese und Proteinabbau Neusynthese des gewünschten Enzyms; Aktivierung oder Deaktivierung von Genen Konformationsänderung (a) Allosterische Effektoren (Inhibitoren oder Aktivatoren) binden an regulatorisches Zentrum des Proteins
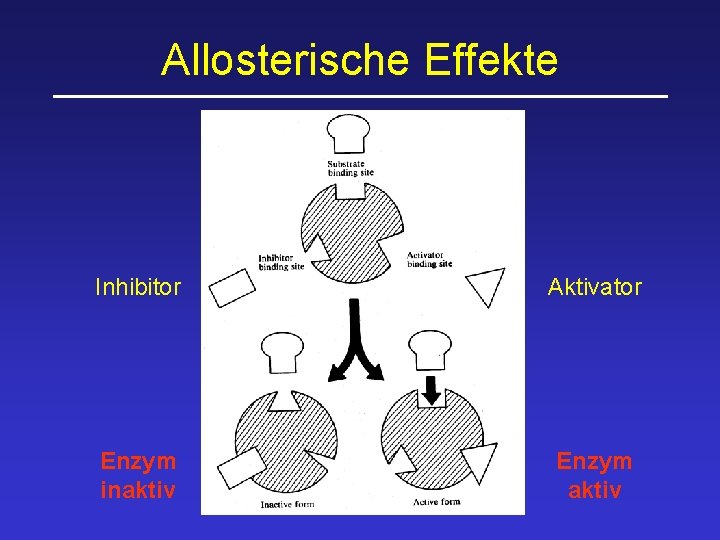
Allosterische Effekte Inhibitor Aktivator Enzym inaktiv Enzym aktiv

Regulation von Enzymen • • • Proteinsynthese und Proteinabbau Neusynthese des gewünschten Enzyms; Aktivierung oder Deaktivierung von Genen Konformationsänderung (a) Allosterische Effektoren (Inhibitoren oder Aktivatoren) binden an regulatorisches Zentrum des Proteins (b) Kompetitive Hemmung „Konkurenz“ um das aktive Zentrum Chemische Veränderung Phosphorylierungen (Protein-Kinasen) oder Dephosphorylierungen (Phosphatasen)

Einteilung von Enzymen 1. Oxidoreduktasen Transfer von H, O oder e- von einem Substrat auf ein anderes 2. Transferasen Transfer von chem. Gruppen zwischen Substraten 3. Hydrolasen hydrolytischer Abbau 4. Lyasen nicht-hydrolytische Spaltung von Bindungen 5. Isomerasen Intramolekulare Umlagerungen 6. Ligasen Knüpfung von kovalenten Bindungen unter ATP-Verbrauch

Benennung von Enzymen Beispiel: Fructose + NADP+ 5 -Anhydro-D-Fruktose + NADH + H+ Bezeichnung Fructose 5 -Dehydrogenase Fructose: NADP 5 -Oxidoreduktase Einteilung EC-Nummer, hier EC 1. 124 (Oxidoreduktase, wirkt an CH-OH Donoren, NAD oder NADP als Akzeptor, Enzymnummer)

Analytisches Arbeiten mit Enzymen 1. Enzymbestimmung Bestimmung der Biologische Aktivität Bestimmung der Enzymaktivität Daneben kann auch der Proteingehalt bestimmt werden (z. B. mit Immunologischen Methoden) 2. Substratbestimmung Bestimmung eines Analyten (eines Substrates) mit Hilfe eines Enzyms Das Enzym muß dazu aber käuflich erhältlich sein, oder selbst gereinigt werden.
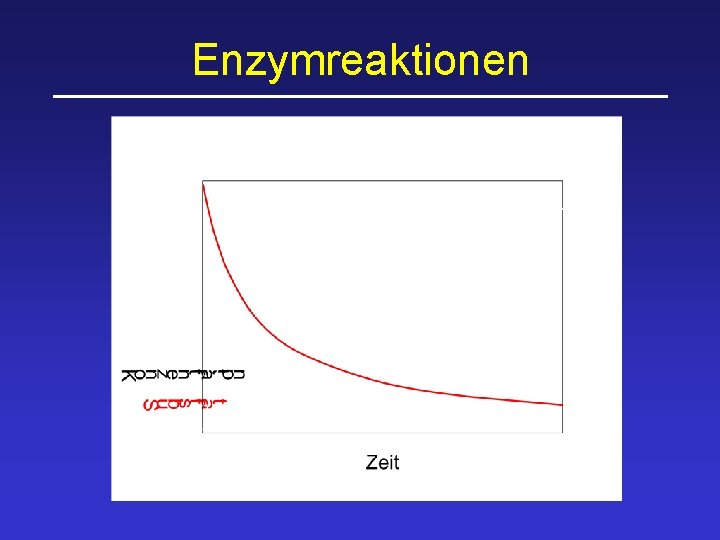
Enzymreaktionen
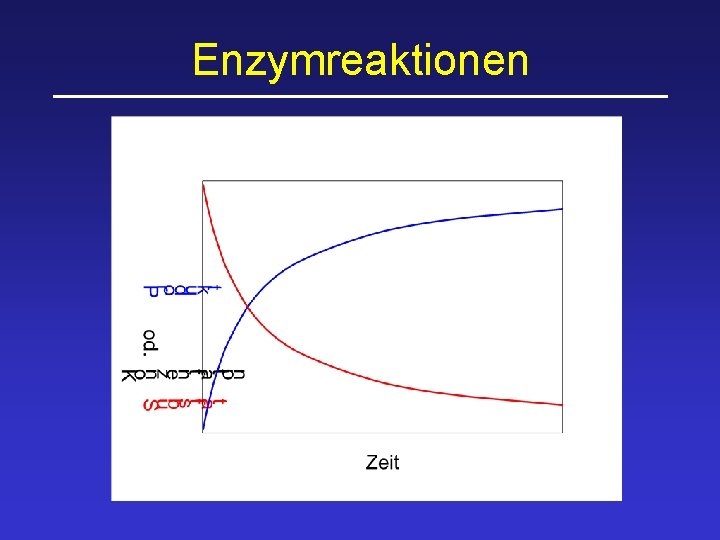
Enzymreaktionen

Enzymatische Substratbestimmung Aufbau eines Testsystems 1. Spezifisches Enzym sollte nur das Substrat umsetzen 2. Co-Substrate wo notwendig muß man Co-Substrate (Co-Enzyme) einsetzen 3. Reaktionsmilleu p. H-Wert, Pufferung, Aktivatoren, etc 4. Detektionsmöglichkeit (a) Direkte Messung mittels Extinktion Produkt absorbiert, Substrat nicht (oder umgekehrt); Co-Substrat oder Co-Produkt absorbiert (b) Produktnachweis chemisch 5. Abfangreaktionen sind notwendig wenn das Gleichgewicht ungünstig liegt.
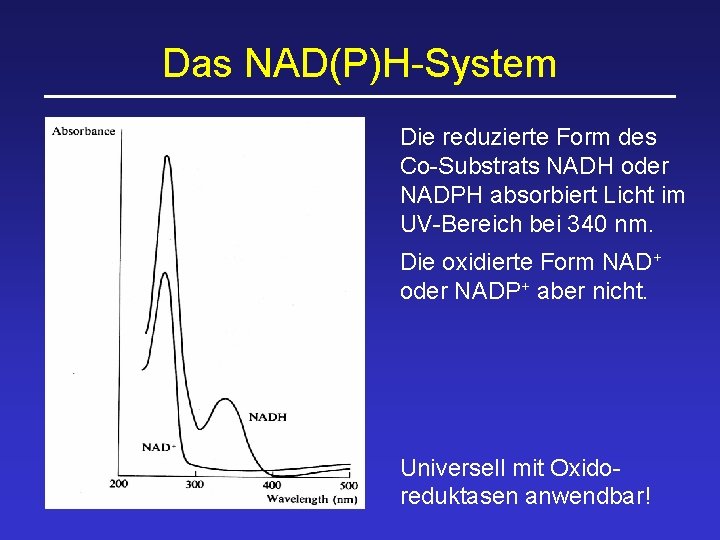
Das NAD(P)H-System Die reduzierte Form des Co-Substrats NADH oder NADPH absorbiert Licht im UV-Bereich bei 340 nm. Die oxidierte Form NAD+ oder NADP+ aber nicht. Universell mit Oxidoreduktasen anwendbar!
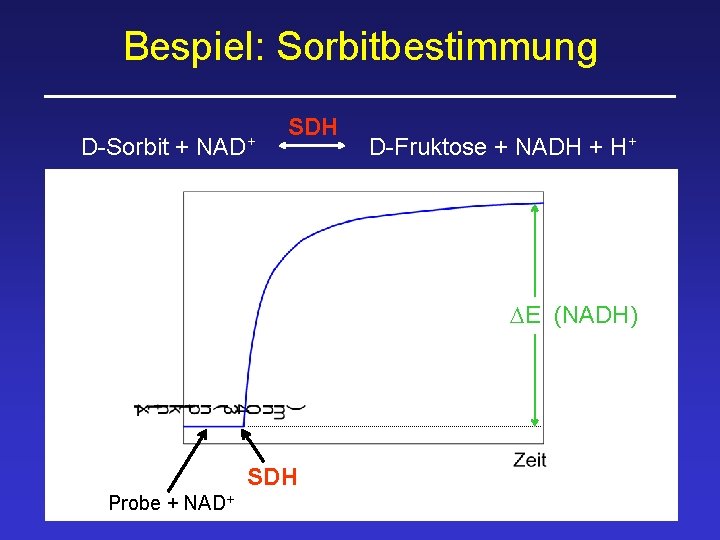
Bespiel: Sorbitbestimmung D-Sorbit + NAD+ SDH D-Fruktose + NADH + H+ DE (NADH) SDH Probe + NAD+

Allgemeine Überlegungen 1 A+B C+D Vorraussetzungen • Gleichgewicht der Reaktion liegt auf Seite von C +D • [Cosubstrat] > [Probe] sonst kann nicht alles an Probe verbraucht werden
![Allgemeine Überlegungen 2 A+B C+D Regeln • v nimmt ab, wenn [c] kleiner wird. Allgemeine Überlegungen 2 A+B C+D Regeln • v nimmt ab, wenn [c] kleiner wird.](http://slidetodoc.com/presentation_image_h/dfddf9e3bb14c05378687e14507f306b/image-21.jpg)
Allgemeine Überlegungen 2 A+B C+D Regeln • v nimmt ab, wenn [c] kleiner wird. Steigung = Geschwindigkeit • Wenn A+B mit C+D im Gleichgewicht, dann v = 0 (kein Netto-Umsatz) • Konzentration (Aktivität) des Enzyms ändert v, hat aber keinen Einfluß auf den Endpunkt (DE bleibt gleich)
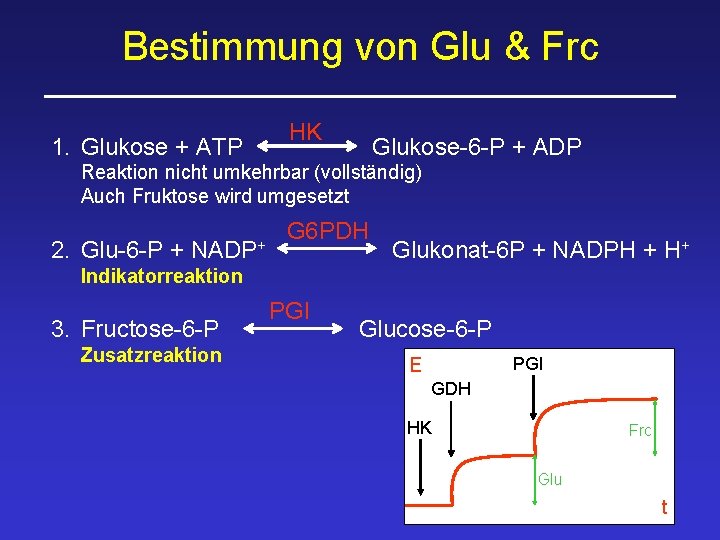
Bestimmung von Glu & Frc 1. Glukose + ATP HK Glukose-6 -P + ADP Reaktion nicht umkehrbar (vollständig) Auch Fruktose wird umgesetzt 2. Glu-6 -P + NADP+ G 6 PDH Glukonat-6 P + NADPH + H+ Indikatorreaktion 3. Fructose-6 -P Zusatzreaktion PGI Glucose-6 -P PGI E GDH HK Frc Glu t
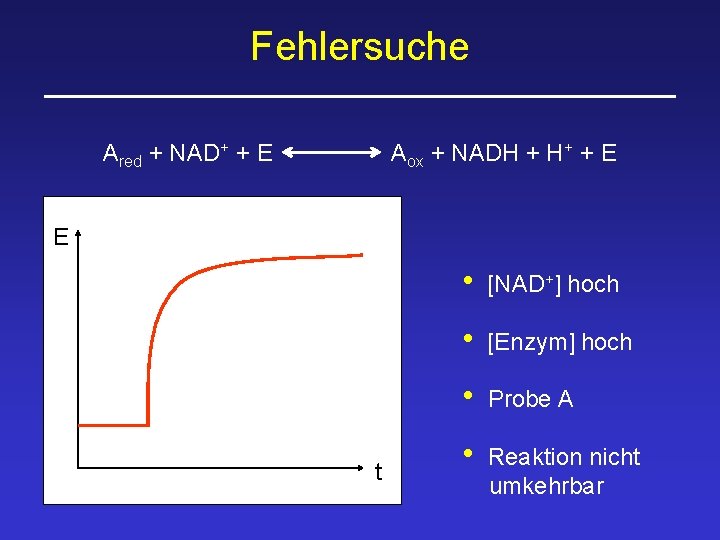
Fehlersuche Ared + NAD+ + E Aox + NADH + H+ + E E t • [NAD+] hoch • [Enzym] hoch • Probe A • Reaktion nicht umkehrbar
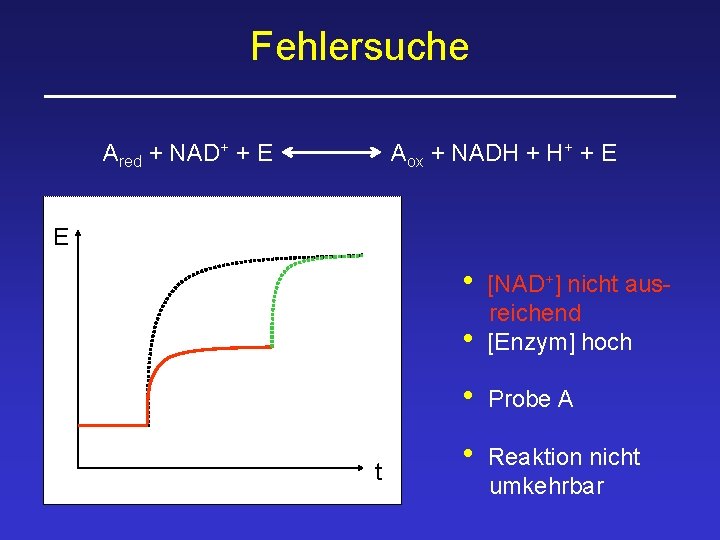
Fehlersuche Ared + NAD+ + E Aox + NADH + H+ + E E • t • [NAD+] nicht ausreichend [Enzym] hoch • Probe A • Reaktion nicht umkehrbar

Fehlersuche Ared + NAD+ + E Aox + NADH + H+ + E E t • [NAD+] hoch • [Enzym] gering • Probe A • Reaktion nicht umkehrbar
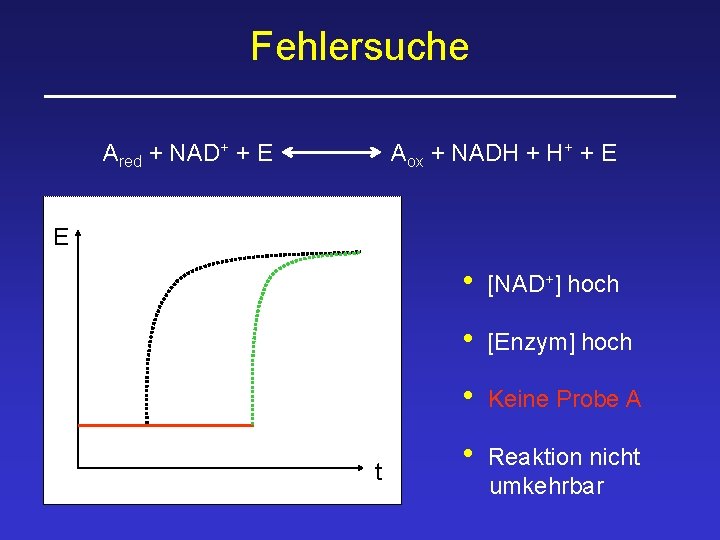
Fehlersuche Ared + NAD+ + E Aox + NADH + H+ + E E t • [NAD+] hoch • [Enzym] hoch • Keine Probe A • Reaktion nicht umkehrbar

Fehlersuche Ared + NAD+ + E Aox + NADH + H+ + E E t • [NAD+] hoch • [Enzym] hoch • Keine Probe A • Reaktion nicht umkehrbar
- Slides: 27