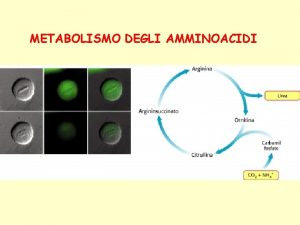
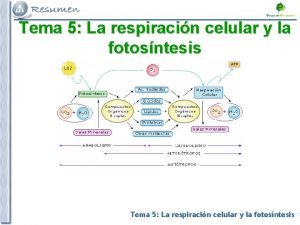
QBQ4020 Qumica Ambiental Noturno Bioqumica Metabolismo Catabolismo e

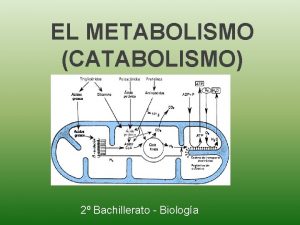
QBQ-4020 Química Ambiental Noturno Bioquímica Metabolismo – Catabolismo e Anabolismo Como retirar energia do ambiente? Como sintetizar moléculas (biomoléculas)?


Curso 1 - Visão estrutural que são açúcares, proteínas, lipídios e ácidos nucléicos. 2 - Visão Energética. Termodinâmica. 3 - Metabolismo do nível celular ao de órgãos e tecidos, e de organismos Associar Fisiologia, Biomol, Nutrição e Ambiente

Como é possível a separação do meio externo do meio Interno? Compartimentalização? Quais as Bases Físicas e Químicas?


A partir deste experimentos- Miller (teoria de Oparin) ficou estabelecido a formação de vários outros compostos como: -Aminoácidos -Ácidos Nucléicos e -Ácidos Graxos. . Chave para a formação de colóides Colóides = Emulsões Óleo em Água ou Água em Óleo Separa as “coisas Hidrofílicas de Hidrofóbicas”. .
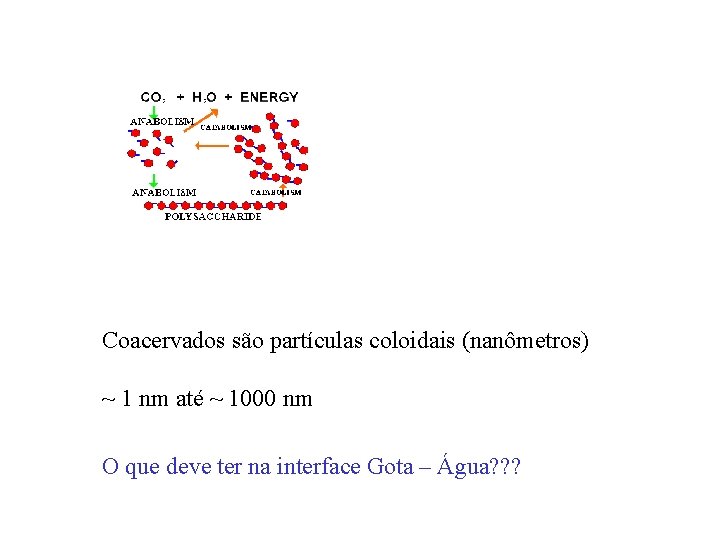
Coacervados são partículas coloidais (nanômetros) ~ 1 nm até ~ 1000 nm O que deve ter na interface Gota – Água? ? ?

Estrutura e Propriedades de H 2 O -ângulo de ligação -polaridade -tensão superficial -dissolução de espécies -coesividade

- H 2 O é o único Líquido inorgânico que ocorre naturalmente na Terra. - Ocorre naturalmente nos três estados Sólido, Líquido e Vapor - Existe no planeta antes da Vida. A Vida segundo nossos conceitos é H 2 O - Ciclo Hidrológico (Combustão, Fotossíntese) Ouro do próximo século - Sólido Líquido (só aumento de desordem? Por que densidade de 0 à 4 0 C ? - Gás Líquido (só aumento de densidade? ) - Líquido de 0 `a 100 0 C. Por que faixa tão alta?

Entre as propriedades ditas anômalas de H 2 O líquida. Estão aquelas que as diferenciam de outros líquidos. H 2 O como sólido tb é diferente de outros sólidos. Como gás é um dos mais leves, Como líquido é muito denso, Como sólido é pouco denso, A vida depende destas propriedades anômalas. -Alta coesão alto ponto de fusão, alta capacidade térmica. Contribuem para regulação térmica - Alto calor latente de evaporação . . resistência à evaporação. Excelente solvente para compostos iônicos e polares.

Anomalias de água (mais importantes) 1. Alto ponto de fusão H-pontes no sólido 2. H 2 O alto ponto de ebulição. H-pontes no líquido

Como Líquido Água é muito mais denso que o esperado!!! E como Sólido é muito mais leve que o esperado!!!! Gas Liquid Solid








Emulsion! Phase Separate! Gmix >> Gseparado
Add surfactant

Qual o estado de polímeros naturais em água? Proteínas? DNA, RNA? Lipídios? Qual deve ser a viscosidade ( ) destas soluções ? Qual o efeito de sais? Como devem ser o estado dos chamados Géis?
![p. OH = -log[OH-] the negative log of the hydroxide ion molarity p. Kw p. OH = -log[OH-] the negative log of the hydroxide ion molarity p. Kw](http://slidetodoc.com/presentation_image/2fc7f1ed2d9cf2c3c69a5954b5e7cd3f/image-24.jpg)
p. OH = -log[OH-] the negative log of the hydroxide ion molarity p. Kw = -log Kw the negative log of the water ion product , Kw p. Ka = -log Ka the negative log of the acid dissociation constant, Ka p. Kb = -log Kb the negative log of the base dissociation constant, Kb

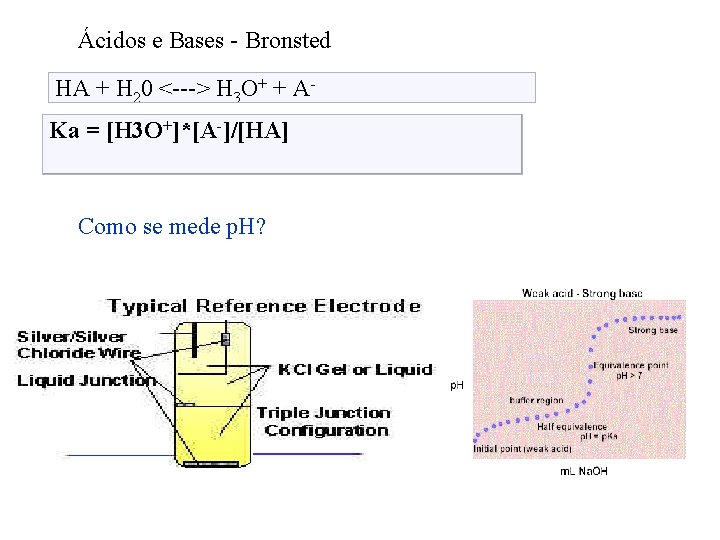
Ácidos e Bases - Bronsted HA + H 20 <---> H 3 O+ + AKa = [H 3 O+]*[A-]/[HA] Como se mede p. H? ? ? Como se mede p. H?
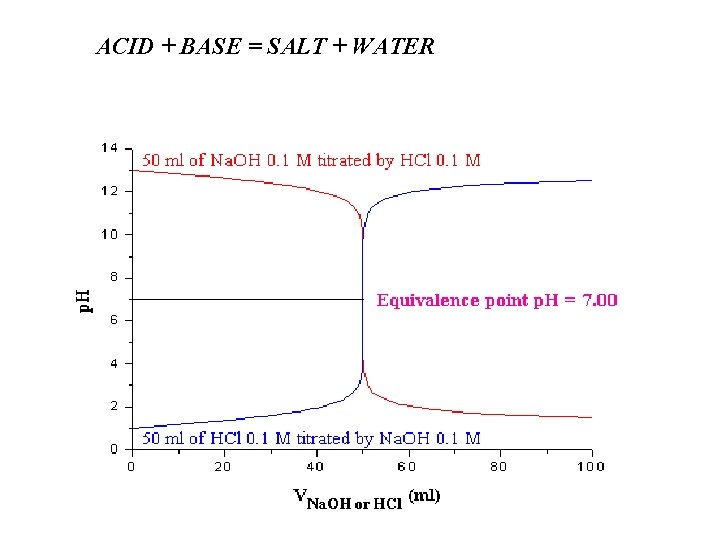
ACID + BASE = SALT + WATER
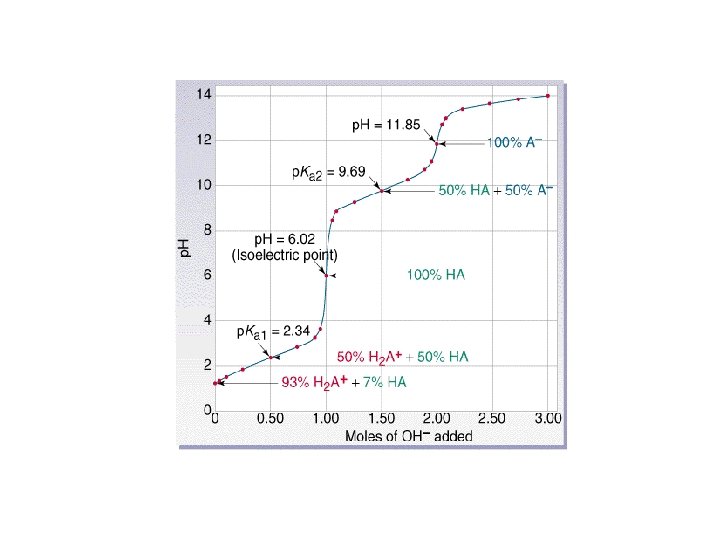
Titration curve for weak acid/strong base. (Figure by MIT OCW. )


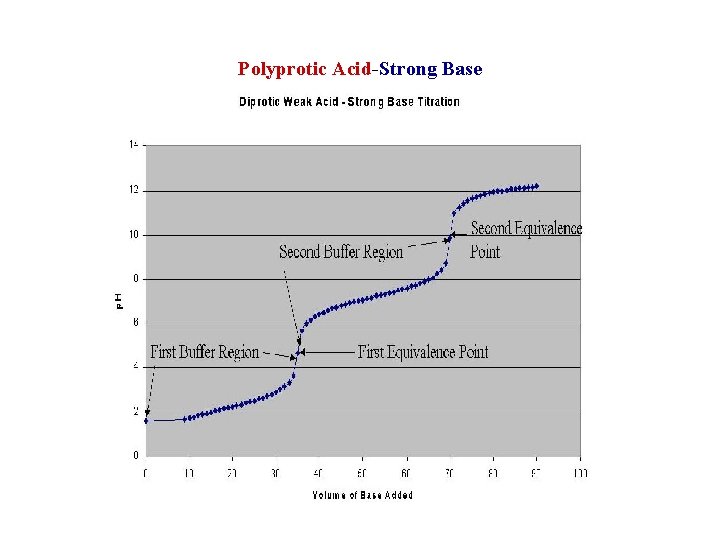
Polyprotic Acid-Strong Base

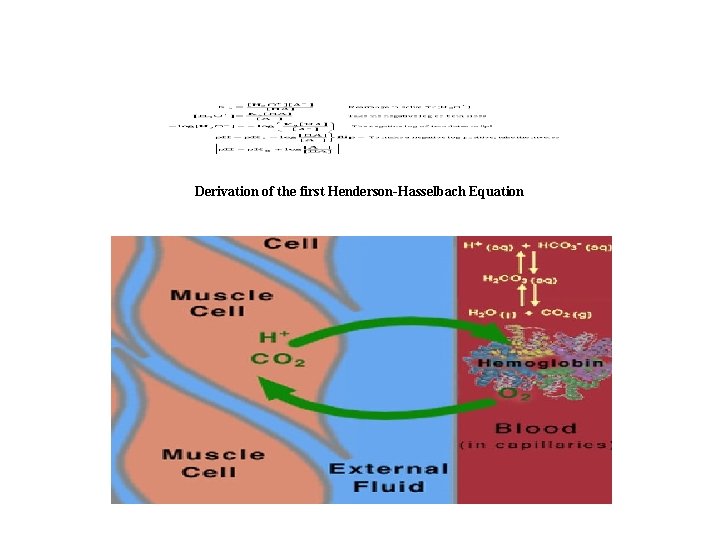
Derivation of the first Henderson-Hasselbach Equation



Como seria uma curva de titulação de um polipeptídeo?
Qual o p. H do sangue? E quais espécies atuam como tampão?






QBQ 4020 N aula 2 Objetivo Principal Metabolismo!!!! Células Podem ser Ensinadas!!!! Ex. Leveduras Álcool Precisa aprender qual a Fonte: Brasil Cana de Açúcar USA Milho!! Qual a Diferença? ? ? Ver Scientific America Br de Agosto Capim Biodiesel

É necessário otimizar condições de fermentação p. H, condições De contorno, fronteira. Quais nutrientes? Quais condições o conjunto de enzimas são expressos? Serve também para doenças, trabalhos de músculo condicionamento Físico etc. Nossa intenção é compreender como a máquina celular, tecidual, por Órgãos e por Organismos se comportam ! No aprendizado de Genes e Bilo. Molecular, buscamos aprender como Atuar em nível Genético. Início do curso Qual é o cenário? H 2 O – Propriedades: Polaridade Proticidade Ácidos-Bases Cargas de moléculas Interações Eletrostáticas Pontes de H, Van der Valls etc. .

Quais são os Blocos Construtores? ? Amino Ácidos Proteinas ENZIMAS!!! Lipídios Membranas, Reserva “Energia” Açúcares Estruturas, Reconhecimento, Energia Ácidos nucléicos Material Genético Ainda que muito se fale de Genomas (sopa de letrinhas) O quente são os ENZIMAS!!! Permite acelar até 108 x velocidade de reações. . . Controle de fluxos METABOLISMO ENZIMAS

Conhecemos ~500 AA´s, Somente 20 constituem essenciais Valina, Leucine, Isoleucine, Alanina, Arginina, Glutamina, Lisina, Aspartico Glutamatico, Prolina, Cisteine, Treonina, Methionina, Histidina, Phenylalanina, Tyrosina, Triptofano, Asparagina, Glicina, Serina — = Essenciais Alimentação protéica fornece AA´s livres que são “remontados para formar proteínas do corpo


. Em 1806, 10 amino acid descoberto do aspargo asparagine. Após cisteine, glicine, and leucine de cálculo urinário, gelatina músculo e algodão. Por cerca de 1935 todos AA´s conhecidos 6 M HCl Proteína AA´s livres
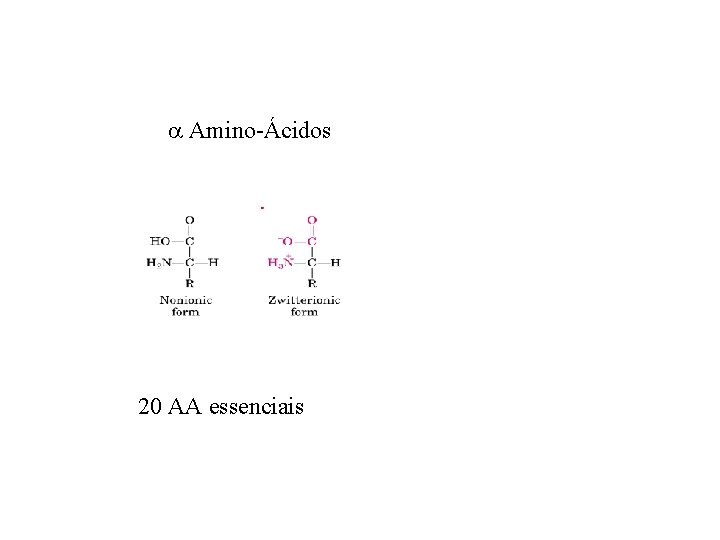
Amino-Ácidos 20 AA essenciais


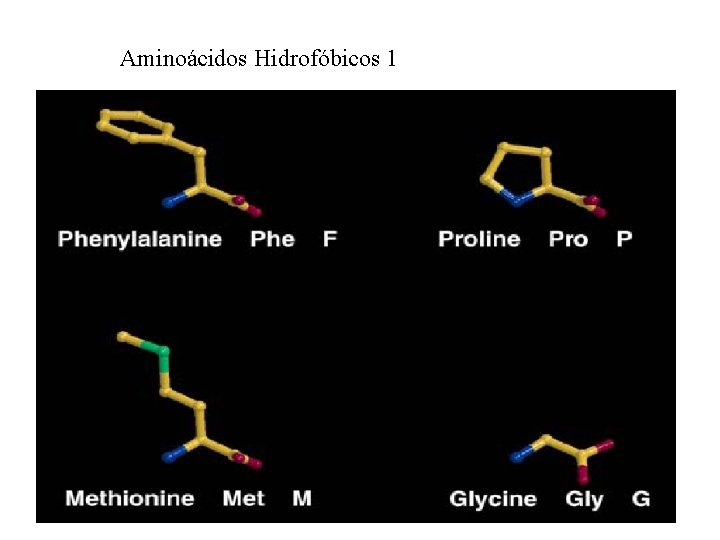
Aminoácidos Hidrofóbicos 1
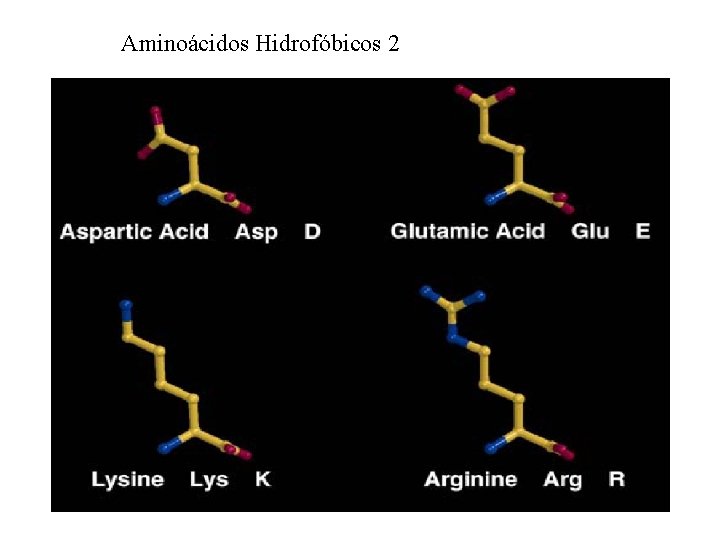
Aminoácidos Hidrofóbicos 2
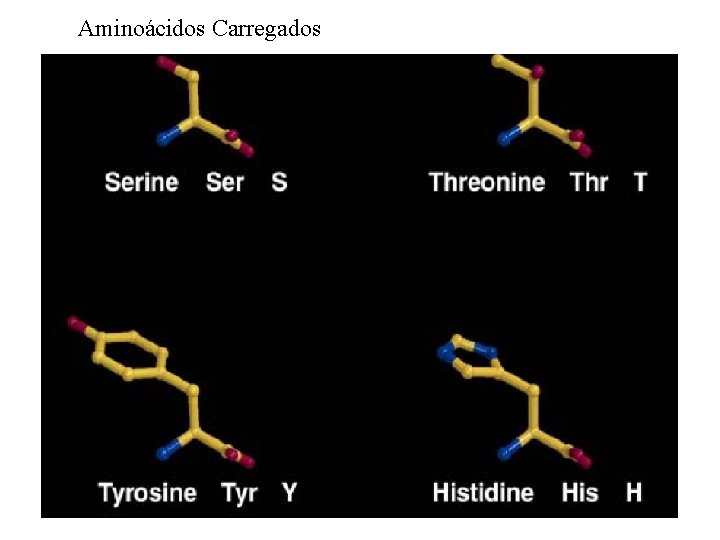
Aminoácidos Carregados
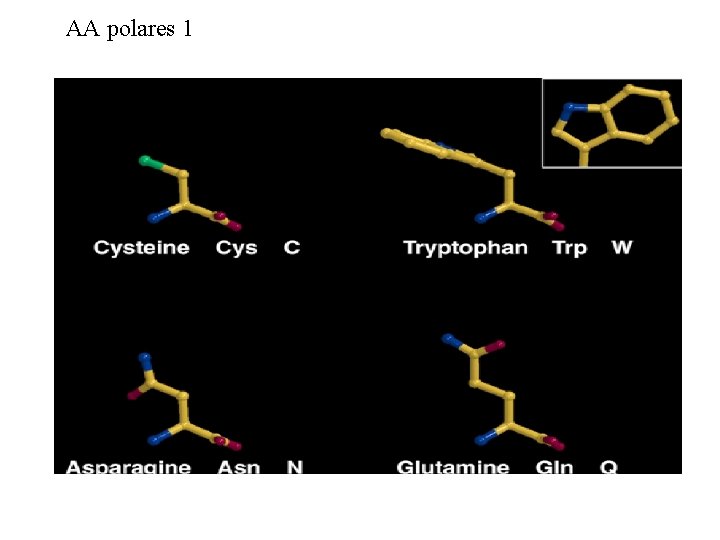
AA polares 1
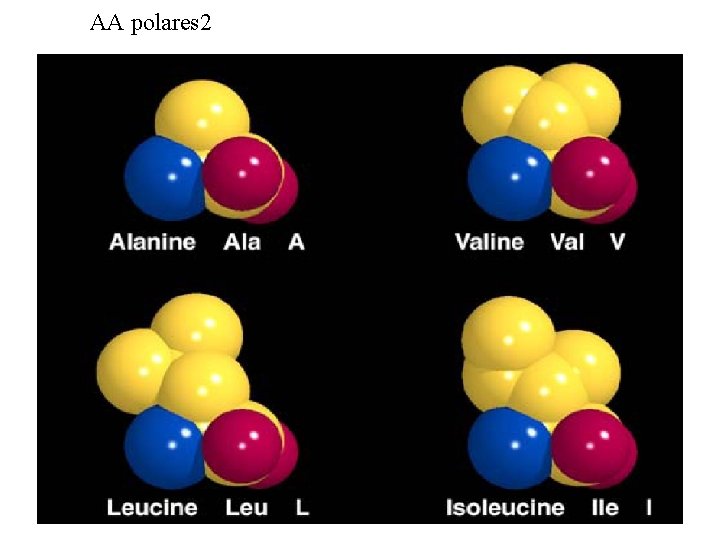
AA polares 2
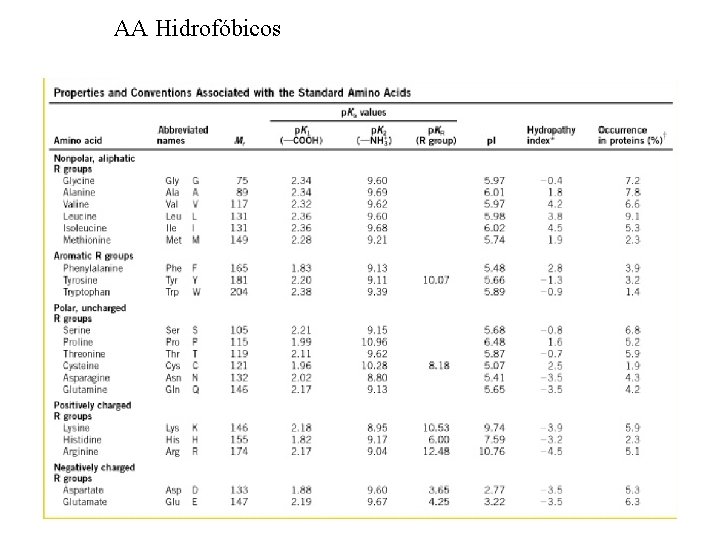
AA Hidrofóbicos




O p. Ka do Ácido Acético 3 HC-COOH 4. 5, O p. Ka do R-NH 3+ 10 Por que os p. Ka´s dos grupos carboxila e Amônio dos AA´s são menores? ~2, e ~9 respectivamente?



AA´s em proteínas são via de regra L ! Será a vida Quiral? ? ? Será que tem a ver com a síntese de proteínas RNAm? ?

Reação de Ninhidrina UV-Vis espectro, 280 nm Métodos identificar aa´s



Aminas 1árias Violeta Aminas 2árias Amarelo (Prolina)

Excepto pelo Triptofano os outros AA´s são pouco fluorescentes Porém existem associações que levam a fluorescência O que é fluorescência ? ?












Estrutura tri-D de proteinas, note a proteina é escrita do N terminal (esquerda) para o C terminal (direita). A sequência é única Sequência 1ária.

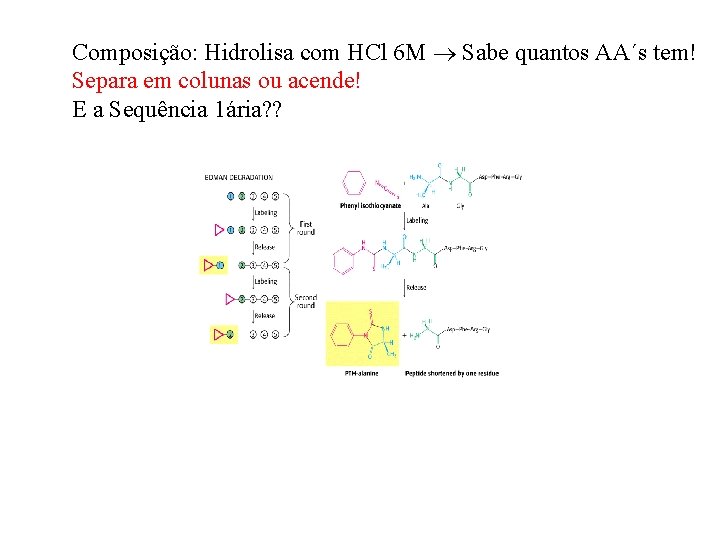
Composição: Hidrolisa com HCl 6 M Sabe quantos AA´s tem! Separa em colunas ou acende! E a Sequência 1ária? ?
Reage no N-terminal, repete processo várias vezes Hoje em dia síntese e geração de proteínas é +/- fácil Proteoma!!!
- Slides: 84