CHEMIOTERAPIA NOWOTWORW PRZEWODU POKARMOWEGO RAK JELITA GRUBEGO Epidemiologia

CHEMIOTERAPIA NOWOTWORÓW PRZEWODU POKARMOWEGO

RAK JELITA GRUBEGO

Epidemiologia 2 miejsce u obu płci w strukturze zachorowań (po 10%) Ø Około 11000 nowych zachorowań/rok (2000 r. ) Ø Wzrost ryzyka > 45 – 50 r. ż. Ø U 75% stadium wczesne, ale u 50% nawrót w ciągu 2 lat po pierwotnie radykalnym leczeniu operacyjnym a u 25% rak wyjściowo zaawansowany (gł. rozsiew do wątroby) Ø Przeżycia 5 letnie ok. 20 -30% - o połowę mniej niż w Europie Zach i USA Ø

Czynniki ryzyka Ø 65 -85% zachorowań ma charakter sporadyczny Ø 10% ma charakter rodzinny Ø 3% jest spowodowana mutacją silnych genów predyspozycji

Czynniki ryzyka Ø Polipy gruczołowe jelita grubego l Większość raków powstaje z gruczolaków, a ich wspólną cechą jest dysplazja nabłonka l Ryzyko przemiany gruczolaka do raka zwiększa się wraz z następującymi cechami gruczolaka: • wielkością > 2 cm • typem siedzącym, nieuszypułowanym, typem kosmkowym • stopniem dysplazji l Zaleca się usuwanie wszystkich polipów stwierdzonych w czasie badania endoskopowego

Czynniki ryzyka Czynniki środowiskowe (dietetyczne): l przewaga tłuszczów zwierzęcych l mało błonnika, wapnia l brak aktywności fizycznej l zaparcia Ø Choroby zapalne jelita grubego: colitis ulcerosa – ryzyko 20 x większe, choroba Leśniowskiego-Crohna Ø Uwarunkowania dziedziczne i genetyczne Ø

Uwarunkowania dziedziczne Ø Zespoły z obecnością gruczolaków l l Zespół polipowatości gruczolakowatej rodzinnej: FAP: 0, 5 -1% Dziedziczny rak jelita grubego bez polipowatości: HNPCC (Lynch): 2% Ø Zespoły z polipami hamartomatycznymi: <1% l l l Zespół Peutz-Jeghersa Zespół polipowatości młodzieńczej Zespół Cowdena

Zespół gruczolakowatej polipowatości rodzinnej (FAP) Mnogie (>100) polipy gruczolakowate w jelicie grubym od wczesnej dorosłości – 10 -20 lat Ø Rozpoznawany w endoskopii Ø Mutacja genu APC Ø Średni wiek zachorowania na raka j. grubego – ok. 40 lat Ø Inne nowotwory: żołądka, j. cienkiego, tarczycy, Ø brodawki Vatera, hepatoblastoma, mięsaki, guzy mózgu Ø Nie-nowotworowe: kostniaki żuchwy, guzy desmoidalne, łagodne guzy nadnerczy

Zespół Lynch - HNPCC Mutacje w genach naprawy MMR (mismatch repair genes) Ø Ryzyko raka j. grubego – 80% Ø Towarzyszą inne nowotwory: endometrium (70%), jajnika, żołądka, j. cienkiego, dróg żółciowych Ø Cechy szczególne raka j grubego: zachorowania synchroniczne i metachroniczne, 70% w prawej okrężnicy, mała tendencja do meta, śr. wiek zachorowania 45 lat Ø

Zespół Lynch - HNPCC Ø Kryteria Amsterdamskie rozpoznawania zespołu Lynch: l l Ø Zachorowanie na raka j grubego lub nowotwory ze spektrum Lynch u 3 i więcej osób w 2 kolejnych pokoleniach Jedno zachorowanie < 50 rż Jeden chory jest krewnym I stopnia dla pacjenta Wykluczenie FAP – weryfikacja histologiczna Modyfikacja Bethesda: l Nowotwór j grubego < 50 rż lub zachorowanie na neo ze spektrum Lynch o 10 lat wcześniej niż typowo

Zespół Peutz`a-Jeghers`a Mnogie polipy w p. pokarmowym o typie hamartoma (hamartoma – obok elem. nabłonkowych zawierają też inne elementy tkankowe, gł. włókna m gładkich), gł. w jelicie cienkim Ø Przebarwienia na bł. śluzowych policzków, czerwieni wargowej, palców Ø Często 1 szy objaw – wgłobienie j. cienkiego przed 20 rż. , inne: niedrożność, bóle brzucha, krwawienie Ø Ryzyko raka podwyższone: j cienkiego, grubego, trzustki, żołądka, piersi, jajnika, czerniaka Ø

Polipowatość młodzieńcza Mnogie polipy hamartomatyczne na całej długości przewodu pokarmowego spowodowane wzrostem blaszki właściwej Ø Występowanie: 1 lub 2 dekada życia Ø Przeciętny wiek RJG – 34 lata Ø Choroba Cowdena: mnogie polipy hamartomatyczne podobne do młodzieńczych, tłuszczaki, nerwiaki, rak piersi < 25 roku życia, rak tarczycy, glejaki, grudkowe zmiany skórne Ø

Rodzinnie występujący RJG Ø Ok. 10 -15% chorych na RJG ma krewnego w I st. z pozytywnym wywiadem, ale inaczej niż w FAP i HNPCC Ø Ryzyko rozwoju raka 2 x większe gdy krewny I st. , 3 -4 x gdy dwóch krewnych I st.

Umiejscowienie 30 -50% - odbytnica l 15 -20% - esica l 14% - jelito ślepe i okrężnica wstępująca l 9% - poprzecznica l 6% - okrężnica zstępująca l 1% - kanał odbytu Ø 5% - mnogie guzy (synchroniczne – w tym samym czasie, metachroniczne – po latach) Ø makroskopowo l Polipowaty, owrzodziały, rozlegle naciekający l

Histologia Ø 90 -95% rak gruczołowy Ø Gruczołowo - śluzowy Ø Sygnetowokomórkowy Ø Drobnokomórkowy Ø Płaskonabłonkowy Ø Gruczołowo – płaskonabłonkowy Ø Niezróżnicowany

Rak jelita grubego - objawy Ø Wczesny: l l l Bez objawów Pobolewania brzucha Nadmierne oddawanie gazów Zaburzenia rytmu wypróżnień Krwawienie utajone/jawne Niedokrwistość

Rak jelita grubego - objawy Ø Późny – prawa strona: l l Ø Niespecyficzne bóle brzucha, obj. zapal wyrostka u osoby po 65 rż. Osłabienie, utrata wagi ciała Niedokrwistość mikrocytarna Wyczuwalny guz Późny –lewa strona: l l Zmiana rytmu wypróżnień, zaparcia lub biegunka Kolkowy ból brzucha Podniedrożność/niedrożność Stolec z domieszką świeżej krwi

Rak jelita grubego - objawy Ø Rak odbytnicy: l l l Zaburzenia rytmu wypróżnień Uczucie pełności w odbytnicy Konieczność wypróżnienia Krwawienie jawne Bolesne parcie na stolec Ból w miednicy małej

Rak jelita grubego - objawy Ø Rak odbytu: Krwawienie (najczęściej klinicznie jawne) l Świąd odbytu, wydzielina śluzowopodobna, brudzenie bielizny l Ból lub bolesne parcie l Uczucie przeszkody bądź ciała obcego l Nietrzymanie gazów i/lub stolca l Wyczuwalny lub nawet widoczny guz l Powiększenie węzłów chłonnych pachwinowych l

Drogi rozprzestrzeniania § Miejscowe naciekanie § Rak odbytnicy: w kierunku pęcherza moczowego i kości § krzyżowej Rak okrężnicy: perforacja żołądka, jelita cienkiego lub sąsiedniego odcinka jelita grubego (np. rak esicy wywołuje perforację kątnicy) § Przerzuty drogą limfatyczną § Rozsiew po otrzewnej § Przerzuty drogą krwionośną, głównie przez naczynia układu wrotnego

Stopniowanie Ø Klasyfikacja Dukesa w modyfikacji Astlera- Collera Ø Klasyfikacja TNM

Rak jelita grubego – miejsca przerzutów Wątroba 38 -60% Węzły chłonne jamy brzusznej 39% Płuca 38% Otrzewna 28% Jajnik 18% Nadnercza 14% Opłucna 11% Kości 10% Mózg 8%

Czynniki prognostycznie niekorzystne § Obecność przerzutów w regionalnych węzłach chłonnych i liczba zmienionych przerzutowo węzłów § § § § Zajęcie naczyń chłonnych/krwionośnych przez komórki raka Mikro-inwazja raka wzdłuż nerwów Naciek guza przez całą ścianę jelita lub na tkanki otaczające Stopień histologicznej złośliwości G 3 lub G 4 Typ z komórek sygnetowatych lub drobnokomórkowy Operacja z powodu niedrożności lub perforacji Podwyższone stężenie CEA przed- i po operacji

Molekularne czynniki prognostyczne Ø Delecja 18 q – niekorzystny Ø Niestabilność mikrosatelitarna (MSI) – korzystna Ø Inne: wysoka ekspresja syntazy tymidylanowej, mutacja p 53 - niekorzystne

Rak jelita grubego – ogólne zasady terapii § Leczeniem zasadniczym jest radykalne wycięcie jelita z guzem z limfadenektomią – operacja musi być makroskopowo doszczętna § Leczenie adiuwantowe jest zawsze wskazane, jeżeli obecne są niekorzystne czynniki prognostyczne Leczenie adiuwantowe należy zastosować nie później niż po 6 -8 tygodniach od operacji

Leczenie uzupełniające Ø Adjuwantowe l Stosowanie cytostatyków skojarzone z radykalną radioterapią lub radykalnym operacyjnym usunięciem guza pierwotnego, a skierowane przeciwko domniemanym przerzutom, dla których istnienia brakuje wykładników w badaniach diagnostycznych, ale których późniejsze ujawnienie jest bardzo prawdopodobne

Leczenie uzupełniające Ø Neoadjuwantowe l Leczenie uzupełniajace, które poprzedza leczenie radykalne i ma na celu wczesne oddziaływanie na mikroprzerzuty Ø Leczenie indukcyjne l Poprzedza leczenie miejscowe o założeniu radykalnym, ale jego celem jest przede wszystkim uzyskanie zmniejszenie masy guza i ułatwienie przeprowadzenia leczenia radykalnego (operacji lub radykalnej rth)

Ogólne zasady terapii § Rodzaj terapii adiuwantowej zależy od lokalizacji guza § Okrężnica lub odbytnica powyżej załamka otrzewnej § W adiuwancie tylko CTH § Odbytnica poniżej załamka otrzewnej § RTH przed operacją w adiuwancie tylko CTH § Bez RTH przed operacją w adiuwancie RTH/CTH § RTH w raku odbytnicy poprawia przeżycie

Rak jelita grubego – chirurgia Ø Rodzaje resekcji guza (R – residual tumor) l R 0 – zabieg doszczętny makroskopowo i mikroskopowo – CEL l R 1 – zabieg niedoszczętny mikroskopowo l R 2 – zabieg niedoszczętny makroskopowo (leczenie paliatywne) Ø Minimum 12 węzłów chłonnych powinno być zbadanych hist- pat.

Rak jelita grubego – leczenie adiuwantowe 1. Chemioterapia systemowa (PS 2): 1. Zawsze jeżeli są niekorzystne czynniki prognostyczne 2. Złoty standard”: dożylne podawanie 5 fluorouracylu z leukoworyną (5 -FU/FA) przez 6 miesięcy 3. Obecnie w raku okrężnicy udowodniono wyższość nad „złotym standardem” w terapii adiuwantowej w zakresie dłuższego przeżycia: 4. Kapecytabiny – doustna pochodna 5 -FU 5. Schematu FOLFOX (Oxaliplatyna + 5 -FU/FA)

Fluorouracyl Pochodna fluoropirymidynowa, pro-lek, aktywne metabolity hamują syntezę DNA, fazowo-specyficzny, działa w fazie S Ø Działania niepożądane: zapalenie błon śluzowych, biegunki, mielosupresja, odczyny skórne Ø Wąski indeks terapeutyczny: RR u 10 -15% Ø Poprawa indeksu terapeutycznego przez: l Podawanie kwasu folinowego wapnia przed 5 Fu: puli wewnątrzkom folianów, większe hamowanie DNA – podwojenie RR l Wydłużone wlewy (22 h): RR ale mediana przeżycia podobna, lepsza tolerancja l Chronomodulacja: najlepsza tolerancja o 4 rano, więc wlewy nocne Ø

Rak jelita grubego –najczęstsze leki Kapecytabina: doustna pochodna fluoropirymidynowa, prekursor 5 Fu, aktywność odpowiada aktywności 5 Fu we wlewach ciągłych Ø Irynotekan: pochodna kamptotecyny, hamuje topoizomerazę I i syntezę DNA Ø l Ø Działania niepożądane: biegunki cholinergiczne (atropina przed!), neutopenia, zsp. zatorowo-zakrzepowe Oksaliplatyna: pochodna platyny III generacji, hamuje replikację DNA l Działania niepożądane: neurotoksyczność

Kliniczne skale oceny stanu sprawności (PS-Performance Status) Ø Skala WHO = ECOG = Zubroda (i Skala Karnofsky’ego) l l l 0: brak objawów i normalna aktywność życiowa; pełna sprawność (100%) 1: niewielkie objawy i pacjent ambulatoryjny, i nie ma przeszkód w zwykłej codziennej aktywności życiowej (90 -80%) 2: obecne objawy i pacjent spędza w łóżku < 50% dnia, i czasami wymaga opieki pielęgniarskiej; może zadbać o większość swoich potrzeb osobistych (70 -60%) 3: obecne znaczne objawy i pacjent spędza w łóżku > 50% dnia, i wymaga opieki pielęgniarskiej; niepełnosprawny (50 -40%) 4: obecne znaczne objawy i pacjent leżący cały czas w łóżku; w znaczącym stopniu niepełnosprawny i może wymagać szybkiej hospitalizacji (30 -10%) Śmierć (0)

CRC – choroba rozsiana 1. Chemioterapia systemowa jest podstawą terapii (PS 2 wg WHO) 1. Na podstawie badań III fazy za standard w leczeniu I rzutu można uznać stosowanie schematów trójlekowych: 1. Irinotekan + 5 -FU/FA (np. FOLFIRI) lub 2. Oxaliplatyna + 5 -FU/FA (np. FOLFOX) 2. Miejscowo zaawansowany i nieresekcyjny guz odbytnicy – wskazanie do RTH/CTH

CRC – choroba rozsiana Ø U chorych z przerzutami ważne by rozważyć leczenie chirurgiczne Ø U chorych z przerzutami do wątroby podanie neoadjuwantowej chemioterapii zwiększa o 30% liczbę resekcji

Terapia celowana Cetuksymab – Erbitux: przeciwciało skierowane przeciw miejscu wiązania ligandu w receptorze EGF (naskórkowego czynnika wzrostu) Ø Zarejestrowany do leczenia raka j. grubego z przerzutami w skojarzeniu z irinotekanem u pacjentów ze stwierdzoną ekspresją EGFR, u których doszło do niepowodzenoia chemioterapii z zastosowaniem irinotekanu (ASCO 2005 cetuksymab + IRI w 3 lub 4 rzucie leczenia czasu całkowitego przeżycia) Ø

Terapia celowana Bevacizumab – Avastin: blokuje VEGF zanim ten zwiąże się z receptorem Ø VEGF: czynnik wzrostu śródbłonków naczyniowych, najsilniejszy czynnik pobudzajacy angiogenezę Ø Bevacizumab jest dopuszczony do stosowania w leczeniu pierwszego rzutu uogólnionego raka jelita grubego z przerzutami w skojarzeniu z chemioterapią opartą na stosowaniu 5 Fu ( przeżycia o 30%) Ø

Terapia celowana Ø Badania kliniczne: Skojarzone leczenie cetuksymabem z oksaliplatyną i kapecytabiną l Cetuksymab z IRI i 5 Fu w 1 szej linii leczenia l Skojarzone leczenie cetuksymabem i bevacizumabem + chtp (badanie BOND II) l

Badania kontrolne po zakończeniu leczenia Ø Badanie lekarskie i CEA co 3 mies przez 2 lata, potem co 6 miesięcy Ø Kolonoskopia co 3 lata Ø Sigmoidoskopia co 6 mies w raku odbytnicy Ø USG/CT j. brzusznej co 6 miesięcy Ø Rtg kl. piersiowej co rok

Rak jelita grubego – chemoprewencja Ø Zapobieganie: polipektomia Ø Zatrzymanie transformacji nowotworowej przy użyciu leków: ASA, NLPZ, kw. foliowy, Ca Ø ekspresja COX-2 w gruczolakach i raku j. grubego, stężenia Pg w ścianie j. grubego Ø ASA i inne NLPZ: ryzyka raka j grubego o ok. 50%, częstości gruczolaków

Rak jelita grubego –badania przesiewowe Ø Test na krew utajoną w stolcu Ø Badanie per rectum Ø Badanie endoskopowe jelita grubego Ø Radiologiczne badanie kontrastowe jelita grubego (wlew doodbytniczy)

Rak jelita grubego – badania przesiewowe Ø Grupa zwykłego ryzyka zachorowania na raka jelita grubego: l l l Ø Chorzy > 50 rż Bez indywidualnego i/lub rodzinnego wywiadu w kierunku gruczolaka, raka Bez wywiadu w kierunku choroby zapalnej Profilaktyka: l Badania przesiewowe po 50 rż l Badanie na krew utajoną w stolcu 1 x w roku l Badanie endoskopowe: sigmoidoskopia co 5 lat lub kolonoskopia co 10 lat lub l Wlew metodą podwójnego kontrastu co 10 lat

Rak jelita grubego Przebycie jednego z następujących: Ø Polip gruczołowy l Ø Kolonoskopia 3 lata po wykryciu polipa, jeżeli prawidłowa to następne badania co 5 lat Przewlekłe zapalne choroby jelit l Kolonoskopia co 1– 2 lata • U pacjentów z pancolitis – począwszy od 8 roku od wykrycia choroby zapalnej • U pacjentów ze zmianami tylko po lewej stronie – począwszy od 15 roku od wykrycia choroby zapalnej

Zespół gruczolakowatej polipowatości rodzinnej (FAP) Ø Badania profilaktyczne gdy mutacja APC: l l 0 -7 rż. – bad fizykalne, USG j brzusznej, AFP (hepatoblastoma) Od 15 rż. – kolonoskopia co roku • Jeśli w j. grubym dużo gruczolaków: kolektomia • Badanie górnego odc. p. pokarmowego – brodawki Vatera (gastroskopia co 1 -3 lata od 25 rż). • Inhibitory COX-2 (hamowanie powst. polipów w zachowanym fragm. jelita)

Zespół Lynch - HNPCC Ø Postępowanie u nosicieli mutacji: l l Kolonoskopia co 2 lata od 25 rż. Kobiety: USG tv + Ca 125 + cytologia co 1 -2 lata od 30 -35 rż Gastroskopia co 1 -2 lata od 30 -35 rż Wykonanie kolonoskopii co 3 lata z polipektomią zmniejszyło o 50% ryzyko raka jelita grubego

Leczenie raka żołądka

Rak żołądka – zasady leczenia Leczenie operacyjne: standard postępowania w I, III • Leczenie operacyjne może być uznane za jedyny zabieg radykalny w < p. T 3 i p. N 0 (wymagane pobranie w Ø czasie operacji 15 węzłów chłonnych) • W pozostałych (ale M 0) stopniach klinicznego zaawansowania operacja powinna być skojarzona z terapią okołooperacyjną: neoadiuwantową/indukcyjną lub adiuwantową → brak standardu

Leczenie adjuwantowe CHT adiuwantowa (aczkolwiek powszechnie stosowana) nie może być uznana za postępowanie standardowe na podstawie wyników dotychczas przeprowadzonych badań; może nowe leki (? ) • CTH/RTH może stać się standardem w leczeniu adiuwantowym po gastrektomii R 0, jeżeli potwierdzą się w innych badaniach wyniki uzyskane w badaniu GCI 0116 (korzyści w sensie 3 -letniego wydłużenia DFS – 48% vs 31% i OS – 50% vs 41% u pacjentów w stadiach IB – IV-M 0) •

Leczenie adjuwantowe Ø Wskazania do uzupełniającej radiochemioterapii u chorych po radykalnej operacji żołądka: l l l Naciek całej grubości ściany żołądka (p. T 3, p. T 4) N+ G 3 Zatory w naczyniach Naciekanie pni nerwowych, tkanki tłuszczowej

Leczenie uzupełniające CTH neoadiuwantowa/indukcyjna i CTH/RTH neoadiuwantowa są przedmiotem szeregu prospektywnych badań klinicznych u chorych z T 3/T 4 lub N 1 -N 3 Ø Leki: • l l 5 FU wlewy ciągłe Duże dawki LV, 5 FU, MTX

Rak żołądka –leczenie choroby rozsianej • CTH paliatywna podstawową metodą terapii choroby rozsianej – udowodnione wydłużenie przeżycia Zalecane schematy chemioterapii w leczeniu paliatywnym • PELF (Cis-Platin, Epirubicin, Leucovorin, 5 -FU) • ECF (Epirubicin, Cis-Platin, 5 -FU) • DCF (Docetaxel, Cis-Platin, 5 -FU): RR 65%, śr przeżycie 10 mies. • II rzut: irinotekan lub oxaliplatyna + 5 FU • Preferencja paliatywnej resekcji nad zespoleniami omijającymi • RTH paliatywna – bardzo ograniczone zastosowanie, ew. w przerzutach do kości i czasami w hamowaniu krwawień z żołądka •

Nowotwory podścieliskowe żołądka (GIST – gastrointestinal stromal tumors) Wywodzą się z mezenchymalnych komórek rozrusznikowych nerwów zwojowych – komórek Cajala Ø Ich rozwój wynika z mutacji genu c-KIT (4 q 12) Ø Następstwem mutacji c-KIT jest naddekspresja receptorowego białka CD 117, wykazującego aktywność kinazy tyrozynowej (KT) Ø 60 -70% GIST występuje w ścianie żołądka, 20 -30% jelita cienkiego, < 10% przełyku i jelita grubego, sporadycznie w sieci lub krezce Ø

Nowotwory podścieliskowe żołądka (GIST – gastrointestinal stromal tumors) Objawy ü Zwykle przypadkowo wykrywane, bezobjawowe lub niespecyficzne objawy ü Przy naciekaniu śluzówki lub surowicówki pp objawy krwawienia, perforacji, niedrożności ü Wyczuwalny guz, przerzuty do otrzewnej, wątroby, rzadziej płuc i kości Ø Leczenie ü Operacja (jeżeli nie ma przeciwwskazań) 50 -60% przeżyć 5 -letnich ü W chorobie rozsianej, nawrocie po operacji o wątpliwej resekcyjności, przy przeciwwskazaniach do operacji IMATINIB (Glivec, Gleevec) – bloker KT, 400 -800 mg/d, kontynuować do czasu wystąpienia progresji > 80% odpowiedzi klinicznych w ciągu 12 miesięcy Ø

Leczenie raka trzustki

Epidemiologia raka trzustki Ø Ø 3% wszystkich npl - około 3000 rocznie; 7/100 000 u mężczyzn, 4/100 000 u kobiet; 5. zabójca wśród npl; Rak trzustki jest rozpoznawany zwykle w zaawansowanym stadium nowotworu (T 3 -4/N 1 lub M 1) co zasadniczo wpływa na skuteczność leczenia: • • resekcyjność w 10 -15% przypadków średnie całkowite przeżycie od momentu rozpoznania = 3 -6 miesięcy 12 -miesięczne przeżycie = ~10% pięcioletnie przeżycie = 0. 5 -3%

Leczenie – zasady ogólne 1. Decyzja terapeutyczna zależy od zakwalifikowania chorego do jednej z 3 grup: 1. 2. 3. Z rakiem pierwotnie resekcyjnym (stopnie 0, I, II) – mediana przeżycia 13 -20 mies. Z rakiem pierwotnie nieresekcyjnym, ale bez przerzutów odległych (stopień III - nie nacieka pnia trzewnego ani tętnicy krezkowej górnej) – 6 -10 mies Z rakiem pierwotnie rozsianym (stopień IV) – 3 -6 mies.

Rak pierwotnie resekcyjny Ø Resekcja R 0 (pankreatoduodenektomia, pankreatektomia dystalna lub całkowite usunięcie trzustki) wraz z regionalnymi w. chłonnymi pierwszą metodą terapii w stadiach w guzach T 1 T 2 i N 0.
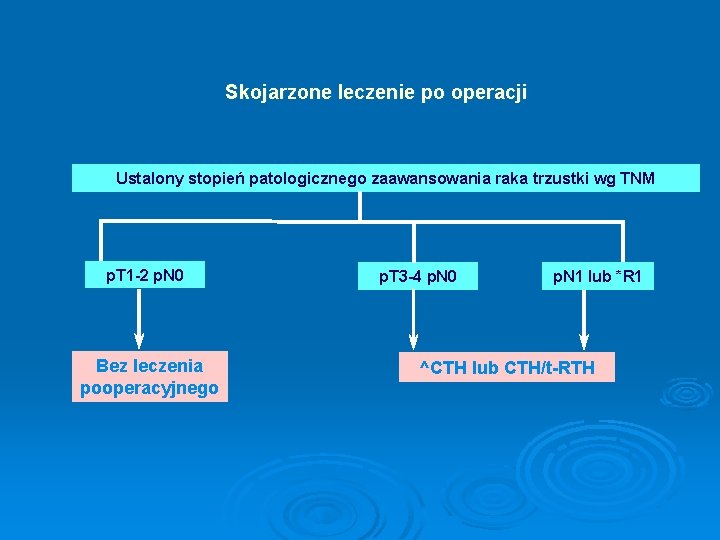
Skojarzone leczenie po operacji Ustalony stopień patologicznego zaawansowania raka trzustki wg TNM p. T 1 -2 p. N 0 Bez leczenia pooperacyjnego p. T 3 -4 p. N 0 p. N 1 lub *R 1 ^CTH lub CTH/t-RTH
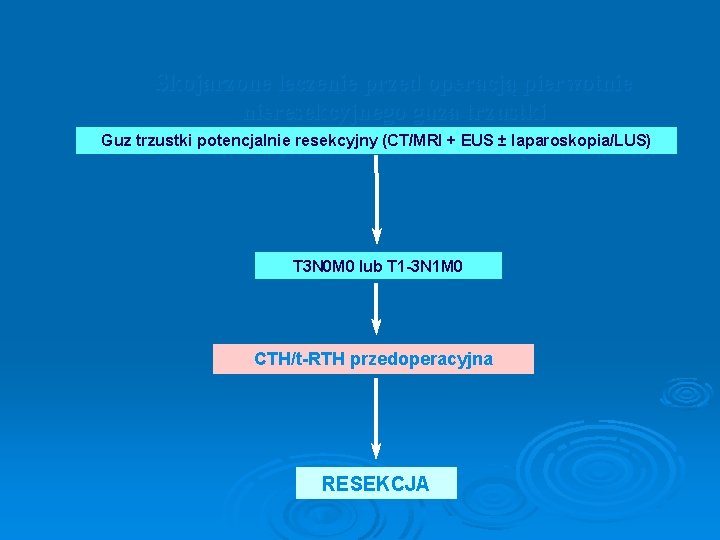
Skojarzone leczenie przed operacją pierwotnie nieresekcyjnego guza trzustki Guz trzustki potencjalnie resekcyjny (CT/MRI + EUS ± laparoskopia/LUS) T 3 N 0 M 0 lub T 1 -3 N 1 M 0 CTH/t-RTH przedoperacyjna RESEKCJA
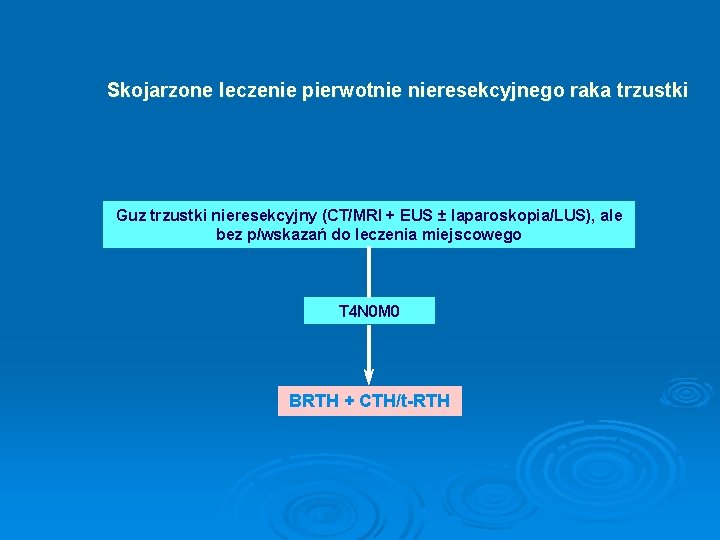
Skojarzone leczenie pierwotnie nieresekcyjnego raka trzustki Guz trzustki nieresekcyjny (CT/MRI + EUS ± laparoskopia/LUS), ale bez p/wskazań do leczenia miejscowego T 4 N 0 M 0 BRTH + CTH/t-RTH
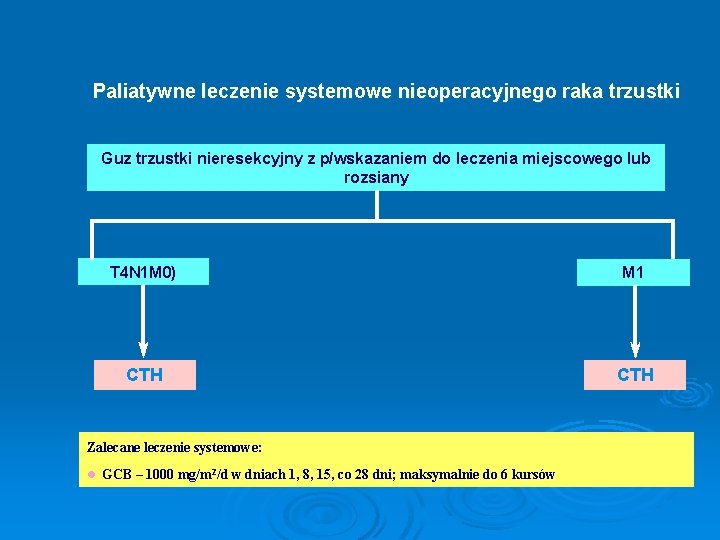
Paliatywne leczenie systemowe nieoperacyjnego raka trzustki Guz trzustki nieresekcyjny z p/wskazaniem do leczenia miejscowego lub rozsiany T 4 N 1 M 0) M 1 CTH Zalecane leczenie systemowe: l GCB – 1000 mg/m 2/d w dniach 1, 8, 15, co 28 dni; maksymalnie do 6 kursów
- Slides: 61