Cromatografia Gasosa de Lipdios como Ferramenta para Estudos


































































































- Slides: 124

Cromatografia Gasosa de Lipídios como Ferramenta para Estudos de Ecologia Microbiana Marcelo Ferreira Fernandes

Resumo • Parte I. Ecologia Microbiana • Parte II. Diversidade Genética, Estrutural e da Composição Química de Lipídios em Microrganismos • Parte III. Lipídios como Ferramenta para Estudos de Ecologia Microbiana

PARTE I Ecologia Microbiana

Ecologia Microbiana • Objetivos: – Entender a biodiversidade de microrganismos na natureza e como diferentes guildas interagem em comunidades microbianas – Medir a atividade dos microrganismos na natureza e monitorar seus efeitos sobre o ecossistema (componentes bióticos e abióticos)

Interações entre Microrganismos e Impactos Ambientais e Econômicos Derivados de suas Atividades

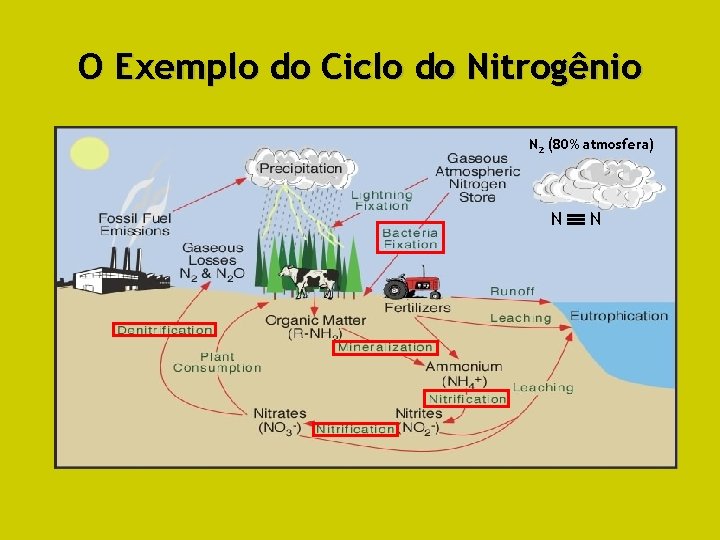
O Exemplo do Ciclo do Nitrogênio N 2 (80% atmosfera) N N

Outros Exemplos de Impactos Ambientais e Econômicos Derivados da Atividade de Microrganismos

• Controle da disponibilidade de nutrientes minerais para as plantas – Ciclagem de nutrientes, associações simbióticas (FBN, micorrizas), perdas de nutrientes • Seqüestro de carbono e balanço de gases de efeito estufa • Melhoria da qualidade física e química do solo – Formação de húmus, formação e estabilização de agregados de solo • Controle biológico de pragas e doenças vegetais e animais • Processos infecciosos (doenças) em plantas e animais • Decomposição de alimentos e outros bens • Biolixiviação de minerais de importância econômica (cobre, ouro, urânio. . . ) • Biorremediação de xenobióticos (pesticidas, petróleo, explosivos, nylon. . . ) • Tratamento de águas; eutroficação de águas e poluição de lençóis freáticos • Corrosão de metais, entupimento de tubulações de água e óleo • Produção de enzimas de importância industrial, fármacos, combustíveis, polímeros para plásticos biodegradáveis etc. . . •

Fatores que Controlam Estes Processos e Impactos • Bióticos – Presença e atividade de uma guilda específica – Interações entre guildas • Abióticas

A Atividade do “Fator Biótico” Visa à Sobrevivência • Obtenção de energia ou de compostos para síntese celular – Ciclos biogeoquímicos (C, N, P, S, Fe, Mn, Hg. . . ) – Associações simbióticas com plantas e animais – Patógenos, predadores e parasitas • Transformação de compostos tóxicos ao crescimento microbiano – Ciclos biogeoquímicos • Proteção contra fatores ambientais adversos • . . .

Diversidade Metabólica Microbiana • Vasta diversidade de “modos de vida” ou de conseguir recursos para sobrevivência – Entre espécies de microrganismos – Dentro da mesma espécie

Obtenção de Energia (Aerobiose) – Corg → CO 2 (Fungos, bactérias, protozoários. . . ) • Decomposição de restos animais e vegetais • Formação do solo (CO 2 + H 2 O H 2 CO 3), formação de humus, ciclagem de nutrientes – NH 4+ → N 2 O → NO 3 - (Nitrosomonas, Nitrobacter. . . ) • Contaminação de águas com NO 3 • Gases de efeito estufa – Fe 2+ → Fe 3+ (Thiobacillus ferroxidans) • Biolixiviação de metais (cobre, ouro, urânio. . . ) – CH 4 + 2 O 2 → CO 2 + 2 H 2 O • Importante dreno de metano – So + H 2 O + 1 ½ O 2 → SO 42 - + 2 H+ (Thiobacillus, Beggiatoa. . . ) • Solubilização de fosfatos de rocha pela acidificação do solo, corrosão de estruturas metálicas. . . – 2 H 2 + O 2 → 2 H 2 O (Alcaligenes, Ralstonia. . . ) – CO + ½ O 2 → CO 2 (carboxidotróficas: Pseudomonas carboxydovorans) • Principal dreno de monóxido de carbono da Terra

Obtenção de Energia (Anaerobiose: Aceptores de Elétrons) – CO 2 → CH 4 (Arqueas metanogênicas: Methanobacterium, Methanococcus) • Gás de efeito estufa e combustível – NO 3 - → NO → N 2 (Alcaligenes, Pseudomonas. . . ) • Perda de fertilizantes • Gases de efeito estufa – Fe 3+ → Fe 2+ (Geobacter, Shewanella, Geospirillum, Thiobacillus ferroxidans, Sulfolobus. . . ) • Degradação de compostos aromáticos (benzoato, toleno) utilizados como fonte de energia (doadores de elétrons) • Biolixiviação de metais de sulfetos metálicos. – SO 42 - + acetato ou H 2 → H 2 S (Desulfovibrio, Desulfobacter. . . ) • Toxidez à vida aquática • Desclorinação redutiva de pesticidas clorados

Obtenção de Compostos para Síntese e Metabolismo Celulares • Fotoautotrofia (algas, cianobactérias, Euglena) – Fixação de CO 2, via luz • Quimoautotrofia (muitas bactérias e arqueas) – Fixação de CO 2, via oxidação de compostos minerais • Heterotrofia (fungos, protozoários, bactérias, arqueas) – C orgânico (saprofitismo, simbiose, parasitismo ou predação) • Fixação Biológica do N 2 (algumas bactérias) – N 2 • . . . Dinitrogenase NH 4+

Interações entre Guildas Microbianas • Rizóbios (fixadores simbióticos de N 2) vs. actinomicetos (produtores de antibióticos) → controle do processo da FBN em soja • Fermentadores (diversos mcgs) vs. metanogênicos (arqueas anaeróbicas) vs. metanotróficos (bactérias anaeróbicas): balanço de metano entre solo e atmosfera → controle do processo de efeito estufa H 2 CO 2 CH 4

Fatores Abióticos de Controle da Atividade, Biomassa e Composição de Comunidades Microbianas

Atividade, Biomassa e Composição Microbianas são Afetadas por: – Disponibilidade de oxigênio • De modo geral, bactérias e arqueas mais versáteis que eucariotos – Disponibilidade de água • Fungos e actinomicetos mais resistentes a seca • Holoarqueas = extremófilos Temperatura • Extremófilos = poucas bactérias; ultra-extremófilos = muitas arqueas – Disponibilidade de nutrientes • Oligotróficos vs. copiotróficos – Disponibilidade de energia – p. H • Fungos = ácido; bactérias = neutro (Extremos em Arquea e Bacterias) – Toxidez por produtos naturais e artificiais – Interações biológicas. . .

Impactos Antropogênicos sobre a Microbiota e Processos Associados • Preparo do solo: – aeração, temperatura, umidade, p. H • Pesticidas e outros compostos químicos: – toxidez seletiva ou geral • Culturas, sistemas de culturas, mudanças de uso da terra – quantidade e qualidade de substrato, relações hospedeiro e microrganismos, temperatura e umidade • Adubações e calagem: – disponibilidade de nutrientes, p. H. . . • Irrigação e drenagem: – disponibilidade de água, temperatura e oxigênio. . . • Pecuária: – disponibilidade de nutrientes, oxigênio. . . • Deposições atmosféricas industriais: – disponibilidade de nutrientes, p. H. . .

Exemplos de Impactos de Atividades Humanas sobre a Atividade, Biomassa e Composição das Comunidades Microbianas

Mudança do Uso da Terra • Substituição de florestas por pastagens: – Pisoteio animal → compactação do solo → reduz fluxo de oxigênio para o solo • Ambiente aeróbico → anaeróbico • Favorecimento de metanogênicos em detrimento de metanotróficos • Aumento da emissão de CH 4 para a atmosfera – Remoção da cobertura vegetal → maior incidência solar → dessecamento da superfície do solo • Limitação de água na superfície, mas não no subsolo • Menor atividade de metanotróficos • Aumento da emissão de CH 4 para a atmosfera


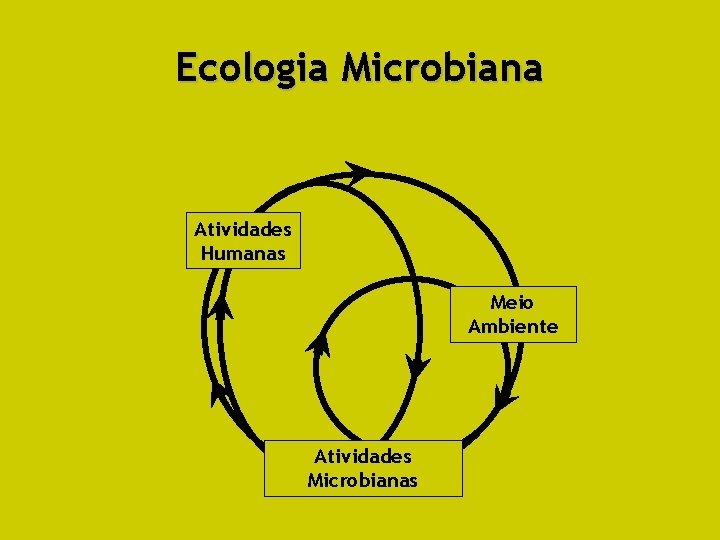
Ecologia Microbiana Atividades Humanas Meio Ambiente Atividades Microbianas

PARTE II Diversidade Genética, Estrutural e da Composição Química de Lipídios em Microrganismos

De Onde Vem a Capacidade dos Microrganismos de Realizar Tantas Funções e de se Adaptar a Tantos Ambientes Distintos?

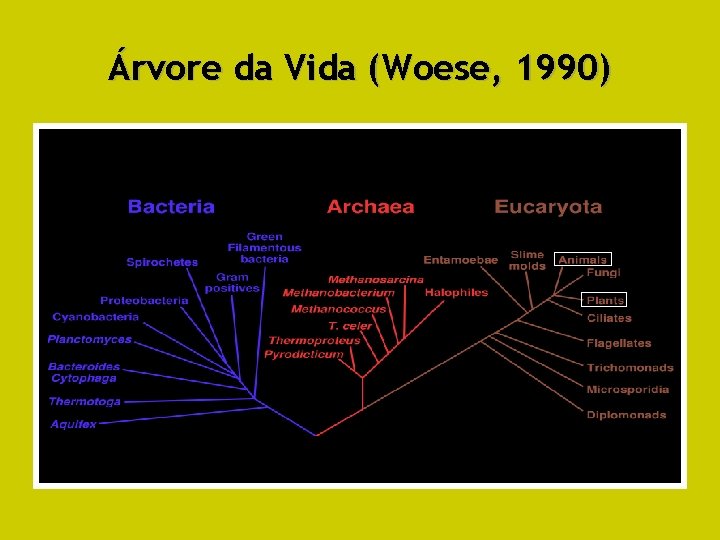
Diversidade Genética • “Alta diversidade de genes” – Diversidade metabólica potencial determinada pelos genes de cada espécie. – Evolução cria novos genes a partir de outros existentes – Acúmulo de genes diferentes do ancestral: nova sps. • Taxonomia molecular baseada em similaridade nas seqüências de genes – Seqüências r. RNA (Woese, 1990) – Três domínios muito distintos • Bacteria • Archea • Eukarya

Árvore da Vida (Woese, 1990)

Evolução, estruturas celulares e composições de macromoléculas • Além de gerar diversidade metabólica, a evolução genética resultou em diferenças marcantes em estruturas celulares e composições de macromoléculas entre grupos taxonômicos de microganismos: – Ex: parede celular e estrutura química dos lipídios

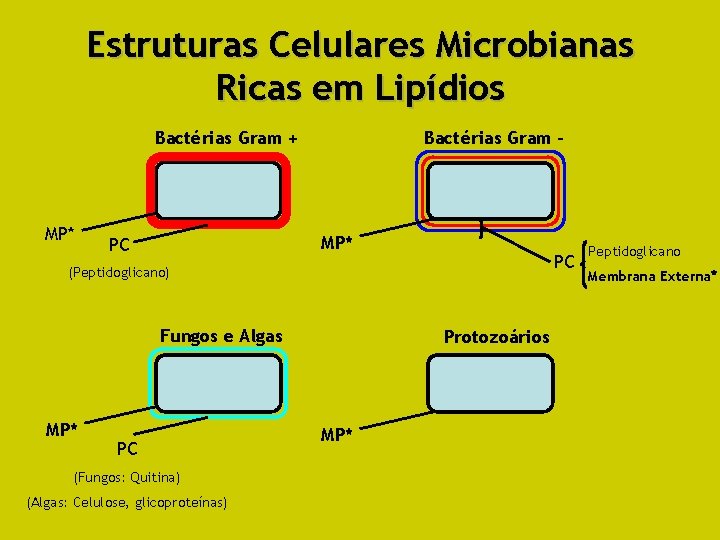
Estruturas Celulares Microbianas Ricas em Lipídios Bactérias Gram + MP* Bactérias Gram - MP* PC PC (Peptidoglicano) Fungos e Algas MP* PC (Fungos: Quitina) (Algas: Celulose, glicoproteínas) Protozoários MP* Peptidoglicano Membrana Externa*

Estruturas Celulares Microbianas Ricas em Lipídios (cont. ) Achaea MP* PC (Pseudpeptidoglicano ou glicoproteínas ou polissacarídeos)

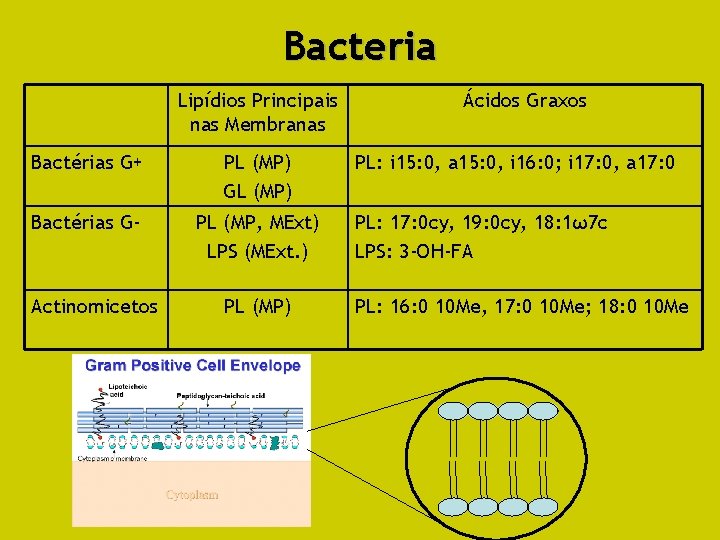
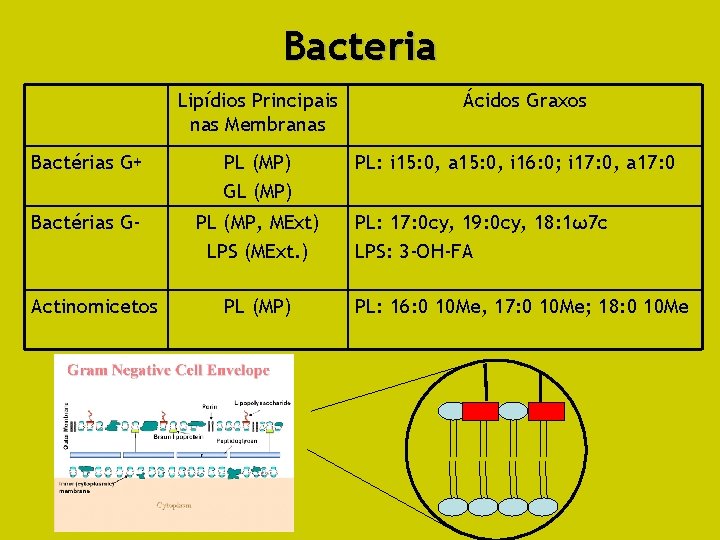
Bacteria Lipídios Principais nas Membranas Bactérias G+ PL (MP) GL (MP) Bactérias G- PL (MP, MExt) LPS (MExt. ) Actinomicetos PL (MP) Ácidos Graxos PL: i 15: 0, a 15: 0, i 16: 0; i 17: 0, a 17: 0 PL: 17: 0 cy, 19: 0 cy, 18: 1ω7 c LPS: 3 -OH-FA PL: 16: 0 10 Me, 17: 0 10 Me; 18: 0 10 Me

Bacteria Lipídios Principais nas Membranas Bactérias G+ PL (MP) GL (MP) Bactérias G- PL (MP, MExt) LPS (MExt. ) Actinomicetos PL (MP) Ácidos Graxos PL: i 15: 0, a 15: 0, i 16: 0; i 17: 0, a 17: 0 PL: 17: 0 cy, 19: 0 cy, 18: 1ω7 c LPS: 3 -OH-FA PL: 16: 0 10 Me, 17: 0 10 Me; 18: 0 10 Me

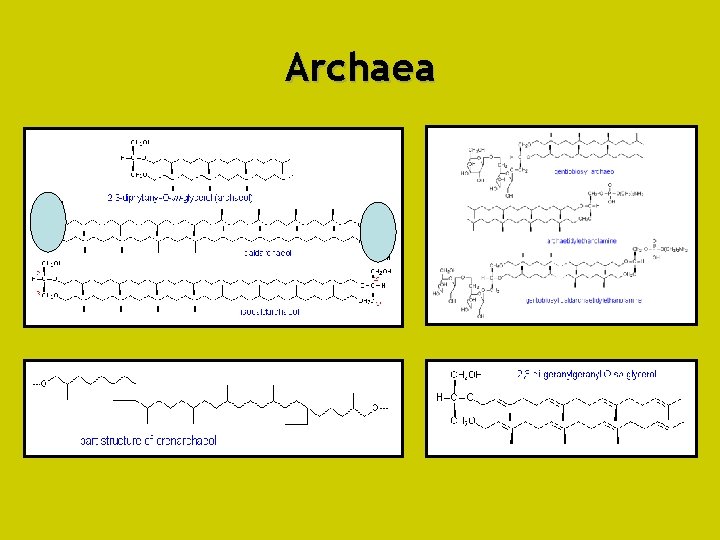
Archaea

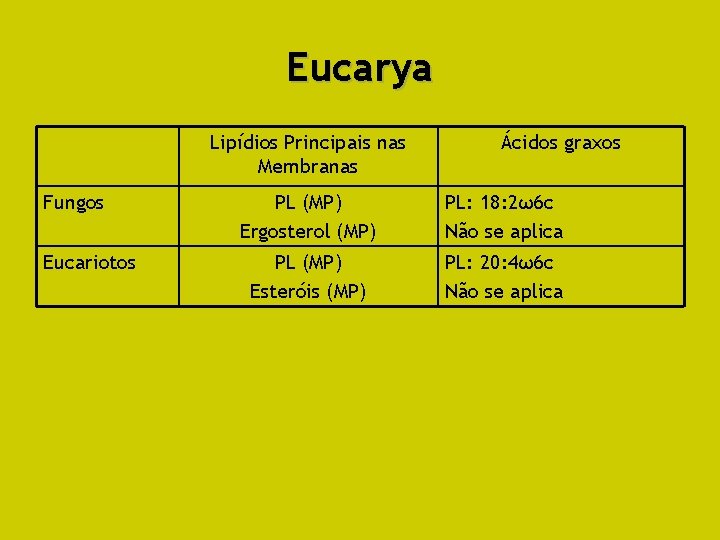
Eucarya Lipídios Principais nas Membranas Fungos Eucariotos Ácidos graxos PL (MP) Ergosterol (MP) PL: 18: 2ω6 c Não se aplica PL (MP) Esteróis (MP) PL: 20: 4ω6 c Não se aplica

PARTE III Lipídios como Ferramenta para Estudos de Ecologia Microbiana

Ecologia Microbiana Aspectos de Interesse • Biomassa microbiana • Atividade microbiana • Composição ou estrutura da comunidade

Métodos para Investigação da Estrutura da Comunidade Microbiana • Dependentes de cultivo – Meios seletivos para organismos de interesse – Plaqueamento da amostra em meio de cultura sólido – Enumeração e identificação de microrganismos

Organismos Cultiváveis Fungos Actinomicetos Protozoários, Bactéria Archaea Algas


Organismos Viáveis, Não-Cultiváveis • Torsvik, V. et al. High Diversity in DNA of Soil Bacteria. Applied and Environmental Microbiology, 56(3): 782 -787, 1990. • Apenas 1 a 10% dos microrganismos na natureza são cultiváveis em laboratório; • Embora não cultiváveis, esses organismos são ativos na natureza; • Exemplos de impacto: – Morris et al. (Nature, 2002): • SAR 11, ser vivo mais abundante do planeta, não-cultivável. – Nitrificação: • Bactérias Nitrosomonas e Nitrobacter (Winogradsky, 1888) • Wuchter et al. (PNAS, 2006): – Archaea (Crenarchaeota): 100 -1000 x mais abundante que bactérias nos oceanos • Leininger et al. (Nature, 2006): – Archaea (Crenarchaeota): ~3000 x mais abundante que bactérias no solo

Métodos de Investigação da Comunidade Microbiana Independentes de Cultivo

Métodos Independentes de Cultivo – DNA • taxons e funções mais específicos • Primers específicos para grupos taxonômicos microbianos (r. RNA) ou genes para enzimas relacionadas a uma determinada função (ex: bactérias nitrificantes = gene amo. . . ) – Lipídios • em geral, compara grandes grupos taxonômicos de microrganismos • poucos marcadores para grupos funcionais específicos • em alguns casos, atividade de guilda com uma função específica pode ser investigada em associação com técnicas isotópicas • Marcador fenotípico

Métodos Baseados em DNA (opcional) • Extração do DNA da amostra ambiental • Amplificação de regiões específicas do DNA (PCR e primers específicos) – Taxonomia (r. RNA) – Funções (genes específicos) • Padrão de bandas em gel de eletroforese – DGGE – LH-PCR – T-RFLP. . . • Clonagem e seqüenciamento de fragmentos amplificados ou recuperados das bandas do gel • Identificação microbiana utilizando-se ferramentas de comparação de similaridades entre seqüências obtidas com as disponíveis em bancos de dados de seqüências de DNA (NCBI)

Métodos Baseados em Lipídios • Princípio de avaliação da estrutura das comunidades microbianas: – Diversidade Estrutural de Ácidos Graxos – Associação entre estrutura e grupos microbianos (biomarcadores microbianos) – Inferências sobre mudanças na estrutura da comunidade a partir de mudanças no perfil de ácidos graxos

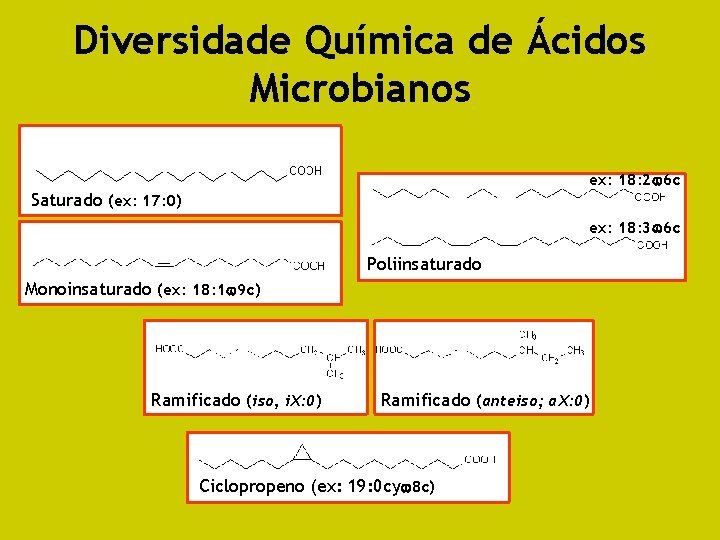
Diversidade Química de Ácidos Microbianos ex: 18: 2 6 c Saturado (ex: 17: 0) ex: 18: 3 6 c Poliinsaturado Monoinsaturado (ex: 18: 1 9 c) Ramificado (iso, i. X: 0) Ramificado (anteiso; a. X: 0) Ciclopropeno (ex: 19: 0 cy 8 c)

Nomenclatura dos Ácidos Graxos • X: Y – X = no de carbonos da molécula – Y = no de insaturações (duplas ligações) Ex: 16: 0 (ácido hexadecanóico) – Se Y>0 (insaturados): • X: Y Zc, onde Z é a posição da primeira insaturação à partir do C distal, e “c” indica a conformação “cis”, e t, a “trans” Ex: 16: 1 5 c; 18: 1 7 t; 18: 2 6 c • i. X: Y, a. X: Y, X: Y 10 -Me – Radical metil lateral na posição 2, 3 ou 10, a partir do C distal Ex: i 15: 0; a 15: 0; i 17: 0; 18: 0 10 -Me • X: Ycy Zc – cy representa presença de anel ciclopropeno Ex: 19: 0 cy 8 c

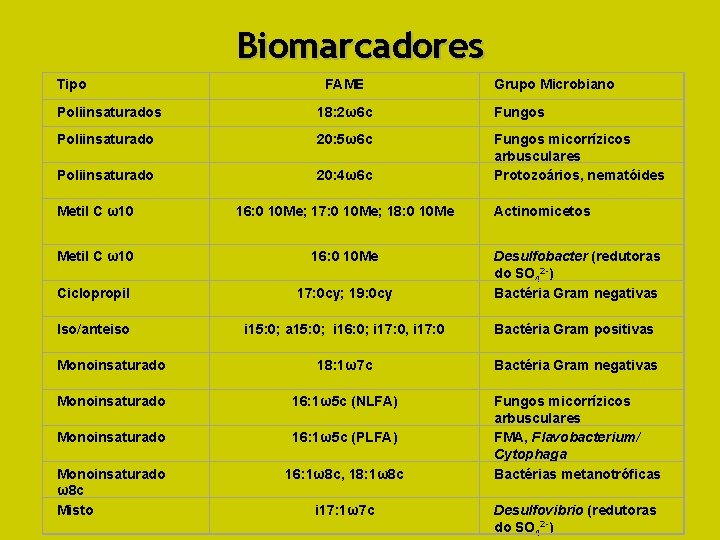
Ácidos Graxos Biomarcadores • Grupos Taxonômicos • Poucos de Grupos Funcionais Específicos

Biomarcadores Tipo FAME Grupo Microbiano Poliinsaturados 18: 2ω6 c Fungos Poliinsaturado 20: 5ω6 c Poliinsaturado 20: 4ω6 c Fungos micorrízicos arbusculares Protozoários, nematóides Metil C ω10 16: 0 10 Me; 17: 0 10 Me; 18: 0 10 Me Metil C ω10 Desulfobacter (redutoras do SO 42 -) Bactéria Gram negativas Monoinsaturado 16: 0 10 Me 17: 0 cy; 19: 0 cy i 15: 0; a 15: 0; i 16: 0; i 17: 0, i 17: 0 18: 1ω7 c Monoinsaturado 16: 1ω5 c (NLFA) Monoinsaturado 16: 1ω5 c (PLFA) Monoinsaturado ω8 c Misto 16: 1ω8 c, 18: 1ω8 c Fungos micorrízicos arbusculares FMA, Flavobacterium/ Cytophaga Bactérias metanotróficas i 17: 1ω7 c Desulfovibrio (redutoras do SO 42 -) Ciclopropil Iso/anteiso Actinomicetos Bactéria Gram positivas Bactéria Gram negativas

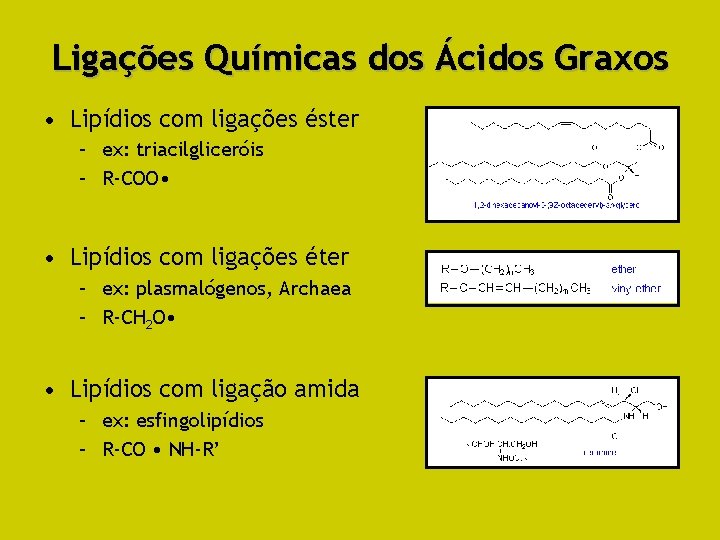
Ácidos Graxos em Diferentes Classes de Lipídios Complexos • Ácidos graxos raramente ocorrem livres em células • Normalmente, eles integram lipídios estruturalmente mais complexos • Diferentes tipos de ligações químicas unem os ácidos graxos ao restante da molécula dos lipídios complexos

Ligações Químicas dos Ácidos Graxos • Lipídios com ligações éster – ex: triacilgliceróis – R-COO • • Lipídios com ligações éter – ex: plasmalógenos, Archaea – R-CH 2 O • • Lipídios com ligação amida – ex: esfingolipídios – R-CO • NH-R’

Éster Metílico de Ácido Graxo “Fatty Acid Methyl Ester”(FAME) Ácido Graxo COOHR Metanólise Alcalina Branda (PLFA e EL-FAME) ou Saponificação – Metanólise Ácida (MIDI) FAME COOCH 3 Altamente volátil

Saponificação/Metilação • Duas etapas: – Saponificação: Ácido graxo sabão – Metilação: substituição do Na por metil FAME • Condições de reação: – Saponificação: altas temperaturas, 3, 8 M Na. OH em Me. OH: H 2 O (100 o. C, 30’) – Metilação: presença de água, 6 M HCl: Me. OH (85 o. C, 10’) • Ligações-alvo: – Éster, éter, amina, ácidos graxos livres • Altamente danosas à estrutura de alguns ácidos graxos: – ciclopropanos

Metanólise Alcalina Branda • Uma só etapa (transesterificação) – Separação de ácidos graxos das moléculas complexas e esterificação com ·CH 3 • Condições de reação: – 0, 2 M KOH em Me. OH (37 o. C, 1 h) – Ausência de água • Ligações-alvo – Ésteres

Principais Lipídios Complexos Contendo Ácidos Graxos

Fosfolipídios • Universal em membranas celulares, proporções aproximadamente constantes por massa celular – Exceto em Archaea, ligações são principalmente éster • Rápida hidrólise do fosfato após morte microbiana (Fosfolipídio -> Lipídio Neutro) • Microbiota viável

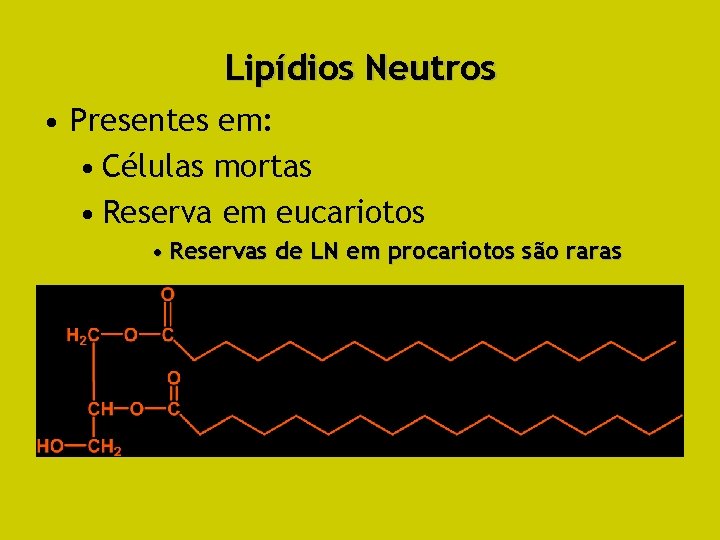
Lipídios Neutros • Presentes em: • Células mortas • Reserva em eucariotos • Reservas de LN em procariotos são raras

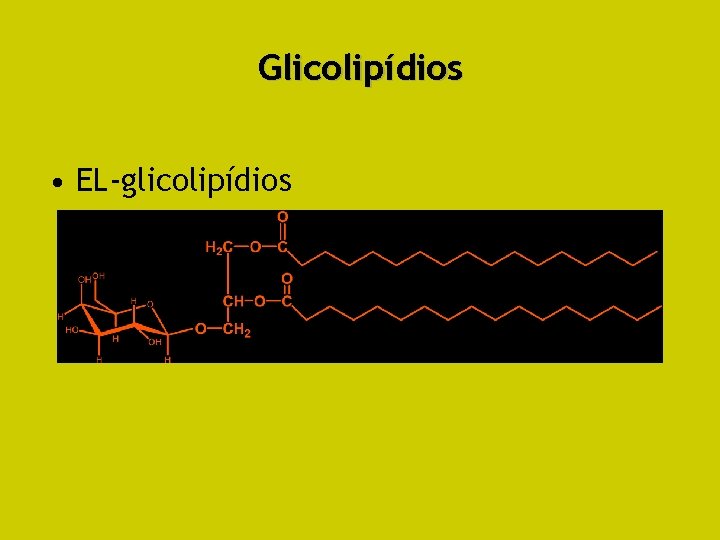
Glicolipídios • EL-glicolipídios

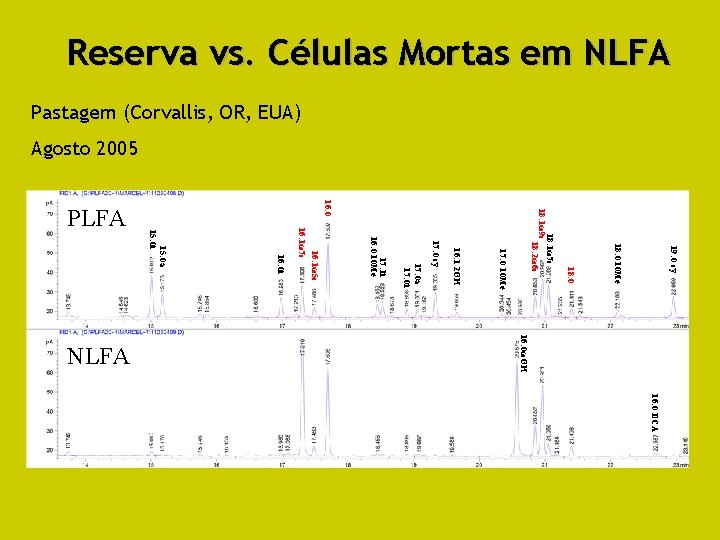
Reserva vs. Células Mortas em NLFA Pastagem (Corvallis, OR, EUA) Agosto 2005 19: 0 cy 18: 0 10 Me 18: 0 17: 1 i 16: 0 10 Me 17: 0 a 17: 0 i 17: 0 cy 16: 1 2 OH 17: 0 10 Me 18: 2ω6 c 18: 1ω7 c 18: 1ω9 c 16: 0 16: 1ω5 c 16: 1ω7 c 16: 0 i 16: 0ωOH NLFA 15: 0 a 15: 0 i PLFA 16: 0 DCA

Protocolos para Extração de FAMEs do Solo

Principais Protocolos de Extração de FAMEs • PLFA (Phospholipid Fatty Acids) – White e Ringelberg (1998) • MIDI (Microbial Identification™) - Sasser (1990) • EL-FAME (Ester-linked FAME) – Direto do solo (Schutter e Dick, 2000) – Extrato lipídico (Drjiber et al. , 2000)

Método: PLFA • Método mais utilizado (padrão) • Mais caro e trabalhoso – Coluna de SPE-Si: ~R$ 10, 00 (no Brasil) – 40 -50 ml de clorofórmio, acetona e metanol amostra-1 – 24 amostras em 2 dias • Extrai apenas ácidos graxos esterificados em fosfolipídios

Protocolo PLFA

Fase 1. Extração de Lipídios Totais do Solo • Bligh e Dyer (1959) modificado – Mistura monofásica metanol: clorofórmio: tampão fosfato 50 m. M (2: 1: 0, 8) – Solo: clorofórmio (1: 1, m/v) – Volumes de água e tampão fosfato 100 m. M – Ex: 4 g solo úmido com 25% umidade (b. u. ) • • 3 g solo seco + 1 g água 6 ml de metanol, 3 ml de clorofórmio, 2, 4 ml TF 50 m. M (combinação de água e TF 100 m. M) 1 ml água do solo + 0, 2 ml água adicionada + 1, 2 ml TF 100 m. M

1. 1. Solo e mistura de solventes em tubo de centrífuga com tampa com revestimento interno de teflon; 1. 2. Agitar por 2 h, decantar “overnight” – Variações: • • sonicação (2 min) tempo de agitação, omissão da decantação; 1. 3. Ressuspender solo e centrifugar (10 min e 2000 x g); 1. 4. Filtrar sobrenadante papel Whatman #1; 1. 5. Adicionar metanol: clorofórmio ao solo remanescente no tubo e repetir passos 1. 3 e 1. 4 mais duas vezes;

1. 6. Partição do filtrado em duas fases: adicionar solução Na. Cl 2 M (solução: clorofórmio, 1: 1); 1. 7. Esperar até que a desaparecimento da turbidez na fase superior (aquosa); 1. 8. Transferir a fase inferior (orgânica) para um tubo de ensaio e secá-la sob atmosfera de N 2 ultra-puro, a 37 o. C. Armazenar a -20 o. C.


Fase 2. Fracionamento das Classes de Lipídios (Cromatografia de Afinidade) • Extração em fase sólida (ácido silícico) • Partição de lipídios entre radicais silanóis ativos nos grânulos de ácido silícico e solventes de polaridade crescente (clorofórmio, acetona e metanol)



2. 1. Colocar coluna de ácido silícico (3 ml, 500 mg) em aparato de vácuo com tubo de ensaio diretamente abaixo da mesma; 2. 2. Adicionar 2 ml de clorofórmio à coluna, sem deixar drenar; 2. 3. Ressuspender extrato de lipídios em volume mínimo (100 -200 μL) de clorofórmio e transferir para coluna de ácido silícico. Repetir 3 vezes para assegurar transferência quantitativa; 2. 4. Acionar vácuo e adicionar 3 x 2 ml de clorofórmio, e coletar esses volumes no tubo de ensaio colocado abaixo; 2. 5. Trocar tubo de ensaio por um novo, adicionar 3 x 2 ml de acetona, e coletar volumes no tubo de ensaio abaixo; 2. 6. Trocar tubo de ensaio por um novo, adicionar 3 x 2 ml de metanol, e coletar volumes no tubo de ensaio abaixo; 2. 7. Secar frações sob atmosfera de N 2 ultrapuro , a 37 o. C, armazenar a -20 o. C.

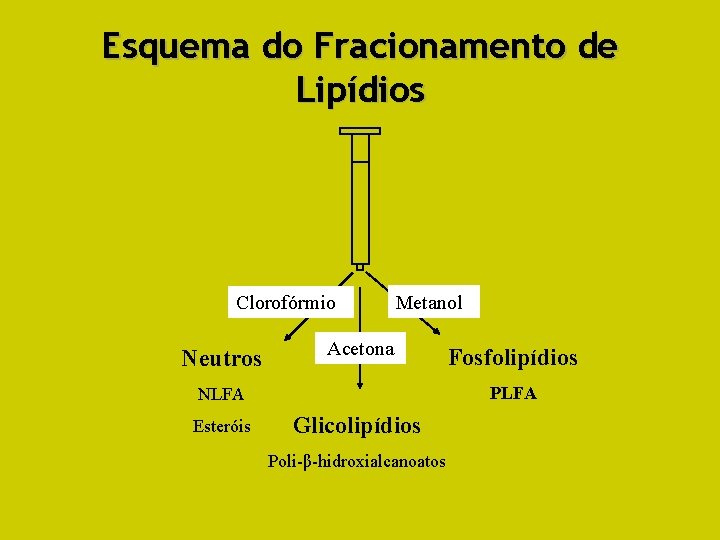
Esquema do Fracionamento de Lipídios Clorofórmio Neutros Metanol Acetona PLFA NLFA Esteróis Fosfolipídios Glicolipídios Poli-β-hidroxialcanoatos


Fase 3. Metanólise Alcalina para Produção dos FAMES de PL • Geração dos FAMEs a partir de fosfolipídios esterificados; • Remoção dos ácidos graxos do restante da molécula lipídica e substituição das ligações com glicerol por grupos metil > aumenta a volatilidade dos compostos • Para PLFA, proceder reação apenas na fração contendo fosfolipídios; • Nota: Dependendo do objetivo do estudo, a fração neutra e glicolipídica também poderão ser tratadas posteriormente para análise cromatográfica de compostos de interesse.

3. 1. Redissolver os lipídios fracionados secos em 1 ml de tolueno: metanol (1: 1, v/v) e 1 ml de KOH metanólico (0, 2 N); 3. 2. Agitar tubo em vortex, rapidamente, e colocá-los em banho-maria a 37 o. C por 15 min. ; 3. 3. Após amostras esfriarem até a temperatura ambiente, adicionar 2 ml de hexano: clorofórmio (4: 1, v/v), e misturar amostra; 3. 4. Neutralize p. H (6 a 7) da mistura com adição de 0, 2 ml de ácido acético 1 N. Verificar p. H final em papel de tornassol; 3. 5. Adicione 2 ml de água destilada para separar fases e misture amostra em vortex por 30 s. Esperar separação de fases se completar (~10 -15 min. ); 3. 6. Transferir fase orgânica (superior) para um tubo de ensaio novo, 3. 7. Reextrair fase inferior: adicionar 2 ml de clorofórmio: hexano (4: 1 v/v), agitar em vortex 30 s. , esperar separação de fases, transferir para tubo novo (repetir 2 x) 3. 8. Evaporar solvente sob N 2 ultrapuro, a 37 o. C; armazenar a -20 o. C, sob N 2.

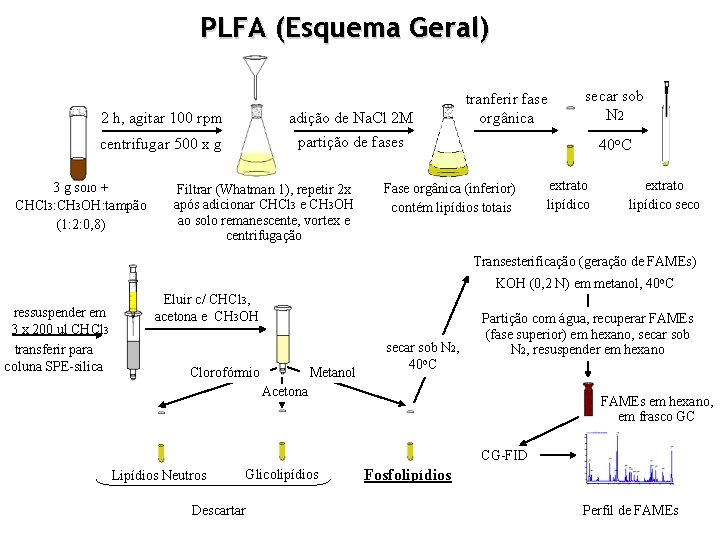
PLFA (Esquema Geral) 2 h, agitar 100 rpm adição de Na. Cl 2 M centrifugar 500 x g partição de fases 3 g solo + CHCl 3: CH 3 OH: tampão (1: 2: 0, 8) Filtrar (Whatman 1), repetir 2 x após adicionar CHCl 3 e CH 3 OH ao solo remanescente, vortex e centrifugação tranferir fase orgânica secar sob N 2 40 o. C Fase orgânica (inferior) contém lipídios totais extrato lipídico seco Transesterificação (geração de FAMEs) KOH (0, 2 N) em metanol, 40 o. C ressuspender em 3 x 200 ul CHCl 3 transferir para coluna SPE-silica Eluir c/ CHCl 3, acetona e CH 3 OH Clorofórmio Metanol secar sob N 2, 40 o. C Partição com água, recuperar FAMEs (fase superior) em hexano, secar sob N 2, resuspender em hexano Acetona FAMEs em hexano, em frasco GC CG-FID Lipídios Neutros Glicolipídios Descartar Fosfolipídios Perfil de FAMEs

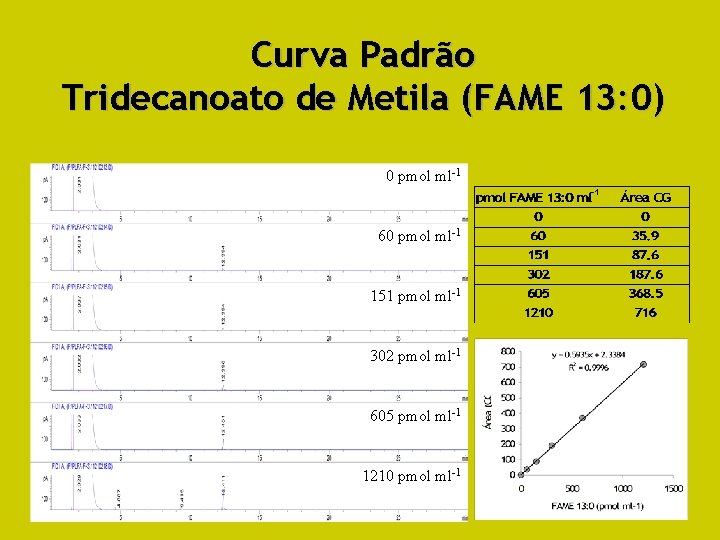
Fase 4. Preparo de Amostras, Separação em CG, Quantificação e Identificação de Compostos 4. 1. PLFA secos são ressuspensos em hexano, agitados em vortex, e transferidos para frasco GC com “insert” de 200 μL; 4. 2. Injeção em CG-FID, equipado com coluna não-polar (ex: 5% diphenyl, 95% methylpolysiloxane fase estacionária; ex: Ultra-2, DB-5, HP-5), com 25 m, 0, 2 mm diam. int. ; 0, 33 m espessura filme); rampa de temperatura: 170 -280 o. C a 4 o. C min-1; mais 5 min. a 280 o. C para limpeza da coluna. 4. 3. Curva-padrão: FAME 13: 0 (“methyl tridecanoic acid”): relação entre área de pico cromatográfico e quantidades conhecidas do FAME. Alternativamente: adição de padrão interno: usualmente FAME 19: 0. Resultados em mol de FAMEs individuais por g de solo (pmol FAME g-1 solo seco). 4. 4. Misturas padrões de FAMEs microbianos (BAME e FAME-37): comparar TR com amostras 4. 5. ECL vs. TR (Biblioteca de ECLs. Ex: MIDI) - Relação linear entre TR e número de C de série homóloga de ácidos graxos saturados de cadeia linear 4. 5. CG-EM (confirmação de compostos): importante, mas, em geral, não realizada.


Curva Padrão Tridecanoato de Metila (FAME 13: 0) 0 pmol ml-1 60 pmol ml-1 151 pmol ml-1 302 pmol ml-1 605 pmol ml-1 1210 pmol ml-1

Brancos - Verificar contaminações das amostras durante procedimento de extração - Todo o procedimento é realizado de modo idêntico às amostras, porém sem solo PLFA Br NLFA Br

Efeito do Desmatamento sobre a Estrutura da Comunidade Microbiana

Floresta Adulta (>150 a) vs. Floresta Recem-Cortada (10 a) 18: 2 6 c fungo >150 anos 16: 0 comum ~ 10 anos

Método: MIDI • Adaptado de método comercial para identificação de bactérias em cultura pura, de acordo com perfil de lipídios celulares totais • Mais rápido (? ) e barato que PLFA • Requer menor quantidades de solo (? ? ) • Mais perigoso (base e ácido concentrados, alta temperatura) • Extração direta, direta sob condições extremas de p. H e temperatura (saponificação/metilação ácida) • Extrai FAMEs de potencialmente todos os lipídios celulares (éster, éter, amida. . . ) e não-celulares (reserva, células mortas, fontes nãomicrobianas, matéria orgânica do solo. . . ), incluindo ácidos graxos livres • Forte potencial de alterar a estrutura química de muitos ácidos graxos, especialmente os com aneis ciclopropeno e os insaturados

Protocolo MIDI

Saponificação • Pesar 3 g de solo em tubo de de vidro (20 ml) com tampa de rosca revestida com Teflon; • Adicionar 3 ml de solução de Na. OH (3, 8 N) em água: metanol (1: 1 v/v); • Agitar em vortex e ferver por 30 min. • Produto: sais de sódio de cadeia longa (sabão)

Metilação Ácida • Adicionar 6 ml de mistura HCl (6 M): metanol (1: 0, 85 v/v); • Aquecer em banho-maria 85 o. C, 10 min. • Produto: FAMEs

Recuperação dos FAMEs • Adicionar 3 ml de hexano (partição de fases); • Transferir todo conteúdo do frasco para tubos de centrífuga de 35 ml, com rosca revestida por Teflon; • Centrifugar a 480 x g por 10 min. para separar MOS da fase orgânica; • Transferir fase orgânica (superior) para tubos de 13 x 100 mm com tampa revestida de Teflon;

Lavagem da Fase Orgânica • Adicionar 3 ml de base fraca (0, 3 M Na. OH) para lavar residual de reagentes ácidos • Agitar tubo lentamente por 5 min • Transferência da fase superior para tubos CG (2 ml)

Análise cromatográfica, quantificação e identificação dos compostos • Idem PLFA

Método: EL-FAME • Mais rápido (!), fácil (!) e barato que PLFA • Extrai ácidos graxos esterificados em diversas classes de lipídios (neutros, glicolipídios e fosfolipídios) • Contribuição de lípídios de reserva e de células mortas (LN), além de glicolipídios esterificados, para o perfil de FAMEs • Duas variações de extração: – direta do solo (Schutter e Dick, 2000); – a partir do extrato de lipídios totais (Drijber et al. , 2000).

Protocolo EL-FAME

Metanólise Alcalina Branda • Pesar 3 g de solo em tubo centrífuga de 35 ml com tampa revestida de Teflon; • Adicionar 15 ml de KOH (0, 2 N) em metanol; • Agitar em vortex e incubar a 37 o. C por 1 h (transesterificação, idêntica à do PLFA) • Agitar tubos em vortex a cada 10 min. durante o tempo de incubação. • Adicionar 3 ml de ácido acético 1, 0 M para neutralizar p. H do conteúdo do frasco

Recuperação dos FAMEs • Partir fases adicionando 10 ml de hexano; • Centrifugar a 480 x g, 10 min. ; • Transferir fase orgânica para tubo de ensaio e secar sob N 2 ultrapuro; • Ressuspender extrato seco em 3 x ~70 µL de hexano, agitando em vortex após cada adição do solvente, e transferir para frasco CG, com insert de 200 µL.

Análise cromatográfica, quantificação e identificação dos compostos • Idem PLFA

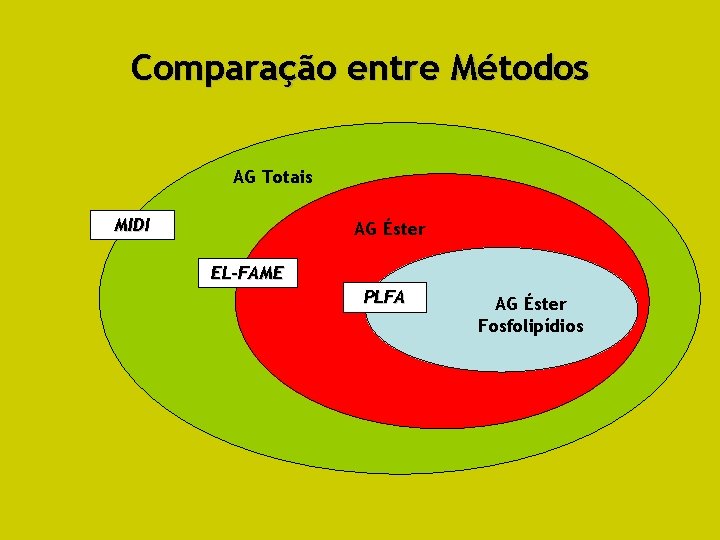
Comparação entre Métodos AG Totais MIDI AG Éster EL-FAME PLFA AG Éster Fosfolipídios

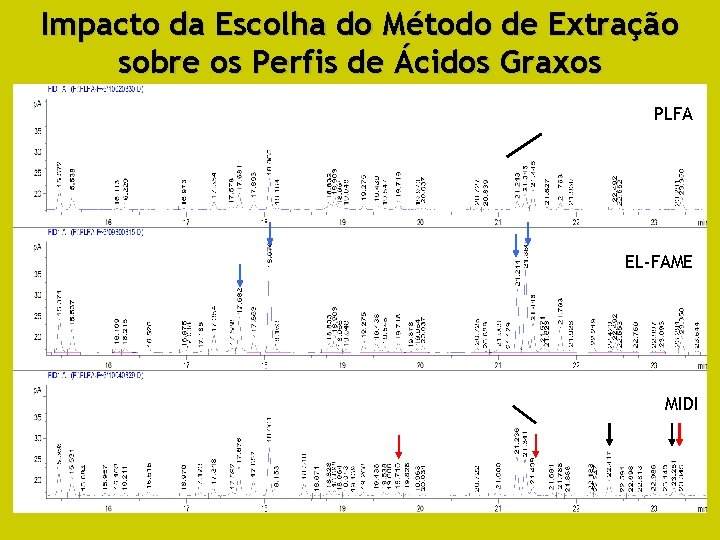
Impacto da Escolha do Método de Extração sobre os Perfis de Ácidos Graxos PLFA EL-FAME MIDI

Efeito da Escolha do Protocolo de Extração sobre a Interpretação de Resultados de Estrutura da Comunidade Microbiana

Amostras de Solo • 29 amostras de solo através do Estado do Oregon, EUA (0 -10 cm depth) • Ecossistemas diversos – Sem vegetação na data de amostragem – Herbáceas (culturas anuais, pastagens e pomares) – Florestas (gimnospermas com >150 a; clareiras de 10 a; mistas) • Ampla faixa de propriedades do solo – COT, MOP, MO-n. P, p. H, textura • Amostras de solo peneiradas (< 2 mm) • Extração de FAMEs pelos 3 métodos

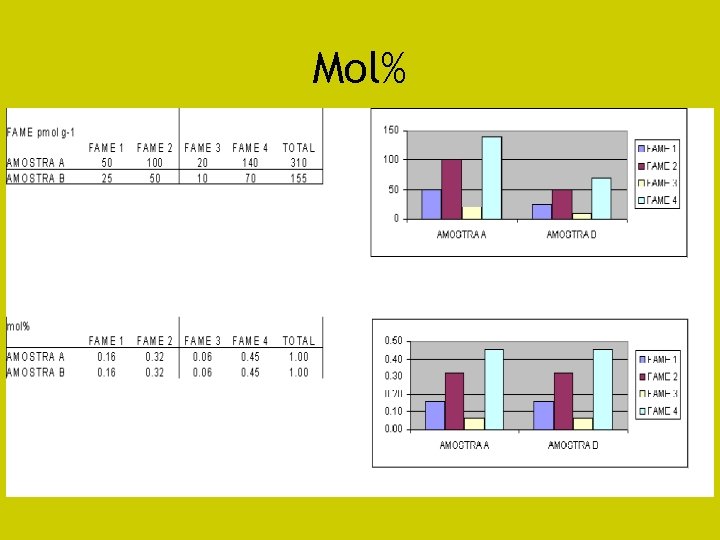
Análise de FAMEs • Cromatografia gasosa • Identificação inicial por comparação dos TR entre amostras e padrões de FAMEs microbianos • Confirmação de compostos abundantes por EM • Dados de composição de AG analisados em mol%

Mol%

MIDI versus PLFA • Análise estatística: ordenação multivariada NMS – Distância de Sorensen – PC-ORD 4, modo autopiloto “lento e abrangente” – Correlações com variáveis de solo e caracterização da mudanças no perfil de FAMEs utilizando coeficiente de Pearson (“joint plots”)

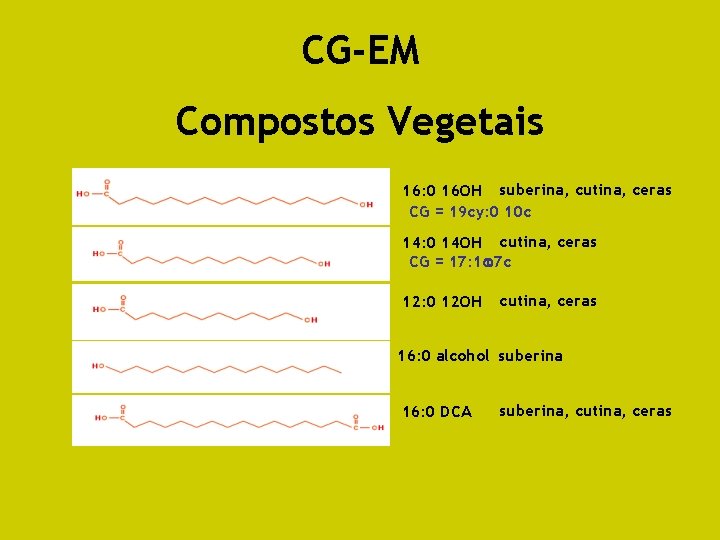
MIDI versus PLFA - Resultados • CG-MS: alguns biomarcadores de substâncias vegetais (cutina, suberina, e ceras) presentes em grandes quantidades no extrato de MIDI, mas não em PLFA

CG-EM Compostos Vegetais 16: 0 16 OH suberina, cutina, ceras CG = 19 cy: 0 10 c 14: 0 14 OH cutina, ceras CG = 17: 1 7 c 12: 0 12 OH cutina, ceras 16: 0 alcohol suberina 16: 0 DCA suberina, cutina, ceras

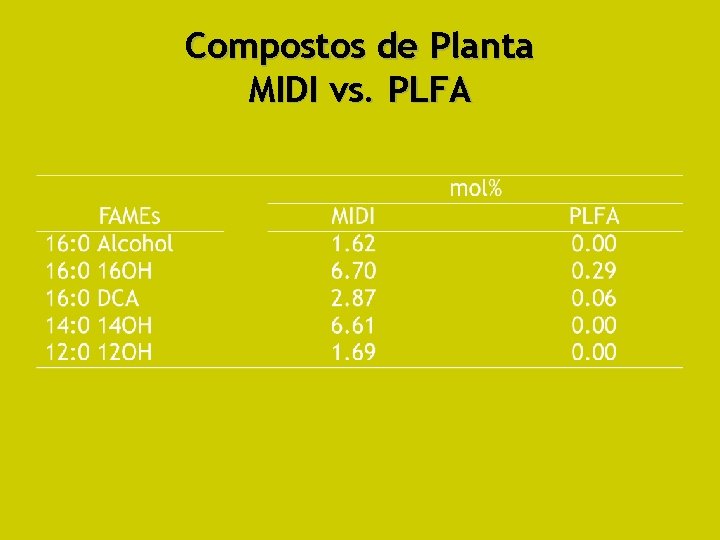
Compostos de Planta MIDI vs. PLFA

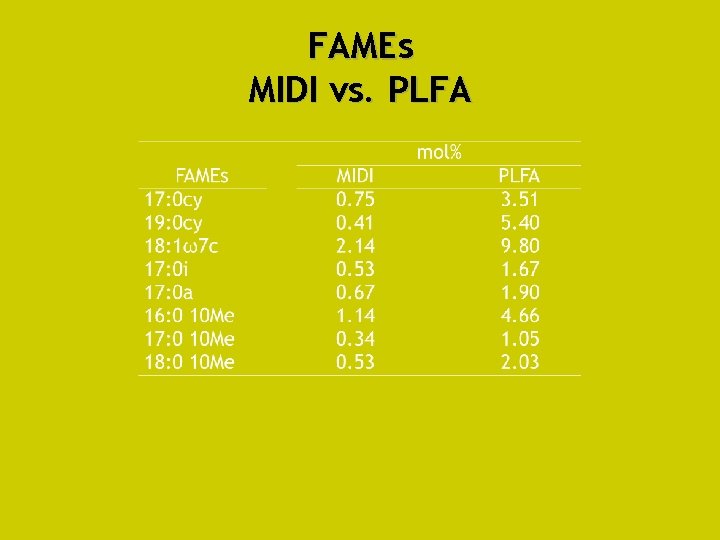
FAMEs MIDI vs. PLFA

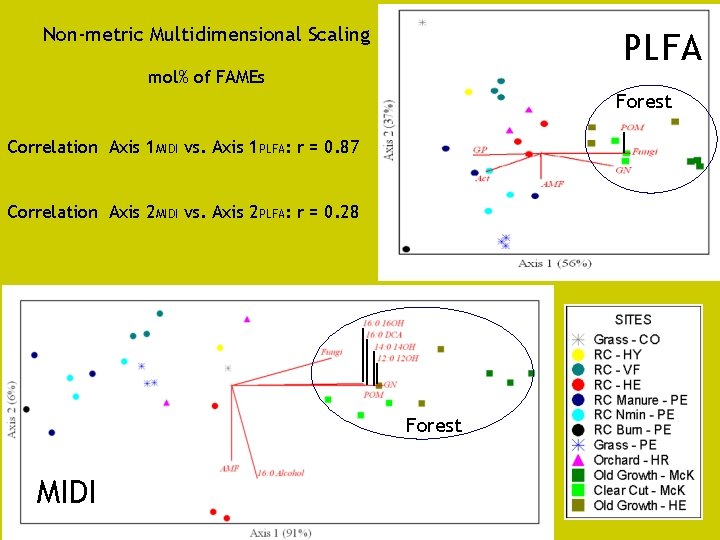
Non-metric Multidimensional Scaling PLFA mol% of FAMEs Forest Correlation Axis 1 MIDI vs. Axis 1 PLFA: r = 0. 87 Correlation Axis 2 MIDI vs. Axis 2 PLFA: r = 0. 28 MIDI Forest MIDI

EL-FAME versus PLFA • Mesmo método de produção de FAMEs (metanólise alcalina branda) • Diferentes reservatórios de lipídios alvos de produção de FAMEs PLFA vs. PLFA + NLFA + GLFA

EL-FAME versus PLFA Objetivo: Avaliar a interferência de NL e GL no que se refere à comparação da interpretação de dados de comunidade microbiana entre o EL-FAME e o PLFA (padrão) Amostras de solo: Idem estudo de comparação entre PLFA vs. MIDI Análises estatísticas: Modelos de regrassão múltipla (stepwise) Ordenação das amostras com base na relação entre EL/PL com respeito às concentrações molares dos FAMEs (mol%) nos respectivos extratos

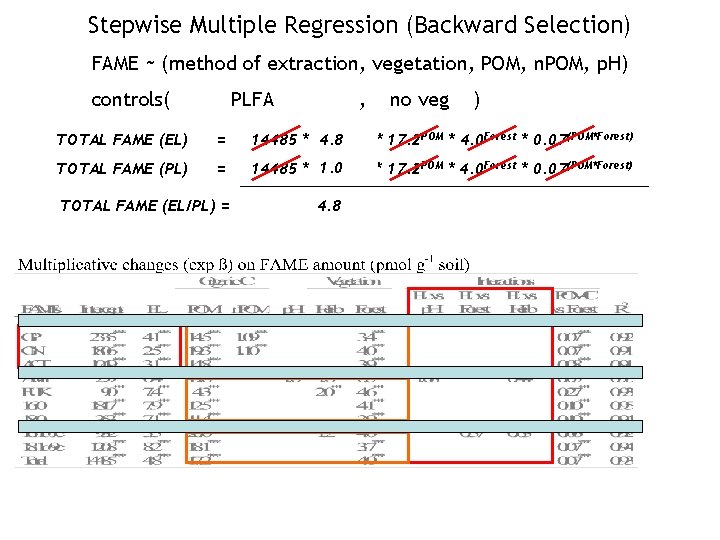
Stepwise Multiple Regression (Backward Selection) FAME ~ (method of extraction, vegetation, POM, n. POM, p. H) controls( PLFA , no veg ) TOTAL FAME (EL) = 14485 * 4. 8(EL=1) * 17. 2 POM * 4. 0 Forest * 0. 07(POM*Forest) TOTAL FAME (PL) = 1. 0(EL=0) * 17. 2 POM * 4. 0 Forest * 0. 07(POM*Forest) 14485 * 4. 8 TOTAL FAME (EL/PL) = 4. 8

Stepwise Multiple Regression (Backward Selection) FAME ~ (lipid source, vegetation, POM, n. POM, p. H) Vegetation: non-vegetation at sampling (control), herbaceous, and forest Lipid source: PLFA (control), NLFA or GLFA Multiplicative changes (exp ß) on FAME amount (pmol g-1 soil) associated with lipid sources (neutral lipids vs. phospholipids; and glycolipids vs. phospholipids

NMS with EL-FAME: PLFA mol% ratios EL-FAME (mol%) 15: 0 i 18: 2 6 c … 20: 4 6 c CO 0. 05 0. 26 0. 20 PMa 0. 09 0. 21 0. 23 Forest No vegetation … OGc 0. 01 0. 34 0. 12 PLFA (mol%) 15: 0 i 18: 2 6 c CO 0. 12 0. 15 0. 11 PMa 0. 16 0. 12 0. 16 OGc 0. 06 0. 22 ELFA/PLFA 15: 0 i 18: 2 6 c CO 0. 41 1. 73 1. 82 PMa 0. 56 1. 75 1. 44 0. 17 1. 53 0. 55 … 20: 4 6 c … OGc Herbaceous

Outros Lipídios Importantes • Ergosterol (esterol): – exclusivo de fungos (biomassa de fungos) – altamente correlacionado com PLFA 18: 2 6 c • Poli-hidroxialcanoatos (PHAs) – reservas em bactérias – em SPE-Si é eluído com acetona

Outros Usos dos Métodos Baseados em Lipídios na Investigação da Microbiota • Diversidade e estrutura da comunidade microbiana • Biomassa microbiana – Total – Grupos microbianos específicos • Estado nutricional de fungos do solo • Respostas de bactérias a estresses ambientais

Biomassa Microbiana Viável Método 1. Soma dos PLFAs BM total: soma de todos os PLFAs 3, 0 x 104 células/pmol PLFA (bactéria) 1, 2 x 104 células/pmol PLFA (algas) BM grupo-específica: soma de PLFAs do grupo Dados quantitativos obtidos na análise de PLFA Método 2. Quantificação do P na fase orgânica Princípio: P na fase orgânica do extrato é derivado de fosfolipídios. Vantagem: simples, dispensa CG

Efeito da Substituição de Floresta por Agricultura (Trigo ~26 anos) sobre a BM

Método BM 1 (Soma dos PLFAs) Floresta vs. Agricultura (Trigo ~26 anos) Floresta Agricultura

Método BM 2. Quantificação do P na Fase Orgânica do Extrato de Solo • Protocolo: White et al. (1979) (resumo) 1. 2. 3. 4. 5. 6. 7. Extração de lipídios totais, por 2 h (Bligh e Dyer, 1959); Partição com Na. Cl 2 N; Recuperação da fase orgânica (inferior); Secagem sob N 2 ultrapuro; Digestão com ácido perclórico, 180 o. C (3 -4 h); Adicionar solução molibdênio (White et al. , 1979); Após 10 min, adicionar solução de ANSA (1 -amino-2 -naftol-4ácido sulfônico); Ferver por 10 min. em banho-maria; Ler absorvância a 830 nm. 8. 9.

Comparação com Outros Métodos de Deteminação da BM (Frostegard et al. , 1991) • P-lipídio vs. SIR (respiração induzida por substrato) SIR ( g CO 2/g solo) = 17, 6 + 0, 13 P-lipídio (nmol P/g solo) R 2 = 0, 86 • P-lipídio vs. conteúdo celular de ATP ( g ATP/g solo) = 0, 92 + 0, 0046 P-lipídio (nmol P/g solo) R 2 = 0, 89

Estado Nutricional de Fungos do Solo • Bååth, 2003 – Princípio: sob excesso de C e deficiência de N ou P, a comunidade fúngica não cresce, mas acumula lipídios. – Experimento e Resultados: • Glucose apenas: NL aumenta e PL permanece constante • Glucose + N + P: NL constante e PL aumenta – Bååth, E. Microbial Ecology, 45: 373 -383, 2003

Protocolo: Estado Nutricional de Fungos do Solo • Bååth et al. , 2003 • Idem procedimento para estrutura da comunidade, exceto: – – Não descartar a fração LN Fração de LN e PL são transesterificada Relação NL: PL do FAME 18: 2 6 c (fungo) Quanto maior a relação NL: PL maior é a deficiência nutricional (N ou P) da comunidade fúngica

Respostas de Bactérias a Estresses Ambientais • Sob estresses (dessecamento do meio e restrição nutricional) – Aumento da relação entre FAMEs cíclicos e precursores • 19: 0 cy / 18: 1 7 c ou 17: 0 cy /16: 1 7 c – Kieft et al. , 1994, AEM, 60: 3292 -3299, 1994 – Custo de manutenção para mitigar estresse: aumenta gasto de energia, menor eficiência de conversão de carbono em biomassa microbiana: impacto na conservação de MOS.

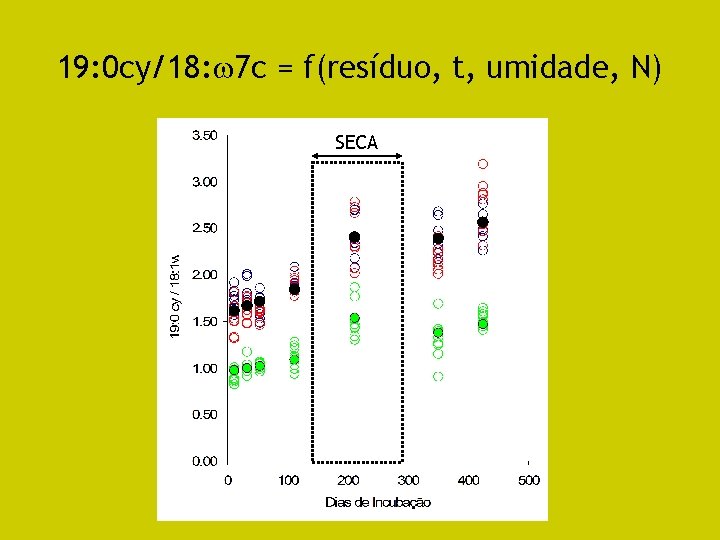
Experimento (Fernandes, 2007) • Incubação por 425 d, microcosmos, solo de Tabuleiros Costeiros, SE (Argissolo amarelo) • 3 resíduos x 2 N x 7 datas, 4 repetições – Resíduos: controle, palha de milho, casca de coco – Doses N: equivalente 150 kg N ha-1 – Datas: 12, 33, 54, 112, 212, 350 e 425 dias – 130 aos 280 d sob seca (-1, 5 MPa) • Variável resposta: 19: 0 cy/18: 1 7 c • Estatística: Regressão múltipla – stepwise, forward – Modelo inicial: grande média – Modelo cheio: todas as interações entre todos os fatores – F para incluir termos no modelo < 4, 0

Regressão Múltipla (stepwise forward) • Call: lm(formula = ST ~ MILHO + TIME + UMIDO + TIME: MILHO, data = STRESS. 19. INCUB, na. action = na. exclude) • • • Residuals: Min 1 Q Median 3 Q Max -0. 4682 -0. 1053 -0. 006328 0. 111 0. 6178 • • Coefficients: • • • Residual standard error: 0. 1823 on 163 degrees of freedom Multiple R-Squared: 0. 8908 F-statistic: 332. 3 on 4 and 163 df, the p-value is 0 (Intercept) MILHO TIME UMIDO TIME: MILHO Value Std. Error t value Pr(>|t|) 1. 9131 0. 0448 42. 7342 0. 0000 -0. 6297 0. 0451 -13. 9688 0. 0000 0. 0023 0. 0001 20. 2161 0. 0000 -0. 3261 0. 0404 -8. 0648 0. 0000 -0. 0011 0. 0002 -5. 6939 0. 0000

19: 0 cy/18: 7 c = f(resíduo, t, umidade, N) SECA

• FIM

Obrigado pela atenção Marcelo F. Fernandes marcelo@cpatc. embrapa. br 4009 1360