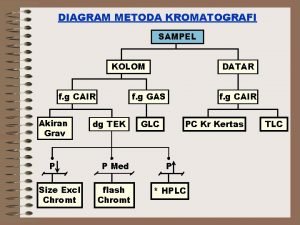
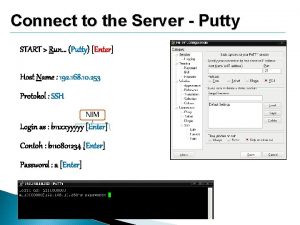
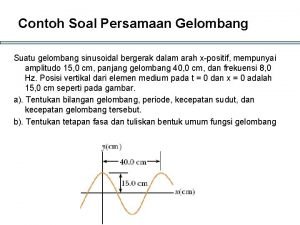
KROMATOGRAFI KOLOM SEDERHANA Any Kromatografi Kolom Sederhana Bergerak

KROMATOGRAFI KOLOM SEDERHANA Any

Kromatografi Kolom Sederhana Bergerak / aliran karena gaya grafitasi ↓ Pemilihan fase diam + fase gerak ↓ Kepolaran ↓ Pita-pita kromatogram ↓ Terbentuk fraksi-fraksi ↓ Dianalisis dengan KLT / KK↓

Pemisahan Secara Kromatografi Mikhail Tswett ↓ Pigmen tumbuhan ↓ Pita-pita
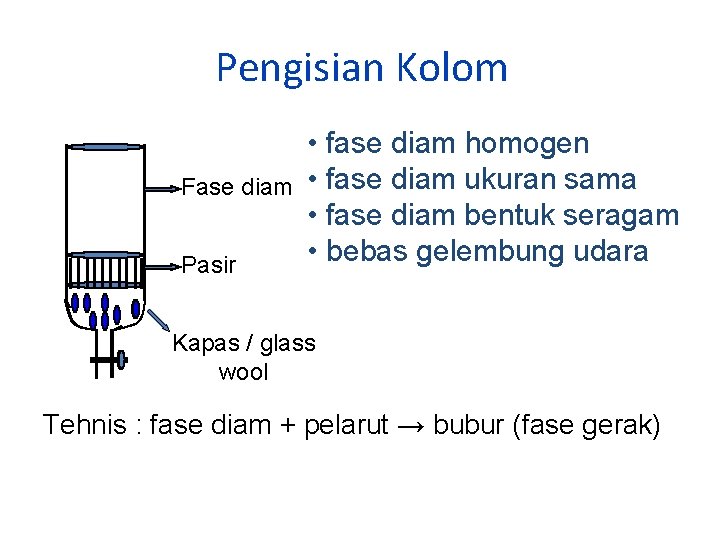
Pengisian Kolom Fase diam Pasir • fase diam homogen • fase diam ukuran sama • fase diam bentuk seragam • bebas gelembung udara Kapas / glass wool Tehnis : fase diam + pelarut → bubur (fase gerak)
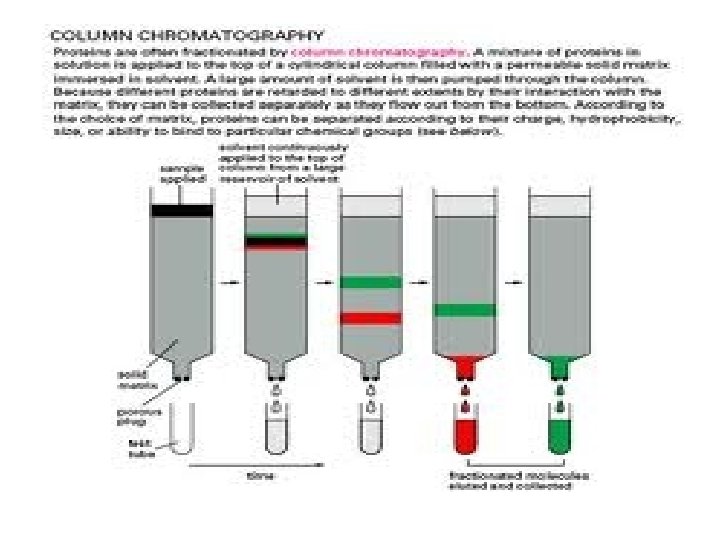

Kolom kromatografi sederhana (learning kolom)

Isolasi hasil fraksi dengan KLT Preparatif CHCl 3 : Me. OH : H 2 O = 6, 5 : 2, 5: 0, 4 Isolat yang diambil Profil KLT preparatif di bawah UV 254 nm fase diam silika dan fase gerak = kloroform: metanol: air = 6, 5: 2, 5: 0, 4
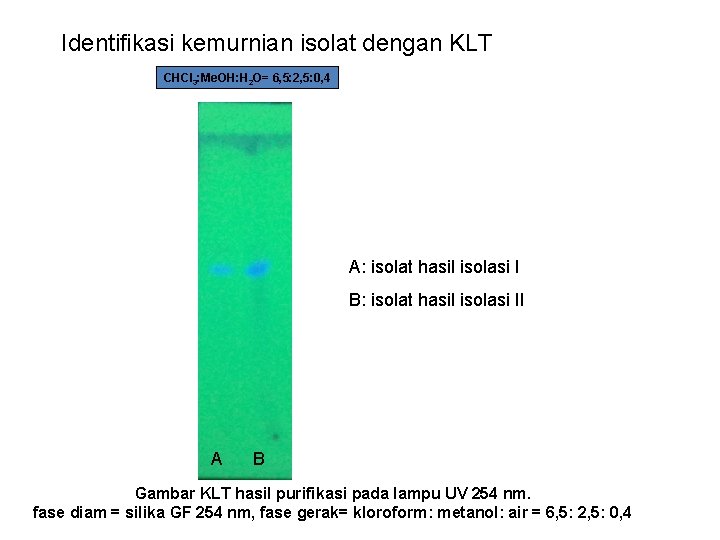
Identifikasi kemurnian isolat dengan KLT CHCl 3: Me. OH: H 2 O= 6, 5: 2, 5: 0, 4 A: isolat hasil isolasi I B: isolat hasil isolasi II A B Gambar KLT hasil purifikasi pada lampu UV 254 nm. fase diam = silika GF 254 nm, fase gerak= kloroform: metanol: air = 6, 5: 2, 5: 0, 4
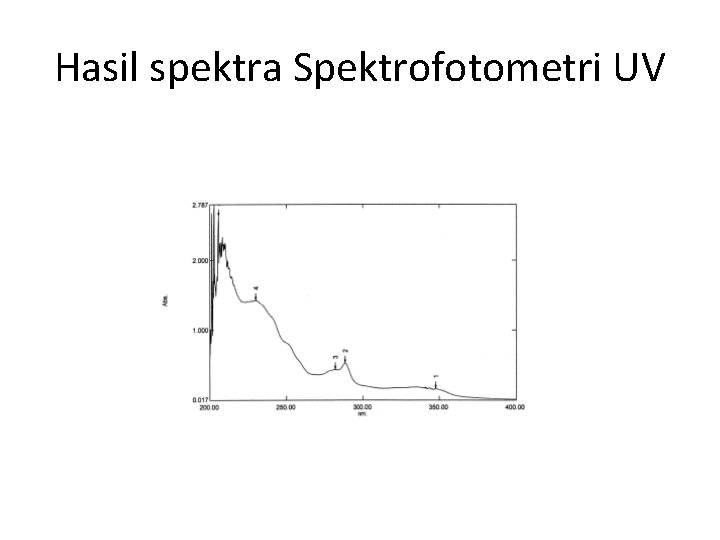
Hasil spektra Spektrofotometri UV

Hasil spektra Infra Red

Gambar. berbagai metode pemisahan • Contoh: 11
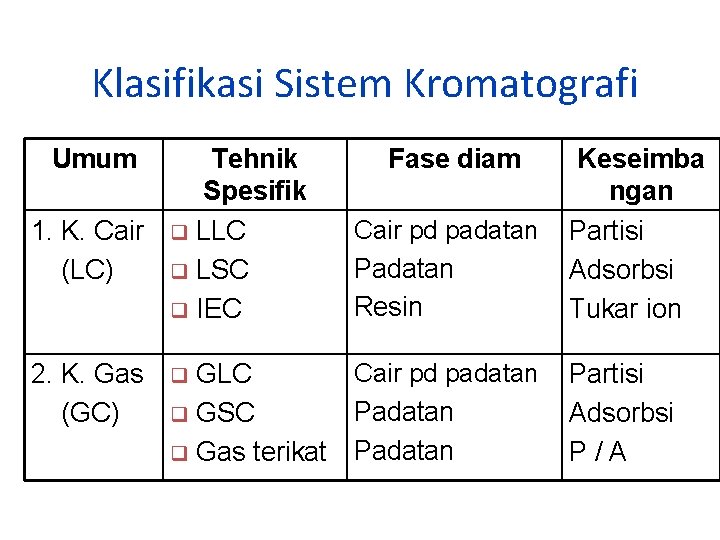
Klasifikasi Sistem Kromatografi Umum Tehnik Spesifik 1. K. Cair q LLC (LC) q LSC q IEC 2. K. Gas (GC) GLC q GSC q Gas terikat q Fase diam Cair pd padatan Padatan Resin Keseimba ngan Partisi Adsorbsi Tukar ion Cair pd padatan Padatan Partisi Adsorbsi P/A
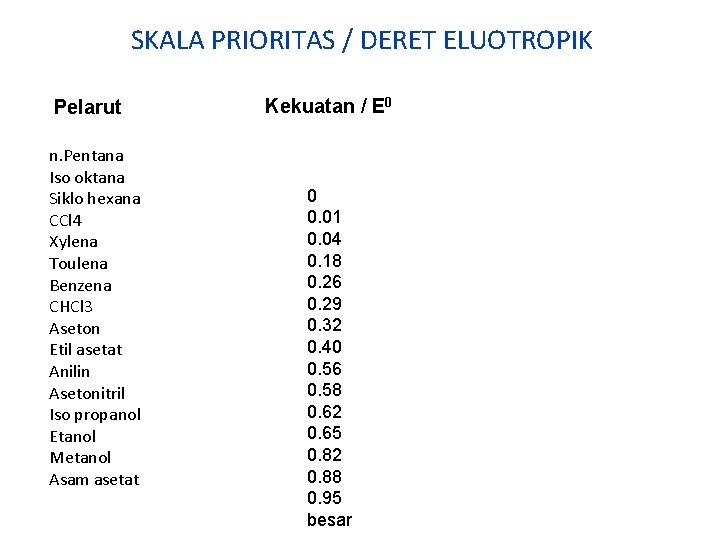
SKALA PRIORITAS / DERET ELUOTROPIK Pelarut n. Pentana Iso oktana Siklo hexana CCl 4 Xylena Toulena Benzena CHCl 3 Aseton Etil asetat Anilin Asetonitril Iso propanol Etanol Metanol Asam asetat Kekuatan / E 0 0 0. 01 0. 04 0. 18 0. 26 0. 29 0. 32 0. 40 0. 56 0. 58 0. 62 0. 65 0. 82 0. 88 0. 95 besar
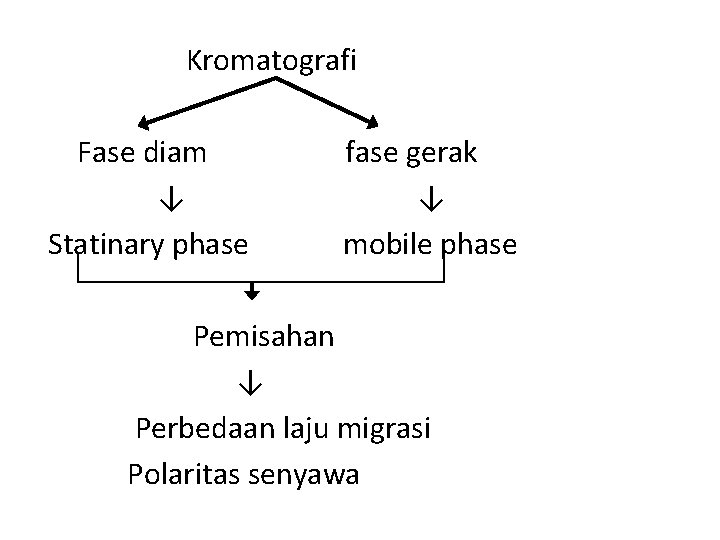
Kromatografi Fase diam ↓ Statinary phase fase gerak ↓ mobile phase Pemisahan ↓ Perbedaan laju migrasi Polaritas senyawa

Hukum Distribusi Kromatografi ↓ perbedaan distribusi komponen di dalam FG & FD ↓ koefisien distribusi / partisi (K) ↓ K = CS /CM CS : kons. Molar komponen dlm FD CM: kons. Molar komponen dlm FG
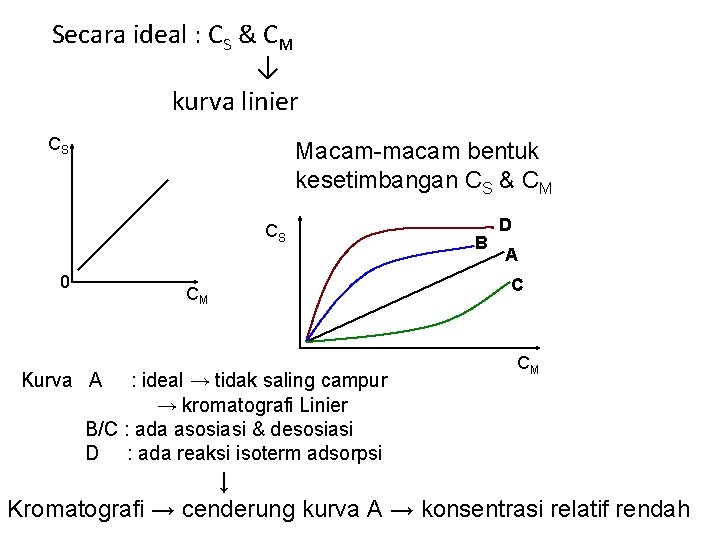
Secara ideal : CS & CM ↓ kurva linier CS Macam-macam bentuk kesetimbangan CS & CM CS 0 CM Kurva A : ideal → tidak saling campur → kromatografi Linier B/C : ada asosiasi & desosiasi D : ada reaksi isoterm adsorpsi B D A C CM ↓ Kromatografi → cenderung kurva A → konsentrasi relatif rendah

Elusi dalam kolom kromatografi Solvent E B+E E kolom Sp A+E E signal D t. R Elusi : proses terbawanya komponen dlm suatu camp, shg ada pemisahan komponen yg dibawa oleh FG dari ujung atas kolom → bawah t. R : waktu yg diperlukan oleh komponen untuk bermigrasi sepanjang kolom Vr : volume FG yg dibutuhkan untuk membawa komponen dari titik awal kolom → akhir kolom

F : laju alir FG yang menyatakan jumlah vol FG per satuan waktu ↓ F = V R / t. R t R = VR / F Dalam kolom yang ideal ↓ Komp. yang tidak teretensi ↓ t=0 ↓ Komp. di atas memerlukan waktu untuk bermigrasi → t. M : waktu FG melewati kolom VM : fraksi volum kolom yang dilalui komponen → t. R’ = t R – t M VR’ = V R – VM terkoreksi

Untuk menerangkan proses pemisahan dlm kromatografi ada 2 macam teori : 1. Teori Lempeng (Plate Theory) ↓ Martin & Synge (1941) ↓ Efisiensi kolom ↓ Apabila jumlah kesetimbangan makin besar → efisiensi >> → menambah jumlah lempeng (N) → tebal lempeng teoritik → H N & H → menyatakan efisiensi ↓ Secara matematis : N = L / H Kelemahan teori : tidak mampu mengidentifikasi variabel-variabel yang mempengaruhi pelebaran pita kromatogram

2. Teori Kinetik ( Kinetics Theory) Dapat mengatasi kelemahan teori Plate. → teori laju / rate theory ↓ Partikel komponen bermigrasi diantara FG & FD ↓ Migrasi sangat tidak teratur ↓ Energi thermal ↓ Gerakan partikelnya random ↓ Ditribusi simetrik Gauss

H. E. T. P H = 16 L x (Wb / t. R)2 N = 16 x (t. R / Wb)2 = (4 t. R/W)2 Simetrik Gauss → t (waktu) lama →puncak lebar

Menurut Van Deemter ↓ Ada 3 proses secara stimultan yg mempengaruhi variabilitas laju migrasi komponen diantara FG & FD : 1. 2. 3. Difusi Eddy (Eddy diffusion) Difusi longitudinal (longitudinal diffusion) Proses transfer massa ↓ Pada tebal lempeng teoritik (H) → merupakan fungsi linier variabilitas laju migrasi komponen ↓ Persamaan Van Deemter H = A + B /µ + C. µ A = koefisien Difusi Eddy B = koefisien Difusi longitudinal C = (CS + CM) = koefisien total

Difussi longitudinal ↓ Pelebaran pita ↓ Molekul komponen dlm FG → bermigrasi dari konsentrasi tinggi ke konsentrasi rendah ↓ Kontribusi variabilitas laju migrasi yg menurun secara hiperbolik terhadap kenaikan kecepatan linier FG (µ) ↓ Pada tebal lempeng teoritik HLD = 2ΨDM µ = B µ DM = koefisien difusi komponen FG Ψ = kualitas packing FD ↓ 0, 6

Pelebaran pita Transfer Massa ↓ Konstribusi H akan naik apabila kec. Linier FG naik ↓ Makin cepat kec. FG akan makin singkat proses transfer massa → pemisahan rendah • Pelebaran pita diffuse Eddy ↓ Akibat tidak homogen pori dalam packing kolom ↓ Ada yang jalannya pendek dan ada yang panjang
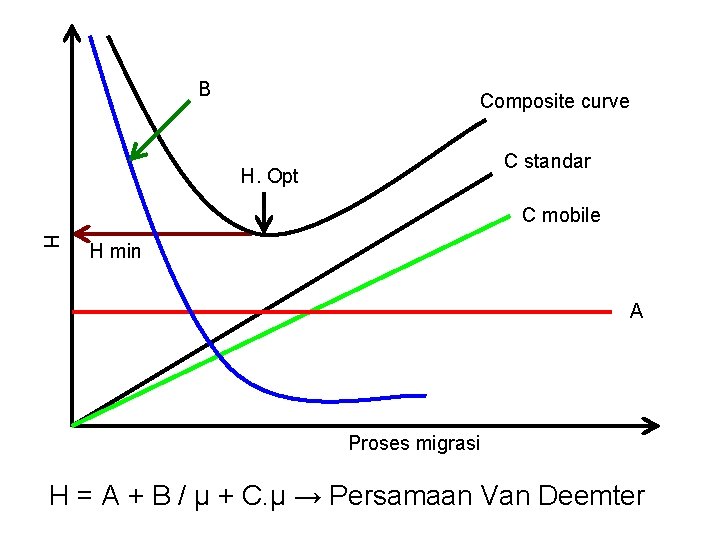
B Composite curve C standar H. Opt C mobile H H min A Proses migrasi H = A + B / µ + C. µ → Persamaan Van Deemter
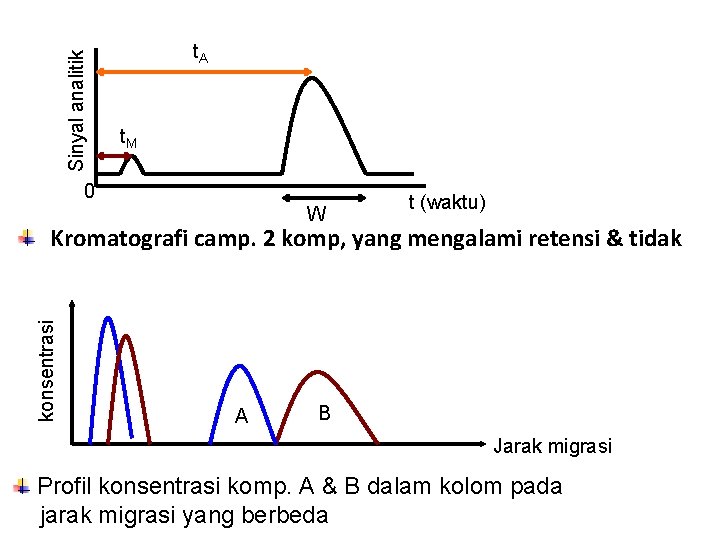
Sinyal analitik t. A t. M 0 W t (waktu) konsentrasi Kromatografi camp. 2 komp, yang mengalami retensi & tidak A B Jarak migrasi Profil konsentrasi komp. A & B dalam kolom pada jarak migrasi yang berbeda

VARIABEL TERMODINAMIKA PADA PEMISAHAN Mempengaruhi kualitas kolom 1. Waktu Retensi V= t. R t. M xµ Laju migrasi komponen 2. Faktor-faktor kapasitas kolom (k’) Ratio jumlah molekul komponen dalam FD terhadap jumlah molekul komponen dalam FG
![Lanjutan… n. S [ CS x V S ] k’ = = n. M Lanjutan… n. S [ CS x V S ] k’ = = n. M](http://slidetodoc.com/presentation_image_h/775ee30a4fd6b8941eb7a4992d919087/image-28.jpg)
Lanjutan… n. S [ CS x V S ] k’ = = n. M [ CM x V M ] VS k’ = xk VM k’ = ( t R – t M) t. M = t. R ’ t. M Pengalaman : k’ < 1 ↓ Tidak memisah Disarankan : k’ semakin besar ↓ Pemisahan ↑ ↓ k’ > 10 ↓ Tidak ekonomis

3. Faktor selektivitas (α) ↓ Ratio koef. Distribusi 2 komponen yang akan dipisahkan ↓ Menggambarkan kemampuan pemisahan suatu kolom ↓ α = KB / KA = koef. Distribusi komp. B / A Dimana : KB = koef. Distribusi komponen B yg teretensi kuat dalam kolom KA = koef. Distribusi komponen A yg teretensi lemah dalam kolom
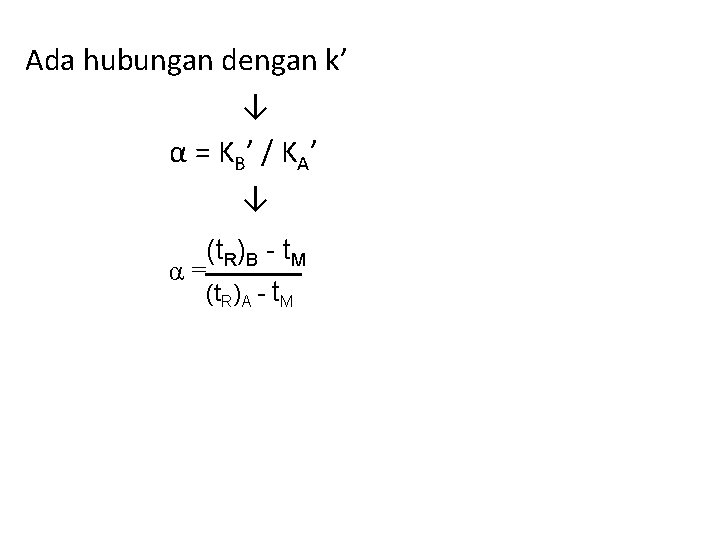
Ada hubungan dengan k’ ↓ α = K B ’ / K A’ ↓ (t. R)B - t. M α= (t. R)A - t. M

4. Resolusi Kolom (Rs) RS = ΔZ 0, 5 WA + 0, 5 WB = 2 ΔZ ( WA + W B ) 2 [ (t. R)B – (t. R)A ] WA + W B ΔZ = jarak puncak A & puncak B WA = lebar dasar kromatogram A WB = lebar dasar kromatogram B Disarankan RS ≥ 1, 5 ↓ Hubungan dengan faktor-faktor lain VN ( α – 1) k’B RS = x x α ( 1 + k’B ) 4


Sesungguhnya sedekah itu dapat menghilangkan murka Alloh & dapat menghilangkan kematian yang buruk (HR. at-Tirmidzi) 33

KROMATOGRAFI CAIR KINERJA TINGGI (KCKT) HIGH PERFORMANCE LIQUID CHROMATOGRAPHY (HPLC) Any Guntarti
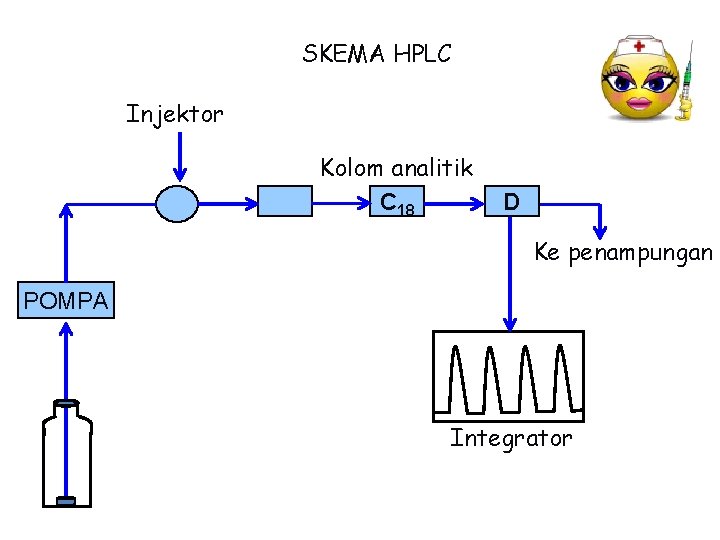
SKEMA HPLC Injektor Kolom analitik C 18 D Ke penampungan POMPA Integrator



Instrumen HPLC

1. Reservoir Fase Gerak ↓ Bisa lebih dari 1 ↓ dari gelas / stainless steel ↓ Daya tampung 1 - 2 L Dilengkapi degasser (menghilangkan gas terlarut) → gas NO 2 & O 2 → membuat gelembung-gelembung di dalam kolom & detektor ↓ - Pelebaran pita analit - Respon detektor terganggu

• Degassing → pompa vakum dihubungkan reservoir & diaduk / dipanaskan Solven disaring dengan kertas Millipore Pemisahan dengan 1 jenis FG dengan konsentrasi konstan → Elusi Isokratik Bila dengan 1 atau lebih FG yang polaritasnya berbeda → Elusi Gradien Digunakan FG segar → mendapatkan hasil yang reprodusibilitas optimum dalam pemisahan

2. Pompa Tekanan ≥ 1000 psi (4000 – 6000 psi) Kec. Alir 1 -3 ml/menit Bahan harus resisten secara kimiawi Ex : dari teflon & stainless steel Tidak ada pulsa getaran Kontinyu

3. Peredam Pulsa Fase Gerak Ada beberapa detektor sensitive terhadap variasi kec. Alir FG → ex : index refraksi, elektrokimia & konduktometer Peredam aliran dengan gas yang ditekan

4. Sistem Injeksi Sampel Menentukan presisi perhitungan → reprodusibilitas sampel Sampel dimasukkan dengan tekanan tinggi → merupakan pita dengan sampel tipis → pelebaran diperkecil Konvensional atau automatik

Injektor Automatik

5. Kolom Kromatografi Bentuk tabung, permukaan dalam rata Dari gelas / stainless steel Lapisan luar kadang dilapisi logam → menahan tekanan ad 6000 psi, rx kimia dari FG Sambungan kolom → tidak menyebabkan FG stagnant Panjang kolom (10 – 30) cm Analisis pemisahan cepat (3 – 8) cm Internal diameter (4 – 5)mm Partikel diameter (3 – 5) µm Guard kolom → sebelum kolom analitik

Kolom dari stainless steel
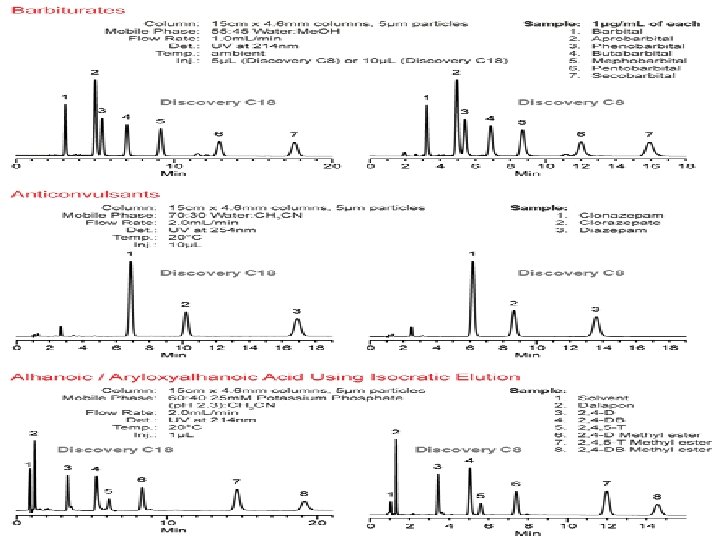

6. Detektor Pemilihan didasarkan pada problem pemisahan ↓ Harus sensitif (menghindari pelebaran) Ada 2 macam : 1. Berdasarkan sifat umum larutan Refraktif indeks → control temperatur Kurang sensitive

2. Berdasarkan sifat solut/analit/sampel UV – Vis Fluorescence Elektrokimia ↓ Sinyal analit yang berbeda dari FG ↓ Lebih sensitif (µg – ng) ↓ Dikembangkan dengan derivatisasi pre & post
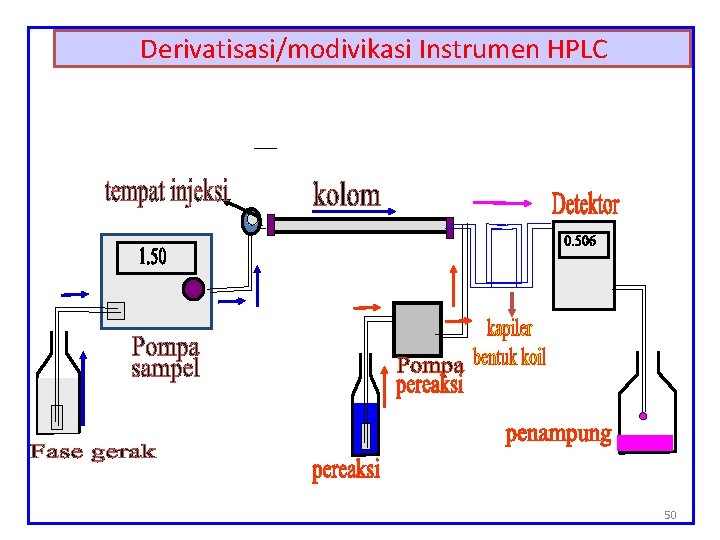
Derivatisasi/modivikasi Instrumen HPLC 50
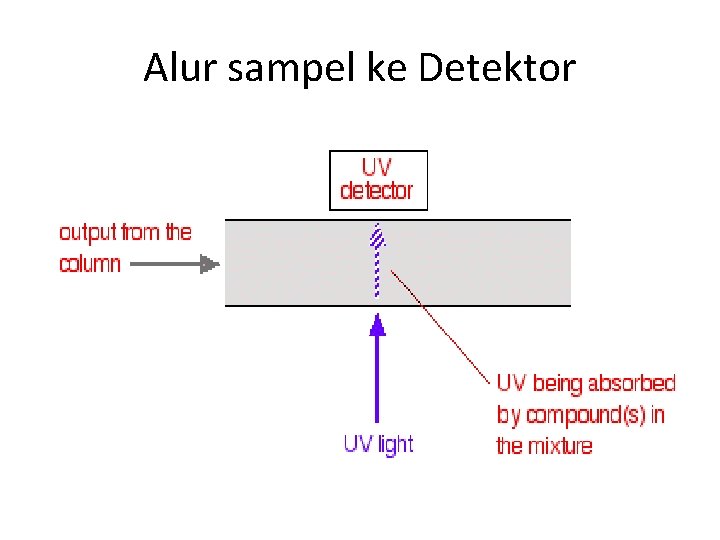
Alur sampel ke Detektor
7. Interpretasi output dari Detektor/integrator • Direkam berupa rangkaian puncak-puncak • Puncak untuk data kualitatif dan kuantitatif
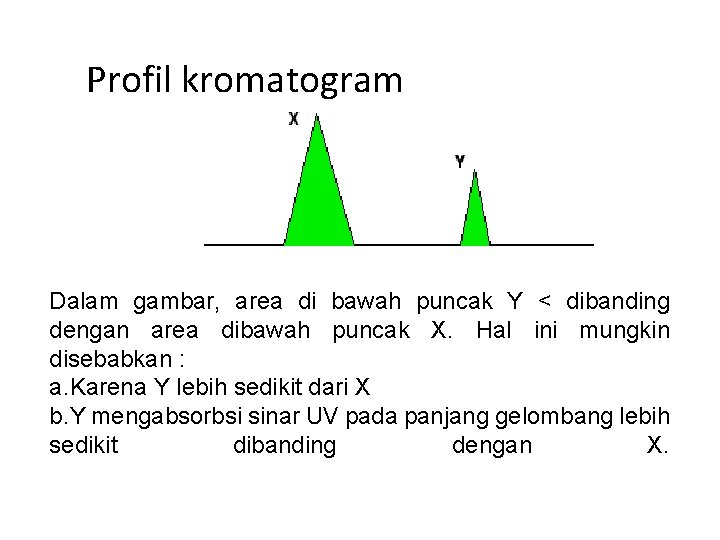
Profil kromatogram Dalam gambar, area di bawah puncak Y < dibanding dengan area dibawah puncak X. Hal ini mungkin disebabkan : a. Karena Y lebih sedikit dari X b. Y mengabsorbsi sinar UV pada panjang gelombang lebih sedikit dibanding dengan X.

Rangkaian HPLC pada spektrometer massa Pada saat detektor menunjukkan puncak, beberapa senyawa sementara melewati detektor dan pada waktu yang sama dapat dialihkan pada spektrometer massa. Pengalihan ini akan memberikan pola fragmentasi yang dapat dibandingkan pada data komputer dari senyawa yang polanya telah diketahui. Ini berarti bahwa identifikasi senyawa dalam jumlah besar dapat ditemukan tanpa harus mengetahui waktu retensinya.

Fase Normal HPLC • Kolom diisi dengan partikel silika yang sangat kecil dan pelarut non polar misalnya heksan. Sebuah kolom sederhana memiliki diameter internal 4. 6 mm panjang 150 sampai 250 mm. Senyawa-senyawa polar dalam campuran melalui kolom akan melekat lebih lama pada silika yang polar dibanding dengan senyawa-senyawa non polar. Oleh karena itu, senyawa yang non polar kemudian akan lebih cepat melewati kolom.

Fase Balik/Reverse Phase HPLC Silika dimodifikasi menjadi non polar berupa atom karbon 8 atau 18. Sebagai contoh, pelarut polar digunakan berupa campuran air dan alkohol seperti metanol. Senyawa-senyawa non polar dalam campuran akan bereaksi dengan gugus hidrokarbon karena adanya dispersi gaya van der Waals. Molekul-molekul polar akan bergerak lebih cepat melalui kolom. Fase balik HPLC adalah bentuk yang biasa digunakan dalam HPLC.


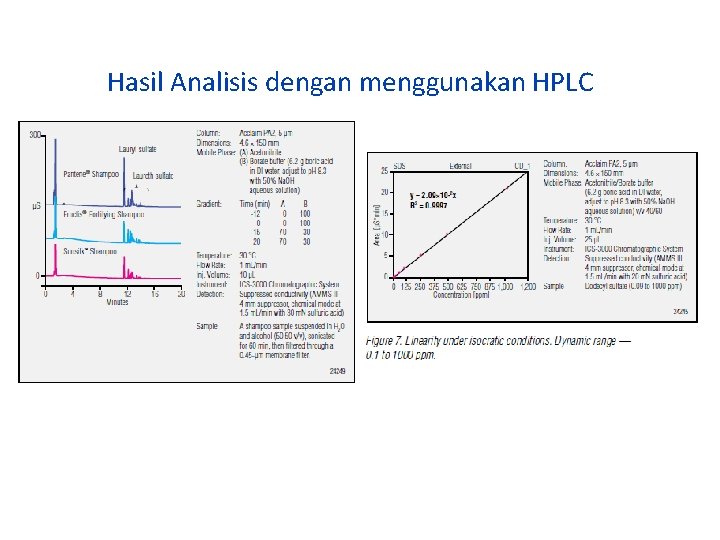
Hasil Analisis dengan menggunakan HPLC
- Slides: 60