Facolt di Medicina e Chirurgia Universit degli Studi




























































- Slides: 108

Facoltà di Medicina e Chirurgia, Università degli Studi di Verona Anno Accademico 2012 -13 Corso di Farmacologia “Chemioterapia ” Prof. Roberto Leone

CHEMIOTERAPIA Antimicrobici Ø ANTIBATTERICI o antibiotici (agiscono sui batteri) Ø ANTIFUNGINI o antimicotici (agiscono sui funghi) Ø ANTIVIRALI (agiscono sui virus) Ø ANTIPROTOZOARI (agiscono sui protozoi) Antiparassitar. I Ø ANTIELMINTICI (agiscono sugli elminti) Ø ANTITUMORALI (agiscono sulle cellule tumorali)

ANTIBIOTICO Sostanza prodotta da alcuni batteri e funghi che inibisce lo sviluppo di altri microrganismi (Gruppo di composti chimicamente eterogenei) CHEMIOTERAPICO Sostanza prodotta per sintesi chimica

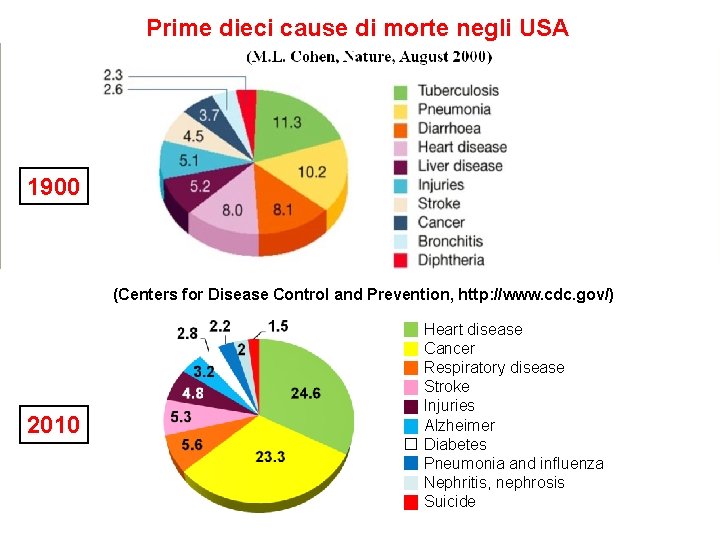
Prime dieci cause di morte negli USA 1900 (Centers for Disease Control and Prevention, http: //www. cdc. gov/) 2010 Heart disease Cancer Respiratory disease Stroke Injuries Alzheimer Diabetes Pneumonia and influenza Nephritis, nephrosis Suicide


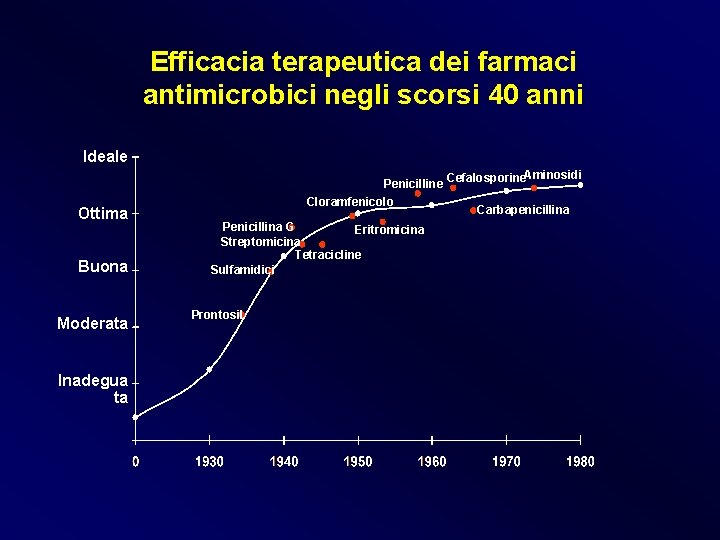
Efficacia terapeutica dei farmaci antimicrobici negli scorsi 40 anni Ideale Ottima Buona Moderata Inadegua ta Penicilline Cloramfenicolo Penicillina G Eritromicina Streptomicina Tetracicline Sulfamidici Prontosil Cefalosporine. Aminosidi Carbapenicillina

CHEMIOTERAPIA: DEFINIZIONI Tossicità Selettiva Proprietà del farmaco di agire selettivamente su strutture e funzioni tipiche della cellula batterica o tumorale

TOSSICITA’ SELETTIVA (alcuni esempi) 1. FATTORI BIOCHIMICI a. Esclusività del bersaglio a 1 Transpeptidasi della parete batterica PBP (penicillin binding proteins) a 2 Componente ergosterolica della membrana citoplasmatica fungina (betalattamine) (antifungini) b. Affinità selettiva Elevata affinità tra enzima e f. inibitore diidrofolatoreduttasi trimetoprim, (batteri) pirimetamina (plasmodi) metotressato (cellule tumorali) c. Attivazione o minore inattivazione c 1 Attivazione di flucitosina fluorouracile (miceti) c 2 Mancanza di idrolasi specifica nella cute e nel parenchima polmonare, che inattiva bleomicina

TOSSICITA’ SELETTIVA 2. FATTORI FARMACOCINETICI CLOROCHINA Maggiore concentrazione in emazie infette TETRACICLINE Diffusione passiva Trasporto attivo (specifico dei batteri) METOTREXATE Inibizione di 3 tappe metaboliche, quando MTX eccede nel citoplasma come anione libero 3. FATTORI CITOCINETICI SULFAMIDICI Batteri in fase di crescita ANTIBLASTICI Cellule proliferanti

CHEMIOTERAPIA: DEFINIZIONI Spettro d’azione Il complesso di specie batteriche contro le quali un antibatterico è attivo. Gli antibatterici vengono definiti ad ampio spettro, intermedio o ristretto a seconda del numero delle specie batteriche sulle quali agiscono.

Spettro d’azione di alcuni antibatterici

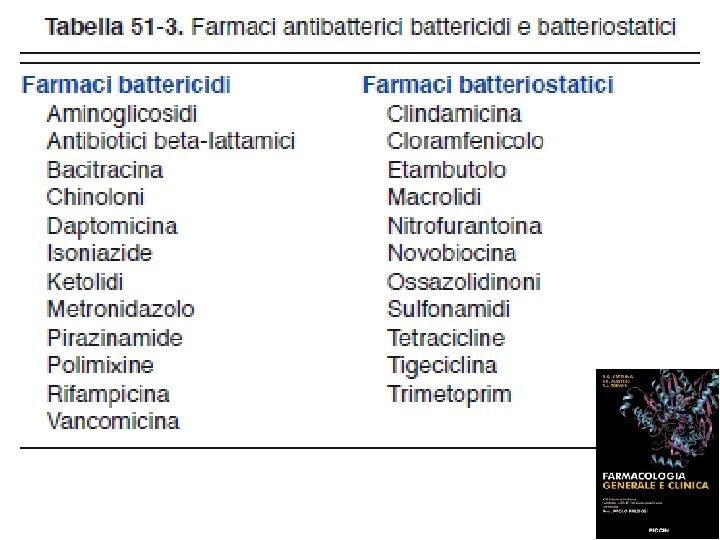
CHEMIOTERAPIA: DEFINIZIONI Battericidi Antibatterici che determinano la morte dei batteri. Esempi di farmaci battericidi: penicilline, cefalosporine, aminoglicosidi Batteriostatici Antibatterici che determinano l’arresto della moltiplicazione cellulare. Esempi di farmaci batteriostatici: tetracicline, cloramfenicolo

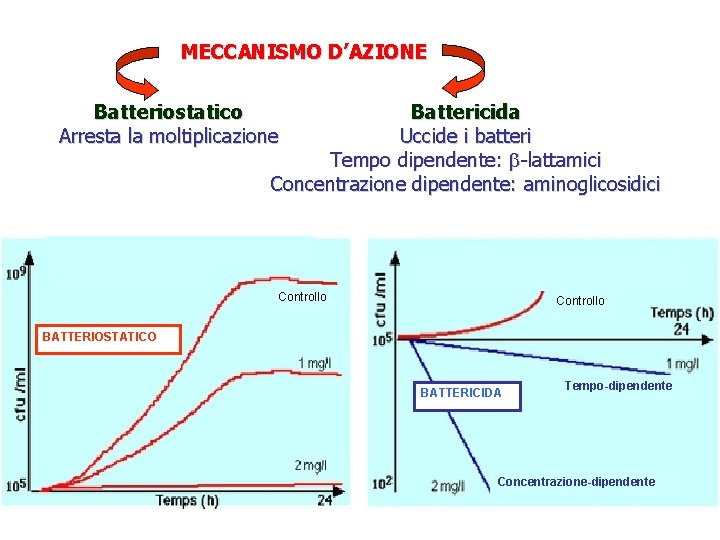
MECCANISMO D’AZIONE Battericida Uccide i batteri Tempo dipendente: -lattamici Concentrazione dipendente: aminoglicosidici Batteriostatico Arresta la moltiplicazione Controllo BATTERIOSTATICO BATTERICIDA Tempo-dipendente Concentrazione-dipendente


CHEMIOTERAPIA: DEFINIZIONI Farmaco di prima scelta Si intende l’antibatterico più indicato, per il suo profilo beneficio/rischio, per una determinata patologia infettiva. Non sempre può essere utilizzato (condizioni particolari del paziente, insorgenza di resistenza, ecc. ) e si utilizzano i farmaci alternativi (seconda o terza scelta).



CHEMIOTERAPIA: DEFINIZIONI Concentrazione Minima Inibitoria (MIC) La concentrazione (es. mcg/ml) di un antibatterico capace di inibire, in vitro, lo sviluppo batterico. MIC 50 = inibire in coltura il 50% dei batteri; MIC 90 = inibire in coltura il 90% dei batteri. La MIC di un antibatterico serve per saggiare la sensibilità di un ceppo batterico a quel determinato antibatterico. Antibiogramma Metodica microbiologica per saggiare contemporaneamente la sensibilità di un ceppo batterico a più antibatterici

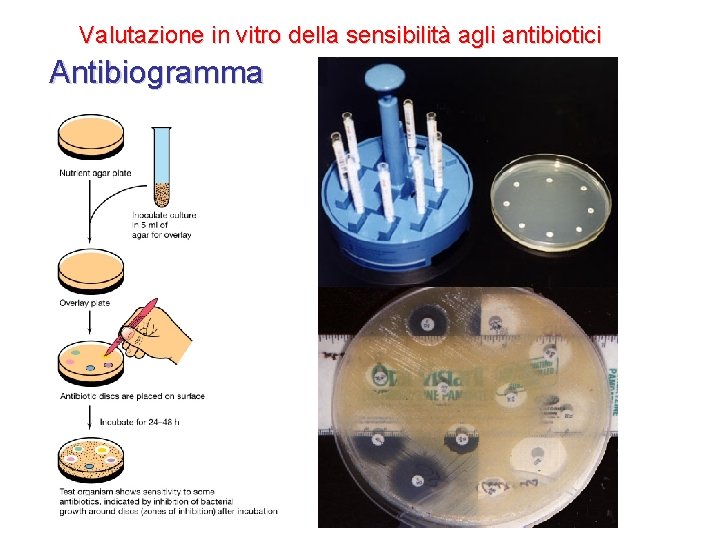
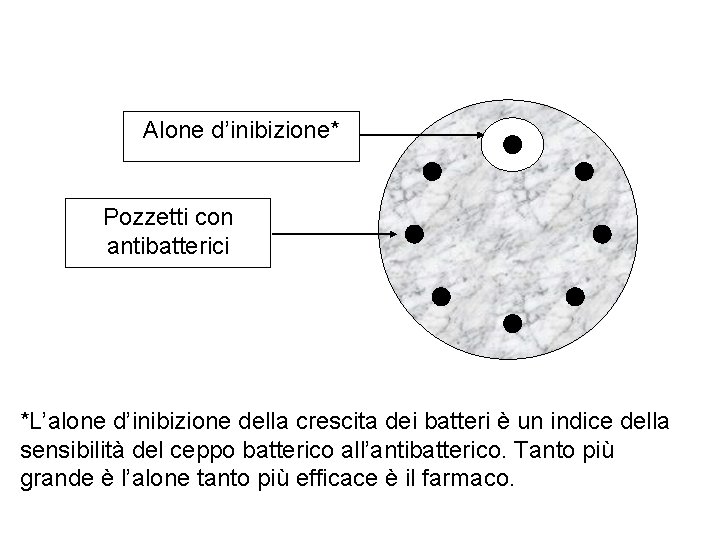
Valutazione in vitro della sensibilità agli antibiotici Antibiogramma

Alone d’inibizione* Pozzetti con antibatterici *L’alone d’inibizione della crescita dei batteri è un indice della sensibilità del ceppo batterico all’antibatterico. Tanto più grande è l’alone tanto più efficace è il farmaco.

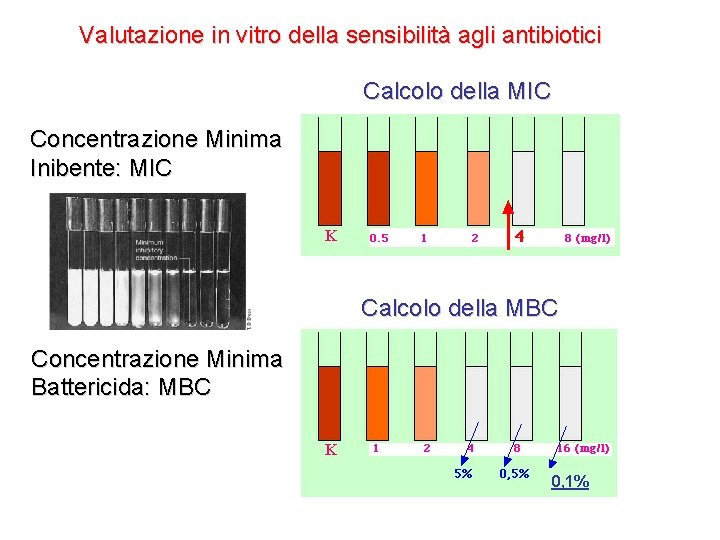
Valutazione in vitro della sensibilità agli antibiotici Calcolo della MIC Concentrazione Minima Inibente: MIC K Calcolo della MBC Concentrazione Minima Battericida: MBC K 0, 1%


RESISTENZA BATTERICA Con il termine di resistenza batterica si indica l’insensibilità di un ceppo batterico ad un determinato antibiotico. La resistenza può essere: Primaria Quando una specie batterica è da sempre insensibile ad un determinato antibiotico, nel senso quindi che non rientra nello spettro d’azione di quel antibiotico. Ad esempio lo Pseudomonas aeruginosa è insensibile all’azione dell’ampicillina.

RESISTENZA BATTERICA Acquisita Quando compaiono ceppi batterici (a seguito di variazioni genetiche) che, pur appartenendo a specie sensibili, non vengono distrutti o bloccati dall’azione di un antibiotico. Ad esempio comparsa di ceppi batterici di Neisseria gonorrhoeae resistenti alla penicillina G in quanto producono degli enzimi ( -lattamasi) in grado di inattivare il farmaco Gli antibatterici non sono causa di resistenza batterica ma hanno un ruolo come fattori di selezione, nel senso che favoriscono la diffusione dei batteri ad essi resistenti

Antibiotico resistenza acquisita Cromosomica Costituisce il 10 -15% di tutte le resistenze acquisite Si verifica per mutazione genetica spontanea L’antibiotico seleziona i ceppi resistenti Gli stessi mutanti possono essere resistenti ad altri antibiotici con caratteristiche simili Si trasmette verticalmente alla discendenza Può essere multi-step o one-step Extra-cromosomica (plasmidica) Costituisce il 90% di tutte le resistenze (alta frequenza di insorgenza) Si origina per acquisizione di informazione genetica che deriva da altri microrganismi e che penetra nella cellula mediante lo scambio di geni presenti su plasmidi o trasposoni (trasmissione orizzontale) con meccanismi di coniugazione, trasformazione e trasduzione Riguarda più antibiotici contemporaneamente (resistenza multipla) Può essere trasferita anche a microrganismi appartenenti a specie differenti


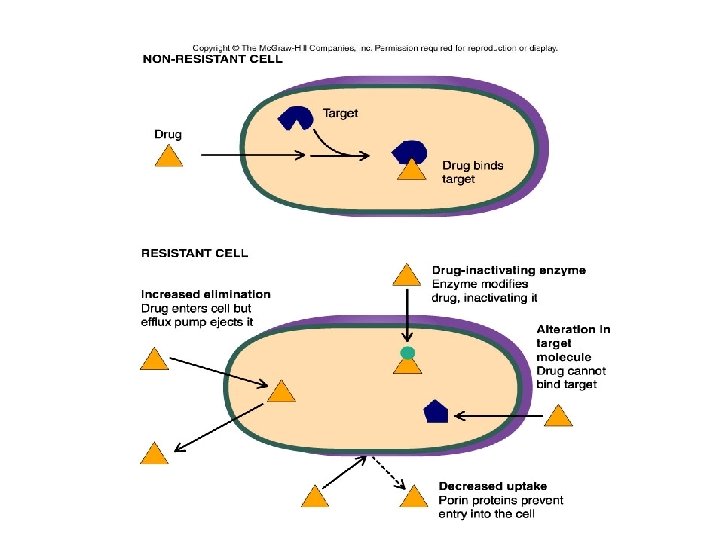
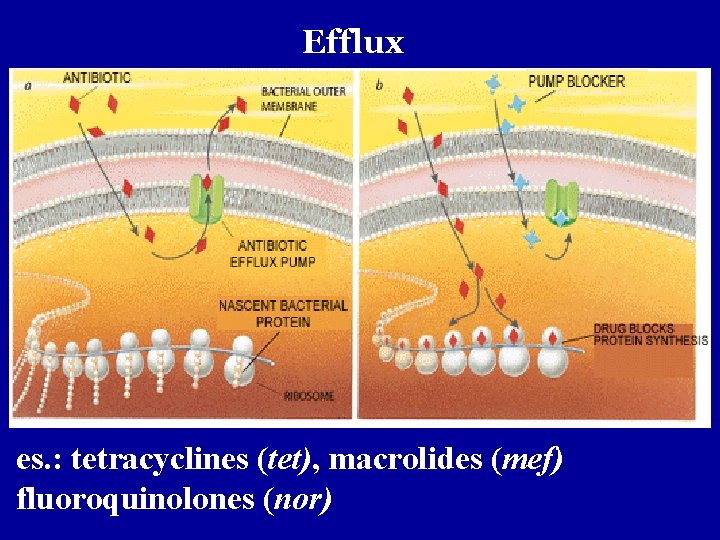
PRINCIPALI MECCANISMI DI RESISTENZA Ø Produzione di enzimi che degradano il farmaco (es. lattamasi che degradano le penicilline) Ø Alterato trasporto intracellulare (es. nei confronti di aminoglicosidi, tetracicline) Ø Alterazione della struttura batterica (es. nei confronti di eritromicina, rifamicine) Ø Bypass del blocco metabolico (es. nei confronti dei sulfamidici) Ø Presenza di pompe di efflusso (es. in G+ presenza ATP Binding Cassette o Motor Facilitator Superfamily : in G- Multidrug and Toxic compound Extrusion)

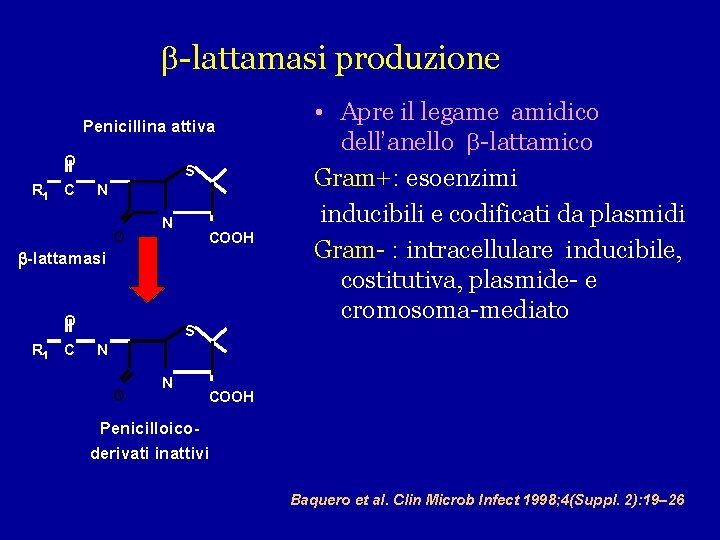
-lattamasi produzione Penicillina attiva O R 1 C S N O N COOH -lattamasi O R 1 C S • Apre il legame amidico dell’anello -lattamico Gram+: esoenzimi inducibili e codificati da plasmidi Gram- : intracellulare inducibile, costitutiva, plasmide- e cromosoma-mediato N O N COOH Penicilloicoderivati inattivi Baquero et al. Clin Microb Infect 1998; 4(Suppl. 2): 19– 26

Efflux es. : tetracyclines (tet), macrolides (mef) fluoroquinolones (nor)

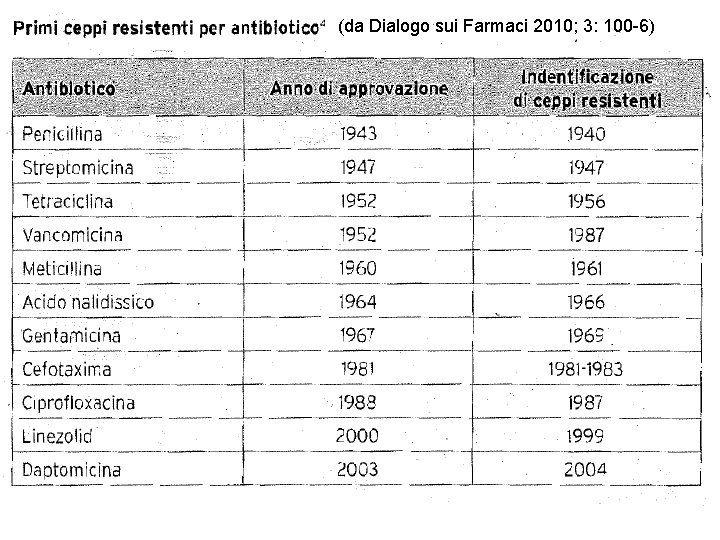
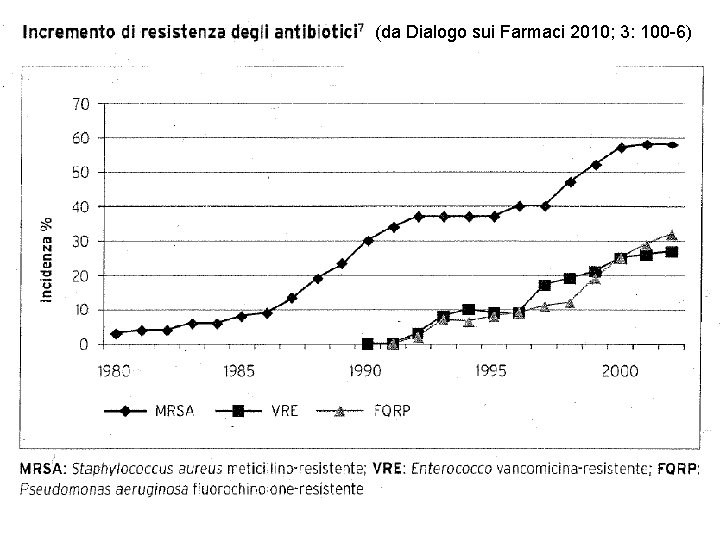
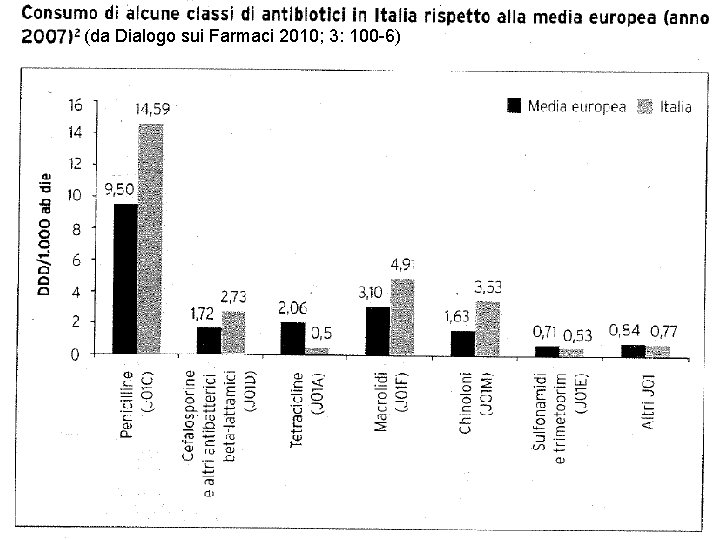
(da Dialogo sui Farmaci 2010; 3: 100 -6)



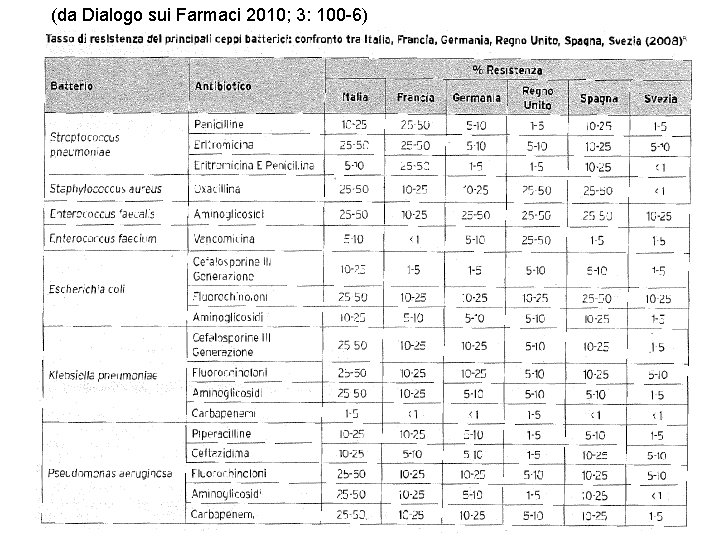
(da Dialogo sui Farmaci 2010; 3: 100 -6)

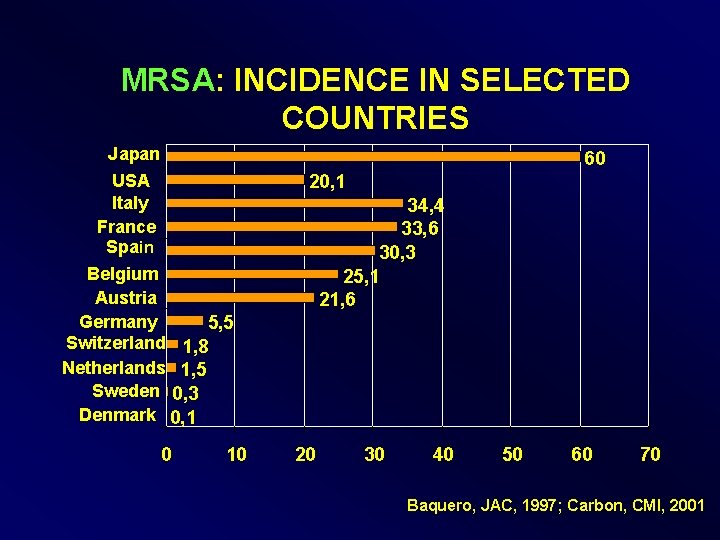
MRSA: INCIDENCE IN SELECTED COUNTRIES Japan USA Italy France Spain Belgium Austria Germany 5, 5 Switzerland 1, 8 Netherlands 1, 5 Sweden 0, 3 Denmark 0, 1 0 10 60 20, 1 34, 4 33, 6 30, 3 25, 1 21, 6 20 30 40 50 60 70 Baquero, JAC, 1997; Carbon, CMI, 2001


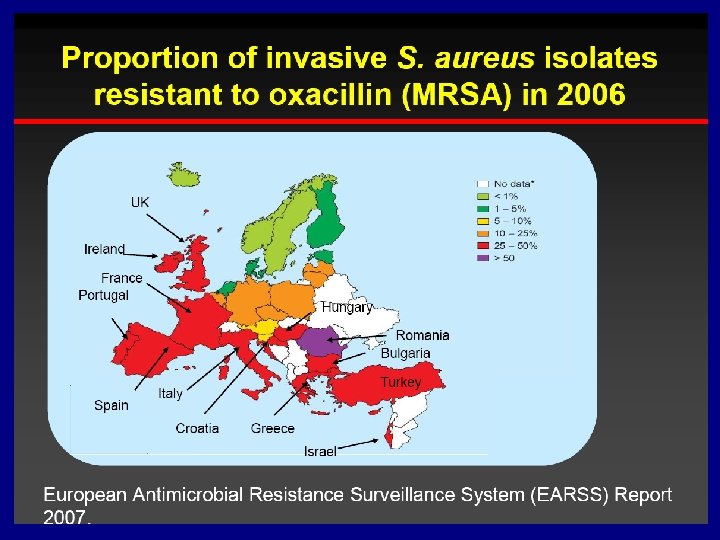
EMA, 2009

Slowing the emergence and spread of antimicrobial resistance 1. Responsibilities of Physicians: must work to identify microbe and prescribe suitable antimicrobials, must educate patients 2. Responsibilities of Patients: need to carefully follow instructions


Slowing the emergence and spread of antimicrobial resistance 3. Educate Public: must understand appropriateness and limitations of antibiotics ; antibiotics not effective against viruses 4. Global Impacts: organism that is resistant can quickly travel to another country - in some countries antibiotics available on non-prescription basis - antibiotics fed to animals can select for drug- resistant organisms


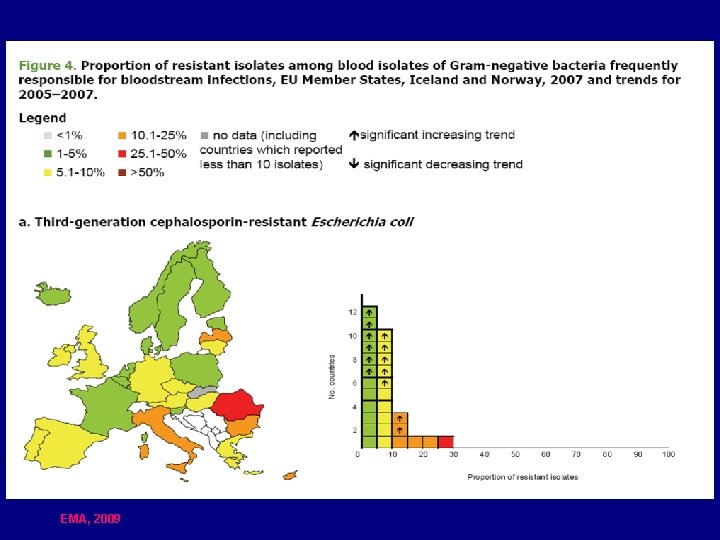
EMA, 2009

OTTIMIZZAZIONE DELL'USO DI ANTIBIOTICI PER RIDURRE LE RESISTENZE v STABILIRE MODALITÀ D'USO DI ANTIBIOTICI v CORRELARE LA RESISTENZA CON L'USO DI ANTIBIOTICI v CAMBIARE GLI SCHEMI D'USO

STRATEGIE PER PREVENIRE O RIDURRE LE RESISTENZE ü Sorveglianza dell’andamento di colonizzazione ü Monitoraggio di compliance delle misure di prevenzione e controllo ü Monitoraggio uso antibiotici ü Linee Guida per uso e profilassi con antibiotici ü Riduzione uso antibiotici ampio spettro ü Riduzione costi ü Sorveglianza rispetto Linee Guida ü Educazione personale e prescrittori

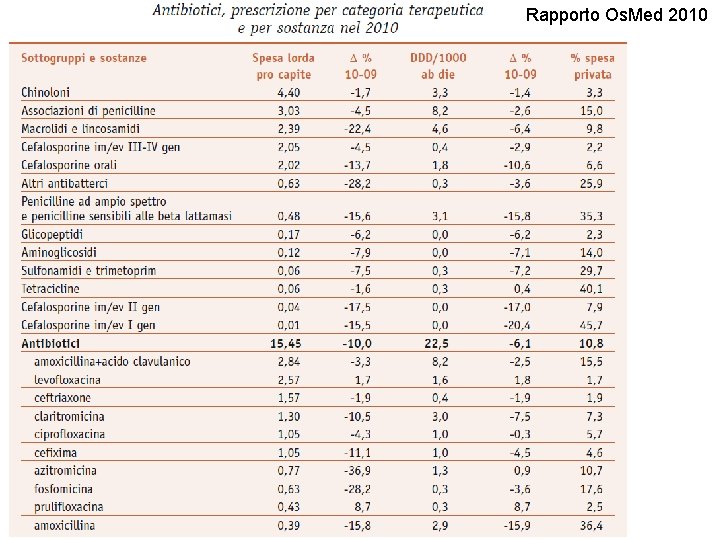
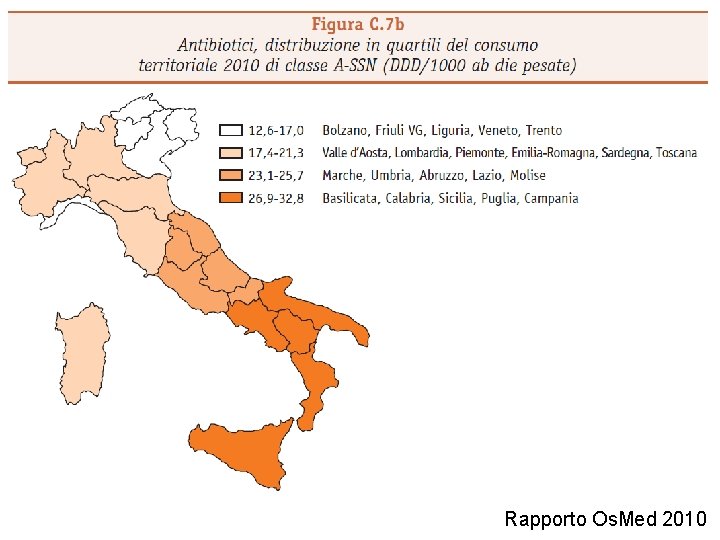
Rapporto Os. Med 2010

Rapporto Os. Med 2010

(da Dialogo sui Farmaci 2010; 3: 100 -6)

(da Dialogo sui Farmaci 2010; 3: 100 -6)

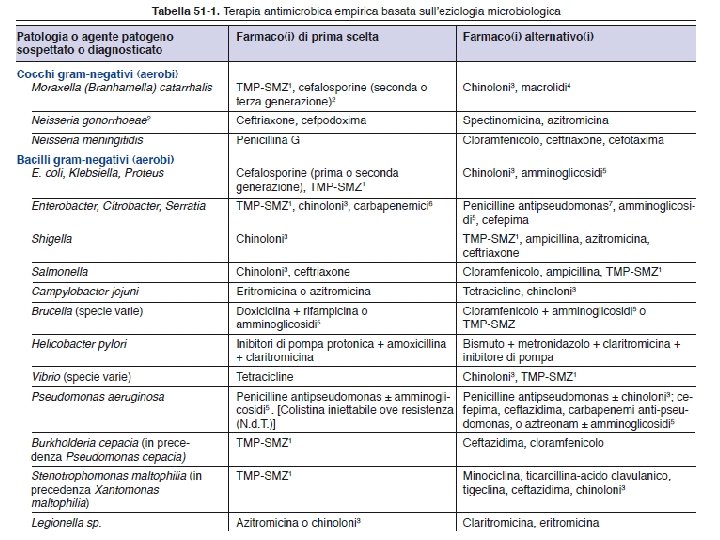
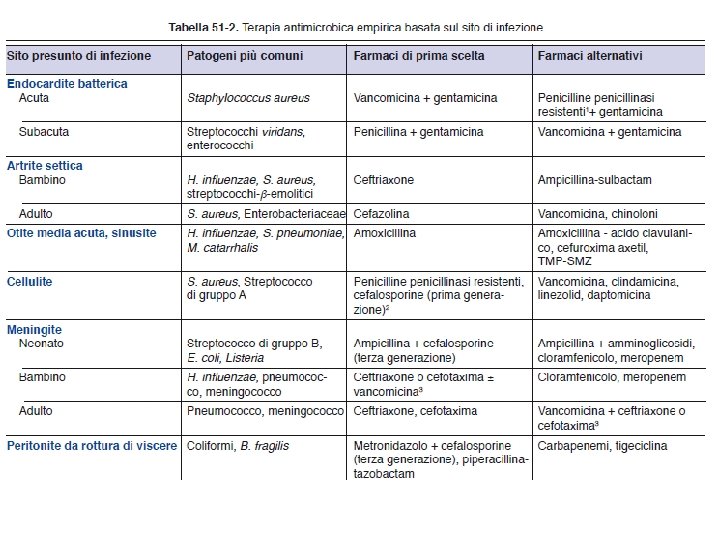
UNA TERAPIA ANTIBATTERICA VA INSTAURATA IN BASE A: Ø Tipo di batteri responsabili dell’infezione (epidemiologia, test microbiologici) Ø Sede dell’infezione Ø Gravità dell’infezione

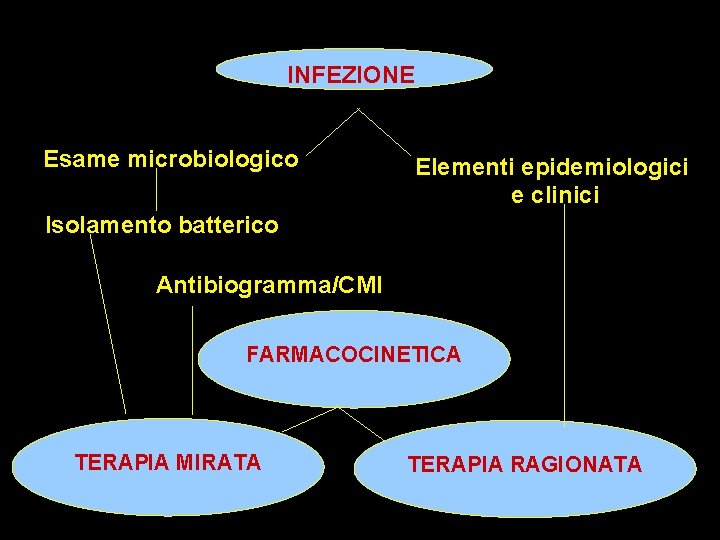
INFEZIONE Esame microbiologico Elementi epidemiologici e clinici Isolamento batterico Antibiogramma/CMI FARMACOCINETICA TERAPIA MIRATA TERAPIA RAGIONATA

LA SCELTA DELL’ANTIBATTERICO SI BASA SU: Ø Efficacia del farmaco (spettro d’azione) anche in relazione a possibile resistenza Ø Caratteristiche farmacocinetiche Ø Profilo tossicologico Ø Caratteristiche del paziente Ø Costo

CRITERI DI SCELTA DI UN CHEMIOTERAPICO MICRORGANISMO FARMACO OSPITE ATTIVITA’ ANTIBATTERICA PROFILO FARMACOCINETICO CARATTERISTICHE DEL PAZIENTE Spettro d’azione Distribuzione Età Gram-positivi, Gram-negativi, Anaerobi, Emivita Peso corporeo Protoplasmi, Forme L, Protozoi Vie di eliminazione Funzionalità renale ed epatica Insufficienza renale Allergie Meccanismo d’azione e tipo d’azione Margine terapeutico Immunodeficienza Battericida, batteriostatico Legame sieroproteico Gravidanza Malattie metaboliche Resistenze batteriche TOSSICITA’ Ipertensione Betalattamsi, transferasi, impermeabilità Renale Scompenso cardiaco Della membrana, fattore R, ecc. Epatica Gastroenterica SEDE D’INFEZIONE A carico dell’VIII nervo cranico SNC, vie urinarie, vie biliari, ecc. A carico del midollo osseo Allergie COSTO

FATTORI CONDIZIONANTI L’EFFICACIA DI UN ANTIBATTERICO Ø Suscettibilità batterica (resistenza primaria) Ø Resistenza batterica (resistenza acquisita) Ø Meccanismo d’azione e cinetica del farmaco Ø Caratteristiche dell’ospite (età, immunodepressione, altre patologie concomitanti, ecc. ) Ø Caratteristiche dell’infezione (sede, gravità, ecc. ) Ø Corretto impiego del farmaco

POSSIBILI CAUSE DI FALLIMENTO DI UNA TERAPIA ANTIBATTERICA Ø Diagnosi errata Ø Batterio resistente Ø Scelta erronea del farmaco (ad es. farmaco che non raggiunge la sede dell’infezione in concentrazioni adeguate) Ø Fattori inerenti il paziente (es. presenza di ascessi, corpo estraneo, immunodepressione, ostruzione) Ø Modalità d’impiego del farmaco errate (dosi, tempi, via di somministrazione, durata terapia) Ø Non compliance da parte del paziente Ø Superinfezione

CONCETTO-GUIDA PER LA SCELTA RAZIONALE DI UN CHEMIO-ANTIBIOTICO ü Il farmaco di scelta è quello dotato di azione specifica sull'agente patogeno ü e deve trovarsi nella sede d'azione - nel momento giusto - in concentrazione adeguata - per un tempo sufficientemente lungo

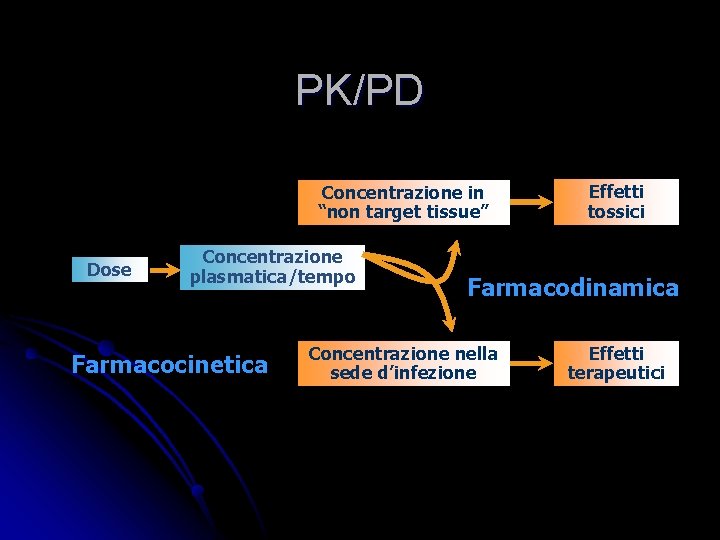
PK/PD Concentrazione in “non target tissue” Dose Concentrazione plasmatica/tempo Farmacocinetica Effetti tossici Farmacodinamica Concentrazione nella sede d’infezione Effetti terapeutici

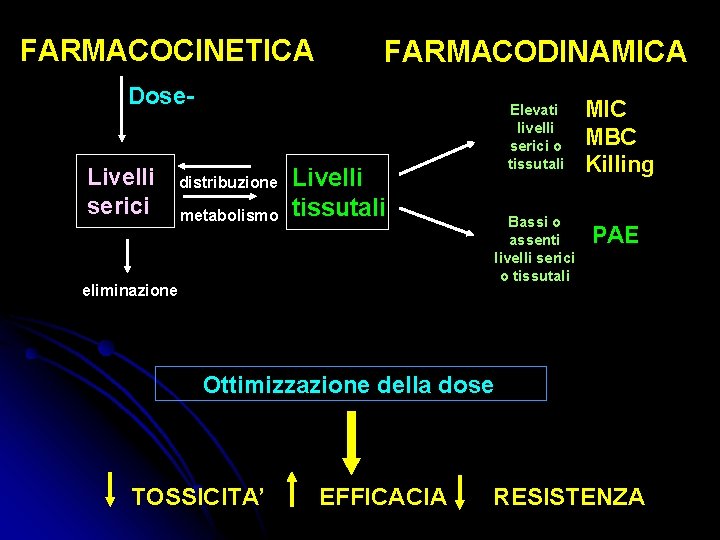
FARMACOCINETICA FARMACODINAMICA Dose- Elevati livelli serici o tissutali assorbimento Livelli serici distribuzione metabolismo Livelli tissutali eliminazione PK Bassi o assenti livelli serici o tissutali MIC MBC Killing PAE PD CORRELAZIONE (T>MIC AUC/MIC Cmax/MIC) Ottimizzazione della dose TOSSICITA’ EFFICACIA RESISTENZA




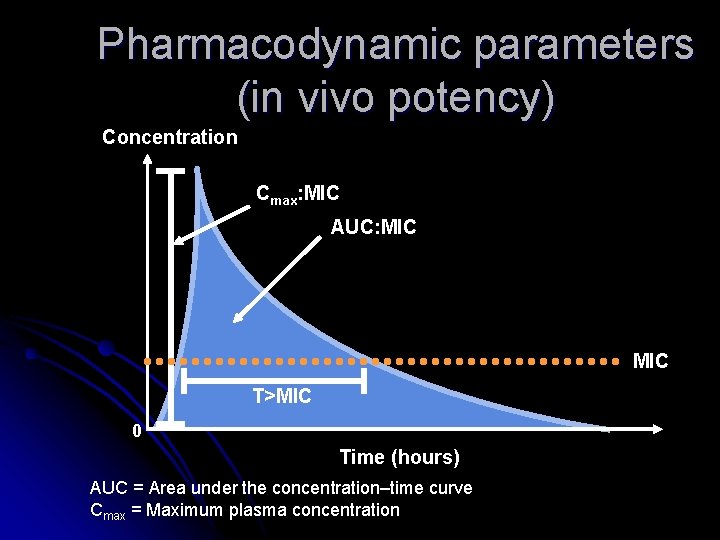
Pharmacodynamic parameters (in vivo potency) Concentration Cmax: MIC AUC: MIC T>MIC 0 Time (hours) AUC = Area under the concentration–time curve Cmax = Maximum plasma concentration

FARMACI ANTIMICROBICI l ATTIVITA’ TEMPO DIPENDENTE BETALATTAMINE l CARBAPENEMI l GLICOPEPTIDI l LINCOSAMIDI l MACROLIDI Naturali l l ATTIVITA’ CONCENTRAZIONE DIPENDENTE AMINOGLICOSIDI l FLUOROCHINOLONI l METRONIDAZOLO l EBM 10 -11

Antimicrobial drugs PK/PD parameters predictive of therapeutic outcome Parameter correlating with efficacy Cmax/MIC AUC/MIC T > MIC Examples Aminoglycosides Fluoroquinolones New macrolides Daptomycin Quinup. /Dalfoprist. Carbapenems Cephalosporins Penicillins Natural macrolides Tigecycline Linezolid Organism kill Concentrationdependent Time-dependent Therapeutic goal Maximize exposure Optimize duration of exposure Nicolau DP, J Infect Chemother, 2003, mod.

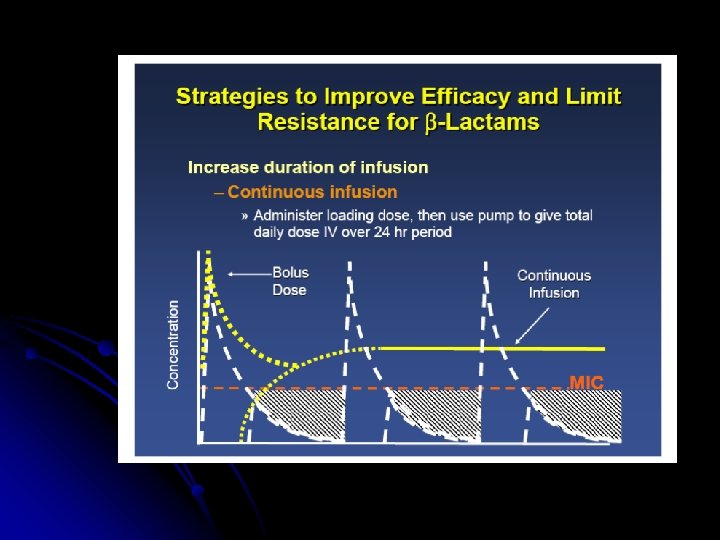
REGIME POSOLOGICO OTTIMALE MODALITA’ DI SOMMINISTRAZIONE CONTINUA (T>MIC) Tempo dipendenti - Betalattamine - Eritromicina ALTE DOSI E LUNGA INTERMITTENZA concentrazione / dipendenti - Aminoglicosidi - Fluorochinoloni - Macrolidi sintetici EBM 07 -08


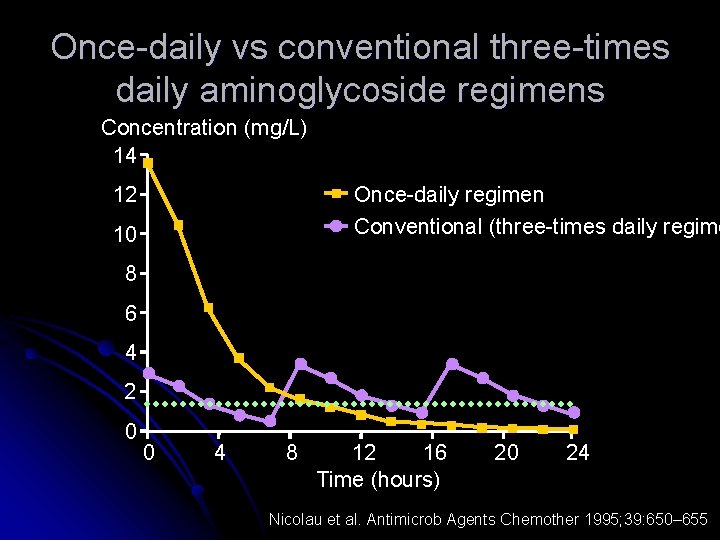
Once-daily vs conventional three-times daily aminoglycoside regimens Concentration (mg/L) 14 Once-daily regimen Conventional (three-times daily regime 12 10 8 6 4 2 0 0 4 8 12 16 Time (hours) 20 24 Nicolau et al. Antimicrob Agents Chemother 1995; 39: 650– 655


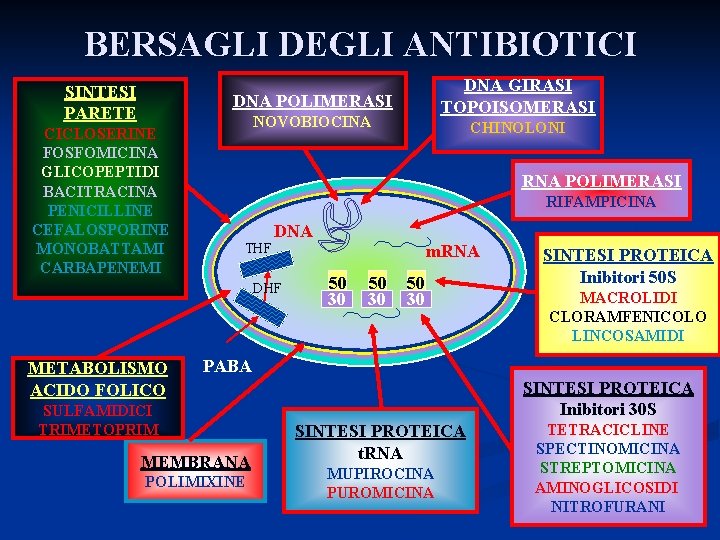
BERSAGLI DEGLI ANTIBIOTICI SINTESI PARETE DNA GIRASI TOPOISOMERASI DNA POLIMERASI CICLOSERINE FOSFOMICINA GLICOPEPTIDI BACITRACINA PENICILLINE CEFALOSPORINE MONOBATTAMI CARBAPENEMI NOVOBIOCINA RNA POLIMERASI RIFAMPICINA THF DNA DHF METABOLISMO ACIDO FOLICO CHINOLONI m. RNA 50 30 SINTESI PROTEICA Inibitori 50 S MACROLIDI CLORAMFENICOLO LINCOSAMIDI PABA SULFAMIDICI TRIMETOPRIM MEMBRANA POLIMIXINE SINTESI PROTEICA Inibitori 30 S SINTESI PROTEICA t. RNA MUPIROCINA PUROMICINA TETRACICLINE SPECTINOMICINA STREPTOMICINA AMINOGLICOSIDI NITROFURANI

PRINCIPALI MECCANISMI D’AZIONE DEI FARMACI ANTIINFETTIVI Ø Inibizione della sintesi della parete batterica § Antibiotici beta-lattamici (penicilline, cefalosporine, carbapenemi, monobattami) § Vancomicina, teicoplanina, daptomicina Ø Alterazione della membrana cellulare § Antifungini azolici (fluconazolo, itraconazolo, voriconazolo, posaconazolo) § Amfotericina B, flucitosina (antifungini)

PRINCIPALI MECCANISMI D’AZIONE DEI FARMACI ANTIINFETTIVI Ø Inibizione della sintesi proteica § § § Macrolidi Tetracicline Cloramfenicolo Clindamicina, lincomicina Aminoglicosidi Ø Azione a livello del DNA § § Nitrofurantoina Metronidazolo Acyclovir, ganciclovir, foscarnet (antivirali) Chinoloni

PRINCIPALI MECCANISMI D’AZIONE DEI FARMACI ANTIINFETTIVI Ø Blocco di tappe metaboliche essenziali per il batterio § Sulfamidici § Trimetoprim

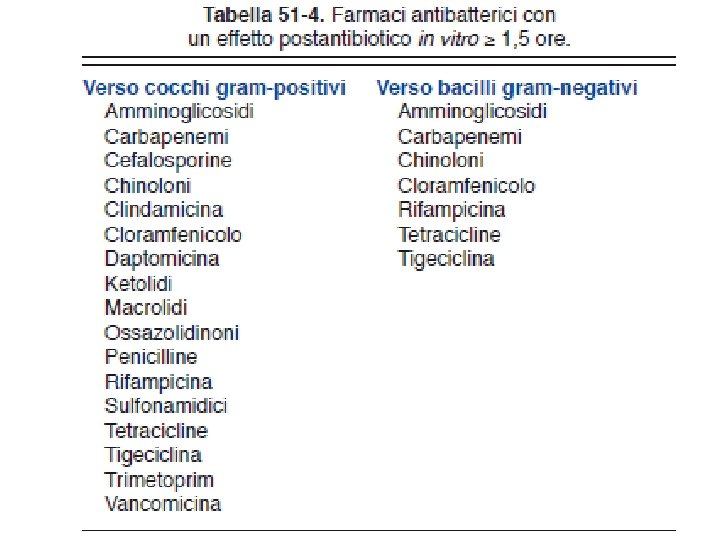
Post-antibiotic effect (PAE) THE PERSISTENT SUPPRESSION OF BACTERIAL GROWTH FOLLOWING EXPOSURE TO AN ANTIMICROBIAL AGENT Bigger J. M. 1944; Parker R. F. 1948, Eagle H. 1949 PAE is demonstrated in vitro by osserving bacterial growth kinetics after antibiotic removal. PAE has also been demonstrated in vivo in a variety of animal infection models.


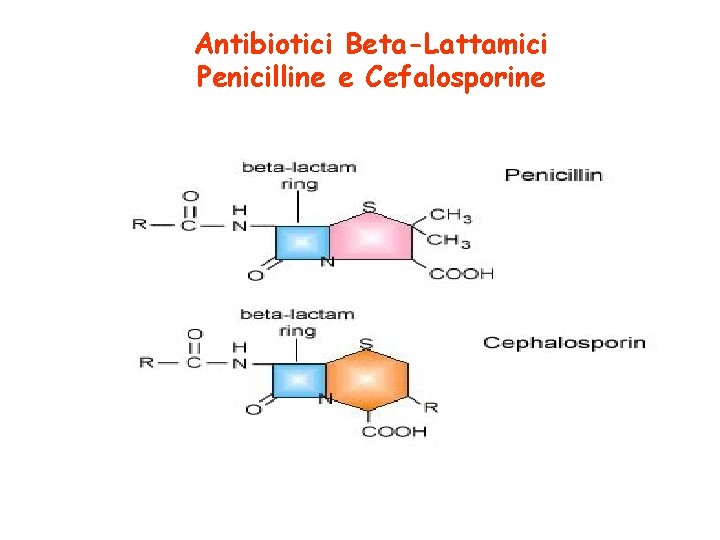
ANTIBATTERICI -LATTAMICI Con questa denominazione si raggruppano le seguenti classi di antibatterici: Ø Penicilline (scoperta da Fleming nel 1928 e sviluppata da Florey e Chan 10 anni dopo) Ø Cefalosporine Ø Carbapenemi Ø Monobattami

Antibiotici Beta-Lattamici Penicilline e Cefalosporine

Caratteristiche comuni dei beta-lattamici Ø Struttura chimica con presenza anello beta-lattamico Ø Meccanismo d’azione (inibizione sintesi parete cellulare) Ø Attività battericida Ø Allergia crociata Ø Farmacocinetica rapida Meccanismi di resistenza ai beta-lattamici Ø Produzione di enzimi (beta-lattamasi) che inattivano il farmaco Ø Modificazioni delle proteine batteriche legano il farmaco

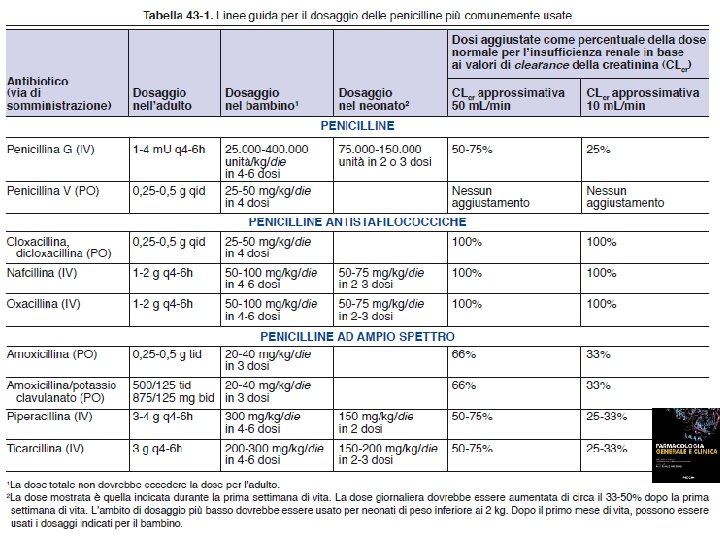
SUDDIVISIONE, IN BASE ALLO SPETTRO D’AZIONE, DELLE PRINCIPALI PENICILLINE Gruppo I: Penicillina G (spettro d’azione ristretto cocchi G+, via parenterale) Benzilpenicillina potassica (generico) Benzilpenicillina benzatinica (generico) Inattivata dalle beta-lattamasi batteriche è ancora efficace per infezioni sostenute da streptococchi (inclusi pneumococchi), gonococchi e meningococchi, tuttavia emergono sempre di più ceppi resistenti. Da tempo non è più farmaco di scelta per la meningite pneumococcica. La penicillina ritardo (benzatinica) è una formulazione deposito a lento assorbimento particolarmente utile nella terapia della sifilide (Treponema pallidum), si utilizza anche pe la profilassi della febbre reumatica; va somministrate esclusivamente per via i. m.

SUDDIVISIONE, IN BASE ALLO SPETTRO D’AZIONE, DELLE PRINCIPALI PENICILLINE Gruppo II: Penicilline ad attività antistafilococcica (resistenti alle beta-lattamasi stafilococciche) Oxacillina (Penstapho®, im - ev) Flucloxacillina (Flucef®, Pantaflux®, ecc. , os - im - ev) L’unica indicazione per il loro uso sono le infezioni causate da stafilococchi resistenti alla penicillina G. Problema rilevante è l’insorgenza in Ospedale di ceppi di S. aureus meticillino resistenti (MRSA) che rendono inefficace il loro uso

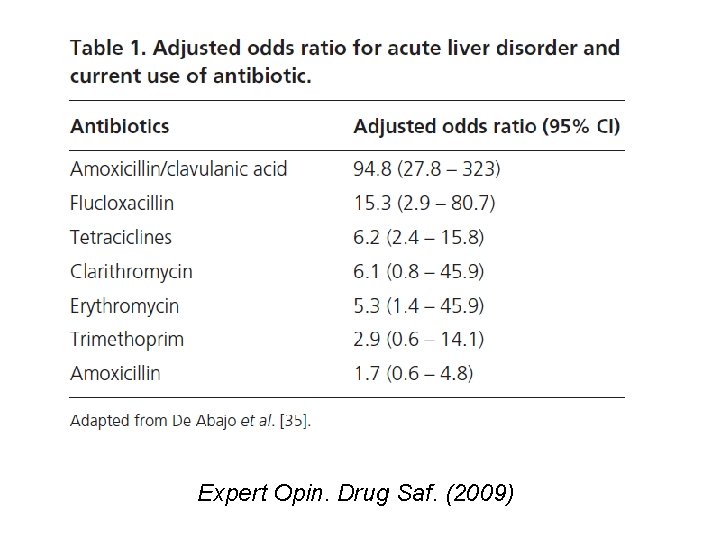
SUDDIVISIONE, IN BASE ALLO SPETTRO D’AZIONE, DELLE PRINCIPALI PENICILLINE Gruppo III: Aminopenicilline (spettro d’azione ampio cocchi G+ e G-) Ampicillina (generico, Amplital®, os - im - ev) Amoxicillina (generico, Velamox®, Zimox®, ecc. , os - iniettabile) Bacampicillina (generico, Bacasint®, ecc. , os) Sono inattivate dalle beta-lattamasi. Molti stafilococchi, ceppi di E. coli e ceppi di H. influenzae sono pertanto resistenti. Non dovrebbero essere utilizzate nei pazienti ospedalizzati senza aver effettuato dei test di sensibilità. Poiché sono sensibili alle -lattamasi si trovano anche in associazione con gli inibitori delle -lattamasi: Ampicillina+Sulbactam (generico, Unasyn®, Loricin®, Bethacil®) Amoxicillina+Ac. clavulanico (generico, Augmentin®, ecc. )

Expert Opin. Drug Saf. (2009)

SUDDIVISIONE, IN BASE ALLO SPETTRO D’AZIONE, DELLE PRINCIPALI PENICILLINE Gruppo IV: Ureidopenicilline (ampio spettro espanso verso P. aeruginosa, via parenterale) Mezlocillina (Baypen®) Piperacillina (generico, Farecillin®, ecc. ) In associazione con inibitori beta-lattamasi Piperacillina + tazobactam (generico, Tazocin®, ecc. , iniettabile) La piperacillina è la più attiva verso lo P. aeruginosa, l’aggiunta del tazobactam la rende efficace anche verso i ceppi resistenti alle ureidopenicilline; il suo spettro d’attività è comparabile a quello dei carbapenemi. Si ricorda che nelle setticemie da Pseudomonas (in particolare se presente neutropenia o endocardite) queste penicilline dovrebbero essere somministrate in associazione con aminoglicosidi.


PRINCIPALI REAZIONI AVVERSE ALLE PENICILLINE Reazioni allergiche in ordine decrescente di frequenza (incidenza complessiva tra 1 e 10%): Ø Eruzioni maculopapulari Ø Orticaria Ø Febbre Ø Broncospasmo Ø Dermatiti Ø Angioedema Ø Vasculiti Ø Sindrome di Lyell e Stevens-Johnson Ø Shock anafilattico (circa 0, 004 -0, 04%)

PRINCIPALI REAZIONI AVVERSE ALLE PENICILLINE Altre reazioni avverse Ø Diarrea (2 -5%) Ø Disturbi elettrolitici Ø Convulsioni (rara) Ø Neutropenia (1 -4%) Ø Aumento enzimi epatici Ø Insufficienza epatica acuta Ø Nefriti interstiziali (1 -2%) soprattutto con la meticillina che non viene più usata per questo

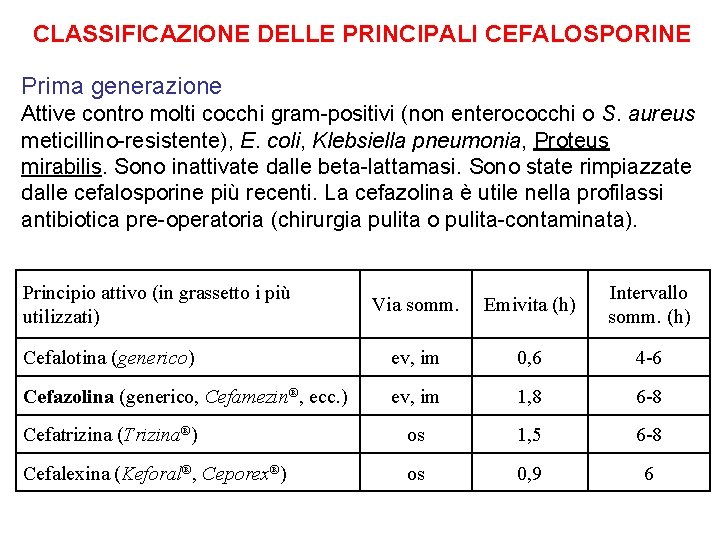
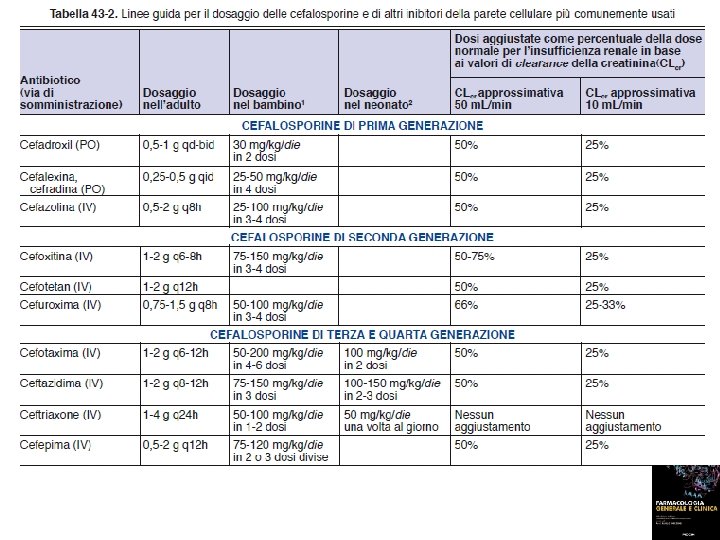
CLASSIFICAZIONE DELLE PRINCIPALI CEFALOSPORINE Prima generazione Attive contro molti cocchi gram-positivi (non enterococchi o S. aureus meticillino-resistente), E. coli, Klebsiella pneumonia, Proteus mirabilis. Sono inattivate dalle beta-lattamasi. Sono state rimpiazzate dalle cefalosporine più recenti. La cefazolina è utile nella profilassi antibiotica pre-operatoria (chirurgia pulita o pulita-contaminata). Principio attivo (in grassetto i più utilizzati) Via somm. Emivita (h) Intervallo somm. (h) Cefalotina (generico) ev, im 0, 6 4 -6 Cefazolina (generico, Cefamezin®, ecc. ) ev, im 1, 8 6 -8 Cefatrizina (Trizina®) os 1, 5 6 -8 Cefalexina (Keforal®, Ceporex®) os 0, 9 6

CLASSIFICAZIONE DELLE PRINCIPALI CEFALOSPORINE Seconda generazione Allargamento dello spettro ad alcuni batteri gram-negativi (es. H. influenzae, Neisseria, Citrobacter diversus) più attive verso enterobatteriacee. Maggiore resistenza alle beta-lattamasi. Cefuroxima utile nelle infezioni respiratorie (S. pneumoniae, H. influenzae, M. catarrhalis). Cefuroxima e cefamandolo utilizzate nella profilassi chirurgia ortopedica. Via somm. Emivita (h) Intervallo somm. (h) Cefamandolo (generico, Cefam®) ev, im 0, 8 4 -6 Cefoxitina (Mefoxin®, ecc. ) ev, im 0, 8 6 im 1, 5 6 -8 -12 ev, im, os 1, 3 8 -12 ev, im 4, 4 24 os os 0, 7 1 -2 8 12 -24 Principio attivo (in grassetto i più utilizzati) Cefmetazolo (Metafar®) Cefuroxima (generico, Curoxim®, Oraxim®, ecc. ) Cefonicid (genericoc, Cefodie®, ecc. ) Cefaclor (generico, Panacef®, ecc. ) Cefprozil (Cronocef®, Rozicef®)

CLASSIFICAZIONE DELLE PRINCIPALI CEFALOSPORINE Terza generazione Più attive delle cefalosporine di seconda contro gli enterobacilli gram negativi compresi quelli di origine nosocomiale. Possiedono anche una moderata attività contro gli anaerobi (a parte la ceftazidima). La ceftazidima ha scarsa attività contro i gram-positivi Via somm. Emivita (h) Intervallo somm. (h) ev, im 1 6 -12 Cefoperazone (Dardum®) im 2, 1 12 Ceftizoxima (Eposerin®) ev, im 2 12 Ceftriaxone (generico, Rocefin®, ecc. ) ev, im 8 24 Ceftazidima (generico, Glazidim®, ecc. ) ev, im 1, 8 8 -12 Cefodizime (Diezime®, ecc. ) ev, im 2, 5 -4 12 -24 Cefixima (generico, Cefixoral®, ecc. ) os 3 -4 12 Cefpodoxima (Cefodox®, ecc. ) os 12 Cefditoren (Glasion®, Redeguan®) os 12 Ceftibuten (Cedax®, Isocef®) os Principio attivo (in grassetto i più utilizzati) Cefotaxima (generico, Zariviz®, ecc. ) 2, 5 12 -24

CLASSIFICAZIONE DELLE PRINCIPALI CEFALOSPORINE Quarta generazione Spettro simile a quello della terza con buona attività sullo Pseudomonas, enterobacteriacee, S. aureus, S. Pneumoniae. Utilizzato nelle infezioni nosocomiali Principio attivo (in grassetto i più Via somm. Emivita (h) utilizzati) Cefepime (Cepim®, ecc. ) ev, im 2, 4 Intervallo somm. (h) 12


PRINCIPALI REAZIONI AVVERSE ALLE CEFALOSPORINE Reazioni allergiche Stesso tipo di reazioni delle penicilline. Non è raccomandabile somministrare una cefalosporina ad un paziente che ha avuto una grave reazione allergica da penicillina per il fenomeno dell’allergia crociata. Gli studi immunologici dimostrano una frequenza di allergia crociata del 20%, gli studi clinici indicano invece una frequenza più bassa (circa 1%).

PRINCIPALI REAZIONI AVVERSE ALLE CEFALOSPORINE Altre reazioni avverse Ø Diarrea Ø Ipoprotrombinemia (con possibili emorragie) Ø Trombocitosi (2 -5%) Ø Neutropenia (< 1%) Ø Alterazioni test epatici (1 -7%) Ø Nefriti interstiziali (rara) Ø Flebiti

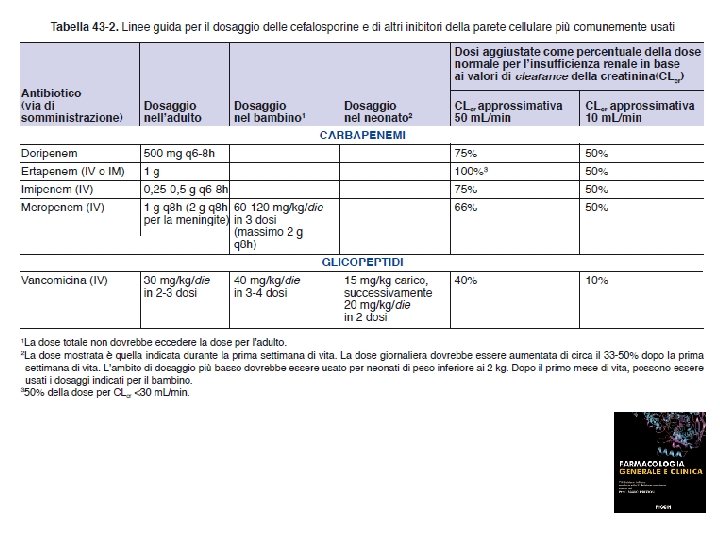
ALTRI ANTIBATTERICI BETA-LATTAMICI CARBAPENEMI Meropenem (generico, Merrem®, parenterale); Ertapenem (Invanz®) Imipenem+cilastatina (generico, Tenacid®, Tienam®, parenterale) Sono gli antibatterici con lo spettro d’azione più ampio disponibile che include G+ e G- aerobi ed anaerobi. La cilastatina è un inibitore delle deidropeptidasi, enzimi che a livello del rene inattivano l’imipenem provocando la produzione di metaboliti nefrotossici (questo non avviene con il meropenem). 50% dei pazienti allergici alle penicilline lo sono anche ai carbapenemi. Convulsioni, dose correlate o in pz con insufficienza renale o meningiti, sono più frequenti con l’imipenem che con il meropenem che può essere utilizzato nel trattamento delle meningiti batteriche. Altre ADR includono nausea, vomito, diarrea e anormale funzionalità epatica. Resistenza ai carbapenemici si è sviluppata in ceppi meticillino-resistenti di Stenotrophomonas (Xanthomonas) maltophilia. I carbapenemi sono da utilizzare nelle infezioni nosocomiali gravi.

ALTRI ANTIBATTERICI BETA-LATTAMICI MONOBATTAMI Aztreonam (Primbactan®, parenterale) Attività esclusiva verso batteri G- incluso lo Pseudomonas. Inefficace contro G+ e anaerobi. Non va utilizzato in terapia empirica. Può essere un alternativa in pazienti allergici a penicilline e cefalosporine in quanto provoca raramente ipersensibilità anche crociata. Può dare occasionali disturbi epatici, altre reazioni avverse sono rare.

ALTRI ANTIBATTERICI CHE AGISCONO SULLA MEMBRANA CELLULARE GLICOPEPTIDI Vancomicina (generico, Vancotex®, ecc. , os e infusione ev) Attività esclusiva verso batteri G+ in particolare stafilococchi. E’ irritante per i tessuti e quindi provoca flebiti. Raramente ototossicità e nefrotossicità. Tra le reazioni più comuni c’è la sindrome dell’uomo rosso o del collo rosso, legata a rilascio di istamina (evitabile prolungando il tempo di infusione) Teicoplanina (Targosid®, parenterale) Simile alla vancomicina, lunga emivita generalmente si somministra una volta al giorno LIPOPEPTIDI Daptomicina (Cubicin®, infusione ev) Spettro d’azione simile alla vancomicina, ma attiva anche su enterococchi e ceppi di S. aureus resistenti alla vancomicina.


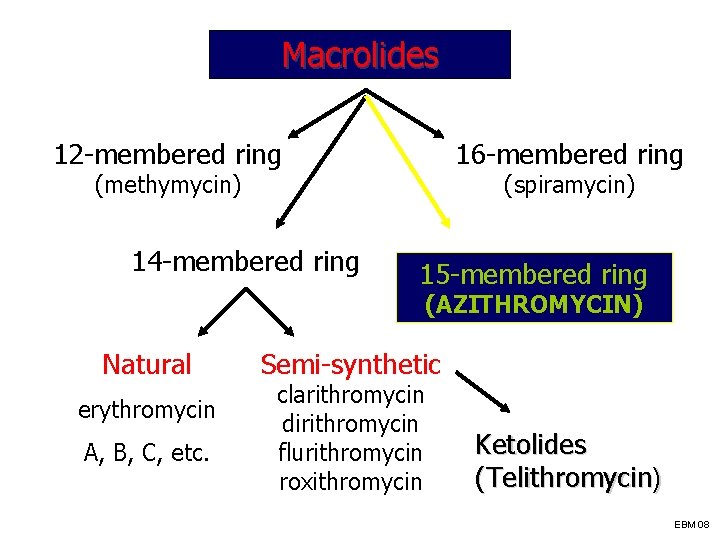
Classificazione dei macrolidi NATURALI SEMISINTETICI Eritromicina Oleandromicina Spiramicina Josamicina Midecamicina Roxitromicina Claritromicina Fluritromicina Diritromicina Azitromicina (azalidi) Miocamicina Rokitamicina Telitromicina (ketolidi)

Macrolides 12 -membered ring 16 -membered ring (methymycin) 14 -membered ring (spiramycin) 15 -membered ring (AZITHROMYCIN) Natural erythromycin A, B, C, etc. Semi-synthetic clarithromycin dirithromycin flurithromycin roxithromycin Ketolides (Telithromycin) EBM 08

MACROLIDI E KETOLIDI Ø Antibatterici ad ampio spettro, attivi sia contro i batteri Gpositivi che i G-negativi, con particolare attività nei confronti di micoplasmi e Legionella. Eritromicina con minore attivitàrispetto agli altri farmaci del gruppo Ø Inibiscono la sintesi proteica. Generalmente somministrate per via orale anche se ci sono preparazioni parenterali. Ø Sono di prima scelta nelle: § Polmoniti da micoplasma o Legionella; § Infezioni da clamidia § Difterite § Pertosse Ø Sono di seconda scelta in molte infezioni dove le penicilline sono di prima scelta.

MACROLIDI ERITROMICINA (generico, Eritrocina®) CLARITROMICINA (generico, Klacid®, Macladin®, ecc. ) AZITROMICINA (generico, Azitrocin®, Zitromax®, ecc. ) MIOCAMICINA (Macroral®, Miocamen®, Miokacin®) JOSAMICINA , SPIRAMICINA, ROXITROMICINA, FLURITROMICINA KETOLIDI TELITROMICINA (Ketek®, os) spettro d’azione similare ai macrolidi ma esteso a comprendere anche ceppi macrolidiresistenti. Il profilo di tossicità è simile ai macrolidi con qualche problema emergente a livello visivo ed epatico.

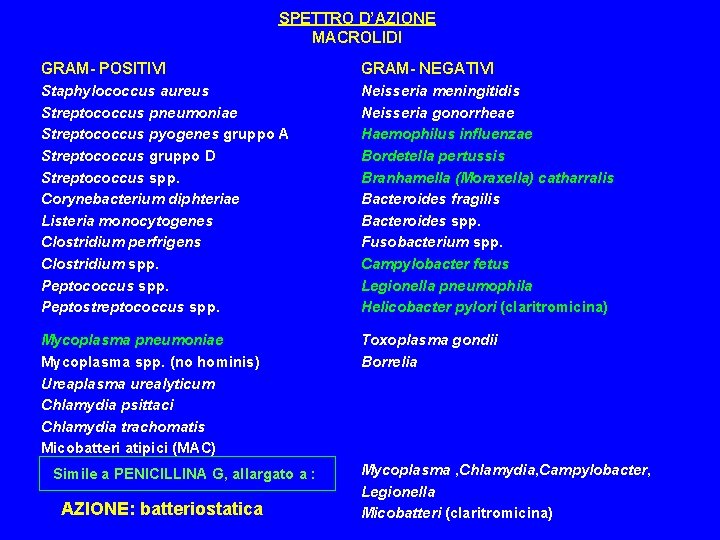
SPETTRO D’AZIONE MACROLIDI GRAM- POSITIVI GRAM- NEGATIVI Staphylococcus aureus Streptococcus pneumoniae Streptococcus pyogenes gruppo A Streptococcus gruppo D Streptococcus spp. Corynebacterium diphteriae Listeria monocytogenes Clostridium perfrigens Clostridium spp. Peptococcus spp. Peptostreptococcus spp. Neisseria meningitidis Neisseria gonorrheae Haemophilus influenzae Bordetella pertussis Branhamella (Moraxella) catharralis Bacteroides fragilis Bacteroides spp. Fusobacterium spp. Campylobacter fetus Legionella pneumophila Helicobacter pylori (claritromicina) Mycoplasma pneumoniae Mycoplasma spp. (no hominis) Ureaplasma urealyticum Chlamydia psittaci Chlamydia trachomatis Micobatteri atipici (MAC) Toxoplasma gondii Borrelia Simile a PENICILLINA G, allargato a : AZIONE: batteriostatica Mycoplasma , Chlamydia, Campylobacter, Legionella Micobatteri (claritromicina)

PHARMACODYNAMICS Comparison among macrolide antibiotics Mode of action Mainly bacteriostatic (bactericidal at high concentrations) Mechanism of action Inhibition of protein synthesis at 50 S ribosome Modes of resistance - Ribosomal methylation (MLS resistance) - Efflux system Activity Time-dependent Erythromycin PK-PD correlation T > MIC PAE Concentration-dependent Clarithromycin Azithromycin Ketolides PEAK/MIC AUC/MIC Generally persistent Blumer JL, Pediatr Infect Dis J, 1999, modified

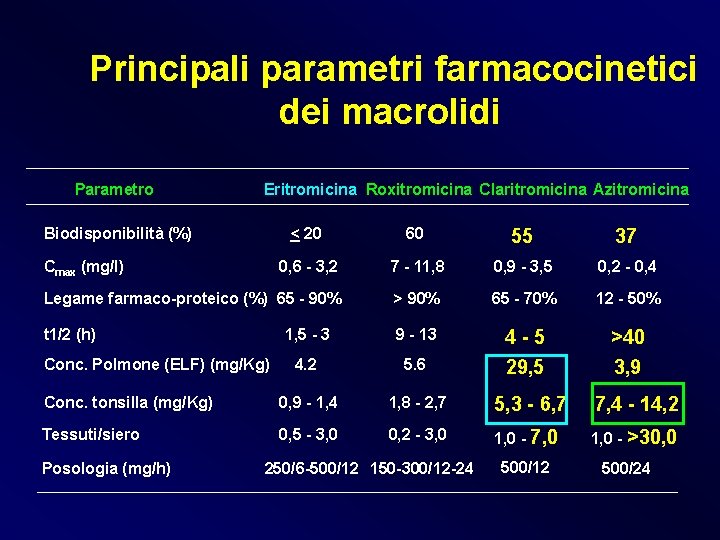
Principali parametri farmacocinetici dei macrolidi Parametro Eritromicina Roxitromicina Claritromicina Azitromicina Biodisponibilità (%) < 20 60 55 37 0, 6 - 3, 2 7 - 11, 8 0, 9 - 3, 5 0, 2 - 0, 4 Legame farmaco-proteico (%) 65 - 90% > 90% 65 - 70% 12 - 50% t 1/2 (h) 1, 5 - 3 9 - 13 4. 2 5. 6 4 -5 29, 5 >40 3, 9 Conc. tonsilla (mg/Kg) 0, 9 - 1, 4 1, 8 - 2, 7 5, 3 - 6, 7 7, 4 - 14, 2 Tessuti/siero 0, 5 - 3, 0 0, 2 - 3, 0 1, 0 - 7, 0 1, 0 - >30, 0 Cmax (mg/l) Conc. Polmone (ELF) (mg/Kg) Posologia (mg/h) 250/6 -500/12 150 -300/12 -24 500/12 500/24

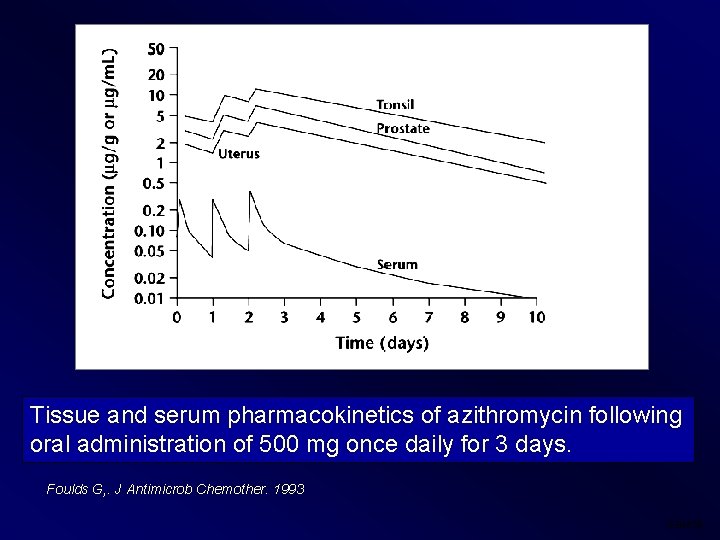
Tissue and serum pharmacokinetics of azithromycin following oral administration of 500 mg once daily for 3 days. Foulds G, . J Antimicrob Chemother. 1993 EBM 08

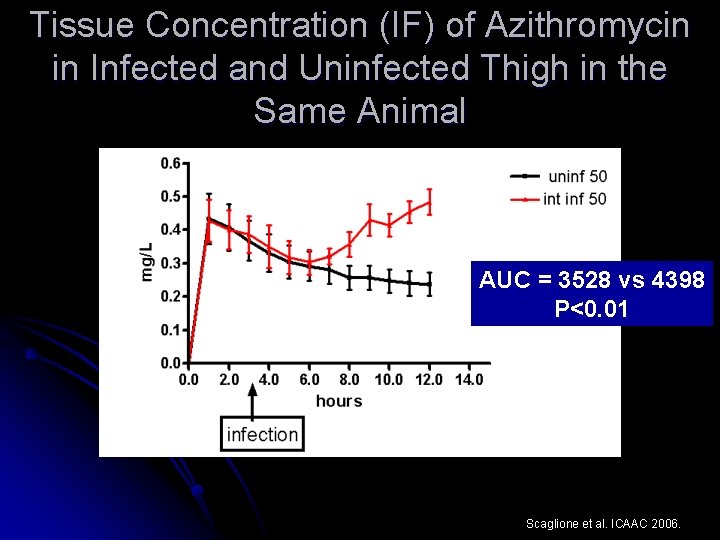
Tissue Concentration (IF) of Azithromycin in Infected and Uninfected Thigh in the Same Animal AUC = 3528 vs 4398 P<0. 01 Scaglione et al. ICAAC 2006.

AZITROMICINA: CARATTERISTICHE FISICOCHIMICHE, BIOLOGICHE, CINETICHE üStruttura di-basica (due centri aminici terziari basici) ü Maggiore stabilità in ambiente acido ü Maggior lipofilia ü Allargamento dello spettro d’azione verso Gram negativi (H influenzae) ü Emivita più lunga ü Maggior volume di distribuzione e penetrazione tissutale ü Rapida distribuzione da siero a tessuti ü Rilascio dai fagociti che aumenta le concentrazioni nei tessuti infetti ü Elevate e prolungate concentrazioni tissutali e il sostenuto rilascio dai tessuti differenziano azitromicina dagli antibiotici convenzionali e permettono un regime posologico particolare Wise R, 1996; Omura S, 2002;

Azione antinfiammatoria dei Macrolidi Int J Antimicrob Agents (2008)

MACROLIDI – REAZIONI AVVERSE Ø I Macrolidi sono tra gli antibatterici più sicuri, il problema più frequente è rappresentato dalle reazioni gastrointestinali (più frequenti con l’eritromicina rispetto ad azitromicina e claritromicina). Ø Reazioni gastrointestinali § Nausea § Vomito § Dolore addominale § Diarrea

MACROLIDI – REAZIONI AVVERSE Ø Reazioni allergiche § Febbre § Eosinofilia § Eruzioni cutanee Ø Altre Reazioni Rare § Reazioni epatiche § Aritmie (con uso e. v. ) § Perdita transitoria dell’udito (con alte dosi) § Alterazioni del gusto e dell’olfatto (claritromicina) Ø Per evitare tromboflebiti da eritromicina quando somministrata per e. v. è bene diluire la dose in almeno 250 ml ed evitare infusioni rapide (infondere in 45 -60 minuiti).

INTERAZIONI CON I MACROLIDI Ø I macrolidi, essendo degli inibitori enzimatici, interferiscono con il metabolismo di con molti farmaci (sotto sono riportati alcuni esempi) con grave rischio di tossicità. § § § Verapamil Warfarin Terfenadina Carbamazepina Metilprednisolone Ciclosporina Simvastatina Quetiapina Fluconazolo Taladafil Cotrimoxazolo Ecc. ecc.