SECONDO INCONTRO Regole di riempimento degli orbitali Gli

SECONDO INCONTRO

Regole di riempimento degli orbitali • Gli elettroni occupano gli orbitali a partire da quello con energia più bassa e proseguendo con gli altri orbitali in ordine di energia crescente. • Principio di esclusione di Pauli: in un atomo non possono esserci due elettroni con tutti e quattro i numeri quantici uguali • Regola di Hund: quando sono disponibili orbitali isoenergetici, gli elettroni tendono a occuparne il maggior numero possibile con spin parallelo

• Indicare i numeri quantici che definiscono i seguenti orbitali, nel caso si tratti di orbitali inesistenti indicarlo: 4 dxy, 6 s, 2 dyz, 4 f, 3 px, 2 s, 1 py, 9 s, 8 pz, 5 f.

• • • 4 dxy 6 s 2 dyz 4 f 3 px 2 s 1 p 9 s 8 pz 5 f y n l m inesistente 6 0 0 inesistente 4 3 (-3, -2, -1. 0, +1. +2. +3) 3 1 (-1, 0, +1) 2 0 0 inesistente 5 3 (-3, -2, -1. 0, +1. +2. +3)

26 • Quale delle seguenti specie possiede il maggior numero di elettroni disaccoppiati: • S+; S; S-. Motivare la risposta.

27 • Le sostanze paramagnetiche sono quelle che presentano elettroni a spin disaccoppiati e sono attratte da un magnete • Le sostanze diamagnetiche sono quelle che non presentano elettroni disaccoppiati e sono poco o affatto attratte da un magnete

28 • L’atomo di un elemento ha 17 elettroni. Senza consultare la tavola periodica, 1. scrivere la configurazione elettronica dello stato fondamentale dell’elemento e 1. dire se questo elemento è paramagnetico o diamagnetico.
![29 [ Ne] 3 s 2 3 p 5 paramagnetico 29 [ Ne] 3 s 2 3 p 5 paramagnetico](http://slidetodoc.com/presentation_image_h/92890de4c16e396d334e8316d5ba63e7/image-8.jpg)
29 [ Ne] 3 s 2 3 p 5 paramagnetico
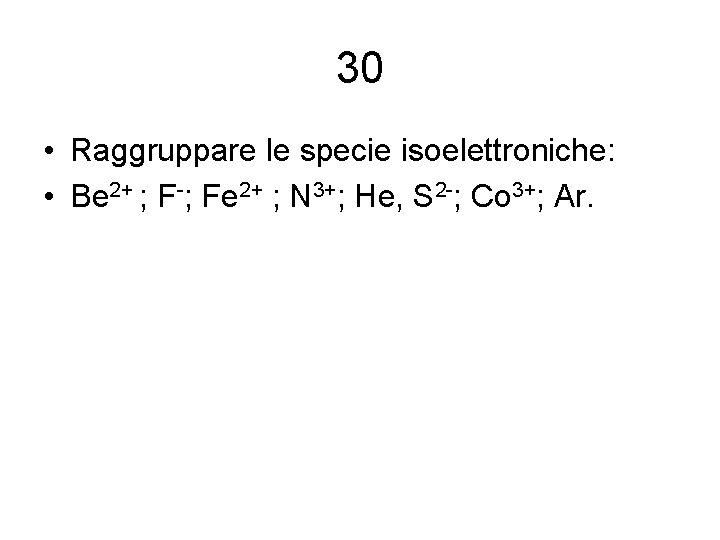
30 • Raggruppare le specie isoelettroniche: • Be 2+ ; F-; Fe 2+ ; N 3+; He, S 2 -; Co 3+; Ar.

31 • Scrivere i possibili valori per i quattro numeri quantici per un elettrone descritto da un orbitale 3 p

32 • Scrivere i quattro numeri quantici per un elettrone descritto da un orbitale 5 p

• Le leggi ponderali della chimica riguardano gli aspetti quantitativi delle reazioni chimiche • Sono la premessa alla formulazione della teoria atomica, in quanto suggerirono agli scienziati, attraverso le proporzioni definite e costanti esprimibili con numeri interi con le quali gli elementi reagiscono per dare i composti, l’idea che la materia sia costituita di atomi.

La legge di Lavoisier • In una reazione chimica la somma delle masse dei reagenti è uguale alla somma delle masse dei prodotti • Si tratta della legge della conservazione della materia nelle reazioni chimiche, valida entro certi limiti. Infatti, in realtà, anche nei processi chimici una parte della massa si trasforma in energia e viceversa, secondo quanto previsto dalla E=mc 2

Legge di Proust • Quando due elementi si combinano per dare un composto, reagiscono secondo rapporti definiti e costanti tra le loro masse, esprimibili con numeri interi e piccoli (cioè i primi termini della serie dei naturali)

• Nel biossido di carbonio il rapporto di combinazione tra carbonio e ossigeno è 0, 375. quanti grammi di ossigeno occorrono per reagire completamente con 156 g di carbonio?

Legge di Dalton • Quando due elementi si combinano secondo rapporti diversi per dare composti diversi, le quantità di un elemento che si combinano con una stessa quantità dell’altro elemento stanno tra loro secondo rapporti espressi da numeri interi e piccoli

• Il cloro e l’ossigeno possono formare quattro composti diversi: • • • Anidride ipoclorosa Cl 2 O Anidride clorosa Cl 2 O 3 Anidride clorica Cl 2 O 5 Anidride perclorica Cl 2 O 7 Una serie di esperimenti ha mostrato che con 142 g di cloro reagiscono le seguenti quantità di ossigeno: 32 g 96 g 160 g 224 g Verificare che questi dati siano in accordo con la legge delle proporzioni multiple.

• Il rapporto di combinazione tra le masse di idrogeno, solfo e ossigeno è di 1: 16 : 32. calcola le masse dei tre elementi in 200 mg di composto.

soluzione • 1+16+32 =49 • 1: 49 =XH: 200 • 16: 49=Xs: 200 • 32: 49= Xo: 200

Reattività dei metalli alcalini e alcalino-terrosi con l’acqua • I metalli alcalini (primo gruppo principale) sono tutti molto reattivi con l’acqua • Nei metalli alcalino-terrosi (secondo gruppo principale) la reattività con l’acqua aumenta dall’alto verso il basso pertanto il berillio non reagisce direttamente con l’acqua mentre il magnesio reagisce soltanto con l’acqua bollente
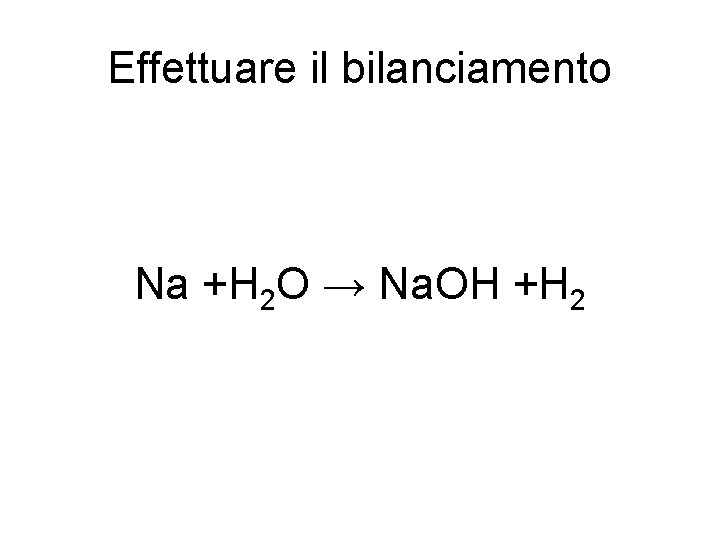
Effettuare il bilanciamento Na +H 2 O → Na. OH +H 2
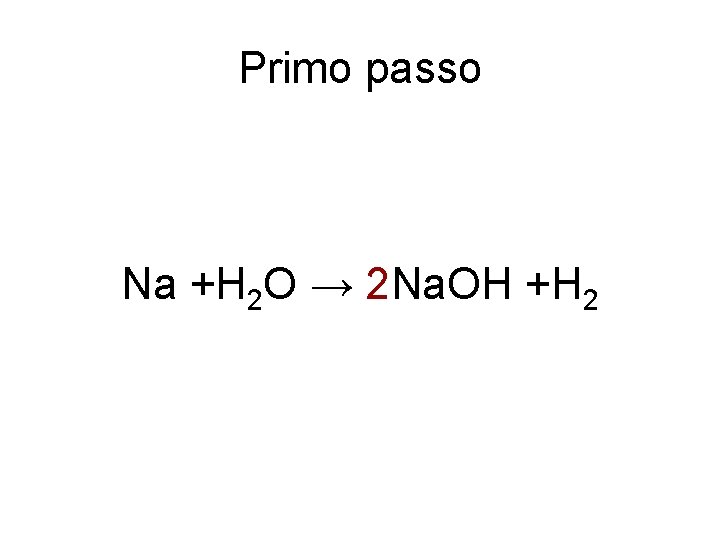
Primo passo Na +H 2 O → 2 Na. OH +H 2
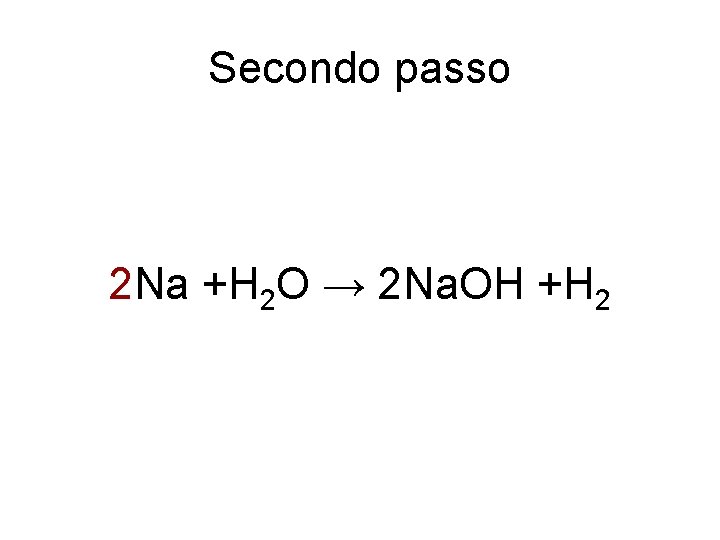
Secondo passo 2 Na +H 2 O → 2 Na. OH +H 2
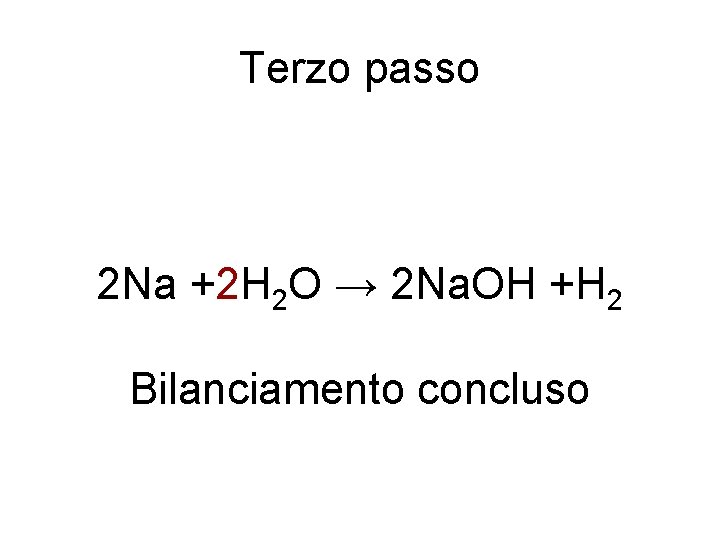
Terzo passo 2 Na +2 H 2 O → 2 Na. OH +H 2 Bilanciamento concluso
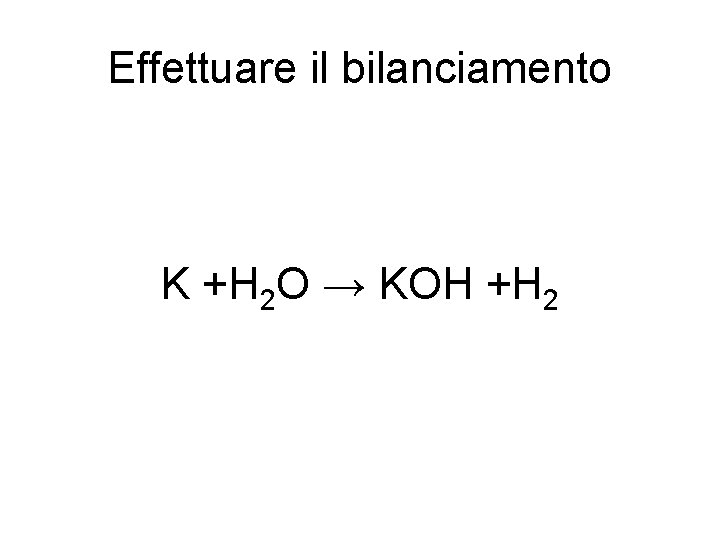
Effettuare il bilanciamento K +H 2 O → KOH +H 2
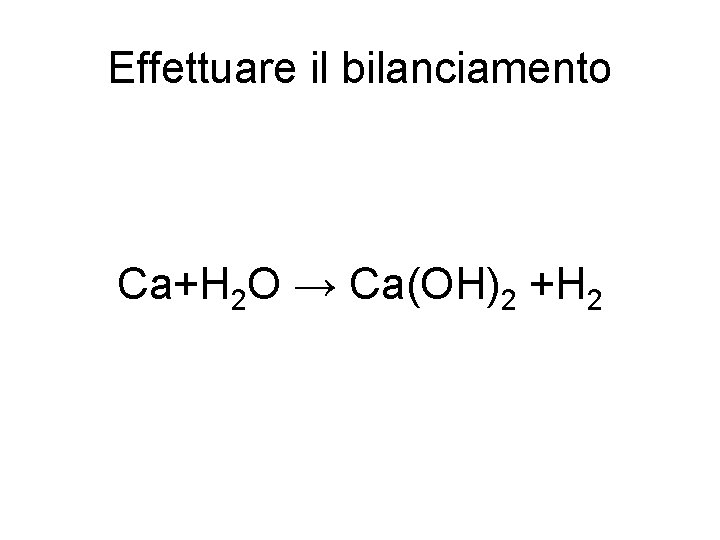
Effettuare il bilanciamento Ca+H 2 O → Ca(OH)2 +H 2
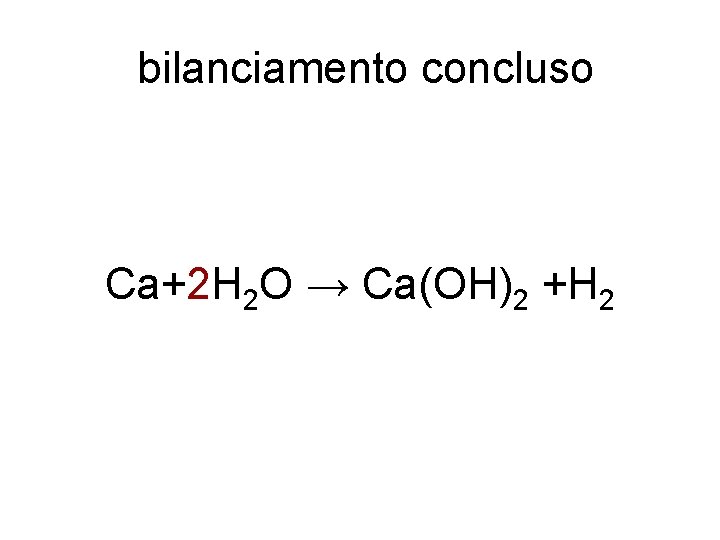
bilanciamento concluso Ca+2 H 2 O → Ca(OH)2 +H 2

• Calcolare quanti grammi di idrogeno si possono ricavare da 70 grammi di Na e una quantità adeguata di H 2 O

Primo passo: bilanciare la reazione 2 Na +2 H 2 O → 2 Na. OH +H 2

Secondo passo • Individuiamo il rapporto stechiometrico • Il rapporto stechiometrico tra sodio e idrogeno è 2: 1 • Cioè due moli di sodio metallico producono una mole di idrogeno gassoso (l’idrogeno è un gas biatomico)

Terzo passo • Determiniamo il peso di una mole di sodio e di una di idrogeno • Na ≈ 23 g • H 2 ≈ 1+1= 2 g

Quarto passo • Impostiamo la proporzione sulla base del rapporto stechiometrico dato dalla reazione bilanciata • 23· 2 : 2 = 70 : X • X = 3, 04 g di idrogeno

risolvere • CH 3 CH 2 OH + O 2 → CO 2 +H 2 O • Data la reazione di combustione dell’alcol etilico (etanolo) calcola quanti grammi di anidride carbonica si ottengono a partire da un chilogrammo di etanolo.

Primo passo: bilanciare la reazione • CH 3 CH 2 OH + O 2 → 2 CO 2 +H 2 O
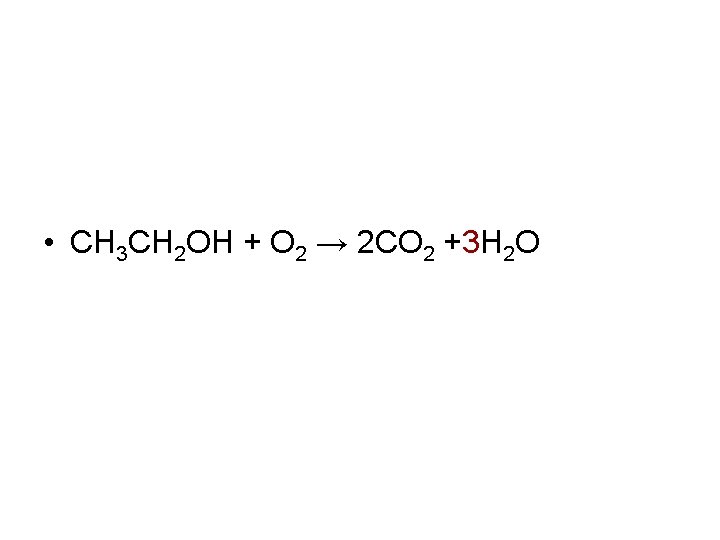
• CH 3 CH 2 OH + O 2 → 2 CO 2 +3 H 2 O
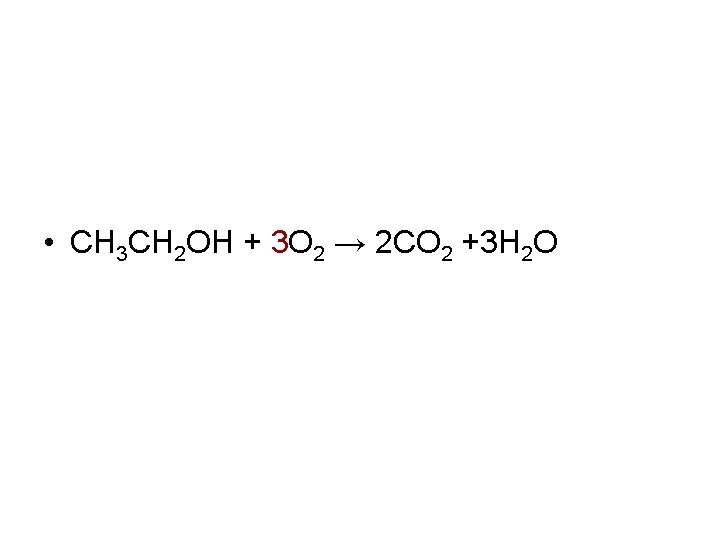
• CH 3 CH 2 OH + 3 O 2 → 2 CO 2 +3 H 2 O

Secondo passo • Individuiamo il rapporto stechiometrico • Il rapporto stechiometrico tra etanolo e anidride carbonica è 1: 2 • Cioè una mole di etanolo produce due moli di CO 2

Terzo passo • Determiniamo il peso di una mole di etanolo e di una di CO 2 • C 2 H 5 OH ≈ 12· 2 + 1· 6 +16 = 46 g • CO 2 ≈ 12+16· 2= 44 g

Quarto passo • Impostiamo la proporzione sulla base del rapporto stechiometrico dato dalla reazione bilanciata • 46 : 2· 44 = 1000 : X • X = 1913 g di CO 2

Risolvere CH 3 COOH + O 2 → CO 2 +H 2 O Data la reazione determinare la quantità di acido acetico necessaria per produrre 783 g di CO 2
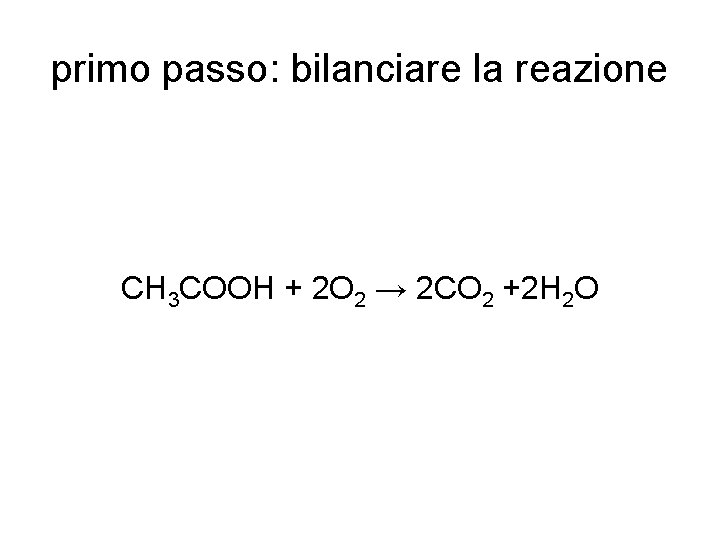
primo passo: bilanciare la reazione CH 3 COOH + 2 O 2 → 2 CO 2 +2 H 2 O

Secondo passo: individuare il rapporto stechiometrico • Il rapporto è di • 1 mole di acido acetico: 2 moli di CO 2

Terzo passo: calcolo della massa molare • Acido acetico = 60 g • Anidride carbonica = 44 g
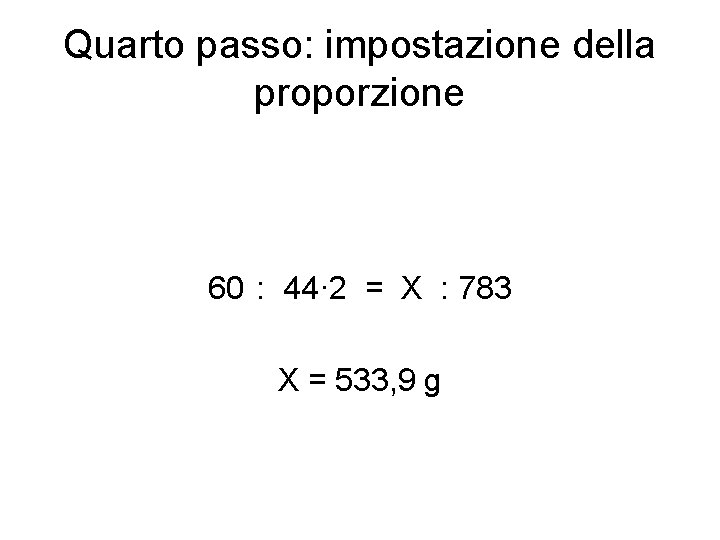
Quarto passo: impostazione della proporzione 60 : 44· 2 = X : 783 X = 533, 9 g

• Un composto costituito da idrogeno, fosforo e ossigeno presenta un rapporto di combinazione delle masse 1 : 10, 3 : 21, 3. Calcola la massa di composto che si ottiene se si utilizzano 30 grammi di idrogeno.

• Per la reazione di formazione dell’ammoniaca il rapporto fra la quantità di idrogeno e quella di azoto che reagiscono è 3: 14. • Calcola quanti grammi di azoto sono necessari per reagire con le seguenti quantità di idrogeno. • 6 g 12 g 15 g 20 g

• Il rapporto di combinazione tra zolfo e ossigeno nel triossido di zolfo , SO 3, è massa solfo : massa ossigeno = 2 : 3 • Quanti grammi di ossigeno occorrono per reagire completamente con 128 g di zolfo?
- Slides: 47