Biochimica CLASSIFICAZIONE INTERNAZIONALE DEGLI ENZIMI 6 classi ciascuna

Biochimica CLASSIFICAZIONE INTERNAZIONALE DEGLI ENZIMI 6 classi, ciascuna divisa in sottoclassi Nome raccomandato es. carbossipeptidasi Nome sistematico es. peptidil-L-ammino-acido idrolasi 3. 4. 17. 1 EC 3 classe principale 4 sottoclasse (legami peptidici) 17 sottoclasse (metallopeptidasi, Zn 2+) 1 numero di serie

Biochimica
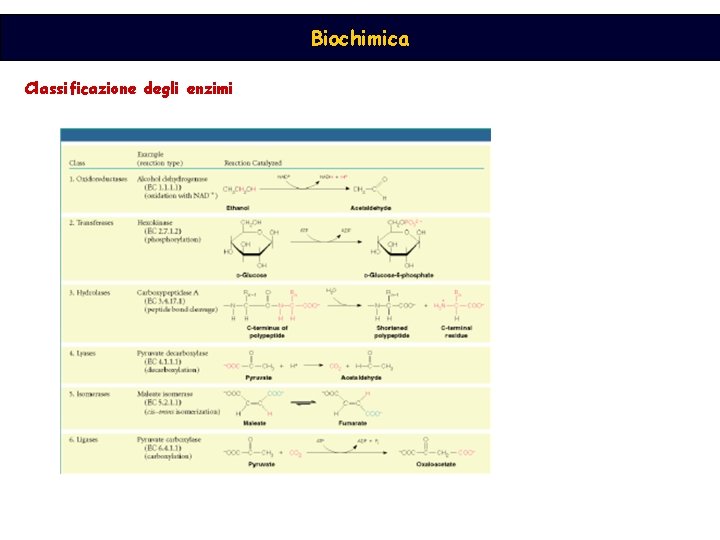
Biochimica Classificazione degli enzimi

Biochimica Nome d’uso raccomandato (nome comunemente usato, spesso di origine “storica”) Nome sistematico (nome dei substrati + termine con suffisso –asi, che definisce il tipo di reazione) alcool deidrogenasi (nome raccomandato) alcool: NAD+ ossidoriduttasi (nome sistematico) EC 1. 1 (numero di classificazione) carbossipeptidasi A (nome raccomandato) peptidil-L-amminoacido-idrolasi (nome sistematico) EC 3. 4. 17. 1 (numero di classificazione)

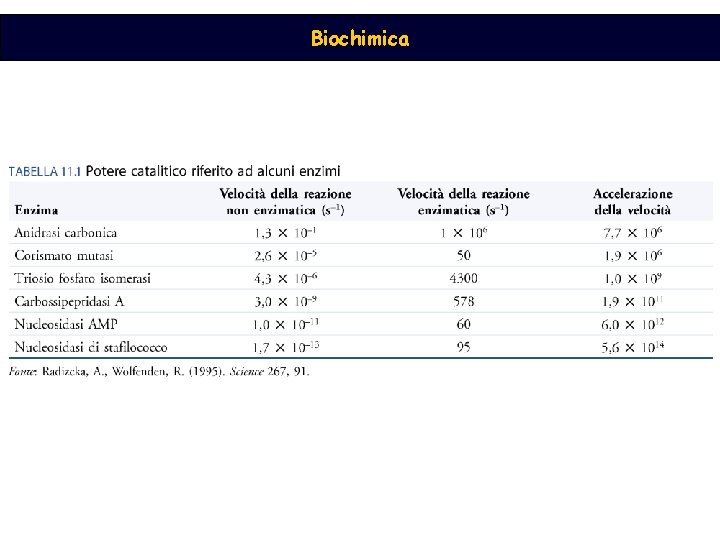
Biochimica Ruolo degli enzimi Un catalizzatore in genere aumenta la velocità di una reazione senza esserne modificato La molecola su cui l’enzima o il catalizzatore agiscono viene chiamato substrato L’enzima accelera la reazione di molti ordini di grandezza Il catalizzatore non modifica l’equilibrio: non si può ottenere più prodotto da una reazione catalizzata, si raggiunge lo stato di equilibrio più velocemente A <−> 2 B Keq = [B]2/[A]
Biochimica

Biochimica Sono caratteristiche degli enzimi: 1. Il potere catalitico 2. Specificità 3. Regolazione

Biochimica Cofattori Ioni metallici (Fe 2+, Fe 3+, Cu 2+, Zn 2+……. )
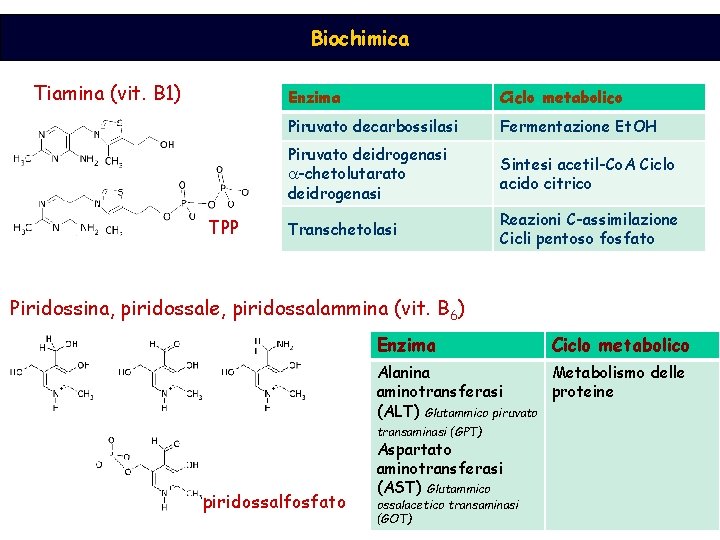
Biochimica Tiamina (vit. B 1) TPP Enzima Ciclo metabolico Piruvato decarbossilasi Fermentazione Et. OH Piruvato deidrogenasi a-chetolutarato deidrogenasi Sintesi acetil-Co. A Ciclo acido citrico Transchetolasi Reazioni C-assimilazione Cicli pentoso fosfato Piridossina, piridossale, piridossalammina (vit. B 6) Enzima Ciclo metabolico Alanina Metabolismo delle aminotransferasi proteine (ALT) Glutammico piruvato transaminasi (GPT) piridossalfosfato Aspartato aminotransferasi (AST) Glutammico ossalacetico transaminasi (GOT)
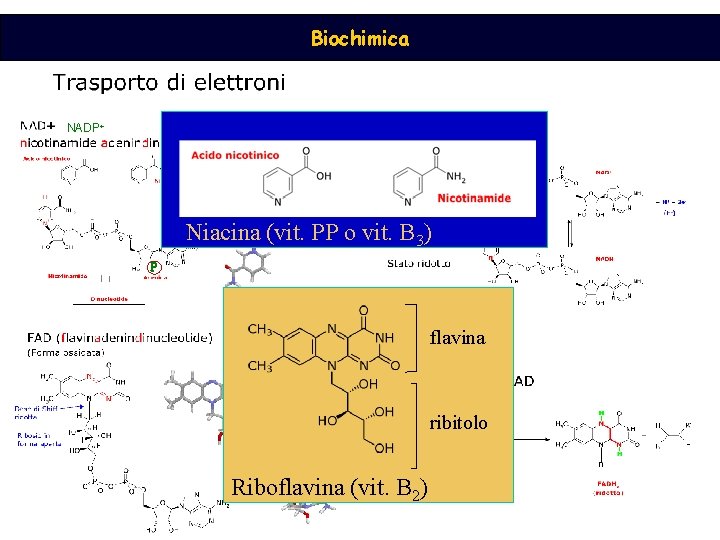
Biochimica NADP+ Niacina (vit. PP o vit. B 3) P P flavina ribitolo Riboflavina (vit. B 2)
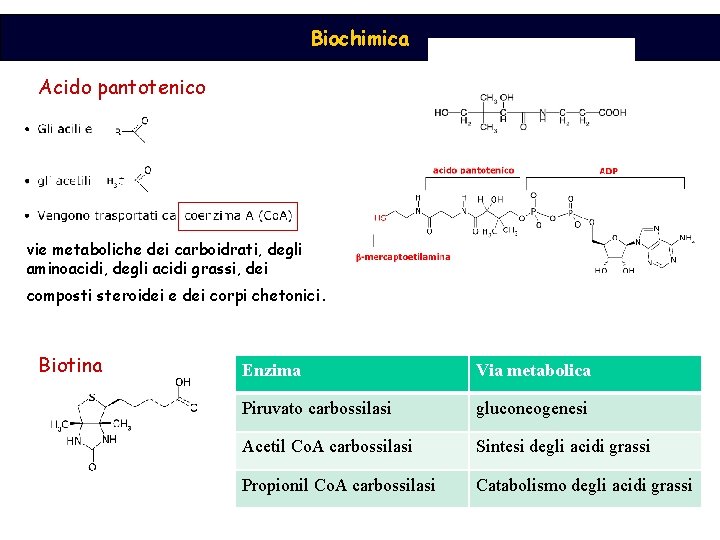
Biochimica Acido pantotenico vie metaboliche dei carboidrati, degli aminoacidi, degli acidi grassi, dei composti steroidei e dei corpi chetonici. Biotina Enzima Via metabolica Piruvato carbossilasi gluconeogenesi Acetil Co. A carbossilasi Sintesi degli acidi grassi Propionil Co. A carbossilasi Catabolismo degli acidi grassi
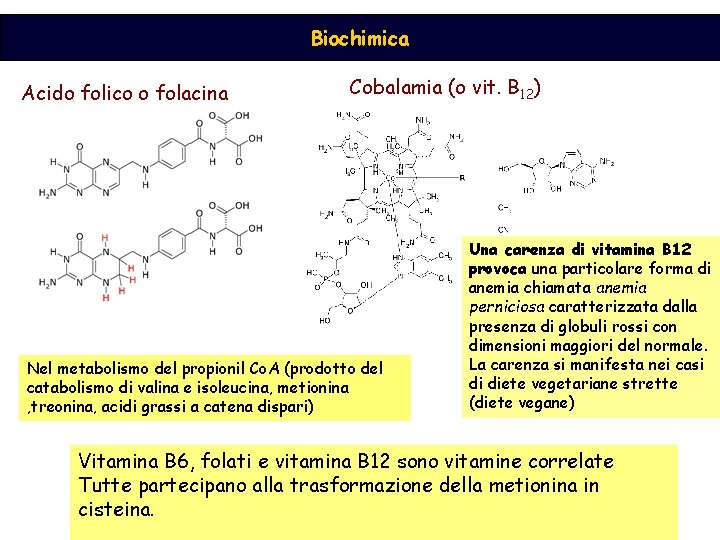
Biochimica Acido folico o folacina Cobalamia (o vit. B 12) Nel metabolismo del propionil Co. A (prodotto del catabolismo di valina e isoleucina, metionina , treonina, acidi grassi a catena dispari) Una carenza di vitamina B 12 provoca una particolare forma di anemia chiamata anemia perniciosa caratterizzata dalla presenza di globuli rossi con dimensioni maggiori del normale. La carenza si manifesta nei casi di diete vegetariane strette (diete vegane) Vitamina B 6, folati e vitamina B 12 sono vitamine correlate Tutte partecipano alla trasformazione della metionina in cisteina.
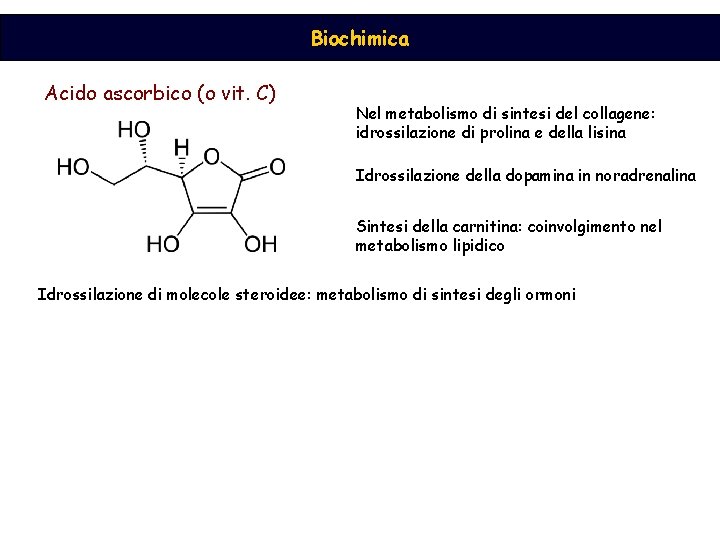
Biochimica Acido ascorbico (o vit. C) Nel metabolismo di sintesi del collagene: idrossilazione di prolina e della lisina Idrossilazione della dopamina in noradrenalina Sintesi della carnitina: coinvolgimento nel metabolismo lipidico Idrossilazione di molecole steroidee: metabolismo di sintesi degli ormoni

Biochimica In cinetica chimica
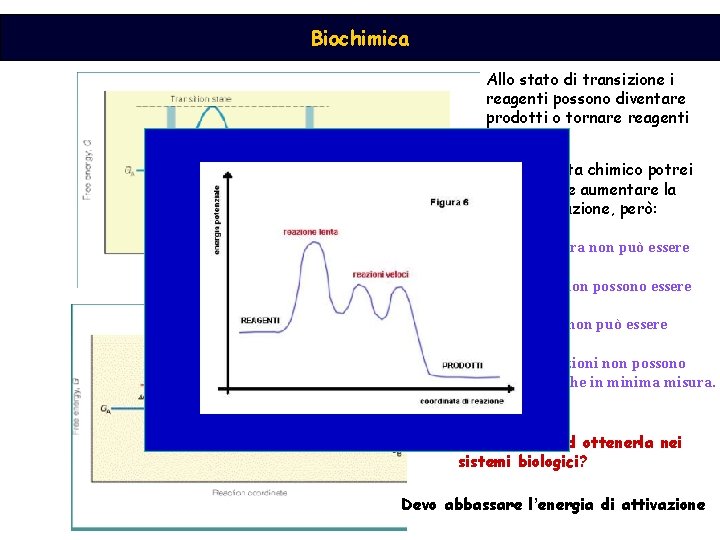
Biochimica Allo stato di transizione i reagenti possono diventare prodotti o tornare reagenti Energia di attivazione Dal p. to di vista chimico potrei statisticamene aumentare la velocità di reazione, però: 1. la temperatura non può essere innalzata 2. acidi o basi non possono essere aggiunti 3. la pressione non può essere aumentata 4. le concentrazioni non possono essere variate che in minima misura. Come faccio ad ottenerla nei sistemi biologici? Devo abbassare l’energia di attivazione
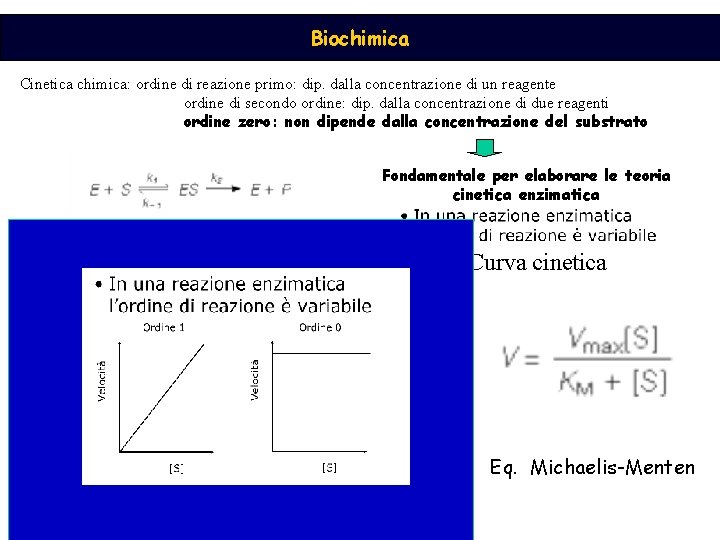
Biochimica Cinetica chimica: ordine di reazione primo: dip. dalla concentrazione di un reagente ordine di secondo ordine: dip. dalla concentrazione di due reagenti ordine zero: non dipende dalla concentrazione del substrato Fondamentale per elaborare le teoria cinetica enzimatica Curva cinetica Eq. Michaelis-Menten

Biochimica Deve essere calcolata sperimentalmente

Biochimica

Biochimica Grafico dei doppi reciproci: trasforma l’eq. dell’iperbole, come eq. di una retta Diviene un valore finito Il valore viene estrapolato L’eq. Di Michaelis Menten è la cinetica di un caso limite, reale, ma nei sistemi biologici sono più facilmente coinvolti più substrati
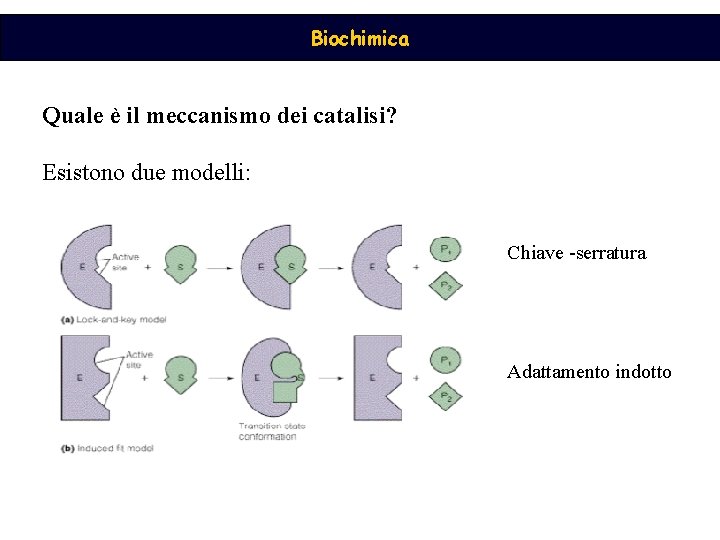
Biochimica Quale è il meccanismo dei catalisi? Esistono due modelli: Chiave -serratura Adattamento indotto

Biochimica
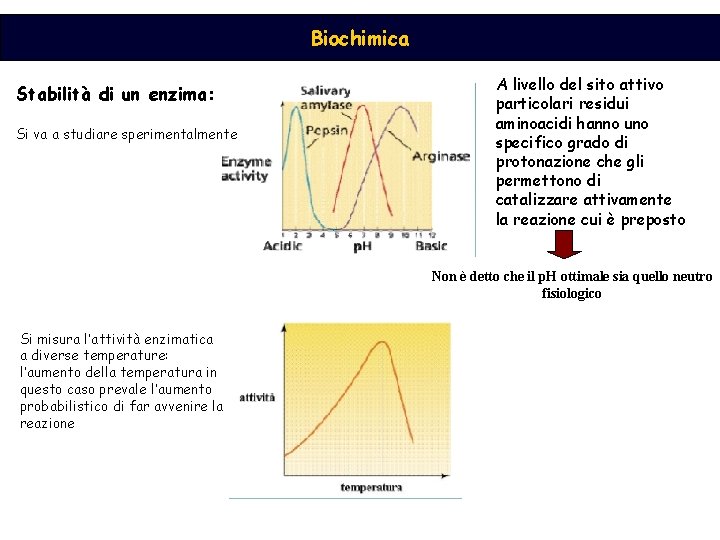
Biochimica Stabilità di un enzima: Si va a studiare sperimentalmente A livello del sito attivo particolari residui aminoacidi hanno uno specifico grado di protonazione che gli permettono di catalizzare attivamente la reazione cui è preposto Non è detto che il p. H ottimale sia quello neutro fisiologico Si misura l’attività enzimatica a diverse temperature: l’aumento della temperatura in questo caso prevale l’aumento probabilistico di far avvenire la reazione

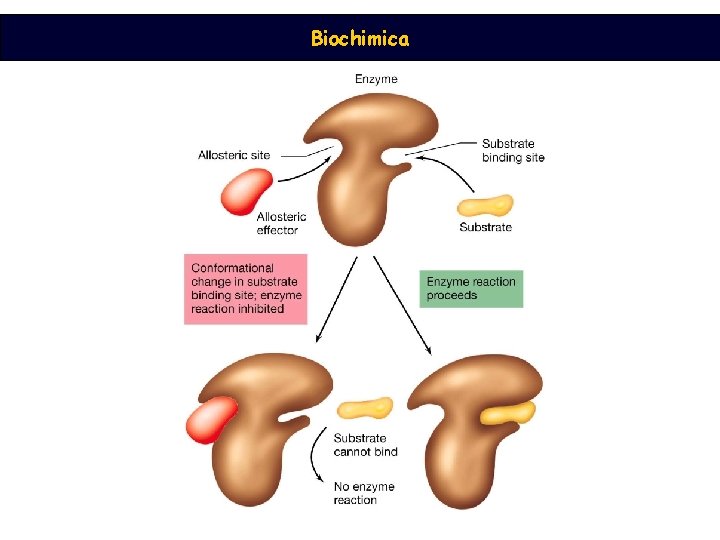
Biochimica MECCANISMI DI REGOLAZIONE enzimatica: Stimolazione/inibizione della sintesi Meccanismo allosterico Modificazione covalente irreversibile Modificazione covalente reversibile

Biochimica Nei processi biologici le vie metaboliche sono modulate da una particolare classe di enzimi : ENZIMI ALLOSTERICI che sono sempre con struttura quaternaria Cosa è una via metabolica? Come posso modulare l’intera via
Biochimica
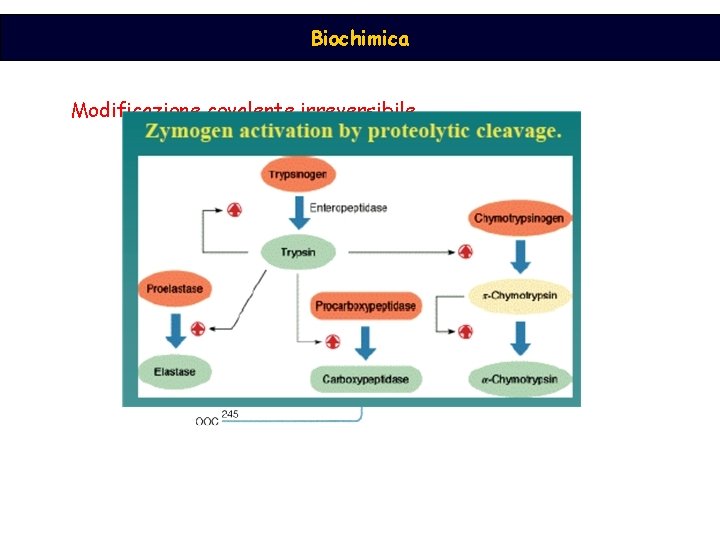
Biochimica Modificazione covalente irreversibile

Biochimica Modificazione covalente reveribile Viene spesso utilizzata per attivare e inibire due vie metaboliche hanno effetto opposto: Sintesi e degradazione del glicogeno Modificazione che ha un effetto tipo on/off Solitamente avviene attraverso una modificazione temporanea a carico di uno o più residui amminoacidici. (fosforilazione, acetilazione, metilazione, adenilazione…. ) Una modificazione di particolare importanza è la fosforilazione a carico di residui –OH di ser e thr, meno spesso d tyr

Biochimica L’attivita enzimatica, proporzionale alla concentrazione dell’enzima, si esprime in UNITA’ Una Unita Internazionale (UI): quantita di enzima che catalizza la conversione di 1 μmole di substrato per minuto in condizioni definite di temperatura, p. H, e concentrazione del substrato ATTIVITA’ ENZIMATICA U/L = ∆A 1000 V εtdv d → spessore cuvetta t → tempo di reazione (min) ∆A → variazione di Abs v → volume campione (m. L) 1000 → conversione a L V → volume di reazione (m. L)
- Slides: 28