CRISTALIZACIN Cristalizacin PROGRAMA IA Tema 6 CRISTALIZACIN Cristalizacin























































- Slides: 74

CRISTALIZACIÓN Cristalización

PROGRAMA IA: Tema 6 CRISTALIZACIÓN • • Cristalización a partir de soluciones: Teoría de MYERS Nucleación Crecimiento de los cristales. Polimorfismo Procesos de cristalización que implican separación de fase, en la industria alimentaria • Cristalización de sustancias fundidas • Cristalizadores: Ø De suspensión mezclada Ø Evaporadores-cristalizadores de circulación forzada Ø De magma coniesférico Ø De tubos de arrastre Ø De enfriamiento Ø Por contacto diretp Ø De superficies enfriadas Ø De superficies rascadas Ø Diseño y cálculo de cristalizadores

PROGRAMA IQ: Tema 7 DISEÑO DE EQUIPOS DE TRANSFERENCIA DE CALOR VI • • • Cristalización a partir de soluciones: Teoría de MYERS Velocidad de crecimiento Nucleación Cristalización de sustancias fundidas Cristalizadores: Ø De suspensión mezclada Ø Evaporadores-cristalizadores de circulación forzada Ø De magma coniesférico Ø De tubos de arrastre Ø De enfriamiento Ø Por contacto directo Ø De superficies enfriadas Ø De superficies rascadas Ø Diseño y cálculo de cristalizadores

Temario Introducción. Nucleación. Periodo de inducción. Cinética de crecimiento de cristales. Teoría de sobresaturación de Miers. Zona metaestable. Aditivos. Procesos secundarios. Equipamientos, clasificación y usos. Bibliografía.

Introducción

Cristalización Definición La Cristalización es un proceso industrial en donde se forman partículas sólidas (cristales) a partir de una fase homogénea (que puede ser gas o líquida), pasando el sistema de un estado de desequilibrio al estado de equilibrio. Implicando un descenso de energía que compense el incremento de orden

Cristal Definición Un sistema de átomos, moléculas o iones altamente ordenados en redes tridimensionales

Objetivos 1. Remover impurezas/purificar productos. 2. Secado para remover algún solvente/agua. 3. formulación para satisfacer el requisito de el consumidor. 4. Lograr la estabilidad del producto.

Importancia Mas del 80 % de las sustancias usadas en productos farmacéuticos, químicos, agroquímicos, alimenticios y cosméticos son aislados o formulados en su forma sólida. La cristalización generalmente es el ultimo paso de purificación química.

Nucleación

Nucleación Formación de amontonamientos de átomos, moléculas o iones constituyentes de la nueva fase en pequeñas zonas separadas en el interior de la antigua fase. Amontonamientos de partículas: Clusters, crecen y desmoronan. Dimensión crítica, dimensión macroscópica

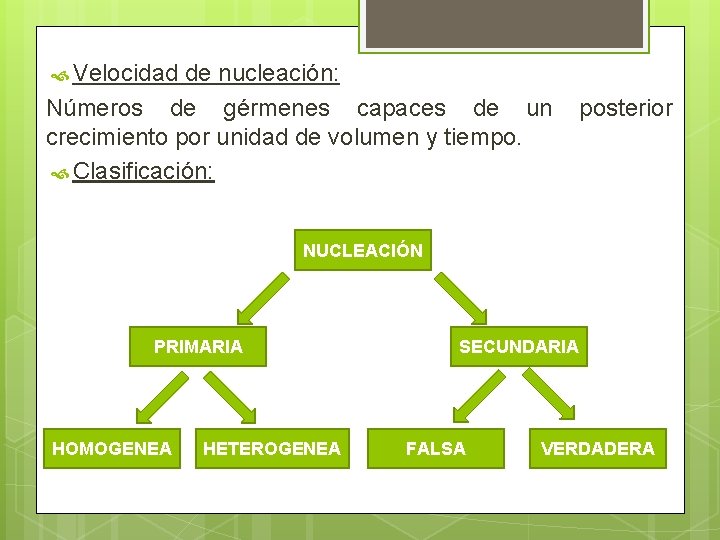
Velocidad de nucleación: Números de gérmenes capaces de un crecimiento por unidad de volumen y tiempo. Clasificación: posterior NUCLEACIÓN PRIMARIA HOMOGENEA HETEROGENEA SECUNDARIA FALSA VERDADERA

Nucleación Primaría El origen de la nueva fase sólida no esta condicionada ni influida por la presencia de la fase sólida que se origina. Si las partículas extrañas a la fase sólida influyen en la nucleación o no: Nucleación Homogénea Nucleación Heterogénea

Nucleación Homogénea El origen de las partículas de la nueva fase no se produce ni está influido por la presencia de fase sólida. No es un mecanismo frecuente. El amontonamiento de átomos/clauster se produce a través de choques graduales. Tamaño crítico: Esta en equilibrio con la disolución sobresaturada. La nueva fase se produce a expensas de liberación de energía, consumida en la formación de nueva estructura.

Nucleación Heterogénea La nueva fase esta condicionada por la presencia en el sistema en nucleación de una fase sólida extraña. (nucleante heterogéneo) La superficie del nucleante facilita la formación de la nueva fase, actúa como catalizador. La nucleación ocurrirá a una sobresaturación mas baja que la que correspondería a la nucleación homogénea.

Nucleación Heterogénea

Nucleación Heterogénea Al aumentar la incongruencia entre las estructuras, aumenta la sobresaturación crítica necesaria para el origen de la nueva fase La velocidad de nucleación disminuirá hasta que se agoten las partículas activas de nucleante heterogéneo. Cuanto menos se diferencien las estructuras, mas fácil será la nucleación heterogénea y mejor catalizador será el sustrato.

Nucleación Secundaria La formación de cristales de la nueva fase que está condicionada por la presencia de partículas de la misma fase en el sistema sobresaturado y por cuya causa ocurre. Obtención de sales muy solubles a partir de disoluciones sobresaturadas. Nucleación Falsa. Nucleación Verdadera. Nucleación de Contacto.

Nucleación Falsa Siembra de cristales en una disolución sobresaturada. Presencia de partículas microscópicas, mayores al germen crítico, en la superficie de los cristales introducidos. Inestabilidad de agregados cristalinos. Macro abrasión.

Nucleación Verdadera Los gérmenes de los nuevos cristales se pueden originar en la superficie del cristal en crecimiento, en capa límite del líquido contiguo al cristal. Desintegración de dendritas.

Nucleación de Contacto Las partículas microscópicas de la fase en formación se generan por la acción de una fuerza mecánica sobre los cristales que hay en la disolución sobresaturada. Partículas mayores a la del núcleo crítico crecen. Predomina sobre los demás mecanismos de nucleación secundaria.

Periodo de Inducción Tiempo que transcurre entre el establecimiento de la sobresaturación y el cambio en una propiedad física del sistema, como consecuencia de la cristalización. Función de la sobresaturación y temperatura. Tiempo de inducción= ti+tn+tg ti, ordenamiento de gérmenes en la disolución. tn, germen crítico. tg, tamaño detectable. Ti despreciable generalmente.

Cinética de crecimiento de cristales

Cinética de Crecimiento Ocurren tres procesos cinéticos: Transporte de materia – unidades constructivas desde el volumen de la disolución sobresaturada hacia el cristal por difusión y/o convección. Incorporación de materia, reacción superficial. Evacuación de calor de cristalización desde el cristal hasta el seno de la disolución. Velocidad determinada por el proceso cuya velocidad es menor.

Cinética de Crecimiento Reacción exotérmica La T de la superficie del cristal en crecimiento será mayor que la temperatura de la disolución, implicando variación de la fuerza impulsora y aumento de la velocidad de reacción. Ejemplo: Na 2 S 2 O 3 – 5 H 2 O, Na 2 SO 4 – 10 H 2 O; Na. Cl, Mg. SO 4 - 7 H 2 O

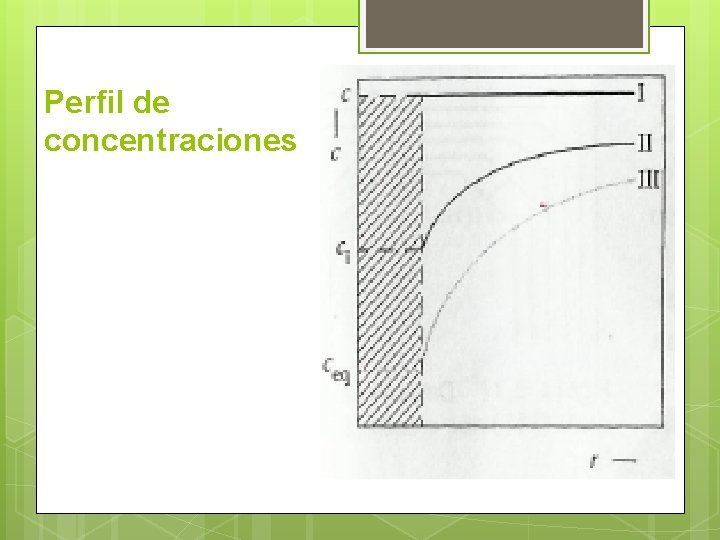
Cinética de Crecimiento La diferencia de concentración entre el seno de la disolución y la sup. del cristal representa la fuerza motriz del transporte de materia. La diferencia entre la concentración de la superficie del cristal y la concentración de equilibrio representa la fuerza motriz de la reacción superficial.

Perfil de concentraciones

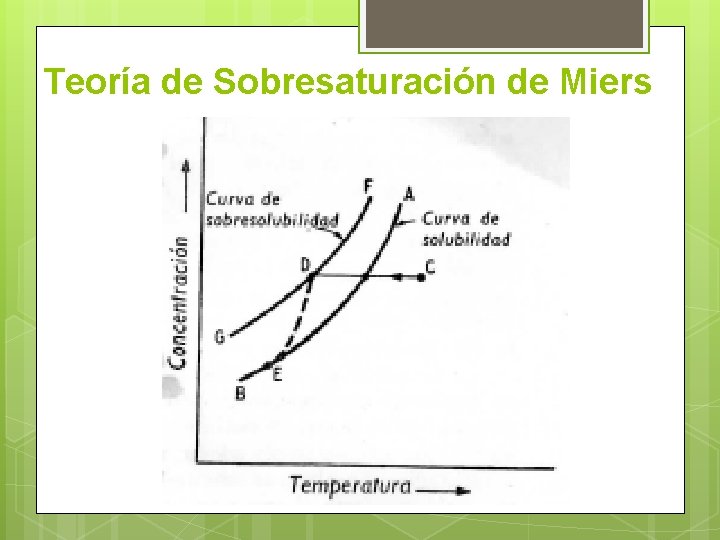
Teoría de Sobresaturación de Miers

Zona Metaestable El tiempo necesario para el origen de las partículas de la nueva fase es largo. La solución es estable Se forman una cantidad despreciables de cristales y después de un largo tiempo. No se produce formación espontanea.

Zona Metaestable Varía en función de: Valencia del anión y catión de la sal, crece. n° de moléculas de agua de hidratación en la sal de formación, crece. Historia térmica de la dilución, crece Contenido de impurezas, ej: polímeros orgánicos, crece; Influencia mecánicas, disminuye. Volumen, crece a menor volumen. Viscosidad, crece a mayor volumen.

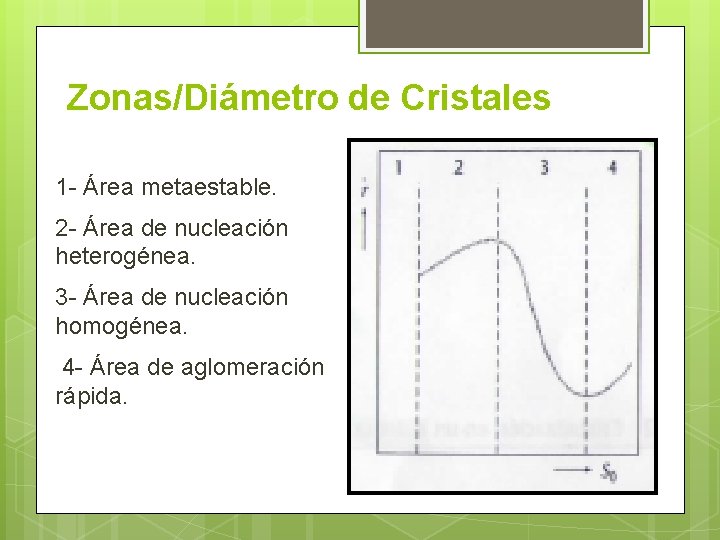
Zonas/Diámetro de Cristales 1 - Área metaestable. 2 - Área de nucleación heterogénea. 3 - Área de nucleación homogénea. 4 - Área de aglomeración rápida.

Aditivos

Aditivos Cambian la velocidad de nucleación y crecimiento, el tamaño, morfología de los cristales y propiedades físicas del producto. Mecanismo: Se absorben en determinada sup. cristalinas y bloquean lugares activos de crecimiento. Cambian la solubilidad de la sustancia. Las propiedades de disolución. Se incorporan al volumen del cristal en crecimiento. Interacción química.

Aditivos Influencia en la nucleación: homogénea: se absorben en la sup. de los gérmenes en formación, disminuye el n° de gérmenes que llegan a la dimensión crítica. heterogénea: interacción entre aditivo y la fase sólida ajena. Cambia la tensión superficial entre cada una de las fases. Influencia en el crecimiento cristalino: reducción de la velocidad de crecimiento, absorción en la superficie del cristal, fuerzas físicas o químicas.

Aditivos Ácidos o Bases Libres: cambian el p. H de la disolución que cristaliza. Aditivos Inorgánicos: altamente y pocos activos, cationes de metales, Fe+3, Cr+3. Aditivos Orgánicos: sustancias superficialmente activas y colorantes orgánicos. 10 -4 hasta 10 -6 moles.

Procesos Secundarios

Procesos Secundarios Cambian la propiedades físicas y químicas de la fase sólida. Recristalización Agregación Envejecimiento

Recristalización Isotérmica Cambio en la dimensión y forma de los cristales. Solución madre en contacto con partículas de diferentes tamaños, r 1, r 2 y r 3, equilibrio con las partículas con una dimensión r 2. Maduración de Ostwald.

Recristalizción No Isotérmica La solubilidad no depende del tamaño de los cristales. Consecuencia de oscilaciones de temperatura y concentración o solubilidad dependiendo del grado de perfección de sus redes Consecuencia, crecimiento de la dimensión media de los cristales.

Agregación Disminución del grado de dispersión del sistema como consecuencia de la agrupación de partículas. Coagulación-Agregación. Dependiente de las fuerzas que actúan entre las partículas de la fase sólida, eléctricas de repulsión y atracción Londo-Van der Waals. Proporcional al potencial químico y capa de hidratación de la partícula. Agentes deshidratantes. Temperatura.

Envejecimiento Cambios en las propiedades físicas de la fase sólida y de su composición química, muy lento. Las partículas de la fase metaestable se disolverán. Los cristales adquieren formas similares al equilibrio.

Equipamiento

Clasificación Según método en que se lleva a cabo la sobresaturación: Por enfriamiento Por evaporación del disolvente. Por evaporación adiabática (evap + enfri) Adición de solubilidad. sustancias que reducen la

Clasificación 1 - únicamente con sustancias con curva de solubilidad que desciende apreciablemente. 2 - principal aplicación en la sal corriente. 3 - método mas importante para producción a escala. 4 - No utilizado con frecuencia, sol electrolíticas de soda cáustica, jabones de glicerina

Clasificación Por enfriamiento únicamente: Proceso discontinuo Depósito de cristalización. Discontinuos Proceso con agitación. continuo Swenson-Walker. Otros tipos.

Clasificación Por enfriamiento adiabático: Cristalizadores al vacío Sin clasificación externa de lecho sembrado. Con clasificación externa de lecho sembrado. Por evaporación: Evaporadores de sales Evaporadores Krystal

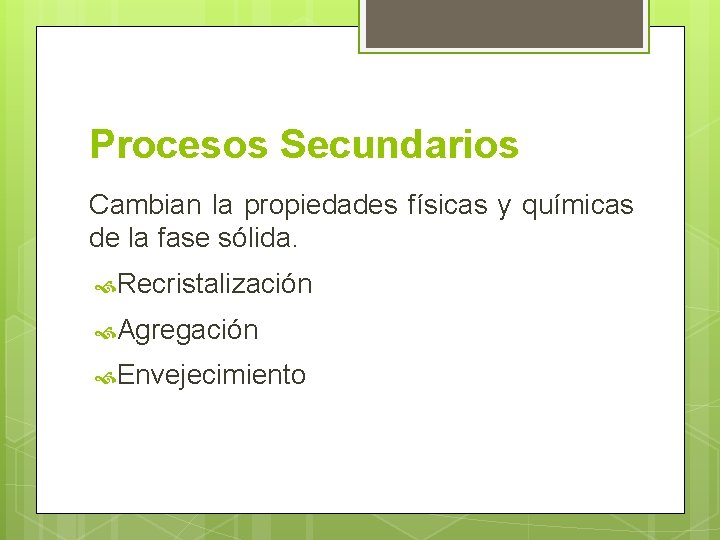
Cristalizadores discontinuos agitados

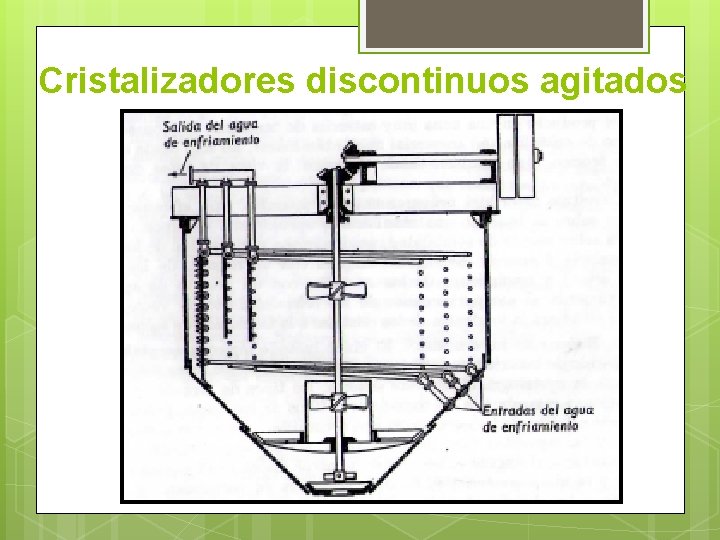
Swenson – Walker

Swenson – Walker

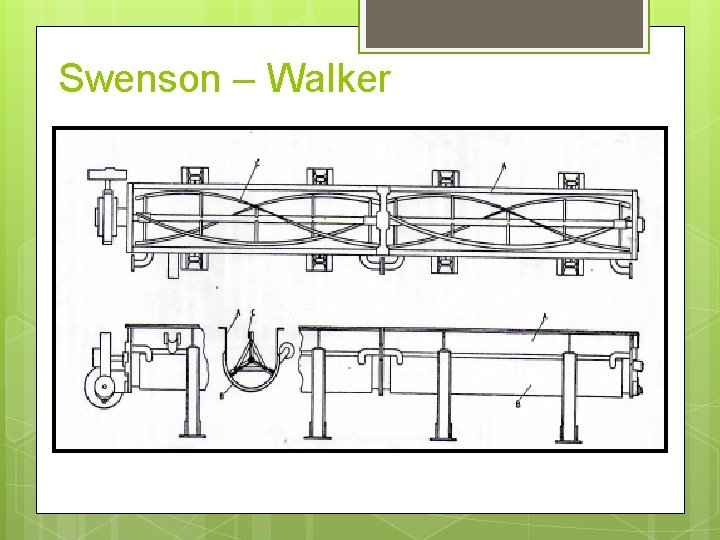
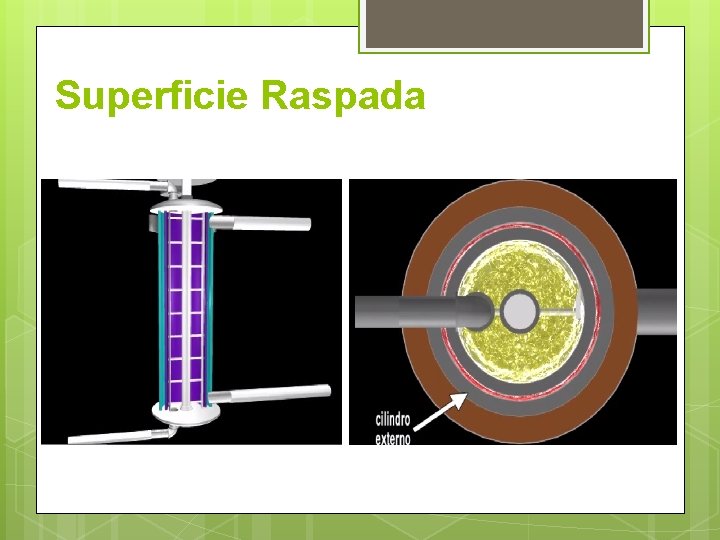
Superficie Raspada

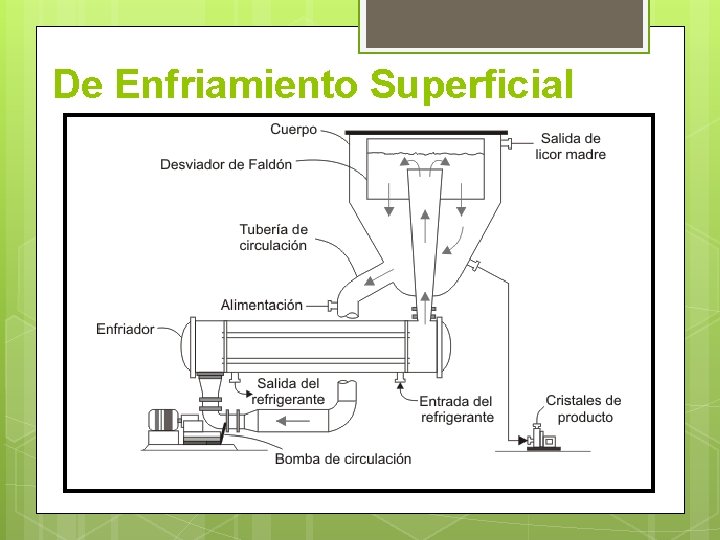
De Enfriamiento Superficial

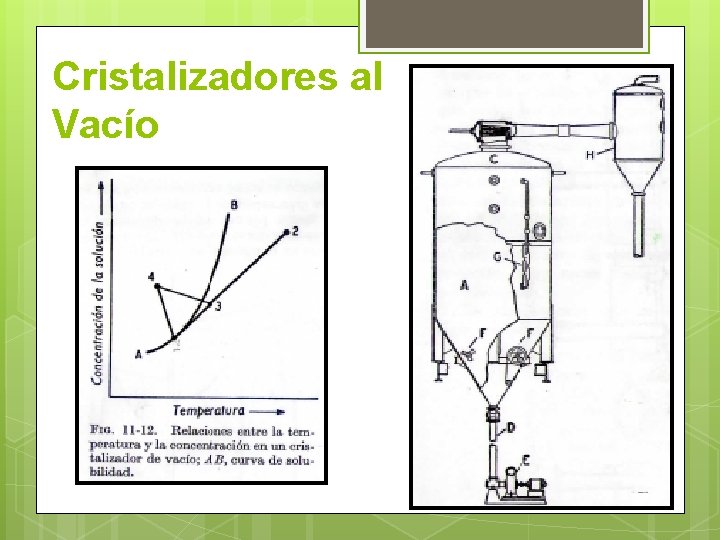
Cristalizadores al Vacío

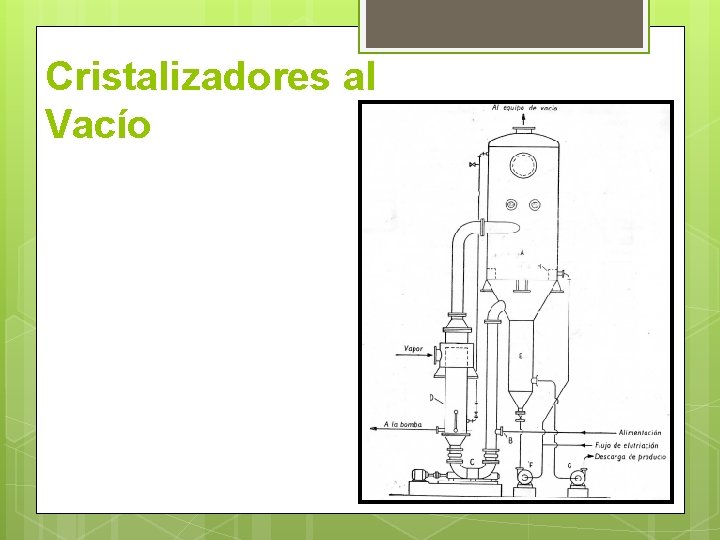
Cristalizadores al Vacío

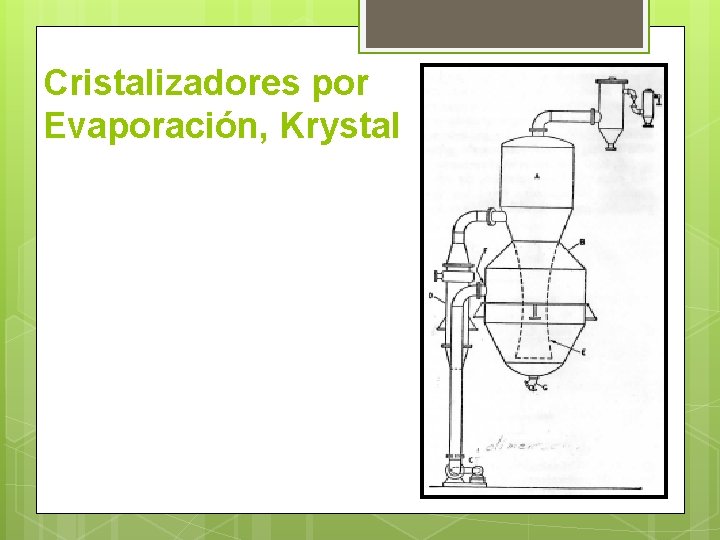
Cristalizadores por Evaporación, Krystal

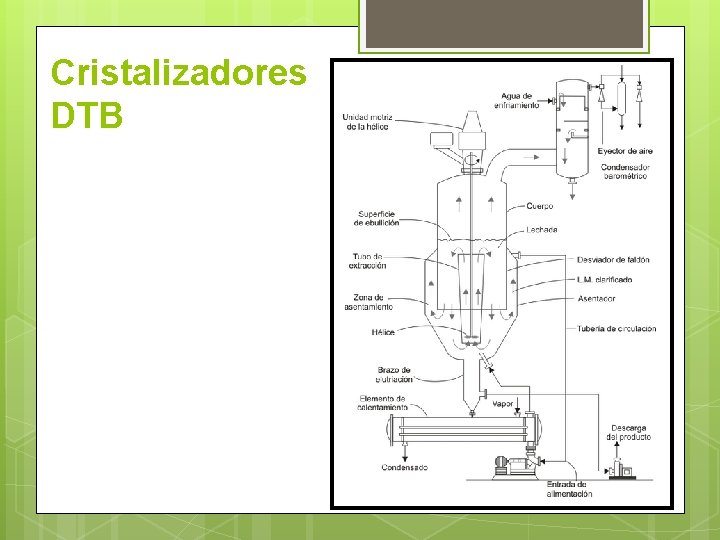
Cristalizadores DTB

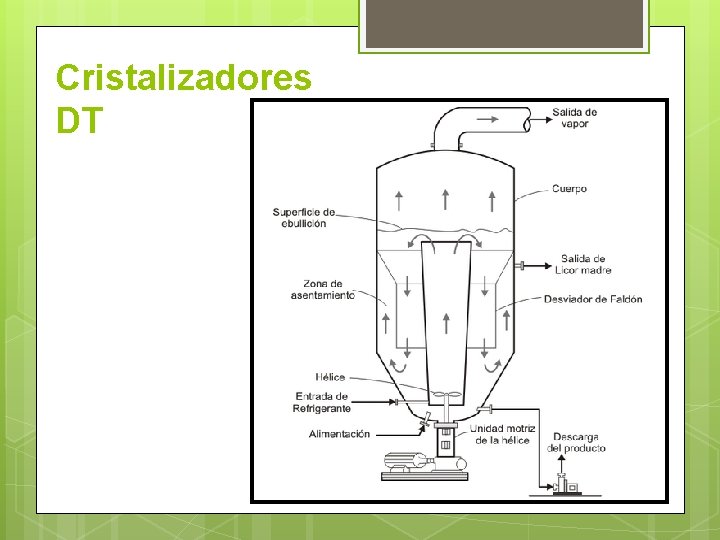
Cristalizadores DT

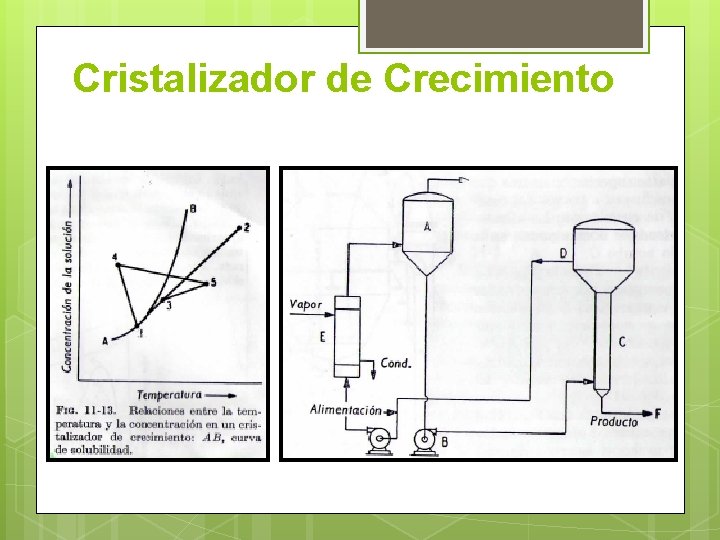
Cristalizador de Crecimiento

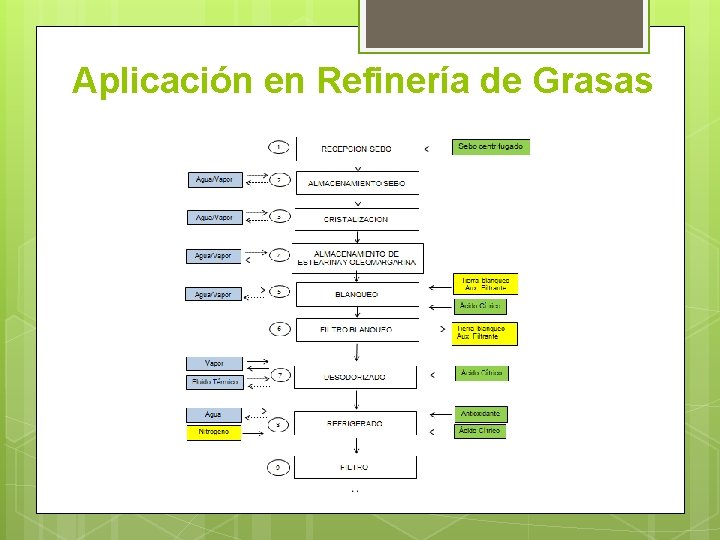
Aplicación en Refinería de Grasas

Aplicación en Refinería de Grasas

Aplicación en Refinería de Grasas

Aplicación en Refinería de Grasas

Aplicación en Refinería de Grasas

Aplicación en producción de azúcar La evaporación del agua se realiza manteniendo calor constante hasta que el jugo de la caña se convierta en miel (la operación de concentración se inicia aproximadamente a partir de los 98 a 100 º C). Cuando la miel alcanza la temperatura de punteo (120 ó 126 °C), se retira de la fuente de calor y se trasvasa a la batidora.

Aplicación en producción de azúcar Con ayuda de una batidora industrial eléctrica monofásica se agita la miel por un tiempo aproximado de 10 minutos hasta lograr una granulación total

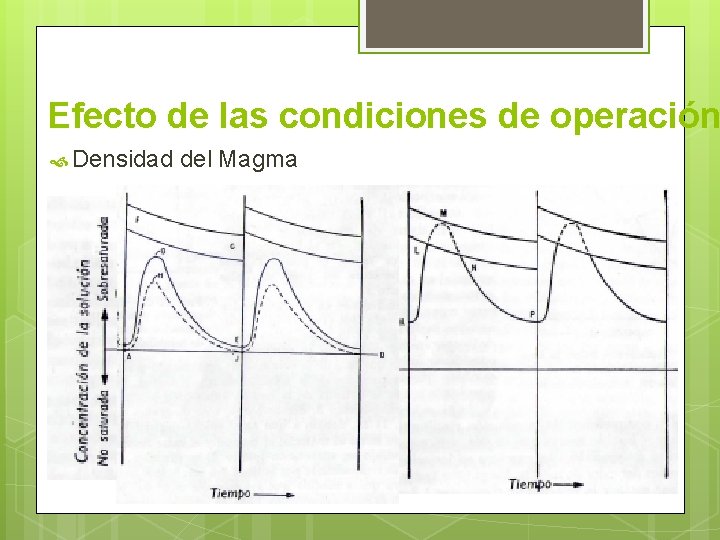
Efecto de las condiciones de operación Densidad del Magma

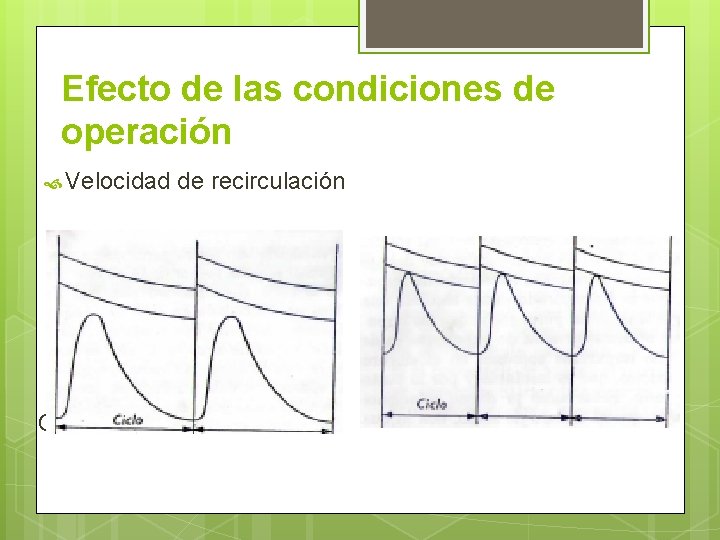
Efecto de las condiciones de operación Velocidad de recirculación Cristalizador al vacío

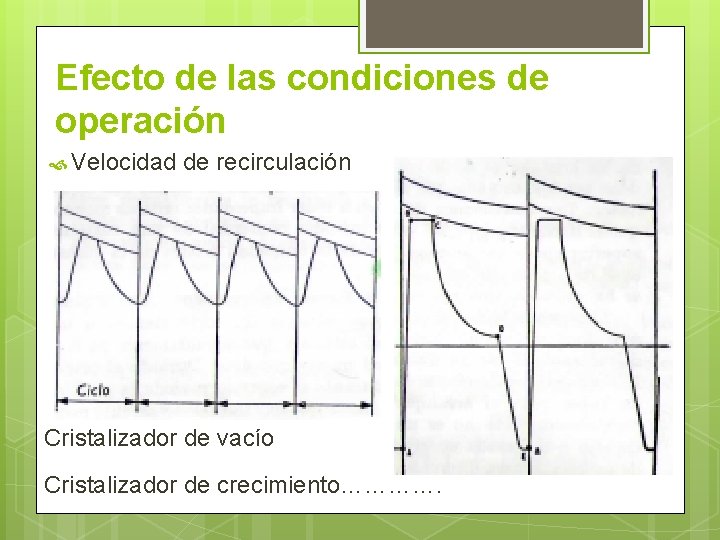
Efecto de las condiciones de operación Velocidad de recirculación Cristalizador de vacío Cristalizador de crecimiento………….

Efecto de las condiciones de operación Limitaciones Relación de volumen cristales/magma extraído. Permitir el bombeo, 1/4 o 1/2 Temperatura, al disminuir T aumenta rendimiento, volumen de la cabeza de vapor aumenta. T según coste mínimo total.

Efecto de las condiciones de operación Limitaciones Humedad Critica Absorción de agua hasta disolución. Impurezas. Aglomerados Humedad crítica alta. Granos de tamaño uniforme. Revestimiento, polvos inertes.

¿Como elegir un Cristalizador? Primero: Elegir un medio de generación de sobresaturación en base a las características de las curvas de solubilidad-temperatura de las sustancia a cristalizar. Segundo: Decidir si la cristalización sera batch o continuo Tipo y tamaño de cristales a producir. Características físicas de la alimentación. Resistencia a la corrosión

Factores a Considerar 1 - Poder del solvente: disolver el soluto y permitir después la obtención de cristales. 2 -Pureza: No debe introducir impurezas que afecten la apariencia y propiedades del cristal. 3 - Reactividad Química: Debe ser estable. 4 - Manejo y procesamiento: Poco viscoso y con temperatura de fusión debajo de 5°C. De baja inflamabilidad y toxicidad.

Criterios Para Especificar un Cristalizador 1 - El cristal será anhidro o hidratado? 2 - Cual es la solubilidad del compuesto en el solvente y como cambia con la temperatura? 3 - Hay otros compuesto que coprecipiten con el producto? 4 - Cual será el efecto de impurezas en la solución, en el hábito, el crecimiento, y la velocidad de nucleación de los cristales? 5 - Cuales son las propiedades físicas y su tendencia a formar espuma?

Criterios Para Especificar un Cristalizador 6 7 - Cuál es el calor de cristalización del producto? Cuál es la velocidad de producción? 8 - Cuál es la tendencia del material a crecer en las paredes del cristalizador? 9 - Que material de construcción se pueden utilizar para entrar en contacto con la solución a varias temperaturas? 10 - El producto final se mezclara o estará mezclado permanentemente con otros materiales o sólidos cristalinos?

Referencias DR. F GRASES FREIXEDAS. “Cristalización en disoluciones”. Editorial Reverté SA. GEANKOPLIS. “Procesos de Transporte y Operaciones Unitarias”. 12 CECSA. BADGER; BANCHERO. “ Introducción a la Ingeniería Química”. Ediciones del Castillo. PERRY. “Manual del Ingeniero Químico”. Capítulo 18. Mc Graw Hill. KING J. “Procesos de Separación”. Capítulo 1. Ediciones Repla. FOUST, A. “Principios de Operaciones Unitarias”. Capítulo 11. Continental S. A. México. 1997. http: //www. textoscientificos. com/quimica/cristales/cristalizadores http: //www. ecoplanning. fi/files/img/media/Ecoplanning_brochure_2013_ESP. pdf Manual para ingenieros azucareros, por E HUGOT