Tema 7 Reaccions cidbase Tema 2 Termoqumica Tema

Tema 7 Reaccions àcid-base
Tema 2 Termoquímica Tema 3 Espontaneïtat Tema 4 Equilibri Desprén calor? Quina quantitat? Per què es produeix? En quina direcció? Quan s’arriba? Com es modifica? Tipus Reaccions químiques Tema 10 Cinètica Tema 11 Mecanismes Quina velocitat té? Té diverses etapes? De què depén? Com l’accelerem? Tema 5 Eq. de fases Tema 7 Eq. àcid-base Tema 6 Dissolucions Tema 8 Eq. solubilitat Tema 9 Eq. redox

“Probablemente no haya otro tipo de equilibrio tan importante como el de ácidos y bases” B. M. Mahan i R. J. Myers Química. Curso Universitario (4ª ed. ).

CONTINGUT 1. - Definicions d’àcids i bases. 2. - L’autoionització de l’aigua. Escala de p. H. 3. - Força d’àcids i bases. Constants d’ionització. 4. - Indicadors. 5. - Tractament exacte dels equilibris d’ionització. 6. - Hidròlisi. 7. - Dissolucions amortidores. 8. - Corbes de valoració.

1 DEFINICIONS D’ÀCIDS I BASES. 1. 1. - Arrhenius (1883) Àcid: Substància que, en dissolució aquosa, dóna H+ HCl ® H+ (aq) + Cl- (aq) Base: Substància que, en dissolució aquosa, dóna OHNa. OH® Na+ (aq) + OH- (aq)

1903 Tercer premi Nobel de Química “En reconeixement als extraodinaris serveis que ha prestat al progrés de la química mitjançant la seua teoria electrolítica de la dissociació”. [http: // nobelprize. org /chemistry/laureates/1903/index. html] Svante August Arrhenius (1859 -1927) Limitacions: * Substàncies amb propietats bàsiques que no contenen ions hidroxil (p. ex. : NH 3 líquid) * Es limita a dissolucions aquoses. Es requereix una perspectiva més general

1. 2. - Brønsted-Lowry (1923) Àcid: Espècie que té tendència a cedir un H+ Base: Espècie que té tendència a acceptar un H+ CH 3 COOH (aq) + H 2 O (l) « H 3 O+ (aq) + CH 3 COO- (aq) àcid base Transferència protònica Parell àcid-base conjugat Avantatges * Ja no es limita a dissolucions aquoses * S’explica el comportament bàsic de, p. ex. , NH 3 Substància anfòtera NH 3 (aq) + H 2 O (l) « NH 4+ (aq) + OH- (aq) (pot actuar com a àcid o com a base)

Johannes Nicolaus Brønsted (1879 -1947) Thomas Martin Lowry (1874 -1936)

1. 3. - Lewis (1923) Per a que una substància accepte un H+ ha de posseir un parell d’electrons no compartits. H H+ + : N H H + H H N H H Àcid: Espècie que pot acceptar parells d’electrons Base: Espècie que pot cedir parells d’electrons

El H+ és àcid de Lewis, però no és l’únic. La base pot cedir parells d’electrons a altres espècies Definició més general F H N: H + B H F F base àcid F H H N H B F F Gilbert Newton Lewis (1875 -1946)

2 L’AUTOIONITZACIÓ DE L’AIGUA. ESCALA DE p. H. Equilibri d’autoionització de l’aigua H 2 O (l) + H 2 O (l) « H 3 O+ (aq) + OH- (aq) Kw = [H 3 O+][OH-] Producte iònic de l’aigua A 25ºC, Kw = 10 -14 p. H = - log [H 3 O+] p. OH = - log [OH-] [Aplicant logaritmes i canviant el signe] - log 10 -14 = - log [H 3 O+] - log [OH-] 14 = p. H + p. OH
![Aigua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7 Aigua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7](http://slidetodoc.com/presentation_image_h/bf138a3fd79374990eb2efa19cdcc9f5/image-12.jpg)
Aigua pura: [H 3 O+] = [OH-] ; [H 3 O+] = 10 -7 Þ p. H = 7 [OH-] = 10 -7 Þ p. OH = 7 DISSOLUCIÓ NEUTRA DISSOLUCIÓ ÀCIDA DISSOLUCIÓ BÀSICA [H 3 O+] = [OH-] p. H = 7 [H 3 O+] > [OH-] p. H < 7 [H 3 O+] < [OH-] p. H > 7 àcida 7 bàsica p. H

3 FORÇA D’ÀCIDS I BASES. CONSTANTS D’IONITZACIÓ. Força d’un àcid o base: major o menor tendència a transferir o acceptar un protó. Mesura quantitativa: constant d’equilibri de la seua reacció amb aigua. HA(aq) + H 2 O (l) « H 3 O+ (aq) + A- (aq) Constant d’acidesa (de dissociació, d’ionització) Major força d’un àcid: major serà Ka (menor p. Ka) Cas extrem: àcid fort (p. ex. HCl, HNO 3, HCl. O 4, . . . ) es troba totalment dissociat (Ka >> 1, Ka ® ¥)

Anàlogament amb les bases: B (aq) + H 2 O (l) « BH+ (aq) + OH- (aq) Constant de basicitat Major força d’una base: major serà Kb (menor p. Kb) Cas extrem: base forta (p. ex. Na. OH, KOH, . . . ) es troba totalment dissociada (Kb >> 1, Kb ® ¥) En el cas d’un parell àcid-base conjugat, Ka i Kb estan relacionades B (aq) + H 2 O (l) « BH+ (aq) + OH- (aq) Kw = K a Kb

4 INDICADORS. Indicadors: Àcids o bases dèbils les formes àcid/base conjugades dels quals presenten colors diferents. HInd (aq) + H 2 O (l) « H 3 O+ (aq) + Ind- (aq) Color A Color B Quan a una dissolució li afegim un indicador, estaran presents les dos espècies HInd i Ind-.
![Quin color voré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma àcida) Quin color voré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma àcida)](http://slidetodoc.com/presentation_image_h/bf138a3fd79374990eb2efa19cdcc9f5/image-16.jpg)
Quin color voré? • Si [HInd]/[Ind-] ³ 10 Þ Color A (predomina forma àcida) • Si [HInd]/[Ind-] £ 0. 1 Þ Color B (predomina forma bàsica) • Si 0. 1< [HInd]/[Ind-]< 10 Þ Color mescla d’A i B El quocient depén de la Ka i del p. H: • Si [HInd]/[Ind-] ³ 10 Þ [H 3 O+] ³ 10 KInd Þ p. H £ p. KInd – 1 Color A (predomina forma àcida) • Si [HInd]/[Ind-] £ 0. 1 Þ [H 3 O+] £ 0. 1 KInd Þ p. H ³ p. KInd +1 Color B (predomina forma bàsica) • Si 0. 1< [HInd]/[Ind-]< 10 Þ p. KInd – 1 < p. H < p. KInd +1 Mescla A i B Interval de viratge (2 unitats de p. H)
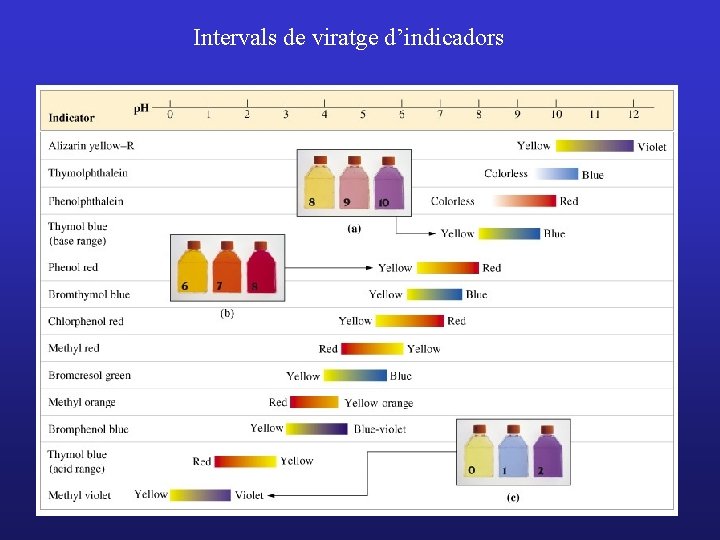
Intervals de viratge d’indicadors

5 TRACTAMENT EXACTE DELS EQUILIBRIS D’IONITZACIÓ. ¿Com podem calcular les concentraciones de totes les espècies presents en una dissolució en la que s’estableixen diversos equilibris d’ionització? MÈTODE GENERAL 1. 2. 3. 4. Expressions de les constants d’equilibri Balanç de matèria Balanç de càrregues (condició de electroneutralitat) Resolució del sistema d’equacions

P. ex. : equilibri d’ionització d’un àcid dèbil HA en aigua HA(aq) + H 2 O (l) « H 3 O+ (aq) + A- (aq) 1. Expressions de les constants d’equilibri Equilibris presents HA(aq) + H 2 O (l) « H 3 O+ (aq) + A- (aq) 2 H 2 O (l) « H 3 O+ (aq) + OH- (aq) Kw = [H 3 O+][OH-] 2. Balanç de matèria: [HA]o + [A-]o = [HA] + [A-] 3. Balanç de càrregues (condició de electroneutralitat) [H 3 O+] = [A-] + [OH-] 4. Resolver el sistema: 4 equacions amb 4 incògnites

6 HIDRÒLISI. Comportament àcid–base de les sals Neutres Àcides Bàsiques Com determinar-lo de forma qualitativa? 1. 2. 3. 4. Dissociar la sal en els seus ions Identificar la seua procedència Determinar quins poden hidrolitzar-se Plantejar i analitzar l’equilibri d’hidròlisi
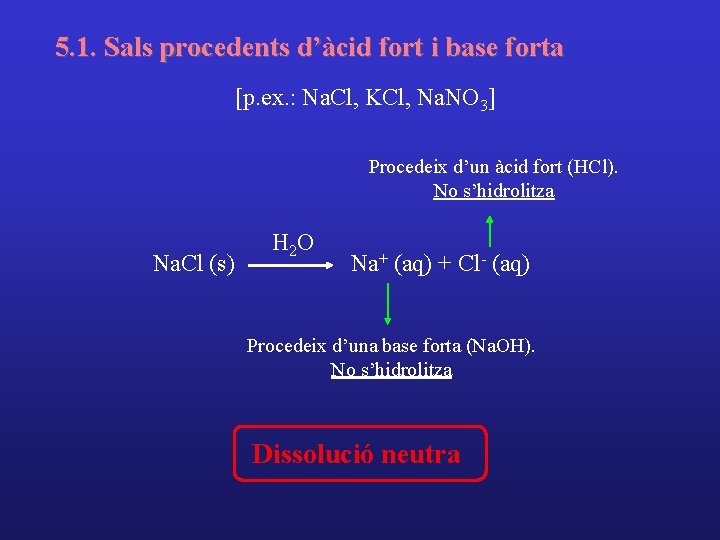
5. 1. Sals procedents d’àcid fort i base forta [p. ex. : Na. Cl, KCl, Na. NO 3] Procedeix d’un àcid fort (HCl). No s’hidrolitza Na. Cl (s) H 2 O Na+ (aq) + Cl- (aq) Procedeix d’una base forta (Na. OH). No s’hidrolitza Dissolució neutra

5. 2. Sals procedents d’àcid fort i base dèbil [p. ex. : NH 4 Cl] NH 4 Cl (s) H 2 O Procedeix d’un àcid fort (HCl). No s’hidrolitza NH 4+ (aq) + Cl- (aq) Procedeix d’una base dèbil (NH 3). S’hidrolitza NH 4+ (aq) + H 2 O (l) « NH 3 (aq) + H 3 O+ (aq) Dissolució àcida

5. 3. Sals procedents d’àcid dèbil i base forta [p. ex. : CH 3 COONa] CH 3 COONa (s) H 2 O Procedeix d’una base forta (Na. OH). No s’hidrolitza CH 3 COO- (aq) + Na+ (aq) Procedeix d’un àcid dèbil (CH 3 COOH). S’hidrolitza CH 3 COO- (aq) + H 2 O (l) « CH 3 COOH (aq) + OH- (aq) Dissolució bàsica

5. 4. Sals procedents d’àcid dèbil i base dèbil [p. ex. : NH 4 CN] Procedeix d’un àcid dèbil (HCN). S’hidrolitza NH 4 CN (s) H 2 O NH 4+ (aq) + CN- (aq) Procedeix d’una base dèbil (NH 3). S’hidrolitza Si Kh (catió) > Kh (anió) Þ Dissolució àcida Si Kh (catió) < Kh (anió) Þ Dissolució bàsica Si Kh (catió) = Kh (anió) Þ Dissolució neutra [Per al NH 4 CN: dissolució bàsica]

7 DISSOLUCIONS AMORTIDORES. Per a molts processos, el control del p. H resulta fonamental (p. ex. reaccions bioquímiques) Dissolucions amortidores (o tampó): Dissolucions que mantenen un p. H aproximadament constant quan s’agreguen xicotetes quantitats d’àcid o base o quan es dilueixen. Composició Quantitats substancials d’un àcid dèbil i de la seua base conjugada (o una base dèbil i el seu àcid conjugat). (p. ex. : CH 3 COOH/CH 3 COONa)

Mecanisme d’acció: HA (aq) + H 2 O (l) « H 3 O+ (aq) + A- (aq) Si a l’equilibri li afegesc, p. ex. , un àcid, es desplaçarà a l’esquerra, disminuirà el quocient [A-]/[HA] i el p. H baixarà. Però si la quantitat afegida és xicoteta comparada amb les quantitats (grans) que hi ha d’A- i HA, el quocient canviarà molt poc i el p. H gairebé no es modificarà. P. ex. : * si afegesc 0. 001 mols d’HCl a un 1 L d’aigua, el p. H passa de 7 a 3. * si afegesc 0. 001 mols d’HCl a un 1 L de dissolució que conté 0. 7 mols d’acètic i 0. 6 mols d’acetat sòdic, el p. H passa de 4. 688 a 4. 686.

Com calcular el p. H d’una dissolució tampó? Amb el tractament exacte (apartat 5). Com estimar aproximadament el p. H d’una dissolució tampó? Exacta Com que les concentracions inicials d’àcid i de la seua base conjugada són grans, es pot suposar que les quantitats que desapareixeran i que apareixeran mentre s’aconsegueix l’equilibri seran xicotetes, comparades amb les inicials. Per tant, en la fórmula anterior les concentracions en l’equilibri es poden aproximar per les concentracions inicials. Equació de Henderson-Hasselbalch Aproximada

Lawrence Joseph Henderson (1878 -1942) Karl Albert Hasselbalch (1874 -1962)

Característiques importants d’una dissolució amortidora: * El seu p. H Þ depén de Ka i de les concentracions * La seua capacitat amortidora Capacitat amortidora: Quantitat d’àcid o base que es pot afegir a un tampó abans que el p. H comence a canviar apreciablement. De què depén? * Del nombre de mols d’àcid i base (han de ser alts per a que la capacitat també ho siga) * Del quocient [base]/[àcid]. (per a que la capacitat siga alta, ha de ser pròxim a 1. Si és < 0. 1 ó > 10, no serà molt eficient. Major eficiència: quan p. H = p. Ka)

8 VALORACIONS ÀCID-BASE. Com podem determinar la concentració d’un àcid o d’una base en una dissolució? Mètode més utilitzat: valoració àcid-base Una dissolució que conté una concentració coneguda de base (o àcid) es fa reaccionar amb una dissolució d’àcid (o de base) de concentració desconeguda. Mesurem el volum de la dissolució de base (o àcid) necessari per a que consumisca (neutralitze) tot l’àcid (o base). Quan s’aconsegueix la neutralització completa: Punt d’equivalència
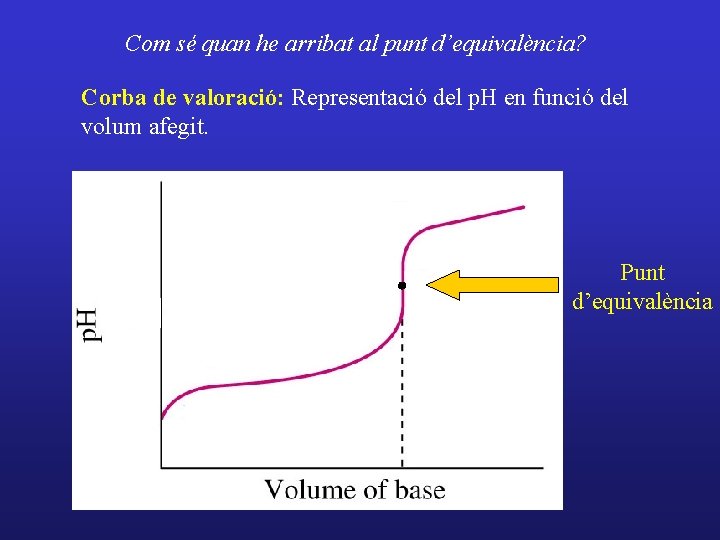
Com sé quan he arribat al punt d’equivalència? Corba de valoració: Representació del p. H en funció del volum afegit. Punt d’equivalència

Quin és el p. H del punt d’equivalència? • Si valore àcid fort amb base forta (o a l’inrevés) Þ p. H = 7 • Si valore àcid dèbil amb base forta Þ p. H > 7 • Si valore base dèbil amb àcid fort Þ p. H < 7 Com calcular el p. H d’eixe punt o de qualsevol punt de la corba? Amb el tractament exacte (apartat 5). Com sé que he arribat al punt d’equivalència sense necessitat de representar la corba de valoració sencera? Mitjançant un indicador apropiat Apropiat: que canvie de color just quan la reacció arriba al punt d’equivalència.
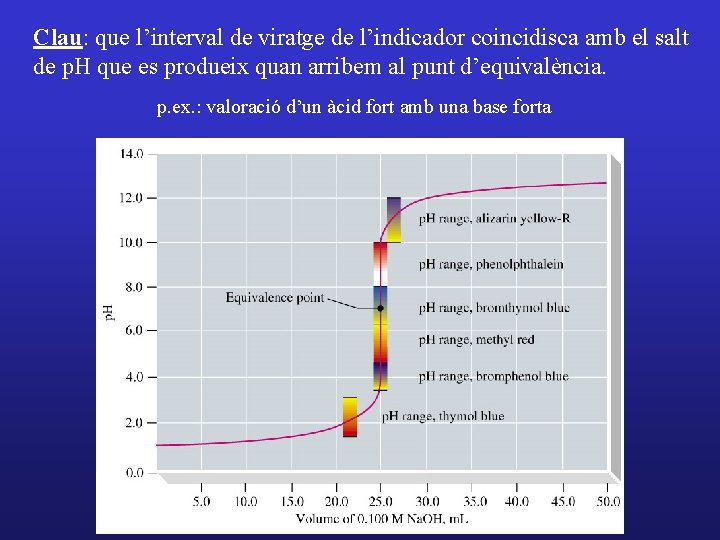
Clau: que l’interval de viratge de l’indicador coincidisca amb el salt de p. H que es produeix quan arribem al punt d’equivalència. p. ex. : valoració d’un àcid fort amb una base forta
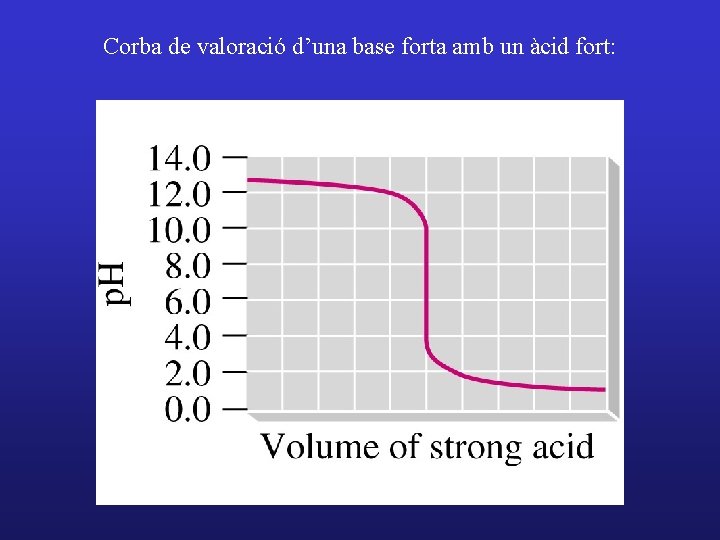
Corba de valoració d’una base forta amb un àcid fort:
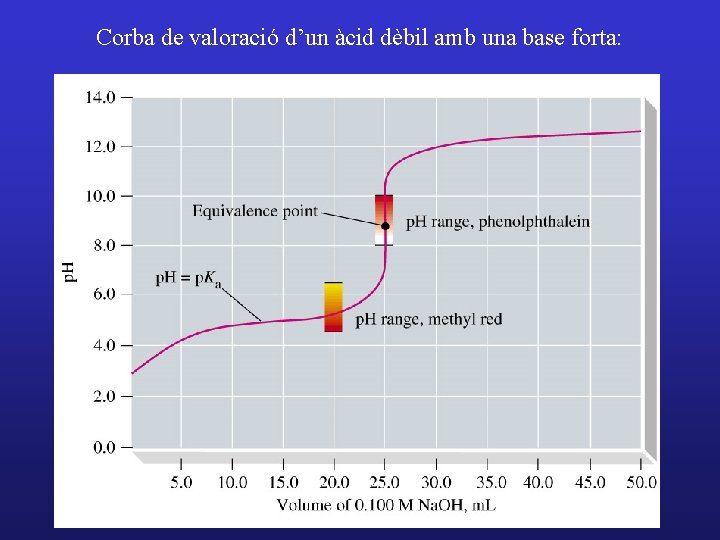
Corba de valoració d’un àcid dèbil amb una base forta:
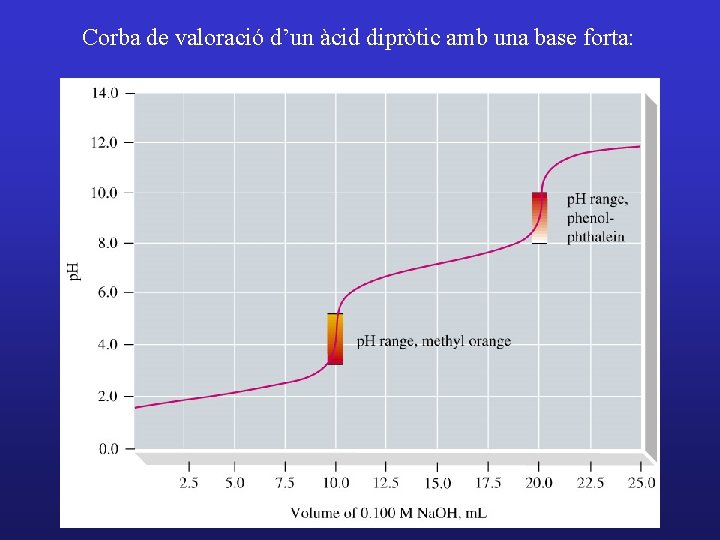
Corba de valoració d’un àcid dipròtic amb una base forta:
- Slides: 36