Programa institucional de tecnovigilancia Qu es Estrategia de




















- Slides: 23

Programa institucional de tecnovigilancia

¿Qué es? “Estrategia de vigilancia post mercado y evaluación sanitaria, para la identificación, gestión y comunicación oportuna de los eventos o incidentes adversos que presentan los dispositivos médicos durante su uso, con el fin de mejorar la protección de la salud y la seguridad de los pacientes, usuarios y todo aquel que se vea implicado directa o indirectamente con la utilización de DISPOSITIVOS MEDICOS. ” Resolución 4816 de 2008, articulo 4

¿Qué es un dispositivo medico ? Cualquier instrumento, aparato, máquina, software, equipo biomédico utilizado en atención en salud.

Equipo biomédico Dispositivo médico operacional y funcional que reúne sistemas y subsistemas eléctricos, electrónicos o hidráulicos.

Evento Adverso Daño no intencionado al paciente u operador que ocurra como consecuencia del uso de un dispositivo medico. Incidente Adverso Potencial daño no intencionado al paciente u operador que ocurra como consecuencia del uso de un dispositivo medico.

Fuente de eventos e incidentes adversos

Clasificación de riesgo de los dispositivos biomédicos Se fundamenta en los riesgos potenciales relacionados con el uso y en criterios tales como, duración del contacto con el cuerpo, grado de invasión y efecto local contra efecto sistémico. CLASE Clasificación de riesgo I Riesgo bajo IIA Riesgo moderado IIB Riesgo alto III Riesgo muy alto

Clase I Dispositivos médicos de bajo riesgo, sujetos a controles generales. No representan un riesgo potencial no razonable de enfermedad o lesión.

Clase IIa Son los dispositivos médicos de riesgo moderado, sujetos a controles especiales en la fase de fabricación para demostrar su seguridad y efectividad.

Clase IIb Son los dispositivos médicos de riesgo alto, sujetos a controles especiales en el diseño y fabricación para demostrar su seguridad y efectividad.

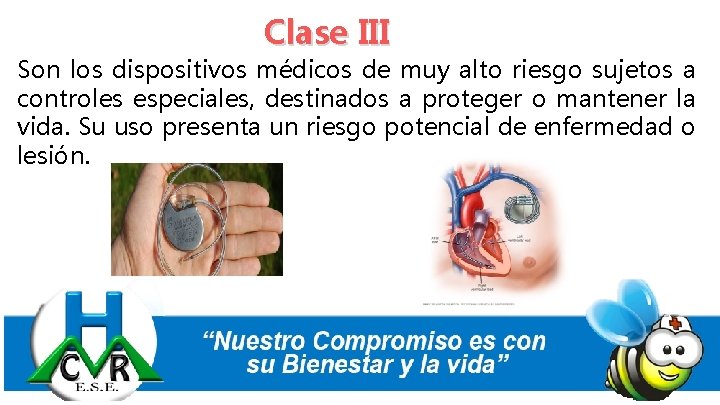
Clase III Son los dispositivos médicos de muy alto riesgo sujetos a controles especiales, destinados a proteger o mantener la vida. Su uso presenta un riesgo potencial de enfermedad o lesión.

Importancia del reporte ü Seguridad al paciente. ü Prevenir riesgo de infecciones. ü Prevenir que un incidente se convierta en un evento adverso. ü Evita daños a equipos. El reporte de eventos una cultura que fomenta la seguridad

¿Como participar en la cultura del reporte ? ü A través del formato de reporte definido institucionalmente (PANACEA). ü En caso de fallo en la plataforma, reportar a través del formato de reporte de eventos o incidentes adversos de equipos y dispositivos médicos.

Formato de reporte institucional

Datos relevantes del dispositivo/ equipo biomédico Para conservar la trazabilidad del evento o incidente es necesario conocer los siguientes datos: ü Nombre del equipo o dispositivo involucrado. ü Marca, modelo, serie/lote. ü Descripción de lo ocurrido. ü Detección del evento.

Riesgos de ECG Mal diagnostico: Desajuste de parámetros El equipo no es apto para ser usado debido a golpes o caídas Infecciones: Mala limpieza y desinfección de las chupas y pinzas. Riesgo eléctrico: Malas conexiones eléctricas.

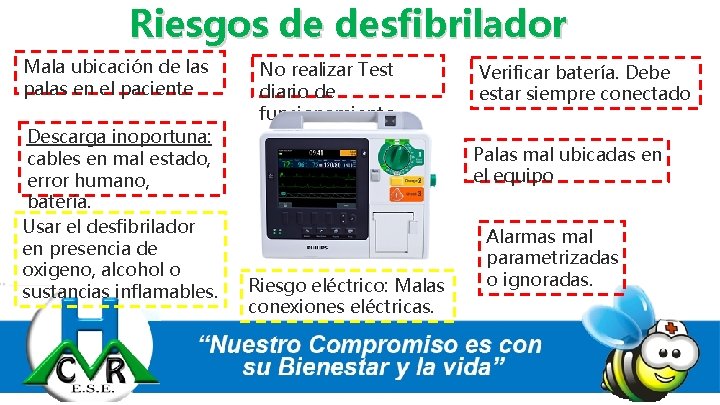
Riesgos de desfibrilador Mala ubicación de las palas en el paciente Descarga inoportuna: cables en mal estado, error humano, batería. Usar el desfibrilador en presencia de oxigeno, alcohol o sustancias inflamables. No realizar Test diario de funcionamiento Verificar batería. Debe estar siempre conectado Palas mal ubicadas en el equipo Riesgo eléctrico: Malas conexiones eléctricas. Alarmas mal parametrizadas o ignoradas.

Riesgos de Maquina de anestesia Falla de alarmas visuales y auditivas: Alarmas mal parametrizadas o ignoradas. Falta de oxigeno: • Conexiones inadecuadas • Desconexión del circuito del paciente • Problemas en la planta de oxigeno Reabsorción de CO 2: Falta del cambio de la cal Fugas en el equipo: Fallas en el circuito del paciente por rehúso, daño de algún componente neumático Explosión espontanea de oxígeno: • Contacto de oxígeno con materiales aceitosos o grasas • Equipos que producen chispas usados muy cercas del oxígeno

Riesgos de Ventilador mecánico Falla de alarmas visuales y auditivas: Alarmas mal parametrizadas o ignoradas. Falla en el blender: La alimentación de los gases con una presión diferente dispuesta por el fabricante, por ejemplo cuando se conecta al flujometro. No entrega la correcta concentración. Fugas en el equipo: Fallas en el circuito del paciente por rehusó, daño de algún componente neumático. Falta de uso de humidificadores: laceraciones en las vías respiratorias de neonatos

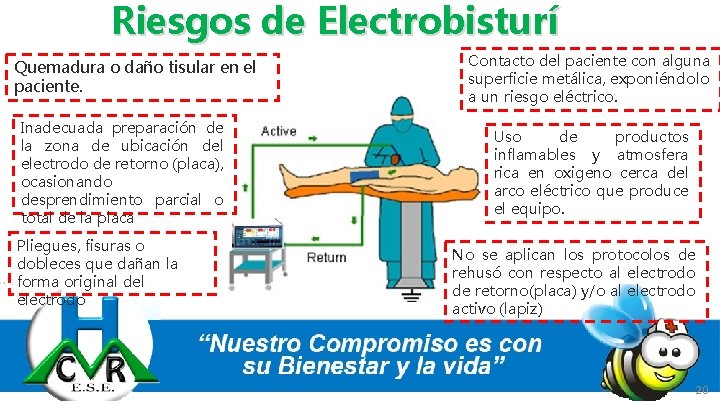
Riesgos de Electrobisturí Quemadura o daño tisular en el paciente. Inadecuada preparación de la zona de ubicación del electrodo de retorno (placa), ocasionando desprendimiento parcial o total de la placa Pliegues, fisuras o dobleces que dañan la forma original del electrodo Contacto del paciente con alguna superficie metálica, exponiéndolo a un riesgo eléctrico. Uso de productos inflamables y atmosfera rica en oxigeno cerca del arco eléctrico que produce el equipo. No se aplican los protocolos de rehusó con respecto al electrodo de retorno(placa) y/o al electrodo activo (lapiz) 20

Riesgos de Bomba de infusión Suministro inadecuado de medicamentos por inadecuada programación de la infusión: El operario introduce un inadecuado programa infusión. Elde equipo no es apto para ser usado debido a golpes o caídas. El equipo no responde debido a que los cables o baterías se encuentran en mal estado. Riesgo de golpe por caída Riesgo eléctrico: Malas conexiones eléctricas. Alarmas ignoradas

Riesgos de Monitor de signos vitales Presión excesiva del brazalete: Brazalete en mal estado y le colocan esparadrapo, mala programación de insuflado. Riesgo de golpe por caída Riesgo eléctrico: Malas conexiones eléctricas. Acciones retrasadas o falta de atención oportuna al paciente Falso diagnostico: Falla en accesorios, interferencia electromagnética por celulares Lesión en la piel: no se realiza el cambio periódico de electrodos Alarmas mal parametrizadas o ignoradas
