SVEUILITE U ZAGREBU Fakultet kemijskog inenjerstva i tehnologije

SVEUČILIŠTE U ZAGREBU Fakultet kemijskog inženjerstva i tehnologije Zavod za tehnologiju nafte i petrokemiju Zagreb, Savska cesta 16 / II NAFTNO-PETROKEMIJSKO INŽENJERSTVO Prof. dr. sc. Katica Sertić - Bionda

KATALITIČKO KREKIRANJE • proces toplinske razgradnje ugljikovodika uz sudjelovanje katalizatora (zeoliti), s ciljem pretvorbe CH iz višeg destilacijskog područja u frakciju benzina, uz ostale produkte (mehanizmi reakcija karbokationa) Razvoj: Period Proces Namjena < 1928. Toplinsko krekiranje benzin, olefini 1928. E. Houdry: reaktor s fiksnim slojem katalizatora: glina (obrada s H 2) veći prinos benzina bolja kvaliteta 1930 -35. Reaktor s fluidiziranim slojem (FCC), Si-Al amorfni kat. kontinuirani proces

KATALITIČKO KREKIRANJE Period Proces Namjena 1935 -50. FCC - optimiranje procesa postaje najvažniji sekundarni proces prerade 1960. Zeolitni katalizatori aktivnost. kat. , (sintetski kristalni Al - silikati) velika bolja selektivnost, manje nastajanje koksa 1970. Poboljšanje konstrukcije konstruk. reaktora jednostavnija
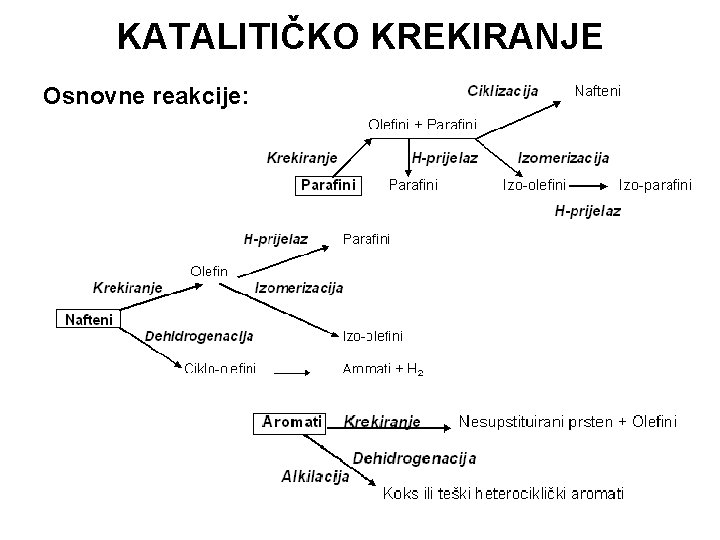
KATALITIČKO KREKIRANJE Osnovne reakcije:

KATALITIČKO KREKIRANJE Katalizatori: • Nekad: amorfni aluminosilikati s niskim ( 13%) ili visokim ( 27%) udjelom Al 2 O 3. • Danas: katalizatori zeolitnog tipa, općenitog sastava: ( R’ R 2 ) O · Al 2 O 3 · n Si. O 2 · m H 2 O R’. . . kationi rijetkih metala R. . . kationi alkalijskih metala n = 2 -12 H 2 O 2%

KATALITIČKO KREKIRANJE • Zamjena Si s Al - daje anionski karakter kiselog centra ( Al O 4 - ). Nastali H+ ioni adiraju se na = vezu olefina - karbokation • Ravnoteža naboja - Na+ionima - mala katalitička aktivnost • Kationi elemenata rijetkih metala (Y, La, Ce. . . ) povećavaju aktivnost i stabilnost katalizatora Lewis-ov kiseli centar Brősted-ov kiseli centar

KATALITIČKO KREKIRANJE Struktura zeolita: • Trodimenzionalne mreže (Si. O 4)4 - i (Al. O 4)5 - tetraedara, povezanih preko atoma kisika primarne strukturne jedinice koje stvaraju sekundarne strukturne jedinice, čijom kombinacijom nastaju trodimenzionalne prostorno mrežaste strukture zeolita. • Y - zeolit oktaedarske jedinice, međusobno povezane preko heksagonalnih ploha u globalnu strukturu zeolita.

KATALITIČKO KREKIRANJE • Y- zeolit - veličina pora: 0. 8 -0. 9 nm, Si. O 2/Al 2 O 3=3 -6 • X- zeolit - veličina pora: 0. 8 -1. 3 nm, Si. O 2/Al 2 O 3=2 -3 U odnosu na amorfne aluminosilikate karakterizira ih: visoka selektivnost ( i šupljine definiranih promjera ) velika aktivnost otpornost prema neugljikovodičnim spojevima ( otrovi S i N ) smanjena sklonost nastajanju koksa mogućnost podešavanja kiselosti (promjena omjera Si/Al), što omogućuje široku primjenu kao katalizatora.

KATALITIČKO KREKIRANJE Reakcijski mehanizam (mehanizam karbokationa): Nastajanje: 1. Vezanje H iona iz molekule alkana na Lewis-ov kiseli centar: 2. Adicija protona ( Brönsted-ov kiseli centar ) na = vezu olefina:

KATALITIČKO KREKIRANJE Reakcije: • Reaktivnost ugljikovodika u procesu katalitičkog krekiranja raste u nizu: – nesupstituirani aromati – parafini – polimetil aromati – nafteni – alkil benzeni ( s dužim bočnim lancima ) – olefini • Karbokationi - nastali iz molekula olefina i parafina na kiselim kat. aktivnim centrima - vrlo reaktivni • Brzine stvaranja i nestajanja ovise o njihovoj stabilnosti, koja opada u nizu: tercijarni sekundarni primarni
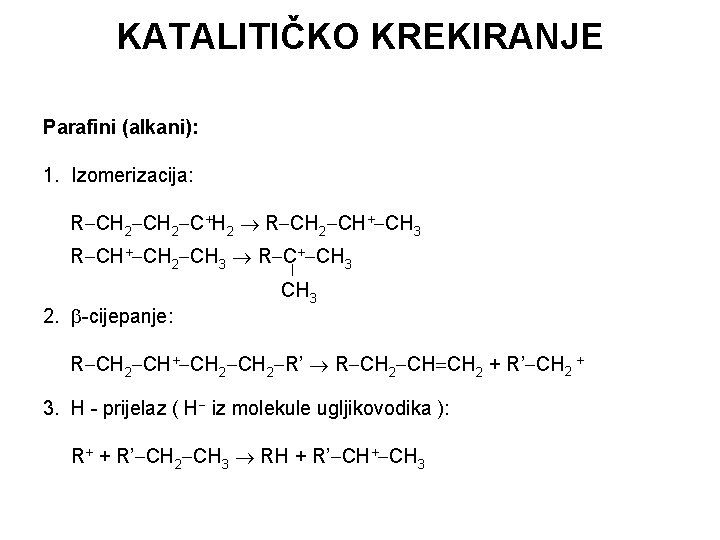
KATALITIČKO KREKIRANJE Parafini (alkani): 1. Izomerizacija: R CH 2 C+H 2 R CH 2 CH+ CH 3 R CH+ CH 2 CH 3 R C+ CH 3 2. -cijepanje: CH 3 R CH 2 CH+ CH 2 R’ R CH 2 CH CH 2 + R’ CH 2 + 3. H - prijelaz ( H iz molekule ugljikovodika ): R+ + R’ CH 2 CH 3 RH + R’ CH+ CH 3

KATALITIČKO KREKIRANJE Olefini (alkeni): - najreaktivniji ugljikovidici u procesu katalitičkog krekiranja. • konverzija u olefine manje molekulske mase (krekiranje) • izomerizacija - nastaje smjesa izomera. • reakcije prijelaza vodika: 3 Cn. H 2 n + Cn. H 2 m 3 Cn. H 2 n+2 + Cm. H 2 m-6 olefini naften parafini aromat

KATALITIČKO KREKIRANJE Nafteni (cikloparafini): 1. Deciklizacija: 2. Izomerizacija prstena: 3. Dehidrogenacija i dealkilacija:

KATALITIČKO KREKIRANJE Aromati: 1. Dealkilacija: 2. Premještanje metilnih skupina kod polimetilnih homologa benzena: 3. Kondenzacija - nastajanje kondenziranih policikličkih CH – koks

KATALITIČKO KREKIRANJE Termodinamika i kinetika: ∆G = ∆H - T ∆S -∆G = RTln K = - ∆G / R (1) (2) (3) Ako je ∆H pozitivna ( endotermna reakcija) - K se povećava s porastom temperature. • endotermne reakcije: krekiranje, dealkilacija, dehidrogenacija • egzotermne reakcije: prijelaz vodika, ciklizacija, izomerizacija Reakcijska smjesa ( plinsko ulje ) je vrlo kompleksna - kinetika procesa može se opisati uz pomoć modelnih reakcija. Reakcijske sheme uključuju karakteristične CH grupe (pseudokomponente ).

KATALITIČKO KREKIRANJE Primjer 1. Campbell i Wojciechowski: Plinsko ulje k 2 Plinovi + koks k 3 k 1 Benzin • Model pretpostavlja kinetičke izraze prvog reda za sve prisutne CH. -d. CA / dτ = ( k 1 + k 2 ) CA • τ. . prostorno vrijeme u nepokretnom katal sloju • CA. . . koncentracija reakt. ( plinsko ulje ) • k 1 i k 2 konstante brzine reakc.
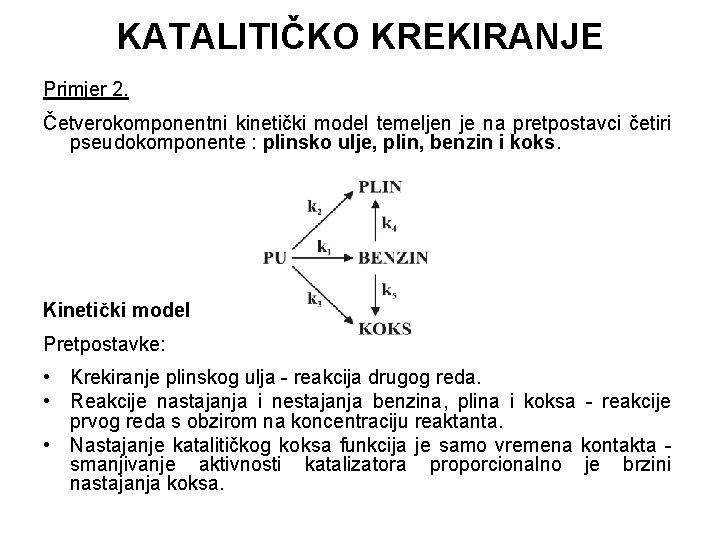
KATALITIČKO KREKIRANJE Primjer 2. Četverokomponentni kinetički model temeljen je na pretpostavci četiri pseudokomponente : plinsko ulje, plin, benzin i koks. Kinetički model Pretpostavke: • Krekiranje plinskog ulja - reakcija drugog reda. • Reakcije nastajanja i nestajanja benzina, plina i koksa - reakcije prvog reda s obzirom na koncentraciju reaktanta. • Nastajanje katalitičkog koksa funkcija je samo vremena kontakta smanjivanje aktivnosti katalizatora proporcionalno je brzini nastajanja koksa.

KATALITIČKO KREKIRANJE Jednadžbe brzina kemijskih reakcija u procesu krekiranja plinskog ulja dane su izrazima 1 do 4. Model obuhvaća 4 jednadžbe i 5 kinetičkih konstanti: • Nestajanje plinskog ulja: • Nastajanje benzina: • Nastajanje plinske frakcije: • Nastajanje koksa: • Funkcija deaktivacije katalizatora:

KATALITIČKO KREKIRANJE Popis oznaka • K konstanta, k 4 + k 5, s-1 • k 1 kinetička konstanta reakcije krekiranja plinskog ulja, gcat-1 cm 3 s-1 • k(2 -5) kinetičke konstante, s-1 • r(1 -4) brzina reakcije, gkatcm-3 s-1 • t vrijeme reakcije, • yi masenih udjeli komponenti • φ funkcija deaktivacije katalizatora • Ac konstanta funkcije deaktivacije katalizatora, -

KATALITIČKO KREKIRANJE Utjecaj procesnih parametara Fizikalno-kemijska svojstva katalizatora: 1. omjer Si / Al • Povećanje omjera Si/Al - smanjenje katalitičke aktivnosti i povećanje stabilnosti katal. • Smanjuje se gustoća katalitički aktivnih centara (Al) - naglašene reakcije krekiranja (monomolek. ) u odnosu na reakcije prijelaza vodika (bimolekul. ).

KATALITIČKO KREKIRANJE • Utjecaj: • niži prinosi benzina uz viši oktanski broj - IOB posebno povećavaju olefinski ugljikovodici. • manja sklonost stvaranju koksa (smanjeni udjeli reakcija prijelaza vodika). • viši prinosi plinske frakcije (naglašene reakcije krekiranja). Viši prinosi frakcije ukapljenog naftnog plina ( C 3 -C 4 ) - poželjni ako se frakcija UNP-a koristi kao sirovina u procesima alkilacije i dobivanja oksigenata ( MTBE ) - dodataka motornim benzinima radi povećanja OB.

KATALITIČKO KREKIRANJE 2. kationi rijetkih metala - RE 2 O 3 (eng. : rare earth; oksidi Y, La, Ce. . ) • • Veći sadržaj RE 2 O 3 u strukturi zeolita - povećava stabilnost i aktivnost katalizatora. Povećana gustoća katalitički aktivnih centara - uvjetovana djelovanjem RE 3+ kationa na polarizaciju molekula vode ( nastajanje H+ iona): RE 3+. . . H 2 O RE (OH)2+ + H+ Utjecaj: povećava se selektivnost katalizatora za reakcije prijelaza vodika u odnosu na reakcije krekiranja. Postižu se viši prinosi benzina (olefini se ne krekiraju u plin), ali povećana koncentracija parafina utječe na smanjenje oktanskog broja benzina. Prinosi plinske frakcije su niži ( manje zastupljeno krekiranje ), a koksa viši (povećano stvaranje aromata reakcijama prijelaza vodika - mogućnost kondenzacije, uz dehidrogenaciju ).

KATALITIČKO KREKIRANJE Fizikalna svojstva: 1. Otpornost prema trošenju • Trošenjem čestica zbog međusobnih sudara i sudara sa stjenkama reaktora i regeneratora (oštri uvjeti u regeneratoru) - prosječna veličina čestica se smanjuje. • Dio čestica može se pretvoriti u praškasti materijal i izgubiti preko ciklona-utjecaj na smanjenje aktivnosti cjelokupne katalitičke mase. 2. Specifična površina, volumen pora i nasipna gustoća • Specifična površina – određuje se postupkom adsorpcije dušika na dekoksiranom uzorku, a važan je parametar za praćenje aktivnosti i stabilnosti katalizatora. • Ukupna površina (m 2 g-1) - uključuje zeolitnu i matričnu komponentu. 1. Zeolitna površina - primarno krekira plinsko ulje i ključna je za selektivnost katalizatora, 2. Matrična površina - važna u krekiranju molekula velike molekulske mase (destilacijski ostaci).

KATALITIČKO KREKIRANJE 3. Raspodjela čestica • Svojstvo koje daje važne informacije o cirkulacijskim karakteristikama i karakteristikama trošenja katalizatora, kao i o radu ciklona. • Dobra cirkulacija katalizatora u FCC jedinici - postiže se kada čestice katalizatora imaju široku raspodjelu. • Tijekom rada procesa događaju se promjene u raspodjeli veličine čestica, kao i u drugim fizikalnim svojstvima. 4. Stabilnost katalizatora • Laboratorijski testovi termičke stabilnosti – provode se izlaganjem uzorka katalizatora utjecaju povišenih temperatura (540 i 8700 C) u određenom vremenskom periodu (3 -4 h). Utvrđuju se nastale promjene mjerenjem specifične površine i veličine jedinične ćelije (adsorpcijske metode, uz metodu difrakcije x-zraka).

KATALITIČKO KREKIRANJE Svojstva sirovine: • • Sirovine u procesu katalitičkog krekiranja su destilati višeg vrelišta (područje : 350 -5500 C ): 1. vakuum plinska ulja su standardne sirovine - mogućnost dodavanja ostataka 2. “teški” produkti sekundarnih procesa (koking, visbreaking, hidrokreking i sl. ). Sastav sirovine utječe na djelotvornost katalizatora - veći sadržaj policiklčkih CH u sirovini - veća vjerojatnost nastajanja koksa - brza deaktivacija katalizatora. Metali Ni i V - djeluju kao katalitički otrovi i promotori reakcija dehidrogenacije - nastajanje velike količine vodika (problemi u radu procesa i mogući utjecaj na prinose). • Potrebna hidroobrada sirovine (posebno ako su dodani ostaci) učinak smanjenog nastajanja koksa, uklanjanje S i N. • Fizikalno-kemijske značajke sirovine utječu na raspodjelu produkatalitičkog krekiranja - sirovine parafinskog tipa ( veći faktor K ) viši prinosi frakcije benzina.
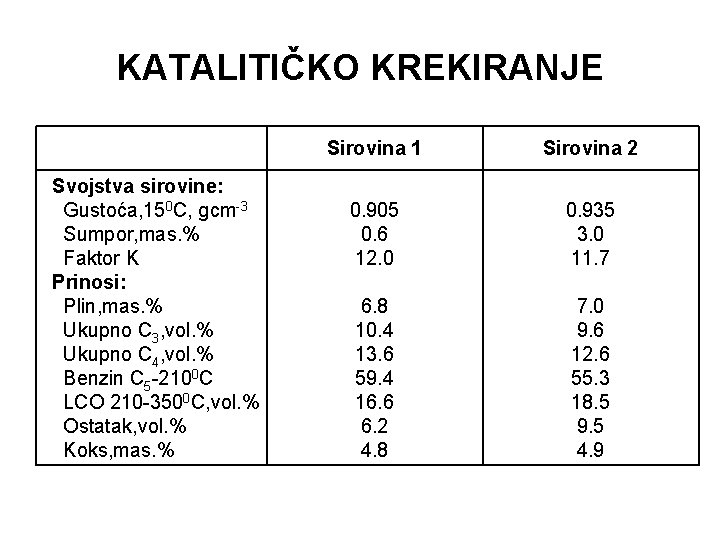
KATALITIČKO KREKIRANJE Svojstva sirovine: Gustoća, 150 C, gcm-3 Sumpor, mas. % Faktor K Prinosi: Plin, mas. % Ukupno C 3, vol. % Ukupno C 4, vol. % Benzin C 5 -2100 C LCO 210 -3500 C, vol. % Ostatak, vol. % Koks, mas. % Sirovina 1 Sirovina 2 0. 905 0. 6 12. 0 0. 935 3. 0 11. 7 6. 8 10. 4 13. 6 59. 4 16. 6 6. 2 4. 8 7. 0 9. 6 12. 6 55. 3 18. 5 9. 5 4. 9

KATALITIČKO KREKIRANJE Procesne varijable: 1. Temperatura u reaktoru • Uobičajeno područje temperature: 480 - 5400 C. • Povećanjem temperature - povećava se konverzija i utječe na selektivnost za pojedinačne reakcije u procesu - u skladu s termodinamikom: – Prinosi benzina - rastu s povećanjem temperature do 5200 C zatim “ prekrekiranje” - prijelaz u frakciju nižeg vrelišta - plin. 1. Oktanski broj benzina - raste s povećanjem temperature (posebno IOB - radi velike konc. olefinskih CH). • • Omjer katalizator / sirovina Definira se kao omjer količine katalizatora (kg/h) i količine sirovine (kg/h ) koji ulaze u reaktor. Može biti izražen i u volumnim jedinicama: m 3/h / m 3/h . Važan parametar koji određuje oštrinu procesa - povećanje omjera C/O uvjetuje povećanje konverzije.
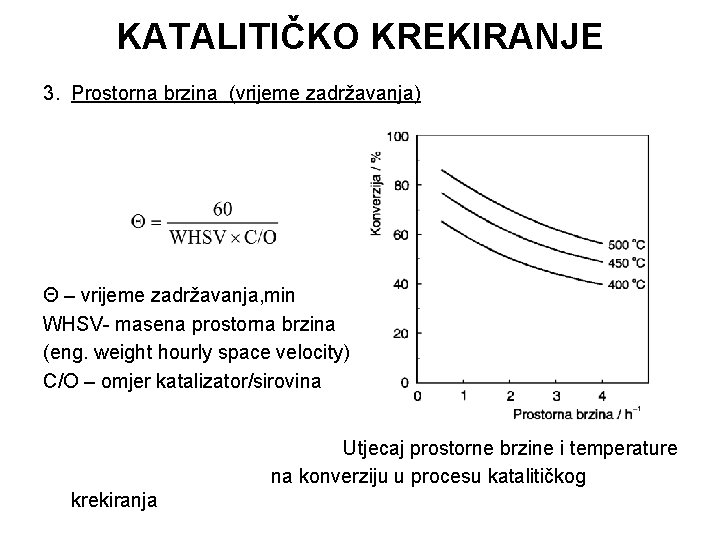
KATALITIČKO KREKIRANJE 3. Prostorna brzina (vrijeme zadržavanja) Θ – vrijeme zadržavanja, min WHSV- masena prostorna brzina (eng. weight hourly space velocity) C/O – omjer katalizator/sirovina Utjecaj prostorne brzine i temperature na konverziju u procesu katalitičkog krekiranja
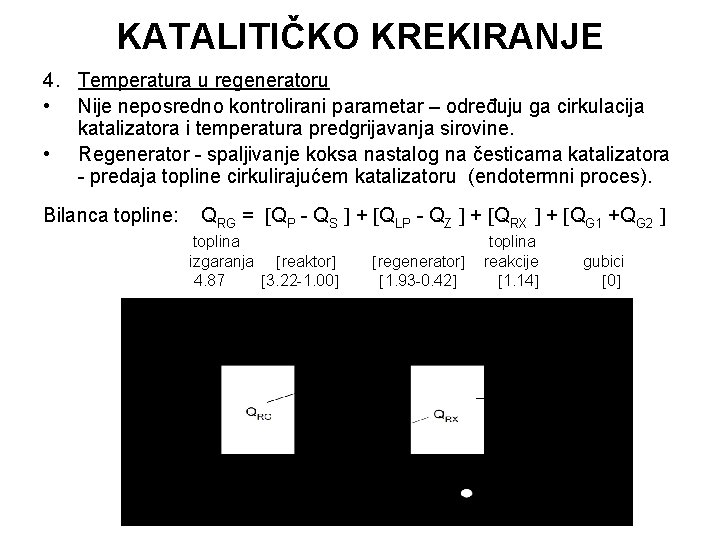
KATALITIČKO KREKIRANJE 4. Temperatura u regeneratoru • Nije neposredno kontrolirani parametar – određuju ga cirkulacija katalizatora i temperatura predgrijavanja sirovine. • Regenerator - spaljivanje koksa nastalog na česticama katalizatora - predaja topline cirkulirajućem katalizatoru (endotermni proces). Bilanca topline: QRG = QP - QS + QLP - QZ + QRX + QG 1 +QG 2 toplina izgaranja reaktor 4. 87 3. 22 -1. 00 regenerator 1. 93 -0. 42 toplina reakcije 1. 14 gubici 0
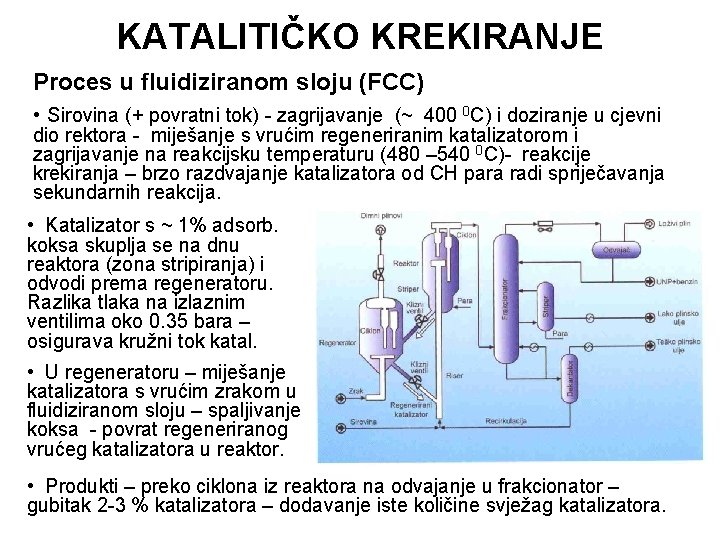
KATALITIČKO KREKIRANJE Proces u fluidiziranom sloju (FCC) • Sirovina (+ povratni tok) - zagrijavanje (~ 400 0 C) i doziranje u cjevni dio rektora - miješanje s vrućim regeneriranim katalizatorom i zagrijavanje na reakcijsku temperaturu (480 – 540 0 C)- reakcije krekiranja – brzo razdvajanje katalizatora od CH para radi spriječavanja sekundarnih reakcija. • Katalizator s ~ 1% adsorb. koksa skuplja se na dnu reaktora (zona stripiranja) i odvodi prema regeneratoru. Razlika tlaka na izlaznim ventilima oko 0. 35 bara – osigurava kružni tok katal. • U regeneratoru – miješanje katalizatora s vrućim zrakom u fluidiziranom sloju – spaljivanje koksa - povrat regeneriranog vrućeg katalizatora u reaktor. • Produkti – preko ciklona iz reaktora na odvajanje u frakcionator – gubitak 2 -3 % katalizatora – dodavanje iste količine svježag katalizatora.

KATALITIČKO KREKIRANJE Produkti: • C 3 -C 4 - frakcija ukapljenog naftnog plina – sirovina za alkilaciju, oligomerizaciju i procese dobivanja oksigenata ( MTBE). • Benzin – lakša frakcija (tv =75. . . 125 o. C) – niski OB - prerada u procesu katalitičkog reformiranja. Teža frakcija (tv = 125. . . 210 o. C) – nakon uklanjanja S spojeva namješavanje u motorne benzine. • Lako cikličko ulje – frakcija (tv = 200. . . 350 o. C) – ovisno o cetanskom broju – komponenta dizelskih goriva ili loživog ulja. • Teško cikličko ulje - frakcija (tv = 350. . . 420 o. C) – sirovina za proces koksiranja ili komponenta loživog ulja. Tri načina (područja) rada reaktora: Područje Srednji destilat Benzin Laki olefini temperatura reaktora, °C 449 -510 527 -538 538 -560 vrijeme zadržavanja < Base > Base omjer katalizator/sirovina < Base > Base Radni uvjeti
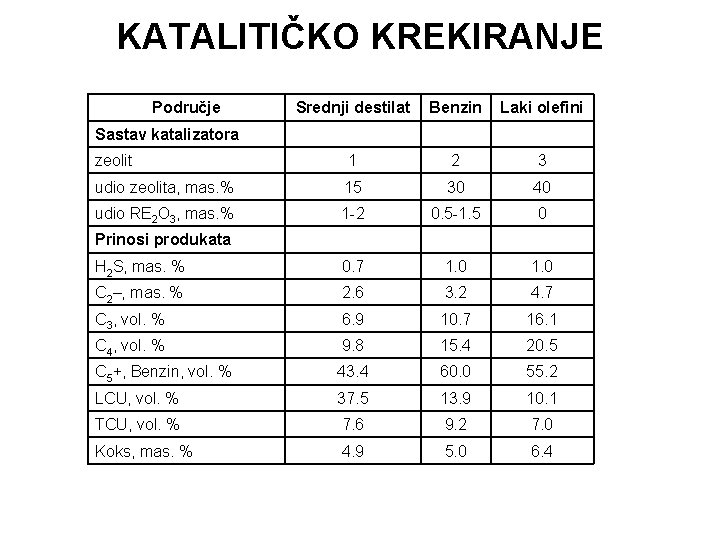
KATALITIČKO KREKIRANJE Područje Srednji destilat Benzin Laki olefini zeolit 1 2 3 udio zeolita, mas. % 15 30 40 udio RE 2 O 3, mas. % 1 -2 0. 5 -1. 5 0 H 2 S, mas. % 0. 7 1. 0 C 2–, mas. % 2. 6 3. 2 4. 7 C 3, vol. % 6. 9 10. 7 16. 1 C 4, vol. % 9. 8 15. 4 20. 5 C 5+, Benzin, vol. % 43. 4 60. 0 55. 2 LCU, vol. % 37. 5 13. 9 10. 1 TCU, vol. % 7. 6 9. 2 7. 0 Koks, mas. % 4. 9 5. 0 6. 4 Sastav katalizatora Prinosi produkata
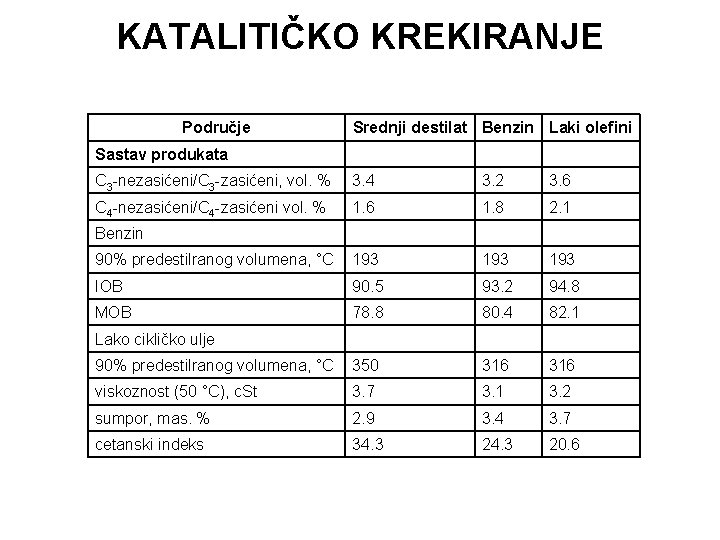
KATALITIČKO KREKIRANJE Područje Srednji destilat Benzin Laki olefini Sastav produkata C 3 -nezasićeni/C 3 -zasićeni, vol. % 3. 4 3. 2 3. 6 C 4 -nezasićeni/C 4 -zasićeni vol. % 1. 6 1. 8 2. 1 90% predestilranog volumena, °C 193 193 IOB 90. 5 93. 2 94. 8 MOB 78. 8 80. 4 82. 1 90% predestilranog volumena, °C 350 316 viskoznost (50 °C), c. St 3. 7 3. 1 3. 2 sumpor, mas. % 2. 9 3. 4 3. 7 cetanski indeks 34. 3 20. 6 Benzin Lako cikličko ulje
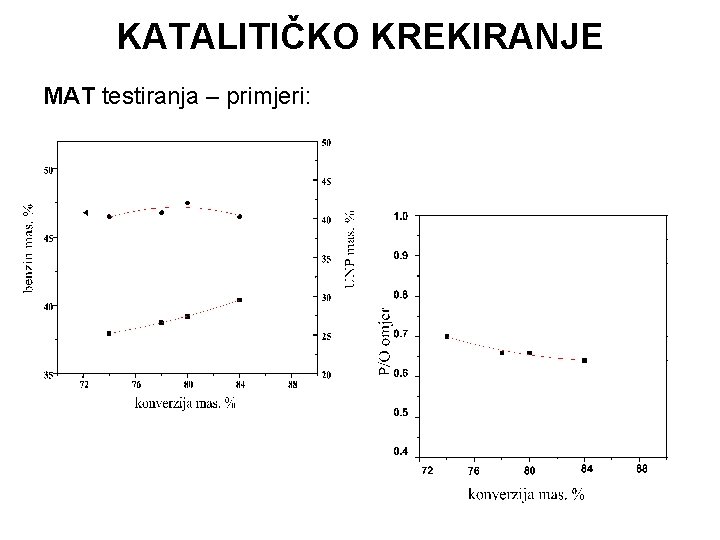
KATALITIČKO KREKIRANJE MAT testiranja – primjeri:
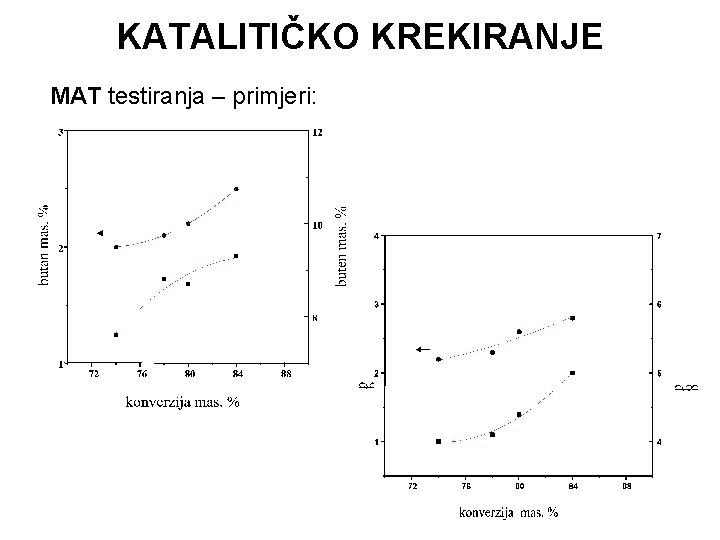
KATALITIČKO KREKIRANJE MAT testiranja – primjeri:
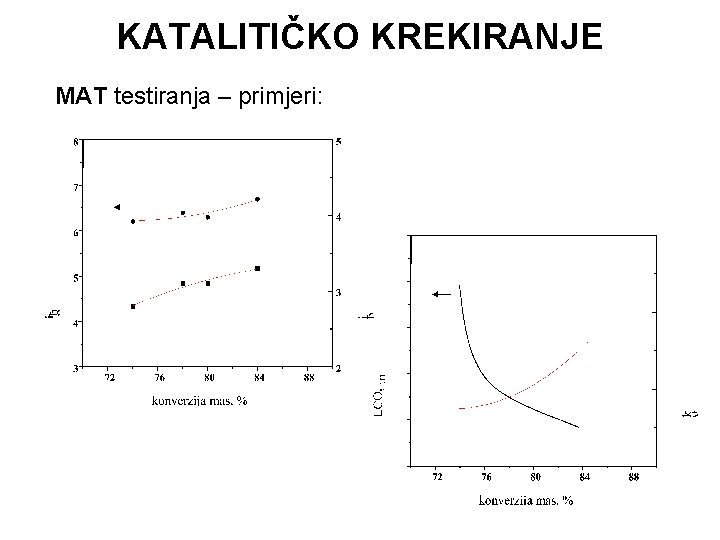
KATALITIČKO KREKIRANJE MAT testiranja – primjeri:

REFORMIRANJE BENZINA Razvoj katalitičkog reformiranja benzina Ø Zahtjevi automobilske industrije za visoko oktanskim gorivom Ø Zakonske odredbe o zaštiti okoliša Ø Proizvodnja BTX Ø Proizvodnja H 2 • Prvo katalitičko reformiranje: ranih 40 -tih Mo. O 3 katalizator brza deaktivacija • 1949. god. UOP Platforming (Pt/Al 2 O 3 katalizator) • 1969. god. bimetalni katalizator (Pt - Re) veća stabilnost

REFORMIRANJE BENZINA Cilj: povećanje vrijednosti oktanskog broja benzina. Proces: Benzin s atmosferske destilacije (pr. aromati 10%, nafteni 30%, parafini 60%) (frakcija: 75 -190 °C) Hidrodesulfurizacija uz (Ni(Co) – Mo / Al 2 O 3 katalizator Reforming: 3 reaktora, Pt + Re/Al 2 O 3 katalizator Procesi: 1. s nepokretnim slojem katalizatora 2. s kontinuiranom regeneracijom katalizatora
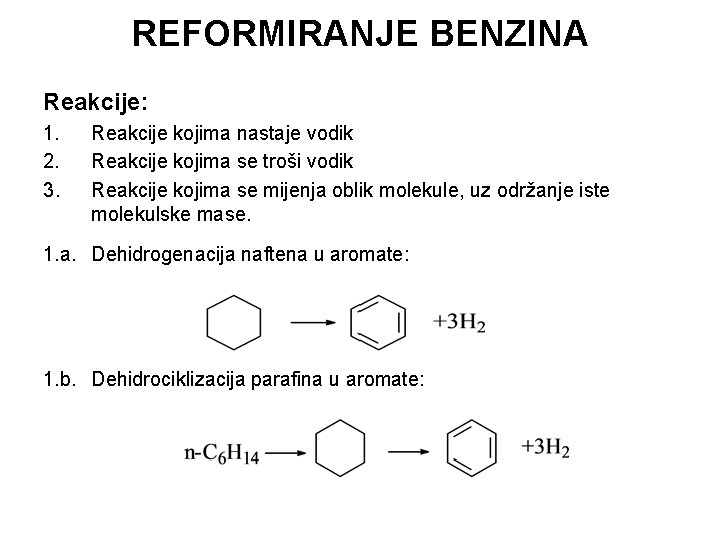
REFORMIRANJE BENZINA Reakcije: 1. 2. 3. Reakcije kojima nastaje vodik Reakcije kojima se troši vodik Reakcije kojima se mijenja oblik molekule, uz održanje iste molekulske mase. 1. a. Dehidrogenacija naftena u aromate: 1. b. Dehidrociklizacija parafina u aromate:
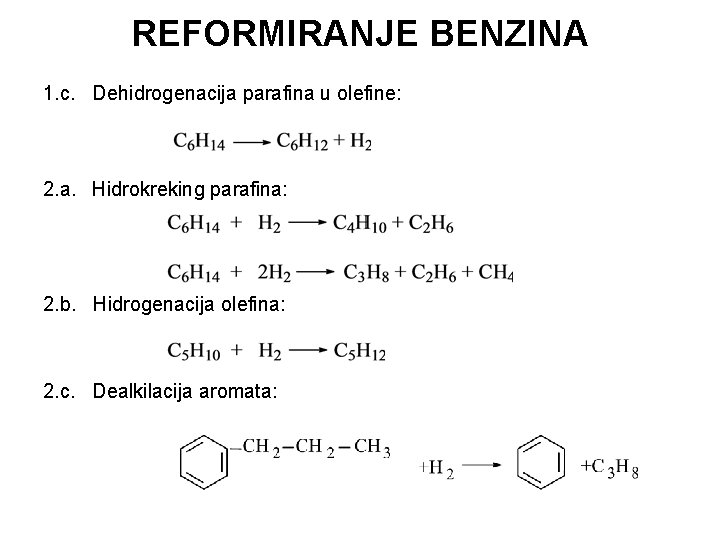
REFORMIRANJE BENZINA 1. c. Dehidrogenacija parafina u olefine: 2. a. Hidrokreking parafina: 2. b. Hidrogenacija olefina: 2. c. Dealkilacija aromata:
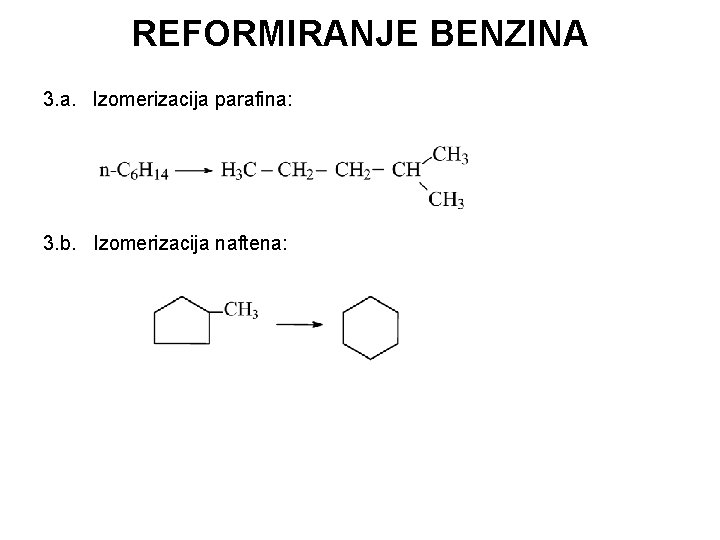
REFORMIRANJE BENZINA 3. a. Izomerizacija parafina: 3. b. Izomerizacija naftena:

REFORMIRANJE BENZINA Katalizatori: • Difunkcionalna kataliza - ravnoteža metalne i kisele komponente katalizatora • Metalna komponenta Pt – Re dispergirana je na nosaču - Al 2 O 3 + 1 % mas. Cl (promotor kisele funkcije) - površina 150 -300 m 2/g. • Monometalni katalizatori 0. 25 - 0. 6 % mas. Pt • Bimetalni katalizatori 0. 2 - 0. 4 % mas. Pt + 0. 2 - 0. 6 % mas. Re - niža cijena, veća stabilnost katalizatora
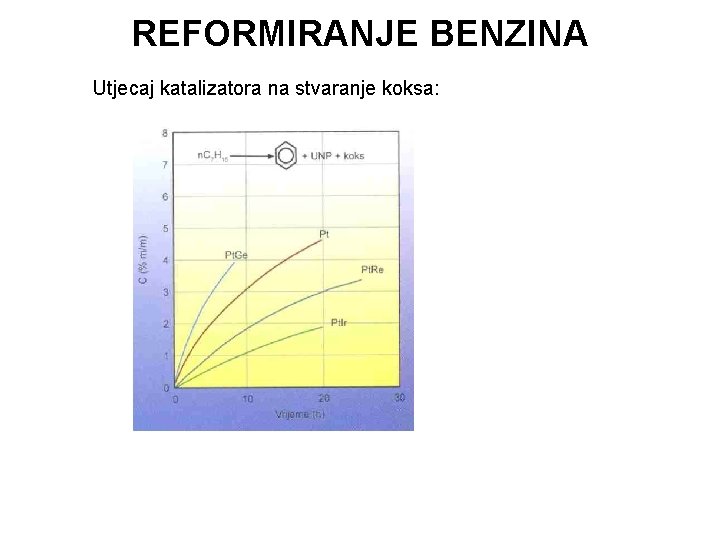
REFORMIRANJE BENZINA Utjecaj katalizatora na stvaranje koksa:
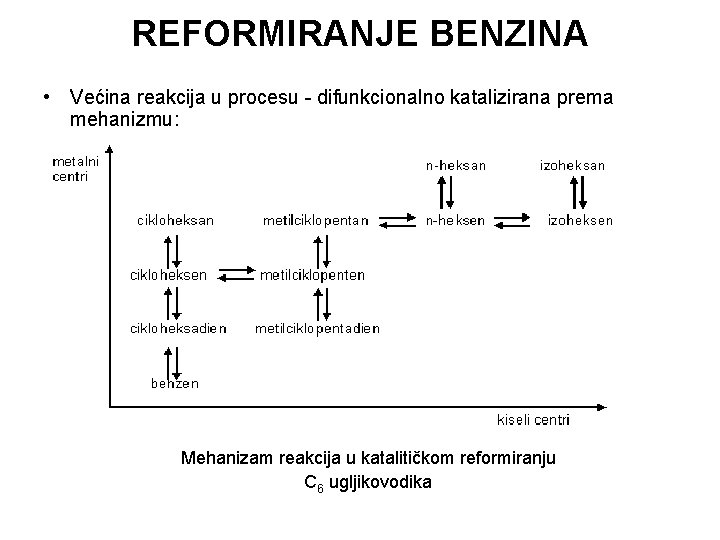
REFORMIRANJE BENZINA • Većina reakcija u procesu - difunkcionalno katalizirana prema mehanizmu: Mehanizam reakcija u katalitičkom reformiranju C 6 ugljikovodika

REFORMIRANJE BENZINA Reakcije: 1. Dehidrogenacija • • Pt katalitički aktivna komponenta Primjer: konverzija MCH: M k 1 Ma Ta k 2 T (Sinfelt) (M - metilcikloheksan, T – toluen) • Postupna dehidrogenacija (Corma): – reakcija nije "strukturno osjetljiva", pogoduje niski tlak i visoka T – endotermna reakcija

REFORMIRANJE BENZINA 2. Izomerizacija: Sadržaj halogena - bitno povećava aktivnost katalizatora za ovaj tip reakcija. Kod koncentracija Pt. iznad 0. 1 % mas. - konverzija neovisna o metalnoj komponenti katalizatora. Pod uvjetima katalitičkog reformiranja - brza reakcija, povoljan utjecaj nižeg tlaka.

REFORMIRANJE BENZINA 3. Dehidrociklizacija: konverzija parafinskih CH u aromatske Reakcija katalizirana djelovanjem metalnih i kiselih katalitički aktivnih centara - difunkcionalna kataliza. Mehanizam dehidrociklizacije: • ciklički spoj - pentanske ili heksanske strukture:

REFORMIRANJE BENZINA 4. Hidrogenoliza - cijepanje C-C veza na metalnim katalitički aktivnim centrima Mehanizam prema Cimino-u: (za etan) C 2 H 6 C 2 H 5 (ads) + H (ads) C 2 H 5 (ads) + H(ads) C 2 HX (ads) • • C 2 HX (ads) + a. H 2 CHY (ads) + CHZ (ads) CH 4 Brzina reakcije ovisi o parcijalnim tlakovima etana i vodika Aktivnost plemenitih metala opada u nizu: Ru Rh Ir Pd = Pt 4. Među neplemenitim metalima grupe VIII Ni je najaktivniji

REFORMIRANJE BENZINA • Za odvijanje reakcija potreban "multiplet" - "strukturno-osjetljive" reakcije CH 2 C • • • C M M Postepena dehidrogenacija i stvaranje višestrukih veza sa metalom. Nakon pucanja C-C veza - ponovna hidrogenacija i stvaranje CH 4. Za spriječavanje prekomjerne hidrogenolitičke aktivnosti katalizatora dodavanje sumpora blokiranje katalitički aktivnih centara 5. Hidrokrekiranje (metalni i kiseli katalitički centri) 1. 2. 3. dehidrogenacija – metalni centri stvaranje karbokationa – kiseli centri - krekiranje (uz izomerizaciju) hidrogenacija – metalni centri

REFORMIRANJE BENZINA • U frakciji plina prevladavaju C 3 i C 4 ugljikovodici.

REFORMIRANJE BENZINA Termodinamika i kinetika: Pri temperaturi od 773 K za reakcije dehidrogenacije i dehidrociklizacije n-heksana konstante ravnoteže K imaju visoke vrijednosti. Termodamički podaci za reakcije C 6 ugljikovodika: Reakcija K ( 773 K ) H / k. J mol-1 Cikloheksan → Benzen + 3 H 2 Metilciklopentan → Cikloheksan n-Heksan → Benzen + 4 H 2 n-Heksan → 2 -Metilpentan n-Heksan → 3 -Metilpentan n-Heksan → 1 -Heksen + H 2 6 x 105 0. 086 1. 0. 78 x 105 1. 1 0. 76 0. 037 221 -16. 0 226 -5. 9 -4. 6 130

REFORMIRANJE BENZINA • Dehidrogenacija naftena (najviše doprinosi OB i prinosima benzina) – endotermna reakcija - sa stajališta ravnoteže povoljan utjecaj visoke temperature i niskog tlaka. • Izomerizacija – blago egzotermna reakcija, mala vrijednost - ΔH. Ravnoteža metilcikopentan cikloheksan - pomaknuta prema metilciklopentanu (stabilniji). Izomerizacija n-heksana - prema 2 -metilpentanu. • Dehidrociklizacija – endotermna reakcija – povoljan utjecaj visoke temperature i niskog tlaka, ograničena kinetičkim parametrima. • Hidrokrekiranje parafina - vrlo egzotermna reakcija - ograničena u procesu kinetičkim parametrima. Najsporije reakcije u procesu - dehidrociklizacija parafina i hidrokrekiranje lakših ugljikovodika.
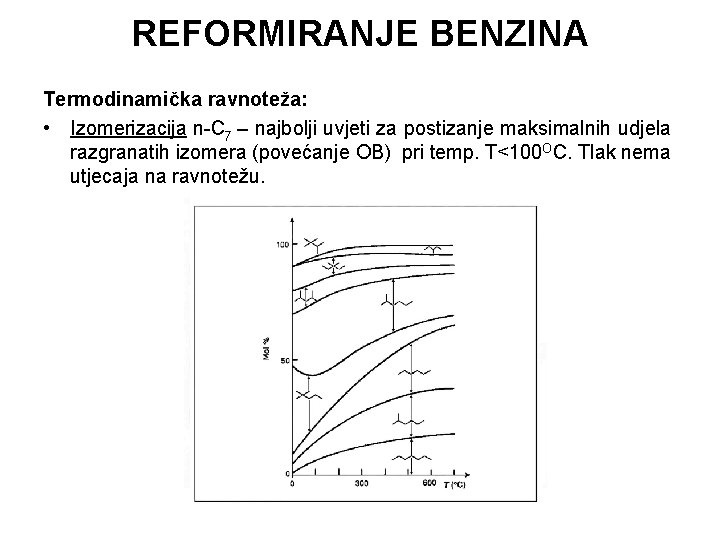
REFORMIRANJE BENZINA Termodinamička ravnoteža: • Izomerizacija n-C 7 – najbolji uvjeti za postizanje maksimalnih udjela razgranatih izomera (povećanje OB) pri temp. T<100 OC. Tlak nema utjecaja na ravnotežu.
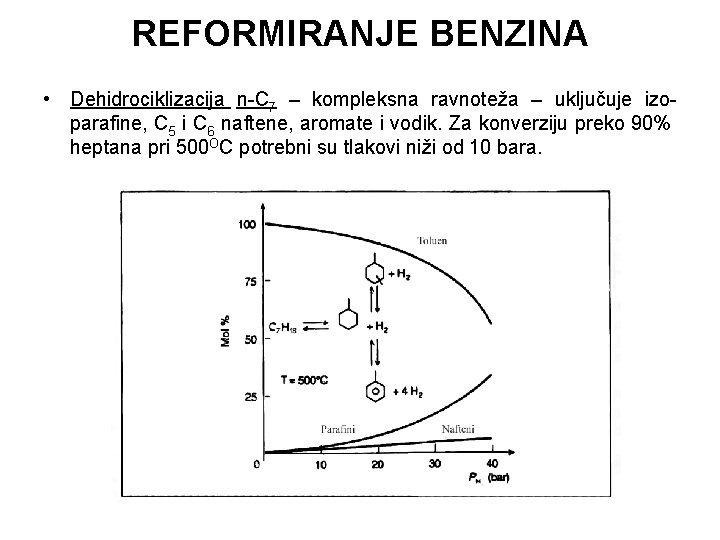
REFORMIRANJE BENZINA • Dehidrociklizacija n-C 7 – kompleksna ravnoteža – uključuje izoparafine, C 5 i C 6 naftene, aromate i vodik. Za konverziju preko 90% heptana pri 500 OC potrebni su tlakovi niži od 10 bara.

REFORMIRANJE BENZINA Kinetički modeli: • Kinetički model Marin-a i Froment-a temelji se na istraživanjima modelnih reakcija izomerizacije, dehidrociklizacije i hidrokrekiranja heksana i heptana u prisutnosti komercijalih reforming katalizatora. • Reakcijska shema reforminga n-heptana: • Brzine reakcija reforminga n-heptana uz Pt-Re/Al 2 O 3 katalizator

REFORMIRANJE BENZINA Shema procesa:

REFORMIRANJE BENZINA Procesne varijable – utjecaj na prinose i kakvoću produkata Tlak • Općenito u širokom rasponu (8 -40 bar) – stariji procesi - visokotlačni (27 -40 bar) – noviji procesi - niskotlačni (8 -20 bar) - dvometalni katalizatori (stabilniji) • Tlak utječe na odvijanje reakcija u procesu - porastom tlaka raste stupanj hidrokrekiranja, a smanjuju se udjeli reakcija aromatizacije (dehidrogenacija naftena i dehidrociklizacija parafina) – posljedica – smanjenje prinosa tekućeg produkta. • Visoki tlak - smanjuje nastajanje koksa na katalizatoru - usporava proces deaktivacije.

REFORMIRANJE BENZINA Temperatura • Temperaturno područje 470 - 5400 C – na temperaturama nižim od 4700 C - reakcije prespore – iznad 5400 C naglašeno krekiranje - rezultira gubitkom prinosa tekućeg produkta (reformata). Također, brza deaktivacija katalizatora (koksiranje). • Povećanje temperature – povećava se OB benzina ( porast brzine reakcija u procesu). • Povećanje temperature povoljno utječe na ravnotežu nastajanja aromata - gornja temperaturna granica postavljena (u odnosu na prostornu brzinu ) – uvažavajući aspekt deaktivacije katalizatora te ekonomičnost procesa.

REFORMIRANJE BENZINA Prostorna brzina • Definira se kao omjer volumnog protoka sirovine i volumena katalizatora. • LHSV (liquid hourly space velocity) m 3 /h/m 3 = h-1 • WHSV (weight hourly space velocity) kg /h/kg = h-1 • Prostorna brzina (vrijeme zadržavanja) - ima velik utjecaj na raspodjelu produkata. Brže reakcije - u uvjetima većih prostornih brzina (kraćeg vremena) - dehidrogenacija naftena, izomerizacija i hidrokrekiranje dužih CH molekula. • Sporije reakcije - u uvjetima dužeg vremena zadržavanja hidrokrekiranje manjih CH molekula i dehidrociklizacija parafina. • Oštrina procesa - pogoduje svim reakcijama u procesu ( postizanje željenog OB benzina) - podešava se izborom temperature i prostorne brzine - uvažavajući kriterije ekonomičnosti procesa (posebno važan aspekt je dekativacija katalizatora).

REFORMIRANJE BENZINA • Utjecaj smanjenja prostorne brzine (povećanja prostornog vremena) - povećanje konverzije svih CH - porast sadržaja aromata uz smanjenje naftena i parafina (dehidrogenacija naftena, hidrokreking i dehidrociklizacija parafina). • Povećavaju se vrijednosti OB benzina, raste sadržaj benzena, a opada ukupni prinos C 5+ frakcije benzina.

REFORMIRANJE BENZINA Omjer H 2/CH Definicija: molovi H 2 u recirkulirajućem plinu / molovi sirovine. • Primarni utjecaj - na sprječavanje deaktivacije katalizatora – monometalni katalizatori: 5 -10: 1 (manje stabilni) – bimetalni katalizatori: 3, 5 - 7: 1 (stabilniji) – u kontinuiranim procesima - omjeri mogu biti niži • Deaktivacija katalizatora - određuje donju granicu omjera • Troškovi (kompresija recirkuliranog vodika) - određuje gornju granicu omjera H 2/CH
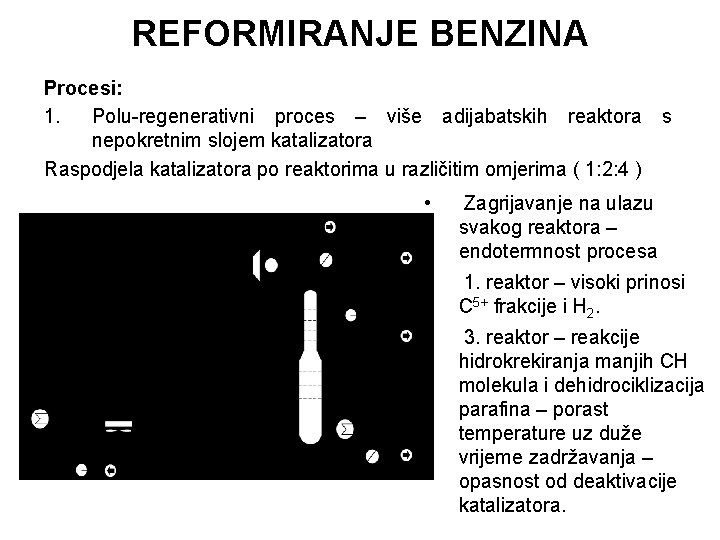
REFORMIRANJE BENZINA Procesi: 1. Polu-regenerativni proces – više adijabatskih reaktora nepokretnim slojem katalizatora Raspodjela katalizatora po reaktorima u različitim omjerima ( 1: 2: 4 ) s • Zagrijavanje na ulazu svakog reaktora – endotermnost procesa • 1. reaktor – visoki prinosi C 5+ frakcije i H 2. • 3. reaktor – reakcije hidrokrekiranja manjih CH molekula i dehidrociklizacija parafina – porast temperature uz duže vrijeme zadržavanja – opasnost od deaktivacije katalizatora.
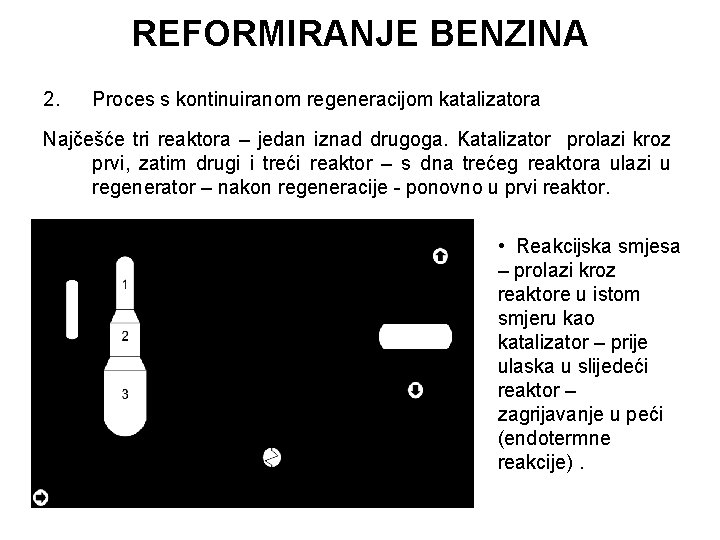
REFORMIRANJE BENZINA 2. Proces s kontinuiranom regeneracijom katalizatora Najčešće tri reaktora – jedan iznad drugoga. Katalizator prolazi kroz prvi, zatim drugi i treći reaktor – s dna trećeg reaktora ulazi u regenerator – nakon regeneracije - ponovno u prvi reaktor. • Reakcijska smjesa – prolazi kroz reaktore u istom smjeru kao katalizator – prije ulaska u slijedeći reaktor – zagrijavanje u peći (endotermne reakcije).

REFORMIRANJE BENZINA • Za postizanje željene vrijednosti IOB – važna “oštrina” procesnih uvjeta (temperatura, WHSV ) – utjecaj na brzinu svih reakcija u procesu. • Za postizanje povoljnog omjera prinos / IOB – važan parametar tlak – niži tlak potiskuje reakcije hidrokrekiranja u odnosu na dehidrociklizaciju – viši prinosi C 5+ frakcije i H 2. • Niži tlak i temperatura – povoljan utjecaj na kakvoću produkta – manji sadržaj benzena i niži tlak para. Kontinuirana regeneracija omogućuje rad u uvjetima: • nižeg tlaka – viši prinosi tekućeg produkta. • nižeg omjera H 2/CH – smanjeni troškovi energenata. • viših temperatura – niži zahtjevi vezani uz katalizator – mogućnost korištenja katalizatora niže stabilnosti.
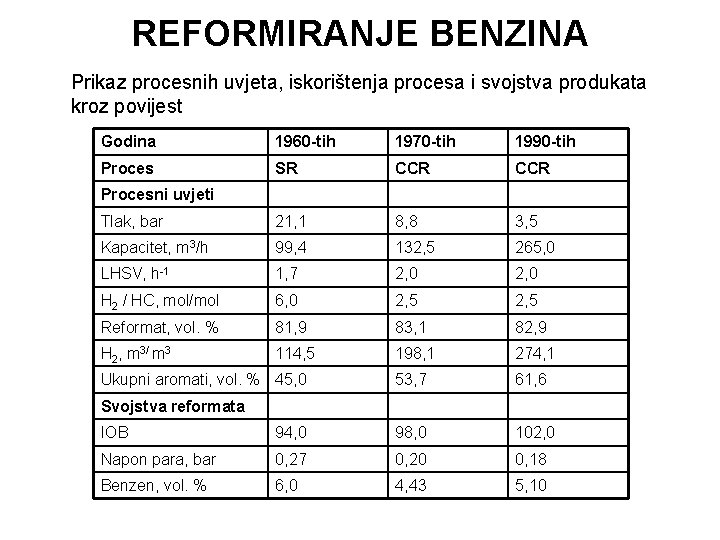
REFORMIRANJE BENZINA Prikaz procesnih uvjeta, iskorištenja procesa i svojstva produkata kroz povijest Godina 1960 -tih 1970 -tih 1990 -tih Proces SR CCR Tlak, bar 21, 1 8, 8 3, 5 Kapacitet, m 3/h 99, 4 132, 5 265, 0 LHSV, h-1 1, 7 2, 0 H 2 / HC, mol/mol 6, 0 2, 5 Reformat, vol. % 81, 9 83, 1 82, 9 H 2, m 3/ m 3 114, 5 198, 1 274, 1 53, 7 61, 6 Procesni uvjeti Ukupni aromati, vol. % 45, 0 Svojstva reformata IOB 94, 0 98, 0 102, 0 Napon para, bar 0, 27 0, 20 0, 18 Benzen, vol. % 6, 0 4, 43 5, 10
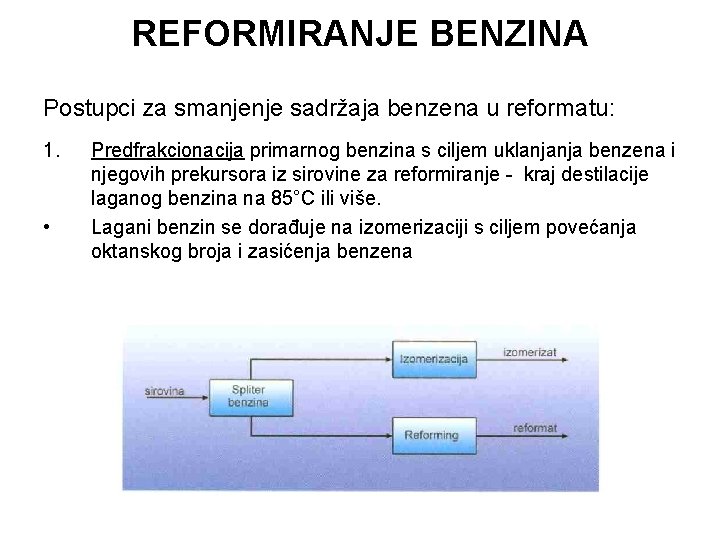
REFORMIRANJE BENZINA Postupci za smanjenje sadržaja benzena u reformatu: 1. • Predfrakcionacija primarnog benzina s ciljem uklanjanja benzena i njegovih prekursora iz sirovine za reformiranje - kraj destilacije laganog benzina na 85°C ili više. Lagani benzin se dorađuje na izomerizaciji s ciljem povećanja oktanskog broja i zasićenja benzena
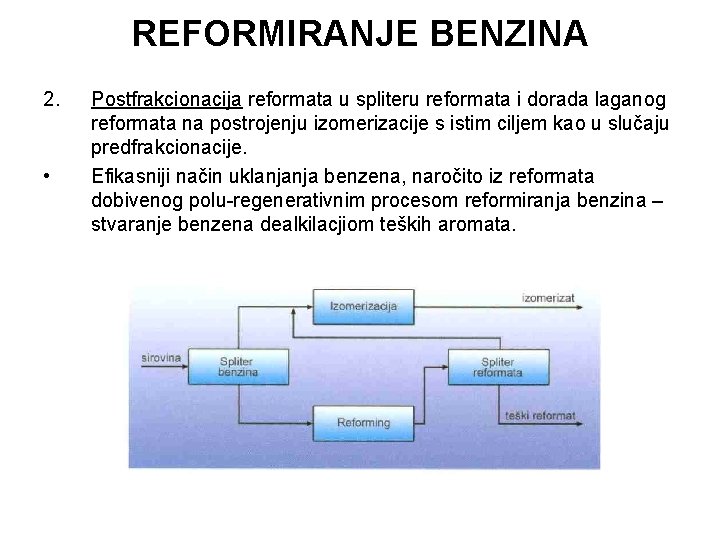
REFORMIRANJE BENZINA 2. • Postfrakcionacija reformata u spliteru reformata i dorada laganog reformata na postrojenju izomerizacije s istim ciljem kao u slučaju predfrakcionacije. Efikasniji način uklanjanja benzena, naročito iz reformata dobivenog polu-regenerativnim procesom reformiranja benzina – stvaranje benzena dealkilacjiom teških aromata.
- Slides: 67