Fakultet kemijskog inenjerstva i tehnologije Sveuilita u Zagrebu

Fakultet kemijskog inženjerstva i tehnologije Sveučilišta u Zagrebu STEHIOMETRIJA II KEMIJSKA RAVNOTEŽA II Ravnoteže u otopinama elektrolita dr. sc. Biserka Tkalčec
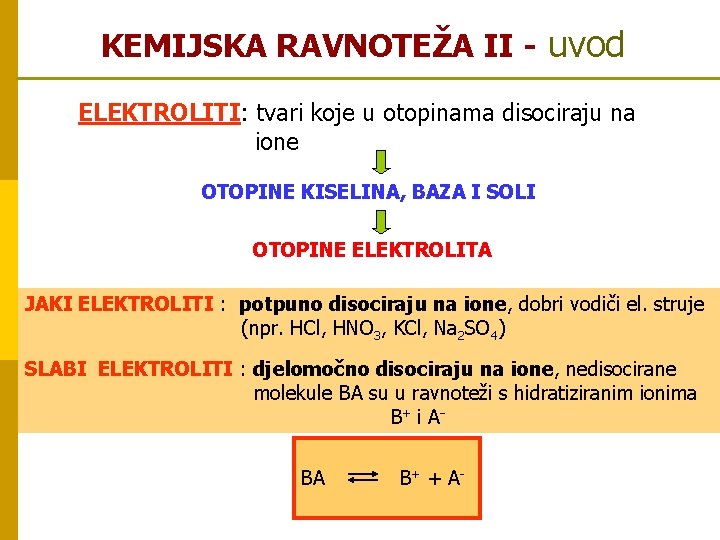
KEMIJSKA RAVNOTEŽA II - uvod ELEKTROLITI: tvari koje u otopinama disociraju na ione OTOPINE KISELINA, BAZA I SOLI OTOPINE ELEKTROLITA JAKI ELEKTROLITI : potpuno disociraju na ione, dobri vodiči el. struje (npr. HCl, HNO 3, KCl, Na 2 SO 4) SLABI ELEKTROLITI : djelomočno disociraju na ione, nedisocirane molekule BA su u ravnoteži s hidratiziranim ionima B+ i A BA B + + A-

KEMIJSKA RAVNOTEŽA II - uvod Ravnoteže u vodenim otopinama elektrolita: 1) ravnoteže u otopinama jakih i slabih kiselina i baza 2) ravnoteže u otopinama soli - hidroliza 3) ravnoteže u otopinama kompleksa 4) ravnoteža između otopine i neotopljenog kristala 5) redoks ravnoteže

KEMIJSKA RAVNOTEŽA II - uvod Općeniti prikaz ravnotežne reakcije disocijacije: BA Konstanta ravnoteže prikazane reakcije: B + + A-
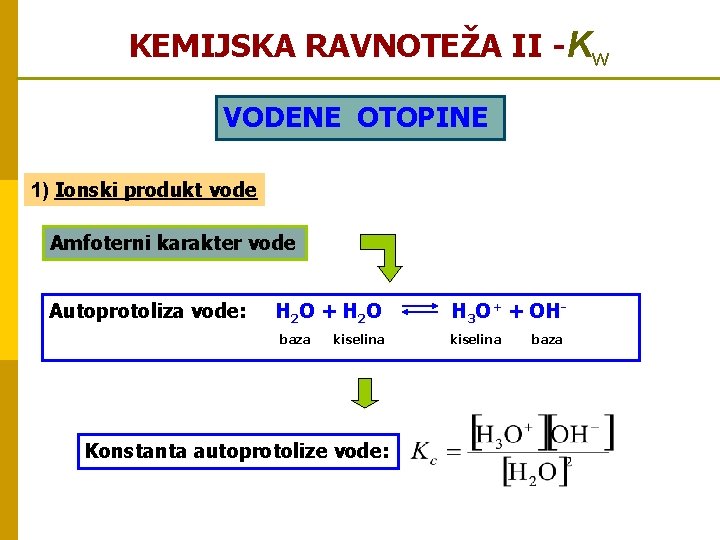
KEMIJSKA RAVNOTEŽA II -Kw VODENE OTOPINE 1) Ionski produkt vode Amfoterni karakter vode Autoprotoliza vode: H 2 O + H 2 O baza kiselina Konstanta autoprotolize vode: H 3 O+ + OHkiselina baza
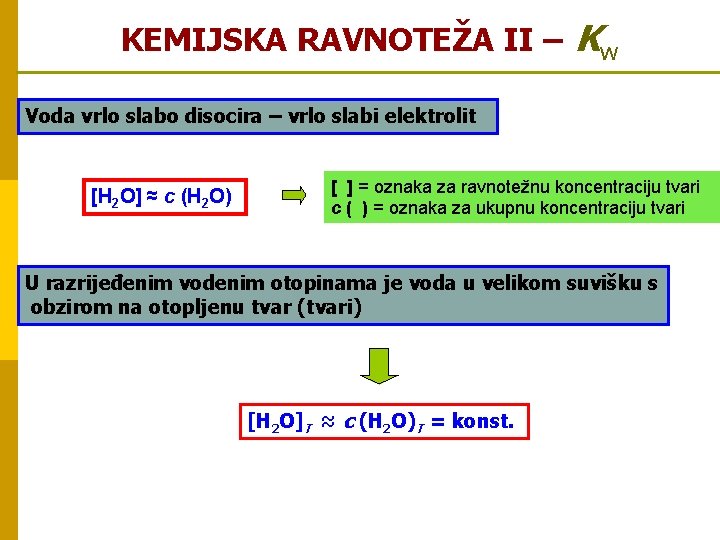
KEMIJSKA RAVNOTEŽA II – Kw Voda vrlo slabo disocira – vrlo slabi elektrolit [H 2 O] ≈ c (H 2 O) [ ] = oznaka za ravnotežnu koncentraciju tvari c ( ) = oznaka za ukupnu koncentraciju tvari U razrijeđenim vodenim otopinama je voda u velikom suvišku s obzirom na otopljenu tvar (tvari) [H 2 O]T ≈ c (H 2 O)T = konst.
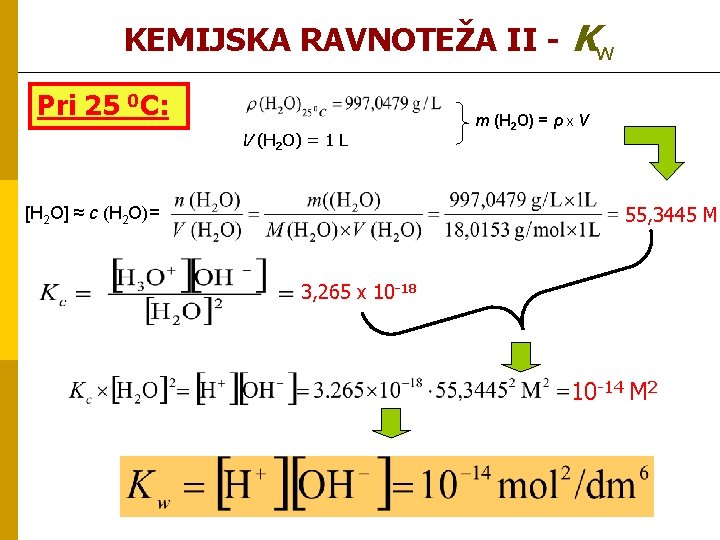
KEMIJSKA RAVNOTEŽA II - Kw Pri 25 0 C: V (H 2 O) = 1 L m (H 2 O) = ρ x V 55, 3445 M [H 2 O] ≈ c (H 2 O)= 3, 265 x 10 -18 10 -14 M 2
![KEMIJSKA RAVNOTEŽA II- p. H Pri 25 0 C: potpuno čista voda : [H+] KEMIJSKA RAVNOTEŽA II- p. H Pri 25 0 C: potpuno čista voda : [H+]](http://slidetodoc.com/presentation_image_h/7cbb320fac99570d0fac3b1a2041258f/image-8.jpg)
KEMIJSKA RAVNOTEŽA II- p. H Pri 25 0 C: potpuno čista voda : [H+] = [OH-] = 10 -7 M U svim vodenim otopinama: [H+] > 10 -7 M KISELA OTOPINA [H+] < 10 -7 M LUŽNATA OTOPINA
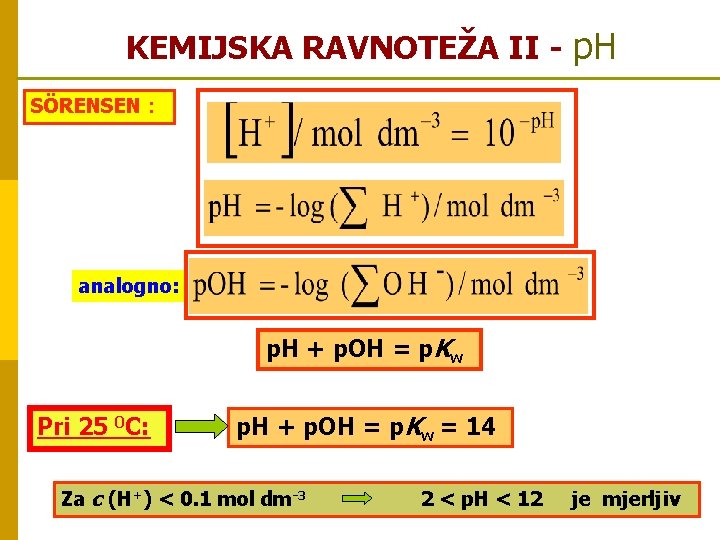
KEMIJSKA RAVNOTEŽA II - p. H SÖRENSEN : analogno: p. H + p. OH = p. Kw Pri 25 0 C: p. H + p. OH = p. Kw = 14 Za c (H+) < 0. 1 mol dm-3 2 < p. H < 12 je mjerljiv

KEMIJSKA RAVNOTEŽA II – aktivitet iona AKTIVITET IONA N. Lewis : ac relativni aktivitet tvari (jedinke) B y. B koeficijent aktiviteta tvari (jedinke) B c. B koncentracija tvari (jedinke) B c 0 standardna koncentracija referentne otopine = 1 mol dm -3
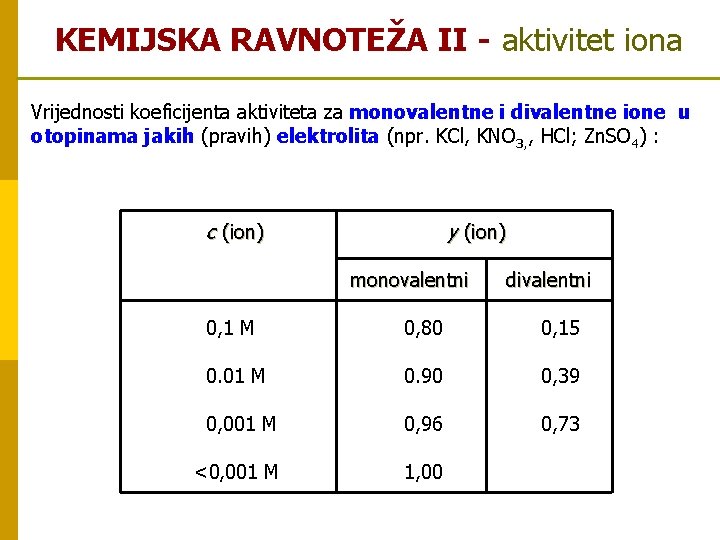
KEMIJSKA RAVNOTEŽA II - aktivitet iona Vrijednosti koeficijenta aktiviteta za monovalentne i divalentne ione u otopinama jakih (pravih) elektrolita (npr. KCl, KNO 3, , HCl; Zn. SO 4) : c (ion) y (ion) monovalentni divalentni 0, 1 M 0, 80 0, 15 0. 01 M 0. 90 0, 39 0, 001 M 0, 96 0, 73 <0, 001 M 1, 00

KEMIJSKA RAVNOTEŽA II - aktivitet iona Jaki elektroliti P. Debye, E. Hückel (25 0 C), ako je c (ion) < 0. 01 M: z + , z -. . . z i naboj kationa i aniona Ic ionska jakost otopine (na temelju koncentracija) ci koncentracija pojedinog kationa, odn. aniona u otopini

KEMIJSKA RAVNOTEŽA II - aktivitet iona Ravnotežna reakcija : AB A + + B- Termodinamička konstanta ravnoteže : Koncentracijska konstanta ravnoteže : Kc = K, jer aktivitet iona ovisi o koncentraciji

KEMIJSKA RAVNOTEŽA II - aktivitet iona Kc = f (T ) ≈ K. . . samo za vrlo, vrlo razrijeđene otopine: slabi elektroliti : c < 0. 1 M y≈1 jaki elektroliti : c < 0. 001 M a=c ILI uz stalnu veliku ionsku jakost otopine, što se postiže dodatkom u otopinu “indiferentnog elektrolita” (ne učestvuje u ravnotežnoj reakciji) u koncentraciji puno većoj od koncentracije sudionika promatrane ravnotežne reakcije, npr. c (Na. Cl. O 4) = 2 M. Tada ionsku jakost određuje taj elektrolit, pa se aktiviteti iona u promatranoj ravnotežnoj reakciji mogu smatrati konstantnima, bez obzira na promjenu njihove koncentracije (ali u dozvoljenim granicama). Samo tada se smije u izraz za konstantu ravnoteže uvrstiti koncentracija vrsta, umjesto njihova aktiviteta.
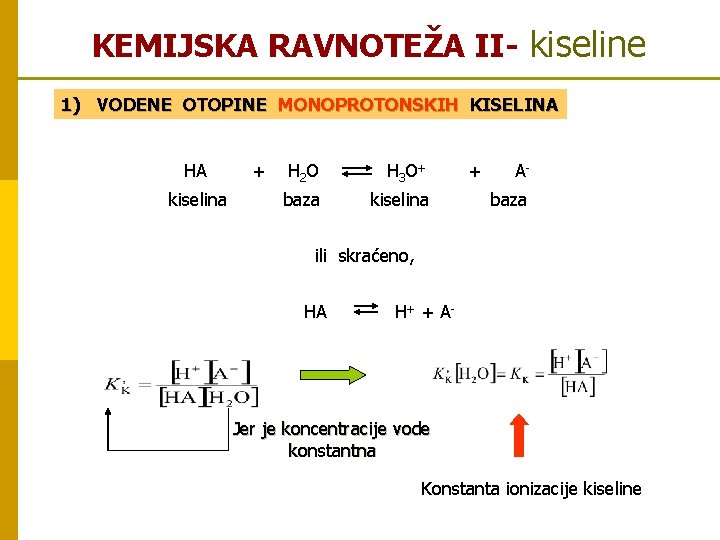
KEMIJSKA RAVNOTEŽA II- kiseline 1) VODENE OTOPINE MONOPROTONSKIH KISELINA HA kiselina + H 2 O H 3 O+ baza kiselina + Abaza ili skraćeno, HA H + + A- Jer je koncentracije vode konstantna Konstanta ionizacije kiseline

KEMIJSKA RAVNOTEŽA II- jake kiseline a) jake kiseline: potpuno disocirane HA H + + A- c (kis. ) = c (H+) 1. ) p. H = - log [H+] = - log c (kis. ) 2. ) p. H = - log a [H+] = - log y∙c (kis. ) ako je y = 1 (c < 0. 001) ako je y < 1 (c < 0. 1 M i c > 0. 001 M ) • Primjer računa za vrlo, vrlo razrijeđenu otopinu HCl, c (HCl) = 10 -8 M, kada se disocija vode ne smije zanemariti (seminarski zadatak).
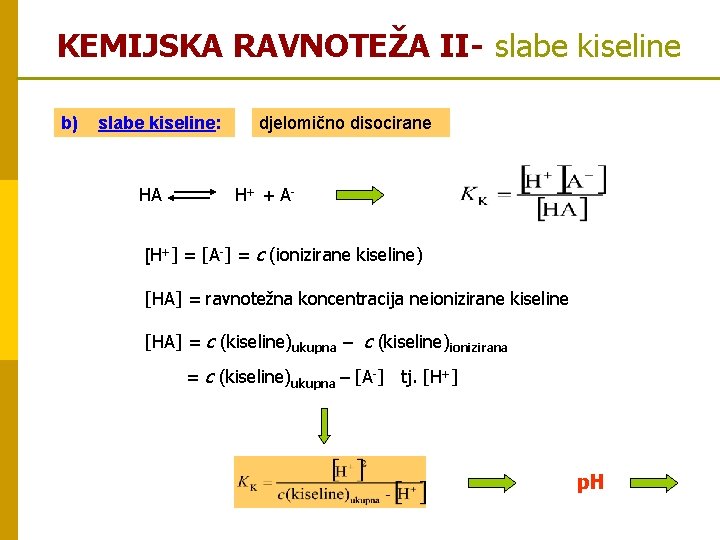
KEMIJSKA RAVNOTEŽA II- slabe kiseline b) slabe kiseline: HA djelomično disocirane H+ + A- [H+] = [A-] = c (ionizirane kiseline) [HA] = ravnotežna koncentracija neionizirane kiseline [HA] = c (kiseline)ukupna – c (kiseline)ionizirana = c (kiseline)ukupna – [A-] tj. [H+] p. H
![KEMIJSKA RAVNOTEŽA II– slabe kiseline Računanje p. H slabe kiseline [H+] 1. ) bez KEMIJSKA RAVNOTEŽA II– slabe kiseline Računanje p. H slabe kiseline [H+] 1. ) bez](http://slidetodoc.com/presentation_image_h/7cbb320fac99570d0fac3b1a2041258f/image-18.jpg)
KEMIJSKA RAVNOTEŽA II– slabe kiseline Računanje p. H slabe kiseline [H+] 1. ) bez aproksimacije: 2. ) aproksimativno: HA je slabo disocirana, pa se uz približni uvjet, c (HA) > 10 -2 M), K (HA) < 10 -3 M može smatrati: [H+] = [A-] << [HA] ≈ c (HA) Kriterij procjene: 1. stupanj ionizacije, α > 3 % račun bez aproksimacije 2. stupanj ionizacije, α ≤ 3 % aproksimativni račun p. H
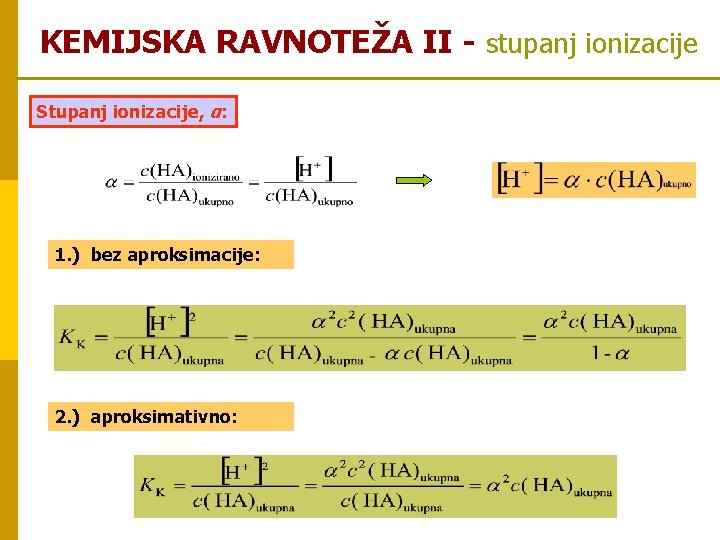
KEMIJSKA RAVNOTEŽA II - stupanj ionizacije Stupanj ionizacije, α: 1. ) bez aproksimacije: 2. ) aproksimativno:
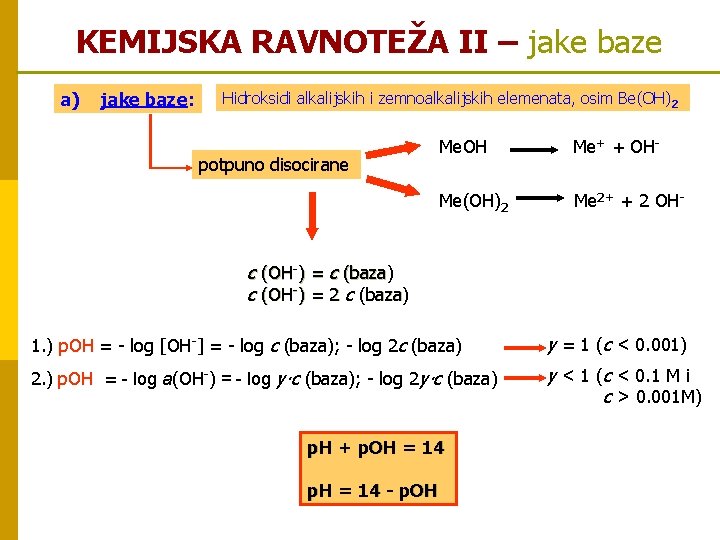
KEMIJSKA RAVNOTEŽA II – jake baze a) jake baze: Hidroksidi alkalijskih i zemnoalkalijskih elemenata, osim Be(OH) 2 potpuno disocirane Me. OH Me+ + OH- Me(OH)2 Me 2+ + 2 OH- c (OH-) = c (baza) (baza c (OH-) = 2 c (baza) (baza 1. ) p. OH = - log [OH-] = - log c (baza); - log 2 c (baza) y = 1 (c < 0. 001) 2. ) p. OH = - log a(OH-) = - log y∙c (baza); - log 2 y∙c (baza) y < 1 (c < 0. 1 M i c > 0. 001 M) p. H + p. OH = 14 p. H = 14 - p. OH
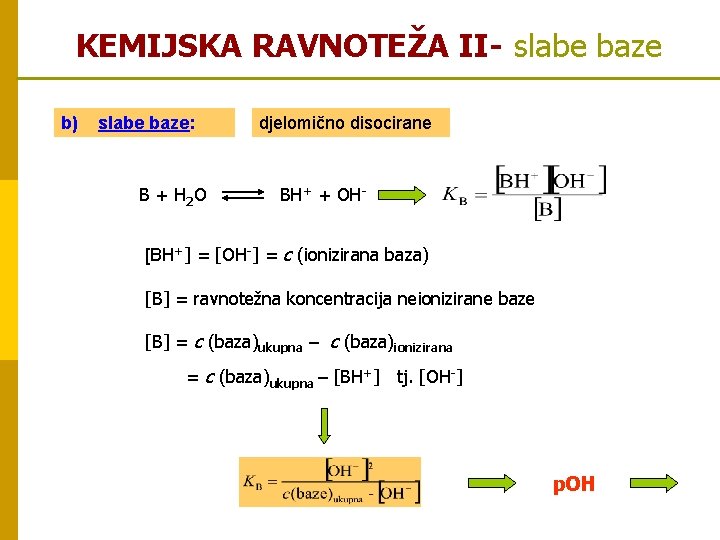
KEMIJSKA RAVNOTEŽA II- slabe baze b) slabe baze: B + H 2 O djelomično disocirane BH+ + OH- [BH+] = [OH-] = c (ionizirana baza) [B] = ravnotežna koncentracija neionizirane baze [B] = c (baza)ukupna – c (baza)ionizirana = c (baza)ukupna – [BH+] tj. [OH-] p. OH
![KEMIJSKA RAVNOTEŽA II– slabe baze Računanje p. H slabe baze [OH-] 1. ) bez KEMIJSKA RAVNOTEŽA II– slabe baze Računanje p. H slabe baze [OH-] 1. ) bez](http://slidetodoc.com/presentation_image_h/7cbb320fac99570d0fac3b1a2041258f/image-22.jpg)
KEMIJSKA RAVNOTEŽA II– slabe baze Računanje p. H slabe baze [OH-] 1. ) bez aproksimacije: 2. ) aproksimativno: p. OH p. H B je slabo disocirana, pa se uz približni uvjet, c (B) > 10 -2 M), K (B) < 10 -3 M može smatrati: [OH-] = [BH+] << [B] p. H [B] ≈ c (B) Kriterij procjene: 1. stupanj ionizacije, α > 3 % račun bez aproksimacije 2. stupanj ionizacija, α ≤ 3 % aproksimativni račun
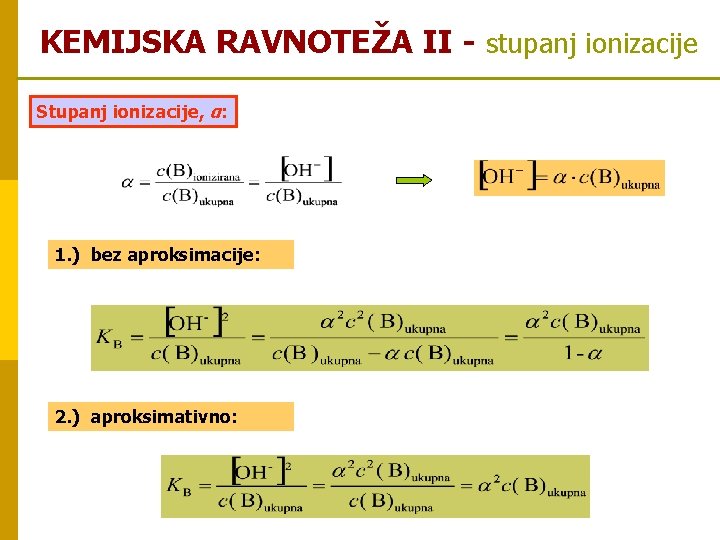
KEMIJSKA RAVNOTEŽA II - stupanj ionizacije Stupanj ionizacije, α: 1. ) bez aproksimacije: 2. ) aproksimativno:

1. Domaća zadaća 1. Ionski produkt za tešku vodu, D 2 O, iznosi pri 25 0 C, Kw = 2 ∙ 10 -15 M 2. a) Izračunajte p. H čiste vode, H 2 O, i čiste teške vode, D 2 O. b) Da li razlika u vrijednosti p. H znači da teška voda nije neutralna ? Obrazložite! 2. a) U vodenoj otopini natrijeva hidroksida, c (Na. OH) = 0, 005 M, izmjerena vrijednost p. H otopine je, p. H = 11, 66. Izračunajte koeficijent aktiviteta otopine. b) Volumen od 5 m. L te otopine otpipetiran je u odmjernu tikvicu od 250 m. L te je tikvica nadopunjena destiliranom vodom do oznake. Izračunajte p. H tako pripremljene otopine natrijeva hidroksida. c) Koliki je koeficijent aktiviteta hidroksidnog aniona u pripremljenoj otopini ? Obrazložite! R: a) y = 0, 92; b) p. H = 10. 3. a) Izračunajte p. H otopine koja je pripremljena tako da je 315, 3 mg barijeva hidroksida oktahidrata otopljeno u 12 litara vode. b) Hoće li izračunati i izmjereni p. H otopine biti jednaki ? Obrazložite! R: a) p. H = 10, 2 4. Boca napunjena plinom klorovodikom začepljena je čepom s provučenom staklenom cijevi, čiji je kraj uronjen u vodu. Sav klorovodik u boci se otopio u vodi, koja je ulazeći kroz staklenu cijev velikom brzinom potpuno ispunila volumen boce. Pokus je proveden pri temperaturi, t = 25 0 C i tlaku, p = 100 k. Pa. R: p. H = 1, 38

1. Domaća zadaća - nastavak 5. Izračunajte p. H vodene otopine klorovodične kiseline, c (HCl) = 10 -7 M. R: p. H = 6, 79 6. U otopini octene kiseline izmjeren je p. H = 3, 5. Konstanta ionizacije octene kiseline je, KK =1, 8 ∙ 10 -5 M. Izračunajte a) ravnotežnu koncentraciju OH- i CH 3 COO- iona, b) ravnotežnu koncentraciju neionizirane kiseline i ukupnu množinsku koncentraciju kiseline u otopini, c) stupanj ionizacije kiseline u otopini. R: a) [OH-] = 3, 16 ∙ 10 -11 M; b) = [CH 3 COOH] = 5, 55 ∙ 10 -3 M; c (CH 3 COOH) = 5, 86 ∙ 10 -3 M ; c) α = 5, 4 % 7. Izračunajte volumen vode koju treba dodati u 1 dm 3 cijanovodične kiseline, c (HCN) = 1 M, da bi se stupanj ionizacije kiseline povećao tri puta. R: V (H 2 O) = 8 L 8. Otopina kojoj je p. H = 14, 0 sadrži natrijev hidroksid i amonijak koncentracije, c (NH 3) = 2 M. Izračunajte a) ravnotežnu koncentraciju (µmol/L) amonijevog iona i stupanj ionizacija amonijaka u otopini, b) množinsku koncentraciju natrijevog hidroksida u otopini. c) Obrazložite postupak rješavanja zadatka! Konstanta ionizacije amonijaka je, KB = 1, 8 ∙ 10 -5 M. R: a) [NH 4+] = 36 µmol/L, α = 0, 0018 %; b) c (Na. OH) = 1 M

1. Domaća zadaća - nastavak 9. Otopina kojoj je p. H = 0, 0 sadrži klorovodičnu kiselinu i octenu kiselinu koncentracije, c (CH 3 COOH) = 2 M. Izračunajte a) ravnotežnu koncentraciju (µmol/L) acetat iona i stupanj ionizacija octene kiseline u otopini, b) množinsku koncentraciju klorovodične kiseline u otopini. c) Obrazložite postupak rješavanja zadatka! Konstanta ionizacije octene kiseline je, KK = 1, 8 ∙ 10 -5 M R: a) [CH 3 COO-] = 36 µmol/L, α = 0, 0018 %; b) c (HCl) = 1 M 10. Neka otopina je smjesa fenola i mliječne kiseline. Koncentracija fenola je, c (C 6 H 5 OH) = 1 M, a mliječne kiseline, c (CH 3 C(OH)COOH = 1 M. a) Izračunajte ravnotežne koncentracije vodikovog iona, fenolat iona i laktat iona u otopini. b) Obrazložite postupak rješavanja zadatka! Konstanta ionizacije fenola je, KK (fenol) = 1, 05 ∙ 10 -10 M, a konstanta ionizacije milječne kiseline je, KK (mliječna kiselina) = 1, 38 ∙ 10 -4 M. R: a) [H+] = 0, 0117 M; [C 6 H 5 O-] = 8, 9 ∙ 10 -9 M
- Slides: 26


















































