AMMINOACIDI PEPTIDI PROTEINE Classificazione degli Amminoacidi Anche se




























- Slides: 107

AMMINOACIDI PEPTIDI PROTEINE

Classificazione degli Amminoacidi Anche se il nome implica la presenza di un gruppo amminico —NH 2 e di un gruppo carbossilico —CO 2 H, in realtà sono presenti i gruppi —NH 3+ and —CO 2–. Sono classificati come a, b, g, ecc. ammino acidi in funzione del carbonio che porta la funzione ammonio

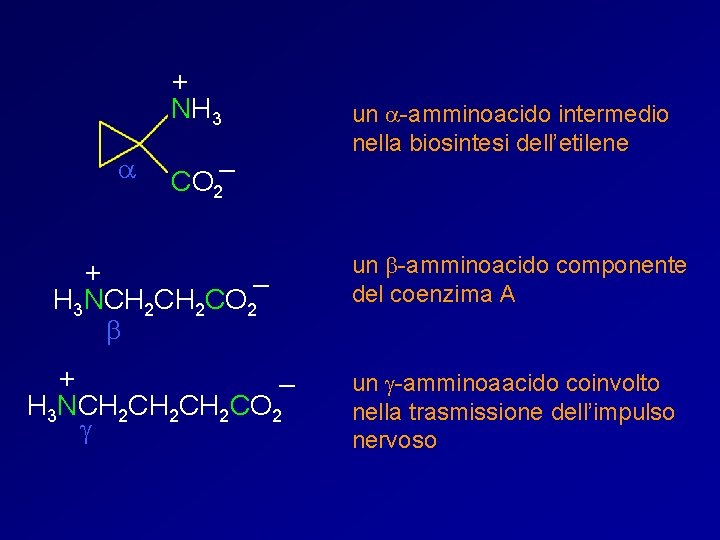
+ NH 3 a CO 2– un a-amminoacido intermedio nella biosintesi dell’etilene + – H 3 NCH 2 CO 2 b un b-amminoacido componente del coenzima A + – H 3 NCH 2 CH 2 CO 2 g un g-amminoaacido coinvolto nella trasmissione dell’impulso nervoso

Sono noti 700 amminoacidi naturali 20 ammino acidi, tutti a-amminoacidi, sono i componenti delle proteine. I 20 amminoacidi differiscono per il gruppo legato al carbonio a. + H 3 N H C R O C – O

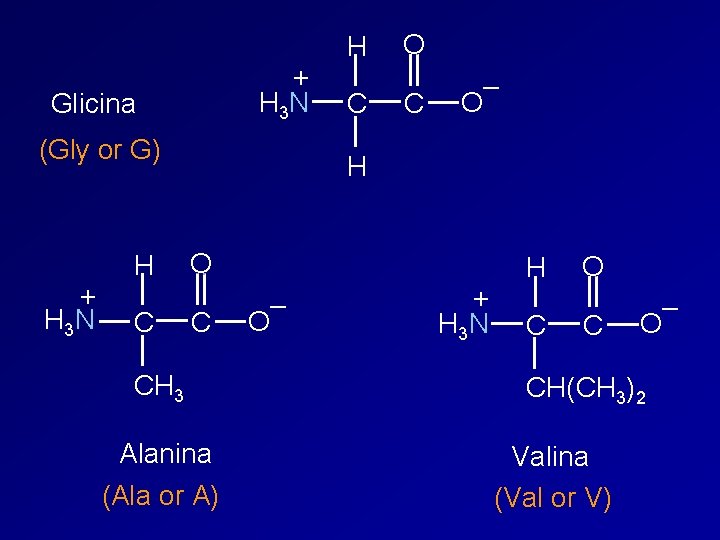
+ H 3 N Glicina (Gly or G) + H 3 N H C O C – O H O C CH 3 Alanina (Ala or A) – O + H 3 N H C O C – O CH(CH 3)2 Valina (Val or V)

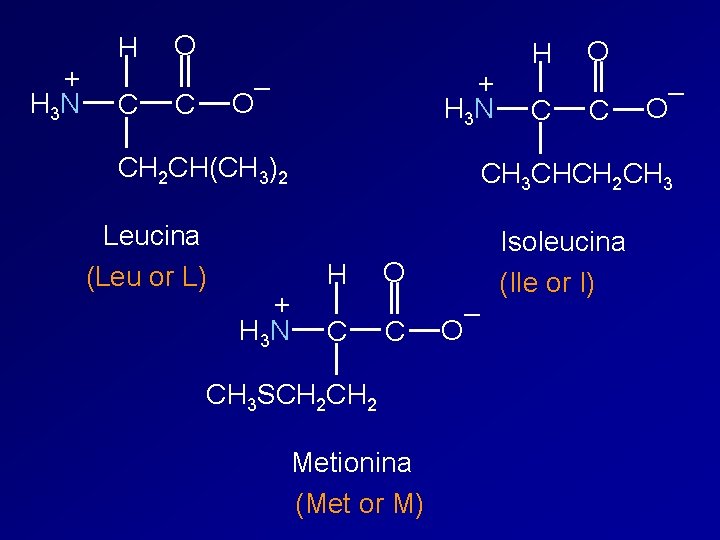
+ H 3 N H C O + H 3 N – O C CH 2 CH(CH 3)2 Leucina (Leu or L) H C O C – O CH 3 CHCH 2 CH 3 + H 3 N H C O C CH 3 SCH 2 Metionina (Met or M) – O Isoleucina (Ile or I)

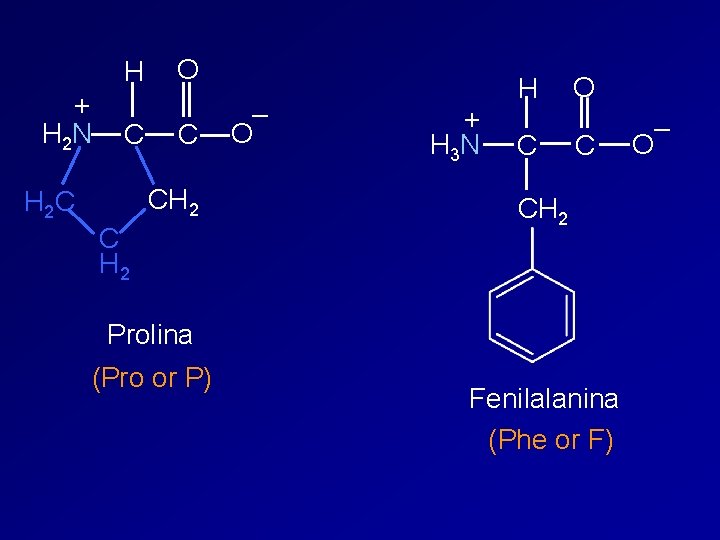
H + H 2 N C O C CH 2 H 2 C C H 2 – O + H 3 N H C O C CH 2 Prolina (Pro or P) Fenilalanina (Phe or F) – O

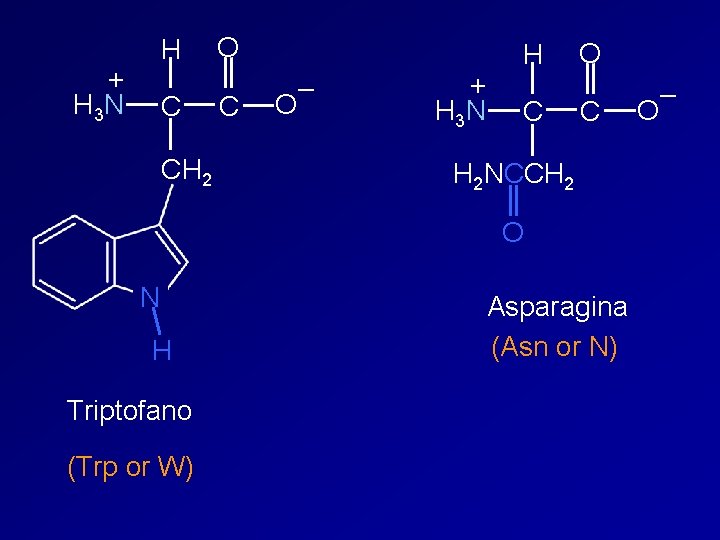
+ H 3 N H C CH 2 O C – O + H 3 N H C O C H 2 NCCH 2 O N H Triptofano (Trp or W) Asparagina (Asn or N) – O

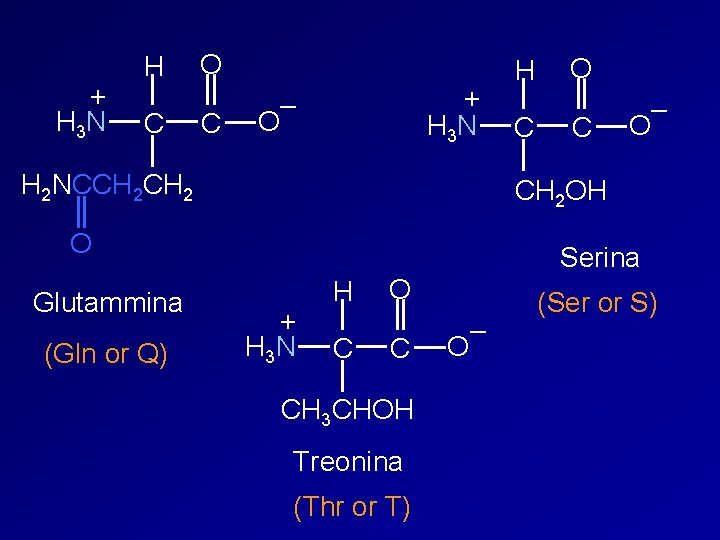
+ H 3 N H C O C + H 3 N – O H 2 NCCH 2 (Gln or Q) C O C – O CH 2 OH O Glutammina H + H 3 N H C Serina O C CH 3 CHOH Treonina (Thr or T) – O (Ser or S)

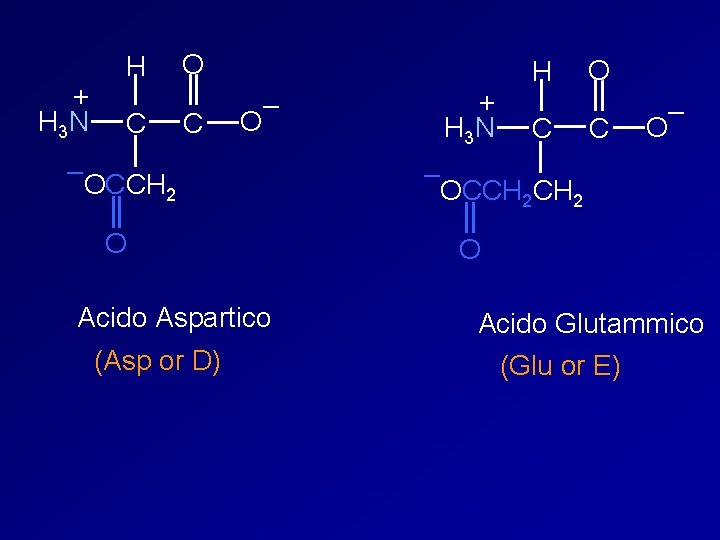
+ H 3 N H C O C – OCCH 2 O Acido Aspartico (Asp or D) + H 3 N H C O C – OCCH 2 O Acido Glutammico (Glu or E)

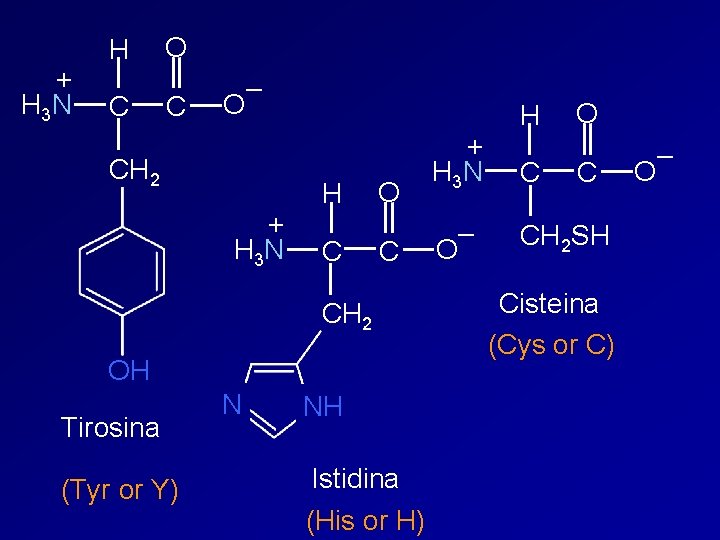
+ H 3 N H C O C – O CH 2 + H 3 N H C O C CH 2 OH Tirosina (Tyr or Y) N NH Istidina (His or H) + H 3 N – O H C O C CH 2 SH Cisteina (Cys or C) – O

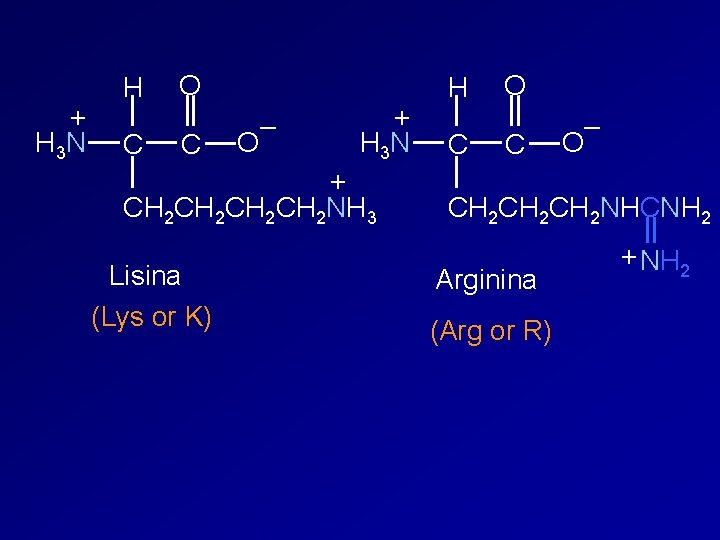
+ H 3 N H C O C – O + H 3 N + CH 2 CH 2 NH 3 Lisina (Lys or K) H C O C – O CH 2 CH 2 NHCNH 2 Arginina (Arg or R) + NH 2

Stereochimica degli Amminoacidi

La Glicina è achirale. Tutti gli altri ammino acidi presenti nelle proteine hanno L -configurazione al carbonio a. – CO 2 + H 3 N H R

Proprietà Acido-Base degli Amminoacidi

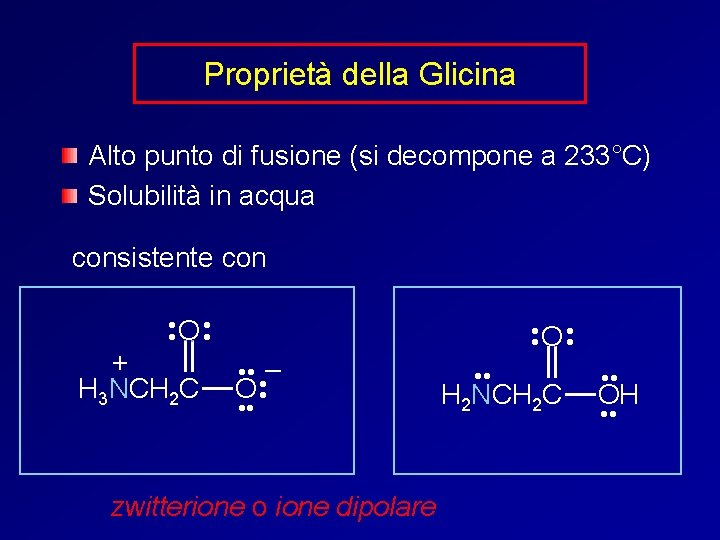
Proprietà della Glicina Alto punto di fusione (si decompone a 233°C) Solubilità in acqua consistente con • • O • • + H 3 NCH 2 C • • • – O • • • zwitterione o ione dipolare • • O • • H 2 NCH 2 C • • OH • •

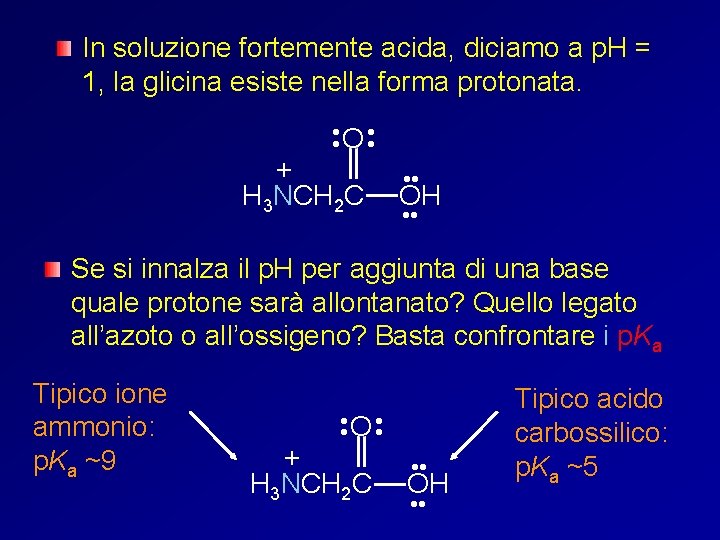
In soluzione fortemente acida, diciamo a p. H = 1, la glicina esiste nella forma protonata. • • O • • + H 3 NCH 2 C • • OH • • Se si innalza il p. H per aggiunta di una base quale protone sarà allontanato? Quello legato all’azoto o all’ossigeno? Basta confrontare i p. Ka Tipico ione ammonio: p. Ka ~9 • • O • • + H 3 NCH 2 C • • OH • • Tipico acido carbossilico: p. Ka ~5

La forma neutra più stabile della glicina è lo ione dipolare • • O • • + H 3 NCH 2 C • • • – O • • • Il p. Ka sperimentale della glicina è 2. 34. L’acidità maggiore di quella di un tipico acido carbossilico si giustifica con l’azione elettronattrice stabilizzante del gruppo ammonio.

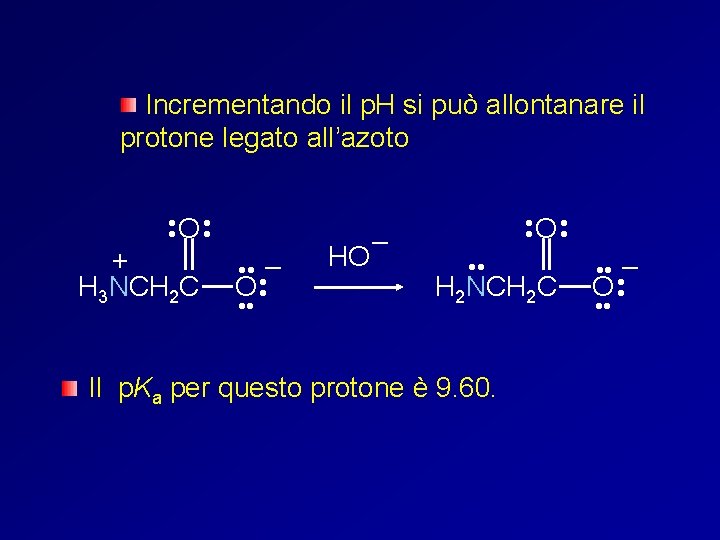
Incrementando il p. H si può allontanare il protone legato all’azoto • • O • • + H 3 NCH 2 C • • • – O • • • HO – • • O • • H 2 NCH 2 C Il p. Ka per questo protone è 9. 60. • • • – O • • •

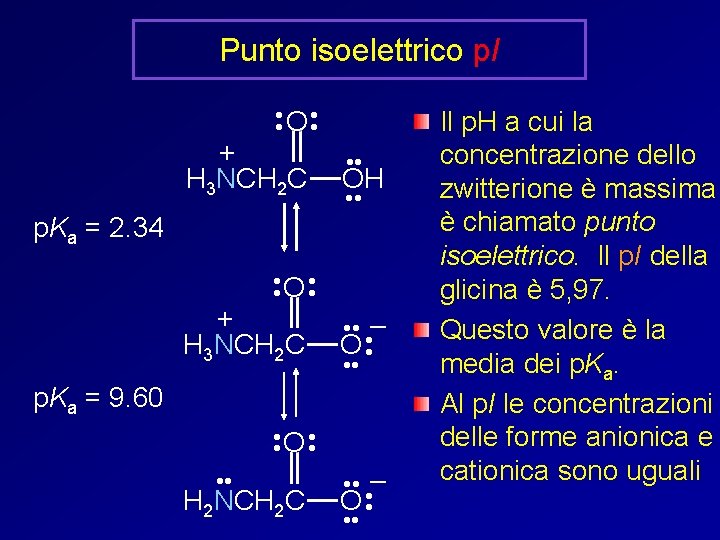
Punto isoelettrico p. I • • O • • + H 3 NCH 2 C p. Ka = 2. 34 • • OH • • O • • + H 3 NCH 2 C • • • – O • • • p. Ka = 9. 60 • • O • • H 2 NCH 2 C • • • – O • • • Il p. H a cui la concentrazione dello zwitterione è massima è chiamato punto isoelettrico. Il p. I della glicina è 5, 97. Questo valore è la media dei p. Ka. Al p. I le concentrazioni delle forme anionica e cationica sono uguali

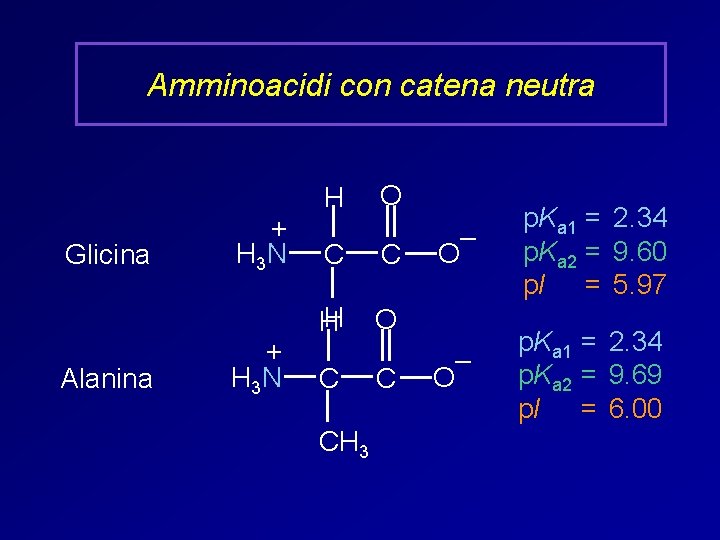
Amminoacidi con catena neutra Glicina Alanina + H 3 N H O C C H H O C CH 3 C – O p. Ka 1 = p. Ka 2 = p. I = 2. 34 9. 60 5. 97 – O p. Ka 1 = 2. 34 p. Ka 2 = 9. 69 p. I = 6. 00

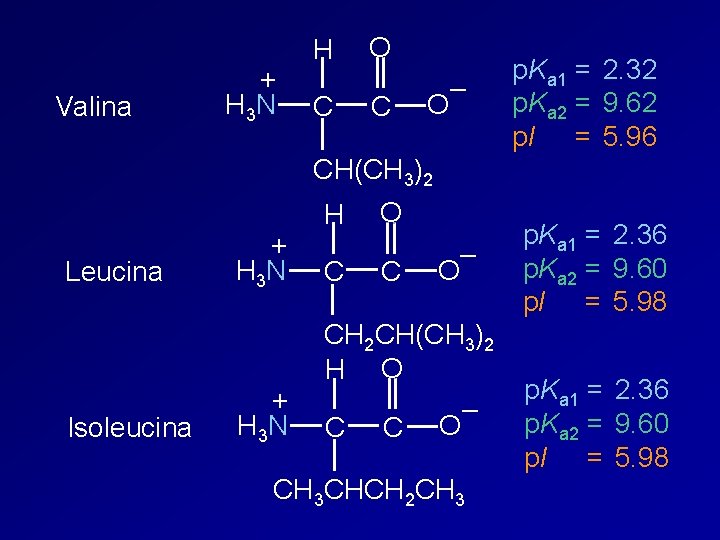
Valina + H 3 N H C O C – O p. Ka 1 = 2. 32 p. Ka 2 = 9. 62 p. I = 5. 96 CH(CH 3)2 Leucina Isoleucina H O + H 3 N CH 2 CH(CH 3)2 H O – C C O C – O CH 3 CHCH 2 CH 3 p. Ka 1 = p. Ka 2 = p. I = 2. 36 9. 60 5. 98

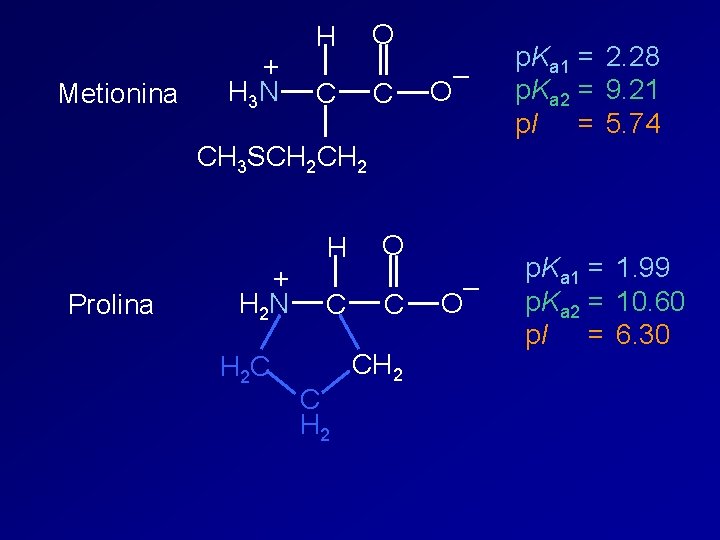
Metionina + H 3 N O H C C – O p. Ka 1 = p. Ka 2 = p. I = 2. 28 9. 21 5. 74 CH 3 SCH 2 Prolina + H 2 N H 2 C H C C H 2 O C CH 2 – O p. Ka 1 = 1. 99 p. Ka 2 = 10. 60 p. I = 6. 30

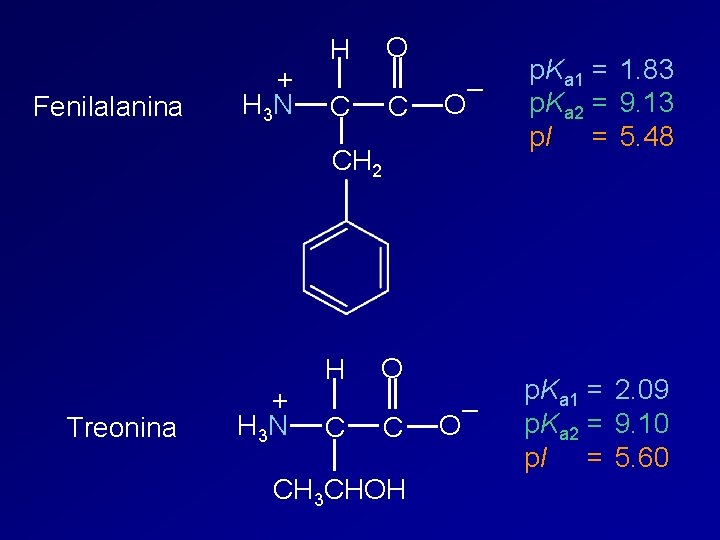
Fenilalanina + H 3 N O H C C – O p. Ka 1 = 1. 83 p. Ka 2 = 9. 13 p. I = 5. 48 – O p. Ka 1 = p. Ka 2 = p. I = CH 2 Treonina + H 3 N H C O C CH 3 CHOH 2. 09 9. 10 5. 60

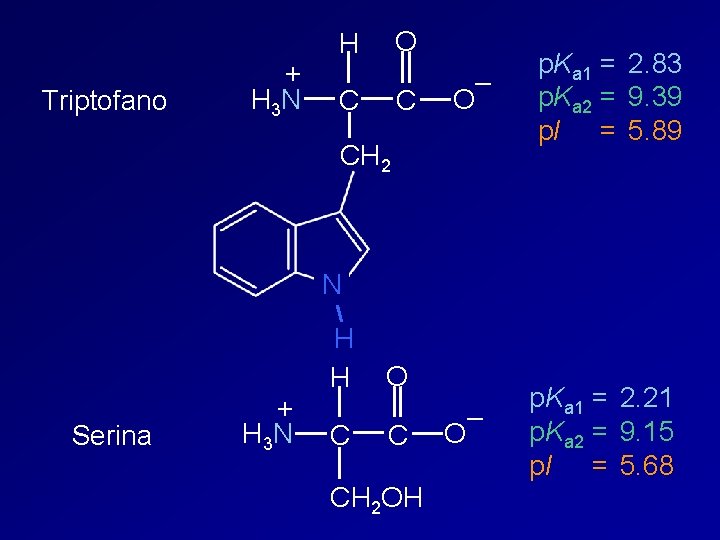
Triptofano + H 3 N O H C C – O p. Ka 1 = 2. 83 p. Ka 2 = 9. 39 p. I = 5. 89 – O p. Ka 1 = p. Ka 2 = p. I = CH 2 N Serina + H 3 N H H C O C CH 2 OH 2. 21 9. 15 5. 68

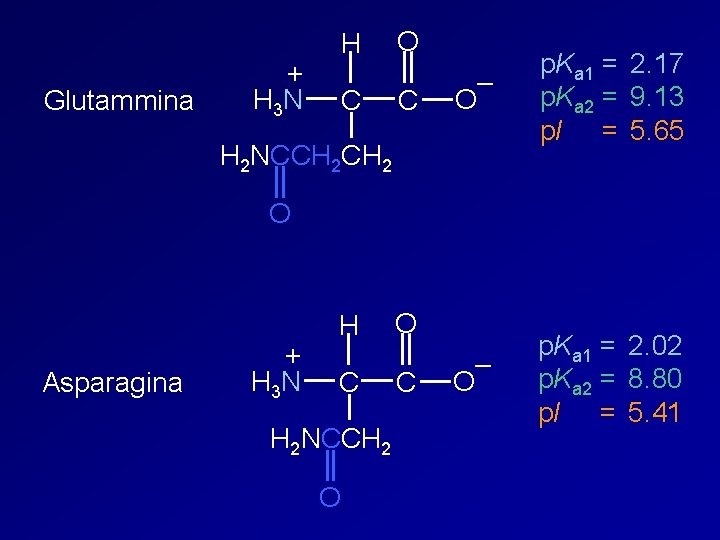
Glutammina + H 3 N H C O C – O p. Ka 1 = 2. 17 p. Ka 2 = 9. 13 p. I = 5. 65 – O p. Ka 1 = 2. 02 p. Ka 2 = 8. 80 p. I = 5. 41 H 2 NCCH 2 O Asparagina + H 3 N H C H 2 NCCH 2 O O C

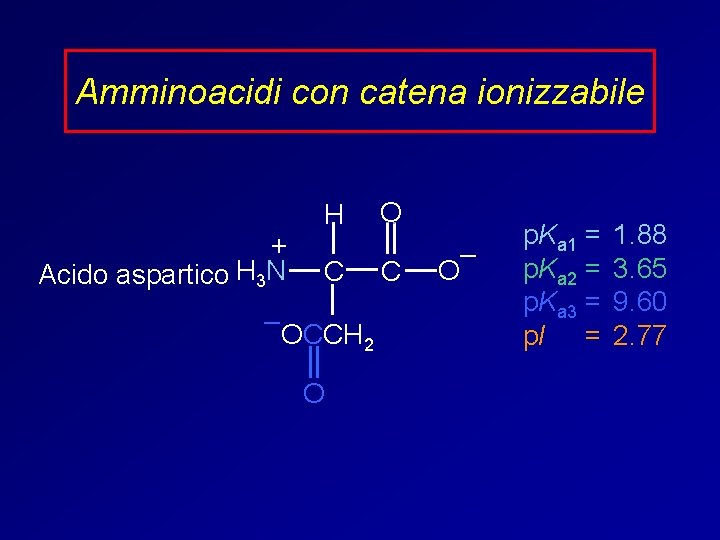
Amminoacidi con catena ionizzabile + Acido aspartico H 3 N H C – OCCH 2 O O C – O p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 1. 88 3. 65 9. 60 2. 77

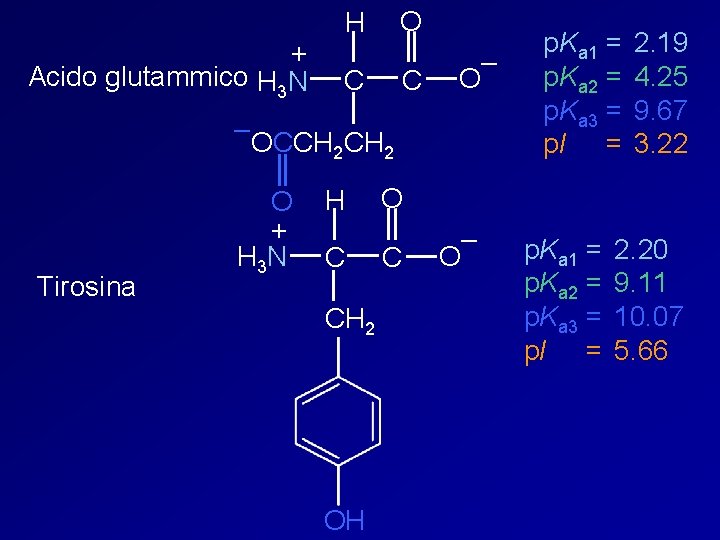
+ Acido glutammico H 3 N O H C C – OCCH 2 Tirosina O + H 3 N H C CH 2 OH p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 2. 19 4. 25 9. 67 3. 22 O C – O p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 2. 20 9. 11 10. 07 5. 66

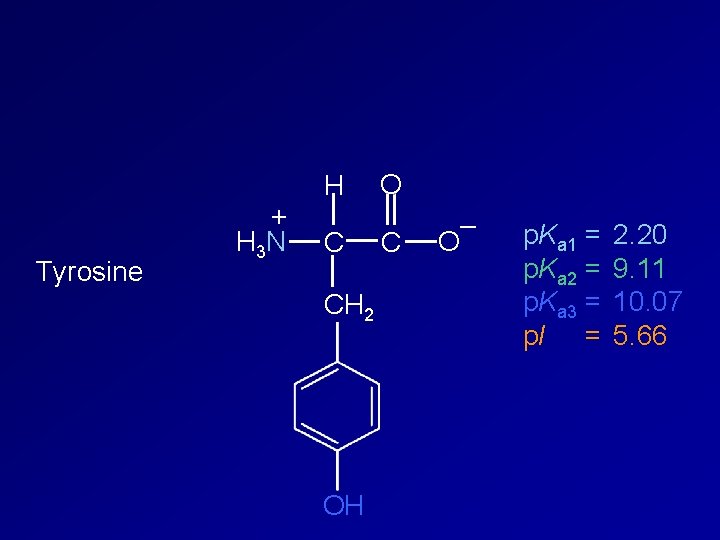
Tyrosine + H 3 N H C CH 2 OH O C – O p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 2. 20 9. 11 10. 07 5. 66

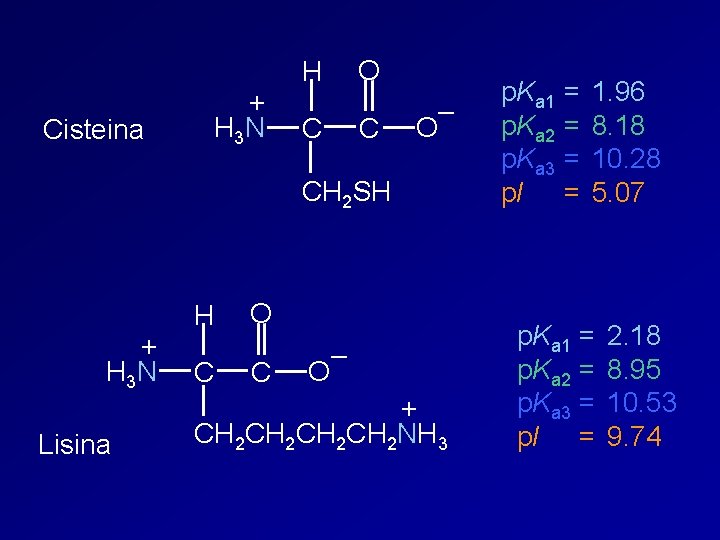
Cisteina + H 3 N H C O C – O CH 2 SH + H 3 N Lisina H C O C – O + CH 2 CH 2 NH 3 p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 1. 96 8. 18 10. 28 5. 07 p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 2. 18 8. 95 10. 53 9. 74

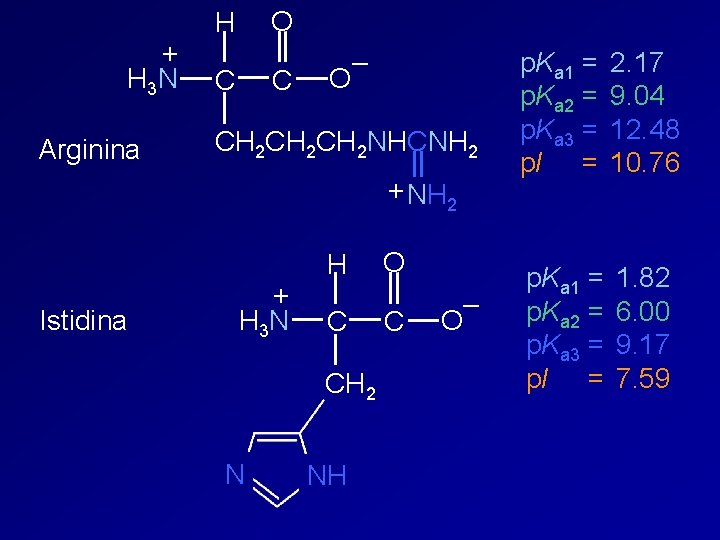
+ H 3 N Arginina O H C C – O CH 2 CH 2 NHCNH 2 + NH 2 Istidina + H 3 N H C CH 2 N NH O C – O p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 2. 17 9. 04 12. 48 10. 76 p. Ka 1 = p. Ka 2 = p. Ka 3 = p. I = 1. 82 6. 00 9. 17 7. 59

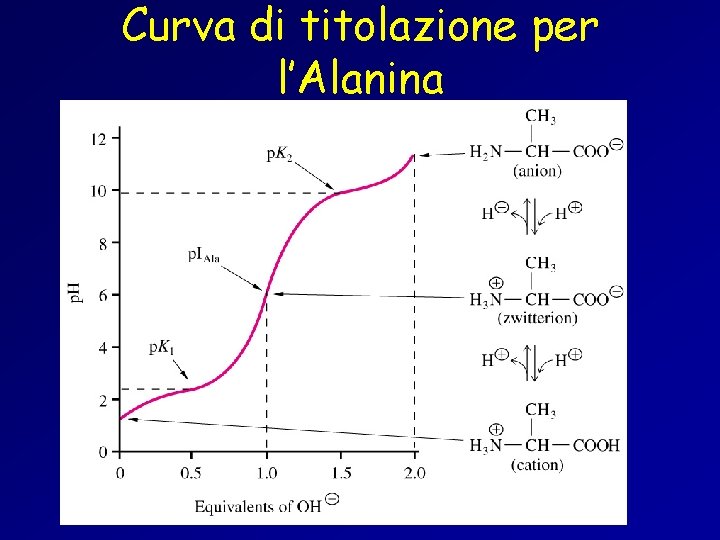
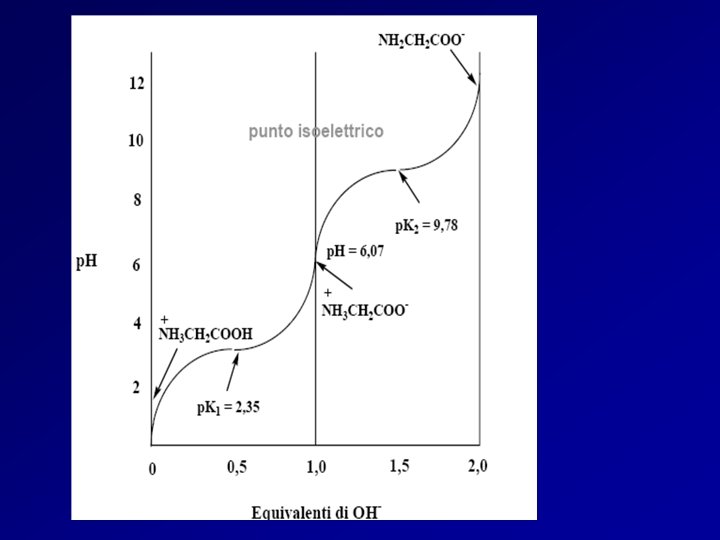
Curva di titolazione per l’Alanina


Sintesi degli Amminoacidi

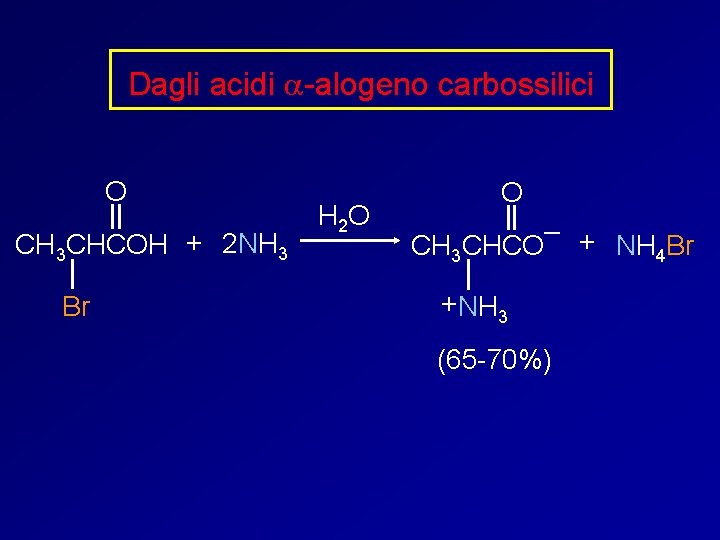
Dagli acidi a-alogeno carbossilici O CH 3 CHCOH + 2 NH 3 Br H 2 O O – CH 3 CHCO + NH 4 Br + NH 3 (65 -70%)

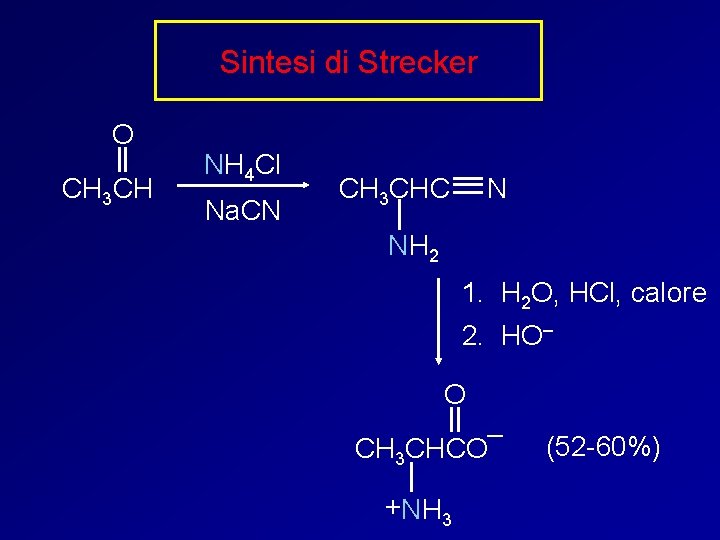
Sintesi di Strecker O CH 3 CH NH 4 Cl Na. CN CH 3 CHC N NH 2 1. H 2 O, HCl, calore 2. HO– O – CH 3 CHCO + NH 3 (52 -60%)

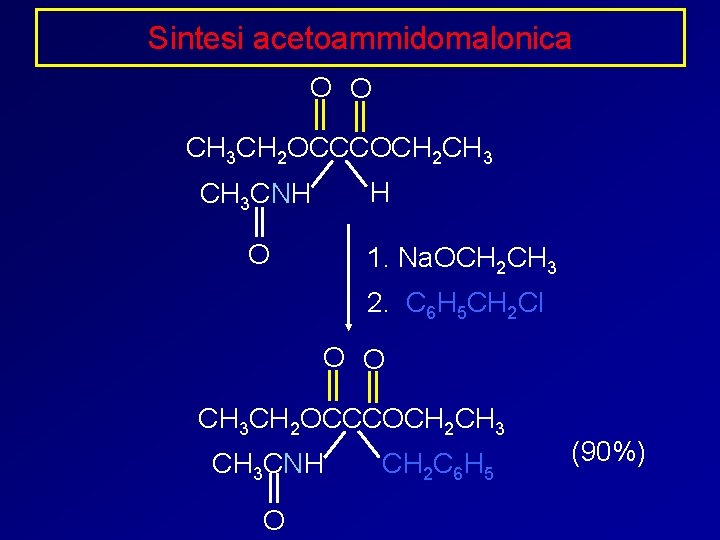
Sintesi acetoammidomalonica O O CH 3 CH 2 OCCCOCH 2 CH 3 H CH 3 CNH O 1. Na. OCH 2 CH 3 2. C 6 H 5 CH 2 Cl O O CH 3 CH 2 OCCCOCH 2 CH 3 CNH O CH 2 C 6 H 5 (90%)

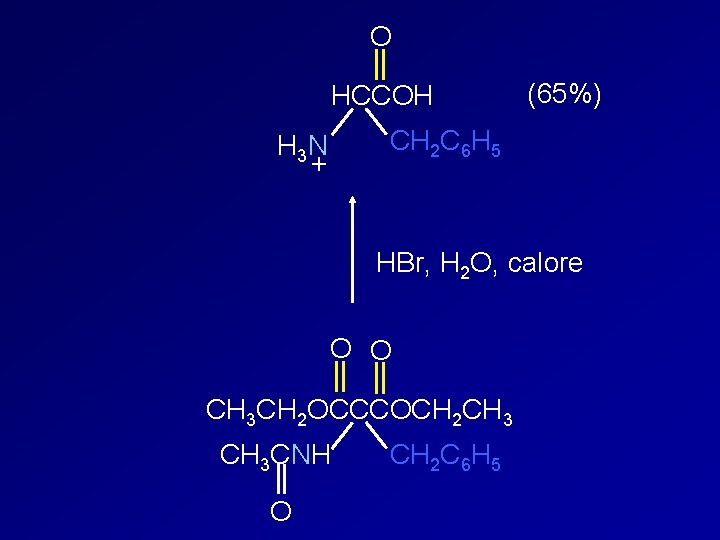
O HCCOH (65%) CH 2 C 6 H 5 H 3 N + HBr, H 2 O, calore O O CH 3 CH 2 OCCCOCH 2 CH 3 CNH O CH 2 C 6 H 5

Reazioni degli Amminoacidi

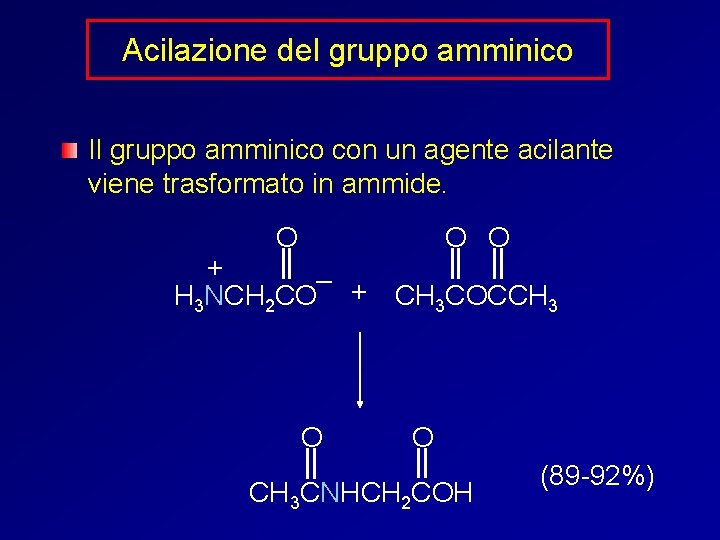
Acilazione del gruppo amminico Il gruppo amminico con un agente acilante viene trasformato in ammide. O O O + – + H 3 NCH 2 CO CH 3 COCCH 3 O O CH 3 CNHCH 2 COH (89 -92%)

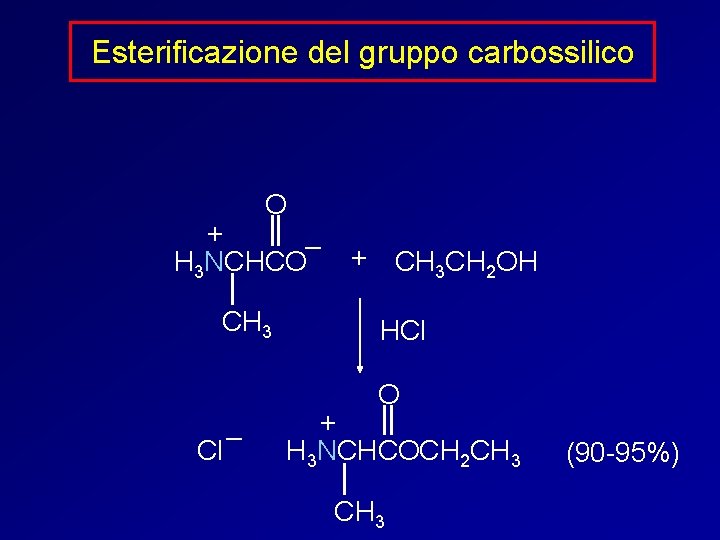
Esterificazione del gruppo carbossilico O + – H 3 NCHCO CH 3 + CH 3 CH 2 OH HCl O – Cl + H 3 NCHCOCH 2 CH 3 (90 -95%)

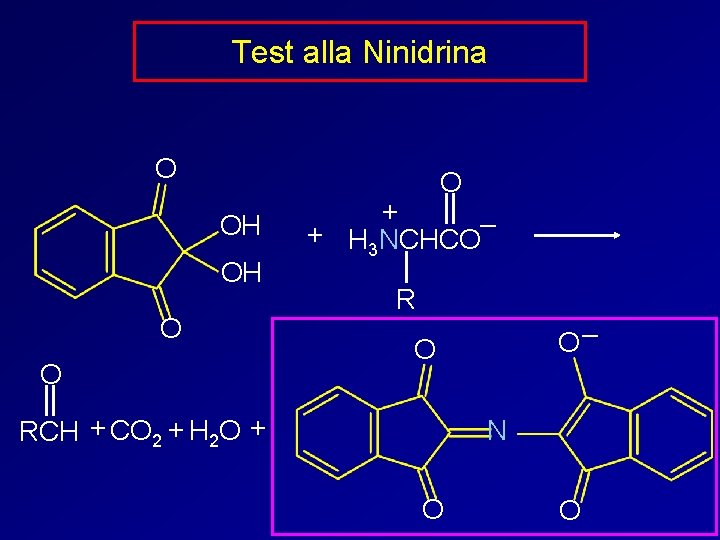
Test alla Ninidrina O O OH OH O O + + H 3 NCHCO– R O– O RCH + CO 2 + H 2 O + N O O

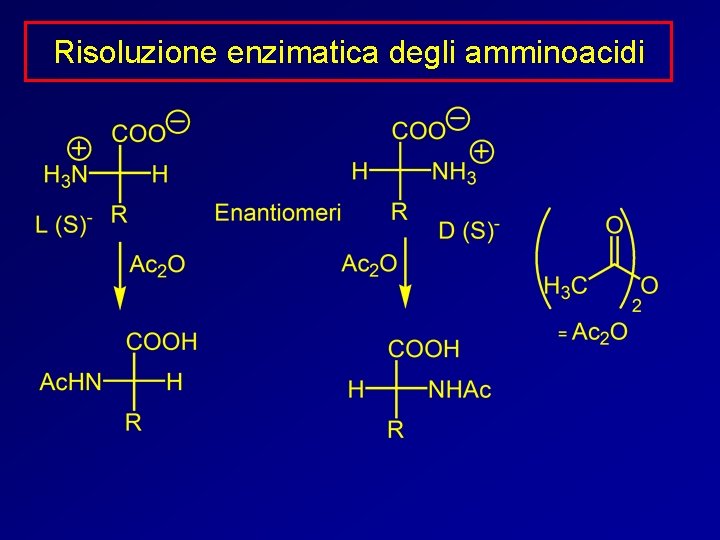
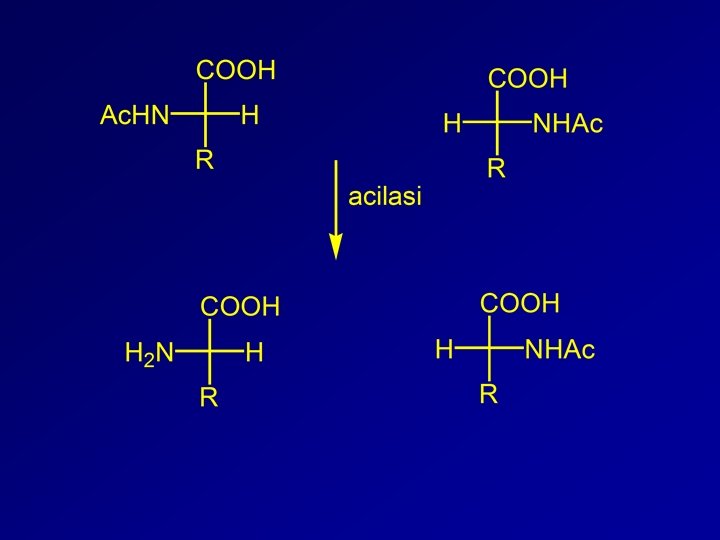
Risoluzione enzimatica degli amminoacidi


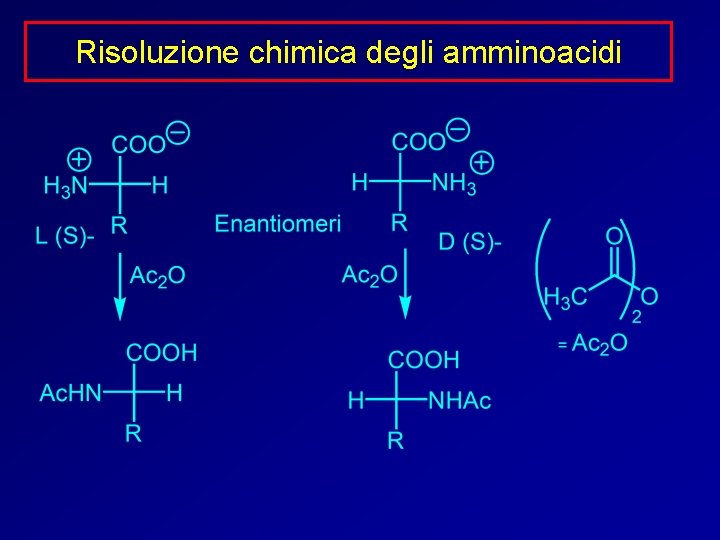
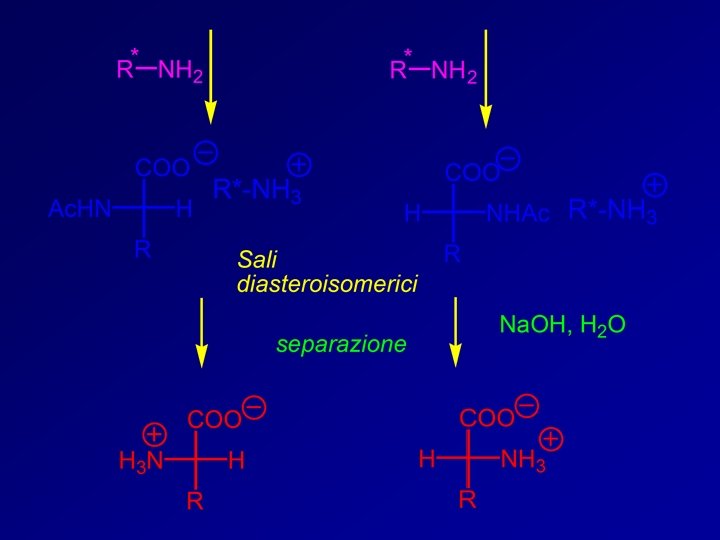
Risoluzione chimica degli amminoacidi


Peptidi

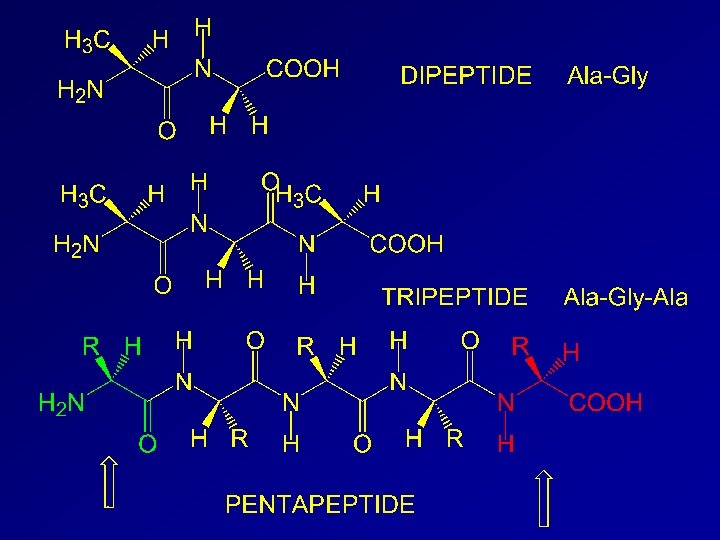
Peptidi I peptidi sono composti in cui un legame ammidico (legame peptidico) lega il gruppo amminico di un a-ammino acido con il gruppo carbossilico di un altro.

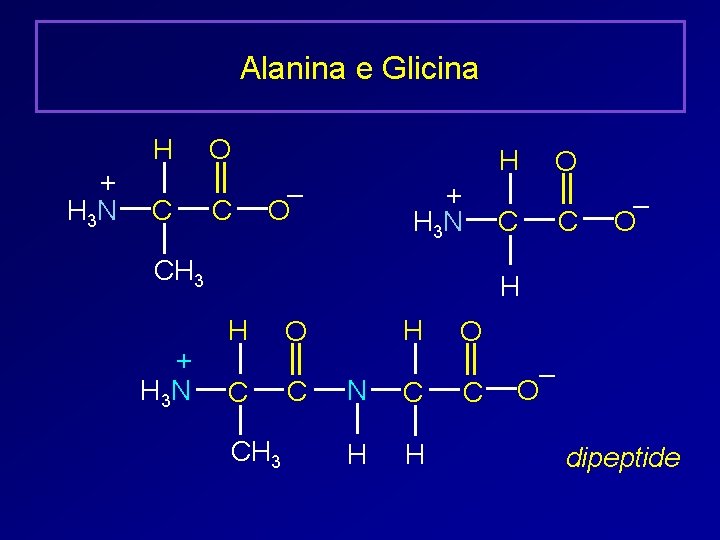
Alanina e Glicina H + H 3 N C O C H – O + H 3 N CH 3 + H 3 N O C C – O H H C CH 3 H O C N C H H O C – O dipeptide

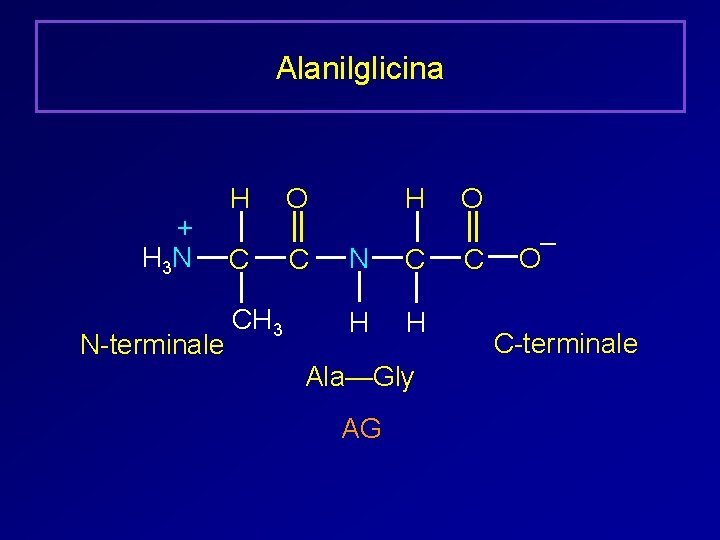
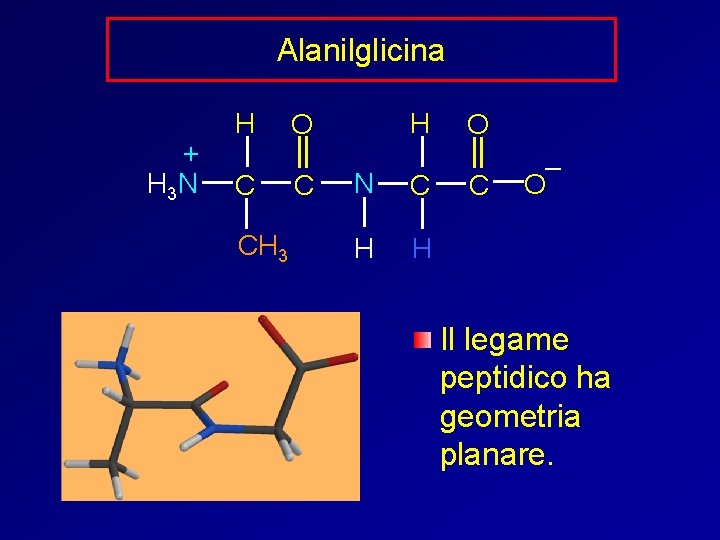
Alanilglicina + H 3 N N-terminale H C CH 3 H O C N C H H Ala—Gly AG O C – O C-terminale

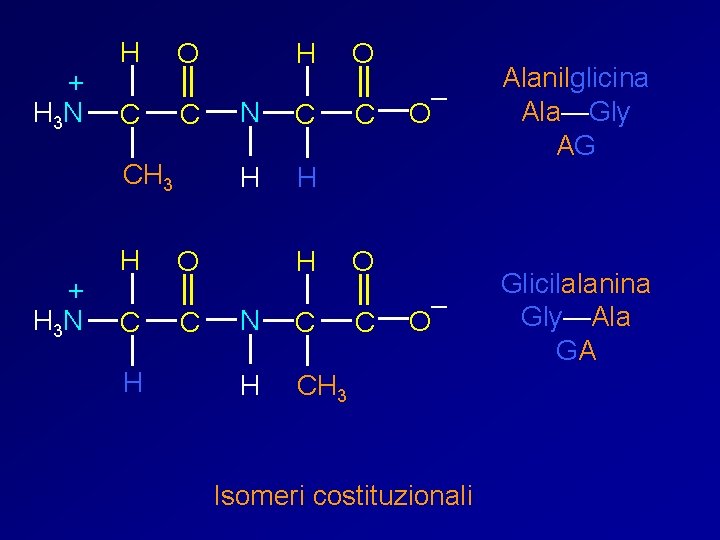
+ H 3 N H C C CH 3 + H 3 N H C H H O N C H H H O C N C H CH 3 O C – O Alanilglicina Ala—Gly AG – O Glicilalanina Gly—Ala GA O C Isomeri costituzionali

Alanilglicina + H 3 N H C CH 3 H O C N C H H O C – O Il legame peptidico ha geometria planare.



Determinazione della struttura di un Peptide

Struttura primaria La struttura primaria è data dalla sequenza di amminoacidi e dai ponti disolfuro Strategia (Sanger) Premio Nobel per la Chimica 1958 e 1980 Sequenza dei peptidi

1. Determinazione degli amminoacidi presenti e loro rapporto molare. 2. Scissione del peptide in frammenti e determinazione della composizione amminoacilica dei frammenti. 3. Identificazione degli amminoacidi Nterminale e C-terminale nel peptide e nei frammenti. 4. Organizzzione delle informazioni fino a defenire la sequenza.

L’idrolisi acida del peptide (6 M HCl, 24 hr) porta alla miscela degli amminoacidi. La miscela può essere smistata nei suoi componenti mediante cromatografia a scambio ionico, che dipende dal p. I degli amminoacidi. Gli amminoacidi sono evidenziati mediante ninidrina. Un analizzatore automatico richiede solo 10 -5 - 10 -7 g di peptide. L’idrolisi acida scinde tutti i legami peptidici, per ottenere frammenti bisogna condurre un’idrolisi parziale mediante enzimi.

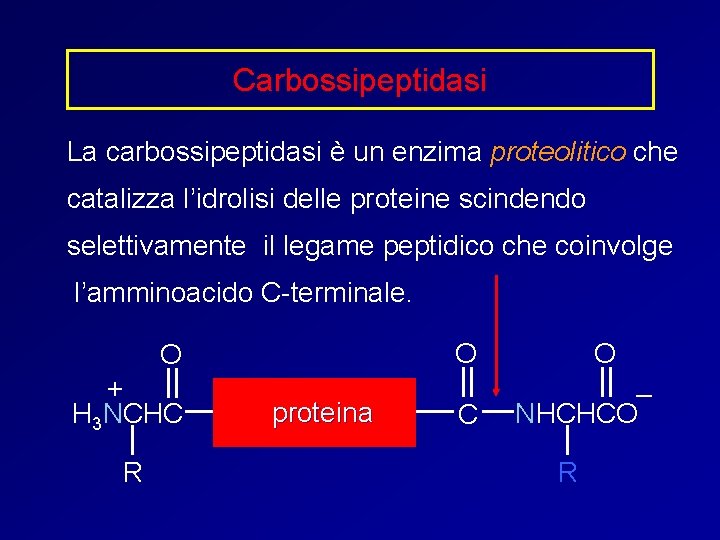
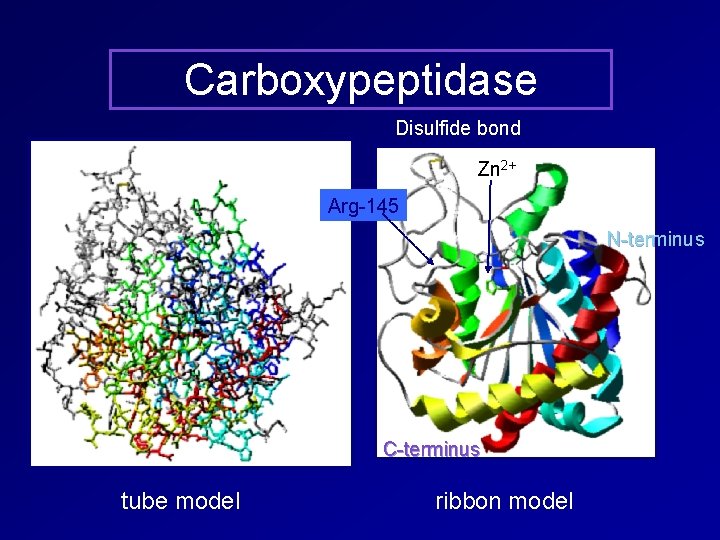
Carbossipeptidasi La carbossipeptidasi è un enzima proteolitico che catalizza l’idrolisi delle proteine scindendo selettivamente il legame peptidico che coinvolge l’amminoacido C-terminale. O O + H 3 NCHC R proteina C O – NHCHCO R

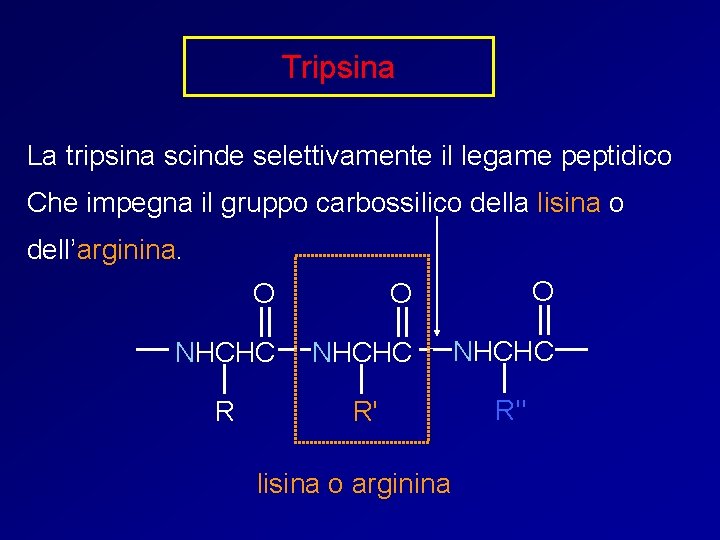
Tripsina La tripsina scinde selettivamente il legame peptidico Che impegna il gruppo carbossilico della lisina o dell’arginina. O O O NHCHC R R' R" lisina o arginina

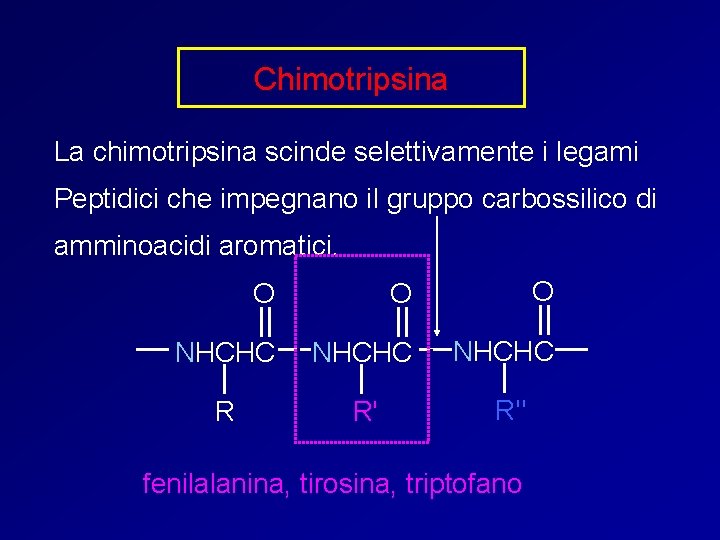
Chimotripsina La chimotripsina scinde selettivamente i legami Peptidici che impegnano il gruppo carbossilico di amminoacidi aromatici. O O O NHCHC R R' R" fenilalanina, tirosina, triptofano

Amminoacido N-terminale La sequenza amminoacilica è ambigua fino a che non si definiscono gli amminoacidi N- e Cterminali. L’amminoacido C-terminale può essere determinato mediante idrolisi enzimatica con carbossipeptidasi. E’ possibile determinare l’amminoacido Nterminale sfruttando il maggior carattere nucleofilo dedll’N terminale rispetto agli N ammidici.

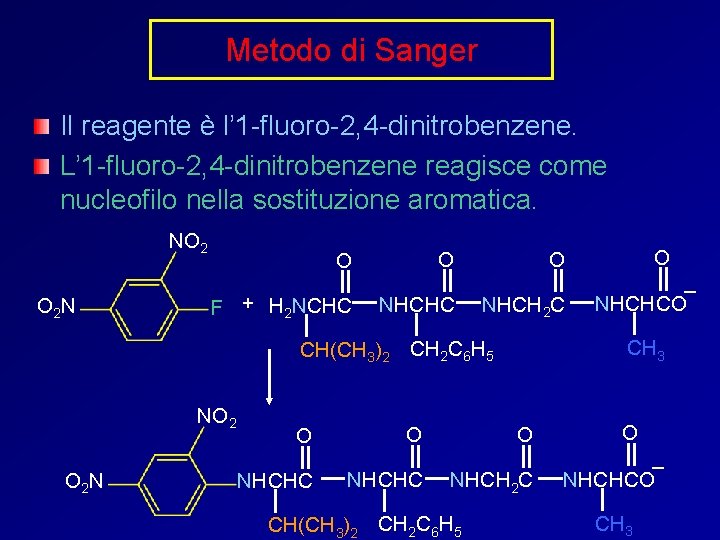
Metodo di Sanger Il reagente è l’ 1 -fluoro-2, 4 -dinitrobenzene. L’ 1 -fluoro-2, 4 -dinitrobenzene reagisce come nucleofilo nella sostituzione aromatica. NO 2 O 2 N O O F + H 2 NCHC NHCH 2 C O 2 N O O O NHCHC NHCH 2 C CH(CH 3)2 CH 2 C 6 H 5 – NHCHCO CH 3 CH(CH 3)2 CH 2 C 6 H 5 NO 2 O O O – NHCHCO CH 3

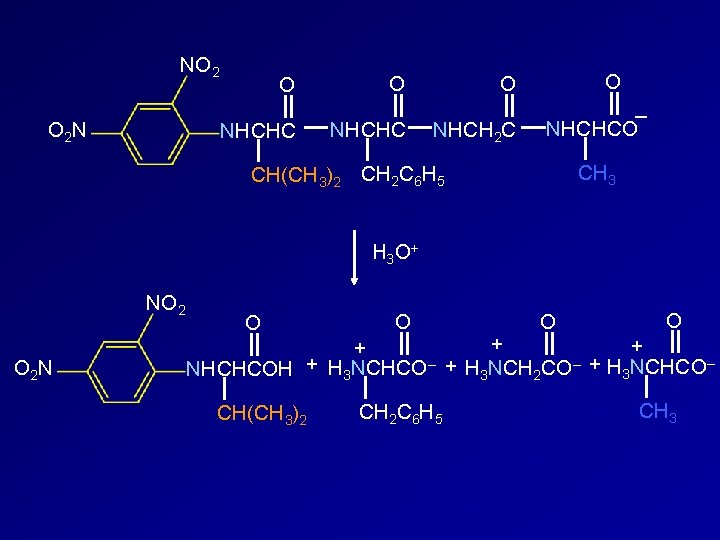
NO 2 O 2 N O O NHCHC O O NHCH 2 C – NHCHCO CH 3 CH(CH 3)2 CH 2 C 6 H 5 H 3 O + NO 2 O 2 N O O + + O O + NHCHCOH + H 3 NCHCO– + H 3 NCH 2 CO– + H 3 NCHCO– CH(CH 3)2 CH 2 C 6 H 5 CH 3

Insulina L’insulina è un polipeptide costituito da 51 amminoacidi. Ha due catene: quella A formata da 21 amminoacidi e quella B formata da 30 amminoacidi. FVNQHLCGSHLVGALYLVCGERGFFYTPKA Catena B

La fenilalanina (F) è N terminale. FVNQHLCGSHL SHLV LVGA VGAL ALY YLVC VCGERGF GFFYTPKA

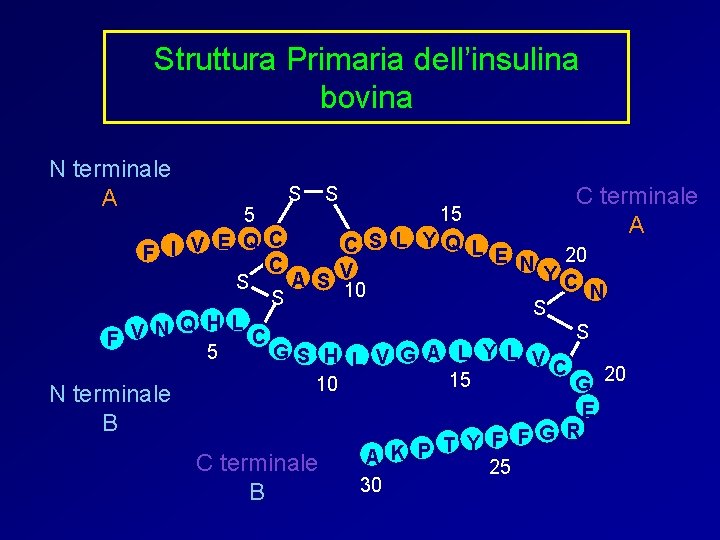
Struttura Primaria dell’insulina bovina N terminale A S S C terminale A 15 5 S L Y Q L E Q C V C I F 20 E N C YC A S V 10 S N S S N Q H LC V S F 5 G S H L V G A L Y L V C 20 15 10 G N terminale E B G R F F Y K P T A C terminale 25 30 B

Degradazione di Edman 1. Metodo per la determinazione dell’amminoacido N-terminale. 2. Può essere utilizzato in sequenza per determinare i primi 20 amminoacidi a partire dall’N-terminale. 3. Richiede campioni di solo 10 -10 g. 4. E’ stato automatizzato. N C S Fenil isotiocianato

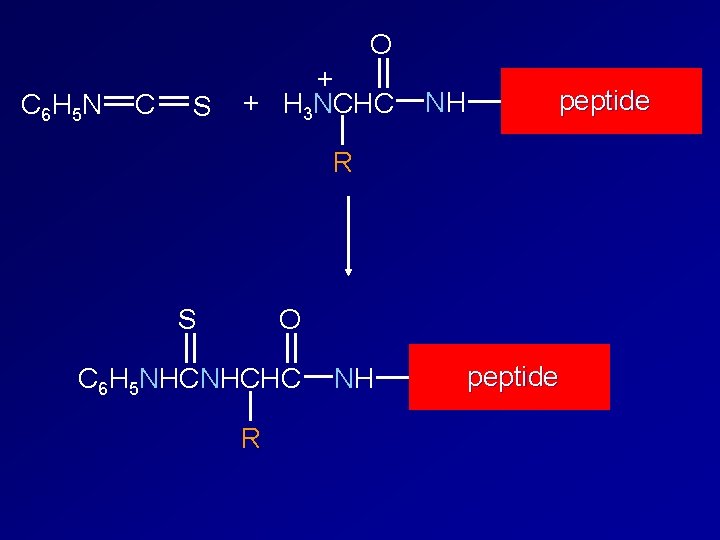
O C 6 H 5 N C S + + H 3 NCHC NH peptide R S O C 6 H 5 NHCNHCHC R NH peptide

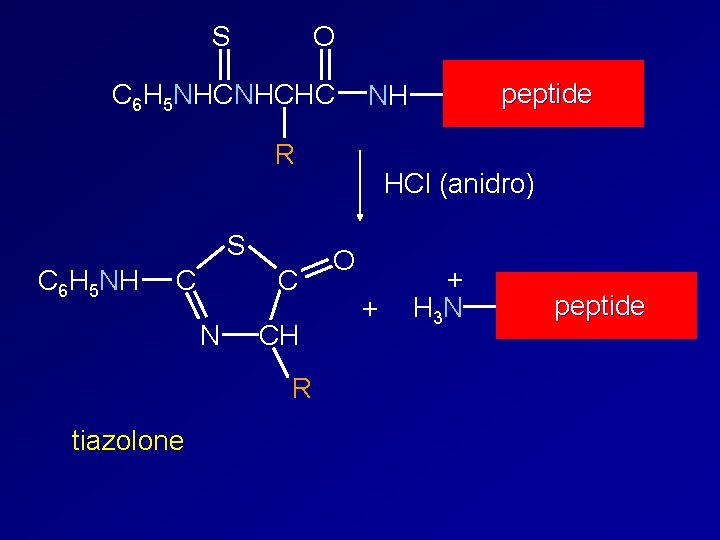
S O C 6 H 5 NHCNHCHC R S C 6 H 5 N H C C N CH R tiazolone peptide NH HCl (anidro) O + + H 3 N peptide

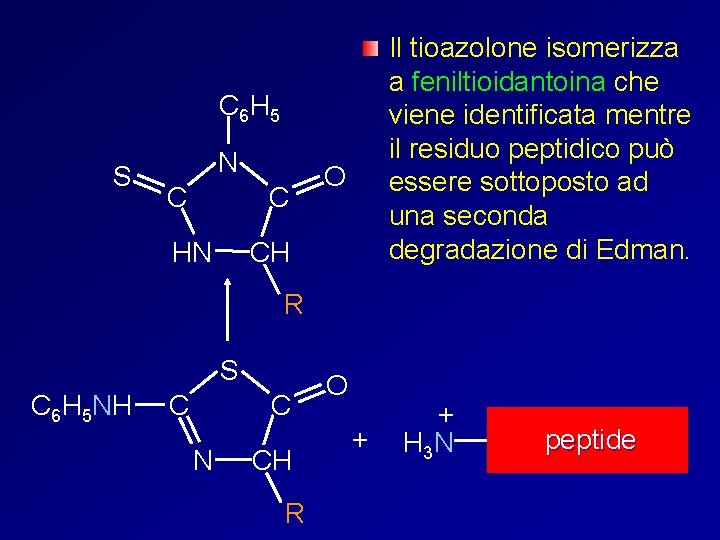
Il tioazolone isomerizza a feniltioidantoina che viene identificata mentre il residuo peptidico può essere sottoposto ad una seconda degradazione di Edman. C 6 H 5 S N C C O CH HN R S C 6 H 5 N H C C N CH R O + + H 3 N peptide

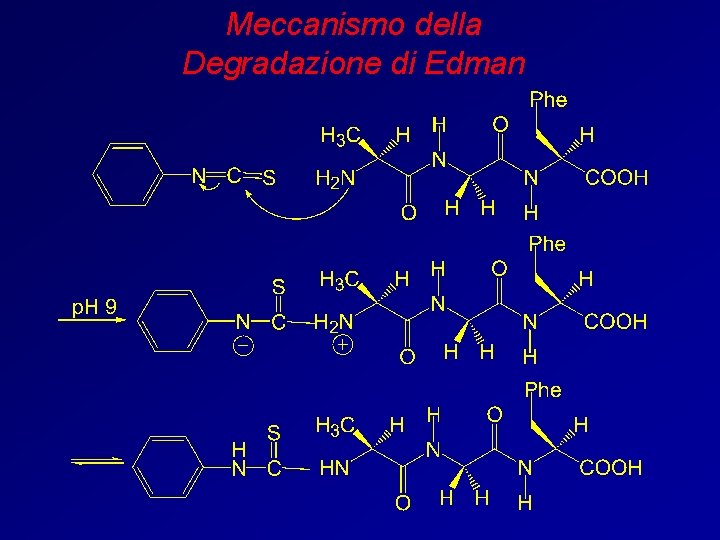
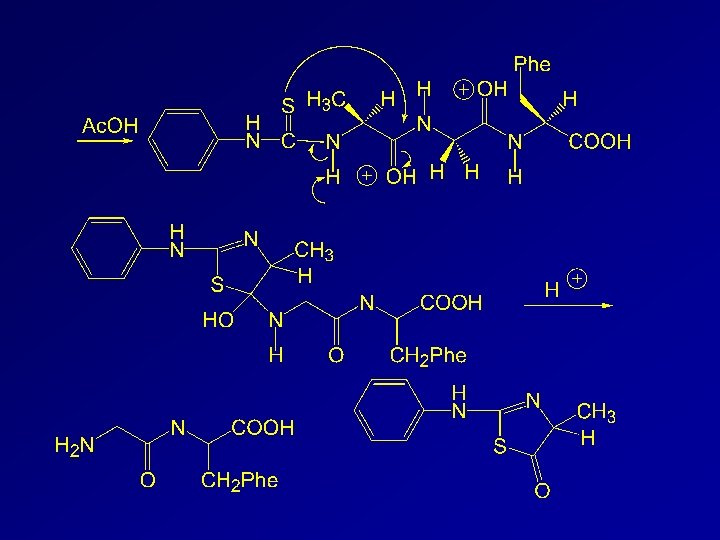
Meccanismo della Degradazione di Edman


Struttura Secondaria delle Proteine

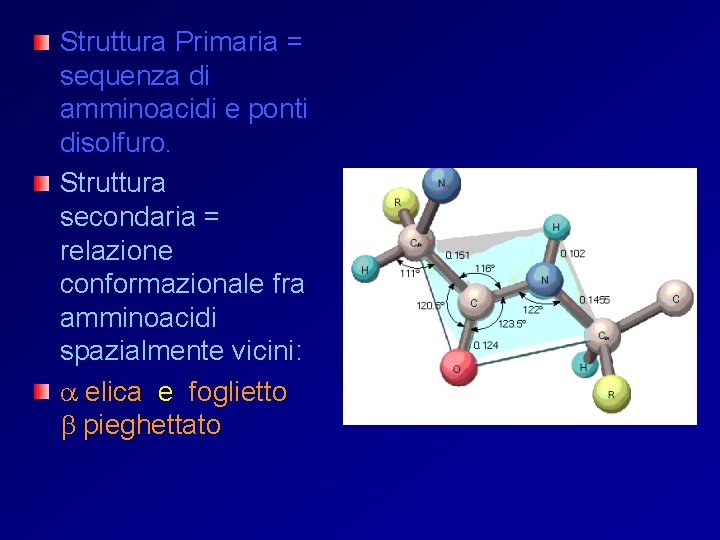
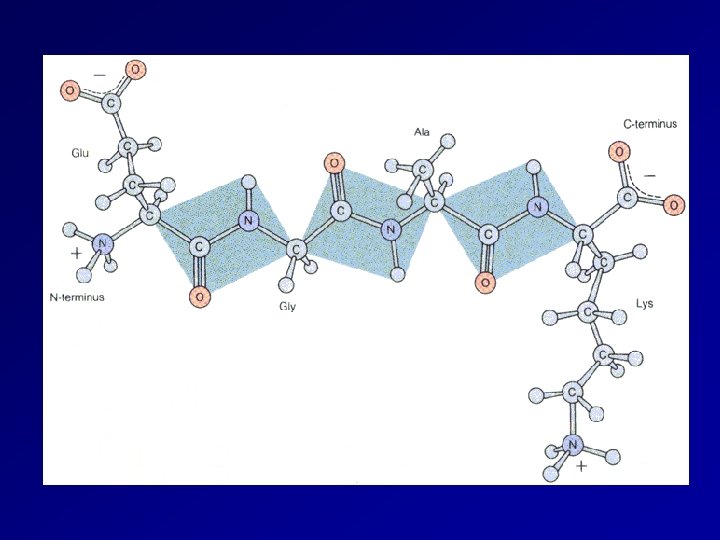
Struttura Primaria = sequenza di amminoacidi e ponti disolfuro. Struttura secondaria = relazione conformazionale fra amminoacidi spazialmente vicini: a elica e foglietto b pieghettato



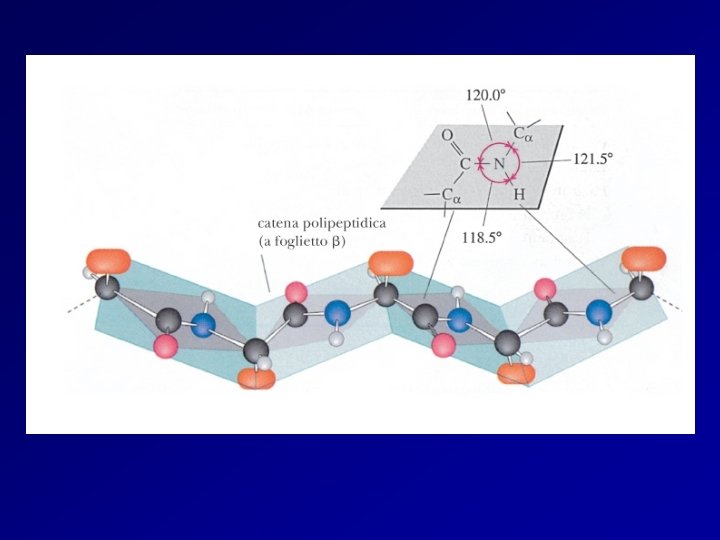
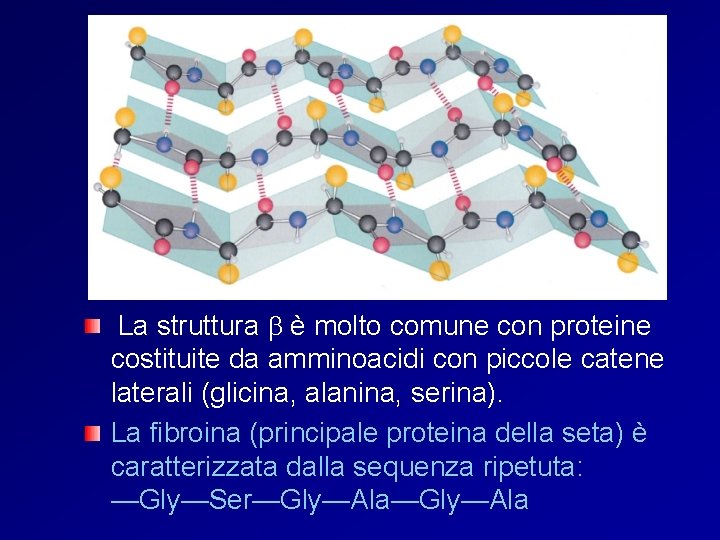
La struttura b è molto comune con proteine costituite da amminoacidi con piccole catene laterali (glicina, alanina, serina). La fibroina (principale proteina della seta) è caratterizzata dalla sequenza ripetuta: —Gly—Ser—Gly—Ala

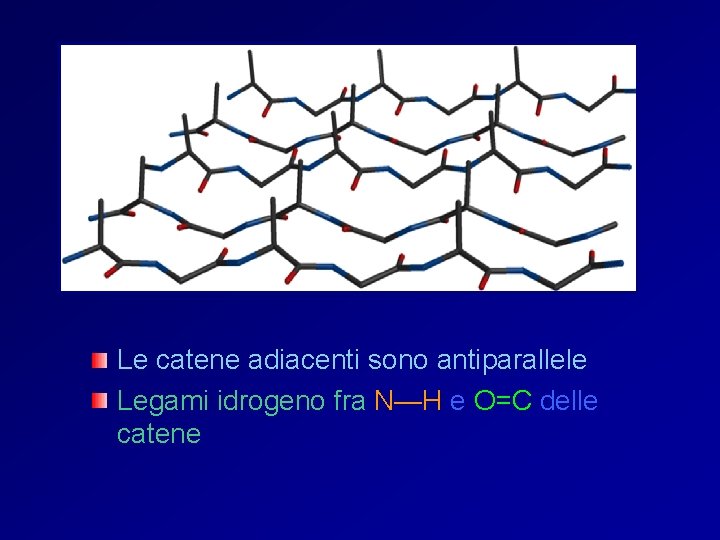
Le catene adiacenti sono antiparallele Legami idrogeno fra N—H e O=C delle catene

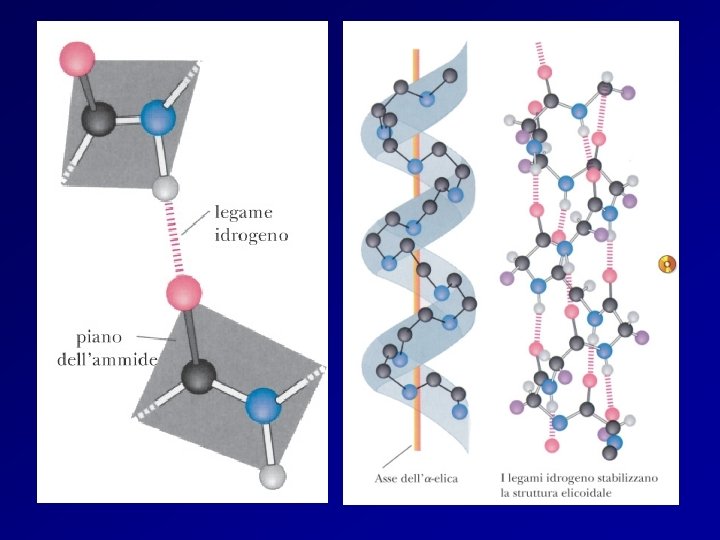
a Elica a elica di una proteina formata solo da L-alanina. L’elica è destrorsa con 3. 6 amminoacidi per giro. I legami idrogeno sono interni alla catena. Proteine dei muscoli (miosina) e della lana(a-cheratina) hanno una struttura a-elica.


Carboxypeptidase Disulfide bond Zn 2+ Arg-145 N-terminus C-terminus tube model ribbon model

Sintesi dei peptidi

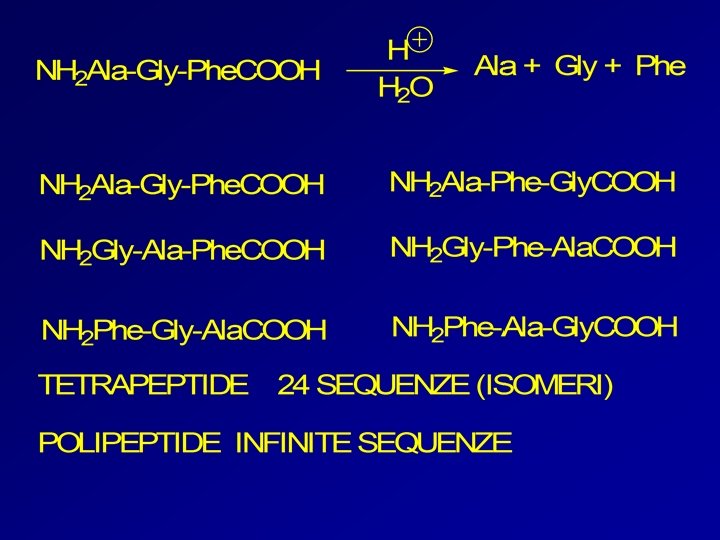
Il problema della sintesi dei peptidi è legato al fatto che devono reagire fra loro molecole bifunzionali per cui per ottenere la voluta sequenza non basta mettere insieme i due amminoacidi. Se ad esempio volendo la sequenza Phe—Gly mettessimo insieme fenil alanina e glicina otterremmo i quattro dipeptidi: Phe—Phe Gly—Gly Phe—Gly Gly— Phe Bisogna proteggere il gruppo anmminco dell’amminoacido che dovrà essere quello Nterminale ed il gruppo carbossilico di quello che sarà C-terminale

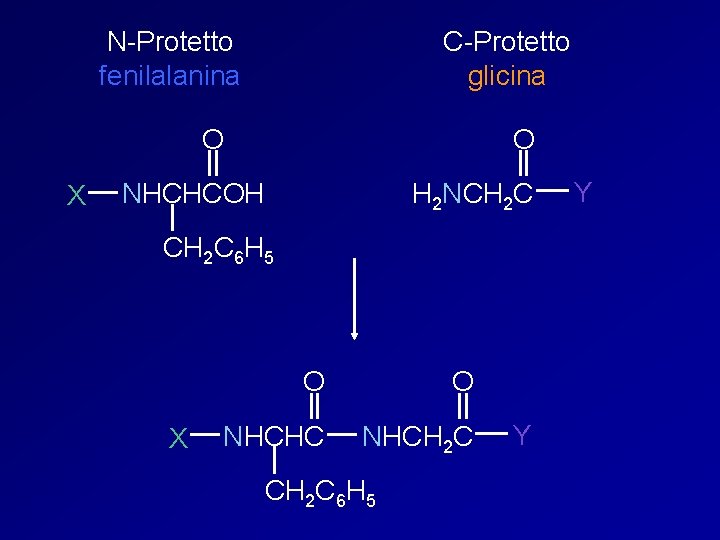
N-Protetto fenilalanina C-Protetto glicina O X O NHCHCOH H 2 NCH 2 C 6 H 5 X O O NHCHC NHCH 2 C 6 H 5 Y Y

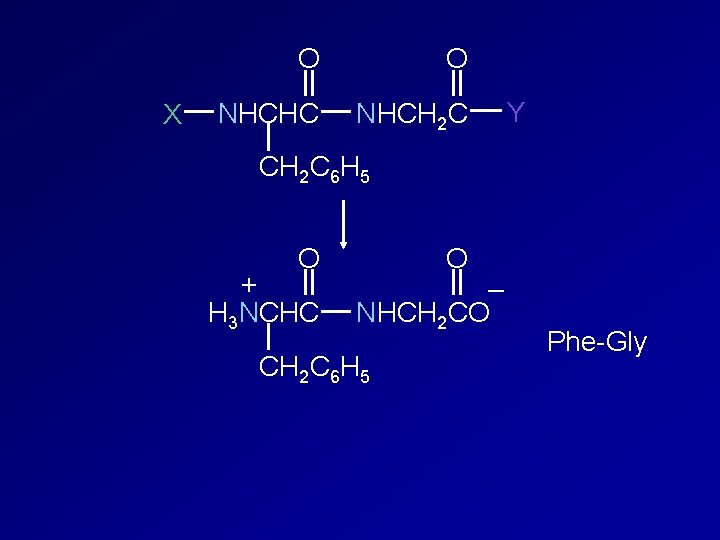
X O O NHCHC NHCH 2 C Y CH 2 C 6 H 5 O + H 3 NCHC O – NHCH 2 CO CH 2 C 6 H 5 Phe-Gly

Protezione gruppo amminico

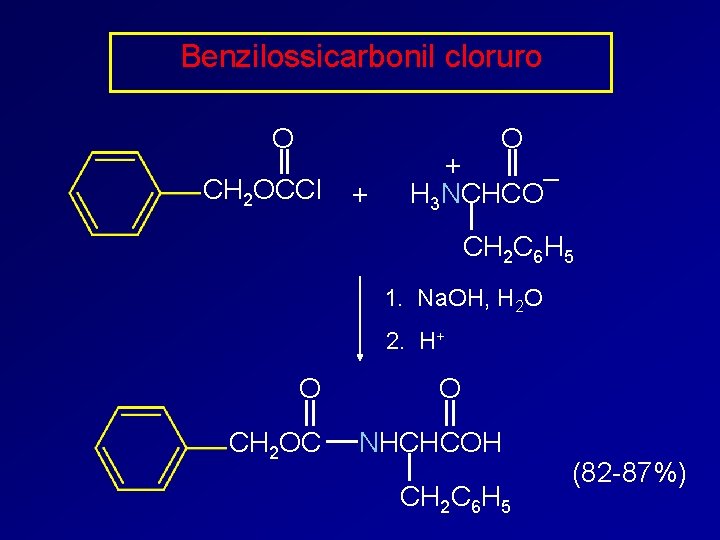
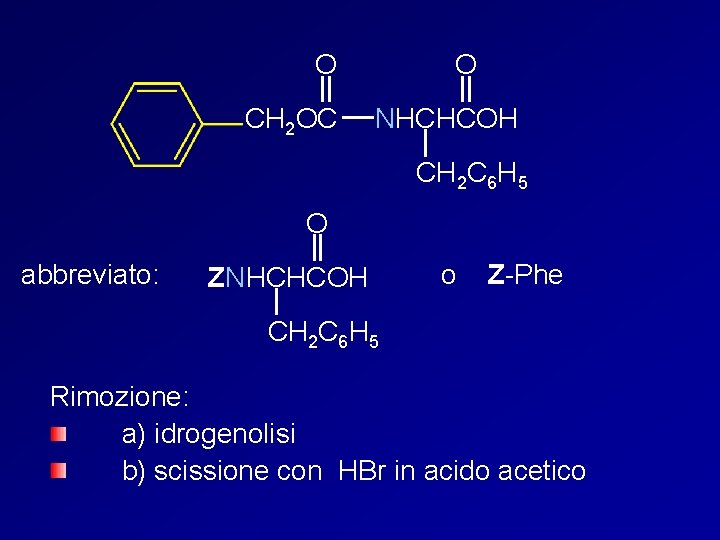
Benzilossicarbonil cloruro O O CH 2 OCCl + + – H 3 NCHCO CH 2 C 6 H 5 1. Na. OH, H 2 O 2. H+ O CH 2 OC O NHCHCOH CH 2 C 6 H 5 (82 -87%)

O CH 2 OC O NHCHCOH CH 2 C 6 H 5 O abbreviato: ZNHCHCOH o Z-Phe CH 2 C 6 H 5 Rimozione: a) idrogenolisi b) scissione con HBr in acido acetico

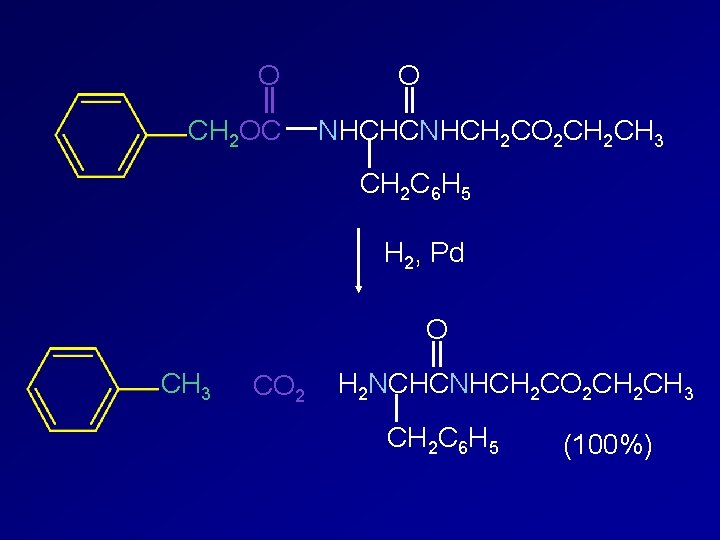
O CH 2 OC O NHCHCNHCH 2 CO 2 CH 3 CH 2 C 6 H 5 H 2, Pd O CH 3 CO 2 H 2 NCHCNHCH 2 CO 2 CH 3 CH 2 C 6 H 5 (100%)

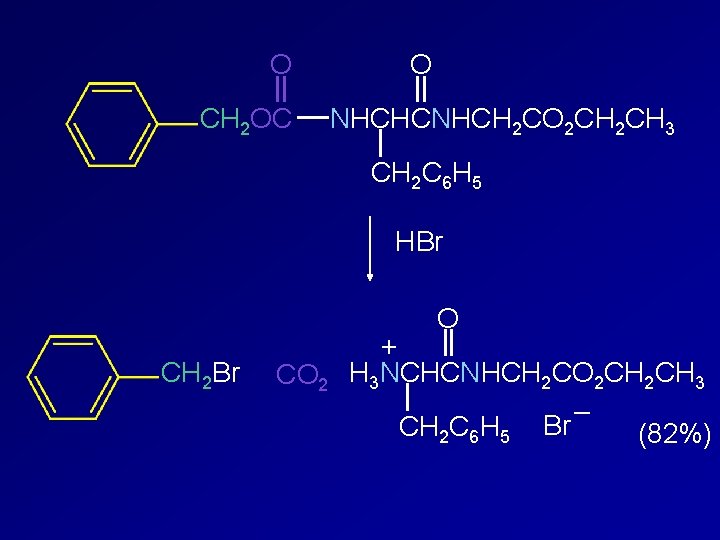
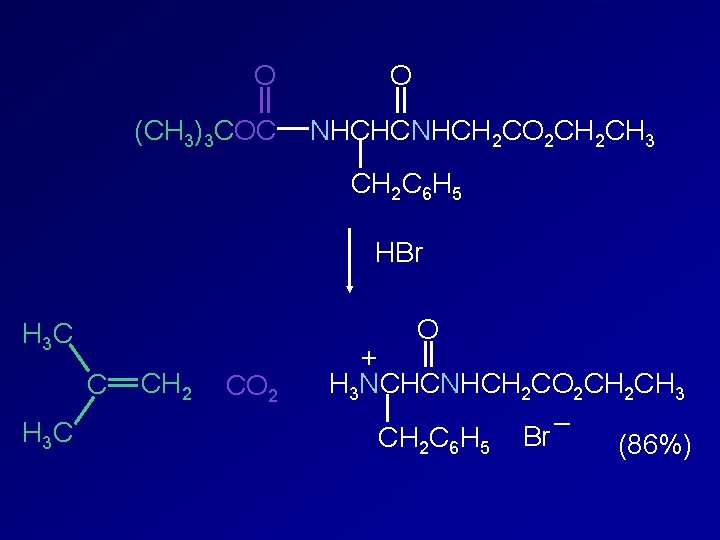
O CH 2 OC O NHCHCNHCH 2 CO 2 CH 3 CH 2 C 6 H 5 HBr O CH 2 Br CO 2 + H 3 NCHCNHCH 2 CO 2 CH 3 – CH 2 C 6 H 5 Br (82%)

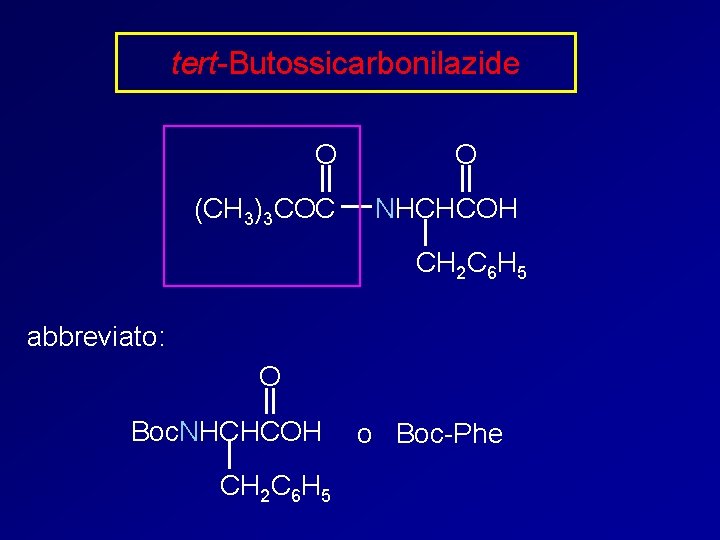
tert-Butossicarbonilazide O (CH 3)3 COC O NHCHCOH CH 2 C 6 H 5 abbreviato: O Boc. NHCHCOH CH 2 C 6 H 5 o Boc-Phe

O (CH 3)3 COC O NHCHCNHCH 2 CO 2 CH 3 CH 2 C 6 H 5 HBr O H 3 C CH 2 CO 2 + H 3 NCHCNHCH 2 CO 2 CH 3 – CH 2 C 6 H 5 Br (86%)

Protezione del gruppo Carbossilico

Deprotezione degli esteri avviene per idrolisi basica. Gli esteri benzilici possono essere subire idrogenolisi. Il gruppo carbossilico viene protetto come estere.

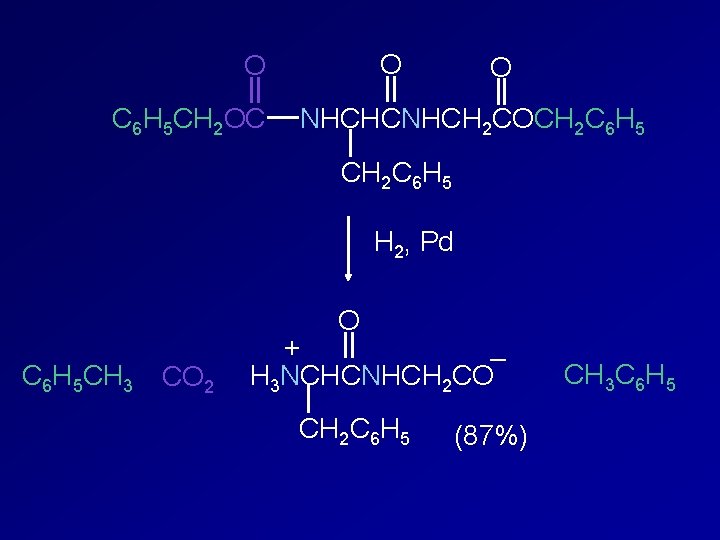
O O C 6 H 5 CH 2 OC O NHCHCNHCH 2 COCH 2 C 6 H 5 H 2, Pd O C 6 H 5 CH 3 CO 2 + – H 3 NCHCNHCH 2 CO CH 2 C 6 H 5 (87%) CH 3 C 6 H 5

Formazione del legame peptidico

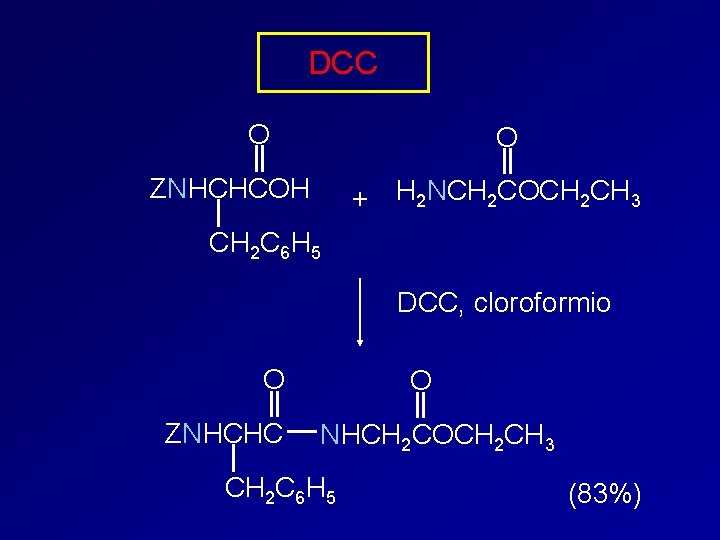
DCC O O ZNHCHCOH + H 2 NCH 2 COCH 2 CH 3 CH 2 C 6 H 5 DCC, cloroformio O ZNHCHC O NHCH 2 COCH 2 CH 3 CH 2 C 6 H 5 (83%)

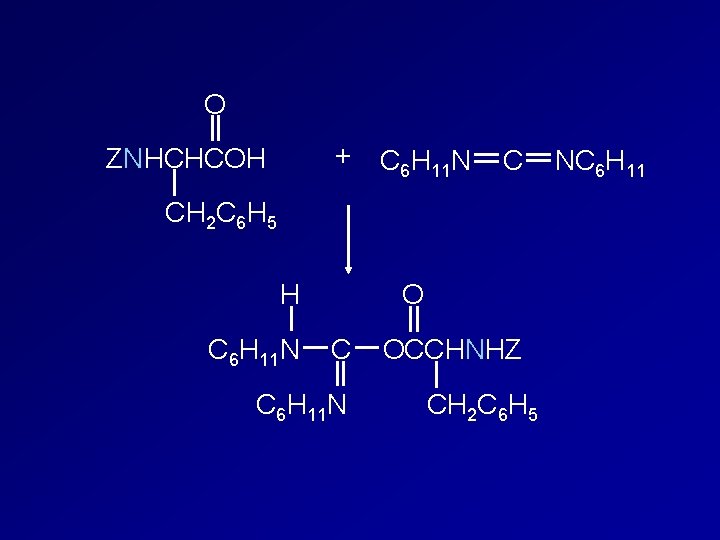
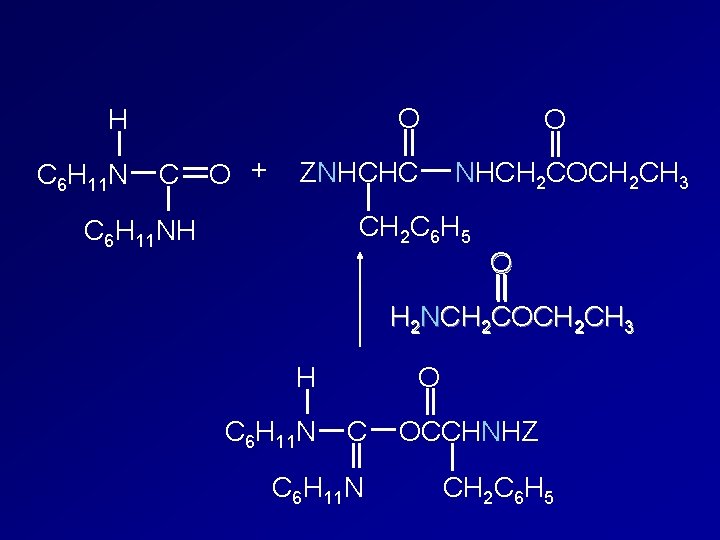
O + C 6 H 11 N ZNHCHCOH C CH 2 C 6 H 5 H C 6 H 11 N O C C 6 H 11 N OCCHNHZ CH 2 C 6 H 5 NC 6 H 11

O H C 6 H 11 N C O + ZNHCHC O NHCH 2 COCH 2 CH 3 CH 2 C 6 H 5 C 6 H 11 NH O H 2 NCH 2 COCH 2 CH 3 H C 6 H 11 N O C C 6 H 11 N OCCHNHZ CH 2 C 6 H 5

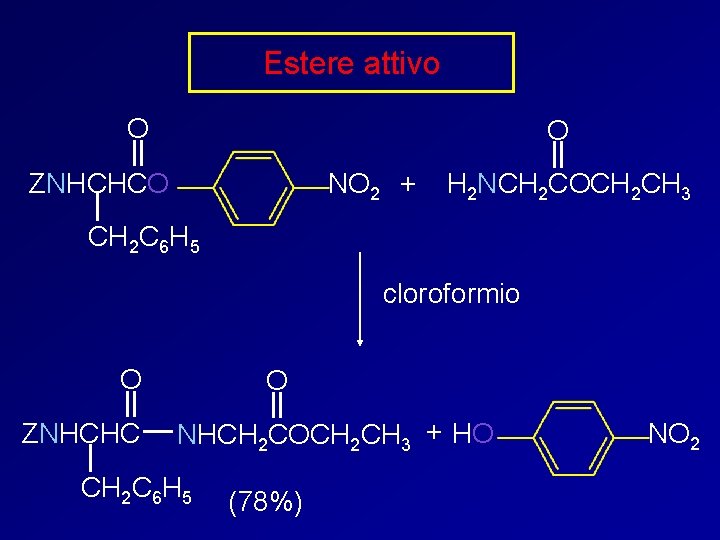
Estere attivo O O ZNHCHCO NO 2 + H 2 NCH 2 COCH 2 CH 3 CH 2 C 6 H 5 cloroformio O ZNHCHC O NHCH 2 COCH 2 CH 3 + HO CH 2 C 6 H 5 (78%) NO 2

Sintesi in fase solida: Merrifield Premio Nobel in Chimica: 1984

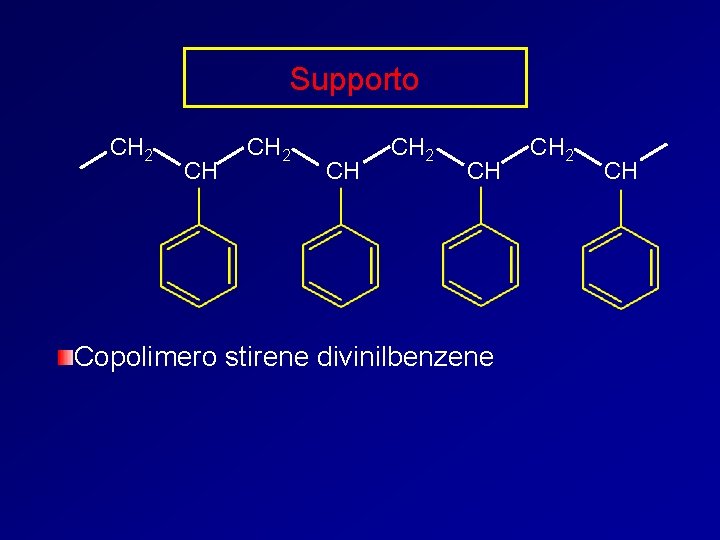
Supporto CH 2 CH Copolimero stirene divinilbenzene CH 2 CH

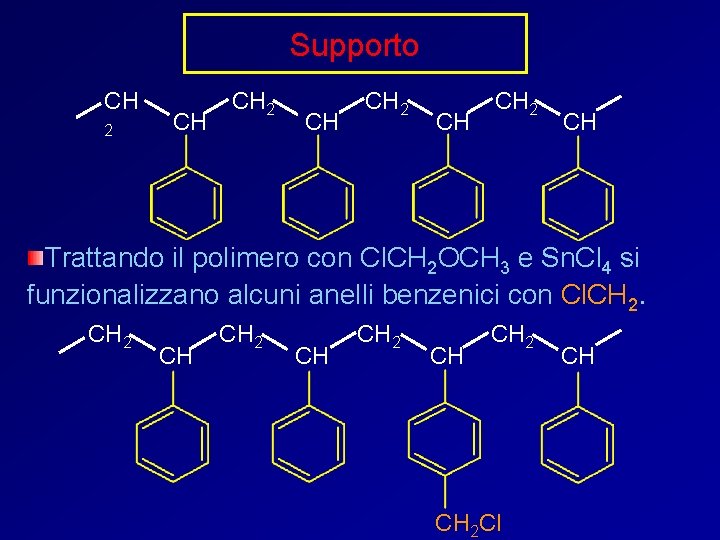
Supporto CH 2 CH Trattando il polimero con Cl. CH 2 OCH 3 e Sn. Cl 4 si funzionalizzano alcuni anelli benzenici con Cl. CH 2 CH CH 2 Cl CH

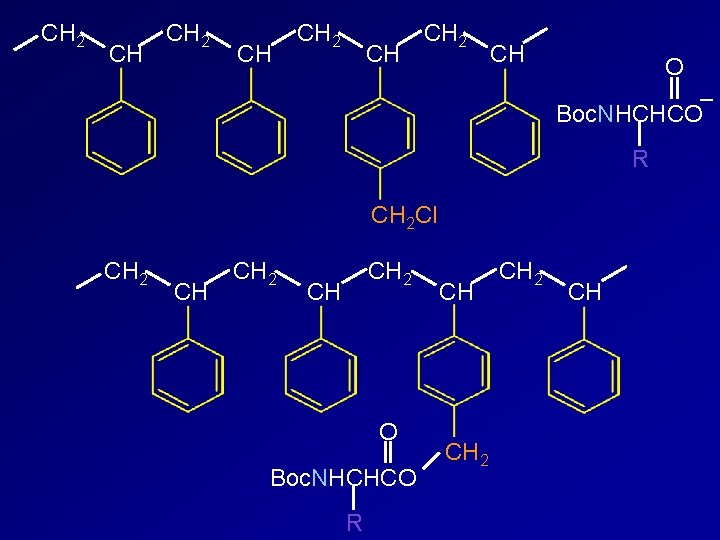
CH 2 CH O – Boc. NHCHCO R CH 2 Cl CH 2 CH O Boc. NHCHCO R CH CH 2 CH

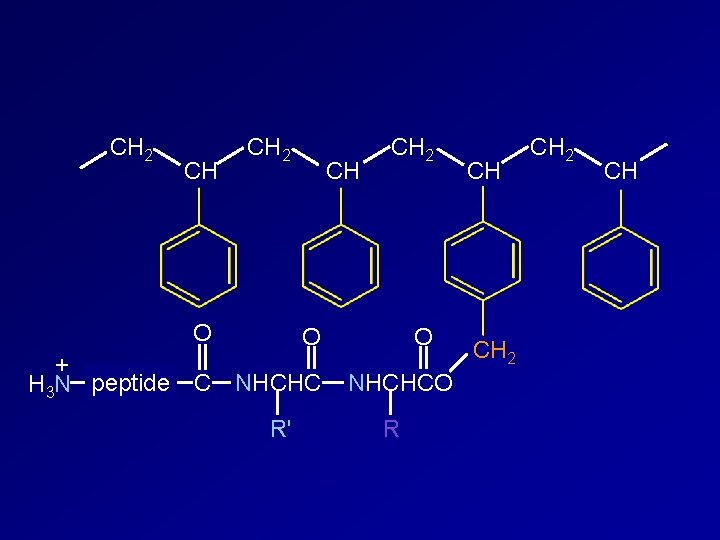
CH 2 CH CH 2 O + H 3 N peptide C NHCHC R' O NHCHCO R CH CH 2 CH

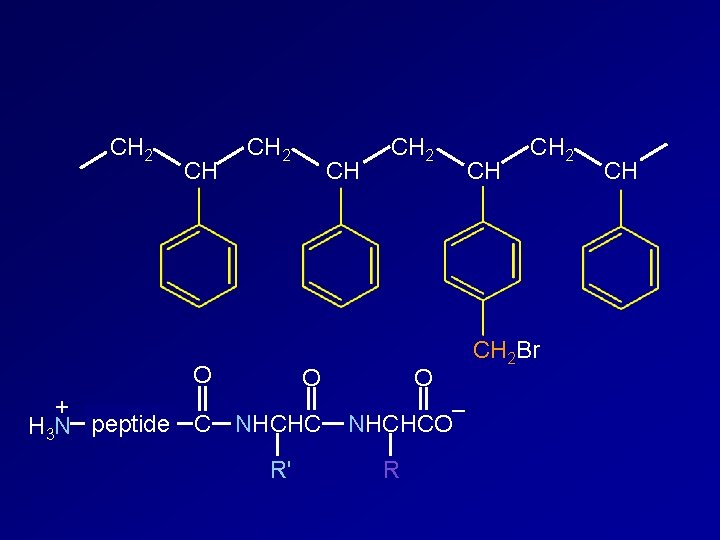
CH 2 CH CH 2 O + H 3 N peptide C NHCHC R' O – NHCHCO R CH CH 2 Br CH