TRANSLASYON Prof Dr Llfer Tamer Gm Salk Slaytlar





















- Slides: 61

TRANSLASYON: Prof. Dr Lülüfer Tamer Gümüş Sağlık Slaytları http: //hastaneciyiz. blogspot. com 1

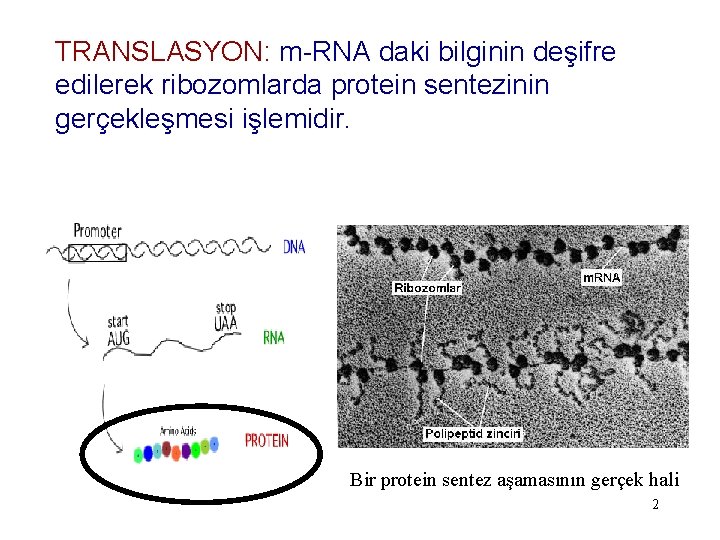
TRANSLASYON: m-RNA daki bilginin deşifre edilerek ribozomlarda protein sentezinin gerçekleşmesi işlemidir. Bir protein sentez aşamasının gerçek hali 2

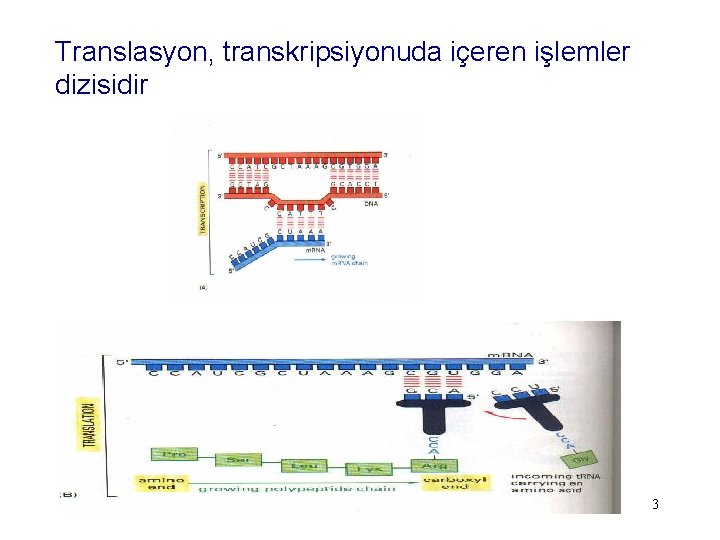
Translasyon, transkripsiyonuda içeren işlemler dizisidir 3

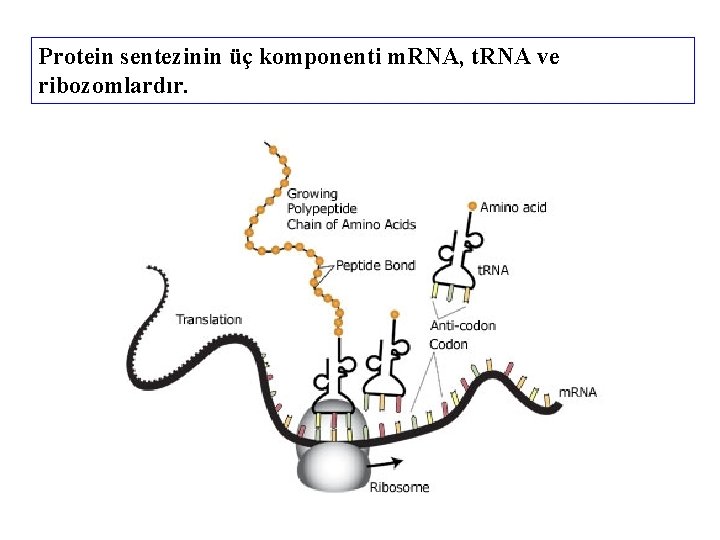
Protein sentezinin üç komponenti m. RNA, t. RNA ve ribozomlardır.

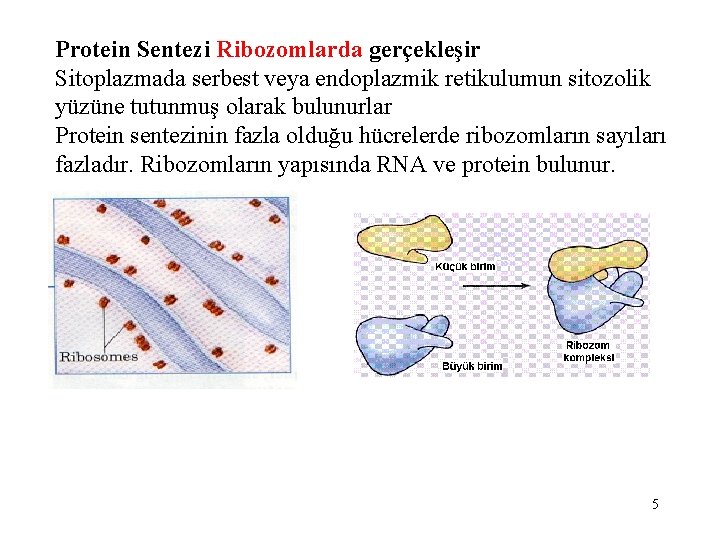
Protein Sentezi Ribozomlarda gerçekleşir Sitoplazmada serbest veya endoplazmik retikulumun sitozolik yüzüne tutunmuş olarak bulunurlar Protein sentezinin fazla olduğu hücrelerde ribozomların sayıları fazladır. Ribozomların yapısında RNA ve protein bulunur. 5

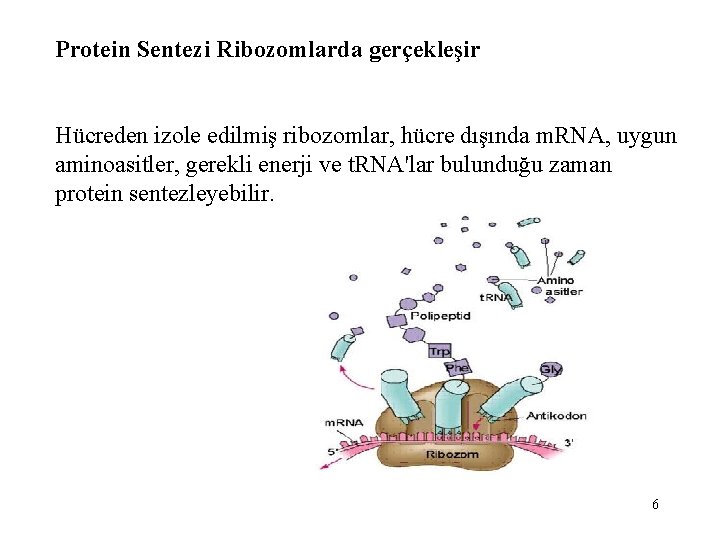
Protein Sentezi Ribozomlarda gerçekleşir Hücreden izole edilmiş ribozomlar, hücre dışında m. RNA, uygun aminoasitler, gerekli enerji ve t. RNA'lar bulunduğu zaman protein sentezleyebilir. 6

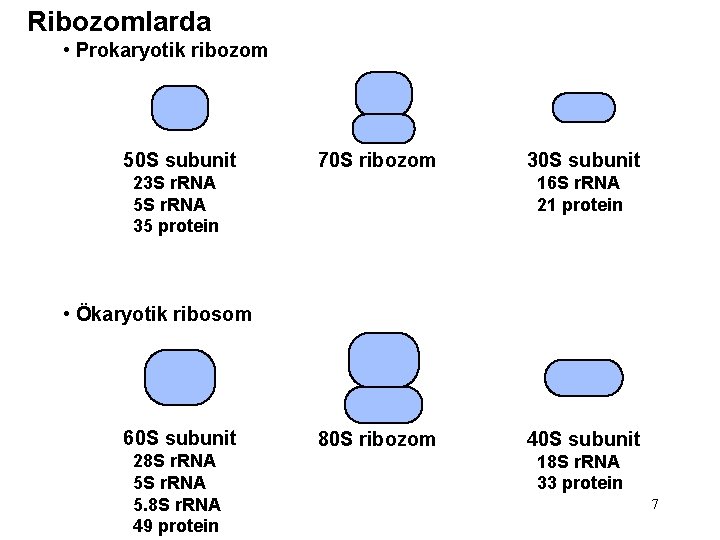
Ribozomlarda • Prokaryotik ribozom 50 S subunit 70 S ribozom 23 S r. RNA 5 S r. RNA 35 protein 30 S subunit 16 S r. RNA 21 protein • Ökaryotik ribosom 60 S subunit 28 S r. RNA 5. 8 S r. RNA 49 protein 80 S ribozom 40 S subunit 18 S r. RNA 33 protein 7

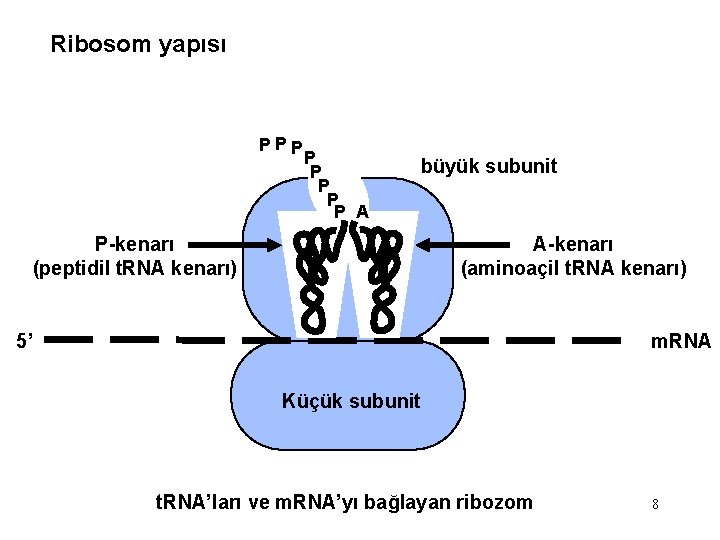
Ribosom yapısı P PP P P A büyük subunit P-kenarı (peptidil t. RNA kenarı) A-kenarı (aminoaçil t. RNA kenarı) 5’ m. RNA Küçük subunit t. RNA’ları ve m. RNA’yı bağlayan ribozom 8

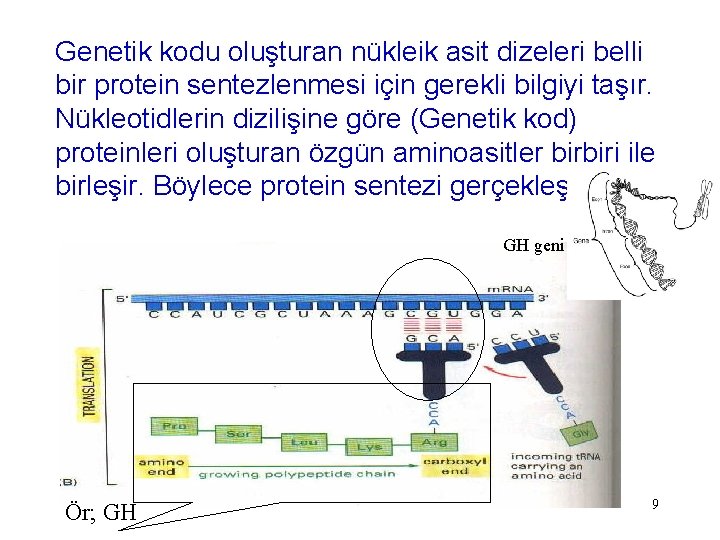
Genetik kodu oluşturan nükleik asit dizeleri belli bir protein sentezlenmesi için gerekli bilgiyi taşır. Nükleotidlerin dizilişine göre (Genetik kod) proteinleri oluşturan özgün aminoasitler birbiri ile birleşir. Böylece protein sentezi gerçekleşir. GH geni Ör; GH 9

Genetik kod, bir nükleotid baz dizesinin karşılık geldiği aminoasit dizesini belirtir. Üç tane nükleotid bazı bir kodonu oluşturur. Kodonlar m. RNA da bulunan A, G, C ve U bazlarından oluşur. Bir kodonda bu bazlardan üçü bulunur 10

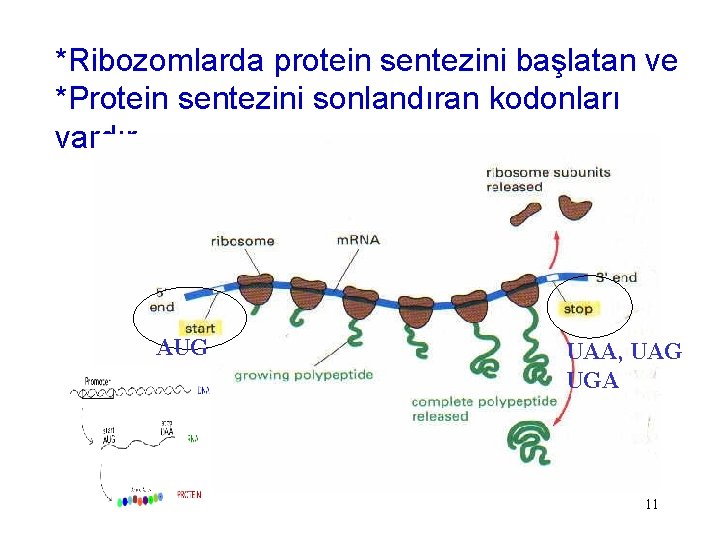
*Ribozomlarda protein sentezini başlatan ve *Protein sentezini sonlandıran kodonları vardır AUG UAA, UAG UGA 11

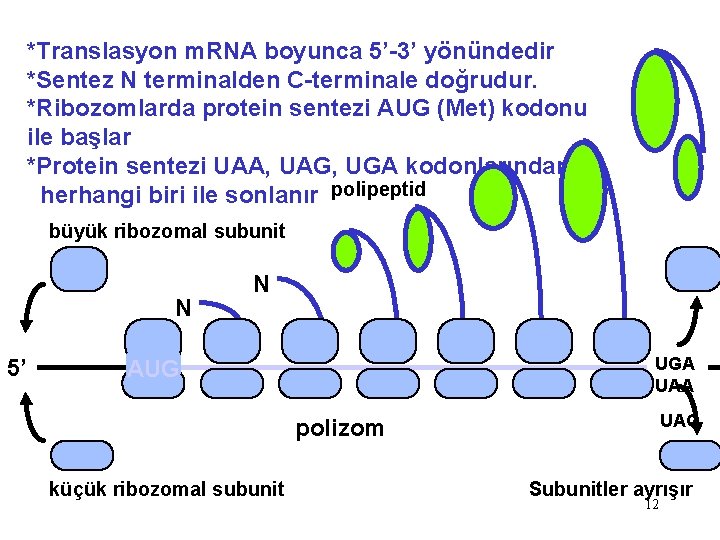
*Translasyon m. RNA boyunca 5’-3’ yönündedir *Sentez N terminalden C-terminale doğrudur. *Ribozomlarda protein sentezi AUG (Met) kodonu ile başlar *Protein sentezi UAA, UAG, UGA kodonlarından herhangi biri ile sonlanır polipeptid büyük ribozomal subunit N 5’ N UGA UAA AUG UAG polizom küçük ribozomal subunit Subunitler ayrışır 12

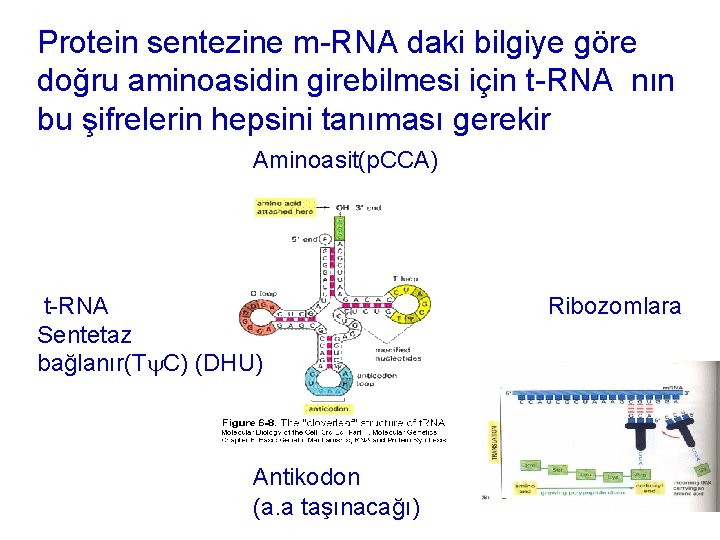
Protein sentezine m-RNA daki bilgiye göre doğru aminoasidin girebilmesi için t-RNA nın bu şifrelerin hepsini tanıması gerekir Aminoasit(p. CCA) t-RNA Sentetaz bağlanır(T C) (DHU) Antikodon (a. a taşınacağı) Ribozomlara 13

14

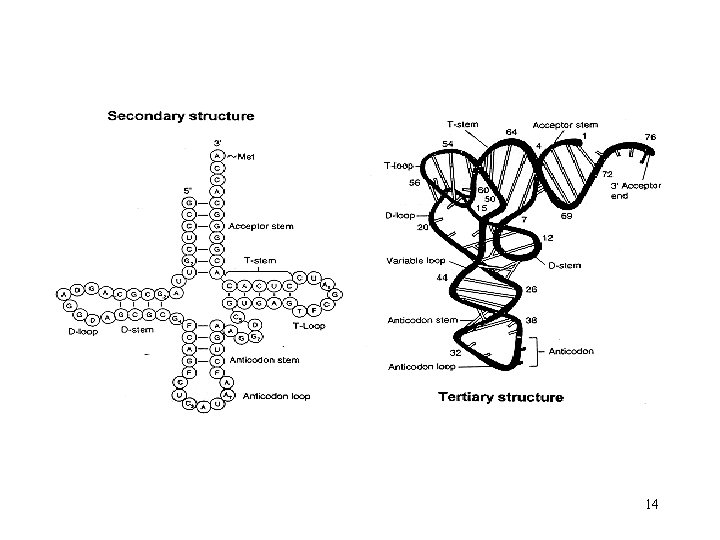
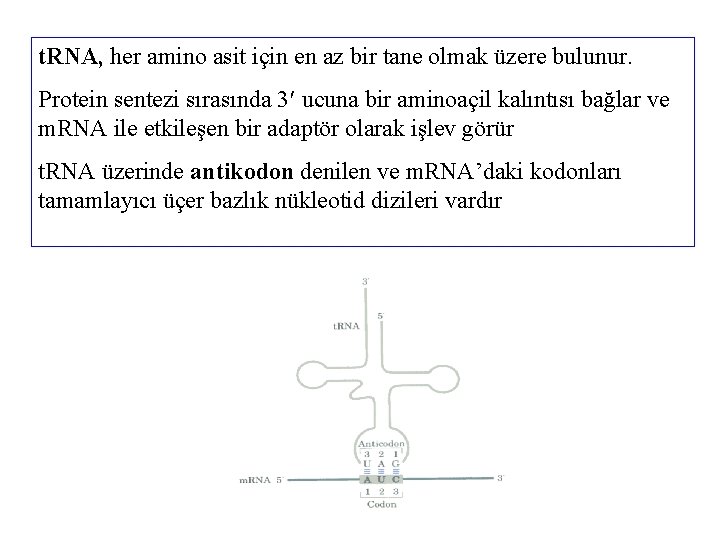
t. RNA, her amino asit için en az bir tane olmak üzere bulunur. Protein sentezi sırasında 3 ucuna bir aminoaçil kalıntısı bağlar ve m. RNA ile etkileşen bir adaptör olarak işlev görür t. RNA üzerinde antikodon denilen ve m. RNA’daki kodonları tamamlayıcı üçer bazlık nükleotid dizileri vardır

Wobble hipotezine göre, bir baz, birden fazla baz ile hidrojen köprüsü yapabilir. Bir t. RNA, aynı amino aside ait üç değişik kodonu tanıyabilir. Örneğin t. RNAArg’ deki (5′)ICG antikodonu, m. RNA’da, arjinine ait (5′)CGA, (5′)CGU, (5′)CGC kodonlarını tanıyabilir

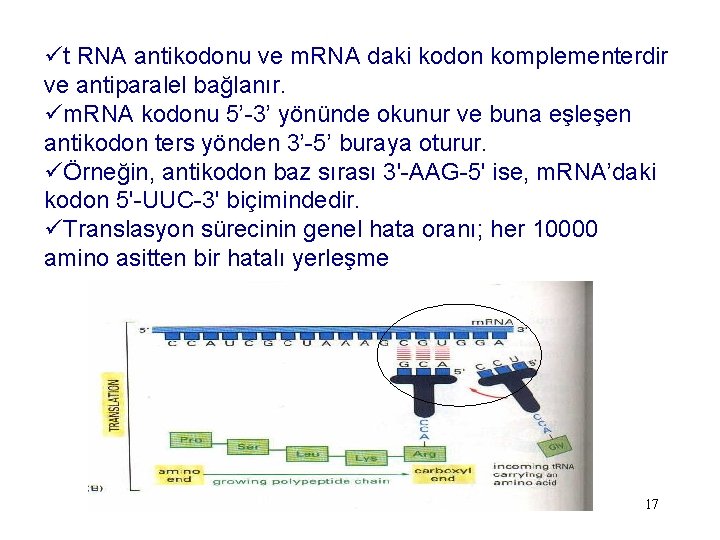
üt RNA antikodonu ve m. RNA daki kodon komplementerdir ve antiparalel bağlanır. üm. RNA kodonu 5’-3’ yönünde okunur ve buna eşleşen antikodon ters yönden 3’-5’ buraya oturur. üÖrneğin, antikodon baz sırası 3'-AAG-5' ise, m. RNA’daki kodon 5'-UUC-3' biçimindedir. üTranslasyon sürecinin genel hata oranı; her 10000 amino asitten bir hatalı yerleşme 17

Translasyon için gerekli bileşenler *Aminoasitler ( Diyetteki esansiyel aminoasitler) *t RNA *m. RNA *Aminoasil t. RNA sentetazlar *Fonksiyonel ribozomlar A bölgesi: A bölgesinde kodona özgü a. a buraya oturur P bölgesi: peptidil t. RNA oturur. *Başlama, uzama ve sonlanma faktörleri 18 * ATP ve GTP

PROTEİN SENTEZİNİN BASAMAKLARI 1 - Aminoasitlerin aktivasyonu ATP, t-RNA Aminoasit t-RNA sentetaz 2 -Protein sentezinin başlaması m-RNA (AUG kodonlu) Ribozom, GTP Başlatıcı t-RNA ( AUG antikodonlu) Başlatıcı Faktörler (IF 1, IF 2, IF 3) 3 -Protein zincirinin uzaması Uzatma faktörü (EF 1, EF 2) GTP 4 -Protein sentezinin sonlandırılması m-RNA bitiş kodonu (UAA, UAG, UGA) Releasing Faktör 19

1 - Aminoasitlerin aktivasyonu ATP, t-RNA Aminoasit t-RNA sentetaz E 1 -ATP+ Aminoasit Enzim-AMP-aminoasit+Ppi E 2 -Enzim-AMP-aminoasit+t-RNA Aminoasil-t. RNA AMP Enzim E: Aminoasil t-RNA sentetaz 20

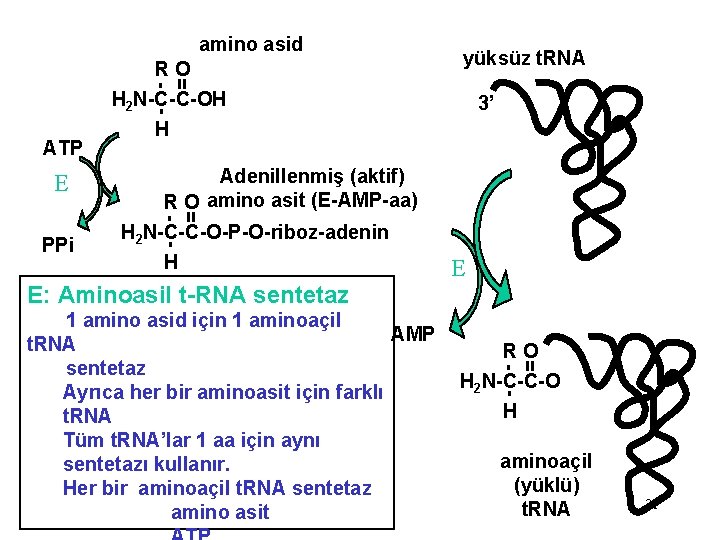
amino asid yüksüz t. RNA - = RO H 2 N-C-C-OH E PPi H Adenillenmiş (aktif) R O amino asit (E-AMP-aa) H 2 N-C-C-O-P-O-riboz-adenin - = ATP 3’ H E E: Aminoasil t-RNA sentetaz RO H 2 N-C-C-O - = 1 amino asid için 1 aminoaçil AMP t. RNA sentetaz Ayrıca her bir aminoasit için farklı t. RNA Tüm t. RNA’lar 1 aa için aynı sentetazı kullanır. Her bir aminoaçil t. RNA sentetaz amino asit H aminoaçil (yüklü) t. RNA 21

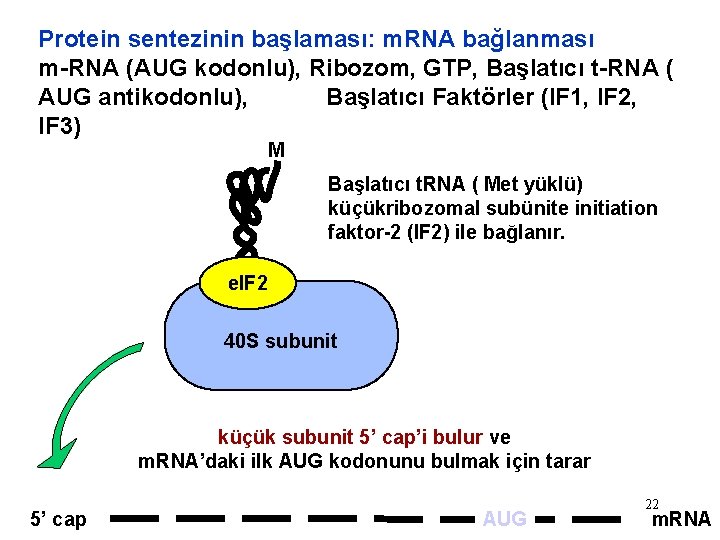
Protein sentezinin başlaması: m. RNA bağlanması m-RNA (AUG kodonlu), Ribozom, GTP, Başlatıcı t-RNA ( AUG antikodonlu), Başlatıcı Faktörler (IF 1, IF 2, IF 3) M Başlatıcı t. RNA ( Met yüklü) küçükribozomal subünite initiation faktor-2 (IF 2) ile bağlanır. e. IF 2 40 S subunit küçük subunit 5’ cap’i bulur ve m. RNA’daki ilk AUG kodonunu bulmak için tarar 5’ cap AUG 22 m. RNA

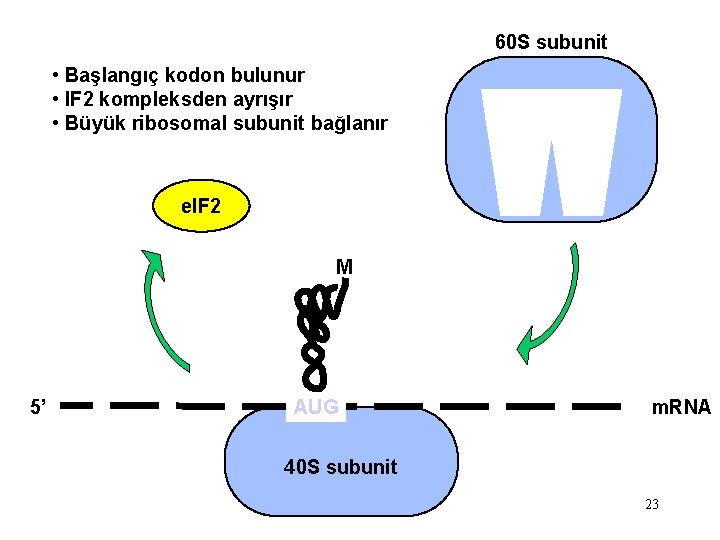
60 S subunit • Başlangıç kodon bulunur • IF 2 kompleksden ayrışır • Büyük ribosomal subunit bağlanır e. IF 2 M 5’ AUG m. RNA 40 S subunit 23

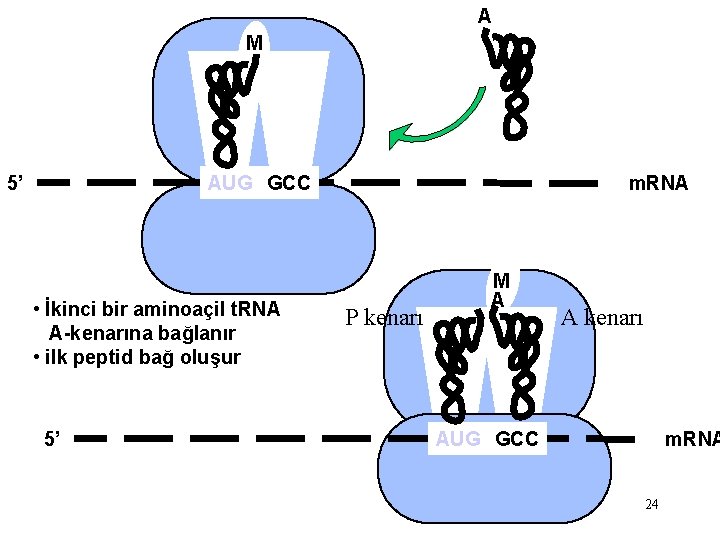
A M AUG GCC 5’ • İkinci bir aminoaçil t. RNA A-kenarına bağlanır • ilk peptid bağ oluşur 5’ m. RNA P kenarı M A A kenarı AUG GCC m. RNA 24

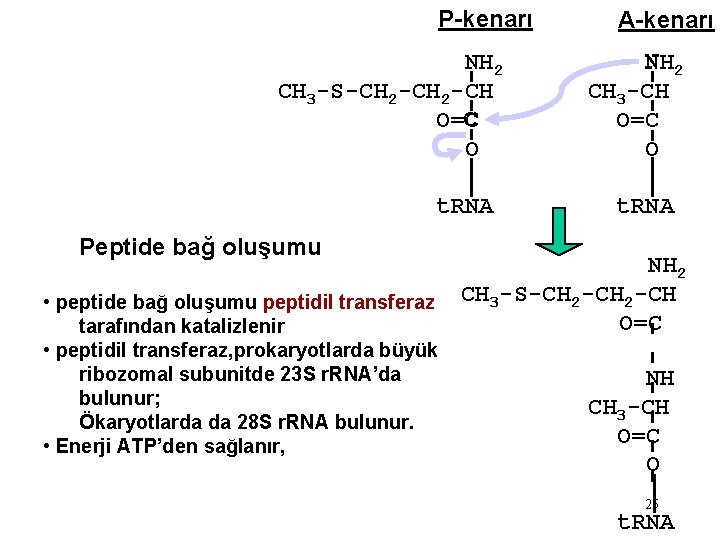
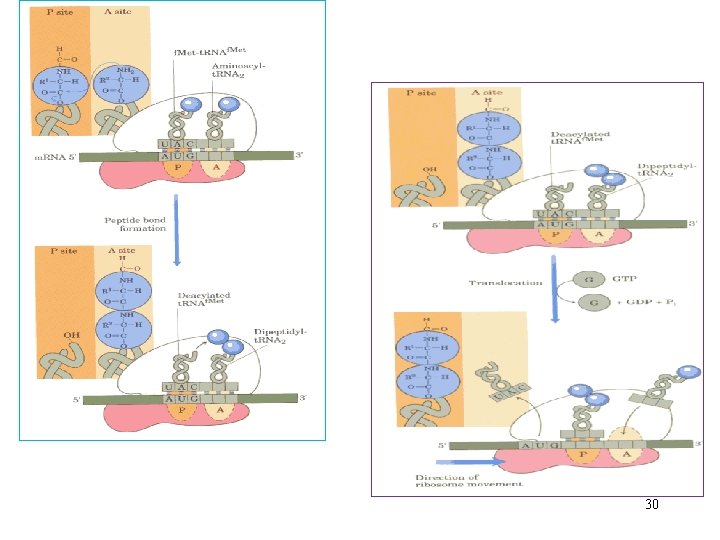
P-kenarı NH 2 CH 3 -S-CH 2 -CH C O=C O t. RNA Peptide bağ oluşumu • peptide bağ oluşumu peptidil transferaz tarafından katalizlenir • peptidil transferaz, prokaryotlarda büyük ribozomal subunitde 23 S r. RNA’da bulunur; Ökaryotlarda da 28 S r. RNA bulunur. • Enerji ATP’den sağlanır, A-kenarı N 2 NH CH 3 -CH O=C O t. RNA NH 2 CH 3 -S-CH 2 -CH O=C NH CH 3 -CH O=C O 25 t. RNA

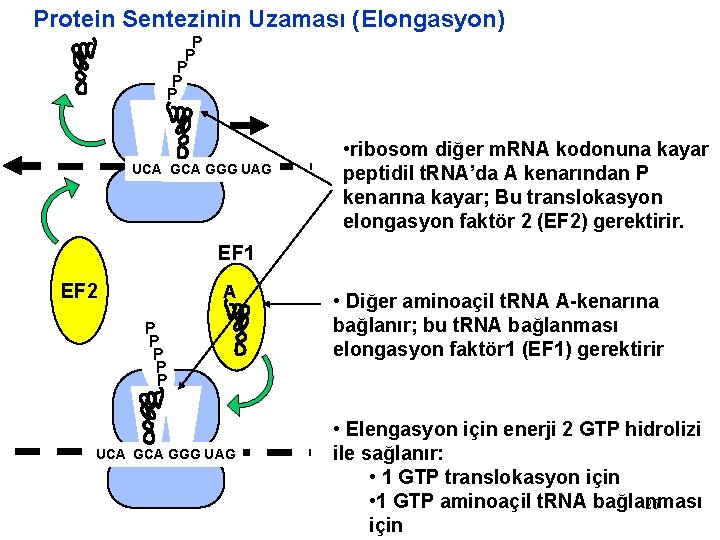
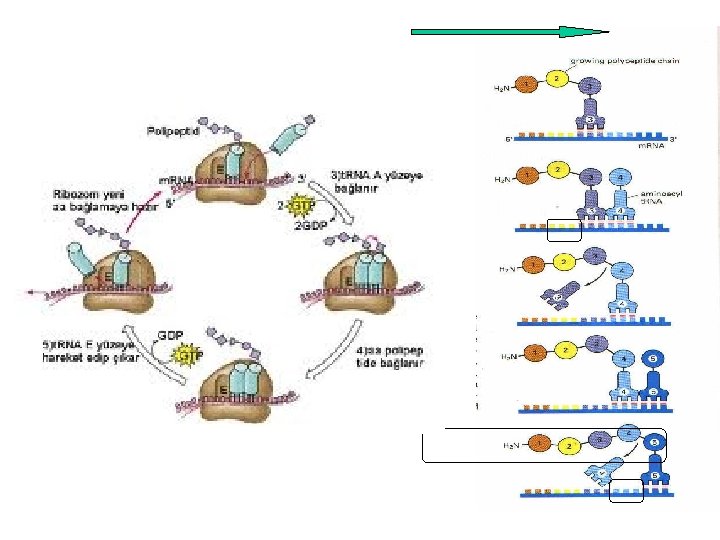
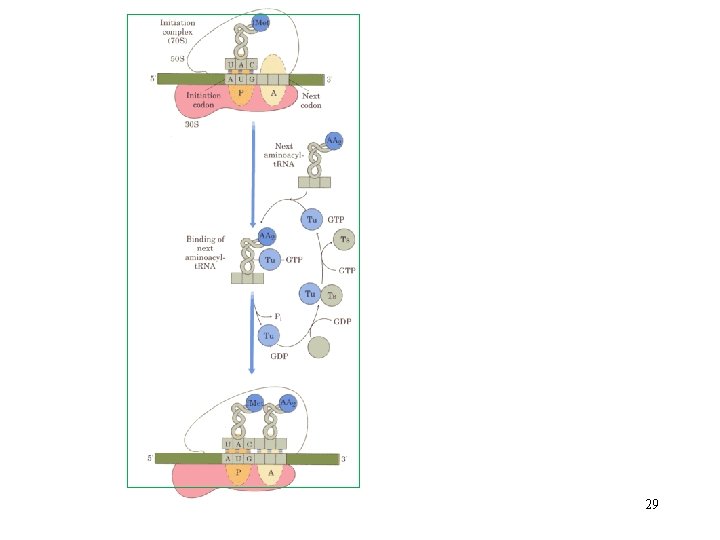
Protein Sentezinin Uzaması (Elongasyon) P P P UCA GGG UAG • ribosom diğer m. RNA kodonuna kayar peptidil t. RNA’da A kenarından P kenarına kayar; Bu translokasyon elongasyon faktör 2 (EF 2) gerektirir. EF 1 EF 2 A P P P UCA GGG UAG • Diğer aminoaçil t. RNA A-kenarına bağlanır; bu t. RNA bağlanması elongasyon faktör 1 (EF 1) gerektirir • Elengasyon için enerji 2 GTP hidrolizi ile sağlanır: • 1 GTP translokasyon için • 1 GTP aminoaçil t. RNA bağlanması 26 için

27

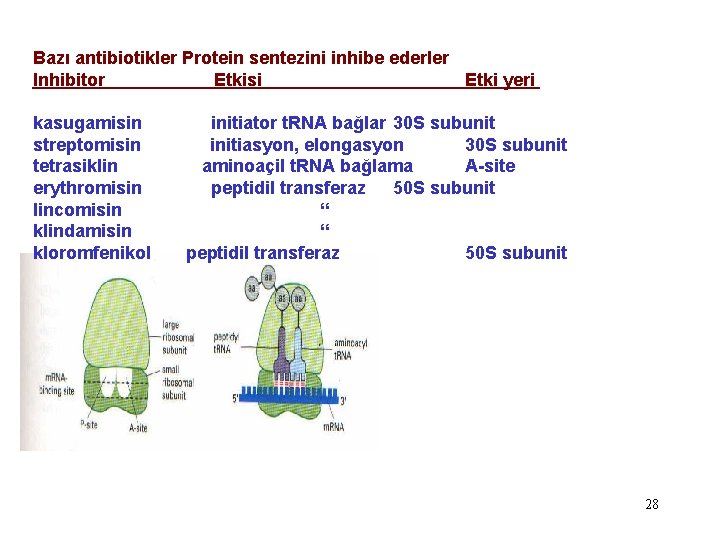
Bazı antibiotikler Protein sentezini inhibe ederler Inhibitor Etkisi Etki yeri kasugamisin streptomisin tetrasiklin erythromisin lincomisin klindamisin kloromfenikol initiator t. RNA bağlar 30 S subunit initiasyon, elongasyon 30 S subunit aminoaçil t. RNA bağlama A-site peptidil transferaz 50 S subunit “ “ peptidil transferaz 50 S subunit 28

29

30

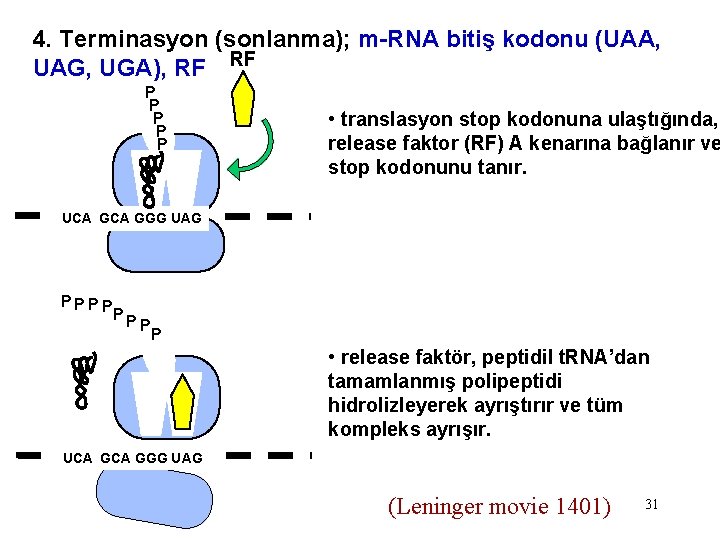
4. Terminasyon (sonlanma); m-RNA bitiş kodonu (UAA, UAG, UGA), RF RF P P P • translasyon stop kodonuna ulaştığında, release faktor (RF) A kenarına bağlanır ve stop kodonunu tanır. UCA GGG UAG PPPP PP P P • release faktör, peptidil t. RNA’dan tamamlanmış polipeptidi hidrolizleyerek ayrıştırır ve tüm kompleks ayrışır. UCA GGG UAG (Leninger movie 1401) 31

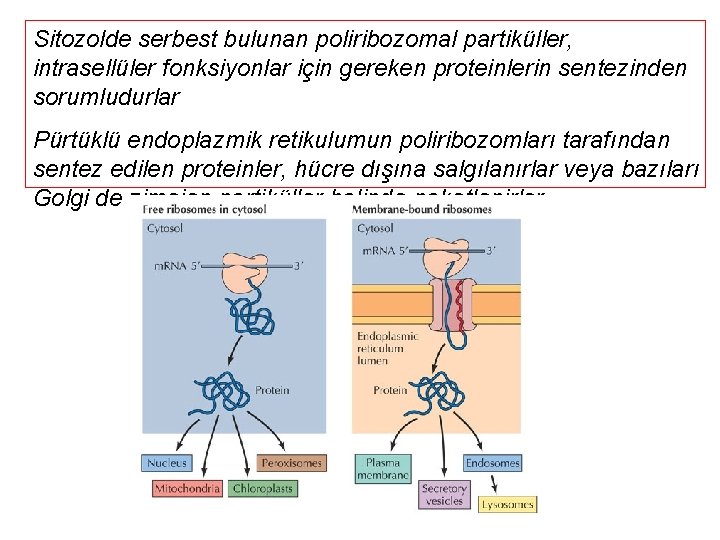
Sitozolde serbest bulunan poliribozomal partiküller, intrasellüler fonksiyonlar için gereken proteinlerin sentezinden sorumludurlar Pürtüklü endoplazmik retikulumun poliribozomları tarafından sentez edilen proteinler, hücre dışına salgılanırlar veya bazıları Golgi de zimojen partiküller halinde paketlenirler

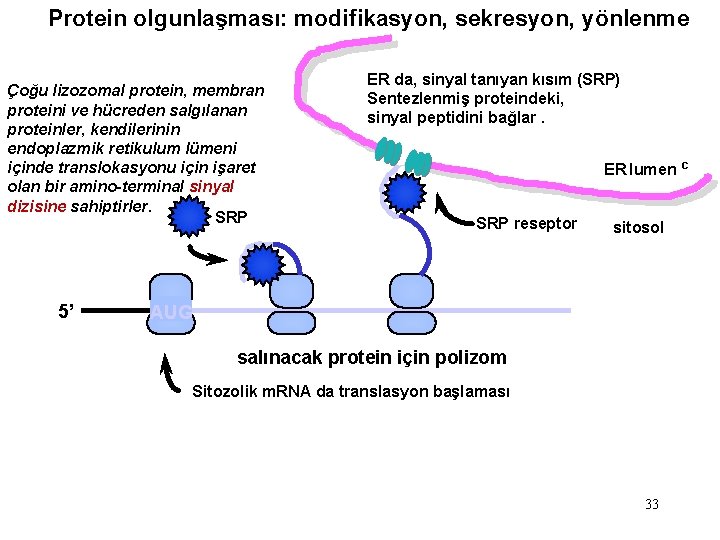
Protein olgunlaşması: modifikasyon, sekresyon, yönlenme Çoğu lizozomal protein, membran proteini ve hücreden salgılanan proteinler, kendilerinin endoplazmik retikulum lümeni içinde translokasyonu için işaret olan bir amino-terminal sinyal dizisine sahiptirler. SRP 5’ ER da, sinyal tanıyan kısım (SRP) Sentezlenmiş proteindeki, sinyal peptidini bağlar. ER lumen c SRP reseptor sitosol AUG salınacak protein için polizom Sitozolik m. RNA da translasyon başlaması 33

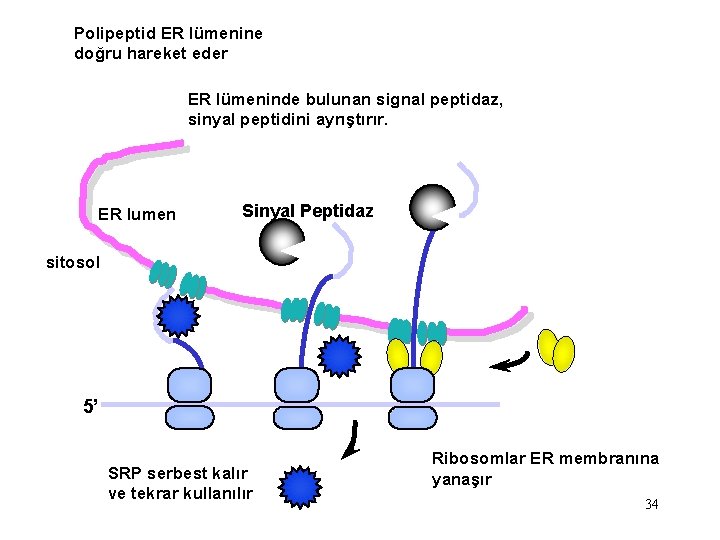
Polipeptid ER lümenine doğru hareket eder ER lümeninde bulunan signal peptidaz, sinyal peptidini ayrıştırır. ER lumen Sinyal Peptidaz sitosol 5’ SRP serbest kalır ve tekrar kullanılır Ribosomlar ER membranına yanaşır 34

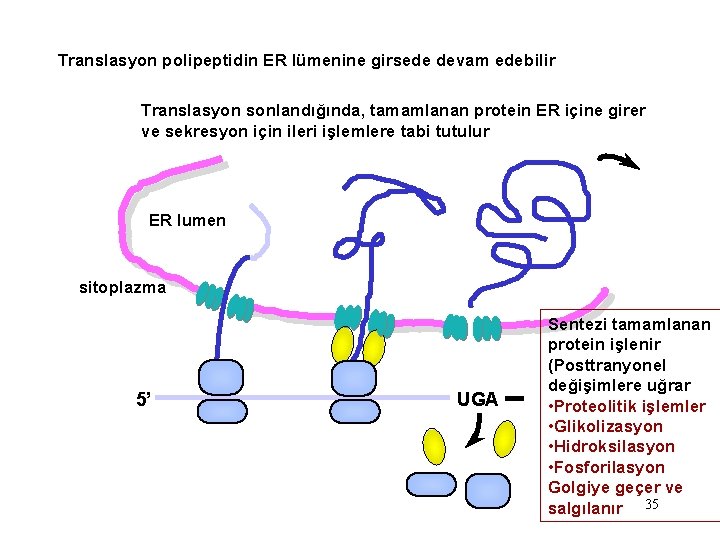
Translasyon polipeptidin ER lümenine girsede devam edebilir Translasyon sonlandığında, tamamlanan protein ER içine girer ve sekresyon için ileri işlemlere tabi tutulur ER lumen sitoplazma 5’ UGA Sentezi tamamlanan protein işlenir (Posttranyonel değişimlere uğrar • Proteolitik işlemler • Glikolizasyon • Hidroksilasyon • Fosforilasyon Golgiye geçer ve salgılanır 35

İNHİBİTÖRLER DNA nın replikasyonunu, transkripsiyonun ve translasyonunu geriye dönüşümsüz ola inhibe eden antibiotik ve antimetabolitler v Bazı antibiotikler Protein sentezini inhibe ederler Inhibitor Etkisi Etki yeri kasugamisin streptomisin tetrasiklin erythromisin lincomisin klindamisin kloromfenikol initiator t. RNA bağlar 30 S subunit initiasyon, elongasyon 30 S subunit aminoaçil t. RNA bağlama A-site peptidil transferaz 50 S subunit “ “ peptidil transferaz 50 S subunit 36

Aktinomisin D Streptomyces suşundan elde edilen bir antibiotikdir. Aktinomisin D, DNA ya bağlı RNA polimeraz enziminin RNA sentezini inhibe eder. DNA zincirinde G-C baz çifti arasına girer ve guanin ile hidrojen bağı kurarak RNA polimeraz enziminin bağlan engeller. 37

Etidium Bromür; Aktinomisin D gibi iki DNA zinciri arasına girer. Bleomisin; DNA zincirinde kopmalar meydana getirir Mitomisin; Bazları alkile eder ve çarpraz bağlar kurulmasına neden olurlar Nalidiksik Asit; DNA polimeraz enzimini inhibe eder, Rifamisin; Direkt olarak RNA polimeraz enzimine bağlanarak m. RNA sentezini engeller. 38

Alfatoksin; Aspergillus flavustan üretilen bir toksin olup, Replikasyon ve transkripsiyonu önler. Alfa-Amanitin; Zehirli bir mantar olan Amanita phalloides’in toksin maddesi olup, RNA polimerazı inhibe eder. Puromisin; Protein sentezinde aynı aminoasit gibi peptid bağı yapar. Fakat yeni gelecek aminoasit bu peptid bağına ilave edilemez. Kloromfenikol; Bu antibiotik, 50 s ribozomlara bağlanarak protein sentezini inhibe eder. 39

Streptomisin Bu antibiotik ise 30 s ribozomlara bağlanarak genetik k yanlış okunmasına neden olarak protein sentezini blok 40

Posttransyonel Modifikasyonlar Polipeptid zincirlerinin çoğunda Posttransyonel Modifikasyonlar (değişim) meydana gelir. Bu değişimler ya polipeptid zinciri ribozom üzerindeyken veya sentez tamamlanıp ribozomdan ayrıldıktan sonra meydana gelir. Değişimler translasyon başladıktan sonra ortaya çıktığı için , bunlara posttransyonel modifikasyonlar denir.

Posttransyonel Modifikasyonlar Proteolitik işlemler (Kısaltmalar) Amino-terminal ve karboksil-terminal modifikasyonlar Proteolitik işlem Kovalen değişimler Fosforilasyon Glikozilasyon ve protein yönlendirilmesi Hidroksilasyon Diğer Disülfid çapraz bağlarının oluşması ve zincir katlanması İzoprenil grupların eklenmesi Prostetik grupların eklenmesi

Amino-terminal ve karboksil-terminal modifikasyonlar: Translasyon sonunda yeni sentezlenmiş olan bütün polipeptitler, prokaryotlarda N-formilmetionin kalıntısı ile, ökaryotlarda ise metionin kalıntısı ile başlar Amino-terminal ve karboksil-terminal metionin kalıntılarına eklenmiş olan formil grupları, enzimatik olarak çıkarılırlar Ökaryotik proteinlerin %50’den fazlasında amino-terminal kalıntıların amino grupları translasyondan sonra asetillenir. Karboksil-terminal kalıntılar da bazen modifiye edilir

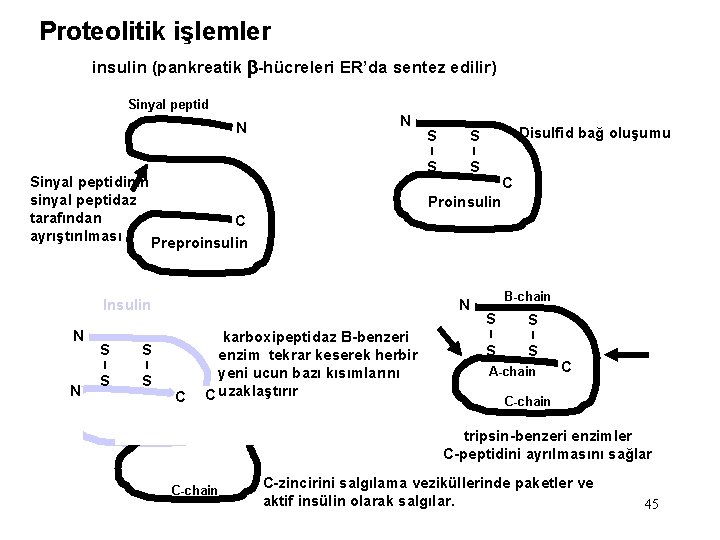
Proteolitik işlem: Birçok protein, örneğin insülin, bazı viral proteinler, tripsin ve kimotripsin gibi proteazlar, başlangıçta büyük ve inaktif prekürsör proteinler olarak sentez edilirler. Bu prekürsörler, son aktif formlarına dönüşmek için proteolitik olarak kısaltılırlar

Proteolitik işlemler insulin (pankreatik b-hücreleri ER’da sentez edilir) Sinyal peptid N N Sinyal peptidinin sinyal peptidaz tarafından C ayrıştırılması Preproinsulin N S S I I S S N C Disulfid bağ oluşumu C Proinsulin Insulin N S karboxipeptidaz B-benzeri enzim tekrar keserek herbir yeni ucun bazı kısımlarını C uzaklaştırır B-chain S S I I S S A-chain C C-chain tripsin-benzeri enzimler C-peptidini ayrılmasını sağlar C-chain C-zincirini salgılama veziküllerinde paketler ve aktif insülin olarak salgılar. 45

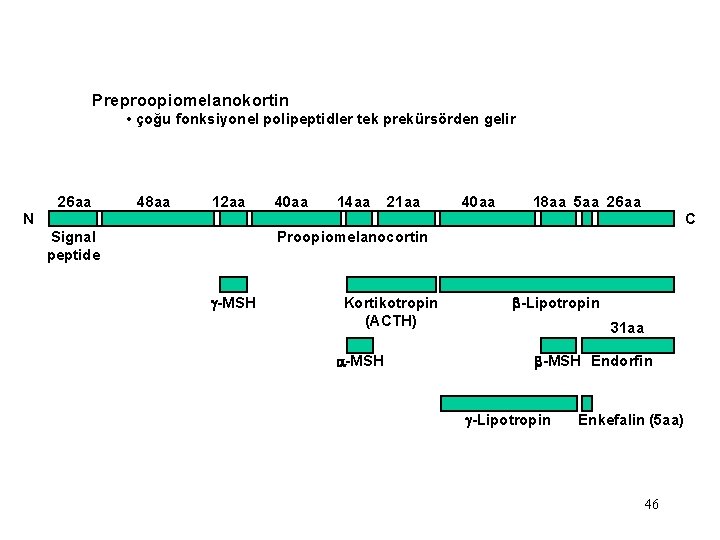
Preproopiomelanokortin • çoğu fonksiyonel polipeptidler tek prekürsörden gelir 26 aa 48 aa 12 aa 40 aa 14 aa 21 aa 40 aa 18 aa 5 aa 26 aa C N Signal peptide Proopiomelanocortin g-MSH Kortikotropin (ACTH) a-MSH b-Lipotropin 31 aa b-MSH Endorfin g-Lipotropin Enkefalin (5 aa) 46

Proteinlerin fosforilasyonu • Serin, threonin ve tirozin aa’lerinde fosforilasyon görülür. • Bu fosforilasyon reaksiyonları protein kinazlar tarafından gerçekleştirilir. • Tirozin kinaz • Serin-Threonin kinaz • Fosforilasyon sonucu proteinlerin aktiviteleri artar veya azalır • Defosforilasyon protein fosfatazlar tarafından gerçekleştirilir. 47

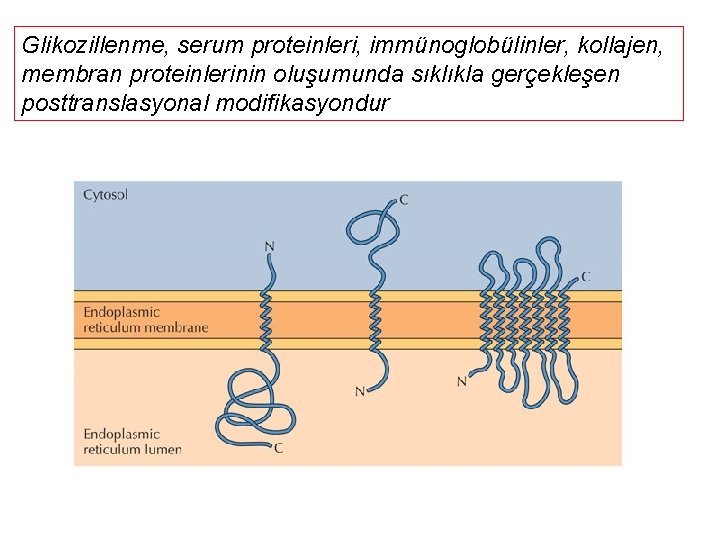
Glikozillenme, serum proteinleri, immünoglobülinler, kollajen, membran proteinlerinin oluşumunda sıklıkla gerçekleşen posttranslasyonal modifikasyondur

Proteinlerin glikolizasyonu Translasyon süresince ER içine girmeden glikozillenir. ER ve Golgi içinde çeşitli oligosakkarid modifikasyonları gerçekleşir - Örnek: Glikoprotein ve proteoglikanlar 49

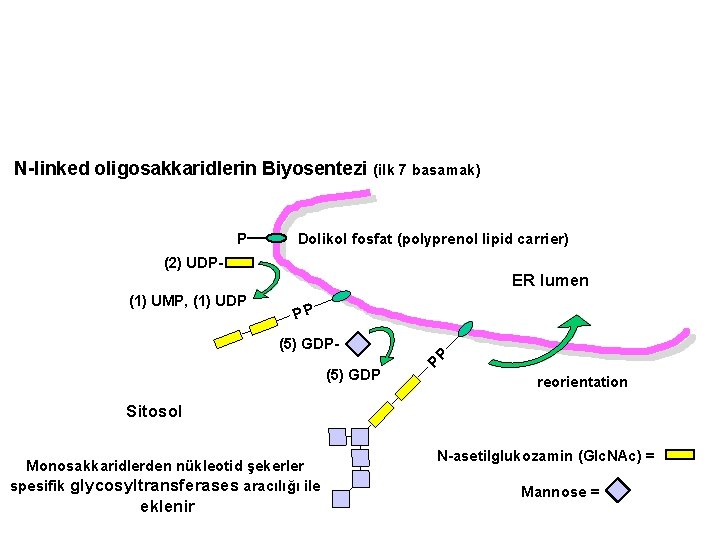
N-linked oligosakkaridlerin Biyosentezi (ilk 7 basamak) P Dolikol fosfat (polyprenol lipid carrier) (2) UDP(1) UMP, (1) UDP ER lumen PP (5) GDP P P (5) GDPreorientation Sitosol Monosakkaridlerden nükleotid şekerler spesifik glycosyltransferases aracılığı ile eklenir N-asetilglukozamin (Glc. NAc) = Mannose =

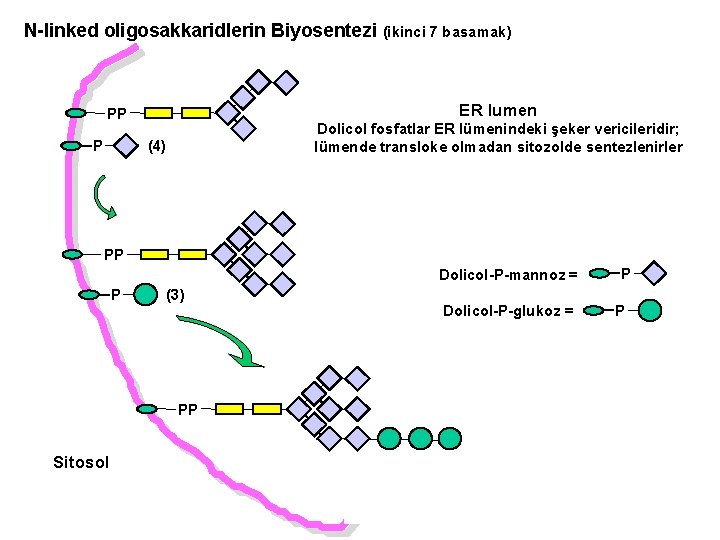
N-linked oligosakkaridlerin Biyosentezi (ikinci 7 basamak) ER lumen PP P Dolicol fosfatlar ER lümenindeki şeker vericileridir; lümende transloke olmadan sitozolde sentezlenirler (4) PP Dolicol-P-mannoz = P (3) PP Sitosol Dolicol-P-glukoz = P P

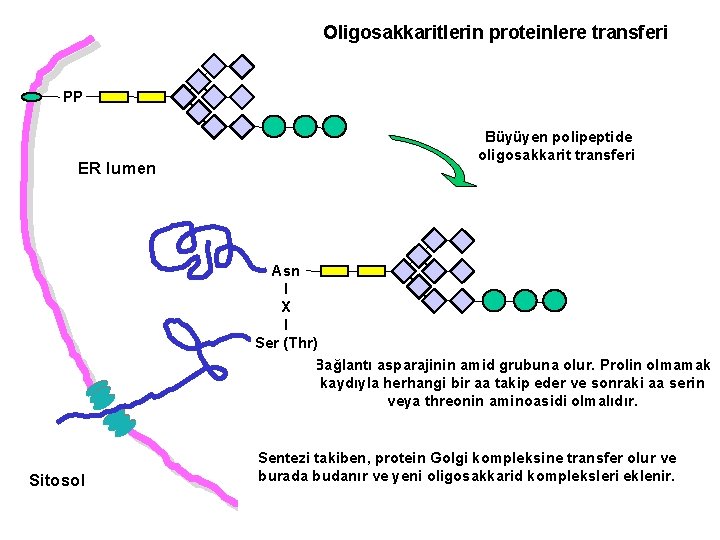
Oligosakkaritlerin proteinlere transferi PP ER lumen Büyüyen polipeptide oligosakkarit transferi Asn I X I Ser (Thr) Bağlantı asparajinin amid grubuna olur. Prolin olmamak kaydıyla herhangi bir aa takip eder ve sonraki aa serin veya threonin aminoasidi olmalıdır. Sitosol Sentezi takiben, protein Golgi kompleksine transfer olur ve burada budanır ve yeni oligosakkarid kompleksleri eklenir.

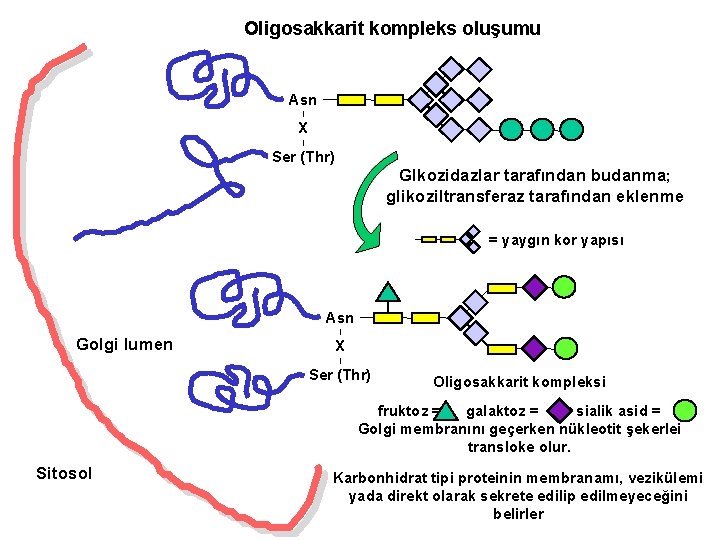
Oligosakkarit kompleks oluşumu Asn I X I Ser (Thr) Glkozidazlar tarafından budanma; glikoziltransferaz tarafından eklenme = yaygın kor yapısı Asn Golgi lumen I X I Ser (Thr) Oligosakkarit kompleksi fruktoz = galaktoz = sialik asid = Golgi membranını geçerken nükleotit şekerlei transloke olur. Sitosol Karbonhidrat tipi proteinin membranamı, vezikülemi yada direkt olarak sekrete edilip edilmeyeceğini belirler

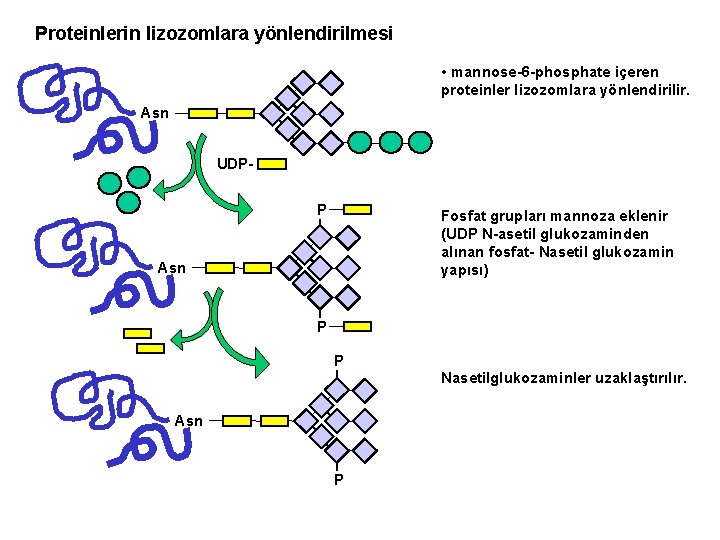
Proteinlerin lizozomlara yönlendirilmesi • mannose-6 -phosphate içeren proteinler lizozomlara yönlendirilir. Asn UDPP Fosfat grupları mannoza eklenir (UDP N-asetil glukozaminden alınan fosfat- Nasetil glukozamin yapısı) Asn P P Nasetilglukozaminler uzaklaştırılır. Asn P

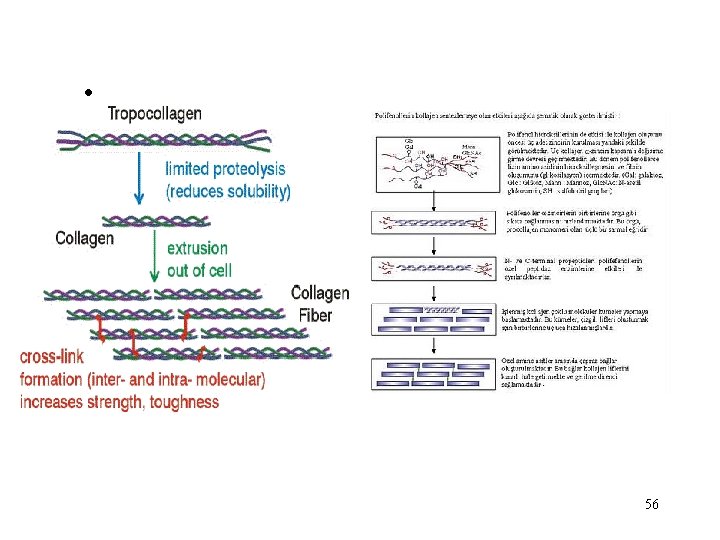
Proteinlerin Hidroksilasyonu • Kolllajenin a-zincirinde bulunan prolin ve lizin aa’lerinin hidroksilasyona uğrayarak hidroksiprolin ve hidroksilizin oluşturma reaksiyonudur. • Bu reaksiyon endoplazmik retikulumda gerçekleşir 55


İzoprenil grupların eklenmesi: Ökaryotik proteinlerin bir grubu izoprenillenmiştir; proteinin bir sistein kalıntısı ile izoprenil grubu arasında bir tiyoeter bağı oluşturulmuştur. İzoprenil grupları, farnesil pirofosfat gibi, kolesterol biyosentez yolunun pirofosfat ara ürünlerinden türemiştir Ras onkogen ve proto-onkogen ürünleri, G proteinleri, nükleer matrikste bulunan laminler, bu yolla modifiye edilmiş proteinlerdir. İzoprenil grupları, bazı hallerde bir membrandaki proteini yerinde tutmak için görev görür

Prostetik grupların eklenmesi: Birçok prokaryotik ve ökaryotik protein, aktiviteleri için, prostetik grupların kovalent olarak bağlanmasını gerektirir. Prostetik gruplar, protein zincire zincir ribozomdan ayrıldıktan sonra bağlanır. Asetil-Co. A karboksilazdaki biotin molekülü ve sitokrom c’deki hem grubu, iki önemli prostetik grup örneğidir Sitokrom c

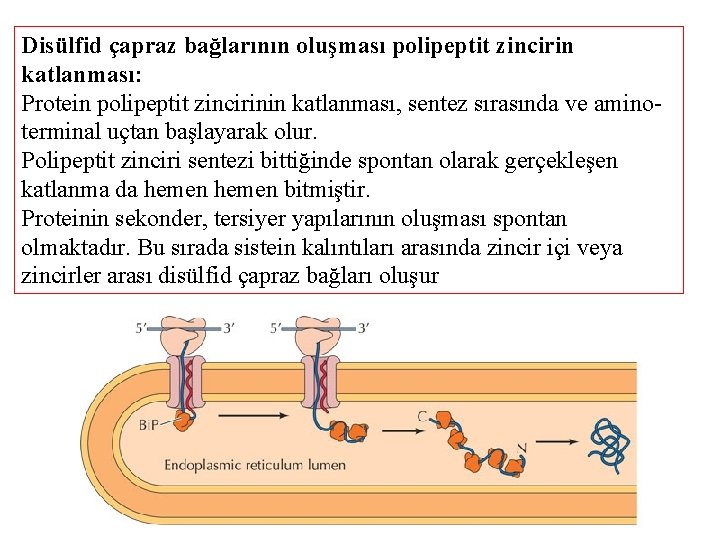
Disülfid çapraz bağlarının oluşması polipeptit zincirin katlanması: Protein polipeptit zincirinin katlanması, sentez sırasında ve aminoterminal uçtan başlayarak olur. Polipeptit zinciri sentezi bittiğinde spontan olarak gerçekleşen katlanma da hemen bitmiştir. Proteinin sekonder, tersiyer yapılarının oluşması spontan olmaktadır. Bu sırada sistein kalıntıları arasında zincir içi veya zincirler arası disülfid çapraz bağları oluşur

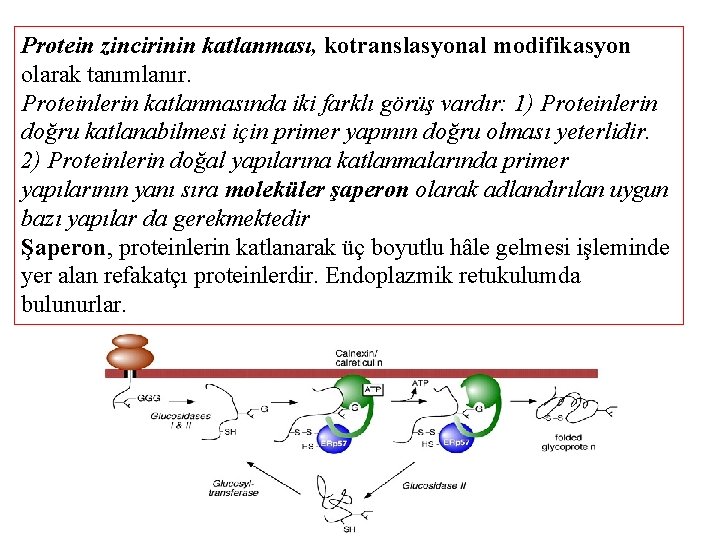
Protein zincirinin katlanması, kotranslasyonal modifikasyon olarak tanımlanır. Proteinlerin katlanmasında iki farklı görüş vardır: 1) Proteinlerin doğru katlanabilmesi için primer yapının doğru olması yeterlidir. 2) Proteinlerin doğal yapılarına katlanmalarında primer yapılarının yanı sıra moleküler şaperon olarak adlandırılan uygun bazı yapılar da gerekmektedir Şaperon, proteinlerin katlanarak üç boyutlu hâle gelmesi işleminde yer alan refakatçı proteinlerdir. Endoplazmik retukulumda bulunurlar.

Moleküler Şaperonlar Ribozomda üretilen proteinlerin kıvrılmalarına engel olurlar Proteinlerin hedeflerine ulaştığında katlanmalarını sağlarlar. Yanlış katlanmış proteinleri tanıyıp, onları düzeltirler Düzeltilmesi mümkün olmayan proteinleri tanırlar. Bunların parçalanmasını ve ortamdan uzaklaşmasını sağlarlar. Moleküler şaperonlar, proteinlerin sentezinde, taşınmasında, polimerlerinin oluşmasında ve denatüre proteinlerin yeniden doğal şekillerine dönüşmesinde (renatürasyonda) rol oynamaktadırlar Sağlık Slaytları http: //hastaneciyiz. blogspot. com