gruppo funzionale carbossilico O C O H Nomenclatura
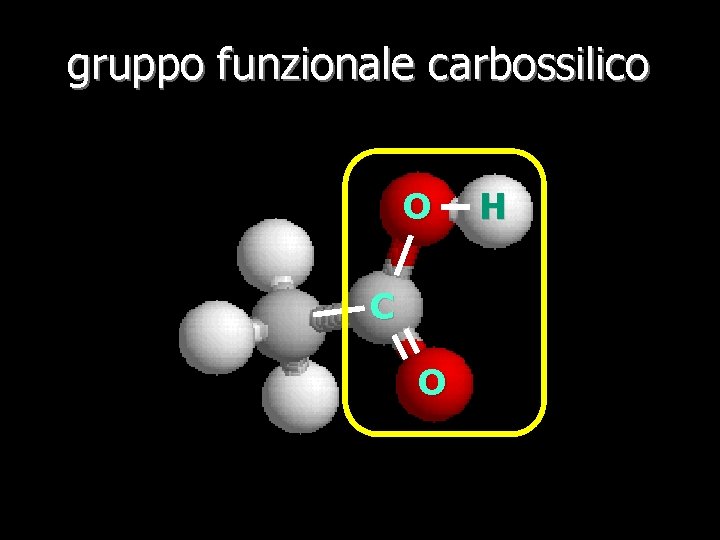
gruppo funzionale carbossilico O C O H
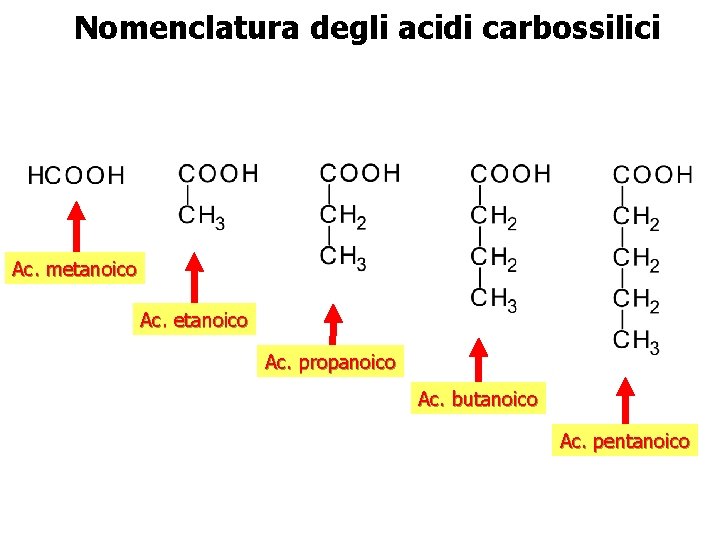
Nomenclatura degli acidi carbossilici Ac. metanoico Ac. propanoico Ac. butanoico Ac. pentanoico
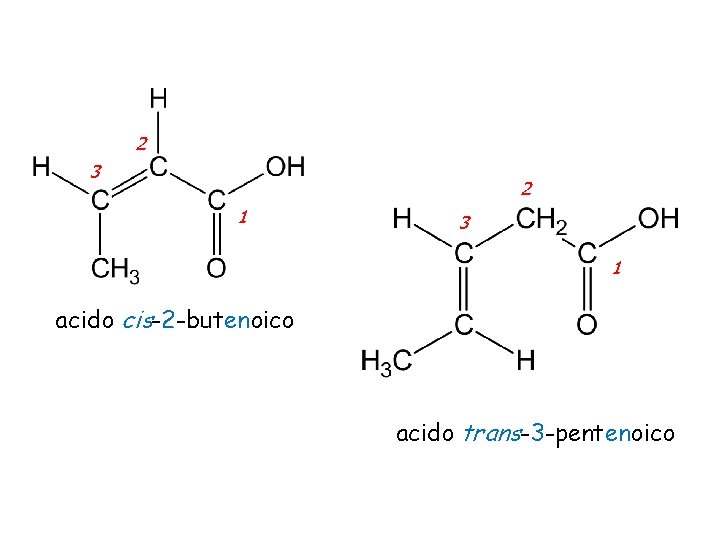
2 3 2 1 3 1 acido cis-2 -butenoico acido trans-3 -pentenoico
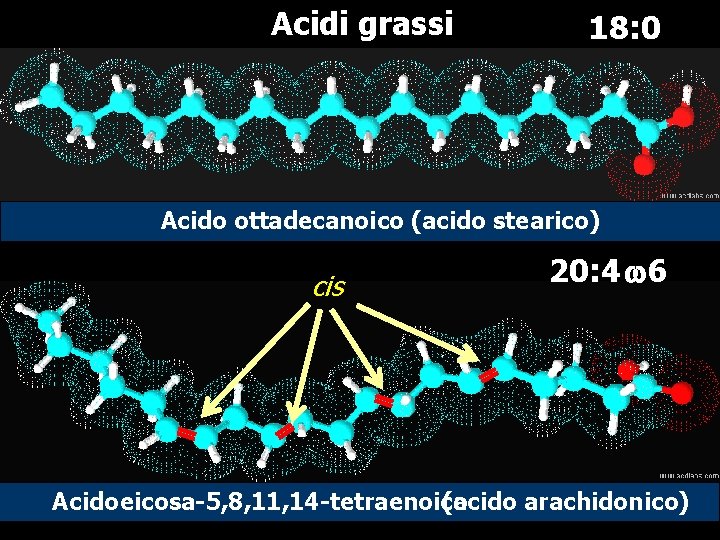
Acidi grassi 18: 0 Acido ottadecanoico (acido stearico) cis 20: 4 w 6 Acido eicosa-5, 8, 11, 14 -tetraenoico (acido arachidonico)
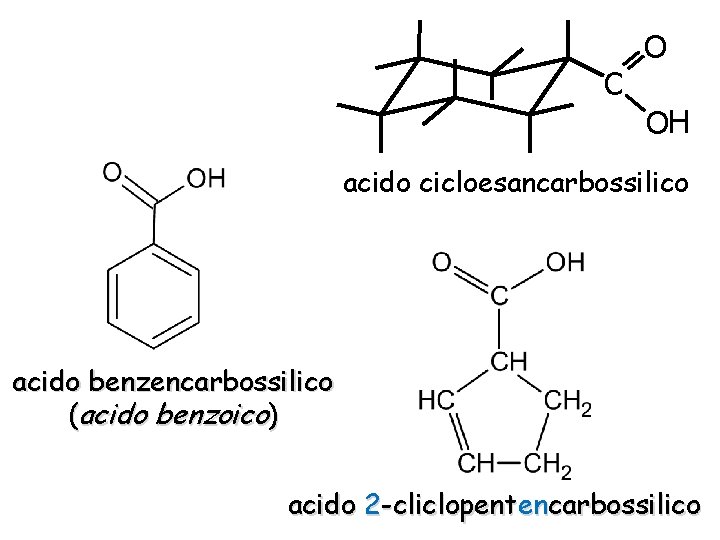
C O OH acido cicloesancarbossilico acido benzencarbossilico (acido benzoico) acido 2 -cliclopentencarbossilico
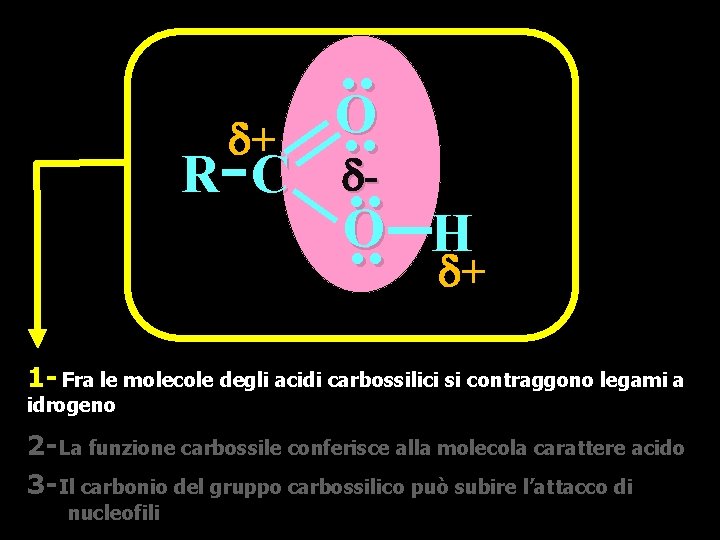
+ R C . . O. . H + 1 - Fra le molecole degli acidi carbossilici si contraggono legami a idrogeno 2 - La funzione carbossile conferisce alla molecola carattere acido 3 - Il carbonio del gruppo carbossilico può subire l’attacco di nucleofili
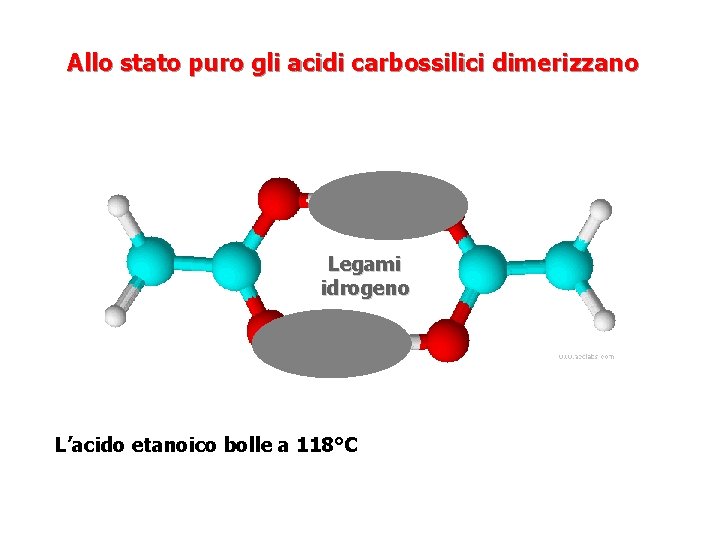
Allo stato puro gli acidi carbossilici dimerizzano Legami idrogeno L’acido etanoico bolle a 118°C
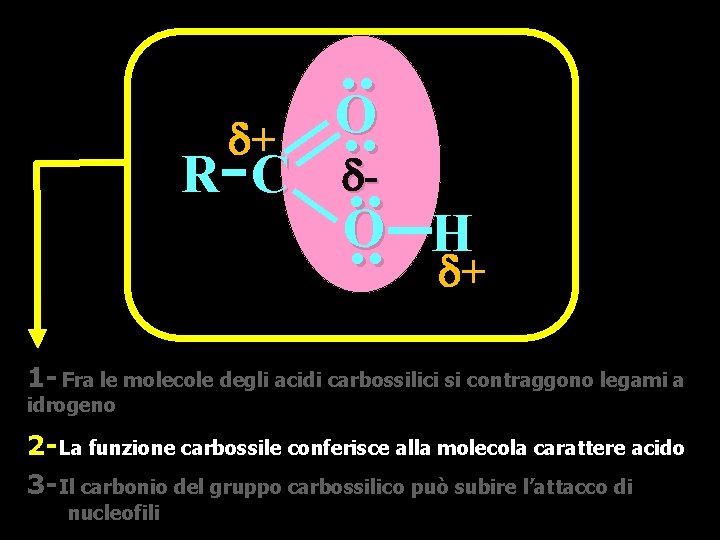
+ R C . . O. . H + 1 - Fra le molecole degli acidi carbossilici si contraggono legami a idrogeno 2 - La funzione carbossile conferisce alla molecola carattere acido 3 - Il carbonio del gruppo carbossilico può subire l’attacco di nucleofili
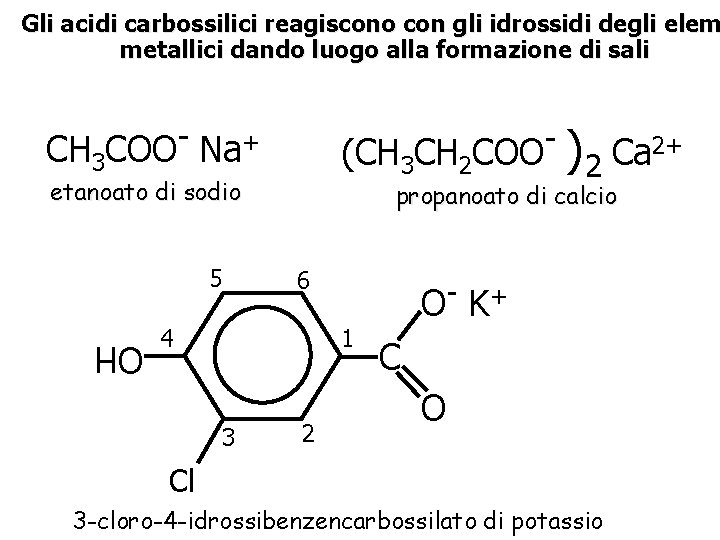
Gli acidi carbossilici reagiscono con gli idrossidi degli elem metallici dando luogo alla formazione di sali CH 3 COO Na+ (CH 3 CH 2 COO )2 Ca 2+ etanoato di sodio 5 propanoato di calcio 6 4 1 OH 3 2 O K+ C O Cl 3 -cloro-4 -idrossibenzencarbossilato di potassio
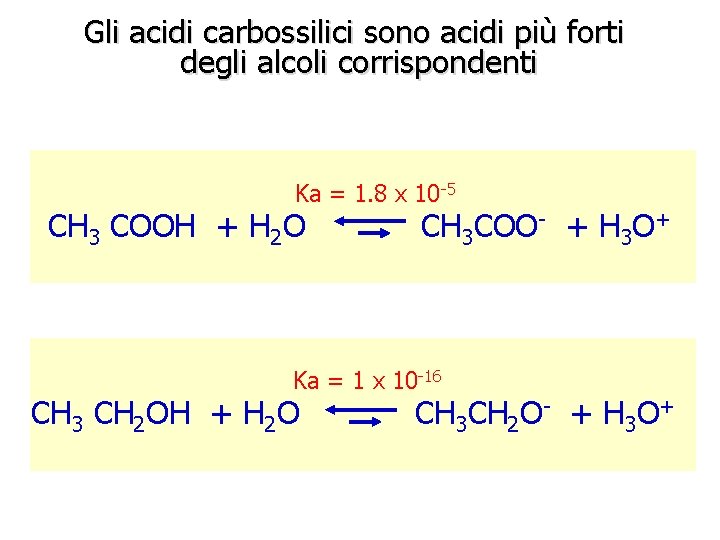
Gli acidi carbossilici sono acidi più forti degli alcoli corrispondenti Ka = 1. 8 x 10 -5 CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ Ka = 1 x 10 -16 CH 3 CH 2 OH + H 2 O CH 3 CH 2 O- + H 3 O+
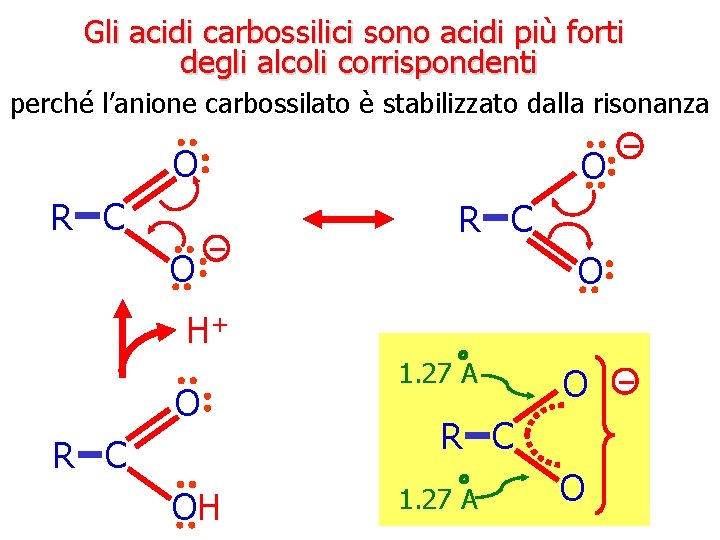
Gli acidi carbossilici sono acidi più forti degli alcoli corrispondenti perché l’anione carbossilato è stabilizzato dalla risonanza O R C O O H+ O R C OH 1. 27 A O R C 1. 27 A O
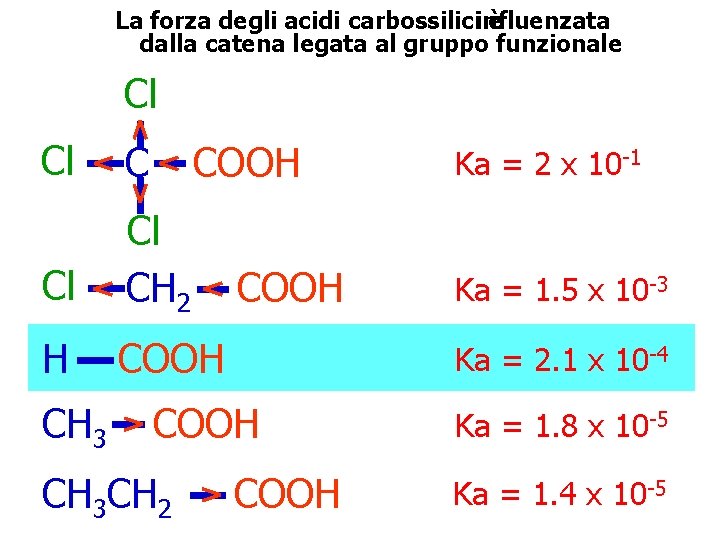
La forza degli acidi carbossiliciinfluenzata è dalla catena legata al gruppo funzionale Cl Cl CH 2 H COOH CH 3 COOH Ka = 1. 5 x 10 -3 Ka = 2. 1 x 10 -4 COOH CH 3 CH 2 Ka = 2 x 10 -1 COOH Ka = 1. 8 x 10 -5 Ka = 1. 4 x 10 -5
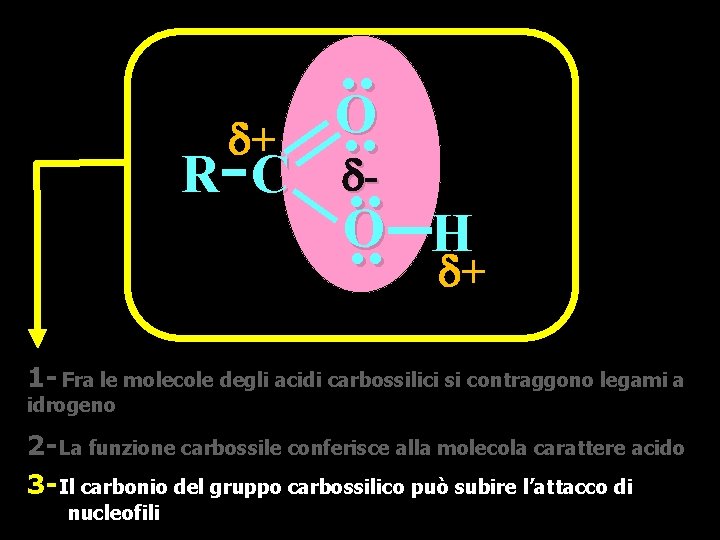
+ R C . . O. . H + 1 - Fra le molecole degli acidi carbossilici si contraggono legami a idrogeno 2 - La funzione carbossile conferisce alla molecola carattere acido 3 - Il carbonio del gruppo carbossilico può subire l’attacco di nucleofili
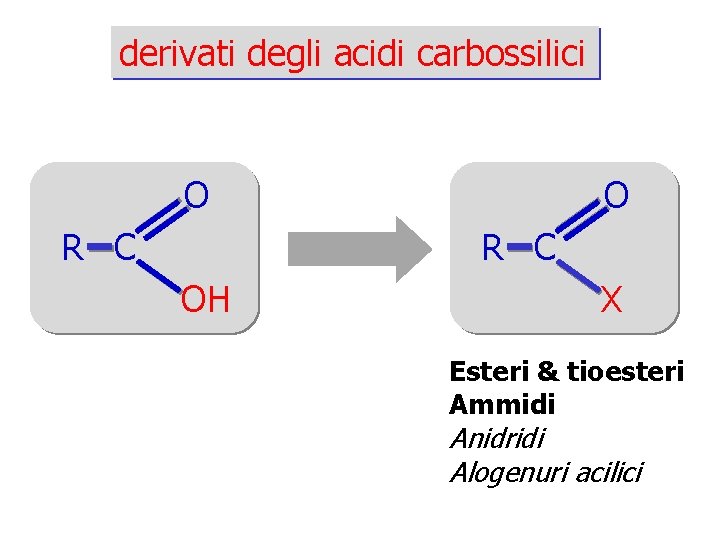
derivati degli acidi carbossilici O R C OH X Esteri & tioesteri Ammidi Anidridi Alogenuri acilici
ESTERI
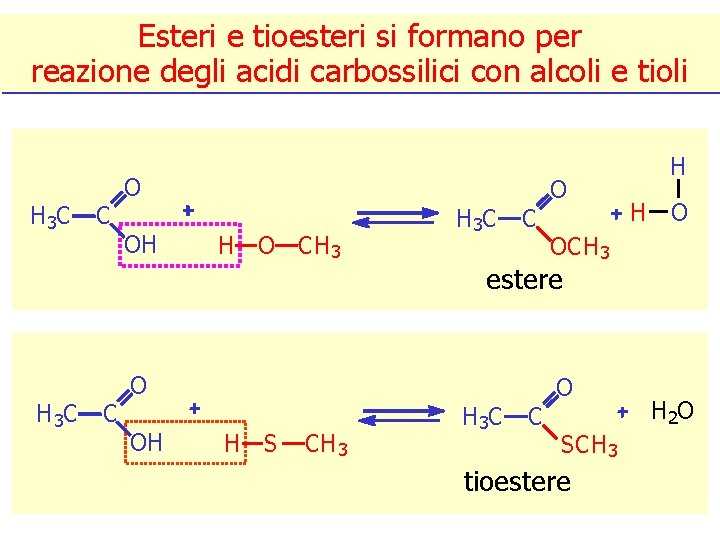
Esteri e tioesteri si formano per reazione degli acidi carbossilici con alcoli e tioli H 3 C C C O OH H O CH 3 H 3 C C H S CH 3 H O OCH 3 estere O OH O H H 3 C C O SCH 3 tioestere H 2 O
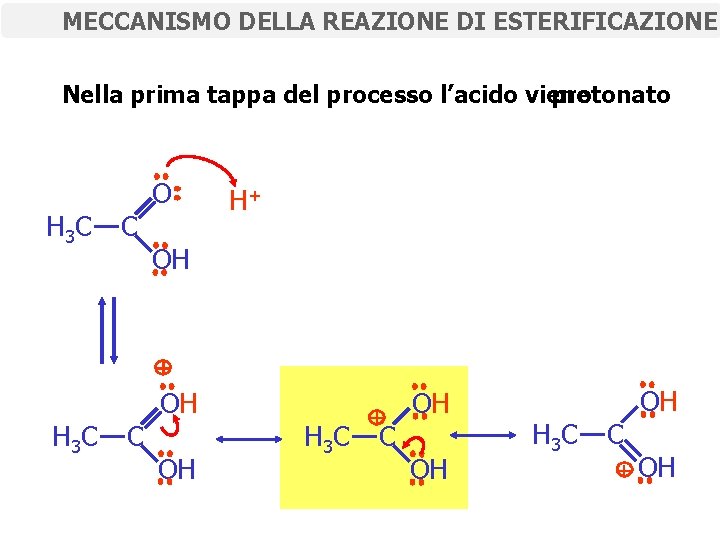
MECCANISMO DELLA REAZIONE DI ESTERIFICAZIONE Nella prima tappa del processo l’acido viene protonato H 3 C C O H+ OH + H 3 C C OH OH H 3 C + C OH OH H 3 C C OH + OH
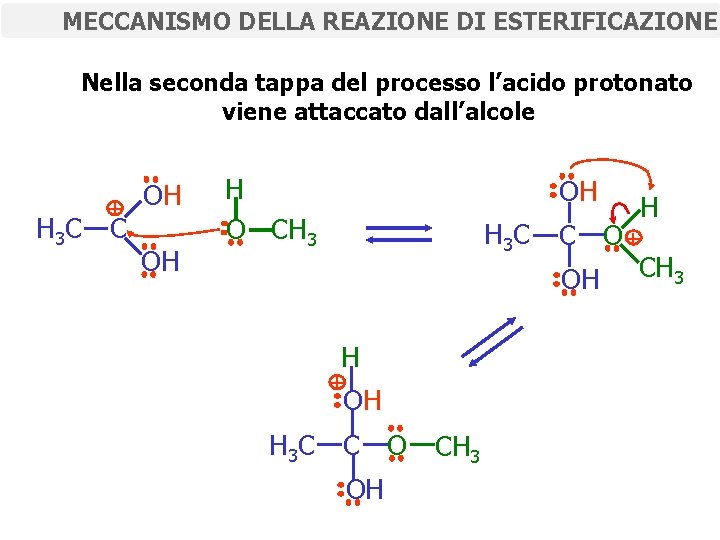
MECCANISMO DELLA REAZIONE DI ESTERIFICAZIONE Nella seconda tappa del processo l’acido protonato viene attaccato dall’alcole H 3 C + C OH OH H O CH 3 OH H 3 C H + OH H 3 C C O CH 3 OH H C O+ OH CH 3
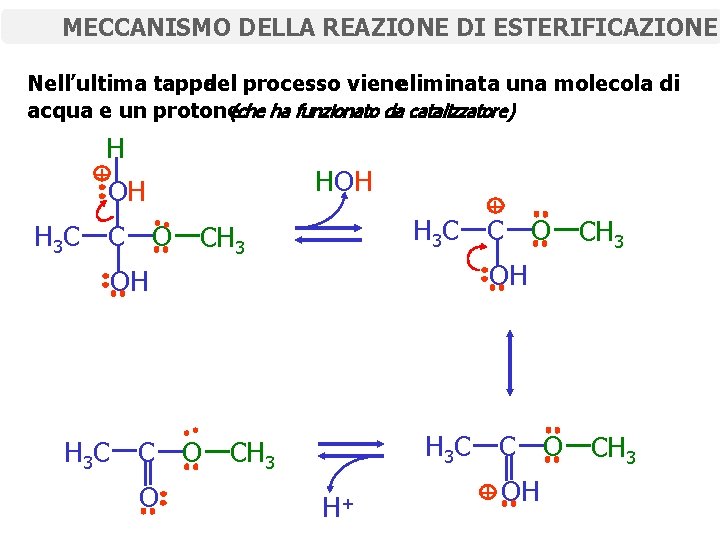
MECCANISMO DELLA REAZIONE DI ESTERIFICAZIONE Nell’ultima tappa del processo vieneeliminata una molecola di acqua e un protone(che ha funzionato da catalizzatore) H + OH H 3 C HOH H 3 C C O CH 3 OH OH H 3 C + H+ C O CH 3 + OH
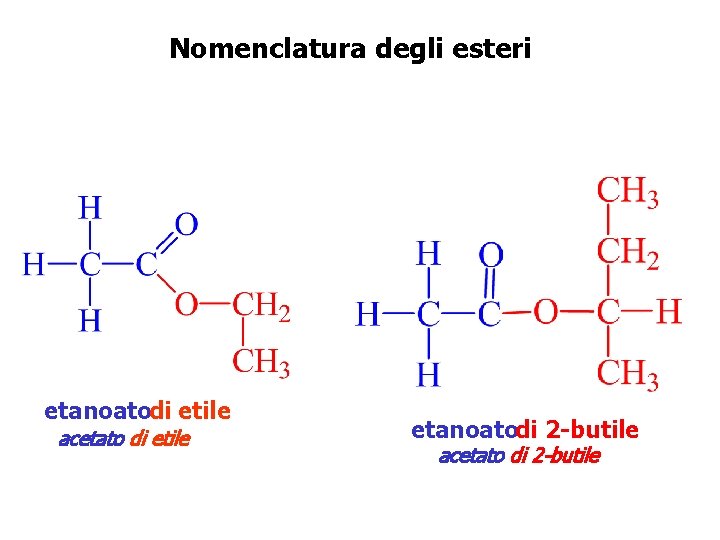
Nomenclatura degli esteri etanoatodi etile acetato di etile etanoatodi 2 -butile acetato di 2 -butile
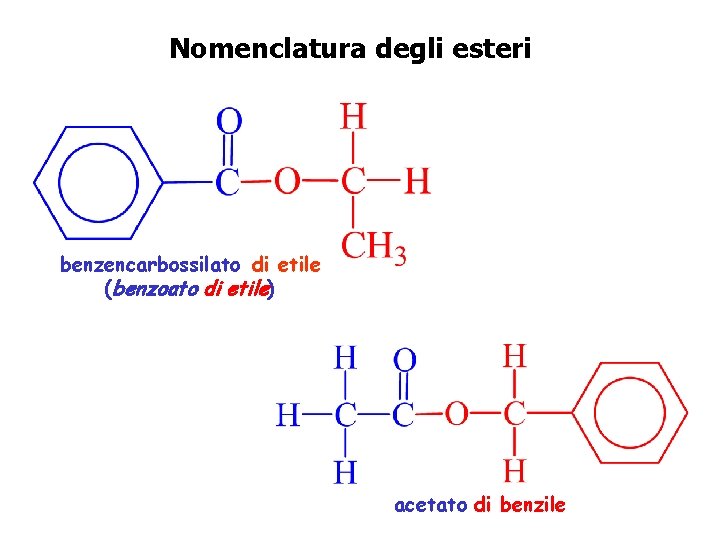
Nomenclatura degli esteri benzencarbossilato di etile (benzoato di etile) acetato di benzile
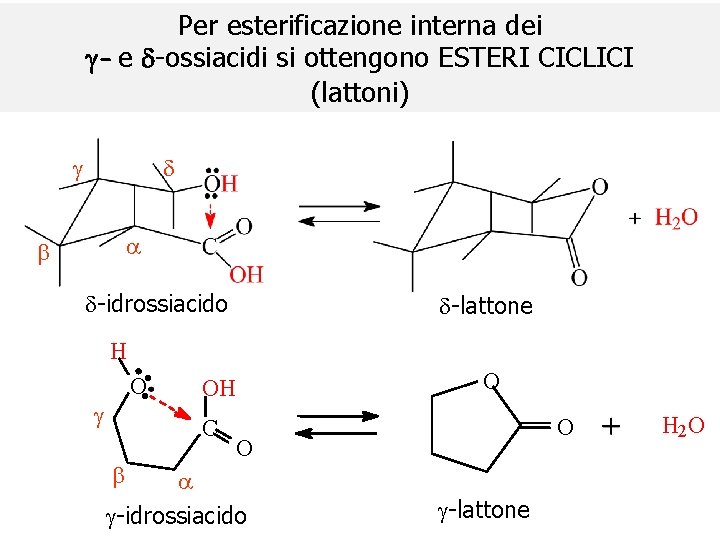
Per esterificazione interna dei g- e -ossiacidi si ottengono ESTERI CICLICI (lattoni) g d a b d-idrossiacido d-lattone H O g C b O OH O O a g-idrossiacido g-lattone H 2 O
Reazioni degli ESTERI SN 2
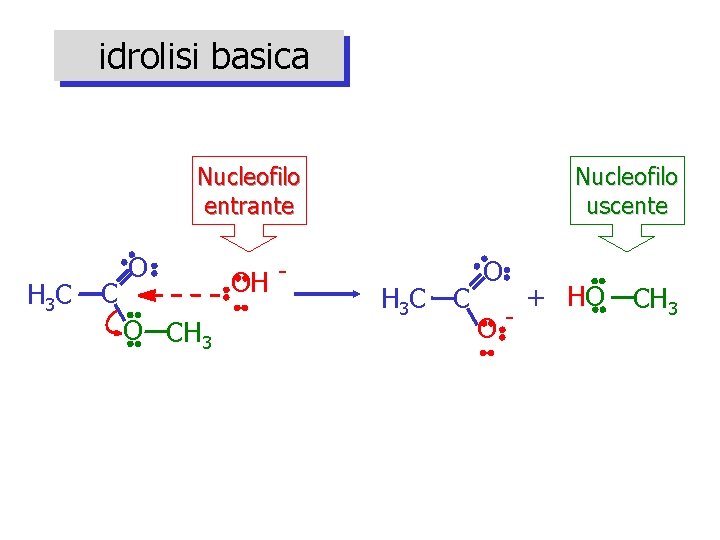
idrolisi basica Nucleofilo entrante H 3 C C O O CH 3 OH - Nucleofilo uscente H 3 C C O O- + HO CH 3

idrolisi acida

transesterificazione
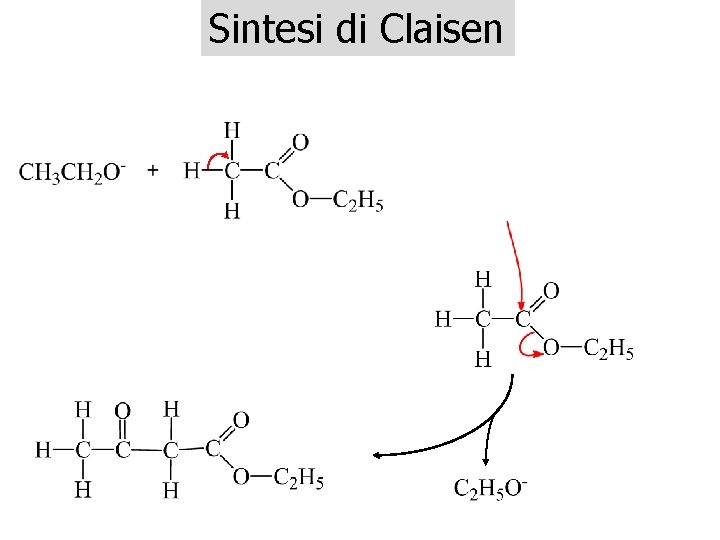
Sintesi di Claisen
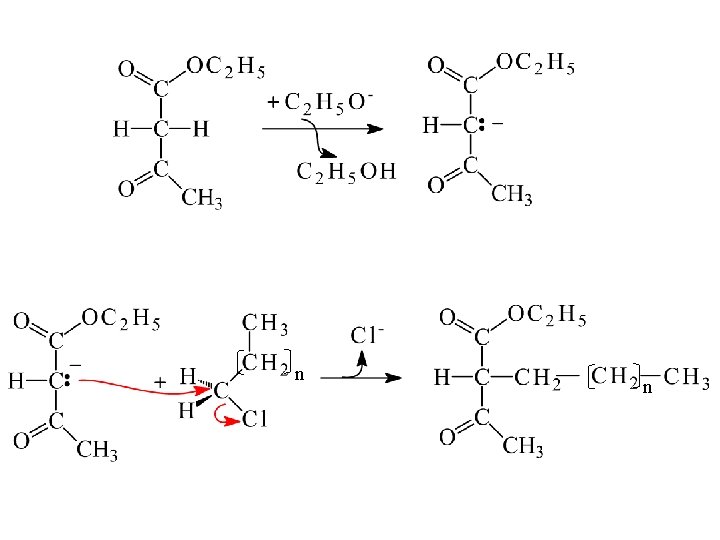
n n
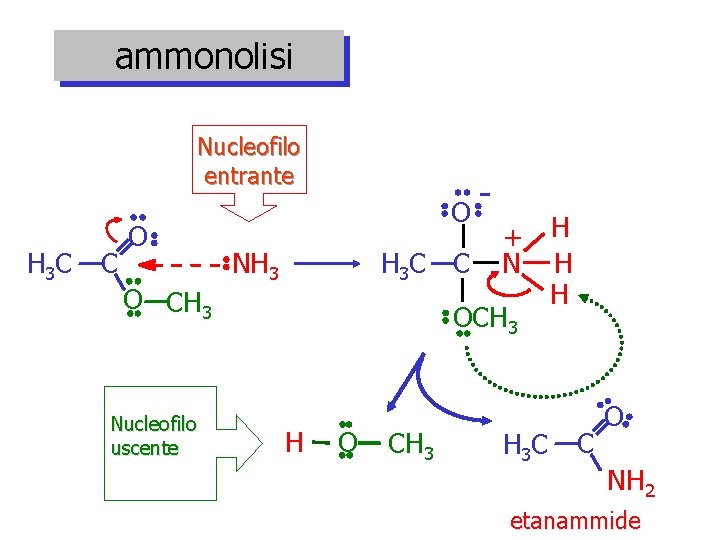
ammonolisi Nucleofilo entrante H 3 C C O O CH 3 Nucleofilo uscente O + H H 3 C C N H H OCH 3 NH 3 H O CH 3 C C O NH 2 etanammide
Ammidi
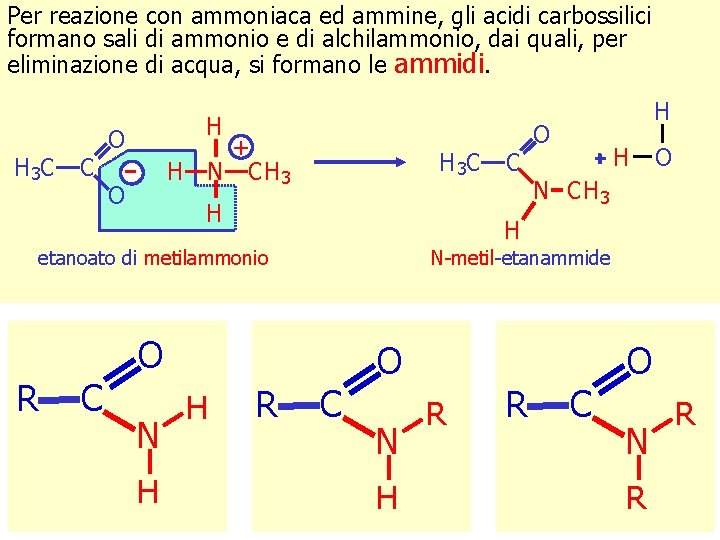
Per reazione con ammoniaca ed ammine, gli acidi carbossilici formano sali di ammonio e di alchilammonio, dai quali, per eliminazione di acqua, si formano le ammidi. H 3 C C H O O + H N CH 3 H 3 C H C N H H O N CH 3 N-metil-etanammide O H etanoato di metilammonio R C H R C O N H R R C O N R R
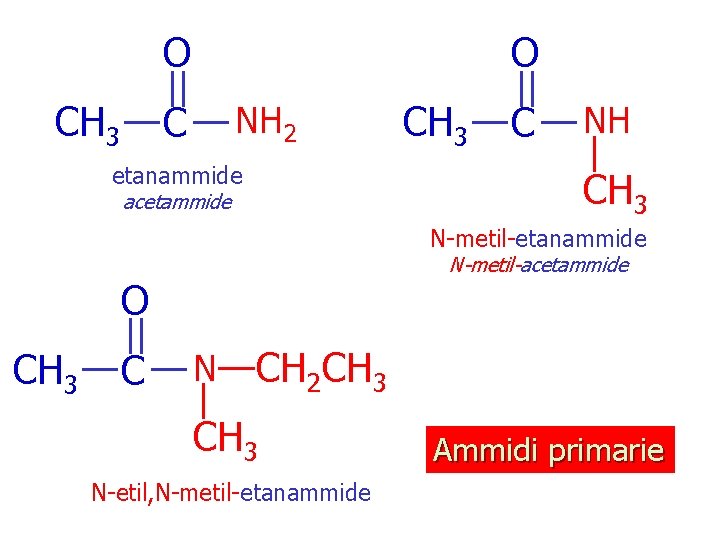
O CH 3 O C NH 2 etanammide CH 3 C NH CH 3 acetammide N-metil-etanammide N-metil-acetammide O CH 3 C N CH 2 CH 3 N-etil, N-metil-etanammide Ammidi primarie
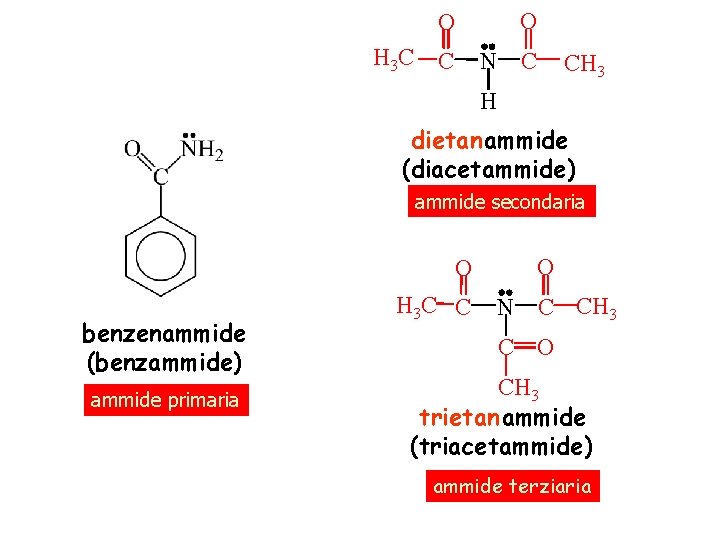
H 3 C O O C N C CH 3 H dietanammide (diacetammide) ammide secondaria O benzenammide (benzammide) ammide primaria H 3 C C O N C CH 3 C O CH 3 trietanammide (triacetammide) ammide terziaria
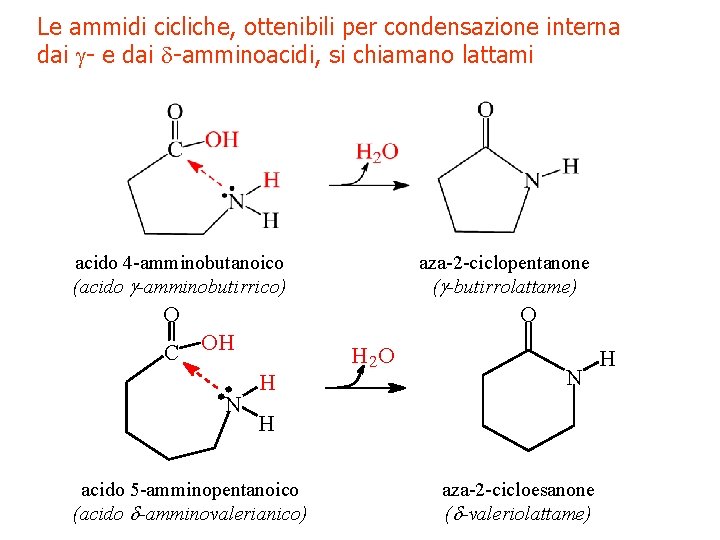
Le ammidi cicliche, ottenibili per condensazione interna dai g- e dai d-amminoacidi, si chiamano lattami acido 4 -amminobutanoico (acido g-amminobutirrico) aza-2 -ciclopentanone (g-butirrolattame) O O C OH N H H 2 O N H acido 5 -amminopentanoico (acido d-amminovalerianico) aza-2 -cicloesanone (d-valeriolattame) H
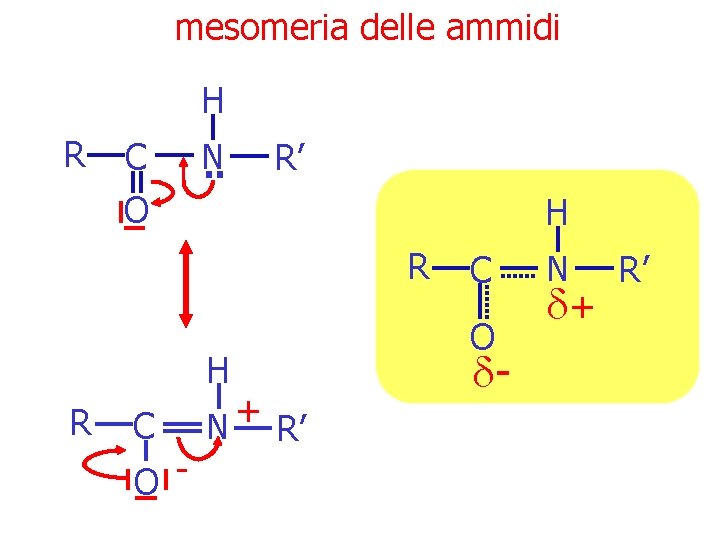
mesomeria delle ammidi H R C O N. . R’ H R C O - + N R’ C O d- N R’ d+
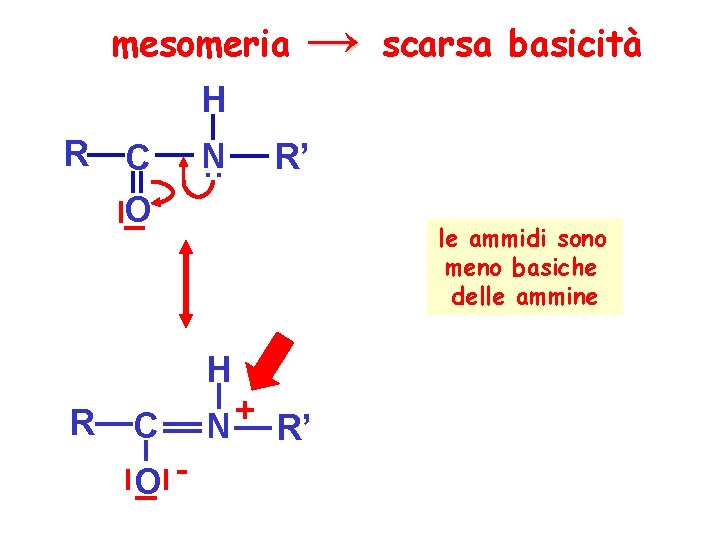
mesomeria → scarsa basicità H R C O N. . R’ le ammidi sono meno basiche delle ammine H R C O- + N R’
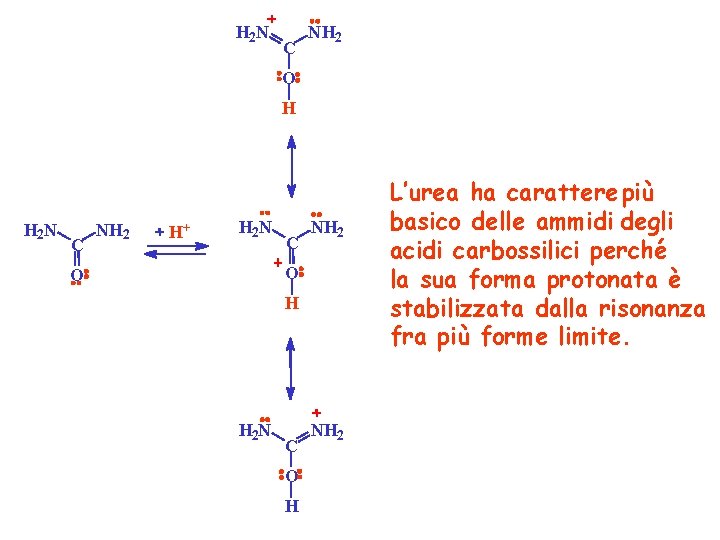
H 2 N C NH 2 O H H 2 N C NH 2 H+ H 2 N C NH 2 O O H H 2 N C O H NH 2 L’urea ha carattere più basico delle ammidi degli acidi carbossilici perché la sua forma protonata è stabilizzata dalla risonanza fra più forme limite.
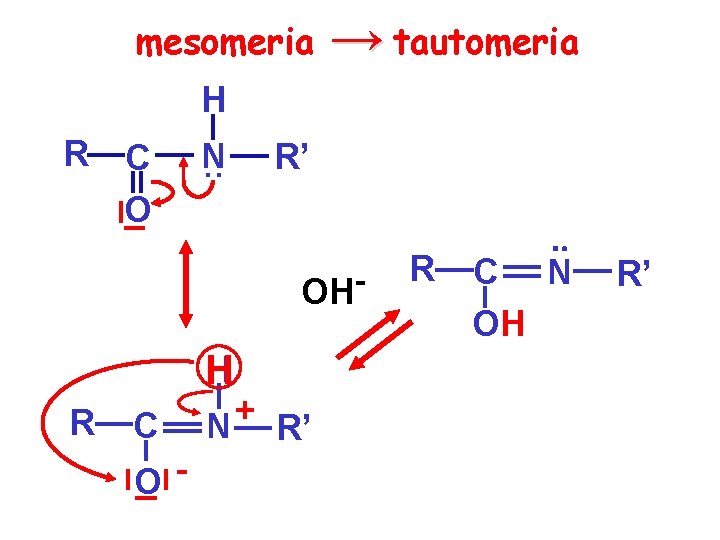
mesomeria → tautomeria H R C O N. . R’ OH H R C O- + N R’ R C N OH R’
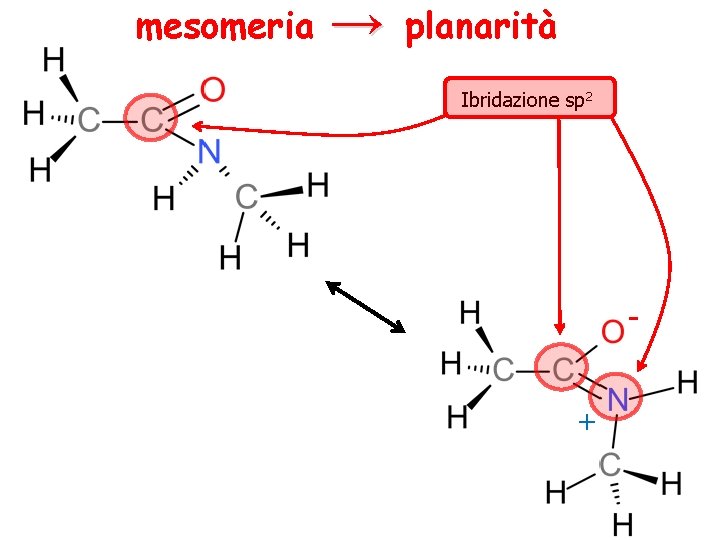
mesomeria → planarità Ibridazione sp 2 +
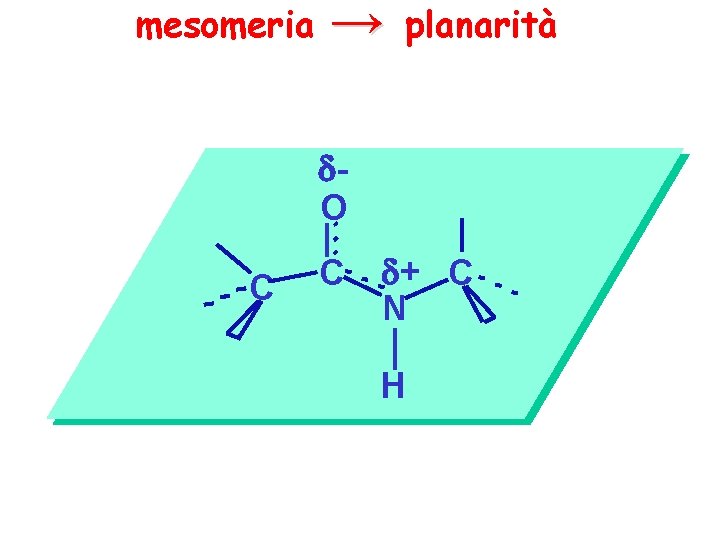
mesomeria → planarità O C C + C N H
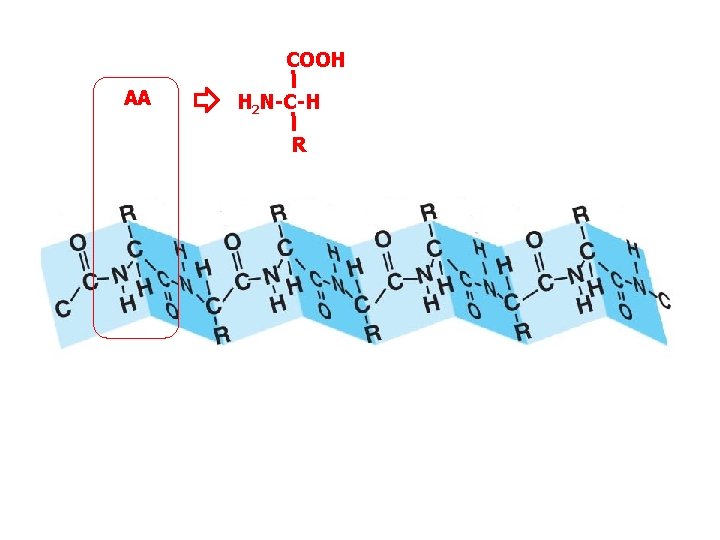
COOH AA H 2 N-C-H R
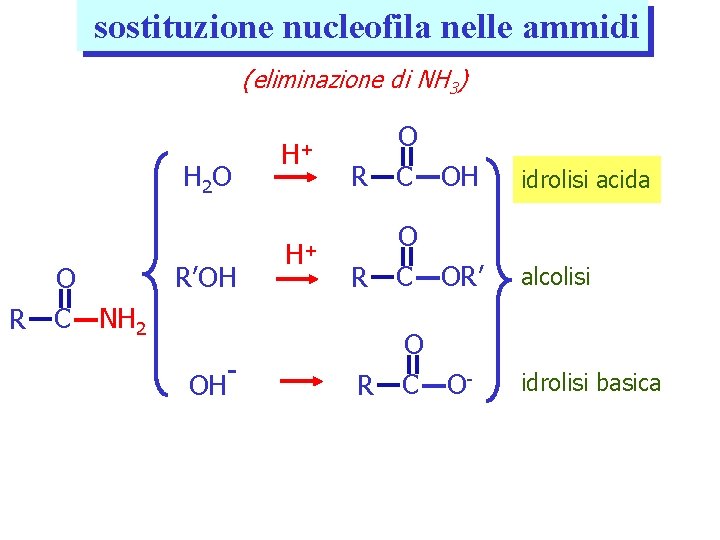
sostituzione nucleofila nelle ammidi (eliminazione di NH 3) H 2 O O R C NH 2 R’OH OH- H+ O R C OH idrolisi acida H+ O R C OR’ alcolisi O R C O- idrolisi basica
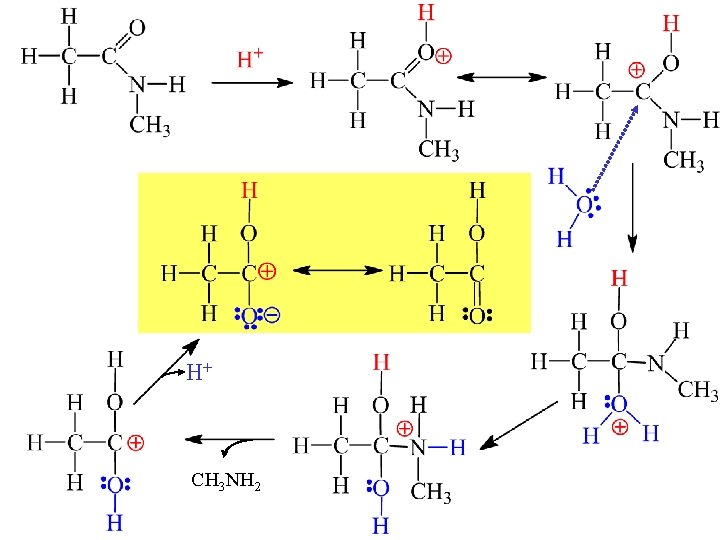
H+ CH 3 NH 2
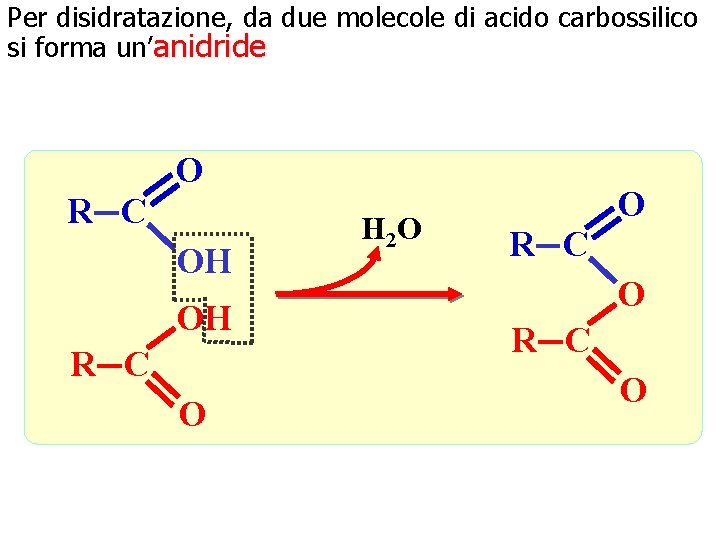
Per disidratazione, da due molecole di acido carbossilico si forma un’anidride O R C OH OH R C O H 2 O O R C O
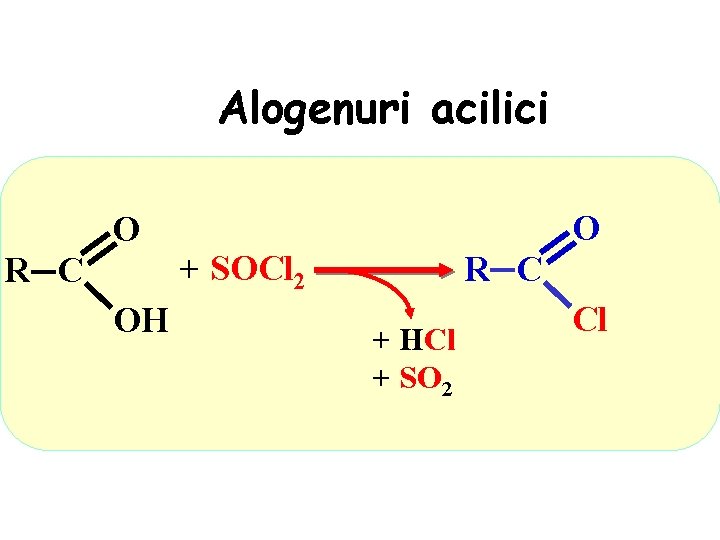
Alogenuri acilici O R C OH O + SOCl 2 R C + HCl + SO 2 Cl

- Slides: 46